用于检测AEDs引起的SJS/TEN的引物、试剂盒及方法与流程
本发明涉及基因工程
技术领域:
,具体涉及用于检测AEDs引起的SJS/TEN的引物、试剂盒及方法。
背景技术:
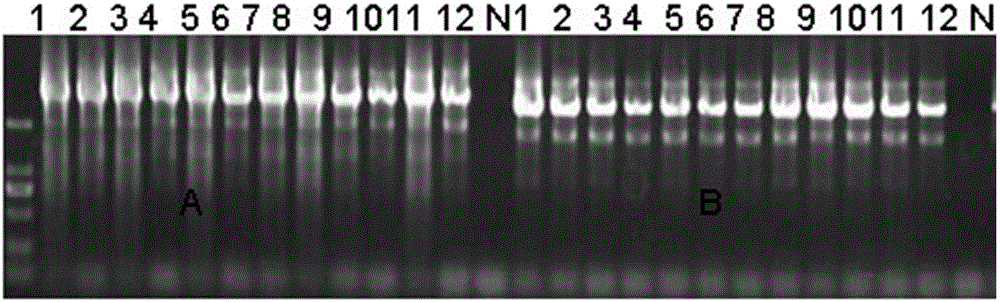
:芳香族抗癫痫药物(aromaticantiepilepticdrugs,AEDs)是引起皮肤型不良反应(cutaneousadversedrugreactions,cADRs)的常见因素之一。cADRs包括轻度的斑丘疹(maculopapularexanthema,MPE),以及严重危及生命的皮肤反应(severecutaneousreaction,SCR),如Stevens-Johnson综合症(SJS),中毒性表皮坏死松解症(toxicepidermalnecrolysis,TEN)及药物超敏综合症(drughypersensitivitysyndrome,HSS)。SJS和TEN属于同一疾病谱,可根据黏膜或皮肤脱落的程度不同分类,SJS皮肤脱落面积与皮肤总面积之比<10%,而TEN的>30%。皮肤型不良反应轻者影响药物的治疗效果,重者致死,致死率达到30%以上,其中SJS/TEN的致死率高达40%。超过90%的严重皮肤反应发生在用药后的两个月,无剂量依赖性,无预见性。芳香族抗癫痫药物AEDs,如卡马西平(carbamazepine,CBZ),拉莫三嗪(lamotrigine,LTG)和苯妥英(phenytoin,PHT),临床常用于治疗癫痫及神经类疾病,三种药物导致的Stevens-Johnson综合症(SJS)发生率约为35.8/10,000,我国南方汉族人群更是高发人群。HLA基因位于人类染色体6p21.3,长约4,000Kb,是人类最复杂的遗传多态系统,在不同的种族或同一种族不同群体中的分布出现明显的种群特性。在南方汉族人群中,HLA-B*1502与卡马西平(CBZ)导致的SJS/TEN存在强相关性,美国FDA推荐亚裔在服用CBZ之前,进行HLA-B*15:02的检测,以避免SJS/TEN的发生。LTG、PHT导致的SJS/TEN的HLA相关基因尚未明确。此外,南方汉族人群HLA-B*15:02阴性SJS患者比例高达30.4%,因此,除HLA-B*15:02之外,可能存在其它风险因子,如能在用药前,开展风险因子的检测,为有效降低药物的高风险性提供了可能。技术实现要素:本发明针对现有技术中存在的上述缺陷,采用病例-对照研究方法,对服用AEDs引起的SJS/TEN和AEDs耐受样本进行HLA-A位点和HLA-B位点Sanger测序分型,在此基础上设计了用于特异性扩增HLA-A*24:02基因和HLA-B*15:02基因的引物,并由此设计了对AEDs引起的SJS/TEN进行检测的方法。本发明的方法快速、简便、准确、灵敏、直观,且实验成本低。为此,本发明一方面提供了一种用于检测AEDs引起的SJS/TEN的引物组合,其由序列1-4所示的引物组成,用于特异性扩增HLA-A*24:02基因和HLA-B*15:02基因。在本发明优选的实施方案中,该引物组合进一步由2组引物组成,第1组由序列1和2所示的引物组成,用于特异性扩增HLA-A*24:02基因,第2组由序列3和4所示的引物组成,用于特异性扩增HLA-B*15:02基因。在本发明进一步优选的实施方案中,每条引物的浓度均为10pmol/l。本发明另一方面提供了一种用于检测AEDs引起的SJS/TEN的试剂盒,其包含本发明所述的引物组合,用于特异性扩增HLA-A*24:02基因和HLA-B*15:02基因。在本发明优选的实施方案中,试剂盒中每条引物的浓度均为10pmol/l。本发明另一方面提供了本发明所述的引物组合在制备检测AEDs引起的SJS/TEN的试剂盒中的应用,该引物组合用于特异性扩增HLA-A*24:02基因和HLA-B*15:02基因。本发明再一方面提供了本发明所述的引物组合,或者本发明所述的试剂盒在检测AEDs引起的SJS/TEN中的应用,该引物组合和试剂盒用于特异性扩增HLA-A*24:02基因和HLA-B*15:02基因。本发明最后一方面提供了一种检测AEDs引起的SJS/TEN的方法,其包含以下步骤:1、获取待测样品DNA。2、采用本发明所述的引物组合,或采用本发明所述的试剂盒,以步骤1中获取的DNA为模板,进行PCR扩增。3、对PCR扩增产物进行Sanger测序。4、得到测序峰图后,进行结果判读,判断待测样品中HLA-A*24:02基因和HLA-B*15:02基因的阳性率。在本发明优选的实施方案中,步骤2中每条引物的浓度均为10pmol/l。在本发明进一步优选的实施方案中,步骤3中还包括测序反应后进行纯化以及进行变性处理的步骤。由上述描述可知,与现有技术相比,本发明具备如下优点。1、本发明采用病例-对照研究,对服用AEDs导致的SJS/TEN和AEDs耐受样本进行HLA-A位点和HLA-B位点进行Sanger测序分型,发现HLA-A*24:02在CBZ、LTG及PHT导致的SJS/TEN的阳性率明显高于耐受组,为三种药物的通用风险因子。本发明进一步发现HLA-A*24:02和HLA-B*15:02基因型为AEDs引起的SJS/TEN的单独风险因子,并且两个基因型具有叠加效应。2、本发明根据HLA-A*24:02和HLA-B*15:02的基因序列,设计了能够高效特异性地扩增这两种基因的引物,具有高度的特异性。并且在此基础上,设计了可以对AEDs引起的SJS/TEN进行检测的试剂盒和方法。3、本发明的检测方法联合检测HLA-A*24:02和HLA-B*15:02基因,可以分别提高CBZ导致的SJS/TEN及CBZ/LTG/PHT三种药物导致的敏感性至82.1%和70.6%,特异性为70.6%和69%。同时,本发明的检测方法通过联合检测HLA-A*24:02和HLA-B*15:02基因,以预测AEDs导致的SJS/TEN,可以降低南方汉族人群SJS/TEN的发生率,从35.8/100000降低至13.0/100000。附图说明图1:PCR扩增产物的琼脂糖凝胶电泳图谱。图2:A2F测序峰形图。图3:A2R测序峰形图。图4:A3F测序峰形图。图5:A3R测序峰形图。图6:A4F测序峰形图。图7:B2F测序峰形图。图8:B2R测序峰形图。图9:B3F测序峰形图。图10:B3R测序峰形图。图11:B4F测序峰形图。具体实施方式下面通过实施例对本发明作进一步的详细说明,旨在用于说明本发明而非限定本发明。应当指出,对于本领域技术人员而言,在不脱离本发明原理的前提下,还可以对本发明进行若干改进和修饰,这些改进和修饰也同样落入本发明的保护范围之内。实施例1:样本采集采集8周内首次服用抗芳香族癫痫药物出现SJS/TEN不良反应的患者91例(即病例组)及服用抗癫痫药物3个月未出现皮肤不良反应的个体322例(即抗癫痫药物耐受对照组)的外周血,用EDTA抗凝管采取4ml,-80℃冰箱保存。病例组和对照组人群均为中国南方汉族人群,且所有人的祖父母、外祖父母的籍贯均为中国南方地区。实施例2:实验技术流程1、DNA提取使用QuickgeneDNA抽提试剂盒及配套的Quickgene-610LDNA提取机提取人外周血白细胞DNA,步骤按操作说明进行。具体步骤如下:A、向15ml离心管加入300μl蛋白酶(EDB)、2ml人外周血标本、2.5mL裂解缓冲液(LysisBuffer,LDB);B、上下颠倒混匀10-15次;C、漩涡混合器2500rpm/分×15秒;D、56℃水浴5分钟;E、加入无水乙醇2.5mL;F、上下颠倒混匀10-15次;G、漩涡混合器2500rpm/分×15秒;H、将混合物倒入Quickgene20ml纯化柱管;I、第一次运行“DNAWHOLEBLOOD”模式,第二次运行“ISOLATEA”模式,可得两管所需的人外周血白细胞DNA;J、充分混匀后采用分光光度计测定DNA的浓度和OD值;所得的每个标本基因组DNA的OD260/OD280均位于1.7-2.0之间,DNA浓度不少于50ng/ul,总量不少于10μg。K、置于-20℃冰箱保存。2、引物设计、PCR扩增反应及纯化根据GenBank公布的基因序列,利用PrimerPremier5.0引物设计软件设计,由生工生物工程(上海)股份有限公司合成。为减少测序峰图底峰,最大限度地保障了测序引物的纯度,通过引物反应条件的优化和比较,筛选出特异性强的引物。具体的引物序列参见表1。表1:HLA-A和HLA-B基因的扩增引物序列表于96孔反应板中,分别按照表2配制各基因组DNA样本的PCR反应体系,并进行PCR反应。表2PCR扩增体系PCR反应程序如下:96℃预变性5min;98℃变性10s、65℃退火30s、72℃延伸60s,5个循环;96℃变性20s、60℃退火30s、72℃延伸60s,30个循环;72℃延伸10min。4℃保存。扩增产物电泳图谱参见附图1。扩增后的产物利用SAP进行纯化。3、Sanger测序及分型Sanger测序以ABI公司BigDyeTerminatorV3.1为主要试剂(含有dNTP、ddNTP和荧光素),用前PCR反应纯化后的产物为模板,加入特异性引物进行循环扩增。HLA-A、HLA-B的测序引物分别为A-2F/R、A-3F/R、A-4F,B-2F/R、B-3F/R、B-4F。具体的测序引物序列参见表3。表3测序反应扩增引物序列表测序引物位点序列A2FCCTCTGYGGGGAGAAGCAA2RTCTCGGACCCGGAGACTGA3FCATTTTCAGTTTAGGCCAAAAATA3RCCAATTGTCTCCCCTCCTTGA4FGGGTGTCCTGTCCATTCTCAB2FAGGAGCGAGGGGACCGCAB2RGATCTCGGACCCGGAGACTB3FGGGGCCAGGGTCTCACAB3RTGGGAGGCCATCCCCGGCB4FGGTCACATGGGTGGTCCTAG测序扩增的反应条件如下:96℃2min;96℃10s,50℃20s,60℃2min(25个循环);15℃∞。测序扩增的反应体系为5ul,其组成如表4所示,其中2.5×Bigdye和5×Buffer均购自美国应用生物系统公司(AppliedBiosystems,ABI)。表4测序反应体系测序扩增产物经过乙醇—EDTA-Na2沉淀纯化处理后,用去离子甲酰胺溶解变性,ABI3730xl全自动DNA测序仪(美国)毛细管电泳并自动对结果进行分析处理,获得所需片段碱基序列,并以4色峰图形式呈现。采用VectorNTI6.0(美国)软件对HLA-A、HLA-B的序列按照http://www.ebi.ac.uk/imgt/hla网上公布的序列进行比对并获得结果。4、统计分析与结果采用SPSS16.0统计分析软件进行统计分析。将病例组与对照组的HLA-A*24:02和HLA-B*15:02的阳性率用χ2检验或精确概率法进行比较,P﹤0.05为差异有统计学意义,显示HLA-A*24:02为CBZ、LTG及PHT的风险基因,同时也为三种药物的通用风险基因;HLA-B*15:02为CBZ的风险基因,同时也为三种药物的通用风险基因(具体数据参见表5)。表5:CBZ,LTG,和PHT导致的SJS/TEN风险因子采用Logtistic回归模型分析两个等位基因在AEDs导致的SJS/TEN的交互作用,进入方程的标准α=0.05,剔除方程标准α=0.10,P<0.05为差异具有统计学意义,保留在Logistic回归模型中的因素确定为有意义危险因素,发现两个基因为单独风险基因,且具有累加效益(具体数据参见表6)。表6:HLA-B*15:02和HLA-A*24:02对AED导致的SJS/TEN累积效应按照三种药物导致的SJS发生率为10万分之35.8,检测HLA-A*24:02及HLA-B*15:02基因型,HLA-A*24:02基因阳性或HLA-B*15:02阳性患者避免服用这三种AEDS,可以降低SJS发生率至10万分之13。当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1
- 用于检测AEDs引起的SJS/TEN的引物、试剂盒及方法与制造工艺
- 检测植原体的LAMP引物组及其试剂盒和应用的制造方法与工艺
- 用于多重PCR检测致腹泻寄生虫的引物组及试剂盒的制造方法与工艺
- 使用重叠非等位基因特异性引物和等位基因特异性阻断剂寡核苷酸的组合物进行等位基因特异性扩增的制造方法与工艺
- 一种基于特异性SS-COI引物的丽草蛉PCR快速检测方法与制造工艺
- 一种利用线粒体D-loop区特异区域鉴定鼋的标记引物及方法
- 一种用于检测大豆拟茎点种腐病菌的特异性lamp引物组合物及其应用
- 一种针对膨胀污泥中Eikelboom Type 0092型丝状菌群特异性引物和方法
- 紫苑石斛的分子特异性标记引物及检测方法
- 一种检测牛hcd携带者的特异性pcr引物、试剂盒及检测方法
- 检测植原体的LAMP引物组及其试剂盒和应用的制造方法与工艺
- 用于多重PCR检测致腹泻寄生虫的引物组及试剂盒的制造方法与工艺
- 使用重叠非等位基因特异性引物和等位基因特异性阻断剂寡核苷酸的组合物进行等位基因特异性扩增的制造方法与工艺
- 一种利用线粒体D-loop区特异区域鉴定鼋的标记引物及方法
- 一种用于检测大豆拟茎点种腐病菌的特异性lamp引物组合物及其应用
- 一种针对膨胀污泥中Eikelboom Type 0092型丝状菌群特异性引物和方法
- 紫苑石斛的分子特异性标记引物及检测方法
- 一种检测牛hcd携带者的特异性pcr引物、试剂盒及检测方法
- 用于检测牛源性成分的lamp引物及其设计方法
- 七种不同种属来源细胞的pcr检测引物和检测方法与应用
- 检测植原体的LAMP引物组及其试剂盒和应用的制造方法与工艺
- 用于多重PCR检测致腹泻寄生虫的引物组及试剂盒的制造方法与工艺
- 使用重叠非等位基因特异性引物和等位基因特异性阻断剂寡核苷酸的组合物进行等位基因特异性扩增的制造方法与工艺
- 一种利用线粒体D-loop区特异区域鉴定鼋的标记引物及方法
- 一种用于检测大豆拟茎点种腐病菌的特异性lamp引物组合物及其应用
- 一种针对膨胀污泥中Eikelboom Type 0092型丝状菌群特异性引物和方法
- 紫苑石斛的分子特异性标记引物及检测方法
- 一种检测牛hcd携带者的特异性pcr引物、试剂盒及检测方法
- 用于检测牛源性成分的lamp引物及其设计方法
- 七种不同种属来源细胞的pcr检测引物和检测方法与应用