一种基于三聚茚的星型化合物的制备方法与流程
本发明属于有机合成技术领域,涉及一种基于三聚茚的星型化合物的制备方法。
背景技术:
光诱导能量/电子转移在光化学反应、太阳能利用、光合作用机理等方面起着重要作用。基于光诱导能量/电子转移机理的分子模型在光学分子器件、太阳能电池和人工光合成等方面应用研究已成为国内外十分活跃的研究领域。具有电子/能量给受体性能的染料分子在有机光电功能材料方面已经展现出广阔的应用前景。在不同结构类型的分子模型中,星型化合物独特的三维星射型结构有利于调控分子的光电性能和形态特征,多个向外延伸支臂可以提高电荷传递和能量转移效率,已受到了广泛关注。然而,具有给体-受体结构星型化合物仍存在着合成步骤多、反应复杂、产率低等不足之处,因此设计合成具有良好能量/电子转移过程的易合成的新型星型化合物具有重要的意义。
三聚茚(truxene)具有大的刚性共轭结构,是一个三重对称性平面刚性的稠环芳烃,有利于分子内电荷转移,它的三个端基2,7和12位易于进行功能化设计和修饰,已经被证明是制备星型理想化合物之一。卟啉、bodipy及富勒烯等光活性基团具有优良光电性质及良好的结构可修饰性。因此,可通过简单化学合成方法将卟啉、bodipy及富勒烯三个不同光活性基团稼接在三聚茚的2,7和12三个端基上,构成具有给体/受体的星型化合物,可用于光吸收天线、太阳能电池、模拟生物体光合作用等方面的应用研究。
技术实现要素:
发明目的:针对现有技术中存在的不足,本发明的目的是提供一种基于三聚茚的星型化合物(tbp-c60)的制备方法。
技术方案:为了实现上述发明目的,本发明采用的技术方案为:
本发明涉及的基于三聚茚的星型化合物(tbp-c60)的结构如下:
本发明涉及的基于三聚茚的星型化合物(tbp-c60)的合成路线为:
本发明涉及的基于三聚茚的星型化合物(tbp-c60)的制备过程包括以下步骤:
步骤1:在氩气保护条件下,将7,12-二双溴三聚茚醛衍生物、bodipy硼酸酯衍生物、无水碳酸钠和催化剂四(三苯基膦)钯溶解于四氢呋喃中,并加入一定比例的甲醇和水的混合溶液,加热回流反应24小时,反应结束后冷至室温,加入适量水,并用二氯甲烷萃取,有机层经饱和氯化铵溶液洗两次,无水硫酸钠干燥,减压旋干溶剂后经硅胶柱层析分离提纯得到化合物tb;
步骤2:将卟啉硼酸酯衍生物和步骤1所得化合物tb以及无水碳酸钠在氩气条件下溶解于四氢呋喃中,再向反应体系中加入一定比例的水与甲醇混合溶液,最后加入催化剂四三苯基膦钯,体系在回流条件下反应24小时,粗产物用二氯甲烷萃取分离,有机层经饱和氯化铵溶液洗后,再用无水硫酸钠干燥,减压旋干溶剂后经硅胶柱层析分离提纯得到化合物tbp;
步骤3:将步骤2所得化合物tbp与富勒烯、肌氨酸溶于甲苯中,在氩气保护下以及加热回流条件下反应12小时,反应结束后粗产物减压蒸干溶剂后经硅胶柱层析分离提纯得到化合物tbp-c60。
上述反应步骤1中,7,12-二溴三聚茚醛衍生物与bodipy硼酸酯衍生物的摩尔量之比为1∶1;
上述反应步骤2中,tb与卟啉硼酸酯衍生物的摩尔量之比为1∶1;
上述反应步骤1和2中,催化剂四(三苯基膦)钯用量为反应原料摩尔量的10%;
上述反应步骤1和2中,甲醇与水的体积比为1∶1;
上述反应步骤3中tbp、富勒烯(c60)与肌氨酸的摩尔量之比1∶5∶10。
本发明的有益效果
与现有技术相比,本发明中基于三聚茚的星型化合物(tbp-c60)的制备方法所具有的优点有:(1)在三聚茚2、7、12三个活性位置分别引入bodipy、卟啉、富勒烯三种不同的光活性基团,构成给体-受体星型分子体系,在同一分子中能发生电子/能量转移过程,可用作模拟生物光合作用过程。(2)合成路线简单、反应选择性好、反应条件温和,具有普适性,可以推广应用到以三聚茚为核心的多种不同的给体-受体星型化合物的合成。
附图说明
图1为本发明实施例1的紫外-可见吸收光谱;
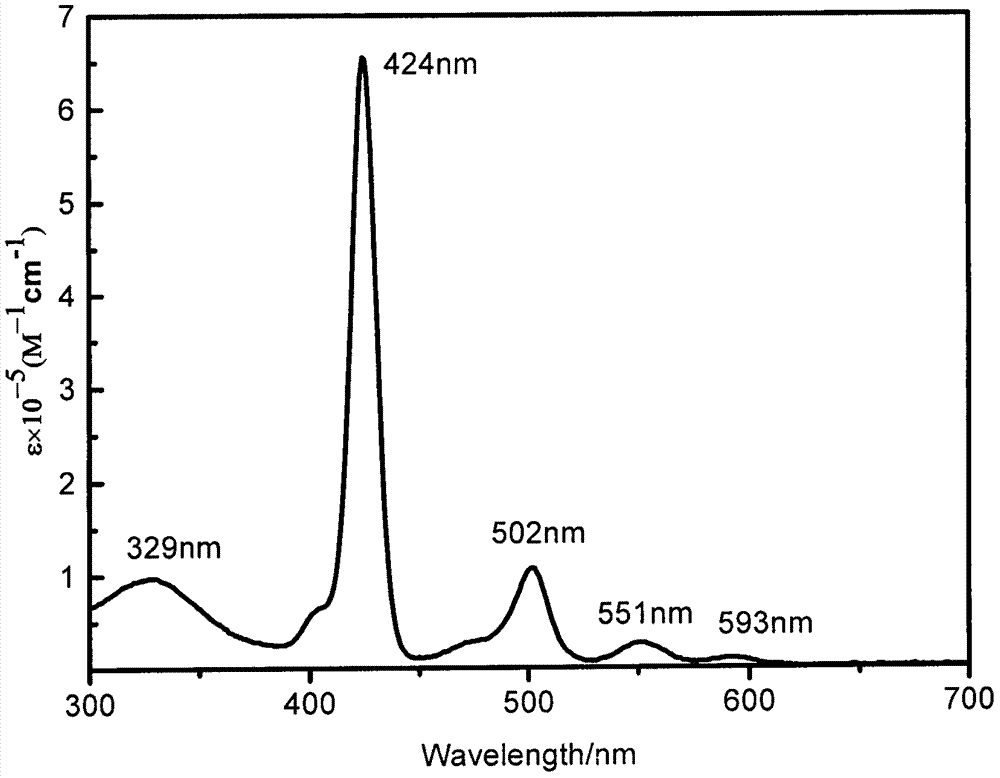
图2为本发明实施例2的紫外-可见吸收光谱;
图3为本发明实施例3的紫外-可见吸收光谱;
图4为本发明实施例1的荧光光谱;
图5为本发明实施例2的荧光光谱;
图6为本发明实施例3的荧光光谱。
具体实施方式
下面结合具体实例对本发明作进一步地解释,具体实施事例并不对本发明作任何限定。
用1h-nmr、紫外-可见光谱及荧光光谱表征化合物的结构并研究化合物的光物理性质。检测所用仪器为:brukerarx500型核磁共振仪(tms为内标,氘代氯仿为溶剂),岛津uv-3100型紫外-可见分光光度计(扫描范围400~800nm,光路狭缝2nm),pels-55型荧光分光光度计(波长范围:激发光200-800nm,发射光200-900nm;狭缝可变:激发光路2.5-15nm,发射光路2.5-20nm;步距:0.1nm)。
实施例1
在氩气环境下将2,7-二溴三聚茚醛(0.7mmol,605.49mg)、bodipy硼酸酯衍生物(0.7mmol,315.10mg)、无水碳酸钠(12.64mmol,1.34g)溶解于四氢呋喃(60ml),并加入甲醇和水的混合液(ch3oh/h2o=5ml/5ml),最后向反应器中加入催化剂pd(pph3)4(0.07mmol,77.39mg),加热至回流条件下反应24小时。反应结束后,用二氯甲烷提取有机物并用饱和氯化铵溶液洗涤,合并有机层后经无水硫酸钠干燥,减压蒸馏除去溶剂并以二氯甲烷-石油醚为洗脱剂经硅胶柱层析分离提纯得到产物tb为233.25mg(产率30.07%)。uv-vis(ch2cl2),λmax/nm[ε×10-5/(l·mol-1·cm-1)]:318(0.192),502(0.219)(附图1);1hnmr(cdcl3,600mhz,ppm)δ10.15(s,2h),8.44-8.48(m,1h),8.25-8.28(m,1h),7.92-7.96(m,3h),7.44(d,j=6hz,2h),7.61(s,1h),6.02(s,2h),2.92-3.03(m,6h),2.09-2.24(m,6h),1.54(d,j=12hz,6h),0.44-0.52(m,26h).emissionwavelength:516nm(附图4).
实施例2
在氩气条件下将化合物tb(0.15mmol,166.22mg)和卟啉衍生物(0.15mmol,144.36mg)溶于干燥的四氢呋喃(40ml)中,加入无水碳酸钠(2.7mmol,286.17mg),并向反应中加入催化剂pd(pph3)4(0.015mmol,17.33mg),再加入甲醇和水的混合液(ch3oh/h2o=1ml/1ml),反应体系在回流条件下反应24小时,反应结束后,用二氯甲烷提取有机物并用饱和的氯化铵溶液洗涤,合并有机层后经无水硫酸钠干燥,减压蒸馏除去溶剂并以二氯甲烷-石油醚为洗脱剂通过硅胶柱层析分离提纯得到产物tbp为73.5mg(产率26.4%)。uv-vis(ch2cl2),λmax/nm[ε×10-5/(l·mol-1·cm-1)]:329(0.97319),424(6.55283),502(1.07515),551(0.26879),593(0.10195)(附图2);1hnmr(cdcl3,600mhz,ppm)δ10.03-10.09(m,1h),9.15(t,j=4.8hz,4h),9.10(t,j=4.8hz,2h),9.05(t,j=4.8hz,2h),8.81-8.86(m,1h),8.68-8.73(m,1h),8.63(d,j=6.6hz,1h),8.47(dd,j=1.2hz,1h),8.40(t,j=3.0hz,1h),8.32(t,j=7.8hz,2h),8.21(s,4h),8.12(s,1h),8.01-8.10(m,3h),7.97(d,j=7.8hz,1h),7.92(t,j=7.2hz,1h),7.87(d,j=9.0hz,3h),7.81(s,3h),7.49-7.53(m,2h),6.07(d,j=7.8hz,2h),3.16-3.43(m,6h),2.64(s,6h),2.39-2.44(m,4h),2.31-2.36(m,2h),2.64(s,6h),1.61(m,42h),1.10-1.20(m,12h),0.61-0.91(m,30h).emissionwavelength:515nm,604nm,648nm(附图5).
实施例3
将化合物tbp(0.0217mmol,40mg)、富勒烯(0.109mmol,78.20mg)和肌氨酸(0.217mmol,19.33mg)溶于干燥甲苯(30ml)中,氩气条件下加热回流反应12个小时,反应结束后减压蒸馏除去溶剂以二氯甲烷-石油醚为洗脱剂经硅胶柱层析分离提纯,得到产物tbp-c60为34.72mg(产率61.51%)。uv-vis(ch2cl2),λmax/nm[ε×10-5/(l·mol-1·cm-1)]:257(1.32673),316(0.78043),424(3.56396),502(0.57231),549(0.14308),590(0.039020)(附图3);1hnmr(cdcl3,600mhz,ppm)δ9.04-9.06(m,4h),9.00(t,j=3.0hz,2h),8.96(s,2h),8.71-8.73(m,1h),8.53(t,j=3.6hz,2h),8.42-8.46(m,1h),8.29(s,2h),8.23(s,2h),8.09-8.14(m,5h),7.95(t,j=6.6hz,2h),7.85(s,1h),7.74-7.80(m,7h),7.42-7.44(d,j=7.2hz,2h),6.02(s,2h),5.05(s,1h),4.94-4.96(m,1h),4.21-4.22(m,1h),3.28-3.31(m,2h),3.04-3.07(m,4h),2.95(s,3h),2.58(s,6h),2.28-2.40(m,6h),1.53(s,36h),1.51(s,6h),1.04-1.11(m,6h),0.56-0.68(m,30h).emissionwavelength:514nm,601nm,651nm(附图6)。
- 还没有人留言评论。精彩留言会获得点赞!
- 一种Ni@C@g-C<sub>3</sub>N<sub>4</sub>纳米复合物及其制备方法和应用
- 一种石墨烯-三聚氰胺泡沫气凝胶及其制备方法
- 制备聚胺的方法
- 一种低温固化三聚氰胺甲醛树脂胶及其制备方法
- 一种生物质改性三聚氰胺甲醛树脂微球泡沫的制备方法
- 一种三羟甲基三聚氰胺的制备方法
- 一种Fe@C@g-C<sub>3</sub>N<sub>4</sub>纳米复合物及其制备方法和应用
- 一种g-C<sub>3</sub>N<sub>4</sub>/Bi<sub>3</sub>TaO<sub>7</sub>表面复合光催化剂的制备方法
- Ag<sub>2</sub>CrO<sub>4</sub>负载的g-C<sub>3</sub>N<sub>4</sub>复合光催化剂及其制备方法和应用
- 一种高聚合度的三聚氰胺聚磷酸盐的制备方法
- 一种PtCu@g?C<sub>3</sub>N<sub>4</sub>/rGO标记的电化学免疫传感器的制备方法及应用
- 一种三聚氰胺类高分子材料及其在处理重金属方面的应用和制备方法
- 三聚氰胺类苯并噁嗪树脂的制备方法
- 一种Sn@C@g?C<sub>3</sub>N<sub>4</sub>纳米复合物及其制备方法
- 一种MIL?53(Fe)/g?C<sub>3</sub>N<sub>4</sub>纳米片复合光催化材料的制备方法
- 一种二氧化钛/g?C<sub>3</sub>N<sub>4</sub>量子点复合催化剂的制备方法
- 一种十聚钨酸盐/氮化碳复合光催化剂的制备方法和应用
- 一种用含磷三聚氰胺树脂制备碳泡沫的方法
- 一种Co@C@g?C<sub>3</sub>N<sub>4</sub>纳米复合物及其制备方法和应用
- 一种Ni@C@g-C<sub>3</sub>N<sub>4</sub>纳米复合物及其制备方法和应用