一种检测人类KRAS基因突变的试剂盒及其检测方法与流程
本发明涉及生物技术领域,尤其涉及的是一种检测人类kras基因突变的试剂盒及其检测方法。
背景技术:
ras基因是被鉴定的第一个致癌基因,根据详细的肿瘤遗传特征分析,ras基因是最为常见的癌基因,约30%的肿瘤中有ras基因突变。ras基因家族中包括nras基因、hras基因以及最常见的与kristen大鼠肉瘤病毒癌基因同源的kras基因(85%以上的ras基因突变为kras突变)。
kras蛋白在各组织间的信号传递中起到重要作用,kras基因的突变通常是癌症产生的一个重要原因,kras突变比较常见并且出现在危及生命的癌症中,比如胰腺癌(70%-90%),结肠癌(35%-50%),小肠肿瘤(35%),胆管癌(20%-30%),肺癌(20%-35%)。和ras家族的其他蛋白一样,kras是一种gtp水解酶,在很多信号传递的前期起作用。kras蛋白的c末端有一个异戊二烯基团能够结合细胞膜,哺乳动物细胞中有两种外显子4(外显子4a和外显子4b),它们分别产生kras4a和kras4b,这两种蛋白c末端的结构有所不同,因此它们结合细胞膜包括质膜的位置有所不同。kras的信号传递通路非常复杂,相比于其他ras基因,可能kras突变能够优先通过癌基因毒性刺激信号。
ddpcr被称为是第三代pcr技术,具有更高的精确度和灵敏度。它通过将样品进行微滴化,形成千上万个微滴,每一个微滴都被认为是一个独立的pcr体系,微滴中含有或者不含有核酸靶分子,用微滴分析仪对每一个微滴进行pcr结果分析检测,有荧光信号的微滴记为1,没有检测到荧光信号的记为0,根据泊松分布原理对统计结果进行分析计算得出目的基因的绝对拷贝数。
了解癌症基因相关的分子结构和图谱对治疗方案确定至关重要,特别是在表皮生长因子受体和alk酪氨酸激酶抑制剂的使用方面。mek抑制剂和紫杉醇药物结合的治疗效果被认为与kras的突变体的类型相关。鉴于此,一种高效、快速的检测kras基因突变试剂盒的发明有利于提高癌症诊断的效率。
技术实现要素:
本发明的目的在于克服现有技术的不足,提供了一种高准确度、高精确度、高灵敏度、高特异性、高效率的基于ddpc检测人类kras基因突变的试剂盒,本发明的另一目的在于提供一种检测人类kras基因突变的方法。
本发明是通过以下技术方案实现的:一种检测人类kras基因突变的试剂盒,其特征在于:包含有一对特异性引物(primerf、primerr)、一条与特异性引物配合使用的探针引物(probe)、
所述的一对特异性引物和探针引物为:
primerf:5’-gtgccttgacgatacagcta-3’
primerr:5’-cacactttgtctttgacttctttt-3’,
所述的探针引物为probe:fam5’-accatctttgctcatcttttct-3’hex
优选的,所述的试剂盒还包括核酸酶抑制剂(dnaseinhibitor)、2×pcr反应混合试剂(2×pcrmix)、微滴发生油、无菌蒸馏水(ddh2o)、kras突变基因阳性对照和阴性对照(ddh2o)。
优选的,所述的2×pcr反应混合试剂包含:dna聚合酶,dntps,mgcl2。
作为优选,所述的2×pcr反应混合试剂各组分的终浓度如下:0.05u/ultaqdna聚合酶,0.4mmdntps和4mmmgcl2。
优选的,所述的kras突变基因阳性对照拷贝数为22-28个,阴性对照拷贝数<1个。
一种检测人类kras基因突变的方法,其特征在于:包括如下步骤:
1)准备待测dna样品,样品尽可能经过多次纯化,确保没有对pcr有抑制作用的物质存在,用ddh2o稀释至浓度约为30ng/ul;
2)pcr反应体系为20μl,包括:primerf2μl,primerr2μl,probe4μl,2×pcrmix10μl,待测dna样品2μl(准备pcr反应液时按照以上体系制备22-25μl);
3)将20μlpcr体系和40μl微滴生成油加如微滴生成卡中,盖上胶垫放入微滴生成仪,生成微滴;
4)微滴生成后进行pcr扩增;
5)扩增完成使用quantasoft分析数据,阳性微滴记为1,阴性微滴记为0,根据分布图可直观得到检测结果。
优选的,所述的pcr扩增反应的条件如下:
本发明相比现有技术具有以下优点:本发明是基于ddpcr技术的kras基因突变检测试剂盒的制备,试剂盒中包括:有一对特异性引物(primerf、primerr)、一条与特异性引物配合使用的探针引物(probe)、核酸酶抑制剂(dnaseinhibitor)、2×pcr反应混合试剂(2×pcrmix)、微滴发生油、无菌蒸馏水(ddh2o)、kras突变基因阳性对照和阴性对照(ddh2o)。传统的免疫组化技术和原位杂交技术判断突变蛋白或基因状态的平均错误率超过15%,本发明利用第三代pcr技术(ddpcr)将待测样品微滴化成若干个微滴,每一个微滴都作为单独的样本进行检测,庞大的样本数大大提高了检测结果的准确度;ddpcr采用的是一对特异性引物加上一个配合使用的荧光探针,这样的引物组合也使检测的特异性更高,更稳定;ddpcr能够检测到1/100000以下浓度的目标分子,这样极高的灵敏度也是其他检测方法所不具备的;相比较与实时定量pcr,ddpcr的定量不需要通过与参照基因表达量进行比对就可以直接定量,绝对定量的结果也排除了内参基因、pcr设备、扩增效率等因素对检测结果产生的干扰,结果精确可信。本发明试剂盒检测的精确结果能够为kras基因突变相关癌症的诊断提供有力的参考依据,同时,本发明也简化了kras基因突变的检测过程,大大提高了检测效率,在一定程度上也提高了kras基因突变相关癌症的诊断效率。
附图说明
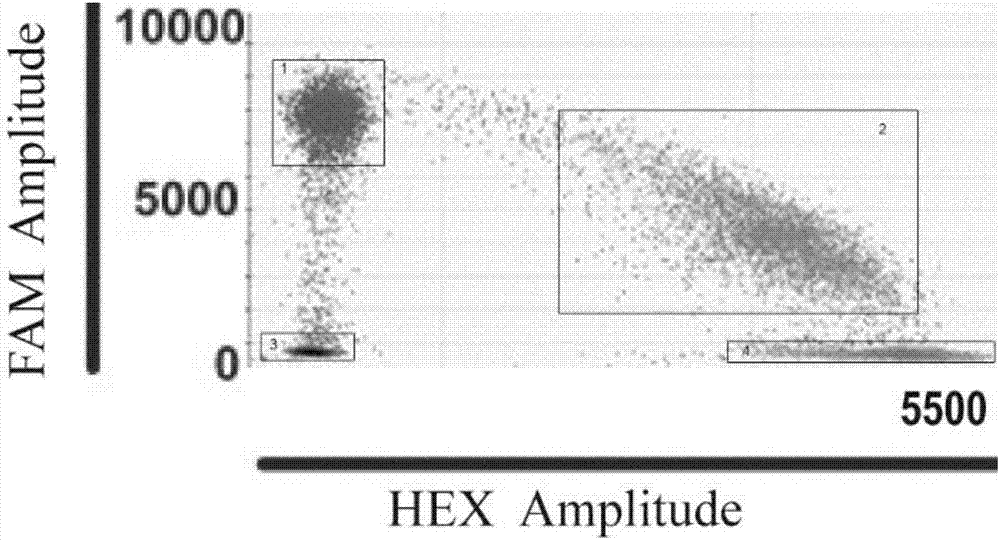
图1为实施例2设置的pcr条件下的阳性样本检测结果图;
图2为实施例3设置的pcr条件下的阳性样本检测结果图
其中,图中框1是突变dnafam阳性微滴,框2是野生型和突变型dna双阳性微滴,框3是空白微滴,框4是野生型dnahex阳性微滴。
具体实施方式
下面对本发明的实施例作详细说明,本实施例在以本发明技术方案为前提下进行实施,给出了详细的实施方式和具体的操作过程,但本发明的保护范围不限于下述的实施例。
实施例1
(1)准备待测dna样品,样品尽可能经过多次纯化,确保没有对pcr有抑制作用的物质存在,用ddh2o稀释至浓度约为30ng/μl;
(2)pcr反应体系1为20μl,包括:primerf1-42μl,primerr1-42μl,2×pcrmix10μl,待测dna样品2μl,ddh2o4μl;
(3)普通pcr反应条件设置
(4)根据琼脂糖凝胶电泳结果,选取没有非特异性扩增产生特异性条带的primerf1和primerr1作为本发明试剂盒中特异性引物。
实施例2
(1)准备待测dna样品,样品尽可能经过多次纯化,确保没有对pcr有抑制作用的物质存在,用ddh2o稀释至浓度约为30ng/μl;
(2)pcr反应体系为20μl,包括:primerf12μl,primerr12μl,probe4μl,2×pcrmix10μl,待测dna样品2μl(准备pcr反应液时按照以上体系制备22-25μl);
(3)将20μlpcr体系和40μl微滴生成油加如微滴生成卡中,盖上胶垫放入微滴生成仪,生成微滴;
(4)微滴生成后进行pcr扩增,反应条件设置为:
(5)扩增完成使用quantasoft分析数据,阳性微滴记为1,阴性微滴记为0,参照附图1可直观得到检测结果,。
实施例3
(1)准备待测dna样品,样品尽可能经过多次纯化,确保没有对pcr有抑制作用的物质存在,用ddh2o稀释至浓度约为30ng/μl;
(2)pcr反应体系为20μl,包括:primerf12μl,primerr12μl,probe4μl,2×pcrmix10μl,待测dna样品2μl(准备pcr反应液时按照以上体系制备22-25μl);
(3)将20μlpcr体系和40μl微滴生成油加如微滴生成卡中,盖上胶垫放入微滴生成仪,生成微滴;
(4)微滴生成后进行pcr扩增,反应条件设置为:
(5)扩增完成使用quantasoft分析数据,阳性微滴记为1,阴性微滴记为0,参照附图2可直观得到检测结果。
综上所述,附图1和附图2是同一阳性样本在两种不同反应条件下ddpcr分析结果,附图中框1为突变dnafam阳性微滴在泊松分布分析结果中的分布情况,附图1和附图2都显示出很高的分离度,相较而言,附图1中的阳性微滴更为集中,特异性更强,所以本发明中实施例2条件为最优选择,最适的pcr反应条件为:预变性95℃,10min;变性95℃,15sec,退火58℃,1min,循环数为40;延伸98℃,10min。
以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!