一种新型喹啉类生物硫醇荧光探针及其制备和应用的制作方法
本发明属于分析化学技术领域,尤其涉及一种新型喹啉类生物硫醇荧光探针及其制备和应用。
背景技术:
生物体内的硫醇如半胱氨酸(cys),谷胱甘肽(gsh),同型半胱氨酸(hcy)在生理和病理过程中起至关重要的作用。然而,细胞内硫醇水平的改变与很多疾病密切相关。体内缺乏半胱氨酸会导致多种病症,如儿童生长缓慢,肝损伤和皮肤损伤等。谷胱甘肽(gsh)在细胞内含量在1mm到15mm之间,是细胞内最富裕的硫醇,在维持细胞的氧化还原动态平衡中起着重要作用。血液中同型半胱氨酸的浓度增加会导致维生素b12的缺失和老年痴呆症。因此,检测生物体系中硫醇具有非常重要的意义。
目前,用于检测硫醇的方法有很多,如高效液相色谱法、电化学法、荧光法等。相比其他方法,荧光法由于具有选择性好、灵敏度高、快速简便等优点,因此,开发硫醇荧光探针越来越受到重视。
技术实现要素:
本发明要解决的技术问题是克服现有技术的不足,提供一种选择性好、灵敏度高、快速简便的新型喹啉类生物硫醇荧光探针,还相应提供该新型喹啉类生物硫醇荧光探针的制备方法及应用。
为解决上述技术问题,本发明采用以下技术方案:
一种新型喹啉类生物硫醇荧光探针,所述新型喹啉类生物硫醇荧光探针为6-二甲胺基-2-甲基-4-喹啉基-2,4-二硝基苯磺酸酯,结构式如式(1):
作为一个总的发明构思,本发明还提供一种上述的新型喹啉类生物硫醇荧光探针的制备方法,包括以下步骤:
(1)n,n-二甲基对苯二胺与乙酰乙酸乙酯发生缩合反应,得到6-二甲胺基-2-甲基-4(1h)-喹啉酮,结构式如式(2):
(2)步骤(1)所得的6-二甲胺基-2-甲基-4(1h)-喹啉酮与2,4-二硝基苯磺酰氯发生磺酰化反应,得到式(1)所示的化合物。
优选的,所述步骤(1)的具体过程为:
将n,n-二甲基对苯二胺、乙酰乙酸乙酯和冰醋酸溶于苯中,加热回流缩合反应30~35h,用分水器分离反应中生成的水分,再将缩合反应液冷却至室温,减压蒸馏除去溶剂所得的粗产物,干燥后用二苯醚溶解,在氩气保护下,加热至245~250℃回流成环反应45~50min,将成环反应液冷却至室温,再加入石油醚,过滤,所得过滤物为6-二甲胺基-2-甲基-4(1h)-喹啉酮。
优选的,所述n,n-二甲基对苯二胺和乙酰乙酸乙酯的摩尔比为1∶1.5~2。
优选的,所述步骤(2)的具体过程为:
将6-二甲胺基-2-甲基-4(1h)-喹啉酮、2,4-二硝基苯磺酰氯和三乙胺溶解于二氯甲烷中,在氩气保护下室温反应0.25~0.5h,反应完毕后,淬灭,二氯甲烷萃取,所得有机相经后处理,得到式(1)所示的化合物。
优选的,所述后处理具体过程为:将所得有机相依次用蒸馏水和饱和食盐水洗涤,再用无水na2so4干燥,经减压蒸馏除去溶剂,所得粗产物用硅胶色谱柱提纯,得到式(1)所示的化合物。
优选的,所述6-二甲胺基-2-甲基-4(1h)-喹啉酮、2,4-二硝基苯磺酰氯和三乙胺的摩尔比为1∶1.1~1.4∶1.2~1.5,柱色谱分离洗脱剂为乙酸乙酯和石油醚,所述乙酸乙酯与石油醚的体积比为1∶4~2。
作为一个总的发明构思,本发明还提供一种上述的新型喹啉类生物硫醇荧光探针或上述的制备方法制得的新型喹啉类生物硫醇荧光探针的应用,将所述新型喹啉类生物硫醇荧光探针与hepes和乙腈的缓冲液混合,再加入待测溶液中,得到混合溶液,利用混合溶液的荧光变化来检测生物硫醇的存在与否。
优选的,所述待测溶液中无生物硫醇时,所述混合溶液为无荧光发射;所述待测溶液中有生物硫醇时,所述混合溶液发出蓝色荧光。
优选的,所述新型喹啉类生物硫醇荧光探针检测生物硫醇的检出浓度下限分别为:半胱氨酸为0.5μm,谷胱甘肽为0.6μm,同型半胱氨酸为0.4μm。
与现有技术相比,本发明的优点在于:
1、基于喹啉的优良的光学性能,本发明的一种新型喹啉类生物硫醇荧光探针是以2,4-二硝基苯磺酰基为识别单元的荧光探针,实践表明,本发明的荧光探针分子在对生物硫醇进行检测时表现出了较高的选择性和灵敏度。
2、本发明的新型喹啉类生物硫醇荧光探针的制备方法,只需要两步就可以完成,且后处理过程简单,适于工业化生产。
附图说明
图1为实施例1的式(1)所示的化合物(即新型喹啉类生物硫醇荧光探针)的合成路线图。
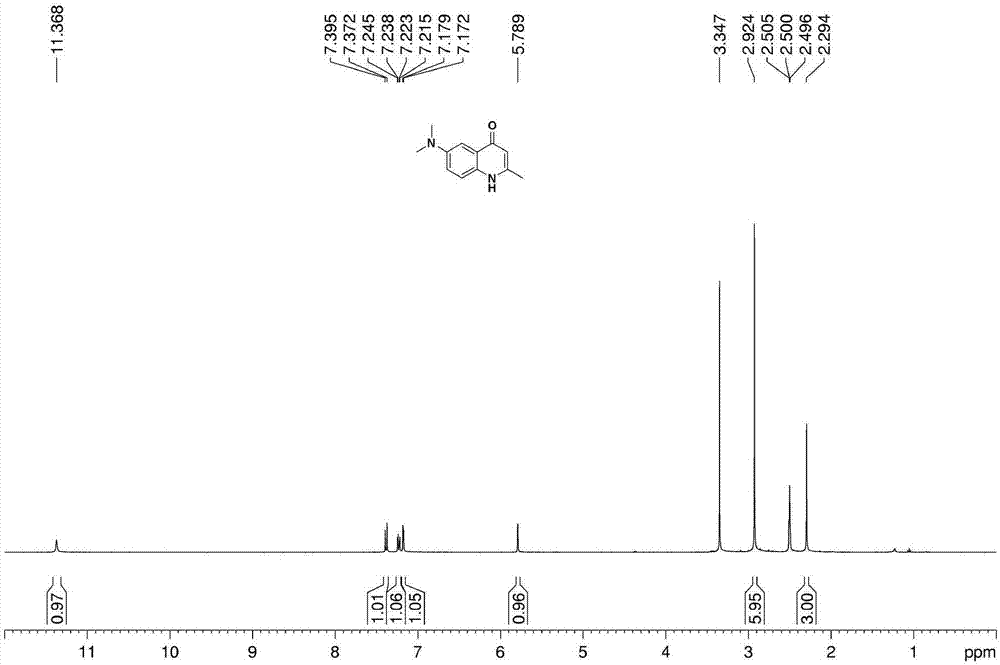
图2为实施例1制备的式(2)所示的化合物的1hnmr图谱。
图3为实施例1制备的式(2)所示的化合物的13cnmr图谱。
图4为实施例1制备的式(2)所示的化合物的esi-ms图谱。
图5为实施例1制备的式(1)所示的化合物的1hnmr图谱。
图6为实施例1制备的式(1)所示的化合物的13cnmr图谱。
图7为实施例1制备的式(1)所示的化合物的esi-ms图谱。
图8为不同ph值对实施例1制备的式(1)所示的化合物和式(2)所示的化合物的荧光强度的影响。
图9为式(2)所示的化合物、式(1)所示的化合物与生物硫醇(cys、gsh和hcy)反应前后的吸收光谱((a)图)和荧光光谱图((b)图)。
图10为实施例1的式(1)所示的化合物与cys反应后的荧光光谱图;其中,(a)图为(1)所示的化合物与cys反应后不同光谱条件下荧光光谱的变化,(b)图为式(1)所示的化合物与cys反应后在472nm处的荧光强度随时间的变化。
图11为实施例1的式(1)所示的化合物与gsh反应后的荧光光谱图;其中,(a)图为式(1)所示的化合物与gsh反应后不同光谱条件下荧光光谱的变化,(b)图为式(1)所示的化合物与gsh反应后在472nm处的荧光强度随时间的变化。
图12为实施例1的式(1)所示的化合物与hcy反应后的荧光光谱图;其中,(a)图为式(1)所示的化合物与hcy反应后不同光谱条件下荧光光谱的变化,(b)图为式(1)所示的化合物与hcy反应后在472nm处的荧光强度随时间的变化。
图13为实施例1的式(1)所示的化合物(即新型喹啉类生物硫醇荧光探针)对生物硫醇检测的反应机理图。
图14为实施例1的式(1)所示的化合物分别与各种氨基酸和常见金属离子反应后在472nm处的荧光强度;
图15为实施例1的式(1)所示的化合物分别与各种氨基酸和常见金属离子反应后的荧光颜色。
图16为不同cys浓度对实施例1的式(1)所示的化合物与cys反应后在472nm处荧光强度的影响示意图;其中(a)图为不同cys浓度条件下,式(1)所示的化合物与cys反应后在472nm处荧光强度随时间的变化,(b)图为式(1)所示的化合物在472nm处的荧光强度随cys浓度的变化。
图17为不同gsh浓度对实施例1的式(1)所示的化合物与gsh反应后在472nm处荧光强度的影响示意图;其中(a)图为不同gsh浓度条件下,式(1)所示的化合物与gsh反应后在472nm处荧光强度随时间的变化,(b)图为式(1)所示的化合物在472nm处的荧光强度随gsh浓度的变化。
图18为不同hcy浓度对实施例1的式(1)所示的化合物与hcy反应后在472nm处荧光强度的影响示意图;其中(a)图为不同hcy浓度条件下,式(1)所示的化合物与hcy反应后在472nm处荧光强度随时间的变化,(b)图为式(1)所示的化合物在472nm处的荧光强度随hcy浓度的变化。
具体实施方式
以下结合具体优选的实施例对本发明作进一步描述,但并不因此而限制本发明的保护范围。
实施例1:
一种本发明的新型喹啉类生物硫醇荧光探针,名称为6-二甲胺基-2-甲基-4-喹啉基-2,4-二硝基苯磺酸酯,分子式为c18h16n4o7s,结构式如式(1)所示:
上述本实施例的新型喹啉类生物硫醇荧光探针的制备方法,其合成路线如图1所示,包括以下步骤:
(1)合成化合物6-二甲胺基-2-甲基-4(1h)-喹啉酮,结构式如式(2):
反应式如式(3):
具体过程为:将n,n-二甲基对苯二胺(1.0g,6mmol),乙酰乙酸乙酯(1.6g,12mmol),冰醋酸(0.5ml)溶于苯(30ml)中,加热回流30小时,并用deanestark分水器除去反应中生成的水分,反应完成后,将反应液冷却至室温,减压蒸馏除去溶剂得到粗产物。将其溶于二苯醚(20ml)中,在氩气保护下,加热至250℃回流反应50min。将反应液冷却至室温,此时有大量沉淀开始析出。加入石油醚,使产物完全沉淀。过滤,用石油醚洗涤,即得到6-二甲胺基-2-甲基-4(1h)-喹啉酮,产率为42%。
所得的6-二甲胺基-2-甲基-4(1h)-喹啉酮的1hnmr图谱如图2所示,1hnmr(400mhz,d6-dmso,ppm)δ11.37(s,1h),7.40(d,j=9.2hz,1h),7.25(dd,j=2.8hz,j=8.8hz,1h),7.18(d,j=2.8hz,1h),5.79(s,1h,2.92(s,6h),2.29(s,3h)。
所得的6-二甲胺基-2-甲基-4(1h)-喹啉酮的13cnmr图谱如图3所示,13cnmr(100mhz,d6-dmso,ppm)δ176.25,147.61,146.75,132.24,125.55,119.31,118.62,106.87,104.46,40.57,19.34。
所得的6-二甲胺基-2-甲基-4(1h)-喹啉酮的esi-ms图谱如图4所示,esi-msm/zforc12h15n2o+([m+h]+):calcd:203.1,found:203.2。
(2)合成结构式如式(1)所示的6-二甲胺基-2-甲基-4-喹啉基-2,4-二硝基苯磺酸酯:
反应式如式(4):
具体过程为:将步骤(1)所得的6-二甲胺基-2-甲基-4(1h)-喹啉酮(202mg,1mmol)、2,4-二硝基苯磺酰氯(301mg,1.2mmol)和三乙胺(0.2ml,1.5mmol)溶解在无水二氯甲烷(20ml)中,在氩气保护下室温反应0.5h,反应完毕后,用水(8ml)淬灭,再采用二氯甲烷分两次萃取,每次萃取剂用量20ml,合并有机相,依次用蒸馏水和饱和食盐水洗涤、再用无水na2so4干燥有机相后,减压蒸馏除去溶剂得到粗产物,随后用硅胶色谱柱提纯,柱色谱分离洗脱剂为乙酸乙酯和石油醚,乙酸乙酯与石油醚的体积比为1∶4~2,得到硫醇荧光探针,即式(1)所示的化合物,产率为86%。
式(1)所示的化合物的1hnmr图谱如图5所示,1hnmr(400mhz,cdcl3,ppm)δ8.63(d,j=2.0hz,1h),8.43(dd,j=2.0hz,j=8.4hz,1h),8.20(d,j=8.8hz,1h),7.84(d,j=9.2hz,1h),7.30(dd,j=2.8hz,j=9.2hz,1h),7.21(s,1h),6.87(d,j=2.8hz,1h),2.98(s,6h),2.68(s,3h)。
式(1)所示的化合物的13cnmr图谱如图6所示,13cnmr(100mhz,cdcl3,ppm)δ154.24,151.29,151.03,148.80,143.68,133.96,133.72,129.25,126.73,121.49,120.42,120.36,113.70,97.39,40.54,25.01。
式(1)所示的化合物的esi-ms图谱如图7所示,esi-msm/zforc18h17n4o7s+([m+h]+):calcd:433.1:found:433.1。
上述本实施例制得的新型喹啉类生物硫醇荧光探针的应用,将10mmhepes/ch3cn体积比为4∶1,ph7.0的缓冲溶液2ml加入比色皿中,加入本实施例制得的新型喹啉类生物硫醇荧光探针混合均匀后,再加入待测溶液进行测试,该待测溶液中无生物硫醇时,混合溶液为无荧光发射;该待测溶液中有生物硫醇时,混合溶液发出蓝色荧光。
上述本实施例制得的新型喹啉类生物硫醇荧光探针的应用研究:
1、ph值对式(1)所示的化合物和式(2)所示的化合物的荧光强度的影响
取实施例1合成的式(1)所示的化合物和式(2)所示的化合物溶于二甲基亚砜中,分别制成2mmol/l的储备液。当ph值不同时,在室温下以405nm为激发光测量式(1)所示的化合物和式(2)所示的化合物的荧光性质,结果如图8所示。实验结果表明,式(1)所示的化合物和式(2)所示的化合物在生理ph5.0~9.0范围内荧光性质几乎不变。
2、式(1)所示的化合物和式(2)所示的化合物与生物硫醇(cys、gsh和hcy)反应的吸收光谱和荧光光谱研究
在最佳测试条件下,即20mmhepes,h2o/ch3cn为4∶1,v/v,ph7.4,25℃,研究式(1)所示的化合物和式(2)所示的化合物与生物硫醇反应的吸收光谱和荧光光谱性质,结果如图9所示。图9中(a)图为式(1)所示的化合物和式(2)所示的化合物与生物硫醇反应前后的吸收光谱图,(b)图为式(1)所示的化合物和式(2)所示的化合物与生物硫醇反应前后的荧光光谱图。化合物2与生物硫醇反应后不同光谱条件下荧光光谱的变化,如图10(a)图(cys),图11(a)图(gsh)和图12(a)图(hcy)所示;化合物2与生物硫醇反应后在472nm处的荧光强度随时间的变化,如图10(b)图(cys),图11(b)图(gsh)和图12(b)图(hcy)所示。实验结果证明,式(1)所示的化合物适用于生物硫醇的快速检测,原理图如图13所示,生物硫醇的巯基通过亲核取代反应,使2,4-二硝基苯磺酰基从式(1)所示的化合物上脱去,使其失去淬灭作用,从而生产强荧光的6-二甲胺基-2-甲基-4(1h)-喹啉酮。
3、式(1)所示的化合物对生物硫醇的选择性研究
为测试式(1)所示的化合物对生物硫醇的选择性,对式(1)所示的化合物与各种氨基酸和常见金属离子:gly,ser,leu,glu,pro,asn,phe,met,na+,k+,ca2+,mg2+,cys,gsh,hcy,反应后在472nm处的荧光强度和荧光颜色变化进行了实验研究,结果如图14和图15所示。由图14和图15可知,式(1)所示的化合物对生物硫醇的检测具有高度的选择性。
4、式(1)所示的化合物检测生物硫醇的灵敏度研究
不同生物硫醇浓度[0-35μm(cys),0-50μm(gsh),0-60μm(hcy)]条件下,式(1)所示的化合物与生物硫醇反应后在472nm处荧光强度随时间的变化分别如图16(a)图(cys),图17(a)图(gsh)和图18(a)图(hcy)所示,式(1)所示的化合物在472nm处的荧光强度随生物硫醇浓度的变化分别如图16(b)图(cys),图17(b)图(gsh)和图18(b)(hcy)所示。由图16(a)图(cys),图17(a)图(gsh)和图18(a)图(hcy)可知,高浓度生物硫醇提供更快和更戏剧性的荧光增强。由图16(b)图(cys),图17(b)图(gsh)和图18(b)(hcy)可以推算出式(1)所示的化合物检测生物硫醇的检测限分别为0.5μm(cys),0.6μm(gsh),0.4μm(hcy)。
以上所述,仅是本申请的较佳实施例,并非对本申请做任何形式的限制,虽然本申请以较佳实施例揭示如上,然而并非用以限制本申请,任何熟悉本专业的技术人员,在不脱离本申请技术方案的范围内,利用上述揭示的技术内容做出些许的变动或修饰均等同于等效实施案例,均属于技术方案范围内。
- 还没有人留言评论。精彩留言会获得点赞!