新C33丛粒藻烷、丛粒藻烷酮及其制备方法和应用与流程
本发明属于地球化学技术领域,具体涉及新c33丛粒藻烷、丛粒藻烷酮及其制备方法和应用。
背景技术:
化石燃料生物标志化合物是沉积有机质、原油、油页岩、煤等中来源于活的生物体,在有机质演化过程中具有一定稳定性,基本保存了原始生化组分的碳骨架,记载了原始生物母质的特殊分子结构信息的有机化合物,包括只含碳、氢元素的烃类化合物以及与其骨架相似的含氧、硫、氮杂原子的非烃类生物标志化合物(它们往往是沉积有机质在向烃类化合物演化过程中的中间产物)。这些化合物的分子组成特征与结构信息可用于判断沉积物的母质类型和沉积环境,并研究有机质的成岩演化和经历的生物降解作用,被广泛应用于石油成因理论研究和烃类生物标志物的生源研究。近十几年来,它们尚被应用于研究油藏地球化学,原油的二次运移,古环境、古气候、油-油对比和严重生物降解油源探索等领域。
其中,丛粒藻类化合物是非常独特的生物标志化合物,只产生于b属丛粒藻(布朗葡萄藻)。丛粒藻是一种淡水浮游绿藻,其提取液的化学成分与石油的化学成分相似,是一种“石油植物”,又被称为油藻,地下的有些石油就是由这些藻产生的。这些藻可产生大量的液态碳氢化合物,用于生产汽油、煤油和柴油。因此,丛粒藻类生物标志化合物的探索发现与研究,对于石油成因的研究、生物能源探索与开发具有十分重要的意义。
技术实现要素:
本发明的目的是提供一种能够指示丛粒藻生源、反映沉积环境、地质氧化还原作用以及推断丛粒藻中新的类异戊二烯四元环合成途径存在的两种新的丛粒藻类生物标志化合物新c33丛粒藻烷和丛粒藻烷酮。
所述的新c33丛粒藻烷,其化学名称为:2,3,6,7,10,12,15,16,19,20-十甲基-10-乙基-二十一烷;其化学结构如式ⅰ所示:
所述的丛粒藻烷酮,其化学名称为:3,5,8,9,12,13-六甲基-3-(3,4,7,8-四甲基-九烷基)-十四烷基-2-酮;其化学结构如式ⅱ所示:
本发明的第二个目的是提供新c33丛粒藻烷或丛粒藻烷酮在推断丛粒藻生物体中一种四元环的类异戊二烯合成路径中的应用。
本发明的第三个目的是提供新c33丛粒藻烷或丛粒藻烷酮在指示地质氧化、氢化情况中的应用。
本发明的第四个目的是提供一种新c33丛粒藻烷和丛粒藻烷酮的制备方法,该方法包括以下步骤:
(1)提取、分离:将选自广东省西南部茂名盆地第三系油柑窝组油页岩富含丛粒藻烷的块状样品粉碎至100目以下,用体积比为9:1的二氯甲烷/甲醇溶液进行索氏抽提,提取液经浓缩得到氯仿沥青“a”;将氯仿沥青“a”溶解于正己烷中,经多次离心分离除去不溶物质沥青质后,滤液经过浓缩,用柱色谱进行分离,用体积比为4:1的硅胶(80~100目)和氧化铝(分析纯)填柱;上样后,用正己烷洗脱得到饱和烃组分,用体积比为3:2的正己烷/二氯甲烷溶液洗脱得到芳香烃组分,用甲醇洗脱得到非烃组分;用填充有100~230目硅胶的柱色谱继续分离非烃组分,用体积比为1:2的二氯甲烷/正己烷溶液洗脱得到非烃目标组分,其中,2,3,6,7,10,12,15,16,19,20-十甲基-10-乙基-二十一烷来自于饱和烃组分,3,5,8,9,12,13-六甲基-3-(3,4,7,8-四甲基-九烷基)-十四烷基-2-酮来自于非烃目标组分;
(2)制备:使用agilent7890-gerstelpfc气相制备色谱仪制备,分离柱为安捷伦db-5,60m×0.530mm×1.50μm的大容量气相色谱柱;饱和烃组分和非烃目标组分均溶于异辛烷进样;饱和烃组分制备2,3,6,7,10,12,15,16,19,20-十甲基-10-乙基-二十一烷时,气相色谱升温程序为:初始温度80℃,保留2min,其后以30℃/min升到300℃,保留40min,饱和烃组分样品连续自动进样,收集保留时间为42.02~43.05min的化合物,即为2,3,6,7,10,12,15,16,19,20-十甲基-10-乙基-二十一烷;非烃目标组分制备3,5,8,9,12,13-六甲基-3-(3,4,7,8-四甲基-九烷基)-十四烷基-2-酮时,气相色谱升温程序为:初始温度80℃,保留2min,其后以10℃/min升到220℃,以3℃/min升到300℃,保留10min,样品连续自动进样,收集保留时间为48.79~49.62min的化合物,即为3,5,8,9,12,13-六甲基-3-(3,4,7,8-四甲基-九烷基)-十四烷基-2-酮。
与现有技术相比,本发明具有以下有益效果:
丛粒藻生物体内直接合成的是丛粒藻烯,本发明提供的是由丛粒藻烯在地质作用中生成的丛粒藻烷和丛粒藻烷酮,分别为2,3,6,7,10,12,15,16,19,20-十甲基-10-乙基-二十一烷和3,5,8,9,12,13-六甲基-3-(3,4,7,8-四甲基-九烷基)-十四烷基-2-酮,该两种化合物作为新的丛粒藻类生物标志化合物可用于指示丛粒藻生源、反映沉积环境、地质氧化还原作用以及推断丛粒藻中新的类异戊二烯四元环合成途径的存在。
附图说明
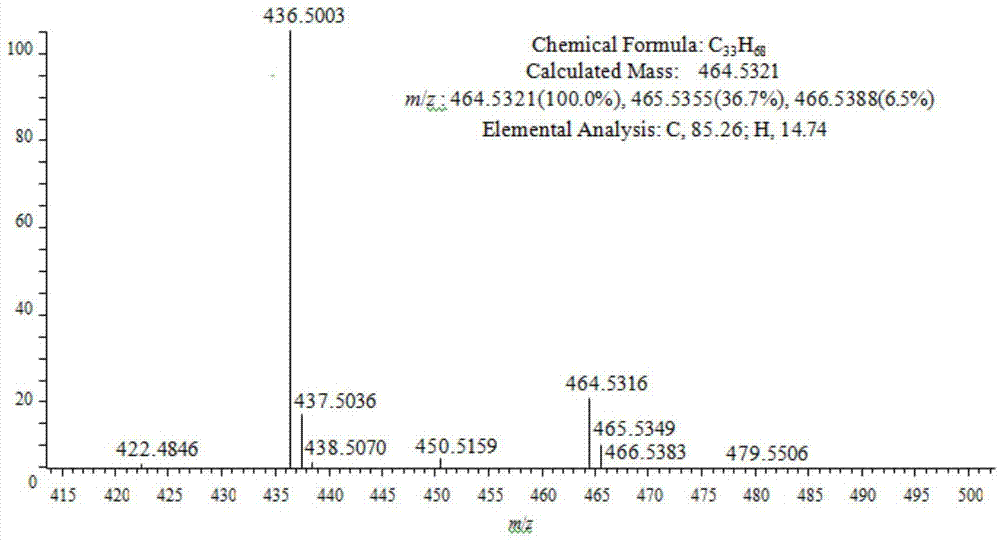
图1为化合物1的hr-ei-ms谱。
图2为化合物1的1h谱。
图3为化合物1的13c谱。
图4为化合物1的hmqc谱。
图5为化合物1的1h-1hcosy谱。
图6为化合物1的hmbc谱。
图7为化合物2的hr-ei-ms谱。
图8为化合物2的1h谱。
图9为化合物2的13c谱。
图10为化合物2的hmqc谱。
图11为化合物2的1h-1hcosy谱。
图12为化合物2的hmbc谱。
图13为化合物2的ir谱。
具体实施方式
以下实施例是对本发明的进一步说明,而不是对本发明的限制。
实施例1
1、样品前处理
将富含丛粒藻烷的块状样品(取自广东省西南部茂名盆地第三系油柑窝组油页岩)粉碎至100目以下,称取100g粉末样品,用体积比为9:1的二氯甲烷/甲醇溶液进行索氏抽提,提取液经减压浓缩后得到有机质氯仿沥青“a”。将氯仿沥青“a”溶解于正己烷中,经多次离心分离除去不溶物质沥青质后,滤液用柱色谱方法分离。其中,柱子使用长为30cm,内径为1cm的空心玻璃柱,并充填体积比为4:1的硅胶(80-100目)和化学纯的氧化铝,加入样品后,用80ml正己烷洗脱得到饱和烃组分,用50ml体积比为3:2的正己烷/二氯甲烷溶液洗脱得到芳香烃组分,用40ml甲醇洗脱得到非烃组分。三个组分样品分别使用100ml的鸡心瓶收集,溶剂用旋转蒸发仪抽干,将样品转移至4ml细胞瓶恒重。用填充有100-230目硅胶的长为30cm,内径为1cm的玻璃柱继续分离非烃组分,用80ml体积比为1:2的二氯甲烷/正己烷溶液洗脱得到非烃目标组分,然后转移至4ml细胞瓶恒重。将所得到的饱和烃组分和非烃目标组分分别用异辛烷溶解,调配浓度为50mg/ml,装入2ml细胞进样瓶,用于下述步骤2的样品制备。
2、样品制备:
使用agilent7890-gerstelpfc(全自动气相色谱馏分收集器)气相制备色谱仪制备,分离柱为安捷伦db-5,60m×0.530mm×1.50μm的大容量气相色谱柱。载气使用氦气(纯度99.999%),流速为3ml/min。在大口径色谱柱后配备馏分分流器,样品经色谱柱分离后,通过馏分分流器的分流作用,10%进入fid检测器,以确定目标化合物的流出时间;其余90%进入馏分收集装置,目标化合物通过冷阱捕集来实现收集。冷阱包括6个样品捕集阱和1个废弃物捕集阱,可设计捕集时间,配备液氮冷凝。
饱和烃组分和非烃目标组分均溶于异辛烷进行进样。饱和烃组分制备2,3,6,7,10,12,15,16,19,20-十甲基-10-乙基-二十一烷时,气相色谱升温程序为:初始温度80℃,保留2min,其后以30℃/min升到300℃,保留40min,饱和烃组分样品连续自动进样,进样体积5μl,收集保留时间为42.02~43.05min的化合物,平均进样20次取下收集管将化合物洗出,装入4ml细胞瓶,恒重,即为化合物1:2,3,6,7,10,12,15,16,19,20-十甲基-10-乙基-二十一烷。非烃目标组分制备3,5,8,9,12,13-六甲基-3-(3,4,7,8-四甲基-九烷基)-十四烷基-2-酮时,气相色谱升温程序为:初始温度80℃,保留2min,其后以10℃/min升到220℃,以3℃/min升到300℃,保留10min,样品连续自动进样,进样体积5μl,收集保留时间为48.79~49.62min的化合物,平均进样20次取下收集管将化合物洗出,装入4ml细胞瓶,恒重,即为化合物2:3,5,8,9,12,13-六甲基-3-(3,4,7,8-四甲基-九烷基)-十四烷基-2-酮。
将制备得到的化合物1和化合物2通过高分辨质谱、红外、核磁共振等方法确定具体结构。
化合物1的高分辨质谱和核磁共振数据如图1-6和表1所示,由此确定化合物1为2,3,6,7,10,12,15,16,19,20-十甲基-10-乙基-二十一烷,其结构如式ⅰ所示:
表1化合物1的核磁共振数据(1h(600mhz)and13c(150mhz)nmr)
化合物2的高分辨质谱、核磁共振和红外数据如图7-13和表2所示,由此确定化合物2为3,5,8,9,12,13-六甲基-3-(3,4,7,8-四甲基-九烷基)-十四烷基-2-酮,其结构如式ⅱ所示:
表2化合物2的核磁共振数据(1h(600mhz)and13c(150mhz)nmr)
实施例2
化合物1和化合物2的单体碳同位素δ13c分别为-8.7‰和-12.4‰,与b属丛粒藻的产物以及衍生产物的δ13c相似(dowlingetal.,1995),都很重。同时,都有相似的季碳直接连接甲基乙基基团的骨架,因此,我们认为本发明的化合物1:2,3,6,7,10,12,15,16,19,20-十甲基-10-乙基-二十一烷和化合物2:3,5,8,9,12,13-六甲基-3-(3,4,7,8-四甲基-九烷基)-十四烷基-2-酮是来自于油藻丛粒藻的藻烯所衍生,就如文献中的各种c34丛粒藻烷(volkmanetal,2014)。如式ⅲ所示,其表明了2,3,6,7,10,12,15,16,19,20-十甲基-10-乙基-二十一烷和3,5,8,9,12,13-六甲基-3-(3,4,7,8-四甲基-九烷基)-十四烷基-2-酮的生成途径,具体为:生物体内两个fpp通过四元环化、阳离子作用开环,反向普林斯反应(al-qallafetal.,2000)以及在甲基化酶(metzgeretal.,1985,1986)的作用下最终生成c33藻烯,生物体沉积过程中,在地质水体氧化环境下,c33藻烯的乙烯基发生双键光氧化,形成羰基,其它双键氢化还原,导致化合物2:3,5,8,9,12,13-六甲基-3-(3,4,7,8-四甲基-九烷基)-十四烷基-2-酮的生成,其后在成岩作用中,3,5,8,9,12,13-六甲基-3-(3,4,7,8-四甲基-九烷基)-十四烷基-2-酮发生氢化还原、脱水、氢化作用,最终生成化合物1:2,3,6,7,10,12,15,16,19,20-十甲基-10-乙基-二十一烷。因此,2,3,6,7,10,12,15,16,19,20-十甲基-10-乙基-二十一烷和3,5,8,9,12,13-六甲基-3-(3,4,7,8-四甲基-九烷基)-十四烷基-2-酮作为生物标志化合物不仅指示了b属丛粒藻的生物来源,提供了一条全新的丛粒藻烯生物合成路径,还指示了地质作用的氧化还原情况。
参考文献:
al-qallaf,f.a.,hodson,l.f.,johnstone,r.a.,liu,j.y.,lu,l.,whittaker,d.,2000.heterogeneousliquidphasecatalysisbymetal(iv)phosphatesofcyclicetherformationandareverseprinsreaction.journalofmolecularcatalysisa:chemical152,187-200.
metzger,p.,casadevall,e.,pouet,m.j.,pouet,y.,1985.structuresofsomebotryococcenes:branchedhydrocarbonsfromtheb-raceofthegreenalgabotryococcusbraunii.phytochemistry24,2995-3002.
metzger,p.,david,m.,casadevall,e.,1986.biosynthesisoftriterpenoidhydrocarbonsintheb-raceofthegreenalgabotryococcusbraunii.sitesofproductionandnatureofthemethylatingagent.phytochemistry26,129-134.
volkmanjk.acyclicisoprenoidbiomarkersandevolutionofbiosyntheticpathwaysingreenmicroalgaeofthegenusbotryococcus[j].organicgeochemistry,2014,75:36-47.
dowling,l.m.,boreham,c.j.,hope,j.m.,murray,a.p.,&summons,r.e.(1995).carbonisotopiccompositionofhydrocarbonsinocean-transportedbitumensfromthecoastlineofaustralia.organicgeochemistry,23(8),729-737.
以上仅是本发明的优选实施方式,应当指出的是,上述优选实施方式不应视为对本发明的限制,本发明的保护范围应当以权利要求所限定的范围为准。对于本技术领域的普通技术人员来说,在不脱离本发明的精神和范围内,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!