一种合成锂离子电池正极材料及其制备方法与流程
本发明属于锂离子电池技术领域,尤其涉及一种合成锂离子电池正极材料及其制备方法。
背景技术:
社会快速发展,人们的生活质量日益提高,但同样也面临着两大发展瓶颈,能源危机与环境污染。现况表明,矿物材料难以维持能源体系的巨大消耗,所以作为可再生利用的高能清洁能源锂离子电池就应运而生。20世纪90年代以来,锂离子电池凭借其能量高、容量大、电压特性曲线平稳、循环寿命长、无记忆效应、污染小等优点,迅速成为世界各国的研发重点。同时,随着社会日益信息化,IT行业的蓬勃发展,便携式手提笔记本电脑、移动电话、摄像机等设备的普遍应用,迫切地要求锂电池有新的发展。我国具有丰富的锂矿资产,从上个世纪60年代开始着手研究锂电池,80年代推出了商品化的Li/MnO2、Li/SOCl2和Li/SO2电池,90年代研制出Li/V6O13二次电池。但锂电池存在着循环寿命低、安全性差的缺点。锂电池是以金属锂作为电池负极的二次电池体系,在反复充放电过程中锂离子易沉积在金属锂负极的表面形成锂枝晶。当枝晶发展到一定程度时,一方面会发生折断,产生“死锂”,造成锂的不可逆;另一方面更严重的是,枝晶穿过隔膜,将正极与负极连接起来,结果产生大电流,生成大量的热,使电池着火,甚至发生爆炸,从而引起严重的安全问题。1990年日本Sony能源技术公司首先推出LixC6/LiClO4-PC+EC/Li1-xCO2实用型锂离子电池,克服了锂电池循环寿命低、安全性差等缺陷,掀起了锂离子电池的研究热潮。2011年4月工信部发布了《新材料产业“十二五”重点产品目录》,将钴酸锂正极材料也列入为这批重点项目。2012年4月科技部发布的《电动汽车科技发展“十二五”专项规划》指出“以锂离子动力电池为重点的车用电池产业竞争能力等方面处于国际先进水平”。钴酸锂正极材料由于其具有的特点,在小型和便携式电子设备中的应用前景相当广阔。LiCoO2材料的理论克容量达到270mAh/g,然而实际可用容量却远小于理论值,基本上约为135mAh/g。其中主要的原因是:为了防止钴酸锂的结构在过充电和过放电过程中的结构破坏和电池的安全性能,限制了材料充放电的截至电压,所以,通常钴酸锂材料中只有一半的锂离子实际可用,导致钴酸锂正极材料的实际容量只有理论容量的一半。为了提高LiCoO2材料的实际可用容量,同时保证其结构的稳定性,现在通常采用的办法是引入一定量的其它离子来增加LiCoO2的结构的稳定性,提高电池的实际容量。
锂离子电池的主要结构包括正极、负极、电解液、隔膜、正负极引线、电池壳等,其中正极材料对锂离子电池的性能具有重要的影响。正极材料的制备方法主要包括高温固相合成法、低温固相合成法、沉淀-冷冻法、喷雾干燥法、溶胶-凝胶法、微波合成法、水热合成法等,目前,最常用的是高温固相合成法。高温固相法是目前LiCoO2的制备中使用最广、最成熟的合成方法,主要步骤是将锂和钴的化合物按n(Li)/n(Co)=1的摩尔比混合,碾磨后将其置于空气的气氛中烧结,烧结温度一般控制在700-900℃,具体工艺根据原材料的成分而定。雷永泉等人将Li2CO3和Co2O3按n(Li)/n(Co)=1的摩尔比混合后,在空气的气氛中先后置于600℃烧结5h,900℃烧结10h,制得稳定的、电化学性能表现良好的LiCoO2。高温固相合成法因其制备方法简单而被工业化生产,但它也存在着问题,例如反应物难混合,反应温度高,反应时间长,产物形貌不规则,粒径宽,电化学性能难以控制。低温固相合成法克服了高温固相合成法的某些缺陷。低温固相合成法主要应用于过渡金属配合物的合成,主要步骤为将锂和钴的化合物按n(Li)/n(Co)=1的摩尔比混合,加入溶剂,然后将该物质置于低温干燥箱中干燥,紧接着在高温的仪器中烧结。用低温固相法合成的物质形态完整,颗粒大小均匀。溶胶-凝胶法可得到纯度高、均匀性好的产品。一般采用含高化学活性组分的化合物作为前驱体,原料经过液相混合、干燥、烧结制备,所得产品除了纯度高、均匀性好等优点,溶胶-凝胶法还可以均匀地掺入微量元素,实现分子水平上的掺杂,并且溶胶-凝胶法所需的反应温度较低,便于控制。但溶胶-凝胶法也存在着问题:陈化时间过长,干燥、烧结时常会形成大量微孔,这些问题都有待改进。Won-Sub Yoon等采用丙烯酸作为载体制备掺杂的LiAly Co1-y O2,在600℃热处理温度时,容量和循环性能较好,初始可逆容量达160mAh/g,10次循环后主体结构没有明显变化。廖钦林等人通过掺杂Cu元素,制备得到电化学性能良好的掺Cu钴酸锂正极材料,测试显示该材料的振实密度超过2.8g/cm3,可逆嵌脱锂容量超过140mAh/g。周建等人采用湿化学法往LiCoO2中掺入B元素,在650-1000℃范围内烧结5-15h,这样得到的样品的层状结构性质不改变,单颗颗粒生长更加完整,且掺B的钴酸锂已长大至3-5um,比未掺B的钴酸锂颗粒大2-4um,从而其电化学循环性能也有所提高。Xiaoming zhu等人对Mg掺杂钴酸锂的结构和性能进行了研究,分析表明所得样品具有良好层状结构的六边形颗粒,且样品的循环性能有所提高,初始放电容量可达169.2mAh/g,50次循环后,仍能保持初始容量的91.1%。
综上所述,现有的LiCoO2材料的理论克容量达到270mAh/g,然而其实际可用容量却远小于理论值,基本上为其理论容量的一半,约为135mAh/g。现有的改进方法和研究方法是对其体相进行离子掺杂改性,但是这些制备方法存在反应物难以混合均匀,反应温度高,反应时间长,容易产生团聚、元素分布不均匀,制备工序繁琐,干燥时间长、电化学性能难以控制等缺点。
技术实现要素:
本发明的目的在于提供一种合成锂离子电池正极材料及其制备方法,旨在解决现有的LiCoO2材料的理论克容量达到270mAh/g,然而其实际可用容量却远小于其理论值的问题,以及其掺杂改性的制备方法存在的反应物难以混合均匀,反应温度高,反应时间长,容易产生团聚、元素分布不均匀,制备工序繁琐,干燥时间长、电化学性能难以控制等问题。
本发明是这样实现的,一种合成锂离子电池正极材料,所述合成的正极材料为LiAl0.01Co0.99O2,其中n(Li):n(Co):n(Al)=1:0.99:0.01;n为摩尔比。
本发明的另一目的在于提供一种所述合成锂离子电池正极材料的制备方法,所述合成锂离子电池正极材料的制备方法包括:
步骤一,按LiAl0.01Co0.99O2中n(Li):n(Co):n(Al)=1:0.99:0.01称取LiNO3、Co(NO3)2·6H2O和Al(NO3)3·9H2O,用玛瑙研钵充分碾磨,直至其结晶水完全析出;
步骤二,然后置于鼓风干燥箱中进行干燥;待水份蒸发后将物质取出,再次碾磨,放入管式电阻炉中,在温度300℃下预烧4h,800℃下烧结10h。
本发明的另一目的在于提供一种由所述合成锂离子电池正极材料制造的锂离子电池。
本发明的另一目的在于提供一种安装有所述锂离子电池的电动汽车。
本发明的另一目的在于提供一种安装有所述锂离子电池的汽车。
本发明提供的合成锂离子电池正极材料及其制备方法,采用流变-固相法合成锂离子电池的正极材料,通过热重法(TG)测量正极材料的质量随温度的变化,分析获得反应的最适宜温度;通过对材料进行X射线衍射(XRD)和扫描电子显微镜(SEM)手段表征,正极材料有良好的层状结构;通过对LiCoO2正极材料电化学性能的测试,样品具有良好的电化学循环性能;通过掺杂金属元素Al,成功得到LiAl0.01Co0.99O2正极材料,测试表明所得物质没有杂质存在,晶体结构良好,表现出明显的层状结构,且颗粒大小分布均匀,直径平均为1um;对其进行电化学性能测试,发现得到的LiAl0.01Co0.99O2有平稳的充放电平台,首次充放电效率达到100%,该材料的比容量在充放电2.7—4.3V范围内可以达到205mAh/g。本发明的钴酸锂正极材料有理想的层状结构,钴层和锂层交替分布于氧层两侧,占据四面体孔隙,可以为Li+的脱嵌提供较大的孔径隧道,从而使得Li+的扩散系数和迁移系数得到提高;同时,钴酸锂的层状结构,在保证Li+保持较高扩散速度的同时提高了其最大工作电流,可以5C放电。
附图说明
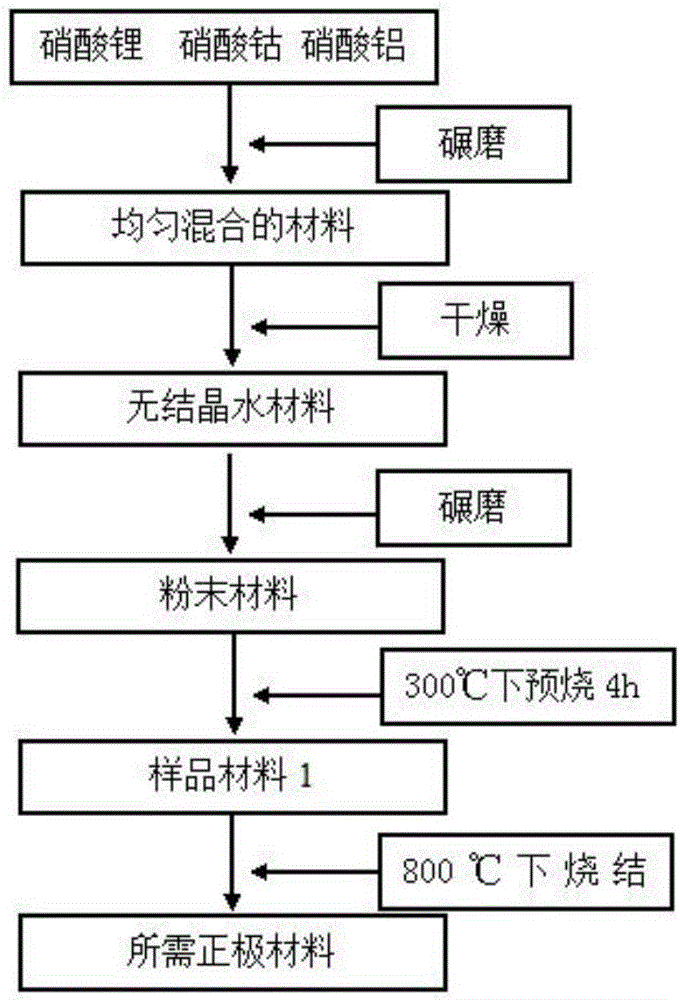
图1是本发明实施例提供的合成锂离子电池正极材料的制备方法流程图。
图2是本发明实施例提供的Al掺杂制备LiCoO2正极材料的流程图。
图3是本发明实施例提供的Co2O3和Li2CO3合成LiCoO2的热失重曲线示意图。
图4是本发明实施例提供的Co2O3和Li2CO3合成LiCoO2的XRD示意图。
图5是本发明实施例提供的Co2O3和Li2CO3合成LiCoO2的SEM示意图。
图6是本发明实施例提供的Co2O3和Li2CO3合成LiCoO2的首次充放电曲线示意图。
图7是本发明实施例提供的Co2O3和Li2CO3合成LiCoO2的充放电循环曲线示意图。
图8是本发明实施例提供的Co2O3和Li2CO3合成LiCoO2不同倍率下充放电曲线示意图。
图9是本发明实施例提供的Al掺杂制备LiCoO2的XRD表征示意图。
图10是本发明实施例提供的Al掺杂制备LiCoO2的SEM表征示意图。
图11是本发明实施例提供的Al掺杂制备LiCoO2的结构表征的首次充放电曲线示意图。
具体实施方式
为了使本发明的目的、技术方案及优点更加清楚明白,以下结合实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。
下面结合附图对本发明的应用原理作详细的描述。
如图1所示,本发明实施例提供的合成锂离子电池正极材料的制备方法包括以下步骤:
S101:按LiAl0.01Co0.99O2中n(Li):n(Co):n(Al)=1:0.99:0.01称取一定质量的LiNO3、Co(NO3)2·6H2O和Al(NO3)3·9H2O,用玛瑙研钵充分碾磨,直至其结晶水完全析出;n为摩尔比。
S102:然后置于鼓风干燥箱中进行干燥。待水份蒸发后将物质取出,再次碾磨,放入管式电阻炉中,在温度300℃下预烧4h,800℃下烧结10h。
下面结合实验对本发明的应用原理作进一步的描述。
1.实验部分
1.1材料与试剂
1.2仪器
1.3LiCoO2制备与LiCoO2掺杂制备
1.3.1LiCoO2制备
本次实验采用三种方法合成LiCoO2正极材料:(1)按LiCoO2中n(Li)/n(Co)=1称取一定质量的Co2O3和Li2CO3,用玛瑙研钵充分碾磨后置于管式电阻炉中,在温度300℃下预烧4h,800℃下烧结10h。(2)按LiCoO2中n(Li)/n(Co)=1称取一定质量的Co3O4和Li2CO3,用玛瑙研钵充分碾磨后将材料分放入管式电阻炉中进行烧结,在温度300℃下预烧4h,800℃下烧结10h。(3)按LiCoO2中n(Li)/n(Co)=1称取一定质量的Co(NO3)2`6H2O和LiNO3,加入适量去离子水,用玛瑙研钵充分碾磨,直至其形成饱和溶液,然后置于管式电阻炉中,在温度300℃下预烧4h,800℃下烧结10h。
1.3.2LiCoO2掺Al制备
按LiAl0.01Co0.99O2中n(Li):n(Co):n(Al)=1:0.99:0.01称取一定质量的LiNO3、Co(NO3)2·6H2O和Al(NO3)3·9H2O,用玛瑙研钵充分碾磨,直至其结晶水完全析出,然后置于鼓风干燥箱中进行干燥。待水份蒸发后将物质取出,再次碾磨,放入管式电阻炉中,在温度300℃下预烧4h,800℃下烧结10h。图2为掺Al制备LiCoO2正极材料的流程图。
1.4电池组装
按质量比为1:1:8的材料、KSC导电剂、聚四氟乙烯(PTFE)乳液混合样品,其中加入少量酒精,混合调浆。将匀浆均匀的涂抹在2032型号扣式电池铝箔上,放在空气中干燥3分钟,在纽扣电池上滴加1-2滴酒精,将纽扣电池放到手动压力机上进行压片,压力控制在2MP附近。将压片后的电极片放入真空干燥中进行进一步干燥,干燥温度为120℃,时间12h。以纯金属锂片为负极,微孔聚乙烯为隔膜,以LiPF6-EC/DMC(1∶1,V/V)为电解液,然后在充满氩气,水和氧含量均小于1ppm的手套箱中装配成模拟电池。
1.5材料表征
1.5.1TG的测定
热分析测试常用的方法有热失重分析(TG)、差热分析(DTA)和示差扫描量热法(DSC)等。本实验采用TG-DTA对钴酸锂正极材料的合成过程进行分析,以确定钴酸锂正极材料的最适烧结方式和温度。本实验选用北京恒久科学仪器有限公司生产的微机差热天平(HCT/3)作为测量仪器进行测试,测试过程中采用动态升温的方法进行,测试条件:起始温度为25℃,终止温度为950℃,升温速率为10℃/min,静态空气气氛。
1.5.2X射线衍射测试(XRD)
X-射线粉末晶体衍射(XRD)是材料研究中最常用的结构表征工具。本次实验采用XRD分析测试仪(PANalytical)来完成样品物相组成和结构的定性鉴定和样品物相组成的定量分析。
1.5.3扫描电镜测试(SEM)
采用扫描电子显微镜测试样品的表面微观形貌,分析样品的形貌与电化学性能、样品的烧结温度与样品晶体形貌之间的关系。
1.6电化学性能测试
组装电池的电化学性能采用BTS充放电测试仪(深圳市新威尔电子有限公司)进行测试,通过将模拟电池接到BTS充放电测试仪上,观测所测材料的充放电比容量和充放电循环性能。测试操作如下:在不同的倍率下调节充放电电流,电压范围3-4.3V。
2.结果与讨论
2.1Co2O3和Li2CO3制备LiCoO2
2.1.1Co2O3和Li2CO3合成LiCoO2的温度范围
Co2O3和Li2CO3按照n(Co)/n(Li)=1称取,碾磨后进行热失重测试,反应过程如下:3Co2O3+3Li2CO3=6LiCoO2+3CO2
测量所得的热失重曲线如图3所示。可以观察到整个过程可以分为两个阶段,第一个阶段发生在350-550℃,Co2O3的存在催化Li2CO3的融化和分解,LiCoO2的合成也在此阶段大致完成。第二阶段发生在900℃以后,原因是高温促使了LiCoO2的分解,并且高温也可能促使LiCoO2晶体结构发生了变化。TG测量的是一个微小的量,受外界影响较大,周围的环境、温度、湿度等都有可能影响到TG图的测量,所以在测试时要合理控制外界环境。
2.1.2Co2O3和Li2CO3合成LiCoO2的晶体结构
图4为Co2O3和Li2CO3合成LiCoO2的XRD图,由图可得:该谱图与LiCoO2的标准X射线谱图对比,不存在明显的杂质峰,说明得到的LiCoO2比较纯净。I003和I104的衍射峰强度大,半峰宽值很小,说明该方法合成的LiCoO2有明显的层状结构,且I003/I104比值较大,说明的LiCoO2层状结构较为完好。
图5为Co2O3和Li2CO3合成LiCoO2的SEM图,可以看出:LiCoO2的颗粒表明清晰光洁,无凝结现象。颗粒结晶均匀,直径小于1um,且颗粒有往一个方向生长的趋势,有明显的棒状结构出现。
2.1.3Co2O3和Li2CO3合成LiCoO2的首次充放电曲线
对由Co2O3和Li2CO3合成的LiCoO2进行了电化学性能,图6为测得LiCoO2的首次充放电曲线图:发现这样获得的LiCoO2表现出平稳的充放电平台,充放电过程中电压变化不大,充放电比容量都较高,首次充电比容量达到120mAh/g,首次放电比容量达到105mAh/g。充放电效率为87.5%。
2.1.4Co2O3和Li2CO3合成LiCoO2的充放电循环曲线
对高温固相法合成的LiCoO2进行了充放电循环测试,选择第一组循环进行分析,如图7所示:从图中可以看出LiCoO2的充放电效率几乎一致,比容量没有出现衰竭现象。材料的首次充放电效率较低,只有87.5%,从第二个循环开始,充放电效率有所提高,都保持在98%附近,且充放电比容量都保持在115mAh/g。可以发现第二次和第五次充放电效率几乎已经达到了100%,表明Co2O3和Li2CO3在800℃合成LiCoO2表现出良好电化学性能。
2.1.5Co2O3和Li2CO3合成LiCoO2不同倍率下充放电曲线
图8为Co2O3和Li2CO3合成LiCoO2不同倍率下充放电曲线,发现0.1C倍率下,LiCoO2的充电比容量为120mAh/g,放电比容量为103mAh/g,充放电效率为85.8%。0.2C倍率下,LiCoO2的充电比容量为98mAh/g,放电比容量为100mAh/g,充放电效率为98%。发现0.1C倍率下的充放电容量要大于0.2C倍率下的充放电容量,但充放电效率不及0.2C倍率高。根据图8还可以发现在电流发生改变时,电压的范围没有发生太大的波动。
2.2Al掺杂制备LiCoO2正极材料
2.2.1Al掺杂制备LiCoO2的结构表征
图9为Al掺杂制备LiCoO2的XRD谱图,由该谱图可得:该谱图中没有明显杂质峰的存在,说明Al已经很好地融入到LiCoO2的结构中;各个衍射峰的强度大,半峰的宽值较小说明合成的LiAl0.01Co0.99O2的结晶性好。I003和I104的峰强度值都较大,表示了LiCoO2的结构和结构的基本单位良好,I003/I104峰强度比值大,表示该的层状结构合成完美。双重峰(006,102)和(018,110)劈裂良好,说明铝和钴已经有序地分布到了LiCoO2的层状结构中。I006/I003的比值较大(>0.037),说明相对于Co3O4和Li2CO3合成LiCoO2,该方法合成钴酸锂正极材料循环使用寿命提高更多。
采用SEM扫描电镜对由LiNO3、Co(NO3)2和Al(NO3)3制备得到的LiCoO2进行电镜测试,得到如下结果:发现以LiNO3、Co(NO3)2和Al(NO3)3原材料,在800℃下烧结得到的LiCoO2有良好的晶体结构,颗粒的大小分布均匀,直径平均为1um,出现了轻微的团聚想象。根据图10,也可以发现这样得到的LiCoO2已经表现出明显的层状结构。
2.2.2Al掺杂制备LiCoO2的首次充放电曲线
图11为Al掺杂制备LiCoO2的充放电循环曲线,发现这样得到的LiCoO2有平稳的充放电平台,充放电过程中电压波动的幅度较小,首次充放电效率达到100%,比容量在充放电2.7—4.3V范围内可以达到205mAh/g。
以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!