香豆素苷类化合物及其制备方法和应用与流程
本发明属于医药及保健食品领域,具体涉及一种香豆素苷类化合物及其制备方法和应用。
背景技术:
糖尿病是一类因糖脂代谢障碍引起的慢性病,主要由先天的基因和后天的不良生活习惯所引起,分为一型糖尿病、二型糖尿病、妊娠糖尿病等,其中二型糖尿病占绝大多数,约占90-95%。目前我国的糖尿病患者超过1亿,而糖尿病前期患者数量超过1.5亿,形势十分严峻。糖尿病的危害主要是其所引起的各种并发症,如血管病变、神经病变、肾脏病变等。因糖尿病引起的心脑血管并发症是第一并发症,甚至可以说糖尿病就是心脑血管疾病,因为糖尿病患者常伴有高血脂症,易促进动脉粥样硬化的发生;糖尿病患者的持续和反复高血糖,使脂肪更容易进入血管壁;糖尿病患者体内血液易呈高凝状态而形成血栓,使微血管闭塞,组织缺氧;二型糖尿病伴有高胰岛素血症,增强了动脉内膜细胞的溶脂作用,而加速动脉硬化过程,这些因素都促使心脑血管并发症的发生。流行病学调查表明,糖尿病患者约75%死于冠心病,约13%死于脑血管疾病,约占全球死亡原因的5%,如不加以控制,10年后的死亡率将翻倍。
尽管现有多种类别的抗糖尿病药物,但一方面这些药物都有不同程度的副作用。另一方面,更重要的是这些药物均会随着用药时间的延长而出现继发性失效,无论是单一疗法还是联合治疗,都没能取得令人满意的结果,我国有三分之二以上二型糖尿病患者的长期血糖控制不达标。因此,仍然需要不断地寻找高效低毒的抗糖尿病药物。
兴安独活(Heracleum dissectum)属菊科多年生草本,是东北鄂伦春族药食两用的野生植物,其鄂语名称为坎库拉,春夏季节其幼嫩的茎叶被当地人用作美味的蔬菜食用,其根作为传统的鄂族药材用于祛风除湿、止痛止泻等。另外,在早期的游牧时代,鄂伦春族人也将坎库拉作为青储饲料喂饲马匹和牛羊,以度过漫长寒冷的冬季。因此,鄂伦春族人将坎库拉视为上天赐予的珍宝。但到目前为止对其化学成分的研究极少,也无药理活性研究报道。
技术实现要素:
本发明的目的在于克服现有技术中存在的问题,提供一种香豆素苷类化合物及其制备方法和应用,该方法简单易行,制备的香豆素苷类化合物抗糖尿病活性高,从而可在糖尿病治疗中进行应用。
为了达到上述目的,本发明采用如下技术方案:
本发明香豆素苷类化合物分子式为C26H34O15。
进一步地,本发明香豆素苷类化合物结构式为:
本发明制备方法:包括以下步骤:
1)取兴安独活的干燥根进行回流提取若干次,将提取液减压浓缩,得到总浸膏或浓缩液;
2)将总浸膏混悬于水中,得到浸膏液,浸膏液或浓缩液经乙酸乙酯萃取若干次后分离出有机层,剩余水层通过正丁醇萃取若干次后合并萃取液,减压除去正丁醇得到正丁醇萃取层;
3)将正丁醇萃取层上样于硅胶柱,以氯仿-甲醇系统作为洗脱液,按体积比(100:0)~(0:100)进行梯度洗脱,对流出液进行检测,将洗脱液体积比为7:1的流份合并,除去溶剂,得到第一次过柱部分;
4)将第一次过柱部分上样于反相硅胶层析柱,以甲醇-水系统作为洗脱液,按体积比(0:100)~(100:0)进行梯度洗脱,对流出液进行检测,将洗脱液体积比为40:70的流份合并,除去溶剂,得到第二次过柱部分;
5)将第二次过柱部分上样于高效液相色谱分离柱,用流动相进行等度洗脱,得到香豆素苷类化合物。
进一步地,步骤1)的回流提取中采用甲醇、水或体积分数10~95%的乙醇作为提取剂,兴安独活的干燥根与提取剂的质量体积比为1kg:(1~8)L;当提取剂为甲醇或体积分数10~95%的乙醇时,将得到的提取液中溶剂回收得到总浸膏;当提取剂为水时,将提取液的体积浓缩至六分之一到十分之一,得到浓缩液。
进一步地,步骤1)中提取次数为1~6次,每次1~4小时。
进一步地,步骤2)中总浸膏和水的体积比为1:1~1:5。
进一步地,步骤2)中浸膏液或浓缩液直接经过乙酸乙酯萃取;或者先依次经石油醚和氯仿萃取后,再经过乙酸乙酯萃取;每次萃取均是等体积萃取;每种溶剂分别萃取1~6次。
进一步地,步骤3)中梯度洗脱后每300~800mL收集一个流份;步骤4)中梯度洗脱后每200~500mL收集一个流份;步骤3)和步骤4)中对流出液均是进行TLC检测;步骤5)中等度洗脱的流速为3~6mL/min。
进一步地,步骤5)中流动相是甲醇-0.5%醋酸水系统或乙腈-0.5%醋酸水系统,甲醇-0.5%醋酸水系统中甲醇、水和醋酸的体积比为25:75:0.5;乙腈-0.5%醋酸水系统中乙腈、水和醋酸的体积比为32:68:0.5。
如上所述的香豆素苷类化合物在制备抗糖尿病药物和/或保健品中的应用。
与现有技术相比,本发明的有益效果是:
本发明公开的一种香豆素苷类化合物具有较好的抑制餐后高血糖的作用。餐后高血糖是糖尿病的一个典型特征,且危害十分严重。经小鼠口服糖耐量实验证明,本发明中的香豆素苷类化合物在给糖后0.5小时和1小时后能有效降低小鼠的血糖值,在0.5小时其20mg/kg的剂量所产生的降糖作用与阳性对照药格列齐特100mg/kg的所产生的降糖作用相当。因此,本发明中的香豆素苷类化合物具有良好的抗糖尿病作用,该化合物具有高效、低毒的特点,有望开发成新的抗糖尿病药物,或者用于制备具有预防和治疗糖尿病作用的保健食品。同时,本发明对充分开发利用兴安独活提供一定的科学依据。
本发明中香豆素苷类化合物的制备方法具有简单易行,环境友好,纯度高等特点,通过几个简单的步骤就能制备出纯度较高(纯度>98%)的目标化合物,具有通用的可行性。
【附图说明】
图1为本发明化合物1的1H-NMR图谱;
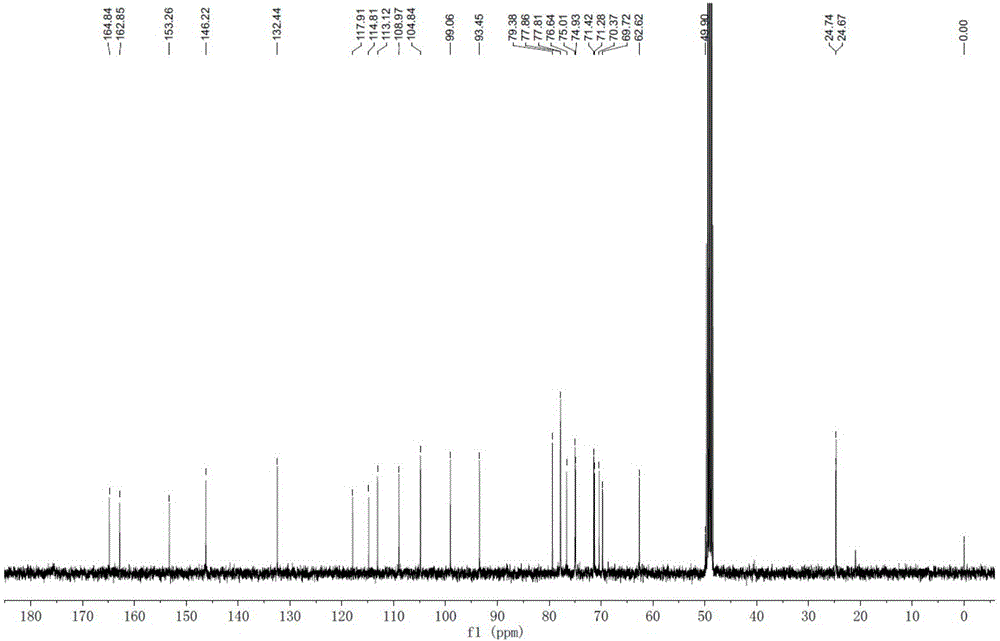
图2为本发明化合物1的13C-NMR图谱;
图3为本发明化合物1的DEPT图谱;
图4为本发明化合物1的1H-1H COSY图谱;
图5为本发明化合物1的HMQC图谱;
图6为本发明化合物1的HMBC图谱;
图7为本发明化合物1的ROESY图谱;
图8为本发明化合物1的HR-ESIMS图谱;
图9为本发明化合物1的小鼠糖耐量实验结果。
【具体实施方式】
下面结合具体实施例及附图对本发明做进一步的详细说明,所述是对本发明的解释而不是限定。
本发明香豆素苷类化合物的化学结构如下:
本发明制备方法,包括以下步骤:
1)取一定质量(kg)的兴安独活干燥根,用体积为兴安独活干燥根质量1~8倍量的甲醇、体积分数为10~95%的乙醇或水(L)在各自沸点附近加热回流提取1~6次,每次1~4小时,当提取剂为甲醇或体积分数10~95%的乙醇时,合并提取液减压回收除去溶剂,得到总浸膏,当提取剂为水时,合并提取液并将其体积浓缩至六分之一到十分之一,得到浓缩液;
2)将总浸膏混悬于水中,总浸膏和水的体积比为1:1~1:5,得到浸膏液,浸膏液或浓缩液分别依次用等体积的有机溶剂萃取,其中,第一次萃取时用石油醚对浸膏液或浓缩液进行等体积萃取,之后每次萃取均是分离出上一次萃取后的有机层,将剩余的水层用有机溶剂等体积进行下一次萃取;每种溶剂各萃取1~6次,合并萃取液,常压或减压蒸馏除去有机溶剂,分别得到各萃取层和水层。有机溶剂包括石油醚、氯仿、乙酸乙酯和正丁醇等,且萃取次序为先用极性小的溶剂,再用极性大的有机溶剂,石油醚和氯仿可以省去。
3)取正丁醇萃取层,通过采用柱层析纯化等分离方法,得到本发明的香豆素苷类化合物。
柱层析包括以下三个阶段:
第一阶段:将正丁醇萃取层上样于硅胶柱,以氯仿-甲醇系统作为洗脱液,按体积比(100:0)~(0:100)进行梯度洗脱,每300~800mL收集一个流份,对流出液进行TLC检测,合并相同流份,共得到30个流份,分别命名为FrB1-FrB30,常压或减压蒸干溶剂,取其中的FrB25流份,即洗脱液体积比为7:1的流份,作为第一次过柱部分;
第二阶段:将第一次过柱部分,上样于反相硅胶层析柱,以甲醇-水系统作为洗脱液,按体积比(0:100)~(100:0)进行梯度洗脱,每200~500mL收集一个流份,对流出液进行TLC检测,合并相同流份,减压除去溶剂,得到3个亚流份,分别命名为FrB25.1-FrB25.3,将FrB25.1流份,即洗脱液体积比为40:70的流份,作为第二次过柱部分;
第三阶段:将第二次过柱部分,上样于高效液相色谱分离柱,分离得到香豆素苷类化合物。其中,高效液相色谱分离柱为江苏汉邦的Megres C18柱,高效液相色谱分离是用示差折光检测器,以甲醇-0.5%醋酸水系统或乙腈-0.5%醋酸水系统作为流动相,按3~6mL/min进行等度洗脱,甲醇-0.5%醋酸水系统中甲醇、水和醋酸的体积比为25:75:0.5;乙腈-0.5%醋酸水系统中乙腈、水和醋酸的体积比为32:68:0.5。
本发明得到的香豆素苷类化合物,其结构式为:
本发明的香豆素苷类化合物能够在糖尿病治疗中进行应用,具体是在制备抗糖尿病类药物中的应用和/或在制备抗糖尿病类保健品中的应用,其中抗糖尿病药物和/或保健品为能够抑制餐后血糖升高的药物和/或保健品。
下面通过具体的实施例对本发明做进一步详细说明。
实施例1
1.香豆素苷类化合物的提取分离和纯化
1)取兴安独活干燥根6kg,用30L的甲醇加热回流提取3次,每次2小时,此时,和甲醇的体积是兴安独活干燥根的质量的5倍,合并甲醇提取液减压回收溶剂,得总浸膏;
2)将总浸膏混悬于3倍体积量水中,用石油醚等体积萃取4次,然后依次经氯仿,乙酸乙酯和正丁醇等体积萃取,每种有机溶剂萃取4次,将有机层常压或减压蒸馏除去溶剂后分别得到石油醚层、氯仿层、乙酸乙酯层、正丁醇层和余下的水层。
3)取正丁醇萃取层100g,上样于硅胶柱色谱,以氯仿-甲醇系统作为洗脱液,按体积比(v/v)为100:0~0:100进行梯度洗脱,每500mL收集一次,常压蒸馏回收溶剂,TLC检识合并相同流份,共得到30个流份,分别命名为FrB1-FrB30,取其中的FrB25流份,即洗脱液体积比为7:1的流份,作为第一次过柱部分。
4)FrB25流份经反相硅胶柱色谱,用甲醇-水系统作为洗脱液,按体积比(v/v)为100:0~0:100进行梯度洗脱,每200mL收集一次,减压除去溶剂,TLC检识合并相同流份,得到3个亚流份,分别命名为FrB25.1-FrB25.3,将FrB25.1流份,即洗脱液体积比为40:70的流份,作为第二次过柱部分。
5)然后FrB25.1流份用半制备高效液相色谱仪,使用Megres C18色谱柱(250×10mm,5μm),以甲醇-0.5%醋酸水系统(25:75)作为流动相等度洗脱,流速为3mL/min,得到香豆素苷类化合物1,保留时间为22min。
本发明通过理化常数和现代波谱学技术手段(HR-ESI-MS,1D-NMR,2D-NMR)鉴定化合物的结构,化合物1为6″-glucopyranosyl-apterin。化合物1的结构鉴定过程如下所述。
2.香豆素苷类化合物的结构鉴定
在图1的1H-NMR中,化学位移δH 6.24(1H,d,J=9.5Hz),7.90(1H,d,J=9.5Hz),7.55(1H,d,J=8.4Hz),6.90(1H,d,J=8.4Hz)是角型香豆素的特征峰信号。
在1H and 13C NMR谱中,如图1和图2所示,特别是结合DEPT谱和HMQC谱,如图3和图5所示,观察到有2个甲基,2个连氧亚甲基,12个连氧次甲基,4个SP2杂化次甲基和6个季碳,2个端基质子δH 4.78(1H,d,J=7.8Hz)and 4.15(1H,d,J=7.8Hz)和他们相应的碳信号δC99.1and 104.9表明分子中有两个糖单位。酸水解后用气相色谱分析为葡萄糖,构型为β构型,因为两个糖的端基质子的偶合常数为7.8Hz。结构中其它位置的氢通过1H-1H COSY谱得到连接,如图4所示。
碳谱数据与Apterin的碳谱数据十分相似,区别在于多了一个葡萄糖单位,在图6的HMBC谱中糖端基质子δH 4.15(1H,d,J=7.8Hz,H-1″′)和另一分子的葡萄糖的6位碳δC69.8(C-6″)相关。同时,内侧葡萄糖6位质子δH 3.61(2H,m,H-6″)和外侧葡萄糖的端基碳δC104.9(C-1″′)相关,因此该化合物鉴定为6″-β-D-glucopyranosyl-apterin,即8-O-β-D-吡喃葡萄糖基(1→6)-β-D-吡喃葡萄糖基-9-羟基-2H呋喃并[2,3h]-1-苯并吡喃-2-酮,是一个未见文献报道的新化合物。另外,在ROESY谱中,如图7,2′和3′位置的氢有相关,说明这两个氢是顺式,与Apterin的立体构型一致。
化合物1为淡黄色无定形粉末,纯度>98%;如图8所示,其HR-ESI-MS中m/z 609.1807[M+Na]+(calcd 609.1790),确定分子式为C26H34O15。其结构如下式,
本发明中化合物1的核磁数据见表1。
表1本发明中化合物1的1H NMR和13C NMR数据
下面对本发明中所分离鉴定的化合物1进一步做药理活性检测。
3.小鼠糖耐量实验
实验方法:
6周龄雄性昆明鼠,禁食过夜,乙醚麻醉下眼眶取血,离心取血清,测定血清中葡萄糖浓度。根据基础血糖值将小鼠分为5组,每组8只,分别为正常组(蒸馏水),对照组(vehicle),阳性对照组(格列齐特100mg/kg),以及两个样品组(化合物1各10mg/kg和20mg/kg),30分钟后除正常组外,其余各组小鼠分别灌胃给予葡萄糖溶液(1.5g/kg),之后在0.5小时、1小时和2小时于乙醚麻醉状态下眼眶取血,离心后测定血糖浓度。血糖值表示为MEAN±SEM(n=8).*p<0.05,**p<0.01(与对照组相比)。
实验结果:见附图9。
结果分析:附图9中的数据表明,本发明中的化合物1具有很好的抗糖尿病作用,在给糖后0.5小时和1小时后能有效降低口服糖耐量小鼠的血糖值,尤其在0.5小时其20mg/kg的剂量所产生的降糖作用与阳性对照药格列齐特100mg/kg的所产生的降糖作用相当。
结合以上实验及其实验结果,表明本发明中的香豆素苷类化合物1具有极强的降低餐后血糖的作用,有望开发为新的抗糖尿病药物;或者用于制备预防和治疗糖尿病的保健食品。
实施例2
1)取兴安独活干燥根6kg,用4倍量的95%乙醇(24L)加热回流提取2次,每次4小时,将提取液减压回收溶剂,得总浸膏;
2)将总浸膏混悬于2倍体积量水中,用乙酸乙酯等体积萃取4次,然后经正丁醇等体积萃取4次,将正丁醇萃取的有机层减压蒸馏除去溶剂后得到正丁醇萃取层。
3)取正丁醇萃取层100g,上样于硅胶柱色谱,以氯仿-甲醇系统作为洗脱液,按体积比(v/v)为100:0~0:100进行梯度洗脱,每600mL收集一次,常压蒸馏回收溶剂,TLC检识合并相同流份,取其中洗脱液体积比为7:1的流份,作为第一次过柱部分。
4)第一次过柱部分经反相硅胶柱色谱,用甲醇-水系统作为洗脱液,按体积比为100:0~0:100进行梯度洗脱,每300mL收集一次,减压除去溶剂,TLC检识合并相同流份,得到3个亚流份,取其中洗脱液体积比为40:70的流份,作为第二次过柱部分。
5)第二次过柱部分用半制备高效液相色谱仪,使用Megres C18色谱柱(250×10mm,5μm),以甲醇-0.5%醋酸水系统(25:75)作为流动相等度洗脱,流速为3mL/min,得到香豆素苷类化合物1,保留时间为22min。
实施例3
1)取兴安独活干燥根20kg,用50L的水煎煮提取3次,每次2小时,得到40L的提取液,将提取液减压浓缩至5L,得水提取物的浓缩液;
2)将水提取物的浓缩液用乙酸乙酯等体积萃取3次,然后经正丁醇等体积萃取3次,将正丁醇萃取液减压除去溶剂后得到正丁醇萃取层。
3)取正丁醇萃取层500g,上样于硅胶柱色谱,以氯仿-甲醇系统作为洗脱液,按体积比(v/v)为100:0~0:100进行梯度洗脱,每800mL收集一次,常压蒸馏回收溶剂,TLC检识合并相同流份,取其中洗脱液体积比为7:1的流份,作为第一次过柱部分。
4)第一次过柱部分经反相硅胶柱色谱,用甲醇-水系统作为洗脱液,按体积比(v/v)为100:0~0:100进行梯度洗脱,每500mL收集一次,减压除去溶剂,TLC检识合并相同流份,得到3个亚流份,取其中洗脱液体积比为40:70的流份,作为第二次过柱部分。
5)第二次过柱部分用半制备高效液相色谱仪,使用制备型Megres C18色谱柱(250×20mm,5μm),以甲醇-0.5%醋酸水系统(25:75)作为流动相等度洗脱,流速为6mL/min,得到香豆素苷类化合物1,保留时间为23min。
实施例4
1)取兴安独活干燥根6kg,用8倍量的10%乙醇(48L)加热回流提取6次,每次1小时,将提取液减压回收溶剂,得总浸膏;
2)将总浸膏混悬于5倍体积量水中,用石油醚等体积萃取4次,然后依次经氯仿,乙酸乙酯和正丁醇各等体积萃取6次,将正丁醇萃取的有机层减压蒸馏除去溶剂后得到正丁醇萃取层。
3)取正丁醇萃取层100g,上样于硅胶柱色谱,以氯仿-甲醇系统作为洗脱液,按体积比(v/v)为100:0~0:100进行梯度洗脱,每300mL收集一次,常压蒸馏回收溶剂,TLC检识合并相同流份,取其中洗脱液体积比为7:1的流份,作为第一次过柱部分。
4)第一次过柱部分经反相硅胶柱色谱,用甲醇-水系统作为洗脱液,按体积比为100:0~0:100进行梯度洗脱,每400mL收集一次,减压除去溶剂,TLC检识合并相同流份,得到3个亚流份,取其中洗脱液体积比为40:70的流份,作为第二次过柱部分。
5)第二次过柱部分用半制备高效液相色谱仪,使用Megres C18色谱柱(250×10mm,5μm),以乙腈-0.5%醋酸水系统(32:68)作为流动相等度洗脱,流速为3mL/min,得到香豆素苷类化合物1,保留时间为19min。
实施例5
1)取兴安独活干燥根6kg,用5倍量的35%乙醇(30L)加热回流提取4次,每次3小时,将提取液减压回收溶剂,得总浸膏;
2)将总浸膏混悬于1倍体积量水中,用石油醚等体积萃取4次,然后依次经氯仿,乙酸乙酯和正丁醇各等体积萃取1次,将正丁醇萃取的有机层减压蒸馏除去溶剂后得到正丁醇萃取层。
3)取正丁醇萃取层100g,上样于硅胶柱色谱,以氯仿-甲醇系统作为洗脱液,按体积比(v/v)为100:0~0:100进行梯度洗脱,每600mL收集一次,常压蒸馏回收溶剂,TLC检识合并相同流份,取其中洗脱液体积比为7:1的流份,作为第一次过柱部分。
4)第一次过柱部分经反相硅胶柱色谱,用甲醇-水系统作为洗脱液,按体积比为100:0~0:100进行梯度洗脱,每300mL收集一次,减压除去溶剂,TLC检识合并相同流份,得到3个亚流份,取其中洗脱液体积比为40:70的流份,作为第二次过柱部分。
5)第二次过柱部分用半制备高效液相色谱仪,使用Megres C18色谱柱(250×20mm,5μm),以乙腈-0.5%醋酸水系统(32:68)作为流动相等度洗脱,流速为6mL/min,得到香豆素苷类化合物1,保留时间为18.5min。
对比例1
将步骤5)中的流动相换成其它流动相(或者色谱柱替换成普通反相硅胶色谱柱),其它步骤和条件与实施例1相同。发现无法分离出香豆素苷类化合物1。
上述实施例为本发明较佳的实施方式,但本发明的实施方式并不受上述实施例的限制,其他的任何未背离本发明的精神实质与原理下所作的改变、修饰、替代、组合、简化,均应为等效的置换方式,都包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!