乙烯酮类化合物及其制备方法和应用与流程
本发明涉及乙烯酮类化合物及其制备方法和应用,尤其涉及乙烯酮类化合物在检测平行结构g-四链体中的应用。
背景技术:
g-四链体是一种富含串联重复鸟嘌呤的dna或rna折叠形成的二级核酸结构。该结构被认为与许多生物学过程相关,例如与调节端粒的稳定性,以及参与rna转录、翻译和运输等相关。某些g-四链体结构还被发现过度表达于某些基因的启动子,以及被视为治疗某些癌症药物的潜在靶点。因此,在体外和体内准确地检测以及追踪g-四链体具有重要的研究意义。
目前,已有的检测g-四链体的方法包括免疫荧光标记法,以及同位素标记法。免疫荧光标记法操作程序复杂,而同位素标记法涉及使用放射性同位素,操作条件更为严苛。而近来,小分子荧光探针因为其操作和使用简便,其发展和应用越来越成为受到重视。发展可以特异性检测某一类g-四链体的小分子荧光探针依然是研究热点。
技术实现要素:
本发明的目的在于提供一类乙烯酮类化合物。
本发明的另一目的在于提供上述乙烯酮类化合物的制备方法。
本发明的又一目的在于提供上述乙烯酮类化合物在检测平行结构g-四链体中的应用。
本发明通过如下技术方案实现:
下式(i)所示的乙烯酮类化合物:
其中,r1、r2、r3、r4相同或不同,彼此独立地选自为h、-f、-cl、-br、-i、-oh、-nh2、=o、c1-6烷基、c1-6烷氧基、-co-c1-6烷基、-co-nh-c1-6烷基、-cooc1-6烷基、芳基、芳氧基、杂芳基、杂芳基氧基、杂环基、杂环氧基。
根据本发明的实施方案,所述r1、r2、r3、r4相同或不同,彼此独立地选自为h、-f、-cl、-br、-i、-oh、-nh2、c1-3烷基或c1-3烷氧基;
优选地,r1、r2、r3、r4相同或不同,彼此独立地选自h,-ch3或-och3。
作为实例,所述式(i)化合物选自包括但不限于如下化合物:
本发明还提供上述式(i)化合物的制备方法,包括如下步骤:
其中,r1、r2、r3、r4如上面所定义;
(a)将化合物(iii)与丙酮反应,得到化合物(ii);
(b)将步骤(a)中得到的化合物(ii)在酸性条件下进行反应,得到式(i)化合物。
根据本发明,步骤(a)中,
所述反应在溶剂环境下进行,所述溶剂优选为乙醇和氢氧化钠水溶液构成的混合溶剂。
化合物(iii)与丙酮的摩尔比为1:(0.3-0.7),优选为1:0.5。
根据本发明,步骤(b)中,
所述反应在溶剂环境下进行,所述溶剂优选为醚类溶剂,如四氢呋喃。
所述酸性条件使用无机酸溶液或有机酸来调节,例如使稀盐酸来调节。
任选地,所述制备方法还包括使用萃取方法对得到的式(i)化合物进行分离提纯。
根据本发明,所述制备方法还包括式(iii)化合物的制备,包括如下步骤:
(c)将化合物(iv)和二苯甲酮亚胺进行反应,得到化合物(iii);
其中,r1、r2、r3、r4如上面所定义;x选自离去基团,例如ots、i、br或cl。
根据本发明,步骤(c)中,
所述反应优选在溶剂中进行,所述溶剂例如为甲苯。
反应温度优选为80-120℃。
所述反应优选在催化剂下进行,所述催化剂选自醋酸钯,联萘二苯磷和碳酸铯的组合物。
化合物(iv),二苯甲酮亚胺,醋酸钯,联萘二苯磷和碳酸铯的摩尔比为1:(1.5-2.5):(0.01-0.03):(0.01-0.05):(2.2-2.6),优选为1:2:0.02:0.03:2.4。
本发明还提供式(i)化合物用于检测平行结构g-四链体的用途。
根据本发明,所述检测在缓冲溶液中进行,例如在tris-hcl(三(羟甲基)氨基甲烷)缓冲溶液中进行。
有益效果
1)本发明所述式(i)化合物可在缓冲溶液中检测平行结构g-四链体。其荧光强度随着平行结构g-四链体的浓度的增加而增强,检测的灵敏度较高。且式(i)化合物对检测平行结构g-四链体有选择性,对反平行g-四链体,混合型g-四链体,以及其他类型dna均无响应性,表现较高的专一性。
2)本发明所述式(i)化合物合成步骤简单,反应时间短,提纯方便,工艺简单。
术语定义和说明:
除非另有定义,否则本文所有科技术语具有的涵义与权利要求主题所属领域技术人员通常理解的涵义相同。应理解,上述简述和下文的详述为示例性且仅用于解释,而不对本申请主题作任何限制。在本申请中,除非另有说明,所用术语“包括”以及其它形式,例如“包含”、“含”和“含有”并非限制性。
术语“烷基”指具有1-6个,优选1-3个碳原子的直链或支链烷基,所述烷基例如为甲基、乙基、丙基、异丙基、丁基、异丁基、叔丁基、仲丁基、戊基、新戊基。
术语“芳基”应理解为优选表示具有6~20个碳原子的一价芳香性或部分芳香性的单环、双环或三环烃环,优选“c6-14芳基”。术语“c6-14芳基”应理解为优选表示具有6、7、8、9、10、11、12、13或14个碳原子的一价芳香性或部分芳香性的单环、双环或三环烃环(“c6-14芳基”),特别是具有6个碳原子的环(“c6芳基”),例如苯基;或联苯基,或者是具有9个碳原子的环(“c9芳基”),例如茚满基或茚基,或者是具有10个碳原子的环(“c10芳基”),例如四氢化萘基、二氢萘基或萘基,或者是具有13个碳原子的环(“c13芳基”),例如芴基,或者是具有14个碳原子的环(“c14芳基”),例如蒽基。
术语“杂芳基”应理解为含有5-20个环原子、5-14个环原子,或5-12个环原子,或5-10个环原子,或5-6个环原子的单环、双环和三环体系,其中至少一个环体系是芳香族的,且至少一个环体系包含一个或多个杂原子(例如n、o、s、se等),其中每一个环体系包含5-7个原子组成的环,且有一个或多个连接点与分子其余部分相连。所述杂芳基基团任选地被一个或多个本发明所描述的取代基所取代。在一些实施方案中,5-10个原子组成的杂芳基包含1,2,3或4个独立选自o、s、se和n的杂原子。在另一些实施方案中,5-6个原子组成的杂芳基包含1,2,3或4个独立选自o、s、se和n的杂原子。
杂芳基基团的单环实例包括,但并不限于,噻吩基、呋喃基、吡咯基、噁唑基、噻唑基、咪唑基、吡唑基、异噁唑基、异噻唑基、噁二唑基、三唑基、噻二唑基、噻-4h-吡唑基等以及它们的苯并衍生物,例如苯并呋喃基、苯并噻吩基、苯并噁唑基、苯并异噁唑基、苯并咪唑基、苯并三唑基、吲唑基、吲哚基、异吲哚基等;或吡啶基、哒嗪基、嘧啶基、吡嗪基、三嗪基等,以及它们的苯并衍生物,例如喹啉基、喹唑啉基、异喹啉基等;或吖辛因基、吲嗪基、嘌呤基等以及它们的苯并衍生物;或噌啉基、酞嗪基、喹唑啉基、喹喔啉基、萘啶基、蝶啶基、咔唑基、吖啶基、吩嗪基、吩噻嗪基、吩噁嗪基等。
术语“杂环基”意指单环,双环或三环体系,其中环上一个或多个原子独立任选地被杂原子所取代,环可以是完全饱和的或包含一个或多个不饱和度,但不是芳香族类,有一个或多个连接点连接到其他分子上去。一个或多个环上的氢原子可以独立地未被取代或被一个或多个本发明所描述的取代基所取代。其中一些实施例是,“杂环基”是3-7个原子组成的单环、或7-10个原子组成的的双环,其包含1-5个,优选1-3个选自n、o、s和se的杂原子。特别地,所述杂环基可以包括但不限于:4元环,如氮杂环丁烷基、氧杂环丁烷基;5元环,如四氢呋喃基、二氧杂环戊烯基、吡咯烷基、咪唑烷基、吡唑烷基、吡咯啉基;或6元环,如四氢吡喃基、哌啶基、吗啉基、二噻烷基、硫代吗啉基、哌嗪基或三噻烷基;或7元环,如二氮杂环庚烷基。任选地,所述杂环基可以是苯并稠合的。所述杂环基可以是双环的,例如但不限于5,5元环,如六氢环戊并[c]吡咯-2(1h)-基环,或者5,6元双环,如六氢吡咯并[1,2-a]吡嗪-2(1h)-基环。含氮原子的环可以是部分不饱和的,即它可以包含一个或多个双键,例如但不限于2,5-二氢-1h-吡咯基、4h-[1,3,4]噻二嗪基、4,5-二氢噁唑基或4h-[1,4]噻嗪基,或者,它可以是苯并稠合的,例如但不限于二氢异喹啉基、1,3-苯并噁唑基、1,3-苯并二氧杂环戊烯基。
除非另有说明,杂环基、杂芳基包括其所有可能的异构形式,例如其位置异构体。因此,对于一些说明性的非限制性实例,吡啶基或亚吡啶基包括吡啶-2-基、亚吡啶-2-基、吡啶-3-基、亚吡啶-3-基、吡啶-4-基和亚吡啶-4-基;噻吩基或亚噻吩基包括噻吩-2-基、亚噻吩-2-基、噻吩-3-基和亚噻吩-3-基。
附图说明
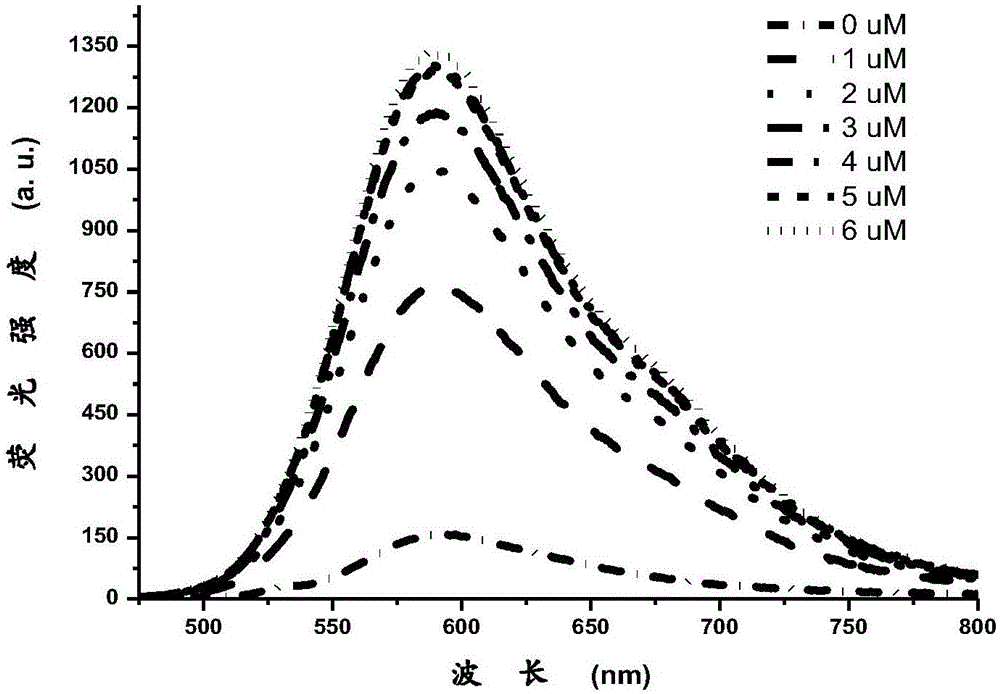
图1为实施例3中制备的化合物(3)对于序列名为vegf的平行结构g-四链体进行荧光滴定光谱图;
图2为实施例3中制备的化合物(3)对于不同平行g-四链体,非平行g-四链体以及其他dna的荧光滴定曲线;
图3为实施例3中制备的化合物(3)用于细胞内平行结构g-四链体的荧光成像。
具体实施方式
下文将结合具体实施例对本发明的技术方案做更进一步的详细说明。应当理解,下列实施例仅为示例性地说明和解释本发明,而不应被解释为对本发明保护范围的限制。凡基于本发明上述内容所实现的技术均涵盖在本发明旨在保护的范围内。
除非另有说明,以下实施例中使用的原料和试剂均为市售商品,或者可以通过已知方法制备。
实施例1
制备化合物(1)
在氩气保护下,在三口瓶中加入醋酸钯(0.2mmol),联萘二苯磷(0.3mmol),碳酸铯(24mmol)以及4-溴-2,6-二甲氧基苯甲醛(2.45g,10mmol)。再向反应体系加入甲苯和二苯甲酮亚胺(20ml),磁子搅拌下,在100℃下反应12小时。反应完成后,有机相旋干,粗产物用展开剂乙酸乙酯/石油醚过硅胶色谱柱,得到浅黄色固体(2.42g,70%)。
实施例2
制备化合物(2)
在圆底烧瓶内加入实施例1制备的化合物(1)(1g,3mmol),再加入乙醇(20ml),丙酮(100μl,1.5mmol)以及几滴氢氧化钠水溶液。反应在磁子搅拌下,在室温进行1小时。接着,加入水(100ml),再用二氯甲烷(50ml)萃取三次,收集有机相。有机相旋干,粗产物用展开剂乙酸乙酯/石油醚过硅胶色谱柱,得到黄色固体(2.42g,70%)。
实施例3
制备化合物(3)
在圆底烧瓶中,加入实施例2制备的化合物(2)(0.712g,1mmol),再加入10ml四氢呋喃和1ml2.0m稀盐酸。接着再转移至0.5m稀盐酸和乙酸乙酯的萃取体系萃取。收集水相,并滴加饱和碳酸氢钠溶液碱化。再加入50ml二氯甲烷萃取。收集有机相。旋干有机相,得到橙色固体(0.34g,90%)。
实施例4
将实施例3中得到的化合物(3)针对不同溶度的序列名为vegf的平行结构g-四链体进行荧光滴定检测:使用10mm的tris-hcl缓冲溶液(含有50mm氯化钾)配制500μl浓度分别为0μm,1μm,2μm,3μm,4μm,5μm,6μm的序列名为vegf的平行结构g-四链体溶液。然后分别加入1μl的1mm化合物(3)的溶液,使化合物(3)的最终浓度为2μm。使用荧光光谱仪测得其荧光光谱见附图1,图1中横坐标刻度为600nm的上方,从下到上依次为0μm,1μm,2μm,3μm,4μm,5μm,6μm的荧光检测结果,由图1可以看出,随着g-四链体的浓度增加,溶液的荧光逐渐增强。
实施例5
将实施例3中得到的化合物(3)针对不同平行结构g-四链体,非平行g-四链体以及其他dna的进行荧光滴定检测:使用10mm的tris-hcl缓冲溶液(含有50mm氯化钾)配制500μl浓度分别为0μm,1μm,2μm,3μm,4μm,5μm,6μm不同序列的平行结构g-四链体,非平行g-四链体以及其他dna(单链dna,双链dna和三链dna)溶液。然后分别加入1μl的1mm化合物(3)的溶液,使化合物(3)的最终浓度为2μm。使用荧光光谱仪测得其荧光光谱,并根据最大发光峰处的荧光强度与不同核苷酸浓度绘制荧光滴定曲线(见图2),从图2可以看出,只有平行结构的g-四链体可以让化合物(3)的荧光逐渐增强。显示出对平行结构g-四链体良好的选择性和响应性。
实施例6
将实施例3中得到的化合物(3)在细胞内检测平行结构g-四链体:首先将arpe-19细胞用甲醇固定,并用0.1%tritonx-100溶液破坏细胞膜,之后再将化合物(3)加入细胞培养基中,最终浓度为1μm。接着再用激光共聚焦显微镜进行荧光成像(见图3),由图3可以看出,平行结构g-四链体在细胞内的分布情况,即在细胞核与细胞质都有分布。
以上,对本发明的实施方式进行了说明。但是,本发明不限定于上述实施方式。凡在本发明的精神和原则之内,所做的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!