基于分析物催化聚合反应的Hg2+比色检测方法与流程
本发明属于纳米化学传感技术领域,具体涉及一种基于分析物催化聚合反应的hg2+比色检测方法。
背景技术:
汞离子(hg2+)是具有严重生理毒性的重金属离子之一。hg2+能够在动物和植物体内积累,并通过食物链逐步富集,其浓度可成千上万甚至百万倍地增加,最终威胁人类健康,例如可严重损害人体的神经、皮肤粘膜、泌尿及生殖等系统,甚至导致死亡。《中华人民共和国环境保护法》所制定的生活饮用水和农田灌溉水的水质标准中规定hg2+含量不得超过0.001mg/l。为保障食物、水和环境中的hg2+不影响人体健康和生命安全,对食物、水和环境中的痕量hg2+进行定量检测意义重大。现有的hg2+检测技术主要包括电感耦合等离子体质谱法、原子吸收光谱法、原子发射光谱法、原子荧光光谱法等。然而,这些方法普遍存在操作步骤繁琐费时、不能用于现场分析等问题。
技术实现要素:
本发明的目的是针对现有技术的不足,提供一种基于分析物催化聚合反应的简单高灵敏hg2+比色检测方法。
本发明的思路:低浓度邻苯二胺小分子可有效介导表面带负电荷的金纳米颗粒凝集导致反应溶液发生由红变蓝的颜色改变反应。而少量的hg2+即能高效、特异地催化氧化聚合邻苯二胺小分子为聚邻苯二胺(聚合物),从而抑制上述溶液变色反应。金纳米颗粒凝集导致反应溶液发生颜色改变的程度反比于样本中hg2+浓度。因此,通过肉眼观察反应溶液的颜色变化即可实现hg2+的简单高灵敏定性或半定量检测。若借助紫外可见分光光度计则可进一步实现目标金属离子分析物的准确定量检测。
具体步骤为:
步骤一,将hg2+样本溶液与邻苯二胺溶液混合,邻苯二胺小分子被hg2+催化氧化聚合化为聚邻苯二胺,制得反应溶液。
步骤二,向步骤一制得的反应溶液中加入表面呈负电荷性质的金纳米颗粒红色溶液,制得混合溶液,混合溶液中剩余的邻苯二胺小分子将介导表面呈负电荷性质的金纳米颗粒凝集,金纳米颗粒的凝集程度与样本溶液中hg2+的浓度呈反比,肉眼观测该混合溶液的颜色变化进行定性或半定量分析,或使用光度计进行定量分析,即实现hg2+比色检测。
所述表面呈负电荷性质的金纳米颗粒通过以下任意一种方式获得:金纳米颗粒在原位合成中表面吸附了还原剂的阴离子或者金纳米颗粒合成完成后被进一步修饰上可电离呈负电荷性质的分子。
所述光度计为台式光度计和便携式光度计中的一种。
与现有的hg2+检测方法相比,本发明的突出优点在于:
1)整个hg2+分析过程中的操作极为简单,未经专业技能培训的操作人员也能开展实验;2)通过协同邻苯二胺有效介导金纳米颗粒凝集反应和hg2+高效、特异催化氧化聚合邻苯二胺小分子为聚邻苯二胺,显著提高方法的检测灵敏度;3)仅需肉眼观测溶液颜色的改变,即可实现hg2+的高灵敏定性或半定量分析,或可通过借助便携式光度计进一步实现分析物的准确定量检测,在极大降低分析成本的同时还能用于hg2+样本的现场分析和即时检测;4)本发明可直接推广应用于医学诊断、环境监测、食品安全等诸多领域里各类型样本中hg2+分析物的简单、经济、快速、超灵敏、特异的定性与定量检测。
附图说明
图1为本发明实施例1和实施例2中基于分析物催化聚合反应的hg2+比色检测方法的原理示意图。
图中标记:1-1—无色超纯水;1-2—邻苯二胺;2—检测试管;3-1—超纯水;3-2—hg2+;4—聚邻苯二胺;5-1—红色溶液;5-2—金纳米颗粒;6—肉眼;7—便携式分光光度计。
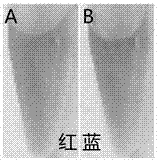
图2为本发明实施例1中使用基于分析物催化聚合反应的hg2+比色检测方法分别检测(a)10μmhg2+样本溶液与(b)空白样(超纯水)所得比色结果的比较。
图3为本发明实施例2中使用基于分析物催化聚合反应的hg2+比色检测方法分析一系列含有不同浓度hg2+的样本溶液时在700nm处的吸收强度值(a700)与hg2+浓度的log值(logchg2+)之间的工作曲线。
具体实施方式
以下实施例将对本发明予以进一步的说明,但并不因此而限制本发明。
实施例1:
使用基于分析物催化聚合反应的hg2+比色检测方法分别检测10μmhg2+样本溶液与空白样(超纯水)。
如图1所示,本实施例的具体步骤为:步骤一,在1个1.5ml的塑料检测试管中加入250μl2μm的邻苯二胺溶液(由电阻率为18.2mω·cm的超纯水配制),随后往该溶液中滴加250μl10μmhg2+样本溶液(由电阻率为18.2mω·cm的超纯水配制的氯化汞溶液),并摇动试管使两种溶液混合均匀后置于50℃下反应60min,制得反应溶液;步骤二,在上述反应溶液中继续加入500μl红色金纳米颗粒溶液(粒径约15nm,由柠檬酸钠还原氯金酸制得,且制备好的金纳米颗粒表面因吸附了柠檬酸根阴离子而呈负电荷性),并摇动试管使溶液混合均匀,5min后,肉眼观测溶液的颜色变化。
根据相同的步骤,分析空白样,即超纯水(电阻率为18.2mω·cm),并肉眼观测溶液的颜色变化。从图2可以看出,检测空白样得到的是蓝色溶液,而检测10μmhg2+分析物所得的是红色溶液。这是因为检测空白样时,邻苯二胺在其水溶液中电离后呈正电荷性,可以通过介导表面带负电荷的金纳米颗粒发生凝集,导致反应溶液产生由红变蓝的颜色变化。而当样本中存在hg2+时,hg2+可以高效、特异地催化氧化聚合邻苯二胺小分子为聚邻苯二胺(聚合物)。由于该产物不能导致金纳米颗粒发生凝集,整个反应溶液依然保持金纳米颗粒溶液的原始红色。图2中的对比实验结果表明,本发明的简单超灵敏的hg2+比色检测方法切实可行。
实施例2:
使用基于分析物催化聚合反应的hg2+比色检测方法分析浓度范围为9.7nm~5μm的hg2+样本溶液。具体实施过程如下:
如图1所示,本实施例中每个hg2+样本溶液分析的具体步骤为:步骤一,在1个1.5ml的塑料检测试管中加入250μl2μm的邻苯二胺溶液(由电阻率为18.2mω·cm的超纯水配制),随后往该溶液中滴加250μl某一浓度hg2+样本溶液(由电阻率为18.2mω·cm的超纯水配制的氯化汞溶液),并摇动试管使两种溶液混合均匀后置于50℃下反应60min,制得反应溶液;步骤二,在上述反应溶液中继续加入500μl红色金纳米颗粒溶液(粒径约15nm,由柠檬酸钠还原氯金酸制得,且制备好的金纳米颗粒表面因吸附了柠檬酸根阴离子而呈负电荷性),并摇动试管使溶液混合均匀,5min后,肉眼观测溶液的颜色变化,并使用紫外-可见分光光度计量测该溶液在700nm处的吸收强度值(a700)。将所有样本的a700值对hg2+浓度的log值(logchg2+)作图(图3),即完成hg2+的定量测定。
由图3可知,随着hg2+浓度的增加,相应的a700值逐渐减少。这是因为,当样本中hg2+浓度较大时,分析物可以高效、特异地催化氧化聚合邻苯二胺小分子为聚邻苯二胺(聚合物)。此时,剩余的邻苯二胺分子不足以通过静电作用介导金纳米颗粒发生凝集,含有较多自由分散的金纳米颗粒的相应混合溶液在700nm处的吸收强度值,即a700值较小。此外,图3显示,新方法量测所有hg2+样本所得a700值与hg2+浓度的log值(logchg2+)在两个浓度范围(即9.7nm~0.62μm和0.62~5μm)内呈现良好的线性关系。
- 还没有人留言评论。精彩留言会获得点赞!
- 用于烯烃聚合的催化剂组分及其制备方法和应用和用于烯烃聚合的催化剂及其应用与制造工艺
- 用于烯烃聚合的催化剂组分及其制备方法和应用和用于烯烃聚合的催化剂及其应用与制造工艺
- 催化剂组分及其制备方法和应用和用于烯烃聚合的催化剂体系及其应用和烯烃聚合方法与制造工艺
- 用于烯烃聚合的催化剂组分及其制备方法和应用和用于烯烃聚合的催化剂及其应用与制造工艺
- 用于烯烃聚合的催化剂组分及其制备方法和应用和用于烯烃聚合的催化剂及其应用与制造工艺
- 用于烯烃聚合的催化剂组分及其制备方法和应用和用于烯烃聚合的催化剂及其应用与制造工艺
- 用于烯烃聚合的催化剂组分及其制备方法和应用和用于烯烃聚合的催化剂及其应用与制造工艺
- 催化剂组分及其制备方法和应用和用于烯烃聚合的催化剂体系及其应用和烯烃聚合方法与制造工艺
- 一种回收甲烷磺酸的装置的制造方法
- 一种用于生产高熔体流动速率聚烯烃的含杂环类化合物的烯烃聚合反应催化剂体系的制作方法