基于富勒烯或其衍生物采用荧光分子探针检测氧气的方法与流程
本发明涉及富勒烯材料的应用领域,特别涉及基于富勒烯或其衍生物采用荧光分子探针检测氧气的方法。
背景技术:
氧气在生物生命活动中发挥着举足轻重的作用。生物体内的细胞需要氧气来进行有氧代谢从而维持日常生理活动。缺氧会使生物的生命活动受到严重的损害,情况严重可能会出现昏迷甚至死亡。而氧过量则会造成“氧中毒”,导致眩晕,感觉迟钝、刺痛感觉、视觉以及听觉受损、意识减退等症状。只有适当的氧浓度才会维持生物生命活动的正常进行。所以对生物体内的氧含量的检测就显得至关重要。
目前已有一些氧气检测方法如滴定法、电流分析法、热致发光法。虽然,这些方法可以有效的检测氧气的含量,但是也存在着一些弊端,比如:响应时间长,无法持续检测,极易被其他气体干扰,而且需要的成本也比较高等,对于微量的氧气很难通过仪器精准的进行观察和测量。
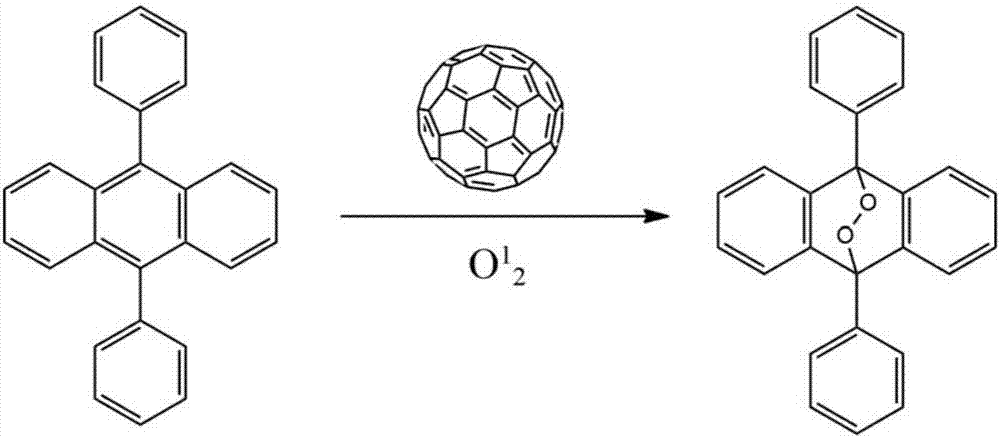
现有可采用荧光探针检测活性氧。单线态氧是氧气的一种激发态,也是一种高活性的分子,也是一种典型的活性氧分子。大多数单线态氧荧光探针都是基于它与蒽的反应。大多数单线态氧荧光探针是选择蒽或者9,10-二苯蒽作为识别基团。荧光探针在单线态氧的作用下,发生环加成反应生成内过氧化物,荧光团的荧光得到猝灭,从而达到检测单线态氧的目的。
因此,可将氧气在一定条件下转变成单线态氧,借助荧光分子与单线态氧相互作用后荧光显著变化的特性来设计一种响应时间快、选择性好、灵敏度高、操作简单的用来检测氧气浓度的荧光分子探针,其有望在生物科学、基础医学和环境检测等领域中被广泛应用。
技术实现要素:
为了解决上述现有技术中的问题,本发明提供了一种采用荧光分子探针检测氧气的方法,具体为基于富勒烯或富勒烯衍生物并采用荧光分子探针来检测氧气的方法。
本发明所提供的采用荧光分子探针检测氧气的方法,包括如下步骤:
(1)将富勒烯和/或富勒烯衍生物溶解在卤代苯、烷基苯或二硫化碳中,配制成含有富勒烯和/或富勒烯衍生物的溶液,即为溶液1;
(2)将荧光分子溶解在卤代苯、烷基苯或二硫化碳中,配制成含有荧光分子的溶液,即为溶液2;
(3)将溶液1和溶液2混合,得到含有富勒烯和/或富勒烯衍生物的荧光分子溶液;
(4)将步骤(3)得到的混合溶液抽真空,使氧气浓度降为0ml/cm3,得到检测体系;
(5)在光照条件下,建立检测体系中荧光信号强度与氧含量的线性关系;
(6)将待测样品通入到与步骤(4)相同的检测体系中,并在与步骤(5)相同的光照条件下测定检测体系中荧光信号强度,进而计算得到待测样品中的氧含量。
富勒烯和/或富勒烯衍生物在光照条件下能够与不同浓度的氧气相互作用产生单线态氧,荧光分子与单线态氧反应生成荧光分子的环氧化合物即内过氧化合物,环氧化合物荧光强度低或不发出荧光,即发生荧光猝灭。
荧光分子和单线态氧的反应为可逆反应:由于荧光分子与单线态氧反应生成的环氧化合物具有热不稳定性,在加热条件下,在温度范围为100~120℃,加热时间为20~60min的条件下,环氧化合物能够发生可逆的反应重新变成荧光强度很大的荧光分子,这使得这种荧光探针可以反复利用,高效、便捷。利用荧光分子本体的特征紫外吸收以及环氧化合物生成之后特征的紫外吸收的变化,能够发现几乎90%以上的环氧化合物都能进行可逆的反应(参见图1)。
所述富勒烯包括空心富勒烯和内嵌富勒烯的至少一种。
所述空心富勒烯包括通式为c2m的由碳原子组成的笼状结构的富勒烯,其中30≤m≤60,可选的为c60、c70、c76、c78、c82、c84中的至少一种。
所述内嵌富勒烯包括n@c60、la@c72、sc2@c74、sc2@c76、la2@c80、sc3n@c80、tm@c82、gd@c82、sc2c2@c84中的至少一种;
所述富勒烯衍生物包括富勒烯氧化物和富勒烯加成产物中的至少一种,可选的富勒烯氧化物为c60o、c70o中的至少一种,富勒烯加成产物为富勒烯1,3-偶极环加成产物、富勒烯宾格尔加成产物中的至少一种。
所述荧光分子为具有联苯结构的共轭结构有机分子,可选的为9,10-二苯蒽、9-蒽-β-丙酸。
所述卤代苯为氯苯,烷基苯为甲苯。
所述溶液1中富勒烯和/或富勒烯衍生物的浓度为10-6mol/l~10-2mol/l。
所述溶液2中荧光分子的浓度为10-6mol/l~10-2mol/l。
所述步骤(3)中溶液1和溶液2进行混合时,溶液1∶溶液2的体积比=1∶3~3∶1。
通入的所述待测样品可包括气态样品或液态样品。
所述光照条件包括氙灯照射、卤灯照射、汞灯照射,可选的为氙灯照射,进一步可选的为氙灯白光光源照射。
所述光照强度为1mw~30mw,光照时间为1min~60min。
步骤(5)中所述建立检测体系中荧光信号强度与氧含量的线性关系的具体步骤是:在检测体系中,根据多个氧气浓度以及每个氧气浓度对应的荧光强度绘制横坐标为氧气浓度、纵坐标为荧光信号强度的标准曲线图并确定线性范围。
与现有技术相比,本发明具有如下有益效果:
(1)富勒烯和/或富勒烯衍生物在光照条件下能够与不同浓度的氧气相互作用,经检测esr(electronspinresonance)电子自旋共振信号变化证明该相互作用能够高效产生不同量的单线态氧(1o2),而荧光分子和单线态氧相互作用所得终产物经核磁共振氢谱检测,可证明为环氧化合物。由于在光照条件下、且在富勒烯和/或富勒烯衍生物和荧光分子足量的情况下,氧气形成单线态氧以及单线态氧与荧光分子反应的速度均非常迅速,因此可粗略认为最先检测到氧气时的氧气浓度即为该检测方法可检测到的最低氧气浓度。在实施例1的实验条件下,通入氧气2s后即可检测到荧光发生下降,此时检测体系中氧气浓度为0.0707ml/cm3,检测限低,检测灵敏度高;在实施例3的实验条件下,光照2min后检测体系荧光强度就发生明显的下降,下降率约为89%,检测方法的响应速度快,因此该检测方法高效,可操作性强。
(2)可以选用的富勒烯种类多,制备分离纯化的条件已经比较成熟。
(3)选用的荧光分子性质稳定,成本低廉,荧光特性明显。
(4)氧气检测完毕后,在加热条件下所得环氧化合物即内过氧化物90%能够发生可逆反应,重新变成荧光强度很大的荧光分子,使得荧光探针可以反复利用。
附图说明
图1是9,10-二苯蒽荧光分子可逆变化的紫外-可见吸收光谱。
图2是实施例1的荧光探针9,10-二苯蒽在空心富勒烯存在的条件下与单线态氧的作用过程图。
图3是荧光探针9,10-二苯蒽与1o2反应前后的核磁共振氢谱图。
图4是实施例1中的检测体系加入捕获剂temp(2,2,6,6-四甲基哌啶醇)条件下光照前后的esr(electronspinresonance)电子自旋共振变化图。
图5是实施例1的检测结果验证步骤中得到的检测体系经不同时间光照的荧光猝灭光谱图。
图6是实施例2的荧光探针9-蒽-β-丙酸在空心富勒烯存在的条件下与单线态氧的作用过程图。
图7是荧光探针9-蒽-β-丙酸与1o2反应前后的核磁共振氢谱图。
图8是实施例2的检测结果验证步骤中得到的检测体系经不同时间光照的荧光猝灭光谱图。
图9是实施例3的荧光探针9,10-二苯蒽与在内嵌富勒烯存在的条件下与单线态氧的作用过程图。
图10是实施例3的检测结果验证步骤中得到的检测体系经不同时间光照的荧光猝灭光谱图。
图11是在实施例1条件下不同氧气含量对应的荧光信号强度的下降趋势图。
具体实施方式
下面结合附图,对本发明的具体实施方式进行详细描述,但应当理解本发明的保护范围并不受具体实施方式的限制。
以下实施例如无特殊说明,检测体系均是建立在4cm3的密闭容器中,其中该容器中的检测体系均为3ml,即含有富勒烯和/或富勒烯衍生物的荧光分子溶液均为3ml。
实施例1~实施例3的检测体系中荧光强度值均是在最大吸收值为445nm的检测条件下读取出来的。
实施例1
一种基于富勒烯c60采用荧光分子探针9,10-二苯蒽检测氧气的方法,反应路线图参见图2,包括如下步骤:
(1)将富勒烯c60溶解在二硫化碳中,配制成富勒烯c60浓度为10-3mol/l的溶液1;
(2)将荧光分子9,10-二苯蒽溶解在二硫化碳中,配制成9,10-二苯蒽浓度为10-2mol/l溶液2;
(3)按溶液2∶溶液1的体积比为1∶1,将溶液2加入到溶液1中,得到含有富勒烯c60的荧光分子溶液;
(4)将步骤(3)得到的混合溶液抽真空,使氧气浓度降为0ml/cm3,得到检测体系,然后分别将0ml、0.555ml、1.11ml、1.665ml、2.22ml、2.775ml、3.33ml体积的纯氧气通入7个独立的检测体系中,每个检测体系中的氧气浓度依次为0ml/cm3、0.1388ml/cm3、0.2775ml/cm3、0.4163ml/cm3、0.555ml/cm3、0.6938ml/cm3、0.8325ml/cm3;
(5)用波长为200~1000nm的20mw的氙灯白光光源照射(其中在445nm样品具有最大吸收)以上检测体系2min,密闭容器中的氧气产生单线态氧,荧光分子与单线态氧生成环氧化合物,发生荧光猝灭,检测体系中荧光信号强度,绘制图11所示的横坐标为氧气浓度、纵坐标为信号强的标准曲线图。
其中,氧气通入的具体过程是:通过一个直径为0.3mm的小孔,向含有以上3ml检测体系的密闭容器中以2m/s的流速通入氧气。
当通入氧气2s后,可检测到荧光发生下降,说明向检测体系通入氧气2s后,在富勒烯存在下,环氧化合物开始产生,此时对应通入的氧气体积为:(2m/s×2s×102)×(π×(0.3mm/2)2×10-2)=0.2826ml,进而得到通入2s时检测体系的氧气浓度为:0.2826/4=0.0707ml/cm3。
由图11可以得出,在氧气浓度为0.707ml/cm3至0.555ml/cm3的范围内,荧光信号强度随氧气浓度的增加呈现线性变化,得到的函数是:
y=3398.2-4173.8x
式中,x为氧气浓度,y为荧光强度
根据此公式,可以在相同条件下(即富勒烯和荧光分子的种类相同、含量相同,待测体系的光线种类、照射时间相同),根据检测的待测样品的荧光信号的强度值得到待检测样品中氧气的浓度,从而检测出待测样品中氧气含量。
检测结果验证:重新准备一个新的体积为4ml的密闭容器,其检测体系与上述步骤(4)中相同,将检测体系抽真空,然后通入0.74ml纯氧气,待光照2min后,检测到体系的荧光强度为2700a.u.;另外,将此氧气浓度0.74/4=0.185ml/cm3代入步骤(5)中所述线性函数y=3398.2-4173.8x中,得到理论的荧光强度为2626a.u.,与检测到的荧光强度2700a.u.仅相差74a.u.,在误差容许范围内,因此本发明采用的检测方法可用于检测待测样品中氧气的具体含量。因此,此检测方法能够精确地检测较低浓度的氧气含量。
在图3核磁共振氢谱图中(采用dmso作为氘代试剂),a、b、c、d、e分别代表9,10-二苯蒽对应的五种氢,a’、b’、c’、d’、e’代表9,10-二苯蒽内过氧化物的五种氢。图3中最上面的图代表9,10-二苯蒽和富勒烯混合均匀未光照的核磁氢谱图,从氢谱中可以看到9,10-二苯蒽并未发生改变,说明在未光照的条件下9,10-二苯蒽与富勒烯不发生化学反应;下面的两幅图分别代表向9,10-二苯蒽和富勒烯混合均匀的溶液通氧气20s、100s且在氙灯光源下光照2min后的核磁氢谱,可以看到,氢谱中出现了新的物质,说明光照条件下混合溶液发生了化学反应。当通氧量为20s时,9,10-二苯蒽还有剩余,氢谱显示的是9,10-二苯蒽和9,10-二苯蒽内过氧化物的混合物;当通入100s时,9,10-二苯蒽完全反应,产物全部是9,10-二苯蒽内过氧化物。从氢谱中可以得出,比对体系光照前后两种物质,氢的个数没有发生变化,但是发生了相对的位移变化,说明有新的物质生成,比对氢的位置,可以确定新生成的物质为9,10-二苯蒽内过氧化物。
还通过esr电子自旋共振检测单线态氧,检测过程是:由于temp捕获1o2的能力很强,极少量的1o2都可以捕获到,因此选用temp(2,2,6,6-四甲基哌啶醇)为捕获剂,temp捕获到经光照后的检测体系中的1o2,生成了tempol(1-氧基-2,2,6,6-四甲基-4-羟基哌啶),检测到tempol的esr信号明显增强(参见图4),证明检测体系生成了单线态氧1o2,从而证明在富勒烯c60的作用下,经光照,将检测体系中的氧气转变成了单线态氧,从而引起荧光的猝灭。
同时,由图5可知,光照前体系荧光强度为3500a.u.,光照2min后,体系荧光强度变为2700a.u.,因此,含有9,10-二苯蒽和富勒烯c60的检测体系经光照后荧光强度明显下降,荧光强度的下降率为23%,响应时间快;同时随着光照时间的延长,分子的荧光信号强度下降不明显。
说明:图5中的荧光信号强度由上到下依次为在9,10-二苯蒽+c60(未光照)、9,10-二苯蒽+c60(光照2min)、9,10-二苯蒽+c60(光照4min)、9,10-二苯蒽+c60(光照6min)、9,10-二苯蒽+c60(光照8min)、9,10-二苯蒽+c60(光照10min)、9,10-二苯蒽+c60(光照12min)的条件下得到的荧光信号强度。
实施例2
一种基于富勒烯c60采用荧光分子探针9-蒽-β-丙酸检测氧气的方法,反应路线图参见图6,包括如下步骤:
(1)将富勒烯c60溶解在二硫化碳中,配制成富勒烯c60浓度为10-3mol/l的溶液1;
(2)将荧光分子9-蒽-β-丙酸溶解在二硫化碳中,配制成9-蒽-β-丙酸浓度为10-4mol/l溶液2;
(3)按溶液2:溶液1的体积比为1:1,将溶液1加入到溶液2中,得到含有富勒烯c60的荧光分子溶液;
(4)按上述实施例1中的步骤(4)构建7个检测体系,同时按上述实施例1中的步骤(5)绘制横坐标为氧气浓度、纵坐标为信号强的标准曲线图,进而得到荧光强度和氧气浓度的线性函数,因此可以根据检测的待测样品的荧光信号的强度值得到待检测样品中氧气的浓度。
检测结果验证:重新准备一个新的体积为4ml的密闭容器,其检测体系与上述步骤(4)中相同,将检测体系抽真空,然后通入0.74ml纯氧气,待光照2min后,检测到体系的荧光强度为2400a.u.;同时,根据步骤(4)得到的函数以及氧气浓度0.74/4=0.185ml/cm3,得到理论的荧光强度为2320a.u.,与检测到的荧光强度2400a.u.仅相差80a.u.,在误差容许范围内。因此,此检测方法能够精确地检测较低浓度的氧气含量。
图7的核磁共振氢谱图中(采用cdcl3作为氘代试剂),a、b、c、d、e、f分别代表9-蒽-β-丙酸对应的六种氢,a’、b’、c’、d’、e’、f’代表9-蒽-β-丙酸内过氧化物的六种氢。图7中最上面的图代表9-蒽-β-丙酸和富勒烯混合均匀未光照的核磁氢谱图,从氢谱中可以看到9-蒽-β-丙酸并未发生改变,说明在未光照的条件下9-蒽-β-丙酸与富勒烯不发生化学反应;下面的图代表向9-蒽-β-丙酸和富勒烯混合均匀的溶液通氧气20s且在氙灯光源下光照2min后的核磁氢谱,可以看到,氢谱中出现了新的物质,说明在光照的条件下混合溶液中发生了化学反应。当通氧20s时,9-蒽-β-丙酸还有剩余,氢谱显示的是9-蒽-β-丙酸和9-蒽-β-丙酸内过氧化物的混合物。从氢谱中可以得出,比对体系光照前后两种物质,氢的个数没有发生变化,但是发生了相对的位移变化,证明有新的物质生成,比对氢的位置,可以确定新生成的物质为9-蒽-β-丙酸内过氧化物。
由图8可知,光照前体系荧光强度为5500a.u.,光照2min后,体系荧光强度为2400a.u.,因此,含有9-蒽-β-丙酸和富勒烯c60的检测体系经光照后荧光强度明显下降,荧光强度的下降率为56%,响应时间快;同时随着光照时间的延长,分子的荧光信号强度下降不明显。
说明:图8中的荧光信号强度由上到下依次为在9-蒽-β-丙酸+c60(未光照)、9,10-二苯蒽+c60(光照2min)、9,10-二苯蒽+c60(光照4min)、9,10-二苯蒽+c60(光照6min)、9,10-二苯蒽+c60(光照8min)、9,10-二苯蒽+c60(光照10min)、9,10-二苯蒽+c60(光照12min)的条件下得到的荧光信号强度。
实施例3
一种基于内嵌富勒烯sc3n@c80采用荧光分子探针9,10-二苯蒽检测氧气的方法,包括如下步骤:
(1)将内嵌富勒烯sc3n@c80溶解在二硫化碳中,配制成内嵌富勒烯sc3n@c80浓度为10-3mol/l的溶液1;
(2)将荧光分子9,10-二苯蒽溶解在二硫化碳中,配制成9,10-二苯蒽浓度为10-4mol/l溶液2;
(3)按溶液1与溶液2的体积比为1:1,将溶液1加入到溶液2中,得到含有内嵌富勒烯sc3n@c80的荧光分子溶液;
(4)按上述实施例1中的步骤(4)构建7个检测体系,同时按上述实施例1中的步骤(5)绘制横坐标为氧气浓度、纵坐标为信号强的标准曲线图,进而得到荧光强度和氧气浓度的线性函数,因此可以根据检测的待测样品的荧光信号的强度值得到待检测样品中氧气的浓度。
检测结果验证:重新准备一个新的体积为4ml的密闭容器,其检测体系与上述步骤(4)中相同,将检测体系抽真空,然后通入0.74ml纯氧气,待光照2min后,检测到体系的荧光强度为300a.u.;同时,根据步骤(4)得到的函数以及氧气浓度0.74/4=0.185ml/cm3,得到理论的荧光强度为350a.u.,与检测到的荧光强度300a.u.仅相差50a.u.,在误差容许范围内。因此,此检测方法能够精确地检测较低浓度的氧气含量。
由图10可知,光照前荧光强度为2750a.u.,光照2min后,体系荧光强度为300a.u.,因此,含有9-蒽-β-丙酸和内嵌富勒烯sc3n@c80的检测体系经光照后荧光强度明显下降,荧光强度下降率为89%,响应时间快;同时随着光照时间的延长,分子的荧光信号强度下降不明显。
说明:图10中的荧光信号强度由上到下依次为在9,10-二苯蒽+sc3n@c60(未光照)、9,10-二苯蒽+sc3n@c60(光照2min)、9,10-二苯蒽+sc3n@c60(光照4min)、9,10-二苯蒽+sc3n@c60(光照6min)、9,10-二苯蒽+sc3n@c60(光照8min)、9,10-二苯蒽+sc3n@c60(光照10min)、9,10-二苯蒽+sc3n@c60(光照12min)的条件下得到的荧光信号强度。
前述对本发明的具体示例性实施方案的描述是为了说明和例证的目的。这些描述并非想将本发明限定为所公开的精确形式,并且很显然,根据上述教导,可以进行很多改变和变化。对示例性实施例进行选择和描述的目的在于解释本发明的特定原理及其实际应用,从而使得本领域的技术人员能够实现并利用本发明的各种不同的示例性实施方案以及各种不同的选择和改变。本发明的范围意在由权利要求书及其等同形式所限定。
- 还没有人留言评论。精彩留言会获得点赞!