白桦脂醇的衍生物的制造方法与工艺
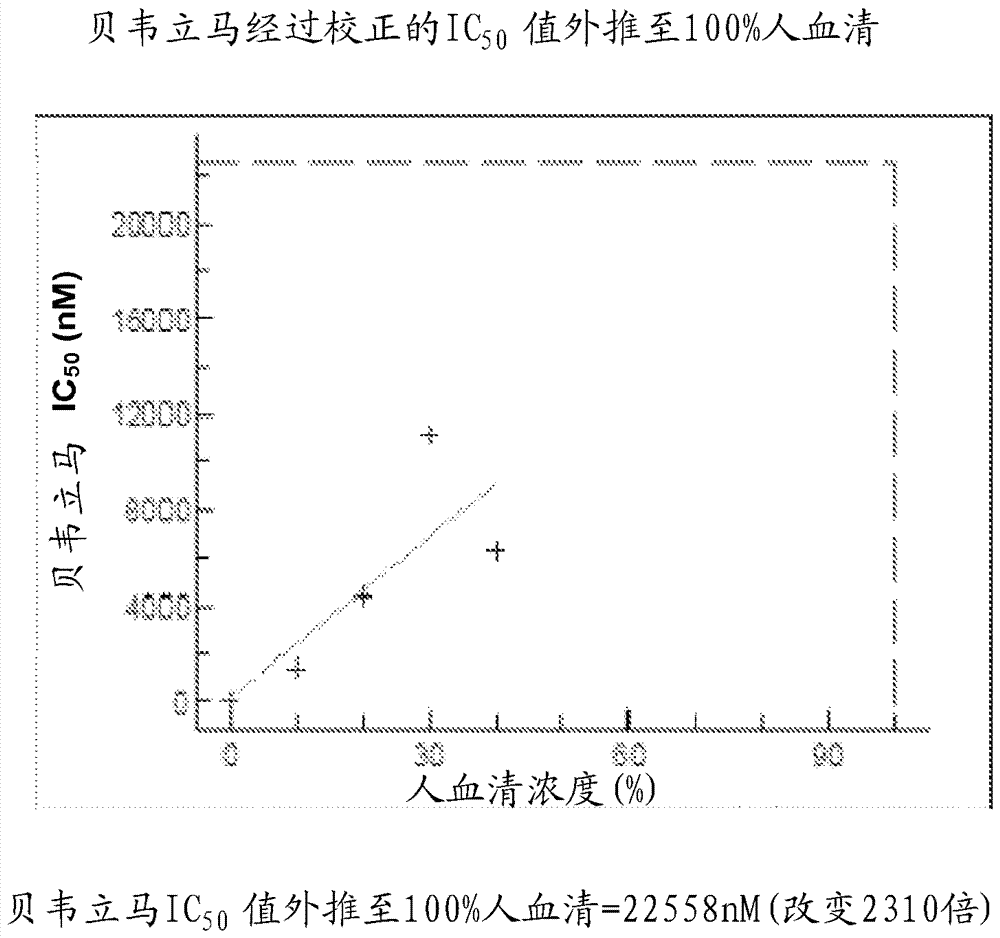
白桦脂醇的衍生物相关专利和专利申请的交叉引用本申请是PCT申请,要求2011年12月16日申请的美国临时专利申请No.61/576,448的权益,本文以引证的方式引入其全部内容。发明领域本发明涉及化合物、药物组合物和其使用方法,其用于:(i)在感染了HIV的患者中抑制HIV复制,或(ii)通过给予这种化合物来治疗感染了HIV的患者。发明背景1型人类免疫缺陷性病毒(HIV-1)导致获得性免疫缺陷疾病(AIDS)的传染。HIV病例的数量持续增加,目前,全世界超过两千五百万名个体因为该病毒而蒙受伤害。目前,用抗逆转录病毒药物来长期抑制病毒复制是治疗HIV-1感染的唯一方案。实际上,美国食物与药品管理局已经批准了二十五种药物,跨过六种不同抑制剂类别,这极大地提高了患者存活率和生活质量。然而,还需要其它疗法,这是由于不合乎需要的药物-药物相互作用、药物-食品相互作用、对治疗的非依存性以及酶靶向突变所造成的耐药性。目前,几乎所有的HIV阳性病人都是用抗逆转录病毒药物组合的治疗方案来治疗的,这种治疗方案被称为高效抗逆转录病毒疗法(“HAART”)。然而,HAART疗法通常很复杂,这是因为,为了避免快速出现耐药的HIV-1变体,通常每天必须给予患者不同药物的组合。尽管对患者存活率有积极影响,但还是会出现耐药性。多药耐受性HIV-1分离株的出现,具有严重的临床后果,并且必须采用被称为挽救治疗的新药方案来抑制。现行的指南推荐挽救治疗包括至少两种完全有效的药物,优选三种完全有效的药物。通常,一线治疗将三至四种靶向病毒酶逆转录酶和蛋白酶的药物进行联用。挽救治疗的一个方案是,给予机理类别相同的药物的不同组合,其中该类药物保持抗耐受性分离株的活性。然而,这种方法的方案通常受到限制,这是因为,耐受性突变经常对于相同类别的不同药物产生广泛的交叉抗药性。最近,随着融合抑制剂、进入抑制剂和整合酶抑制剂的发展,可以使用替代性治疗策略。然而,据报道,在实验室和病人中,对于所有三种新药类别已经出现了耐药性。因此,用抗逆转录病毒药物来持续成功地治疗HIV-1感染的病人,需要继续开发具有新靶向和作用机理的新的改良药物。目前,用抗逆转录病毒药物来长期抑制病毒复制是治疗HIV-1感染的唯一方案。迄今为止,许多批准的药物极大地提高了患者的存活率。然而,被称为高效抗逆转录病毒治疗(HAART)的治疗方案通常很复杂,这是因为,为了避免快速出现耐药的HIV-1变体,通常每天必须给予患者不同药物的组合。尽管HAART对患者存活率有积极影响,但还是会出现耐药性。HIVGag多蛋白前体(Pr55Gag)代表新的治疗靶向,其由四个蛋白结构域(基质(MA)、衣壳(CA)、核衣壳(NC)和p6)以及两种间隔肽(SP1和SP2)组成。虽然Gag多蛋白的裂解在感染性病毒颗粒产生的进程中起着重要作用,但迄今为止,还没有批准这种机理的抗逆转录病毒药物。在大多数细胞类型中,组装出现在质膜中,并且Gag的MA结构域介导膜结合。通过来自细胞的未成熟颗粒的芽殖完成组装。伴随着颗粒释放,病毒编码的PR将Gag裂解为四个成熟的蛋白结构域:MA、CA、NC和p6,以及两种间隔肽:SP1和SP2。Gag-Pol也被PR裂解,释放出病毒酶PR、RT和IN。Gag蛋白水解过程诱导颗粒内的形态重排,被称为成熟。成熟将未成熟的环形颗粒转化为成熟病毒体,该病毒体含有致密的锥形核,这种核由CA壳与NC以及病毒酶RT和IN的复合体组成,CA壳包围病毒RNA基因组。成熟能够产生感染新细胞的病毒,并且对颗粒感染性来说是绝对不可缺少的。贝韦立马(Bevirimat)(PA-457)是成熟抑制剂,其抑制Gag处理的最后一步:衣壳-SP1(p25)转化为衣壳,这是形成传染性病毒颗粒所必需的。贝韦立马(Bevirimat)具有抗ART耐受性和野生型HIV的活性,并且与所有类别的抗逆转录病毒协同作用。在达到≥20μg/mL的波谷水平和在Q369、V370或T371没有任何关键基线Gag多态性的病人中,贝韦立马(Bevirimat)平均降低HIV病毒载量1.3log10/mL。然而,与在Q369、V370或T371没有Gag多态性的病人相比,在这些位点具有Gag多态性的贝韦立马(Bevirimat)使用者表现出显著更低的载量减少。成熟抑制剂的其它例子可以在以下文献中得到:PCT专利申请No.WO2011/100308,"DerivativesofBetulin";PCT专利申请No.PCT/US2012/024288,"NovelAnti-HIVCompoundsandMethodsofUseThereof;中国PCT申请No.PCT/CN2011/001302,"CarbonylDerivativesofBetulin";中国PCT申请No.PCT/CN2011/001303,"MethyleneDerivativesofBetulin";中国PCT申请Nos.PCT/CN2011/002105和PCT/CN2011/002159,"PropenoateDerivativesofBetulin"。在现有技术中,成熟抑制剂在多态性覆盖范围方面还留有开放的缺口,由此,针对大量临床相关的gag序列的效能以及在长期持久性实验中稳定效果所需要的总效能(包括临床相关的蛋白调节的抗病毒活性)是非常重要的。迄今为止,还没有成熟抑制剂能够使这些性能达到最佳平衡。因此,在本领域,还需要发现有效平衡上述性能的、用于预防和/或治疗HIV感染的替代性化合物。本发明概述按照本发明的一个实施方案,提供了式I的化合物:或其可药用盐,其中:A是L1和L2独立地选自键或[C(R6R6')]q;Q在每个情况下独立地选自-CH2-或-C(=O)-;W选自键或O;R1选自氢、(C1-C12)烷基、-C(O)R5、-CH2-O-(C1-C6)烷基、2-四氢-2H-吡喃、和R2选自-H、(C1-C12)烷基、-(C1-C6)烷基-OR4、-(C1-C6)烷基-O-(C1-C6)烷基、-C(O)R5、-(CH2)rNR7R8和-(CH2)rN+(R4)3,其中,当W是O时,R1和R2可以任选与它们分别连接的O和N一起形成4至8元杂环基环,其中该杂环基环可以任选被一个至两个R11基团取代;R3选自氢、(C1-C12)烷基、-NR1R2、-OR5、X是单环的或双环的(C5-C14)芳基,Y选自单环或双环(C2-C9)杂环基,或单环或双环(C2-C9)杂芳基,每个具有一个至三个选自S、N或O的杂原子,Z是单环或双环(C3-C8)环烷基;R2和R3可以任选与它们分别连接的氮和L2一起形成4至8元杂环基环,其中该杂环基环可以任选被一个至两个R11基团取代;R4选自-H和(C1-C6)烷基;R5选自-H、(C1-C6)烷基、-R3、-(CH2)rNR7R8和-(CH2)rOR7;R6和R6'独立地选自-H、(C1-C6)烷基、(C3-C8)环烷基、(C1-C6)烷氧基、卤代烷基、-Y、-(CH2)rNR7R8、-C(O)OH和-C(O)NH2,其中R6和R6'基团可以任选与它们连接的碳一起形成3至8元环烷基环,其中该环烷基环可以任选被一个至三个R11基团取代;R7和R8独立地选自-H、(C1-C6)烷基、(C3-C8)环烷基、-Q-芳基-(R4)n、-NR14R15、-C(O)CH3,其中R7和R8可以任选与它们连接的氮一起形成含有一个至三个选自下列杂原子的4至8元杂环基或杂芳基环:-NR5-、-O-、-S-、-S(O)-或-SO2-,其中该杂环基或杂芳基环可以任选被一个至三个R11基团取代;R9是卤素;R10是-N(R16)2;R11、R12和R13独立地选自氧代、羟基、卤素、(C1-C6)烷氧基、-R6(R9)q、-OR6(R9)q、硝基、-SO2R6、(C1-C6)烷基、-C(O)R10、-R4YR6、-CO(O)R4和-CO(O)R5,其中,任何两个R11、R12或R13基团可以任选连接形成3至8元环烷基、芳基、杂环基或杂芳基环,其中该杂环基或杂芳基环可以含有一个至三个选自下列的杂原子:-NR5-、-O-、-S-、-S(O)-或-SO2-,其中该环烷基、芳基、杂环基或杂芳基环可以任选被一个至三个R16基团取代;R14和R15独立地选自-H、(C1-C6)烷基、(C3-C8)环烷基、(C1-C6)烷氧基、-[C(R6)2]r-、-O[C(R6)2]r-、氧代、羟基、卤素、-C(O)R7、-R10和-CO(O)R2,其中R14和R15可以任选与它们连接的碳一起形成3至8元环烷基环,或含有一个至三个选自下列的杂原子的4至8元杂环基环:-NR5-、-O-、-S-、-S(O)-或-SO2-,其中该环烷基环或杂环基环可以任选被一个至三个R16基团取代;R16独立地选自-H、卤素、氧代、羟基、(C1-C6)烷基、(C1-C6)烷氧基、(C3-C8)环烷基、-R6(R9)q、-OR6(R9)q、-N(R4)2、-(CH2)r杂环基、-C(O)OH、-C(O)NH2、-R5(R9)q、-OR5(R9)q、硝基、-SO2R6、-C(O)R10和-CO(O)R4;m和n在每种情况下独立地是0、1、2、3或4;p独立地是0、1、2、3或4;和r和q在每种情况下独立地是0、1、2、3或4。在第二个方面,本发明涉及药物组合物,其含有:a)式I或式II的化合物或其药用盐;和b)药用赋形剂。在第三个方面,本发明是治疗HIV感染的方法,该方法包括:给予患有HIV感染的患者式I或式II的化合物或其可药用盐。本发明的化合物可用于治疗HIV感染的患者,或治疗处于获得HIV感染的危险之中的患者。附图的简要说明图1给出了柱状图,其对比了贝韦立马(Bevirimat)和化合物51抑制宽范围的一组HIV-1分离株的HIV逆转录酶活性的相对能力。图2给出了柱状图,其对比了化合物51和化合物C抑制宽范围的一组HIV-1分离株的HIV逆转录酶活性的相对能力。图3给出了贝韦立马(Bevirimat)的经过校正的IC50值外推至100%人血清的线形图。图4给出了化合物B的经过校正的IC50值外推至100%人血清的线形图。图5给出了化合物51的经过校正的IC50值外推至100%人血清的线形图。代表性的实施方案的详细说明在本申请中,提到了与化合物、组合物和方法有关的各种实施方案。所描述的各种实施方案意欲提供许多说明性实例,不应该将其理解为对替代性种类的描述。应特别注意的是,本文提供的各种实施方案的说明的范围可以重叠。本文讨论的实施方案仅仅是说明性的实施方案,并不限制本发明的范围。应该理解,本文使用的术语仅仅是为了描述具体实施方案,并不是用来限制本发明的范围。在该说明书和后面的权利要求中,将引用许多术语,它们被定义为具有下列含义。除非另作说明,否则,本文使用的“烷基”是指具有1至14个碳原子的单价饱和的脂肪族烃基,在一些实施方案中,具有1至6个碳原子。“(Cx-Cy)烷基”是指烷具有x至y个碳原子的烷基。例如,术语“烷基”包括直链和支链烃基,例如,甲基(CH3-)、乙基(CH3CH2-)、正丙基(CH3CH2CH2-)、异丙基((CH3)2CH-)、正丁基(CH3CH2CH2CH2-)、异丁基((CH3)2CHCH2-)、仲丁基((CH3)(CH3CH2)CH-)、叔丁基((CH3)3C-)、正戊基(CH3CH2CH2CH2CH2-)和新戊基((CH3)3CCH2-)。“亚烷基”是指具有1至10个碳原子的二价饱和脂肪族烃基,在一些实施方案中,具有1至6个碳原子。“(Cu-Cv)亚烷基”是指具有u至v个碳原子的亚烷基。亚烷基包括支链和直链烃基。例如,“(C1-C6)亚烷基”包括亚甲基、亚乙基、亚丙基、2-甲基亚丙基,二甲基亚乙基、亚戊基,等等。因此,可以通过下列结构举例说明术语“亚丙基”:。同样,可以通过下列三个结构的任一结构或更多结构举例说明术语“二甲基亚丁基”:。此外,术语“(C1-C6)亚烷基”包括支链烃基,例如,环丙基亚甲基,其可以通过下列结构来举例说明:。“烯基”是指具有2至10个碳原子并且具有至少1个乙烯基不饱和位点(>C=C<)的直链或支链烃基,在一些实施方案中,具有2至6个碳原子或2至4个碳原子。例如,(Cx-Cy)烯基是指具有x至y个碳原子的烯基,并且包括,例如,乙烯基、丙烯基、异丙烯基、1,3-丁二烯基,等等。“炔基”是指包含至少一个三键的直链一价烃基或支链一价烃基。术语“炔基”还包括具有一个三键和一个双键的那些烃基。例如,(C2-C6)炔基包括乙炔基、丙炔基,等等。“烷氧基”是指基团-O-烷基,其中烷基如本文所定义。烷氧基包括,例如,甲氧基、乙氧基、正丙氧基、异丙氧基、正丁氧基、叔丁氧基、仲丁氧基和正戊氧基。“酰基”是指基团H-C(O)-、烷基-C(O)-、烯基-C(O)-、炔基-C(O)-、环烷基-C(O)-、芳基-C(O)-、杂芳基-C(O)-和杂环-C(O)-。酰基包括“乙酰基”CH3C(O)-。“酰胺基”是指基团-NR20C(O)烷基、-NR20C(O)环烷基、-NR20C(O)烯基、-NR20C(O)炔基、-NR20C(O)芳基、-NR20C(O)杂芳基和-NR20C(O)杂环,其中R20是氢或烷基。“酰氧基”是指基团烷基-C(O)O-、烯基-C(O)O-、炔基-C(O)O-、芳基-C(O)O-、环烷基-C(O)O-、杂芳基-C(O)O-和杂环-C(O)O-。“氨基”是指基团-NR21R22,其中R21和R22独立地选自氢、烷基、烯基、炔基、芳基、环烷基、杂芳基、杂环、-SO2-烷基、-SO2-烯基、-SO2-环烷基、-SO2-芳基、-SO2-杂芳基和-SO2-杂环,其中R21和R22任选与其中结合的氮连接,形成杂环基团。当R21是氢、R22是烷基时,在本文中,氨基有时指的是烷基氨基。当R21和R22是烷基时,在本文中,氨基有时指的是二烷基氨基。当提及单取代的氨基时,R21或R22的任何一个是氢,但并非两个都是氢。当提及二取代的氨基时,R21和R22两者都不是氢。“羟氨基”是指基团-NHOH。“烷氧基氨基”是指-NHO-烷基,其中烷基如本文所定义。“氨基羰基”是指基团-C(O)NR26R27,其中R26和R27独立地选自氢、烷基、烯基、炔基、芳基、环烷基、杂芳基、杂环、羟基、烷氧基、氨基和酰胺基,其中R26和R27任选与其中结合的氮连接,形成杂环基团。“芳基”是指6至14个碳原子、没有环杂原子、具有单环的芳基(例如苯基),或具有多个缩合(稠合)环的芳基(例如,萘基或蒽基)。对于具有芳香和非芳香环(没有环杂原子)的多环系统,包括稠合、桥接和螺环系统,当连接点在芳碳原子处时(例如,5,6,7,8-四氢化萘-2-基是连接点在芳香苯基环的2位的芳基),使用术语“芳基”或“Ar”。“AUC”是指给药之后药物血浆浓度(不是浓度的对数)相对于时间的曲线下方的面积。“EC50值”是指得到半数最大响应时的药物浓度。“IC50值”是指药物的半数最大抑制浓度。有时,也将其转变为pIC50度量(-logIC50),其中,按指数规律更高的数值表示更大的效能。“进化枝”是指基于试验数据的假设结构。使用许多物种(或样本)的多个(有时数百个)特征,并统计上分析它们,发现它们最可能的系统树,由此发现进化枝。“氰基”或“腈”是指基团-CN。“环烃基”是指3至14个碳原子、没有环杂原子、具有单环或多环(包括稠合、桥接和螺环系统)的饱和或部分饱和的环基团。对于带有芳香和非芳香环(没有环杂原子)的多环系统,当连接点在非芳碳原子处时(例如5,6,7,8、-四氢化萘-5-基),使用术语“环烃基”。术语“环烃基”包括环烯基,例如环己烯基。环烃基的实例包括,例如,金刚烷基、环丙基、环丁基、环己基、环戊基、环辛基、环戊烯基和环己烯基。包括多个双环烷基环系统的环烷基的实例是双环已基、双环戊基、双环辛基,等等。下面列举和命名了两个这种双环烷基多环结构:双环已基和双环已基。“(Cu-Cv)环烷基”是指具有u至v个碳原子的环烷基。“螺环烷基”是指通过取代环结构中或具有2至9个碳原子的亚烷基中的共用碳原子上的两个氢原子所形成的3至10元环取代基,例如下列结构,其中与键(用波状线标明)连接的本文所示基团被螺环烷基取代:。“稠合的环烷基”是指通过取代环烷基环结构中不同碳原子上的两个氢原子所形成的3至10元环取代基,例如下列结构,其中本文示出的环烷基含有波状线标明的键,其与稠合的环烷基取代的碳原子键合:。“羧基”指的是基团(可互换)、、-C(O)O或-CO2。“卤代”或“卤素”是指氟、氯、溴和碘。“卤代烷基”是指被1至3个卤素基团取代的烷基(例如,二氟甲基或三氟甲基)。“卤代烷氧基”是指1至5个卤素基团取代的烷氧基(例如,当烷氧基具有至少2个碳原子时),或在一些实施方案中,被1至3个卤素基团取代(例如,三氟甲氧基)。“人血清蛋白转换试验”是指使用荧光素酶指示剂来测定抑制百分比(pIC50)的HIV试验。该HIV试验使用两种细胞共同培养系统。在该试验中,在存在和不存在化合物的条件下,将受感染的细胞系J4HxB2和指示细胞系HOS(deltaLTR+荧光素酶)共同培养。该试验用来发现能够防止J4HxB2细胞系感染HOS细胞的抑制剂。该试验可以检测HIV感染循环的任一阶段的抑制剂。“羟基”是指基团-OH。“杂芳基”是指1至14个碳原子和1至6个杂原子(选自氧、氮和硫)的芳基,并且包括单环(例如咪唑基)和多环系统(例如苯并咪唑-2-基和苯并咪唑-6-基)。对于具有芳香和非芳香环的多环系统,包括稠合、桥接和螺环系统,如果存在至少一个环杂原子,并且连接点在芳香环的一个原子上,则使用术语“杂芳基”(例如1,2,3,4-四氢喹啉-6-基和5,6,7,8-四氢喹啉-3-基)。在一些实施方案中,杂芳基的氮和/或硫环原子任选被氧化,提供N-氧化物(N→O)、亚磺酰基或磺酰基部分。更具体地说,术语杂芳基包括但不局限于:吡啶基、呋喃基、噻吩基、噻唑基、异噻唑基、三唑基、咪唑基、咪唑啉基、异噁唑基、吡咯基、吡唑基、哒嗪基、嘧啶基、嘌呤基、酞嗪基、萘吡啶基、苯并呋喃基、四氢苯并呋喃基、异苯并呋喃基、苯并噻唑基、苯并异噻唑基、苯并三唑基、吲哚基、异氮茚基、茚嗪基、二氢吲哚基、吲唑基、二氢吲哚基、苯并噁唑基、喹啉基、异喹啉基、喹嗪基、喹唑啉基、喹喔啉基、四氢喹啉基、异喹啉基、喹唑啉酮基、苯并咪唑基、苯并异噁唑基、苯并噻吩基、苯并哒嗪基、喋啶基、咔唑基、咔啉基、菲啶基、吖啶基、菲啰啉基、吩嗪基、吩噁嗪基、吩噻嗪基和邻苯二甲酰亚胺基。“杂环的”或“杂环”或“杂环烷基”或“杂环基”是指具有1至14个碳原子和1至6个杂原子(选自氮、硫、磷或氧)的饱和或部分饱和的环基团,并且包括单环和多环系统,包括稠合、桥接和螺环系统。对于带有芳香和/或非芳香环的多环系统,当存在至少一个环杂原子并且连接点在非芳香环的一个原子上时,使用术语“杂环的”、“杂环”、“杂环烷基”或“杂环基”(例如1,2,3,4-四氢喹啉-3-基、5,6,7,8-四氢喹啉-6-基和十氢喹啉-6-基)。在一个实施方案中,杂环基团的氮、磷和/或硫原子任选被氧化,形成N-氧化物、磷氧化物、亚磺酰基、磺酰基部分。更具体地说,杂环基包括但不局限于:四氢吡喃基、哌啶基、哌嗪基、3-吡咯烷基、2-吡咯烷酮-1-基、吗啉基和吡咯烷基。表示碳原子数目的前缀(例如,C3-C10)是指除了杂原子数目以外的杂环基部分中的碳原子总数。杂环和杂芳基的实例包括但不局限于:氮杂环丁烷、吡咯、咪唑、吡唑、吡啶、吡嗪、嘧啶、哒嗪、吡啶酮、茚嗪、异吲哚、吲哚、二氢吲哚、吲唑、嘌呤、喹嗪、异喹啉、喹啉、酞嗪、萘基吡啶、喹喔啉、喹唑啉、噌啉、蝶啶、咔唑、咔啉、菲啶、吖啶、菲咯啉、异噻唑、吩嗪、异噁唑、吩噁嗪、吩噻嗪、咪唑烷、咪唑啉、哌啶、哌嗪、二氢吲哚、邻苯二酰亚胺、1,2,3,4-四氢异喹啉、4,5,6,7-四氢苯并[b]噻吩、噻唑、噻唑烷、噻吩、苯并[b]噻吩、吗啉、硫吗啉(还称为硫杂吗啉)、哌啶、吡咯烷和四氢呋喃基。“稠合的杂环”或“稠杂环”指的是通过取代环烷基环结构中的不同碳原子上的两个氢原子所形成的3至10元环取代基,可以通过下列结构举例说明,其中本文给出的环烷基含有键(用波状线标明),其与被稠合杂环基团取代的碳原子键合:。本文使用的“化合物”和“化学实体”是指本文所公开的通式、那些通式的任何亚属所包括的化合物,以及在通式和亚属范围内的任何形式的化合物,包括该化合物的外消旋体、立体异构体和互变异构体。术语“杂原子”是指氮、氧或硫,并且包括氮的任何氧化形式(例如,N(O){N+—O-})、硫的氧化形式(例如S(O)和S(O)2)以及任何碱性氮的季铵化形式。“噁唑烷酮”是指5元杂环,含有一个氮和一个氧作为杂原子以及两个碳,且两个碳之一被羰基替代,例如通过下列任何结构举例说明,其中这里所示的噁唑烷酮基团是与母体分子键合的,利用波状线表示与母体分子键合的位置:。“氧代”是指(=O)基团。“多态性”是指两种或多种明显不同的表型存在于相同物种群中,其中出现一种以上的形式或形态。为了分类,形态必须同时占据相同环境,并且属于随机种群(自由匹配)。“蛋白结合”是指药物与血浆、组织膜、红细胞及血液中的其它组分中的蛋白的结合。“蛋白转换”是指,通过对比在不存在和存在人血清条件下测定的EC50值来测定结合转换。“QVT”是指分别在HIV-1Gag的Sp1片段的369、370和371位的氨基酸。“外消旋体”是指对映体的混合物。在本发明的一个实施方案中,式I的化合物或其可药用盐是对映体富集的,富含其中所有提到的手性碳是以一个构型存在的一种对映体。通常,关于对映体富集的化合物或盐,表示特定对映体包含该化合物或盐的所有对映体总重量的50%重量以上。化合物的“溶剂化物”指的是如上所述的那些化合物,其与化学计量或非化学计量的溶剂结合。化合物的溶剂化物包括化合物的各种形式的溶剂化物。在某些实施方案中,溶剂是挥发性、无毒的和/或可为人给药所接受的痕量溶剂。合适的溶剂化物包括水。“立体异构体”指的是一个或多个立构中心的手性不同的化合物。立体异构体包括对映异构体和非对映异构体。“互变异构体”是指的在质子位置方面不同的化合物的交替形式,例如烯醇-酮和亚胺-烯胺互变异构体,或含有一个与环-NH-部分和环=N-部分都连接的环原子的杂芳基基团的互变异构形式,例如吡唑、咪唑、苯并咪唑、三唑和四唑。术语'阻转异构体'是指由不对称的轴所产生的立体异构体。这可以由单键周围的阻旋作用产生,其中,转动势垒足够高,使得异构物种分化为稳定的非互变非对映体或对映体,包括其完全分离。本领域技术人员可以认识到,给核安装一个不对称的Rx,可以形成阻转异构体。此外,一旦第二手性中心建立在含有阻转异构体的给定分子处,结合在一起的两个手性要素可以产生非对映体和对映体的立体化学物种。根据Cx轴周围该取代情况,阻转异构体之间可以出现相互转化,或可以不出现相互转化,并且可能取决于温度。在有些情况下,阻转异构体可以在室温下快速互变,并且在环境条件下不能拆分。其它情况可以进行拆分和分离,但在几秒钟至几小时或甚至几天或几个月期间内,可能出现相互转化,因此,光学纯度随时间变化而显著地降低。在周围环境和/或高温下,可以完全限制其它物种的相互转化,因此,可以进行拆分和分离,并且得到稳定物种。当已知时,拆分的阻转异构体可以使用螺旋命名法来命名。对于这种命名,只考虑在轴前面和轴后面的最高优先级的两个配基。当转向(turn)优先级从前面的配基1转变为后面的配基1是顺时针方向时,构型是P,如果是反时针方向,构型是M。“可药用盐”指的是衍生自下列的可药用盐:本领域众所周知的各种有机和无机反离子,并且包括,例如钠、钾、钙、镁、铵、四烷基铵盐,当分子包含碱性官能团时,包括有机或无机酸的盐,例如盐酸盐、氢溴酸盐、酒石酸盐、甲磺酸盐、醋酸盐、马来酸盐和草酸盐。合适的盐包括下列文献所描述的那些盐:P.HeinrichStahl,CamilleG.Wermuth(Eds.),HandbookofPharmaceuticalSaltsProperties,Selection,andUse;2002。“病人”或“患者”是指哺乳动物,并且包括人和非人哺乳动物。“治疗”患者疾病是指:1)防止该疾病出现在易感染该疾病或还没有显示该疾病症状的患者中;2)抑制该疾病或延滞它的发展;或3)改善该疾病或导致该疾病的衰退。当在靠近以实线表示的单键处出现虚线时,则虚线代表在该位置任选的双键。同样,当在以实线表示的环结构或实线圆圈之内出现虚线圆圈时,则虚线圆圈代表一至三个任选的双键,该双键根据它们的正确化合价排列,同时考虑在环周围该环是否具有任选的取代基,这将为本领域技术人员所熟知。例如,在下面的结构中,虚线可以表示在该位置的双键或在该位置的单键:。类似地,下面的环A可以是一个没有任何双键的环己基环,或它还可以是具有在任何位置排列的、还描述了苯基环的正确的化合价的三个双键的苯基环。同样,在下面的环B中,任何X1-X5可以选自:C、CH、或CH2、N、或NH,且虚线圆圈表示环B可以是环己基或苯基环,或没有双键的含N杂环,或具有一至三个排列在任何位置、还描述了正确的化合价的双键的含N杂芳基:。当所画的具体化合物或通式具有芳香环、例如芳基或杂芳基环时,本领域技术人员应当理解,任何双键的具体的芳香位置都是等效位置的混杂,尽管它们被画到不同的化合物的不同位置或式与式中的不同位置。例如、在下面的两个吡啶环(A和B)中,双键被画在不同位置,然而,它们却是已知的相同的结构和化合物:。本发明包括化合物以及它们的药用盐。相应地,应该理解,在“化合物或其可药用盐”的背景下的单词“或”是指:1)单独的化合物,或化合物和其可药用盐(可供选择),或2)化合物和其可药用盐(组合)。除非另外指定,本文没有明确定义的取代基的命名是如此得出的:从官能团的末端部分开始命名,而后命名与连接点相邻的官能团。例如,取代基“芳基烷氧羰基”是指基团(芳基)-(烷基)-O-C(O)-。在术语例如“C(Rx)2”中,应该理解两个Rx基团可以相同,或如果所定义的Rx具有一种以上的可能身份,则它们可以不同。另外,某些取代基写作-RxRy,其中“-”是指靠近母体分子的键,Ry是官能团的末端部分。类似地,应当理解,上述定义不包括不允许的取代模式(例如,被5个氟基团取代的甲基)。这种不允许的取代模式是本领域技术人员所熟知的。如上所述,贝韦立马(Bevirimat)是还未经批准的抗HIV药物,其衍生自白桦脂酸类化合物,首次从棒花蒲桃(Syzygiumclaviflorum)(中国草药)中分离出来。人们认为它通过新的机理(所谓的成熟抑制)来抑制HIV。象蛋白酶抑制剂一样,贝韦立马(Bevirimat)及其它成熟抑制剂妨碍新转变为HIV多蛋白前体(称为gag)的蛋白酶加工。Gag是HIV病毒的主要结构蛋白。Gag与它本身以及与其它细胞和病毒因子进行一系列相互作用,完成感染性病毒颗粒的组装。然而,在HIV中自然存在的多态性出现于一些感染的个体中,由此降低了一些目前所考虑的疗法的抗HIV效果。实际上,研究表明,在衣壳/SP1间隔蛋白(CA/SP1)分裂位点中存在许多单核苷酸多态性,导致HIV病人对贝韦立马(Bevirimat)的临床耐药性。同样已知的是,SP1肽的谷氨酰胺-缬氨酸-苏氨酸(QVT)基序中的突变,导致HIV感染病人的贝韦立马(Bevirimat)耐药性。SP1肽的QVT基序中的突变,是不能对贝韦立马(Bevirimat)作出反应的主要预测器,并且已经重复地表明了这些突变的影响。这些问题最终导致贝韦立马(Bevirimat)的临床研发终止。参见Knapp,D.,等人,J.Clin.Microbiol.49(1):201-208(2011)。贝韦立马(Bevirimat):。贝韦立马(Bevirimat)的临床问题:多态性问题以及效能弱。MT4抗病毒试验NL4-3毒株,EC50=223nM。MT4抗病毒试验NL4-3毒株(具有V370A位点引导的突变多态性),EC50=6062nM。用人血清试验倍数变化,达到157倍。参见表6。Cmin靶向>20μg/mL*。>40%的进化枝B病人具有QVT多态性*。*参见McCallister等人的XVIIInternationalDrugResistanceWorkshop,June10-14,2008,Sitges,Spain.Conferenceposter"HIV-1GagPolymorphismsDetermineTreatmentResponsetoBevirimat(PA-457)"。报道了贝韦立马(Bevirimat)的上述HIV临床问题之后,发现了一些新的HIV活性成熟抑制剂化合物。例如,PCT公开的申请WO2011/100308和PCT申请系列PCT/CN2011/001302描述了某些成熟抑制剂化合物(下文称化合物“A”、“B”和“C”,如下所示)。此外,本申请也描述了化合物51和56,等等,如本文所详述。相对于PCT公开的申请WO2011/100308和PCT申请系列PCT/CN2011/001302所描述的化合物,本申请描述了新的化合物。此外,与PCT公开的申请WO2011/100308和PCT申请系列PCT/CN2011/001302所描述的化合物(“A”、“B”和“C”)相比,本文所描述的某些化合物显示出了意想不到的优良性能。两个参考文献所描述的化合物与本申请的化合物之间的一个差别是,两个参考文献中的化合物在其中的一个位置需要羰基,而本申请描述了在相同位置不能有羰基的化合物。例如,这种羰基相对于非羰基的差别用下面直接显示的箭头来加以强调。在本申请范围内,式(I)和(II)的通用结构证实了这种情况,因为当W是氧时,在相邻的碳和W之间只能是单键。总而言之,在W和它的相邻碳之间没有双键,结果,在本申请的化学式中不会形成羰基。实际上,现在发现,这种结构差别意想不到地提高了许多性能,这些性能涉及制备用于预防和/或治疗病毒病(例如HIV)的有效药物。本申请描述的某些化合物的一或多种这样的性能包括但不局限于:增加HIV病毒多态性覆盖范围、提高体外效能(EC50)、降低计划的临床人类AUC目标、通过降低所需要的有效剂量而潜在地降低任何毒性窗口、以及降低对计划的临床AUC目标时的蛋白结合和/或血清变换的影响。在下面实施例84-89中,更详细地描述本文所描述的某些化合物的这种对药物动力学和计划的临床用途的改善。化合物A:。化合物B:。化合物C:(PCT公开的申请WO/2011/10038的实施例17-19)。化合物51(本文中的实施例18)。化合物56(本文中的实施例19)。按照本发明的一个实施方案,提供了式I结构的化合物:或其可药用盐,其中:A是L1和L2独立地选自键或[C(R6R6')]q;Q在每种情况下独立地选自-CH2-或-C(=O)-;W选自键或O;R1选自-H、(C1-C12)烷基、-C(O)R5、-CH2-O-(C1-C6)烷基、2-四氢-2H-吡喃和R2选自-H、(C1-C12)烷基、-(C1-C6)烷基-OR4、-(C1-C6)烷基-O-(C1-C6)烷基、-C(O)R5、-(CH2)rNR7R8和-(CH2)rN+(R4)3,其中,当W是O时,R1和R2可以任选与它们分别连接的O和N一起形成4至8元杂环基环,其中该杂环基环可以任选被一个至两个R11基团取代;R3选自-H、(C1-C12)烷基、-NR1R2、-OR5、X是单环或双环(C5-C14)芳基,Y选自单环或双环(C2-C9)杂环基,或单环或双环(C2-C9)杂芳基,每个具有一个至三个选自S、N或O的杂原子,Z是单环或双环(C3-C8)环烷基;R2和R3可以任选与它们分别连接的氮和L2一起形成4至8元杂环基环,其中该杂环基环可以任选被一个至两个R11基团取代;R4选自-H和(C1-C6)烷基;R5选自-H、(C1-C6)烷基、-R3、-(CH2)rNR7R8和-(CH2)rOR7;R6和R6'独立地选自-H、(C1-C6)烷基、(C3-C8)环烷基、(C1-C6)烷氧基、卤代烷基、-Y、-(CH2)rNR7R8、-C(O)OH和-C(O)NH2,其中R6和R6'基团可以任选与它们连接的碳一起形成3至8元环烷基环,其中该环烷基环可以任选被一个至三个R11基团取代;R7和R8独立地选自-H、(C1-C6)烷基、(C3-C8)环烷基、-Q-芳基-(R4)n、-NR14R15、-C(O)CH3,其中R7和R8可以任选与它们连接的氮一起形成含有一个至三个选自下列杂原子的4至8元杂环基或杂芳基环:-NR5-、-O-、-S-、-S(O)-或-SO2-,其中该杂环基或杂芳基环可以任选被一个至三个R11基团取代;R9是卤素;R10是-N(R16)2;R11、R12和R13独立地选自氧代、羟基、卤素、(C1-C6)烷氧基、-R6(R9)q、-OR6(R9)q、硝基、-SO2R6、(C1-C6)烷基、-C(O)R10、-R4YR6、-CO(O)R4和-CO(O)R5,其中,任何两个R11、R12或R13基团可以任选连接形成3至8元环烷基、芳基、杂环基或杂芳基环,其中该杂环基或杂芳基环可以含有一个至三个选自下列的杂原子:-NR5-、-O-、-S-、-S(O)-或-SO2-,其中该环烷基、芳基、杂环基或杂芳基环可以任选被一个至三个R16基团取代;R14和R15独立地选自-H、(C1-C6)烷基、(C3-C8)环烷基、(C1-C6)烷氧基、-[C(R6)2]r-、-O[C(R6)2]r-、氧代、羟基、卤素、-C(O)R7、-R10和-CO(O)R2,其中R14和R15可以任选与它们连接的碳一起形成3至8元环烷基环,或含有一个至三个选自下列的杂原子的4至8元杂环基环:-NR5-、-O-、-S-、-S(O)-或-SO2-,其中该环烷基环或杂环基环可以任选被一个至三个R16基团取代;R16独立地选自-H、卤素、氧代、羟基、(C1-C6)烷基、(C1-C6)烷氧基、(C3-C8)环烷基、-R6(R9)q、-OR6(R9)q、-N(R4)2、-(CH2)r-杂环、-C(O)OH、-C(O)NH2、-R5(R9)q、-OR5(R9)q、硝基、-SO2R6、-C(O)R10和-CO(O)R4;m和n在每种情况下独立地是0、1、2、3或4;p独立地是0、1、2、3或4;r和q在每种情况下独立地是0、1、2、3或4。按照本发明的另一个实施方案,提供了式I结构的化合物:或其可药用盐,其中:A是L1和L2是[C(R6R6')]q;Q在每种情况下独立地选自-CH2-或-C(=O)-;W选自键或O;R1选自-H、(C1-C6)烷基、-C(O)R4和R2选自-H、(C1-C6)烷基、-(C1-C6)烷基-OR4、-(C1-C6)烷基-O-(C1-C6)烷基、-C(O)R5、-(CH2)rNR7R8和-(CH2)rN+(R4)3;R3选自氢、(C1-C12)烷基、-NR1R2、-OR5、X是单环或双环(C5-C14)芳基,Y选自单环或双环(C2-C9)杂环基,或单环或双环(C2-C9)杂芳基,每个具有一个至三个选自S、N或O的杂原子,Z是单环或双环(C3-C8)环烷基;R4选自-H和(C1-C6)烷基;R5选自(C1-C6)烷基、-(CH2)rNR7R8和-(CH2)rOR7;R6和R6'独立地选自-H、(C1-C6)烷基、(C3-C8)环烷基、(C1-C6)烷氧基、卤代烷基、-(CH2)rNR7R8、-C(O)OH和-C(O)NH2,其中R6和R6'基团可以任选与它们连接的碳一起形成3至8元环烷基环,其中该环烷基环可以任选被一个至三个R11基团取代;R7和R8独立地选自-H、(C1-C6)烷基、(C3-C8)环烷基、-NR14R15和-C(O)CH3;R9是卤素;R10是-N(R16)2;R11、R12和R13独立地选自氧代、羟基、卤素、(C1-C6)烷氧基、-R6(R9)q、-OR6(R9)q、硝基、-SO2R6、(C1-C6)烷基、-C(O)R10、-R4YR6、-CO(O)R4和-CO(O)R5;R14和R15独立地选自-H、(C1-C6)烷基、(C3-C8)环烷基、(C1-C6)烷氧基、-[C(R6)2]r-、-O[C(R6)2]r-、氧代、羟基、卤素、-C(O)R7、-R10和-CO(O)R2;R16独立地选自-H、氧代、卤素、羟基、(C1-C6)烷基、(C1-C6)烷氧基、(C3-C8)环烷基、-R6(R9)q、-OR6(R9)q、-N(R4)2、-(CH2)r-杂环、-C(O)OH、-C(O)NH2、-R5(R9)q、-OR5(R9)q、硝基、-SO2R6、-C(O)R10和-CO(O)R4;m和n在每种情况下独立地是0、1、2、3或4;p独立地是0、1、2、3或4;和r和q在每种情况下独立地是0、1、2、3或4。按照本发明的另一个实施方案,提供了式I结构的化合物:或其可药用盐,其中:A是L1和L2两个都是(-CH2-);Q是-C(=O)-;W是O;R1是-H;R2选自-H、(C1-C6)烷基、-(C1-C6)烷基-OR4、-(C1-C6)烷基-O-(C1-C6)烷基、-C(O)R5和-(CH2)rNR7R8;R3选自-H、(C1-C12)烷基、-NR1R2、-OR5、X是单环或双环(C5-C14)芳基,Y选自单环或双环(C2-C9)杂环基,或单环或双环(C2-C9)杂芳基,每个具有一个至三个选自S、N或O的杂原子,和Z是单环或双环(C3-C8)环烷基;R4选自-H和(C1-C6)烷基;R5选自(C1-C6)烷基、-(CH2)rNR7R8和-(CH2)rOR7;R6和R6'独立地选自-H、(C1-C6)烷基、(C3-C8)环烷基、(C1-C6)烷氧基、卤代烷基、-(CH2)rNR7R8、-C(O)OH和-C(O)NH2;R7和R8独立地选自-H、(C1-C6)烷基、(C3-C8)环烷基、-NR14R15和-C(O)CH3;R9是卤素;R10是-N(R16)2;R11、R12和R13独立地选自氧代、羟基、卤素、(C1-C6)烷氧基、-R6(R9)q、-OR6(R9)q、硝基、-SO2R6、(C1-C6)烷基、-C(O)R10、-R4YR6、-CO(O)R4和-CO(O)R5;R14和R15独立地选自-H、(C1-C6)烷基、(C3-C8)环烷基、(C1-C6)烷氧基、-[C(R6)2]r-、-O[C(R6)2]r-、氧代、羟基、卤素、-C(O)R7、-R10和-CO(O)R2;R16独立地选自-H、氧代、卤素、羟基、(C1-C6)烷基、(C1-C6)烷氧基、(C3-C8)环烷基、-R6(R9)q、-OR6(R9)q、-N(R4)2、-(CH2)r-杂环基、-C(O)OH、-C(O)NH2、-R5(R9)q、-OR5(R9)q、硝基、-SO2R6、-C(O)R10和-CO(O)R4;m和n在每种情况下独立地是0、1或2;p独立地是0、1或2;和r和q在每种情况下独立地是0、1、2或3。按照本发明的另一个实施方案,提供了式I结构的化合物:或其可药用盐,其中:A是L1和L2两个都是(-CH2-);Q是-C(=O)-;W是O;R1是-H;R2选自-H、(C1-C6)烷基、-C(O)R5和-(CH2)rNR7R8;R3是,其中X是单环或双环(C5-C14)芳基;R4选自-H和(C1-C6)烷基;R5选自(C1-C6)烷基、-(CH2)rNR7R8和-(CH2)rOR7;R6选自-H、(C1-C6)烷基、(C3-C8)环烷基、(C1-C6)烷氧基、卤代烷基、-(CH2)rNR7R8、-C(O)OH和-C(O)NH2;R7和R8独立地选自-H、(C1-C6)烷基、(C3-C8)环烷基、-NR14R15和-C(O)CH3;R9是卤素;R10是-N(R16)2;R11、R12和R13独立地选自氧代、羟基、卤素、(C1-C6)烷氧基、-R6(R9)q、-OR6(R9)q、硝基、-SO2R6、(C1-C6)烷基、-C(O)R10、-CO(O)R4和-CO(O)R5;R14和R15独立地选自-H、(C1-C6)烷基、(C3-C8)环烷基、(C1-C6)烷氧基、-[C(R6)2]r-、-O[C(R6)2]r-、氧代、羟基、卤素、-C(O)R7、-R10和-CO(O)R2;R16独立地选自-H、氧代、卤素、羟基、(C1-C6)烷基、(C1-C6)烷氧基、(C3-C8)环烷基、-R6(R9)q、-OR6(R9)q、-N(R4)2、-(CH2)r-杂环基、-C(O)OH、-C(O)NH2、-R5(R9)q、-OR5(R9)q、硝基、-SO2R6、-C(O)R10和-CO(O)R4;m和n在每种情况下独立地是0、1或2;p独立地是0、1或2;和r和q在每种情况下独立地是0、1、2或3。按照本发明的另一个实施方案,提供了式I结构的化合物:或其可药用盐,其中:A是L1和L2两个都是(-CH2-);Q是-C(=O)-;W是O;R是-H;R2是-(CH2)rNR7R8;R3是,其中X是苯基;R7和R8独立地选自-H和甲基;R9选自氯、溴和氟;R11选自氯、溴和氟;m是0、1或2;和r是1、2或3。按照本发明的另一个实施方案,提供了式II结构的化合物:或其可药用盐,其中:A是L1和L2独立地选自键或[C(R6R6')]q;Q在每个情况下独立地选自-CH2-或-C(=O)-;W选自键或O;R1选自-H、(C1-C12)烷基、-C(O)R5、-CH2-O-(C1-C6)烷基、2-四氢-2H-吡喃、和R2选自-H、(C1-C12)烷基、-(C1-C6)烷基-OR4、-(C1-C6)烷基-O-(C1-C6)烷基、-C(O)R5、-(CH2)rNR7R8和-(CH2)rN+(R4)3,其中,当W是O时,R1和R2可以任选与它们分别连接的O和N一起形成4至8元杂环基环,其中该杂环基环可以任选被一个至两个R11基团取代;R3选自氢、(C1-C12)烷基、-NR1R2、-OR5、X是单环或双环(C5-C14)芳基,Y选自单环或双环(C2-C9)杂环基,或单环或双环(C2-C9)杂芳基,每个具有一个至三个选自S、N或O的杂原子,和Z是单环或双环(C3-C8)环烷基;R2和R3可以任选与它们分别连接的氮和L2一起形成4至8元杂环基环,其中该杂环基环可以任选被一个至两个R11基团取代;R4选自-H和(C1-C6)烷基;R5选自-H、(C1-C6)烷基、-R3、-(CH2)rNR7R8和-(CH2)rOR7;R6和R6'独立地选自-H、(C1-C6)烷基、(C3-C8)环烷基、(C1-C6)烷氧基、卤代烷基、-Y、-(CH2)rNR7R8、-C(O)OH和-C(O)NH2,其中R6和R6'基团可以任选与它们连接的碳一起形成3至8元环烷基环,其中该环烷基环可以任选被一个至三个R11基团取代;R7和R8独立地选自-H、(C1-C6)烷基、(C3-C8)环烷基、-Q-芳基-(R4)n、-NR14R15、-C(O)CH3,其中R7和R8可以任选与它们连接的氮一起形成含有一个至三个选自下列杂原子的4至8元杂环基或杂芳基环:-NR5-、-O-、-S-、-S(O)-或-SO2-,其中该杂环基或杂芳基环可以任选被一个至三个R11基团取代;R9是卤素;R10是-N(R16)2;R11、R12和R13独立地选自氧代、羟基、卤素、(C1-C6)烷氧基、-R6(R9)q、-OR6(R9)q、硝基、-SO2R6、(C1-C6)烷基、-C(O)R10、-R4YR6、-CO(O)R4和-CO(O)R5,其中,任何两个R11、R12或R13基团可以任选连接形成3至8元环烷基、芳基、杂环基或杂芳基环,其中该杂环基或杂芳基环可以含有一个至三个选自下列的杂原子:-NR5-、-O-、-S-、-S(O)-或-SO2-,其中该环烷基、芳基、杂环基或杂芳基环可以任选被一个至三个R16基团取代;R14和R15独立地选自-H、(C1-C6)烷基、(C3-C8)环烷基、(C1-C6)烷氧基、-[C(R6)2]r-、-O[C(R6)2]r-、氧代、羟基、卤素、-C(O)R7、-R10和-CO(O)R2,其中R14和R15可以任选与它们连接的碳一起形成3至8元环烷基环,或含有一个至三个选自下列的杂原子的4至8元杂环基环:-NR5-、-O-、-S-、-S(O)-或-SO2-,其中该环烷基环或杂环基环可以任选被一个至三个R16基团取代;R16独立地选自-H、氧代、卤素、羟基、(C1-C6)烷基、(C1-C6)烷氧基、(C3-C8)环烷基、-R6(R9)q、-OR6(R9)q、-N(R4)2、-(CH2)r-杂环、-C(O)OH、-C(O)NH2、-R5(R9)q、-OR5(R9)q、硝基、-SO2R6、-C(O)R10和-CO(O)R4;m和n在每种情况下独立地是0、1、2、3或4;p独立地是0、1、2、3或4;和r和q在每种情况下独立地是0、1、2、3或4。按照本发明的另一个实施方案,提供了式II结构的化合物:或其可药用盐,其中:A是L1和L2是[C(R6R6')]q;Q在每种情况下独立地选自-CH2-或-C(=O)-;W选自键或O;R1选自-H、(C1-C6)烷基、-C(O)R4和R2选自-H、(C1-C6)烷基、-(C1-C6)烷基-OR4、-(C1-C6)烷基-O-(C1-C6)烷基、-C(O)R5、-(CH2)rNR7R8和-(CH2)rN+(R4)3;R3选自-H、(C1-C12)烷基、-NR1R2、-OR5、X是单环或双环(C5-C14)芳基,Y选自单环或双环(C2-C9)杂环基,或单环或双环(C2-C9)杂芳基,每个具有一个至三个选自S、N或O的杂原子,和Z是单环或双环(C3-C8)环烷基;R4选自-H和(C1-C6)烷基;R5选自(C1-C6)烷基、-(CH2)rNR7R8和-(CH2)rOR7;R6和R6'独立地选自-H、(C1-C6)烷基、(C3-C8)环烷基、(C1-C6)烷氧基、卤代烷基、-(CH2)rNR7R8、-C(O)OH和-C(O)NH2,其中R6和R6'基团可以任选与它们连接的碳一起形成3至8元环烷基环,其中该环烷基环可以任选被一个至三个R11基团取代;R7和R8独立地选自-H、(C1-C6)烷基、(C3-C8)环烷基、-NR14R15和-C(O)CH3;R9是卤素;R10是-N(R16)2;R11、R12和R13独立地选自氧代、羟基、卤素、(C1-C6)烷氧基、-R6(R9)q、-OR6(R9)q、硝基、-SO2R6、(C1-C6)烷基、-C(O)R10、-R4YR6、-CO(O)R4和-CO(O)R5;R14和R15独立地选自-H、(C1-C6)烷基、(C3-C8)环烷基、(C1-C6)烷氧基、-[C(R6)2]r-、-O[C(R6)2]r-、氧代、羟基、卤素、-C(O)R7、-R10和-CO(O)R2;R16独立地选自-H、氧代、卤素、羟基、(C1-C6)烷基、(C1-C6)烷氧基、(C3-C8)环烷基、-R6(R9)q、-OR6(R9)q、-N(R4)2、-(CH2)r-杂环、-C(O)OH、-C(O)NH2、-R5(R9)q、-OR5(R9)q、硝基、-SO2R6、-C(O)R10和-CO(O)R4;m和n在每种情况下独立地是0、1、2、3或4;p独立地是0、1、2、3或4;和r和q在每种情况下独立地是0、1、2、3或4。按照本发明的另一个实施方案,提供了式II结构的化合物:或其可药用盐,其中:A是L1和L2两个都是(-CH2-);Q是-C(=O)-;W是O;R1是-H;R2选自-H、(C1-C6)烷基、-C(O)R5和-(CH2)rNR7R8;R3是,其中X是单环或双环(C5-C14)芳基;R4选自-H和(C1-C6)烷基;R5选自(C1-C6)烷基、-(CH2)rNR7R8和-(CH2)rOR7;R6选自-H、(C1-C6)烷基、(C3-C8)环烷基、(C1-C6)烷氧基、卤代烷基、-(CH2)rNR7R8、-C(O)OH和-C(O)NH2;R7和R8独立地选自-H、(C1-C6)烷基、(C3-C8)环烷基、-NR14R15和-C(O)CH3;R9是卤素;R10是-N(R16)2;R11、R12和R13独立地选自氧代、羟基、卤素、(C1-C6)烷氧基、-R6(R9)q、-OR6(R9)q、硝基、-SO2R6、(C1-C6)烷基、-C(O)R10、-CO(O)R4和-CO(O)R5;R14和R15独立地选自-H、(C1-C6)烷基、(C3-C8)环烷基、(C1-C6)烷氧基、-[C(R6)2]r-、-O[C(R6)2]r-、氧代、羟基、卤素、-C(O)R7、-R10和-CO(O)R2;R16独立地选自-H、氧代、卤素、羟基、(C1-C6)烷基、(C1-C6)烷氧基、(C3-C8)环烷基、-R6(R9)q、-OR6(R9)q、-N(R4)2、-(CH2)r-杂环、-C(O)OH、-C(O)NH2、-R5(R9)q、-OR5(R9)q、硝基、-SO2R6、-C(O)R10和-CO(O)R4;m和n在每种情况下独立地是0、1或2;p独立地是0、1或2;和r和q在每种情况下独立地是0、1、2或3。按照本发明的另一个实施方案,提供了式II结构的化合物:或其可药用盐,其中:A是L1和L2两个都是(-CH2-);Q是-C(=O)-;W是O;R1是-H;R2是-(CH2)rNR7R8;R3是,其中X是苯基;R7和R8独立地选自-H和甲基;R9选自氯、溴和氟;R11选自氯、溴和氟;m是0、1或2;和r是1、2或3。按照本发明的另一个实施方案,提供了式II的化合物:或其可药用盐,其中:A是L1和L2独立地选自键或[C(R6R6)]q;Q选自-CH2-或-C(=O)-;W选自键或氧;R1选自-H、(C1-C12)烷基、-C(O)R5、-CH2-O-(C1-C6)烷基、2-四氢-2H-吡喃和R2选自-H、(C1-C12)烷基、-C1-6烷基-OH、-C1-6烷基-O-C1-6烷基、-C(O)R5和-(CH2)rNR7R8、-C(O)R5,其中,当W是氧时,R1和R2可以任选与它们各自连接的氧和氮一起形成4至8元杂环基环,其中该杂环基环可以任选被一个至两个R11基团取代;R3选自氢、(C1-C12)烷基、-NR1R2、-OR5、X是单环或双环(C5-C14)芳基,Y选自单环或双环(C2-C9)杂环基,或单环或双环(C2-C9)杂芳基,每个具有一个至三个选自S、N或O的杂原子,和Z是单环或双环(C3-C8)环烷基;R2和R3可以任选与它们分别连接的氮和L2一起形成4至8元杂环基环,其中该杂环基环可以任选被一个至两个R11基团取代;R4选自-H和(C1-C6)烷基;R5选自(C1-C6)烷基、-R3、-(CH2)rNR7R8或-(CH2)rOR7;R6和R6'独立地是-H、(C1-C6)烷基、(C3-C8)环烷基、(C1-C6)烷氧基、卤代烷基、-Y、-(CH2)rNR7R8、-C(O)OH、-C(O)NH2,其中,R6和R6'基团可以任选与它们连接的碳一起形成3至8元环烷基环,其中该环烷基环可以任选被一个至三个R11基团取代;R7和R8独立地选自-H、(C1-C6)烷基、(C3-C8)环烷基、-Q-芳基-(R4)n、-NR14R15、-C(O)CH3,其中R7和R8可以任选与它们连接的氮一起形成含有一个至三个选自下列杂原子的4至8元杂环基或杂芳基环:-NR5-、-O-、-S-、-S(O)-或-SO2-,其中该杂环基或杂芳基环可以任选被一个至三个R11基团取代;R9是卤素;R10是-N(R16)2;R11、R12和R13独立地选自氧代、羟基、卤素、(C1-C6)烷氧基、-R6(R9)q、-OR6(R9)q、硝基、-SO2R6、(C1-C6)烷基、-C(O)R10、-R4YR6和-CO(O)R5,其中,任何两个R9、R10或R11基团可以任选连接形成3至8元环烷基、芳基、杂环基或杂芳基环,其中该杂环基或杂芳基环可以含有一个至三个选自下列的杂原子:-NR5-、-O-、-S-、-S(O)-或-SO2-,其中该环烷基、芳基、杂环基或杂芳基环可以任选被一个至三个R16基团取代;R14和R15独立地选自-H、(C1-C6)烷基、(C3-C8)环烷基、(C1-C6)烷氧基、-[C(R6)2]r-、-O[C(R6)2]r-、氧代、羟基、卤素、-C(O)R7、-R10和-CO(O)R2,其中R14和R15可以任选与它们连接的碳一起形成3至8元环烷基环,或含有一个至三个选自下列的杂原子的4至8元杂环基环:-NR5-、-O-、-S-、-S(O)-或-SO2-,其中该环烷基环或杂环基环可以任选被一个至三个R16基团取代;R16独立地选自卤素、氧代、羟基、(C1-C6)烷基、(C1-C6)烷氧基、(C3-C8)环烷基、-R6(R9)q、-OR6(R9)q、-N(R4)2、-(CH2)r-杂环基、-C(O)OH、-C(O)NH2、-R5(R9)q、-OR5(R9)q、硝基、-SO2R6、-C(O)R10和-CO(O)R4;m和n在每种情况下独立地是0、1、2、3或4;p独立地是0、1、2、3或4;和r和q在每种情况下独立地是0、1、2、3或4。按照本发明的另一个实施方案,提供了具有上述式I或式II结构的化合物,其中L1和L2两个都是[C(R6R6')]q。按照本发明的另一个实施方案,提供了具有上述式I或式II结构的化合物,其中L1和L2两个都是-CH2-。按照本发明的另一个实施方案,提供了具有上述式I或式II结构的化合物,其中q独立地是1、2或3。按照本发明的另一个实施方案,提供了具有上述式I或式II结构的化合物,其中q是1。按照本发明的另一个实施方案,提供了具有上述式I或式II结构的化合物,其中W是O。按照本发明的另一个实施方案,提供了具有上述式I或式II结构的化合物,其中W是键。按照本发明的另一个实施方案,提供了具有上述式I或式II结构的化合物,其中,当W是键时,则R1是-H。按照本发明的另一个实施方案,提供了具有上述式I或式II结构的化合物,其中,当W是O时,则R1是-H。按照本发明的另一个实施方案,提供了具有上述式I或式II结构的化合物,其中,A基团中的Qm不存在,A基团中的Qn是-CH2-,式I结构中的Q是-C(=O)-。按照本发明的另一个实施方案,提供了具有上述式I或式II结构的化合物,其中R1是-H。按照本发明的另一个实施方案,提供了具有上述式I或式II结构的化合物,其中R2是-(CH2)rNR7R8。按照本发明的另一个实施方案,提供了具有上述式I或式II结构的化合物,其中R2是(二甲基氨基)乙基。按照本发明的另一个实施方案,提供了具有上述式I或式II结构的化合物,其中r独立地是0、1、2或3。按照本发明的另一个实施方案,提供了具有上述式I或式II结构的化合物,其中r是2。按照本发明的另一个实施方案,提供了具有上述式I或式II结构的化合物,其中R3是。按照本发明的另一个实施方案,提供了具有上述式I或式II结构的化合物,其中X是单环(C5-C14)芳基。按照本发明的另一个实施方案,提供了具有上述式I或式II结构的化合物,其中X是苯基。按照本发明的另一个实施方案,提供了具有上述式I或式II结构的化合物,其中R4是-H。按照本发明的另一个实施方案,提供了具有上述式I或式II结构的化合物,其中m是0或1。按照本发明的另一个实施方案,提供了具有上述式I或式II结构的化合物,其中m是0。按照本发明的另一个实施方案,提供了具有上述式I或式II结构的化合物,其中m是1。按照本发明的另一个实施方案,提供了具有上述式I或式II结构的化合物,其中n是1。按照本发明的另一个实施方案,提供了具有上述式I或式II结构的化合物,其中R6和R6'两个都是-H。按照本发明的另一个实施方案,提供了具有上述式I或式II结构的化合物,其中R7和R8两个都是(C1-C6)烷基。按照本发明的另一个实施方案,提供了具有上述式I或式II结构的化合物,其中R7是甲基。按照本发明的另一个实施方案,提供了具有上述式I或式II结构的化合物,其中R8是甲基。按照本发明的另一个实施方案,提供了具有上述式I或式II结构的化合物,其中R7和R8两个都是甲基。按照本发明的另一个实施方案,提供了具有上述式I或式II结构的化合物,其中R11是卤素。按照本发明的另一个实施方案,提供了具有上述式I或式II结构的化合物,其中R11选自氯、溴或氟。按照本发明的另一个实施方案,提供了具有上述式I或式II结构的化合物,其中R11是氯。按照本发明的另一个实施方案,提供了具有上述式I或式II结构的化合物,其中R11不存在。按照本发明的另一个实施方案,提供了具有上述式I或式II结构的化合物,其中R14和R15两个都是(C1-C6)烷基。按照本发明的另一个实施方案,提供了具有上述式I或式II结构的化合物,其中R14和R15两个都是甲基。按照本发明的另一个实施方案,提供了具有上述式I或式II结构的化合物,其中A是。按照本发明的另一个实施方案,提供了具有上述式I或式II结构的化合物,其中A是。按照本发明的另一个实施方案,提供了具有上述式I或式II结构的化合物,其中A是。按照本发明的另一个实施方案,提供了具有上述式I或式II结构的化合物,其中A是。按照本发明的另一个实施方案,提供了具有下列结构的化合物:或其可药用盐。按照本发明的另一个实施方案,提供了具有下列结构的化合物:,或其可药用盐。按照本发明的另一个实施方案,提供了具有下列结构的化合物:或其可药用盐。按照本发明的另一个实施方案,提供了具有下列结构的化合物:,或其可药用盐。在本发明的一个进一步的实施方案中,提供了含有式I或式II的化合物或其可药用盐以及药用赋形剂的药物组合物。在本发明的一个进一步实施方案中,提供了治疗HIV的方法,该方法包括:给予患有HIV的患者有效量的式I或式II的化合物或其可药用盐。在本发明的一个进一步的实施方案中,提供了含有式I或式II的化合物或其可药用盐以及药用赋形剂的药物组合物。在本发明的一个进一步的实施方案中,提供了含有式I或式II的化合物或其可药用盐以及药用赋形剂的药物组合物,其中该化合物以无定形形式存在。在本发明的一个进一步的实施方案中,提供了含有式I或式II的组合物或其可药用盐以及药用赋形剂的药物组合物,其中该组合物是片剂形式的组合物。在本发明的一个进一步的实施方案中,提供了含有式I或式II的化合物或其可药用盐以及药用赋形剂的药物组合物,其中该化合物以喷雾干燥的分散体形式存在。在本发明的一个进一步实施方案中,提供了治疗患者HIV感染的方法,该方法包括:给予所述患者式I或式II的化合物或其可药用盐。在某些实施方案中,患者是哺乳动物,在其它实施方案中,患者是人。在本发明的一个进一步实施方案中,提供了治疗患者HIV感染的方法,该方法包括:给予所述患者含有式I或式II的化合物或其可药用盐以及药用赋形剂的药物组合物。在本发明的一个进一步实施方案中,提供了预防处于形成HIV感染危险之中的患者感染HIV的方法,该方法包括:给予所述患者式I或式II的化合物或其可药用盐。在本发明的一个进一步实施方案中,提供了预防处于形成HIV感染危险之中的患者感染HIV的方法,该方法包括:给予所述患者含有式I或式II的化合物或其可药用盐以及药用赋形剂的药物组合物。在其它实施方案中,本发明还提供了式I或式II的任何一个所定义的化合物或盐在制备药物中的用途,这种药物用于治疗人的HIV感染。此外,本发明的化合物可以存在为具体的几何或立体异构形式。本发明包括所有这种化合物,包括顺式-和反式异构体、(-)-和(+)-对映体、(R)-和(S)-对映体、非对映体、(D)-异构体、(L)-异构体、其外消旋混合物以及它们的其它混合物,例如,在本发明范围内的对映体或非对映体富集的混合物。其它不对称碳原子可以存在于取代基中,例如,烷基。所有这种异构体以及其混合物包括在本发明范围内。光学活性的(R)-和(S)-异构体以及d和I异构体,可以使用手性合成单体或手性试剂来制备,或使用传统方法拆分。例如,如果需要本发明化合物的具体对映体,则可以通过不对称合成来制备,或通过手性助剂的衍生化来制备,其中,分离所得到的非对映体混合物,并将助剂基团裂解,提供纯的目标对映体。或者,在分子含有碱性官能团(例如氨基)或酸性官能团(例如羧基)的情况下,可以用合适的光学活性的酸或碱形成非对映体的盐,而后将由本领域已知的分级结晶或色谱方法形成的非对映体拆分,随后回收纯对映体。此外,通常使用色谱(使用手性固定相)来完成对映体和非对映体的分离,任选与化学衍生化组合进行(例如,由胺形成氨基甲酸酯)。在本发明的另一个实施方案中,提供了式I或式II的化合物,其中,该化合物或该化合物的盐用于制备药物,这种药物用于治疗人的病毒感染。在本发明的另一个实施方案中,提供了药物组合物,其含有药用稀释剂和治疗有效量的式I所定义的化合物。在一个实施方案中,含有式I或式II的化合物或其盐的药物制剂是适合于肠胃外给药的制剂。在另一个实施方案中,该制剂是长效的肠胃外制剂。在进一步实施方案中,该制剂是纳米颗粒制剂。本发明的化合物和它们的盐、溶剂化物或它们的其它药用衍生物,可以单独使用,或与其它治疗剂联用。因此,在其它实施方案中,治疗和/或预防患者HIV感染的方法,除了给予式I或式II的化合物之外,还可以进一步包括:给予一或多种有效抗HIV的其它药剂。在这种实施方案中,有效抗HIV的一或多种其它药剂选自:齐多夫定(zidovudine)、去羟肌苷(didanosine)、拉夫米定(lamivudine)、扎西他滨(zalcitabine)、阿巴卡韦(abacavir)、司他维丁(stavudine)、阿德福韦(adefovir)、阿德福韦酯(adefovirdipivoxil)、福齐夫定(fozivudine)、托德西(todoxil)、恩曲他滨(emtricitabine)、阿洛夫定(alovudine)、氨多索韦(amdoxovir)、艾夫他滨(elvucitabine)、内维拉平(nevirapine)、地拉韦啶(delavirdine)、依法韦恩茨(efavirenz)、洛韦胺(loviride)、怡妙康(immunocal)、奥替普拉(oltipraz)、卡普韦林(capravirine)、来司韦林(lersivirine)、GSK2248761、TMC-278、TMC-125、依曲韦林(etravirine)、沙奎那维(saquinavir)、利托那韦(ritonavir)、茚地那韦(indinavir)、奈非那韦(nelfinavir)、安普那韦(amprenavir)、佛萨普那韦(fosamprenavir)、贝卡那韦(brecanavir)、达芦那韦(darunavir)、阿扎那韦(atazanavir)、替拉那韦(tipranavir)、帕利那韦(palinavir)、拉西那韦(lasinavir)、恩夫韦地(enfuvirtide)、T-20、T-1249、PRO-542、PRO-140、TNX-355、BMS-806、BMS-663068和BMS-626529、5-Helix、雷特格韦(raltegravir)、埃替拉韦(elvitegravir)、GSK1349572、GSK1265744、vicriviroc(Sch-C)、Sch-D、TAK779、马拉维若(maraviroc)、TAK449、去羟肌苷(didanosine)、泰诺福韦(tenofovir)、洛匹那韦(lopinavir)和达芦那韦(darunavir)。因此,本发明的化合物和任何其它药学活性剂可以一起或单独给予,并且当单独给予时,可以以任何顺序同时或依次给予。为了达到目标组合的治疗效果,可以选择本发明化合物和其它药学活性剂的量与给药的相对时机。可以通过给予下列联用药形式,给予本发明化合物和其盐、溶剂化物或其它药用衍生物与其它治疗药剂的联用药:(1)包括两者化合物的单一药物组合物;或(2)各自包括所述化合物之一的独立药物组合物。或者,可以以顺序方式单独给予联用药,在这种方式中,首先给予一个治疗药剂,其次给予另一个治疗药剂,反之亦然。这种顺序给药可以在时间上是接近的,或在时间上间隔很长。为了获得目标组合治疗效果,可以选择式I或式II化合物或其盐和其它药学活性剂的数量与给药的相对时机。此外,本发明的化合物可以与一或多种预防或治疗HIV所使用的其它药剂联用。这种药剂的例子包括:核苷酸逆转录酶抑制剂,例如齐多夫定(zidovudine)、去羟肌苷(didanosine)、拉夫米定(lamivudine)、扎西他滨(zalcitabine)、阿巴卡韦(abacavir)、司他维丁(stavudine)、阿德福韦(adefovir)、阿德福韦酯(adefovirdipivoxil)、福齐夫定(fozivudine)、托德西(todoxil)、恩曲他滨(emtricitabine)、阿洛夫定(alovudine)、氨多索韦(amdoxovir)、艾夫他滨(elvucitabine)和类似的药剂;非核苷酸逆转录酶抑制剂(包括具有抗氧化活性的药剂,例如,怡妙康(immunocal)、奥替普拉(oltipraz),等等),例如内维拉平(nevirapine)、地拉韦啶(delavirdine)、依法韦恩茨(efavirenz)、洛韦胺(loviride)、怡妙康(immunocal)、奥替普拉(oltipraz)、卡普韦林(capravirine)、来司韦林(lersivirine)、GSK2248761、TMC-278、TMC-125、依曲韦林(etravirine)和类似的药剂;蛋白酶抑制剂,例如沙奎那维(saquinavir)、利托那韦(ritonavir)、茚地那韦(indinavir)、奈非那韦(nelfinavir)、安普那韦(amprenavir)、佛萨普那韦(fosamprenavir)、贝卡那韦(brecanavir)、达芦那韦(darunavir)、阿扎那韦(atazanavir)、替拉那韦(tipranavir)、帕利那韦(palinavir)、拉西那韦(lasinavir)和类似的药剂;进入、附着和融合抑制剂,例如,恩夫韦地(enfuvirtide)(T-20)、T-1249、PRO-542、PRO-140、TNX-355、BMS-806、BMS-663068和BMS-626529、5-Helix和类似的药剂;整合酶抑制剂,例如雷特格韦(raltegravir)、埃替拉韦(elvitegravir)、GSK1349572、GSK1265744和类似的药剂;成熟抑制剂,例如PA-344和PA-457,以及类似的药剂;和CXCR4和/或CCR5抑制剂,例如,维克雷罗(vicriviroc)(Sch-C)、Sch-D、TAK779、马拉维若(maraviroc)(UK427,857)、TAK449,以及公开在WO02/74769、PCT/US03/39644、PCT/US03/39975、PCT/US03/39619、PCT/US03/39618、PCT/US03/39740和PCT/US03/39732中的那些抑制剂和类似的药剂。本发明的化合物与一或多种预防或治疗HIV所使用的其它药剂联用的其它实施例可以在表1中得到。本发明化合物与HIV药剂的联用药的范围不局限于上述那些联用药,但原则上包括与治疗HIV所使用的任何药物组合物的任何联用药。正如所注释的那样,在这种联用药中,可以单独或结合给予本发明化合物和其它HIV药剂。此外,可以在给予其它药剂之前、与其同时或在其之后给予一种药剂。本发明还可以与一或多种用作药理学增强剂的药剂联用,并且与预防或治疗HIV的其它化合物联用或不与其联用。这种药理学增强剂(或药代动力学促进剂)的例子包括但不局限于:利托那韦、GS-9350和SPI-452。利托那韦是10-羟基-2-甲基-5-(1-甲基乙基)-1-1[2-(1-甲基乙基)-4-噻唑基]-3,6-二氧代-8,11-二(苯基甲基)-2,4,7,12-四氮杂十三烷-13-酸,5-噻唑基甲基酯,[5S-(5S*,8R*,10R*,11R*)],可以从AbbottLaboratoriesofAbbottpark(Illinois)以Norvir名称获得。利托那韦是用其它抗逆转录病毒药剂表示的HIV蛋白酶抑制剂,用于治疗HIV感染。利托那韦还抑制P450介导的药物代谢以及P-糖蛋白(Pgp)细胞传送系统,由此引起有机体内的活性化合物的浓度提高。GS-9350是GileadSciencesofFosterCityCalifornia作为药理学增强剂开发的化合物。SPI-452是SequoiaPharmaceuticalsofGaithersburg,Maryland作为药理学增强剂开发的化合物。在本发明的一个实施方案中,式I或式II的化合物与利托那韦联用。在一个实施方案中,该联用药是口服固定剂量的联用药。在另一个实施方案中,将式I或式II的化合物配制为长效肠胃外针剂,将利托那韦配制为口服组合物。在一个实施方案中,提供了试剂盒,其含有配制为长效肠胃外针剂的式I或式II的化合物以及配制为口服组合物的利托那韦。在另一个实施方案中,将式I或式II的化合物配制为长效肠胃外针剂,将利托那韦配制为注射组合物。在一个实施方案中,提供了试剂盒,其含有配制为长效肠胃外针剂的式I或式II的化合物以及配制为注射组合物的利托那韦。在本发明的另一个实施方案中,式I或式II的化合物与GS-9350联用。在一个实施方案中,该联用药是口服固定剂量的联用药。在另一个实施方案中,将式I或式II的化合物配制为长效肠胃外针剂,将GS-9350配制为口服组合物。在一个实施方案中,提供了试剂盒,其含有配制为长效肠胃外针剂的式I或式II的化合物以及配制为口服组合物的GS-9350。在另一个实施方案中,将式I或式II的化合物配制为长效肠胃外针剂,将GS-9350配制为注射组合物。在一个实施方案中,提供了试剂盒,其含有配制为长效肠胃外针剂的式I或式II的化合物以及配制为注射组合物的GS-9350。在本发明的一个实施方案中,式I或式II的化合物与SPI-452联用。在一个实施方案中,该联用药是口服固定剂量的联用药。在另一个实施方案中,将式I或式II的化合物配制为长效肠胃外针剂,将SPI-452配制为口服组合物。在一个实施方案中,提供了试剂盒,其含有配制为长效肠胃外针剂的式I或式II的化合物以及配制为口服组合物的SPI-452。在另一个实施方案中,将式I或式II的化合物配制为长效肠胃外针剂,将SPI-452配制为注射组合物。在一个实施方案中,提供了试剂盒,其含有配制为长效肠胃外针剂的式I或式II的化合物以及配制为注射组合物的SPI-452。在本发明的一个实施方案中,式I或式II的化合物与先前申请的PCT/CN2011/0013021(本文以引证的方式结合)中得到的化合物联用。当上述其它治疗剂与本文所描述的化学实体联用时,这些其它治疗剂可以使用例如医师桌上手册(PDR)中所标明的那些数量,或本领域普通技术人员另外确定的数量。在本发明的另一个实施方案中,提供了治疗哺乳动物的至少部分地由病毒的逆转录病毒家族中的病毒所介导的病毒感染的方法,该方法包括:给予已经确诊患有所述病毒感染或处于形成所述病毒感染危险之中的哺乳动物式I或式II的化合物。在本发明的另一个实施方案中,提供了治疗哺乳动物的至少部分地由病毒的逆转录病毒家族中的病毒所介导的病毒感染的方法,该方法包括:给予已经确诊患有所述病毒感染或处于形成所述病毒感染危险之中的哺乳动物式I或式II的化合物,其中所述病毒是HIV病毒。在一些实施方案中,HIV病毒是HIV-1病毒。在本发明的另一个实施方案中,提供了治疗哺乳动物的至少部分地由病毒的逆转录病毒家族中的病毒所介导的病毒感染的方法,该方法包括:给予已经确诊患有所述病毒感染或处于形成所述病毒感染危险之中的哺乳动物式I或式II的化合物,该方法进一步包括:给予治疗有效量的有效抗HIV病毒的一或多种药剂。在本发明的另一个实施方案中,提供了治疗哺乳动物的至少部分地由病毒的逆转录病毒家族中的病毒所介导的病毒感染的方法,该方法包括:给予已经确诊患有所述病毒感染或处于形成所述病毒感染危险之中的哺乳动物式I或式II的化合物,该方法进一步包括:给予治疗有效量的有效抗HIV病毒的一或多种药剂,其中所述有效抗HIV病毒的药剂选自:核苷酸逆转录酶抑制剂;非核苷酸逆转录酶抑制剂;蛋白酶抑制剂;进入、附着和融合抑制剂;整合酶抑制剂;成熟抑制剂;CXCR4抑制剂;和CCR5抑制剂。在进一步的实施方案中,本发明的化合物或其可药用盐选自表2中列出的化合物。表2的化合物按照如下所述的合成方法、通用反应路线和实施例来合成。在某些实施方案中,本发明的化合物或其可药用盐选自表2中列出的化合物。合成方法对于所提供的化学实体的合成方法,可以使用容易获得的起始原料、使用下列通用方法和工艺制备。应理解,在给予典型的或优选的工艺条件(即,反应温度、时间、反应物的摩尔比、溶剂、压力,等等)时,还可以使用其它工艺条件,除非另有说明。最佳反应条件可以随或所使用的具体反应物溶剂而变化,但这种条件可以由本领域技术人员通过常规优化过程来确定。另外,本发明方法可能使用保护基,以防止某些官能团进行不希望有的反应。各种官能团的合适保护基以及保护和去保护具体官能团的适宜条件在本领域是众所周知的。例如,许多保护基描述在下列文献中:T.W.GreeneandG.M.Wuts,ProtectingGroupsinOrganicSynthesis,ThirdEdition,Wiley,NewYork,1999,以及其中引用的参考文献。此外,提供的化学实体可能含有一个或多个手性中心,而这样的化合物可以以纯立体异构体的形式制备或分离,即以单一对映体或非对映体,或立体异构体富集的混合物。所有这种立体异构体(和富集的混合物)都包括在本说明书的范围内,除非另有陈述。可以使用例如本领域众所周知的光学活性的起始原料或立体选择性试剂来制备纯立体异构体(或富集的混合物)。或者,可以使用例如手性柱色谱、手性拆解试剂等等来分离这种化合物的外消旋混合物。下列反应的起始原料是通常已知的化合物或可以由已知的方法或其明显的改良法制备。例如,可以从商品供应商获得许多起始原料,例如AldrichChemicalCo.(Milwaukee,Wisconsin,USA)、Bachem(Torrance,California,USA)、Ernka-Chemce或Sigma(St.Louis,Missouri,USA)。其它的可以通过标准参考文献中所描述的方法或其明显的改良法制备,例如,FieserandFieser'sReagentsforOrganicSynthesis,Volumes1-15(JohnWileyandSons,1991)、Rodd'sChemistryofCarbonCompounds,Volumes1-5andSupplemental(ElsevierSciencePublishers,1989)、OrganicReactions,Volumes1-40(JohnWileyandSons,1991)、March'sAdvancedOrganicChemistry(JohnWileyandSons,4thEdition)和Larock'sComprehensiveOrganicTransformations(VCHPublishersInc.,1989)。除非有相反的规定,否则,本文所描述的反应是在常压、通常在-78℃至200℃之内的温度范围进行的。进一步的,除在实施例中使用的或除非另有说明的之外,反应时间和条件都是近似的,例如在大约常压、在大约-78℃至大约110℃的温度范围内、在大约1至大约24小时期间内进行;过夜操作的反应平均时间在大约16小时。该术语“溶剂”、“有机溶剂”和“惰性溶剂”分别指在相关联地描述的反应条件下是惰性的溶剂,包括,例如苯、甲苯、乙腈、四氢呋喃基(“THF”)、二甲基甲酰胺(“DMF”)、氯仿、二氯甲烷(或二氯甲烷)、乙醚、甲醇、N-甲基吡咯烷酮(“NMP”)、吡啶等等。如果需要的话,可以通过任何合适的分离或纯化方法进行本文所描述的化学实体和中间体的分离和纯化例如,通过过滤、提取、结晶、柱色谱、薄层色谱法或厚层色谱法、或这些方法的组合进行。合适的分离(separation)和离析(isolation)方法的具体实例可以参考本文下面的实施例。然而,还可以使用其它等效的分离或离析方法。当需要时,可以通过本领域技术人员已知的方法拆分(R)-和(S)-异构体,例如通过:形成非对映异构体的盐或配合物,其可以例如通过结晶分离;借助于形成非对映异构体的衍生物,其可以例如通过结晶、气体-液体或液相色谱分离;通过一个对映异构体与对映异构体-特异性的试剂的选择性反应,例如酶致氧化或还原,而后分离修饰和未修饰的对映异构体;或处于手性环境的气-液或液相色谱,例如,在手性载体上,例如,与手性配体键合的硅胶或在手性溶剂的存在下。或者,可以使用光学活性的试剂、底物、催化剂或溶剂,通过不对称合成来合成特定对映体,或利用非对称转化将一个对映体转化为另一个对映体。实施例下列实施例用来更充分地描述制备和使用上述发明的方式。应当理解,这些实施例决不用来限制本发明的真正的范围,而是为说明性的目的给出的。在下面的实施例和以上的合成反应路线中,下列缩写具有下列含义。如果没有定义缩写,它具有其公认的含义。aq.=含水的μL=微升μM=微摩尔浓度NMR=核磁共振boc=叔丁氧羰基br=宽峰Cbz=苄氧羰基d=双峰δ=化学位移C=摄氏度DCM=二氯甲烷dd=双二重峰DMEM=Dulbeco改良的Eagle's培养基DMF=N,N-二甲基甲酰胺DMSO=二甲亚砜EtOAc=乙酸乙酯g=克h或hr=小时HCV=丙型肝炎病毒HPLC=高效液相色谱Hz=赫兹IU=国际单位IC50=50%抑制时的抑制浓度J=偶合常数(以Hz给出,除非另外指明)m=多重峰M=摩尔浓度M+H+=母体质谱峰加H+mg=毫克min=分钟mL=毫升mM=毫摩尔浓度mmol=毫摩尔MS=质谱nm=纳摩尔ppm=百万分之一q.s.=足够量s=单峰RT=室温sat.=饱和t=三重峰TFA=三氟乙酸。设备说明书1HNMR谱记录在BrukerAvance-lll400光谱仪上。用百万分之一(ppm,δ单位)表示化学位移。偶合常数的单位是赫兹(Hz)。分裂模式描述表观多重性,并且指定为:s(单峰)、d(双峰)、t(三重峰)、q(四重峰)、quint(五重峰)、m(多重峰)、br(宽峰)。分析型低分辨率质谱(MS)记录在Agilent1200HPLC/6110或Agilent1200HPLC/6130上,使用SunFireC18,4.6x50mm,3.5μm,使用梯度洗脱方法。溶剂A:0.01%三氟乙酸(TFA)/水;溶剂B:0.01%TFA/乙腈;A保持1.2分钟,而后5%-95%或20%-95%B,经过4分钟。反应路线和试验方法下列反应路线和方法举例说明了如何制备本发明的化合物。所提到的具体溶剂和反应条件也是说明性的,不具有限制性。未描述的化合物是商购的化合物,或本领域技术人员使用可获得的起始原料容易制备的化合物。本文公开的实施例的目的只是为了说明,并不限制本发明的范围。使用本文公开的试验,所有实施例显示的LHIVIC50值在1μΜ和1nM之间。对于几个实施例而言,当C28二级醇存在时,其立体化学并没有对其绝对构型来确切地证实。除非另有说明,否则,将本申请列举的化合物分离为光学纯的立体异构体,并且最初指定为所绘制的构型。可能有一些立体异构体可以在单一C28位置以相反的立体化学形式列出(如所示)。这决不限制本发明的范围或式I化合物的应用性。利用本领域技术人员熟知的光谱方法,包括但不限于1D和2DNMR方法、振动圆二色性和X-射线晶体衍射,测定所包括的其它实施例,具有所示的构型。制备两种非对映体的这些实施例和方法,应该用来清楚地举例说明在C28位置的两种R和S构型的纯立体异构体容易获得、分离和鉴定,并且任何仍然未定义的实施例可以容易地用本领域技术人员熟知的类似方法来证实。醛中间体6的合成。步骤A:中间体2乙酸((1R,3aS,5aR,5bR,7aR,9S,11aR,11bR,13aR,13bR)-9-乙酰氧基-5a,5b,8,8,11a-五甲基-1-(丙-1-烯-2-基)二十氢-1H-环戊二烯并[a]-3a-基)甲酯。在室温下,向中间体1(20g,45.2mmol)、4-二甲基氨基吡啶(DMAP,1.66g,13.6mmol)和Et3N(63mL,136mmol)的CH2Cl2(DCM,100mL)溶液中加入乙酸酐(Ac2O,17.1mL,113mmol)。回流加热过夜之后,冷却至室温,用水(50mL)淬灭该反应。然后,用水(50mLx2)洗涤有机相,并用硫酸钠干燥。减压除去大部分有机溶剂之后,加入无水乙醇(50mL),并过滤收集所得到的沉淀白色固体(中间体2,20g,84%)。1HNMR(400MHz,CDCl3)δppm4.69(1H,m),4.59(1H,m),4.51-4.43(1H,m),4.25(1H,d,J=11.2Hz),3.85(1H,d,J=10.8Hz),2.49-2.40(1H,m),2.07(3H,s),2.04(3H,s),1.98-0.77(42H,m)。LC/MS:m/z计算值:526.4,实测值:527.7(M+1)+。步骤B:中间体3乙酸((3aS,5aR,5bR,7aR,9S,11aR,11bR,13aS)-9-乙酰氧基-1-异丙基-5a,5b,8,8,11a-五甲基-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-3a-基)甲酯。将HBr/乙酸(40mL,33%)加入到预先在105℃加热的中间体2(20g,38mmol)的甲苯(40mL)、Ac2O(40mL)和乙酸(AcOH,40mL)的悬浮液中。搅拌该反应混合物,并在此温度下加热1.5小时。冷却后,加入乙酸钠(24g),并将所得到的反应混合物蒸干。将淡褐色的残余物接纳在DCM(200mL)中,用水(100mLx3)洗涤有机相,用硫酸钠干燥,减压蒸干,提供残余物,然后,将残余物用乙醇(EtOH,95%)和DCM重结晶,得到中间体3(13.8g,69%)白色固体。1HNMR(400MHz,CDCl3)δppm4.50-4.46(1H,m),4.02(1H,d,J=10.8Hz),3.98(1H,d,J=10.8Hz),3.18-3.10(1H,m),2.43-2.40(1H,m),2.26-2.22(2H,m),2.04(3H,s),2.05(3H,s),2.00-1.95(1H,m),1.90-1.85(1H,m),1.77-0.83(39H,m)。LC/MS:m/z计算值:526.4,实测值:549.2(M+Na)+。步骤C:中间体4乙酸((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-9-乙酰氧基-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-3a-基)甲酯。将中间体3(7g,13.29mmol)、乙酸钠(NaOAc,6.21g,76mmol)和重铬酸钠二水合物(4.75g,15.95mmol)的混合物在无水甲苯(90mL)、AcOH(119mL)和Ac2O(29mL)中、在60℃搅拌过夜。冷却后,在水(150mL)和乙酸乙酯(EtOAc,250mL)之间分配该反应混合物。依次用水(100mL)、饱和碳酸钠溶液(100mLx2)和盐水(100mLx2)洗涤有机相,然后用硫酸钠干燥,减压浓缩,得到粘稠的油。将该粘稠的油与MeOH(mL)一起研磨,收集沉淀,得到中间体4(6g,11.1mmol,83%)白色固体。1HNMR(400MHz,CDCl3)δppm4.52-4.46(1H,m),4.33(1H,d,J=10.8Hz),4.06(1H,d,J=11.2Hz),3.21-3.16(1H,m),2.86(1H,dd,J=12.8,3.2Hz),2.42-2.36(1H,m),2.05(3H,s),2.00(3H,s),1.94-0.84(40H,m)。LC/MS:m/z计算值:540.4,实测值:563.3(M+Na)+。步骤D:中间体5乙酸(3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(羟甲基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基酯。将中间体4(7g,12.94mmol)和氢氧化钾(KOH,0.872g,15.5mmol)的混合物在EtOH(200mL)和甲苯(200mL)中、在室温下强力搅拌1小时。用HCl水溶液(1N)将该反应混合物中和至pH7,并蒸干。将获得的残余物接纳在水和少量丙酮中。收集沉淀,而后用水洗涤,真空干燥,获得中间体5(6.0g,93%)白色固体。LC/MS:m/z计算值:498.4,实测值:499.3(M+1)+。步骤E:中间体6乙酸(3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-甲酰基-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基酯。在室温下,向中间体5(5.1g,10.23mmol)的DCM(300mL)溶液中加入氯铬酸吡啶(PCC,6.61g,30.7mmol)和硅胶(6.6g)。将该反应混合物在室温下搅拌1小时。用水淬灭该反应之后,用饱和碳酸氢钠溶液(100mL)洗涤有机相,用硫酸钠干燥,减压蒸发,提供粗品,将其用硅胶柱色谱纯化(EtOAc:PE=1:10至1:5),提供中间体6(4.2g,83%)白色固体。LC/MS:m/z计算值:496.4,实测值:497.2(M+1)+。按照下列方法,合成氧代-丁酸酯中间体10。步骤A:中间体84-乙氧基-2,2-二甲基-4-氧代丁酸。将3,3-二甲基-二氢呋喃-2,5-二酮7(25g,195mmol)的无水EtOH(150mL)溶液在50℃搅拌过夜。冷却至室温后,用旋转蒸发器减压除去溶剂,并在-50℃将残余物与己烷一起研磨,得到中间体8(25g,133mmol,67.9%)白色固体。1HNMR(400MHz,CDCl3)δppm4.13-4.18(2H,q,J=7.2Hz),2.62(2H,s),1.28(6H,s),1.32-1.25(3H,t,J=7.6Hz)。LC/MS:m/z计算值:174.1,实测值:173.1(M-1)-。步骤B:中间体92,2-二甲基琥珀酸1-叔丁基4-乙基酯。向中间体8(20g,109mmol)、硫酸镁(52.5g,436mmol)和叔丁醇(60mL)的DCM(480mL)混合物中加入硫酸(8.72mL,164mmol)。在室温下搅拌过夜之后,将该反应混合物倒入饱和碳酸氢钠溶液(300mL)和水(300mL)中。加入DCM,提取目标产物,并将有机相用盐水洗涤,干燥,浓缩,得到中间体9(19g,83mmol,80%)无色油。1HNMR(400MHz,CDCl3)δppm4.02-4.08(2H,q,J=7.2Hz),2.46(2H,s),1.07(9H,s),1.14-1.20(9H,m)。LC/MS:m/z计算值:230.2,实测值:253.1(M+Na)+。步骤C:中间体104-(叔丁氧基)-3,3-二甲基-4-氧代丁酸。在室温下,向中间体9(10g,41.3mmol)的EtOH(200mL)溶液中加入氢氧化钾(12.86g,206mmol)/水(100mL)。将该反应混合物在室温下搅拌2小时。用1NHCl将反应混合物的pH值调节至3-4。将得到的溶液用醚(300mL)提取,并将乙醚相干燥,浓缩,得到粗品,在-10℃,将粗品用己烷再结晶,得到中间体10(4g,19.78mmol,47.9%)白色固体。1HNMR(400MHz,CDCl3)δppm2.58(2H,s),1.43(9H,s),1.25(6H,s)。LC/MS:m/z计算值:202.1,实测值:201.1(M-1)-。合成非对映中间体18和19。步骤A:中间体11乙酸(3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(1-羟基-2-硝基乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基酯。在室温下,向搅拌的乙酸(3b)-21,28-二氧代羽扇-18-烯-3-基酯(6)(25g,50.3mmol)和硝基甲烷(150mL,2782mmol)的混合物中一次性加入三乙胺(75mL,538mmol)。将该反应混合物在室温下搅拌过夜。浓缩该反应混合物,用石油醚/EtOAc(2:1,100mL)洗涤,得到产物(24g,43.0mmol,产率85%)白色固体。LC/MS:m/z计算值:557.4,实测值:558.2(M+1)+。步骤B:中间体12乙酸(3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-氨基-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基酯。在-5℃,向11(15.0g,26.9mmol)的甲醇(300mL)溶液中加入NiCl2.6H2O(9.59g,40.3mmol),并在5-10℃(内部温度)慢慢地加入硼氢化钠(10.17g,269mmol)。将该反应混合物在-5℃(浴温)搅拌30分钟。然后用饱和NH4Cl(200mL)淬灭该混合物,用EtOAc(1500mL)稀释,然后在室温下搅拌过夜。用饱和NH4Cl(50mL)、水(800mL)、盐水(800mL)洗涤有机层,用MgSO4干燥,过滤,浓缩,得到固体,将固体用石油醚洗涤,得到12(14g,24.40mmol,91%产率)白色固体。LC/MS:m/z计算值:527.4,实测值:528.3(M+1)+。步骤C:中间体13乙酸(3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-((叔丁氧羰基)(4-氯苄基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基酯。在室温下,向搅拌的12(8g,14.58mmol)、三乙胺(0.813mL,5.83mmol)和MgSO4(2.63g,21.87mmol)的甲醇(225mL)溶液中加入4-氯苯甲醛(2.056mL,17.50mmol)。将该反应混合物在室温下搅拌2小时,然后冷却至-5℃,在10分钟期间内,以小份形式加入NaBH4,并搅拌30分钟。随后,加入Boc2O(4.06mL,17.50mmol)。将该反应升温至室温,并搅拌1小时。将该反应混合物倒入冰水(300mL)中,收集固体,干燥,得到13(7g,8.56mmol,产率58.7%)白色泡沫体。LC/MS:m/z计算值:751.5,实测值:774.3(M+Na)+。步骤D:中间体14乙酸(3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-((叔丁氧羰基)(4-氯苄基)氨基)乙酰基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基酯。向13(25g,29.9mmol)在二氯甲烷(200mL)中的混合物中加入PCC(50g,232mmol)和50g硅胶。将该混合物在室温下搅拌过夜。过滤除去固体,获得黑色溶液,将其浓缩,并用硅胶柱色谱纯化,用hex:EtOAc(10:1)洗脱,得到14(20g,23.99mmol,80%产率)白色固体。LC/MS:m/z计算值:749.4,实测值:772.2(M+Na)+。步骤E:中间体15(3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-((4-氯苄基)氨基)乙酰基)-9-羟基-1-异丙基-5a,5b,8,8,11a-五甲基-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-2-酮。在室温下,向搅拌的14的1,4-二噁烷(200mL)和甲醇(200mL)溶液中一次性加入浓HCl(100mL)。将该反应混合物在45℃搅拌过夜。浓缩该反应混合物,用丙酮洗涤,得到15(12.5g,17.45mmol,87%产率)白色泡沫体。LC/MS:m/z计算值:607.38,实测值:608.0(M+1)+。步骤F:中间体164-氯苄基(2-((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-9-羟基-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-3a-基)-2-氧代乙基)氨基甲酸叔丁基酯。在室温下,向搅拌的15(6g,9.86mmol)和Et3N(5.50mL,39.5mmol)的二氯甲烷(30mL)溶液中一次性加入Boc2O(2.290mL,9.86mmol)。将该反应混合物在室温下搅拌2小时。由TLC可知,反应完成。真空除去溶剂。粗品16(6g,8.47mmol,86%产率)不用进一步纯化就使用。步骤G:中间体172,2-二甲基琥珀酸4-((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-((叔丁氧羰基)(4-氯苄基)氨基)乙酰基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)1-叔丁基酯。在室温下,向搅拌的10(5.14g,25.4mmol)、DMAP(5.17g,42.3mmol)和16(6g,8.47mmol)的二氯甲烷(50mL)溶液中加入EDC(8.12g,42.3mmol)。将该反应混合物在室温下搅拌,直到用TLC监测起始原料消失为止。反应完成之后,用CH2Cl2稀释该混合物,并用NH4Cl水溶液洗涤。用Na2SO4干燥有机层,并真空除去溶剂。用硅胶色谱纯化该物质(hex:EtOAc,12:1至5:1),得到17(5.4g,6.05mmol,71.4%产率)亮白色固体。质子NMR由旋转异构体的混合物组成。1HNMR(400MHz,氯仿-d)δ7.34-7.24(m,2H),7.23-7.08(m,2H),4.63-4.29(m,3H),4.11-3.39(m,2H),3.28-3.06(m,1H),2.69-0.69(m,68H)。步骤H:中间体18和192,2-二甲基琥珀酸4-((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-(叔丁氧羰基)(4-氯苄基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)1-叔丁基酯(18)和2,2-二甲基琥珀酸4-((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-2-((叔丁氧羰基)(4-氯苄基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)1-叔丁基酯(19)。在0℃,向搅拌的17(1.5g,1.680mmol)的甲醇(10mL)和THF(10.00mL)溶液中加入NaBH4(0.127g,3.36mmol)。将该反应混合物在0℃下搅拌,直到用TLC监测起始原料消失为止(大约2小时)。完成后,用水稀释该混合物,用EtOAc提取,并用Na2SO4干燥有机层。用硅胶色谱纯化残余物(hex:EtOAc,7:1至5:1),得到S构型的非对映体2,2-二甲基琥珀酸4-((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-2-((叔丁氧羰基)(4-氯苄基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)1-叔丁基酯(18)(700mg,0.782mmol,46.6%产率)和R构型的非对映体2,2-二甲基琥珀酸4-((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-((叔丁氧羰基)(4-氯苄基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)1-叔丁基酯(19)(500mg,0.559mmol,33.3%产率),均为亮白色固体。对于18:1HNMR(400MHz,氯仿-d)δ7.40-7.24(m,2H),7.18(d,J=8.3Hz,2H),4.87-4.57(m,1H),4.51(dd,J=5.3,11.0Hz,1H),4.42-4.13(m,2H),3.43-3.05(m,3H),2.97-2.78(m,1H),2.62-2.47(m,2H),2.47-2.29(m,1H),2.01-0.70(m,64H);LC/MS:m/z计算值:893.6,实测值:916.5(M+Na)+。对于19:1HNMR(400MHz,氯仿-d)δ7.36-7.23(m,2H),7.12(d,J=8.3Hz,2H),4.56-4.14(m,4H),3.45-3.18(m,1H),3.15-2.97(m,1H),2.76-0.71(m,69H);LC/MS:m/z计算值:893.6,实测值:916.7(M+Na)+。实施例1:化合物214-((R)-1-((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-9-((3-羧基-3-甲基丁酰基)氧基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-3a-基)-2-((4-氯苄基)氨基)乙氧基)-2,2-二甲基-4-氧代丁酸。步骤A:中间体202,2-二甲基琥珀酸4-((R)-1-((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-9-((4-(叔丁氧基)-3,3-二甲基-4-氧代丁酰基)氧基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-3a-基)-2-((叔丁氧羰基)(4-氯苄基)氨基)乙基)1-叔丁基酯。在室温下,向搅拌的10(543mg,2.68mmol)、DMAP(205mg,1.677mmol)的二氯甲烷(5mL)溶液中加入EDC(514mg,2.68mmol)。将该反应混合物在室温下搅拌1小时。然后将19(300mg,0.335mmol)加入到该反应混合物中。完成后,用2MHCl、水和盐水洗涤该混合物。用Na2SO4干燥有机层,浓缩,得到粗品20(400mg,0.278mmol,83%产率)油。该物质不用进一步纯化就在下一步中使用。步骤B:化合物214-((R)-1-((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-9-((3-羧基-3-甲基丁酰基)氧基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-3a-基)-2-((4-氯苄基)氨基)乙氧基)-2,2-二甲基-4-氧代丁酸。在室温下,向搅拌的20(400mg,0.371mmol)的二氯甲烷(5mL)溶液中加入TFA(2mL,26.0mmol)。将该反应混合物在室温下搅拌1小时。蒸发该混合物,得到浅色油状的中间体21的TFA盐(350mg,0.343mmol,93%产率)。1HNMR(400MHz,氯仿-d)δ7.33-7.12(m,4H),5.76-5.60(m,1H),4.48-4.32(m,1H),4.26-3.98(m,2H),3.18-2.89(m,2H),2.89-2.68(m,2H),2.69-0.60(m,58H);LC/MS:m/z计算值:865.5,实测值:866.3(M+1)+。实施例2:化合物224-((R)-1-((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-9-((3-羧基-3-甲基丁酰基)氧基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-3a-基)-2-((4-氯苄基)(2-(二甲基氨基)乙基)氨基)乙氧基)-2,2-二甲基-4-氧代丁酸。向2-(二甲基氨基)乙醛盐酸盐(441mg,3.57mmol)的甲醇(12mL)溶液中加入21(它的三氟乙酸盐)(350mg,0.357mmol)。用Et3N将该混合物的pH值调节至7-8。将该反应混合物在室温下搅拌2小时,然后加入NaBH3CN(224mg,3.57mmol),并将该混合物搅拌过夜。过滤该反应,蒸发,得到粗品。用制备HPLC纯化残余物,获得化合物22的TFA盐(200mg,0.168mmol,47.2%产率)白色固体。1HNMR(400MHz,氯仿-d)δ7.33(d,J=8.3Hz,2H),7.22(d,J=8.3Hz,2H),5.83-5.67(m,1H),4.54-4.42(m,1H),3.88-3.75(m,1H),3.65-3.49(m,1H),3.04-0.60(m,71H);LC/MS:m/z计算值:936.6,实测值:937.4(M+1)+。实施例3:化合物254-((S)-1-((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-9-((3-羧基-3-甲基丁酰基)氧基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-3a-基)-2-((4-氯苄基)(2-(二甲基氨基)乙基)氨基)乙氧基)-2,2-二甲基-4-氧代丁酸。步骤A:中间体232,2-二甲基琥珀酸4-((S)-1-((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-9-((4-(叔丁氧基)-3,3-二甲基-4-氧代丁酰基)氧基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-3a-基)-2-((叔丁氧羰基)(4-氯苄基)氨基)乙基)1-叔丁基酯。在室温下,向搅拌的10(203mg,1.006mmol)、DMAP(123mg,1.006mmol)的二氯甲烷(10mL)溶液中加入EDC(321mg,1.677mmol)。将该反应混合物在室温下搅拌1小时,然后将18(300mg,0.335mmol)加入到该反应中。完成后,加入硅胶,浓缩该混合物,用色谱纯化(石油醚:EtOAc,6:1至3:1),得到23(344mg,0.319mmol,95%产率)亮白色固体。步骤B:化合物242,2-二甲基琥珀酸4-((S)-1-((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-9-((4-(叔丁氧基)-3,3-二甲基-4-氧代丁酰基)氧基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-3a-基)-2-((叔丁氧羰基)(4-氯苄基)氨基)乙基)1-叔丁基酯。向23(115mg,0.107mmol)的DCM(5mL)溶液中加入TFA(2.5mL,0.107mmol)。将该反应混合物在室温下搅拌2小时,真空蒸发,得到粗品。然后用饱和碳酸氢钠溶液、水和盐水洗涤该物质。过滤有机物,浓缩,得到24(89mg,0.023mmol,21.17%产率)白色固体。1HNMR(400MHz,氯仿-d)δ7.40(s,4H),5.97-5.65(m,1H),4.93-3.75(m,3H),3.59-3.27(m,1H),3.27-2.92(m,3H),2.83-2.11(m,5H),1.98-0.59(m,52H)LC/MS:m/z计算值:865.5,实测值:866.4(M+1)+。实施例4:化合物254-((S)-1-((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-9-((3-羧基-3-甲基丁酰基)氧基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-3a-基)-2-((4-氯苄基)(2-(二甲基氨基)乙基)氨基)乙氧基)-2,2-二甲基-4-氧代丁酸。向2-(二甲基氨基)乙醛(325mg,2.63mmol)的甲醇(5mL)和DCE(50ml)溶液中加入24(228mg,0.263mmol)和三乙胺(0.110mL,0.789mmol)。将该反应混合物在室温下搅拌3小时。将该反应冷却至0℃,加入氰基硼氢化钠(24.80mg,0.395mmol),并将得到的混合物搅拌过夜。过滤该反应,并将滤饼用DCM洗涤。减压浓缩滤液,用制备HPLC纯化残余物,得到标题化合物25的TFA盐(76mg,0.065mmol,24.78%产率)白色固体。1HNMR(400MHz,氯仿-d)δ7.38-7.30(m,2H),7.30-7.19(m,2H),5.82-5.69(m,1H),4.53-4.44(m,1H),4.05-3.89(m,1H),3.70-3.54(m,1H),3.41-2.51(m,15H),2.45-2.12(m,2H),1.97-0.65(m,54H);LC/MS:m/z计算值:936.6,实测值:937.4(M+1)+。实施例5:化合物324-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-((4-氯苄基)氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。步骤A:中间体26乙酸1-((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-9-乙酰氧基-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-3a-基)-2-硝基乙酯。向11(20g,35.9mmol)的乙酸酐(100mL,1065mmol)溶液中加入4-甲基苯磺酸(1.852g,10.76mmol)。将该反应混合物在室温下搅拌过夜。加入EtOAc(50mL)和NaHCO3水溶液(100mL)。分离有机层,用水、盐水洗涤,干燥(Na2SO4)。除去溶剂,得到粗品,其直接用于下一步。LC/MS:m/z计算值:599.4,实测值:600.3(M+1)+。步骤B:中间体27乙酸(3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-1-异丙基-5a,5b,8,8,11a-五甲基-3a-(2-硝基乙基)-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基酯。在冰浴中,向26(21g,35.0mmol)的THF(30mL)和EtOH(80mL)溶液中加入NaBH4(5.30g,140mmol)。然后,将该混合物在室温下保持大约1小时,用乙酸乙酯(200mL)稀释,用10%柠檬酸水溶液(150mL)、饱和NaHCO3水溶液(150mL)和盐水(150mL)提取。干燥有机层(Na2SO4),蒸发,得到粗品27(19g,27.2mmol,78%产率)。其直接用于下一步。LC/MS:m/z计算值:541.4,实测值:542.3(M+1)+。步骤C:中间体28乙酸(3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3a-(2-氧代乙基)-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基酯。在-5℃,向27(10g,18.46mmol)的丙酮(90.00mL)和甲醇(90mL)搅拌溶液中逐滴加入KOH(1.036g,18.46mmol)的5mL水溶液,然后加入KMnO4(1.896g,12.00mmol)和MgSO4(1.666g,13.84mmol)(在90mL水中)。将温度保持低于0℃下1小时,并在室温下再保持1小时。将该反应混合物用DCM(100mL)稀释,然后在CeliteTM上过滤,并用DCM洗涤。浓缩有机相,然后用DCM提取,得到粗品28(5g,8.12mmol,44.0%产率),其不用进一步纯化就直接用于下一步。1HNMR(400MHz,氯仿-d)δ9.64(s,1H),4.49(dd,J=5.5,11.0Hz,1H),3.27-3.06(m,1H),2.87-2.76(m,1H),2.76-2.64(m,1H),2.64-2.54(m,1H),2.45(d,J=18.8Hz,1H),2.20(d,J=18.8Hz,1H),2.05(s,3H),1.99-0.67(m,39H);LC/MS:m/z计算值:510.4,实测值:533.3(M+Na)+。步骤D:中间体29乙酸(3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-((叔丁氧羰基)(4-氯苄基)氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基酯。在室温下,向搅拌的28(1.5g,2.94mmol)、TEA(0.164mL,1.175mmol)和MgSO4(0.530g,4.41mmol)的甲醇(15mL)溶液中加入4-氯苄胺(0.487mL,4.11mmol)。将该反应混合物在20℃下搅拌2小时,然后冷却至-5℃,在10分钟期间内,以小份形式加入NaBH4(0.167g,4.41mmol),并搅拌30分钟。然后加入BOC2O(0.750mL,3.23mmol)。将该反应升温至室温,并搅拌1小时。将该反应混合物倒入冰水(300mL)中,收集固体,干燥,得到29(1.8g,2.106mmol,72%)白色泡沫体。该物质不用进一步纯化就使用。LC/MS:m/z计算值:735.5,实测值:758.3(M+Na)+。步骤E:中间体304-氯苄基(2-((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-9-羟基-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-3a-基)乙基)氨基甲酸叔丁基酯。向29(1.6g,2.173mmol)的甲醇(6mL)、THF(6mL)和水(6mL)溶液中加入NaOH(5.21g,130mmol)。将该反应混合物在室温下搅拌1小时。加入水和EtOAc,完成后,分离各层。用水、盐水洗涤有机层,干燥(Na2SO4)。除去溶剂,得到30(1.4g,1.590mmol,73%)白色固体。LC/MS:m/z计算值:693.5,实测值:716.3(M+Na)+。步骤F:中间体312,2-二甲基琥珀酸4-((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-((叔丁氧羰基)(4-氯苄基)氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)1-叔丁基酯。向在20℃下搅拌30分钟的DMAP(0.862g,7.06mmol)、EDC(1.932g,10.08mmol)和4-叔丁氧基-3,3-二甲基-4-氧代丁酸(10)(1.631g,8.06mmol)的DCM(60mL)溶液中加入30(1.4g,2.016mmol)。将该反应混合物在20℃下搅拌1小时。将该混合物用饱和氯化铵、水和饱和NaHCO3、水洗涤,最后用盐水洗涤。用Na2SO4干燥有机层,过滤,浓缩,得到粗品,将其用硅胶柱纯化,用石油醚/乙酸乙酯(4:1)洗脱,得到产物2,2-二甲基琥珀酸4-((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-((叔丁氧羰基)(4-氯苄基)氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)1-叔丁基酯(1.4g,0.986mmol,49%)黄色固体。步骤G:化合物324-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-((4-氯苄基)氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。向31(1.4g,1.593mmol)的DCM(6mL)溶液中加入TFA(3mL)。将该反应混合物在20℃下搅拌2小时,真空蒸发,得到粗品,将粗品用制备HPLC纯化,得到标题化合物的三氟乙酸盐(1g,73%)白色固体。1HNMR(400MHz,甲醇-d4)δ=7.57-7.42(m,4H),4.51(dd,J=5.1,11.2Hz,1H),4.29-4.15(m,2H),3.30-3.18(m,1H),2.98-2.69(m,3H),2.62(q,J=16.0Hz,2H),2.29(d,J=19.1Hz,1H),2.17-0.79(m,48H);LC/MS:m/z计算值:721.5,实测值:722.3(M+1)+。实施例6:化合物334-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-(苄基氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。按照类似于实施例5的方式,制备标题化合物的TFA盐。1HNMR(400MHz,甲醇-d4)δ=7.48(s,5H),4.51(dd,J=5.1,11.2Hz,1H),4.30-4.17(m,2H),3.31-3.19(m,1H),2.96-2.71(m,3H),2.62(q,J=15.9Hz,2H),2.29(d,J=18.8Hz,1H),2.21-0.78(m,48H);LC/MS:m/z计算值:687.5,实测值:688.4(M+1)+。实施例7:化合物394-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-((3-氯苄基)氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。步骤A:化合物34乙酸(3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-氨基乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基酯。在1小时期间内,向乙酸(3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-1-异丙基-5a,5b,8,8,11a-五甲基-3a-(2-硝基乙基)-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基酯(27)(10g,18.46mmol)和氯化镍(II)(7.18g,55.4mmol)的甲醇(100mL)溶液中分批地加入硼氢化钠(6.98g,185mmol)。将该反应混合物在0℃下搅拌1小时。用EtOAc(250mL)稀释该混合物。用饱和NH4Cl(50mL)洗涤有机相,直到有机层转变为无色为止。用无水Na2SO4干燥合并的有机层,真空浓缩,得到粗品乙酸(3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-氨基乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基酯(34)(7g,12.63mmol,68.4%产率),其不用进一步纯化就使用。1HNMR(400MHz,氯仿-d)δ=9.15(dd,J=4.9,11.4Hz,1H),8.12(br.s.,2H),7.97-7.81(m,1H),7.63-7.49(m,1H),7.26-7.15(m,1H),7.15-7.04(m,1H),6.98(d,J=18.6Hz,1H),6.81-5.38(m,47H);LC/MS:m/z计算值:511.4,实测值:512.3(M+1)+。步骤B:化合物35乙酸(3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-((叔丁氧羰基)氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基酯。向在室温下搅拌的乙酸(3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-氨基乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基酯(34)(5.3g,10.36mmol)、TEA(2.165mL,15.53mmol)和TEA(2.165mL,15.53mmol)的二氯甲烷(DCM)(100mL)溶液中加入BOC2O(2.404mL,10.36mmol)。将该反应混合物在20℃下搅拌2小时。将该反应混合物倒入冰水(300mL)中,收集固体,干燥,得到乙酸(3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-((叔丁氧羰基)氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基酯(35)(5.8g,8.34mmol,81%产率)白色泡沫体。其不用进一步纯化就以粗品形式在下一个反应中使用。1HNMR(400MHz,氯仿-d)δ=4.58-4.37(m,2H),3.26-2.96(m,4H),2.93-2.72(m,2H),2.28(d,J=18.8Hz,1H),2.11-0.71(m,53H);LC/MS:m/z计算值:611.5,实测值:634.3(M+Na)+。步骤C:化合物36(2-((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-9-羟基-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-3a-基)乙基)氨基甲酸叔丁基酯。将乙酸(3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-((叔丁氧羰基)氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基酯(35)(5.8g,9.48mmol)、NaOH(11.37g,284mmol)的甲醇(4mL)、THF(6ml)和水(2mL)溶液在室温下搅拌1小时。加入EtOAc,并将该反应混合物用水洗涤。分离有机层,用水和盐水洗涤,干燥(Na2SO4)。除去溶剂,提供(2-((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-9-羟基-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-3a-基)乙基)氨基甲酸叔丁基酯(36)(5.4g,7.87mmol,83%产率)白色固体。1HNMR(400MHz,氯仿-d)δ=4.53-4.36(m,1H),3.30-2.94(m,4H),2.94-2.67(m,2H),2.28(d,J=18.8Hz,1H),2.11-0.55(m,50H);LC/MS:m/z计算值:569.4,实测值:592.3(M+Na)+。步骤D:化合物372,2-二甲基琥珀酸4-((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-((叔丁氧羰基)氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)1-叔丁基酯。将4-叔丁氧基-3,3-二甲基-4-氧代丁酸(10)(4.79g,23.69mmol)、DMAP(3.47g,28.4mmol)和(2-((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-9-羟基-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-3a-基)乙基)氨基甲酸叔丁基酯(36)(5.4g,9.48mmol)、EDC(9.08g,47.4mmol)的二氯甲烷(DCM)(25mL)溶液在室温下搅拌过夜。加入NH4Cl,并将该混合物用DCM提取,用色谱纯化,使用PE:EA(10:1),得到2,2-二甲基琥珀酸4-((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-((叔丁氧羰基)氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)1-叔丁基酯(37)(6.7g,8.75mmol,92%产率)。1HNMR(400MHz,氯仿-d)δ=4.62-4.39(m,2H),3.24-3.10(m,1H),3.10-2.93(m,1H),2.93-2.68(m,2H),2.62-2.49(m,1H),2.28(d,J=18.8Hz,1H),2.11-0.69(m,66H);LC/MS:m/z计算值:753.6,实测值:776.5(M+Na)+。步骤E:化合物384-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-氨基乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。向在室温下搅拌的2,2-二甲基琥珀酸4-((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-((叔丁氧羰基)氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)1-叔丁基酯(37)(6.7g,8.88mmol)的DCM(20mL)溶液中加入TFA(4mL,51.9mmol)。将该反应混合物在室温下搅拌2小时。用饱和NaHCO3洗涤该反应混合物。形成固体,过滤收集,得到4-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-氨基乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸(38)(4g,6.55mmol,73.7%产率)白色固体。1HNMR(400MHz,DMSO-d6)δ=4.44-4.28(m,1H),3.20-3.05(m,1H),2.87-2.75(m,1H),2.46-2.16(m,6H),1.97-0.66(m,47H);LC/MS:m/z计算值:597.4,实测值:598.3(M+1)+。步骤F:化合物394-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-((3-氯苄基)氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。向在室温搅拌的4-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-氨基乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸(38)(300mg,0.502mmol)、TEA(0.028mL,0.201mmol)和MgSO4(91mg,0.753mmol)的甲醇(15mL)溶液中加入3-氯苯甲醛(85mg,0.602mmol)。将该反应混合物在20℃下搅拌2小时。然后将该反应混合物冷却至0℃,在30分钟之内逐份加入NaBH4(1.541g,40.7mmol),而后将该溶液搅拌1小时。用制备TLC纯化该混合物,用DCM/MeOH(20:1)洗脱,得到39(108mg,0.147mmol,29%)。1HNMR(500MHz,甲醇-d4)δ=7.41(s,1H),7.38-7.24(m,3H),4.48(dd,J=5.7,10.7Hz,1H),3.89-3.67(m,2H),3.26-3.11(m,1H),2.84-2.73(m,1H),2.66-2.47(m,2H),2.46-2.34(m,1H),2.34-2.21(m,2H),2.08-0.77(m,48H)。实施例8:化合物404-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-((3-氯-2-氟苄基)氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。按照类似于实施例7的方式,制备标题化合物,但为TFA盐形式。1HNMR(500MHz,甲醇-d4)δ=7.46-7.38(m,1H),7.35(t,J=6.6Hz,1H),7.17(t,J=7.7Hz,1H),4.48(dd,J=5.5,10.6Hz,1H),3.97-3.72(m,2H),3.27-3.12(m,1H),2.85-2.73(m,1H),2.67-2.45(m,2H),2.44-2.16(m,3H),2.09-0.73(m,48H)。实施例9:化合物414-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-((1-(4-氯苯基)环丙基)氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。按照类似于实施例5的方式,制备标题化合物,但为TFA盐形式。按照下列方法进行最后一步。向在室温下搅拌的4-(叔丁氧基)-3,3-二甲基-4-氧代丁酸(10)(0.988g,4.89mmol)、EDC(1.171g,6.11mmol)和DMAP(0.522g,4.28mmol)的DCM(12mL)溶液中加入(1-(4-氯苯基)环丙基)(2-((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-9-羟基-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-3a-基)乙基)氨基甲酸叔丁基酯(1.1g,1.221mmol)。将该反应混合物在室温下搅拌2小时。紧接着,将TFA(6mL)加入到该反应混合物中。然后,将该反应溶液在室温下再搅拌1.5小时,并用DCM(60mL*3)提取产物,用盐水(100ml)洗涤合并的有机相,用Na2SO4干燥,浓缩,用DCM和己烷(1:6)重结晶纯化残余物,得到800mg41的TFA盐白色固体。1HNMR(400MHz,甲醇-d4)δ=7.64-7.44(m,4H),4.50(dd,J=5.1,11.2Hz,1H),3.26-3.10(m,1H),2.84-2.41(m,5H),2.24-2.12(m,1H),2.12-0.78(m,52H);LC/MS:m/z计算值:747.5,实测值:748.3(M+1)+。实施例10:化合物424-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-((4-氯苄基)(2-(二甲基氨基)乙基)氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。向2-(二甲基氨基)乙醛(244mg,1.977mmol)的甲醇(100mL)溶液中加入4-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-((4-氯苄基)氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸盐酸盐(32)(300mg,0.395mmol)。将该反应混合物在40℃下搅拌2小时。将该反应冷却至室温,加入氰基硼氢化钠(24.84mg,0.395mmol),并将得到的溶液搅拌过夜。将该反应用氯化铵(40mL)稀释,并用DCM(60mLx3)提取。将合并的有机层用盐水(20mL)洗涤,用硫酸钠干燥,过滤,真空浓缩。用制备HPLC纯化残余物,得到42的三氟乙酸盐(200mg,49%产率)白色固体。1HNMR(400MHz,甲醇-d4)δ=7.52-7.34(m,4H),4.50(dd,J=5.0,11.0Hz,1H),4.07-3.88(m,1H),3.83-3.62(m,1H),3.53-3.35(m,2H),3.22-2.89(m,9H),2.71-2.54(m,2H),2.50-2.21(m,4H),2.06-0.83(m,48H);LC/MS:m/z计算值:792.5,实测值:793.4(M+1)+。实施例11:化合物434-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-((1-(4-氯苯基)环丙基)(2-(二甲基氨基)乙基)氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。按照类似于实施例10的方式,制备标题化合物的TFA盐。1HNMR(400MHz,甲醇-d4)δ=7.35(s,4H),4.51(dd,J=5.1,11.2Hz,1H),3.31-3.17(m,2H),3.12-2.73(m,9H),2.73-2.51(m,2H),2.44-2.17(m,3H),2.14-0.77(m,53H);LC/MS:m/z计算值:818.4,实测值:819.4(M+1)+。实施例12:化合物444-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-((4-氯苄基)(甲基)氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。在室温下,向32(150mg,0.208mmol)的MeOH(6mL)溶液中加入甲醛(33.7mg,0.415mmol)。将该反应混合物在室温下搅拌2小时。分批加入NaCNBH4(104mg,1.661mmol),并将该混合物搅拌过夜。蒸发溶剂,并将该混合物用制备HPLC纯化,提供44的TFA盐(60mg,34%)。1HNMR(400MHz,甲醇-d4)δ=7.60-7.44(m,4H),4.56-4.37(m,2H),4.36-4.24(m,1H),3.28-3.14(m,1H),2.89(m,5H),2.73-2.50(m,2H),2.28(d,J=19.1Hz,1H),2.20-0.83(m,49H);LC/MS:m/z计算值:735.5,实测值:736.3(M+1)+。实施例13:化合物454-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-(N-(4-氯苄基)乙酰胺基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。将32(150mg,0.208mmol)、TEA(210mg,2.076mmol)和DMAP(5mg,0.042mmol)的混合物在DCM(5mL)中搅拌3小时。紧接着,将该混合物用水(50mL)淬灭。然后用水(2x50ml)洗涤有机物,用Na2SO4干燥,真空蒸发,得到粗品。然后用制备HPLC纯化,得到45(65mg,0.085mmol,41%)白色固体。旋转异构体的混合物。1HNMR(400MHz,甲醇-d4)δ=7.49-7.18(m,4H),4.80-4.42(m,3H),3.27-2.81(m,4H),2.76-2.52(m,2H),2.36-2.10(m,4H),2.08-0.82(m,48H);LC/MS:m/z计算值:763.5,实测值:764.3(M+1)+。实施例14:化合物464-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-((4-氯苄基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。向在室温下搅拌的2,2-二甲基琥珀酸4-((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-((叔丁氧羰基)(4-氯苄基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)1-叔丁基酯(19)(300mg,0.335mmol)的DCM(30mL)溶液中加入TFA(15mL,195mmol)。将该反应混合物在室温下搅拌,直到LCMS和TLC显示起始物质消失为止。真空除去溶剂,用制备HPLC纯化残余物,得到4-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-((4-氯苄基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸(46)(100mg,0.135mmol,40.4%产率)的TFA盐。1HNMR(400MHz,氯仿-d)δ=7.38-7.18(m,4H),4.54-4.42(m,1H),4.28-4.14(m,1H),3.93-3.70(m,2H),3.19-3.00(m,1H),2.75-0.69(m,52H);LC/MS:m/z计算值:737.4,实测值:738.2(M+1)+。实施例15:化合物474-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-2-((4-氯苄基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。向在室温下搅拌的2,2-二甲基琥珀酸4-((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-2-((叔丁氧羰基)(4-氯苄基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)1-叔丁基酯(18)(130mg,0.145mmol)的DCM(30mL)溶液中加入TFA(15mL,195mmol)。将该反应混合物在室温下搅拌,直到LCMS和TLC显示起始原料消失为止。蒸发溶剂,然后加入CH3CN和水,并将该物质冷冻干燥,得到4-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-2-((4-氯苄基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸(47)的三氟乙酸盐(120mg,0.139mmol,96%产率)。1HNMR(400MHz,氯仿-d)δ=10.30(br.s.,1H),8.08(br.s.,1H),7.38(s,4H),4.73-4.33(m,2H),4.28-4.07(m,2H),3.34-3.06(m,2H),2.99-2.74(m,2H),2.73-2.50(m,2H),2.48-2.29(m,1H),2.05-0.64(m,47H);LC/MS:m/z计算值:737.4,实测值:738.3(M+1)+。实施例16:化合物494-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-1-乙酰氧基-2-((4-氯苄基)氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。步骤A:化合物482,2-二甲基琥珀酸4-((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-1-乙酰氧基-2-((叔丁氧羰基)(4-氯苄基)氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)1-叔丁基酯。向在室温下搅拌的19(500mg,0.559mmol)的二氯甲烷(30mL)溶液中加入Ac2O(0.158mL,1.677mmol)、三乙胺(0.195mL,1.397mmol)和DMAP(6.83mg,0.056mmol)。将该反应混合物在室温下搅拌,直到TLC显示起始物质消失为止。将该混合物后处理,用硅胶色谱纯化(PE:EA=5:1),得到48(510mg,0.517mmol,93%产率)。产物由旋转异构体的混合物组成。1HNMR(400MHz,氯仿-d)δ=7.39-7.20(m,2H),7.21-6.99(m,2H),5.92-5.56(m,1H),5.00-3.88(m,2H),3.40-1.96(m,8H),1.97-0.58(m,67H)。步骤B:化合物494-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-1-乙酰氧基-2-((4-氯苄基)氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。向在室温下搅拌的48(500mg,0.534mmol)的DCM(30mL)溶液中加入TFA(15mL,195mmol)。将该反应混合物在室温下搅拌,直到LCMS和TLC显示起始物质消失为止。蒸发溶剂,加入CH3CN和水,并将混合物冷冻干燥,得到49的三氟乙酸盐(400mg,0.439mmol,82%产率)。1HNMR(400MHz,氯仿-d)δ=7.46-7.19(m,4H),5.94-5.70(m,1H),4.58-4.36(m,1H),4.25-3.88(m,2H),3.25-3.02(m,1H),3.01-2.41(m,5H),2.08(s,3H),2.00-0.64(m,47H);LC/MS:m/z计算值:779.5,实测值:780.4(M+1)+。实施例17:化合物504-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-1-乙酰氧基-2-((4-氯苄基)氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。按照类似于实施例16的方式,制备标题化合物,并以TFA盐形式分离。1HNMR(400MHz,氯仿-d)δ=7.49-7.30(m,4H),5.85-5.71(m,1H),4.59-4.40(m,1H),4.31-4.03(m,2H),3.41-2.79(m,4H),2.79-2.50(m,2H),2.37(d,J=18.1Hz,2H),2.02-0.63(m,49H);LC/MS:m/z计算值:779.5,实测值:780.3(M+1)+。实施例18:化合物514-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-((4-氯苄基)(2-(二甲基氨基)乙基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。向2-(二甲基氨基)乙醛盐酸盐(6.75g,54.6mmol)的甲醇(20mL)溶液中加入4-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-((4-氯苄基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸三氟乙酸盐(46)(9.5g,10.92mmol)。用Et3N将pH值调节至7-8。将该反应混合物在室温下搅拌2小时。然后加入氰基硼氢化钠(0.686g,10.92mmol),并将该混合物在室温下搅拌过夜。反应完成之后,加入水(15mL)和EtOAc(15mL),而后取出有机相,减压浓缩。将产物用EtOAc(80mLx3)提取,用盐水洗涤合并的有机相,干燥,浓缩。用快速色谱纯化产物(DCM:EtOAc=2:1至1:1,然后DCM:MeOH=100:1至20:1),得到4-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-((4-氯苄基)(2-(二甲基氨基)乙基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸(51)(6g,7.41mmol,67.9%产率)白色固体。将多批该物质(合并95g)溶于600mL二氯甲烷中,用NaHCO3(400mL*3)洗涤,用Na2SO4干燥有机相,过滤,浓缩。用EtOAc:石油醚的混合物(600mL)洗涤固体,过滤,而后冷冻干燥,提供最终62g标题化合物白色固体。1HNMR(400MHz,甲醇-d4)δ=7.47-7.29(m,4H),4.48(dd,J=5.8,10.3Hz,1H),4.15-4.04(m,1H),3.80(d,J=13.8Hz,1H),3.57(d,J=14.1Hz,1H),3.21-2.82(m,5H),2.72-2.41(m,9H),2.37-2.05(m,4H),2.05-0.74(m,45H);LC/MS:m/z计算值:808.5,实测值:809.5(M+1)+。实施例19:化合物564-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-2-((4-氯苄基)(2-(二甲基氨基)乙基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。步骤A:化合物52(3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-((4-氯苄基)(2-(二甲基氨基)乙基)氨基)乙酰基)-9-羟基-1-异丙基-5a,5b,8,8,11a-五甲基-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-2-酮。在0℃,向2-(二甲基氨基)乙醛(4.79g,38.8mmol)的甲醇(50mL)和1,2-二氯乙烷(DCE)(25mL)溶液中加入(3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-(4-氯苄基氨基)乙酰基)-9-羟基-1-异丙基-5a,5b,8,8,11a-五甲基-3a,4,5,5a,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十六氢-3H-环戊二烯并[a]-2(5bH)-酮(15)(5g,7.75mmol)。用Et3N将pH值调节至7。将该反应混合物在室温下搅拌1小时。加入氰基硼氢化钠(0.487g,7.75mmol),并将该混合物搅拌过夜。用水(40mL)稀释该反应,并用DCM(60mlx3)提取。将合并的有机层用盐水(20mL)洗涤,用硫酸钠干燥,过滤,得到粗品(3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-((4-氯苄基)(2-(二甲基氨基)乙基)氨基)乙酰基)-9-羟基-1-异丙基-5a,5b,8,8,11a-五甲基-3a,4,5,5a,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十六氢-3H-环戊二烯并[a]-2(5bH)-酮(52)(5g,5.89mmol,76%产率)浅黄色固体,其在下一步中使用。LC/MS:m/z计算值:678.5,实测值:679.3。步骤B:化合物532,2-二甲基琥珀酸1-叔丁基4-((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-((4-氯苄基)(2-(二甲基氨基)乙基)氨基)乙酰基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)酯。向4-(叔丁氧基)-3,3-二甲基-4-氧代丁酸(11.91g,58.9mmol)、N,N-二甲基吡啶-4-胺(4.50g,36.8mmol)的DCM(20mL)溶液中加入EDC(11.29g,58.9mmol)。将该反应混合物在室温下搅拌1小时。然后,加入(3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-((4-氯苄基)(2-(二甲基氨基)乙基)氨基)乙酰基)-9-羟基-1-异丙基-5a,5b,8,8,11a-五甲基-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-2-酮(52)(5g,7.36mmol)。完成后,用2MHCl、水和盐水洗涤该混合物。用Na2SO4干燥有机层,过滤,浓缩,得到粗品。用硅胶柱纯化产物,使用二氯甲烷/甲醇(20:1),得到油状2,2-二甲基琥珀酸1-叔丁基4-((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-((4-氯苄基)(2-(二甲基氨基)乙基)氨基)乙酰基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)酯(53)(1.8g,1.917mmol,26.1%产率)。1HNMR(400MHz,氯仿-d)δ=7.27(s,4H),4.60-4.39(m,1H),3.82(d,J=13.8Hz,1H),3.59(d,J=13.8Hz,1H),3.50-3.05(m,3H),2.82-2.63(m,2H),2.63-0.53(m,67H)。步骤C:化合物54和552,2-二甲基琥珀酸1-叔丁基4-((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-((4-氯苄基)(2-(二甲基氨基)乙基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)酯(54)和2,2-二甲基琥珀酸1-叔丁基4-((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-2-((4-氯苄基)(2-(二甲基氨基)乙基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)酯(55)。向2,2-二甲基琥珀酸1-叔丁基4-((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-((4-氯苄基)(2-(二甲基氨基)乙基)氨基)乙酰基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)酯(53)(1.5g,1.737mmol)的甲醇(10mL)溶液中加入NaBH4(0.131g,3.47mmol)。将该反应混合物在室温下搅拌1小时。然后用DCM提取该混合物,用水和盐水洗涤。用Na2SO4干燥有机层,浓缩,得到粗品。用制备HPLC纯化,然后用SFC纯化,得到54(230mg,15%)和55(360mg23%)。对于54:1HNMR(400MHz,氯仿-d)δ=7.45-7.18(m,4H),4.49(dd,J=5.6,10.7Hz,1H),4.04(d,J=9.8Hz,1H),3.92-3.47(m,3H),3.46-0.45(m,72H);LC/MS:m/z计算值:864.6,实测值:865.4(M+1)+。对于55:1HNMR(400MHz,氯仿-d)δ=7.37-7.19(m,4H),4.50(dd,J=5.5,10.5Hz,1H),4.18-3.98(m,1H),3.75(d,J=13.3Hz,1H),3.55(d,J=13.3Hz,1H),3.29-3.10(m,1H),3.10-2.97(m,1H),2.81-0.63(m,70H);LC/MS:m/z计算值:864.6,实测值:865.9(M+1)+。步骤D:化合物564-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-2-((4-氯苄基)(2-(二甲基氨基)乙基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。向在室温下搅拌的55(360mg,0.416mmol)的DCM(5mL)溶液中加入TFA(2ml,26.0mmol)。将该反应混合物在室温下搅拌1小时。蒸发该混合物,得到粗品。用制备HPLC纯化该物质,提供标题化合物56的TFA盐(300mg,0.285mmol,68.6%产率)白色固体。1HNMR(400MHz,甲醇-d4)δ=7.58-7.34(m,4H),4.50(dd,J=5.0,11.0Hz,1H),4.23-4.10(m,1H),4.09-3.74(m,2H),3.58-3.12(m,3H),3.12-2.37(m,10H),2.12-0.67(m,50H);LC/MS:m/z计算值:808.5,实测值:809.3(M+1)+。实施例20:化合物574-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-1-乙酰氧基-2-((4-氯苄基)(2-(二甲基氨基)乙基)氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。向2-(二甲基氨基)乙醛,盐酸盐(238mg,1.922mmol)的甲醇(12mL)溶液中加入4-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-1-乙酰氧基-2-((4-氯苄基)氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸(50)(150mg,0.192mmol)。将该反应混合物在室温下搅拌2小时,然后加入氰基硼氢化钠(121mg,1.922mmol),并将该混合物搅拌过夜。完成后,用制备HPLC纯化该混合物,提供标题化合物(50mg,24%)。1HNMR(400MHz,氯仿-d)δ=7.35-7.12(m,4H),5.65(d,J=9.3Hz,1H),4.49(dd,J=5.8,10.0Hz,1H),3.83(d,J=13.6Hz,1H),3.55(d,J=13.6Hz,1H),3.25-2.91(m,7H),2.91-2.73(m,7H),2.73-2.52(m,3H),2.33(d,J=18.1Hz,1H),1.99-0.72(m,48H);LC/MS:m/z计算值:850.5,实测值:851.4(M+1)+。实施例21:化合物584-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-1-乙酰氧基-2-((4-氯苄基)(2-(二甲基氨基)乙基)氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。按照类似于实施例20的方式,制备标题化合物。1HNMR(400MHz,氯仿-d)δ=7.40-7.10(m,4H),5.68(d,J=9.8Hz,1H),4.55-4.39(m,1H),3.81(d,J=13.8Hz,1H),3.57(d,J=13.8Hz,1H),3.29-2.74(m,11H),2.74-2.27(m,6H),2.14(s,3H),2.09-0.68(m,46H);LC/MS:m/z计算值:850.5,实测值:851.4(M+1)+。实施例22和23:化合物62和635-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-((4-氯苄基)(2-(二甲基氨基)乙基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-3,3-二甲基-5-氧代戊酸(62)和5-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-2-((4-氯苄基)(2-(二甲基氨基)乙基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-3,3-二甲基-5-氧代戊酸(63)。步骤A:化合物595-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-((叔丁氧羰基)(4-氯苄基)氨基)乙酰基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-3,3-二甲基-5-氧代戊酸。向在室温下搅拌的4-氯苄基(2-((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-9-羟基-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-3a-基)-2-氧代乙基)氨基甲酸叔丁基酯(15)(1g,1.412mmol)、DMAP(0.517g,4.23mmol)的吡啶(2ml)溶液中加入4,4-二甲基-二氢-3H-吡喃-2,6-二酮(1.003g,7.06mmol)。将该反应混合物在50℃下搅拌5小时。将该混合物用EtOAc稀释,并用水洗涤。将得到的提取物用硅胶柱纯化,提供59(800mg,60%)。1HNMR(500MHz,氯仿-d)δ=8.67(br.s.,1H),7.98-7.36(m,1H),7.33-7.27(m,2H),7.21-7.09(m,2H),4.62-4.26(m,3H),4.07-3.42(m,2H),3.30-3.05(m,1H),2.66-0.66(m,61H)。步骤B:化合物605-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-((4-氯苄基)氨基)乙酰基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-3,3-二甲基-5-氧代戊酸。向在室温下搅拌的5-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-((叔丁氧羰基)(4-氯苄基)氨基)乙酰基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-3,3-二甲基-5-氧代戊酸(59)(800mg,0.941mmol)的二氯甲烷(6mL)溶液中加入三氟乙酸(2mL,0.941mmol)。将该反应混合物在室温下搅拌1小时。蒸发该混合物,提供目标化合物(600mg,81%),其不用进一步纯化就使用。LC/MS:m/z计算值:749.4,实测值:750.1(M+1)+。步骤C:化合物615-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-((4-氯苄基)(2-(二甲基氨基)乙基)氨基)乙酰基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-3,3-二甲基-5-氧代戊酸。在0℃,向5-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-((4-氯苄基)氨基)乙酰基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-3,3-二甲基-5-氧代戊酸三氟乙酸盐(60)(700mg,0.810mmol)的甲醇(30mL)溶液中加入2-(二甲基氨基)乙醛(353mg,4.05mmol)。用Et3N将pH值调节至7。将该反应混合物在室温下搅拌1小时,加入氰基硼氢化钠(50.9mg,0.810mmol),并将得到的混合物搅拌过夜。用水(40mL)稀释该反应,并用DCM(60mlx3)提取。将合并的有机层用盐水(20mL)洗涤,用硫酸钠干燥,过滤,得到粗品5-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-((4-氯苄基)(2-(二甲基氨基)乙基)氨基)乙酰基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-3,3-二甲基-5-氧代戊酸三氟乙酸盐(61)(200mg,23%产率)浅黄色固体。1HNMR(500MHz,甲醇-d4)δ=7.39(s,4H),4.49(dd,J=5.7,10.7Hz,1H),3.95(d,J=13.6Hz,1H),3.57(d,J=13.2Hz,1H),3.40-3.29(m,1H),3.27-3.16(m,2H),3.05(s,6H),3.00-2.88(m,2H),2.57-2.26(m,6H),2.09(d,J=19.5Hz,1H),2.04-0.75(m,47H);LC/MS:m/z计算值:820.5,实测值:821.3(M+1)+。步骤D:化合物62和635-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-((4-氯苄基)(异戊基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-3,3-二甲基-5-氧代戊酸(62)和5-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-2-((4-氯苄基)(异戊基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-3,3-二甲基-5-氧代戊酸(63)。向在0℃搅拌的5-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-((4-氯苄基)(2-(二甲基氨基)乙基)氨基)乙酰基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-3,3-二甲基-5-氧代戊酸三氟乙酸盐(61)(140mg,0.133mmol)的甲醇(10mL)溶液中加入NaBH4(10.09mg,0.267mmol)。将该反应混合物在0℃下搅拌1小时,然后加入更多的NaBH4(10.09mg,0.267mmol)。在0℃经过另外1小时之后,将该混合物升温至室温,并再搅拌1小时。LCMS显示反应完成。加入EtOAc,并将该混合物用水洗涤。蒸发有机相,得到粗品,将粗品用制备HPL纯化,得到两个非对映体。分离5mg异构体A(62)(产率3.5%),分离10mg异构体B(63)(7%)。利用与化合物51(类似于62)和56(类似于63)的光谱相似性,指定每个异构体中新形成的立构中心的立体化学。对于异构体A(62):1HNMR(500MHz,甲醇-d4)δ=7.48-7.30(m,4H),4.57-4.43(m,1H),4.14(d,J=10.1Hz,1H),3.91-3.74(m,1H),3.67(d,J=13.9Hz,1H),3.26-3.10(m,2H),3.10-2.93(m,2H),2.93-2.81(m,6H),2.68-2.10(m,9H),2.06-0.65(m,46H);LC/MS:m/z计算值:822.5,实测值:823.5(M+1)+。对于异构体B(63):1HNMR(500MHz,甲醇)δ=7.43(br.s.,4H),4.51(dd,J=5.8,9.9Hz,1H),4.16(d,J=10.1Hz,1H),3.98-3.75(m,2H),3.52-3.37(m,1H),3.31-3.02(m,3H),3.02-2.71(m,9H),2.64-2.34(m,6H),2.19-0.69(m,46H);LC/MS:m/z计算值:822.5,实测值:823.4(M+1)+。实施例24:化合物644-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-2-((2-氯苄基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。按照类似于实施例14的方式,制备标题化合物。试验性地指定立体化学为绘图形式,但没有利用光谱方法充分证实。1HNMR(400MHz,甲醇-d4)δ=7.73-7.38(m,4H),4.65-4.37(m,4H),3.44(d,J=12.3Hz,1H),3.39-3.22(m,1H),3.11-2.96(m,2H),2.62(q,J=16.0Hz,2H),2.48(d,J=18.3Hz,1H),2.21-0.77(m,46H);LC/MS:m/z计算值:737.4,实测值:738.3(M+1)+。实施例25:化合物654-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-((2-氯苄基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。按照类似于实施例14的方式,制备标题化合物。试验性地指定立体化学为绘图形式,但没有利用光谱方法充分证实。1HNMR(400MHz,甲醇-d4)δ=7.63-7.37(m,4H),4.55-4.31(m,4H),3.26-3.11(m,1H),3.01-2.46(m,6H),2.36-2.16(m,1H),2.15-0.79(m,45H);LC/MS:m/z计算值:737.4,实测值:738.0(M+1)+。实施例26:化合物664-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-1-乙酰氧基-2-((4-氟苄基)氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。按照类似于实施例16的方式,制备标题化合物的TFA盐。试验性地指定立体化学为绘图形式,但没有利用光谱方法充分证实。1HNMR(400MHz,氯仿-d)δ=10.54-8.79(m,1H),7.50-7.34(m,2H),7.19-6.99(m,2H),5.81(d,J=9.8Hz,1H),4.49(dd,J=5.8,10.3Hz,1H),4.31-3.93(m,2H),3.26(d,J=12.5Hz,1H),3.20-3.05(m,1H),3.05-2.82(m,2H),2.80-2.47(m,2H),2.36(d,J=18.1Hz,1H),2.05-0.57(m,49H);LC/MS:m/z计算值:763.5,实测值:764.3(M+1)+。实施例27:化合物674-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-1-乙酰氧基-2-((4-氟苄基)氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。按照类似于实施例16的方式,制备标题化合物的TFA盐。试验性地指定立体化学为绘图形式,但没有利用光谱方法充分证实。1HNMR(400MHz,氯仿-d)δ=9.65(br.s.,1H),7.46-7.28(m,2H),7.03(t,J=8.2Hz,2H),5.86(br.s.,1H),4.50(dd,J=5.5,10.3Hz,1H),4.29-4.06(m,1H),4.06-3.85(m,1H),3.19-2.99(m,1H),2.81-2.39(m,6H),2.21-0.62(m,49H);LC/MS:m/z计算值:763.5,实测值:764.3(M+1)+。实施例28:化合物684-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-1-乙酰氧基-2-((4-氯苄基)(甲基)氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。向在空气氛围中、在室温下搅拌的4-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-1-乙酰氧基-2-((4-氯苄基)氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸(50)(150mg,0.192mmol)的MeOH(6mL)溶液中加入甲醛(31.2mg,0.384mmol)。将该反应混合物在室温下搅拌2小时。然后分批地加入NaCNBH3(85mg,1.345mmol),并搅拌过夜。蒸发溶剂,并将残余物用DCM稀释,用水和盐水洗涤。将干燥的有机物过滤,浓缩,得到4-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-1-乙酰氧基-2-((4-氯苄基)(甲基)氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸(68)(120mg,65%产率)白色固体。该物质不用进一步纯化就使用。1HNMR(400MHz,氯仿-d)δ=7.31-7.26(m,2H),7.24-7.16(m,2H),5.65(d,J=8.5Hz,1H),4.50(br.s.,1H),3.66-3.51(m,1H),3.49-3.36(m,1H),3.27-3.06(m,2H),2.73-2.32(m,5H),2.26(s,3H),2.08-0.73(m,49H);LC/MS:m/z计算值:793.5,实测值:794.3(M+1)+。实施例29:化合物694-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-2-((4-氯苄基)(甲基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。向4-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-1-乙酰氧基-2-((4-氯苄基)(甲基)氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸(68)(120mg,0.151mmol)的乙醇(2mL)和甲苯(2mL)溶液中加入氢氧化钾(15.25mg,0.272mmol)。将该反应混合物在室温下搅拌30分钟。将该反应混合物用1NHCl水溶液中和至pH=7,并蒸发,获得残余物。用DCM提取,用水洗涤,干燥,得到粗品,将粗品用制备HPLC纯化,得到4-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-2-((4-氯苄基)(甲基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸作为a三氟乙酸盐盐(95mg,72%产率)白色固体。1HNMR(400MHz,甲醇-d4)δ=7.55(s,4H),4.60-4.12(m,3H),3.32-3.19(m,1H),3.18-2.84(m,5H),2.71-2.52(m,2H),2.11-0.78(m,49H);LC/MS:m/z计算值:751.5,实测值:752.4(M+1)+。实施例30:化合物704-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-1-乙酰氧基-2-((4-氯苄基)(甲基)氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。按照类似于实施例28的方式,制备标题化合物。1HNMR(400MHz,氯仿-d)δ=7.31-7.23(m,2H),7.22-7.13(m,2H),5.66(dd,J=2.4,8.7Hz,1H),4.55-4.43(m,1H),3.51-3.35(m,2H),3.19-3.05(m,1H),2.74-2.42(m,5H),2.42-0.66(m,53H);LC/MS:m/z计算值:793.5,实测值:794.5(M+1)+。实施例31:化合物714-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-((4-氯苄基)(甲基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。按照类似于实施例29的方式,制备标题化合物。1HNMR(500MHz,甲醇-d4)δ=7.63-7.38(m,4H),4.56-4.25(m,4H),3.25-3.14(m,1H),2.99(s,3H),2.82-2.52(m,4H),2.52-2.32(m,2H),2.24(d,J=12.9Hz,1H),2.09-0.77(m,45H);LC/MS:m/z计算值:751.5,实测值:752.3(M+1)+。实施例32:化合物724-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-1-乙酰氧基-2-(N-(4-氯苄基)乙酰胺基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。将4-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-1-乙酰氧基-2-((4-氯苄基)氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸(50)(200mg,0.256mmol)、TEA(0.332mL,2.56mmol)、DMAP(6.3mg,0.05mmol)和DCM(5mL)的混合物搅拌3小时。用水(50ml)淬灭该混合物,用水(2x50ml)洗涤,用Na2SO4干燥,过滤,真空浓缩,得到4-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-1-乙酰氧基-2-(N-(4-氯苄基)乙酰胺基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸(72)(160mg,0.182mmol,71.0%得到)白色固体。1HNMR(400MHz,氯仿-d)δ=7.42-7.24(m,2H),7.24-6.90(m,2H),5.98-5.68(m,1H),5.15-4.56(m,1H),4.56-4.45(m,1H),4.40-3.98(m,2H),2.29-0.68(m,66H),3.48-0.58(m,58H);LC/MS:m/z计算值:821.5,实测值:822.3(M+1)+。实施例33:化合物734-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-2-(N-(4-氯苄基)乙酰胺基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。向4-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-1-乙酰氧基-2-(N-(4-氯苄基)乙酰胺基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸(72)(150mg,0.182mmol)的乙醇(2mL)和甲苯(2mL)溶液中加入氢氧化钾(40.9mg,0.729mmol)。将该反应混合物在室温下搅拌30分钟。将该反应混合物用1NHCl水溶液中和至pH=7,浓缩,获得残余物。用DCM提取残余物,用水洗涤,干燥,得到粗品,将粗品用制备HPLC纯化,得到4-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-2-(N-(4-氯苄基)乙酰胺基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸(73)(40mg,28%)白色固体。化合物以旋转异构体的混合物形态存在;1HNMR(400MHz,DMSO-d6)δ=12.18(br.s.,1H),7.52-7.14(m,4H),5.03-3.77(m,5H),3.39-2.80(m,3H),2.62-2.54(m,1H),2.27(t,J=17.2Hz,1H),2.20-0.58(m,51H);LC/MS:m/z计算值:779.5,实测值:802.3(M+Na)+。实施例34:化合物744-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-(N-(4-氯苄基)乙酰胺基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。将4-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-1-乙酰氧基-2-((4-氯苄基)氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸(49)(150mg,0.192mmol)、Na2CO3(20.37mg,0.192mmol)的混合物在甲醇(3mL)中搅拌3小时,然后用制备HPLC纯化,得到4-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-(N-(4-氯苄基)乙酰胺基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸(74)(45mg,30%)白色固体。化合物以旋转异构体的混合物形态存在;1HNMR(500MHz,甲醇-d4)δ=7.43-7.27(m,2H),7.28-7.11(m,2H),5.30-4.09(m,6H),3.55-2.09(m,11H),2.09-0.78(m,44H);LC/MS:m/z计算值:779.5,实测值:780.4(M+1)+。实施例35:化合物764-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-2-(N-(2-氯苄基)乙酰胺基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。向在室温下搅拌的2,2-二甲基琥珀酸4-((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-1-乙酰氧基-2-((叔丁氧羰基)(2-氯苄基)氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)1-叔丁基酯(75,按照类似于化合物48的方式制备)(100mg,0.107mmol)的DCM(30mL)溶液中加入TFA(15mL,195mmol)。将该反应混合物在室温下搅拌,直到LCMS和TLC显示起始物质消失为止。除去溶剂,得到粗品,将粗品用制备HPLC纯化,得到4-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-2-(N-(2-氯苄基)乙酰胺基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸(40mg,48%)。试验性地指定立体化学为绘图形式,但没有利用光谱方法充分证实。该化合物以旋转异构体的混合物形态存在。1HNMR(400MHz,甲醇-d4)δ=7.55-7.14(m,4H),5.10-4.72(m,2H),4.72-3.97(m,3H),3.54-3.39(m,1H),3.30-3.21(m,1H),3.13-2.97(m,1H),2.84-0.69(m,53H);LC/MS:m/z计算值:779.5,实测值:780.3(M+1)+。实施例36:化合物774-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-1-乙酰氧基-2-((2-氯苄基)(2-(二甲基氨基)乙基)氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。按照类似于实施例20的方式,制备标题化合物。试验性地指定立体化学为绘图形式,但没有利用光谱方法充分证实。1HNMR(400MHz,氯仿-d)δ=7.64-7.06(m,4H),5.61(d,J=8.8Hz,1H),4.50(dd,J=5.4,10.7Hz,1H),3.82(d,J=13.8Hz,1H),3.65(d,J=13.6Hz,1H),3.26-2.92(m,7H),2.89-2.74(m,7H),2.74-2.53(m,3H),2.26(d,J=18.3Hz,1H),1.93-0.67(m,48H);LC/MS:m/z计算值:850.5,实测值:851.4(M+1)+。实施例37:化合物784-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-2-((3-氯苄基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。按照类似于实施例20的方式,制备标题化合物的TFA盐。试验性地指定立体化学为绘图形式,但没有利用光谱方法充分证实。1HNMR(400MHz,甲醇-d4)δ=7.61(s,1H),7.56-7.43(m,3H),4.57-4.44(m,2H),4.35-4.21(m,2H),3.38(dd,J=2.5,12.5Hz,1H),3.31-3.23(m,1H),3.09-3.01(m,1H),2.96(t,J=11.8Hz,1H),2.71-2.51(m,1H),2.46(d,J=18.3Hz,1H),2.15-0.79(m,48H);LC/MS:m/z计算值:737.4,实测值:738.3(M+1)+。实施例38:化合物794-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-((3-氯苄基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。按照类似于实施例20的方式,制备标题化合物的TFA盐。试验性地指定立体化学为绘图形式,但没有利用光谱方法充分证实。1HNMR(400MHz,甲醇-d4)δ=7.77-7.28(m,4H),4.68-4.15(m,4H),3.27-3.11(m,1H),2.73-2.48(m,5H),2.38-2.17(m,1H),2.16-0.71(m,4H);LC/MS:m/z计算值:737.4,实测值:738.4(M+1)+。实施例39:化合物804-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-1-乙酰氧基-2-((3-氯苄基)氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。按照类似于实施例16的方式,制备标题化合物的TFA盐。试验性地指定立体化学为绘图形式,但没有利用光谱方法充分证实。1HNMR(500MHz,氯仿-d)δ=7.43(s,1H),7.42-7.32(m,3H),5.81(d,J=10.1Hz,1H),4.49(dd,J=5.5,10.2Hz,1H),4.24(d,J=13.2Hz,1H),4.13-3.96(m,1H),3.34-3.04(m,2H),3.05-2.82(m,2H),2.75-2.62(m,1H),2.62-2.52(m,1H),2.37(d,J=18.0Hz,1H),1.93(s,3H),1.90-0.65(m,47H);LC/MS:m/z计算值:779.5,实测值:780.3(M+1)+。实施例40:化合物814-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-1-乙酰氧基-2-((3-氯苄基)氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。按照类似于实施例16的方式,制备标题化合物的TFA盐。试验性地指定立体化学为绘图形式,但没有利用光谱方法充分证实。1HNMR(500MHz,氯仿-d)δ=9.77(br.s.,1H),7.50-7.09(m,4H),5.87(br.s.,1H),4.57-4.44(m,1H),4.12(d,J=1.6Hz,1H),3.96(d,J=13.2Hz,1H),3.23-3.00(m,1H),2.86-2.37(m,5H),2.20-0.66(m,50H);LC/MS:m/z计算值:779.5,实测值:780.2(M+1)+。实施例41:化合物824-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-1-乙酰氧基-2-((3-氯苄基)(2-(二甲基氨基)乙基)氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。按照类似于实施例18的方式,制备标题化合物的TFA盐。向2-(二甲基氨基)乙醛(553mg,4.47mmol)的甲醇(10mL)溶液中加入4-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-1-乙酰氧基-2-((3-氯苄基)氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸三氟乙酸盐(80)(400mg,0.447mmol)。将该反应混合物在40℃下搅拌2小时。将该反应冷却至室温,并加入NaBH3CN(281mg,4.47mmol)。将该混合物搅拌过夜。然后真空浓缩,并用制备HPLC纯化,得到4-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-1-乙酰氧基-2-((3-氯苄基)(2-(二甲基氨基)乙基)氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸(82)(80mg,20%)浅黄色固体。试验性地指定立体化学为绘图形式,但没有利用光谱方法充分证实。LC/MS:m/z计算值:850.5,实测值:851.5(M+1)+。实施例42和43:化合物83和844-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-1-乙酰氧基-2-((3-氯苄基)(2-(二甲基氨基)乙基)氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸(83)和4-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-((3-氯苄基)(乙基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸(84)。向2-(二甲基氨基)乙醛,盐酸盐(553mg,4.47mmol)的甲醇(10mL)溶液中加入(3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-(4-氯苄基氨基)乙酰基)-9-羟基-1-异丙基-5a,5b,8,8,11a-五甲基-3a,4,5,5a,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十六氢-3H-环戊二烯并[a]-2(5bH)-酮(81)(15g,24.66mmol)。将该反应混合物在40℃下搅拌2小时。将该反应冷却至室温,加入氰基硼氢化钠(7.75g,123mmol),并将得到的混合物搅拌过夜。将该反应用氯化铵溶液(40mL)稀释,并用DCM(60mLx3)提取。将合并的有机层用盐水(20mL)洗涤,用硫酸钠干燥,过滤,真空浓缩,得到粗品,将粗品用制备HPLC纯化,得到4-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-1-乙酰氧基-2-((3-氯苄基)(2-(二甲基氨基)乙基)氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸(83)(80mg,20%)和4-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-((3-氯苄基)(乙基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸(84)(14mg,3%)的它们相应的TFA盐。试验性地指定立体化学为绘图形式,但没有利用光谱方法充分证实。对于83:1HNMR(500MHz,氯仿-d)δ=7.25-7.10(m,3H),7.04(d,J=3.8Hz,1H),5.57(d,J=9.1Hz,1H),4.42(dd,J=5.0,10.7Hz,1H),3.72(d,J=13.9Hz,1H),3.42(d,J=14.2Hz,1H),3.16-2.90(m,6H),2.90-2.79(m,1H),2.79-2.65(m,7H),2.65-2.41(m,3H),2.22(d,J=18.3Hz,1H),1.89(s,3H),1.84-0.62(m,45H);LC/MS:m/z计算值:850.5,实测值:851.4(M+1)+。对于84:1HNMR(400MHz,甲醇-d4)=7.65(s,1H),7.62-7.46(m,3H),4.58-4.28(m,4H),3.49-3.38(m,1H),3.31-3.23(m,2H),3.13-2.91(m,2H),2.62(q,J=15.9Hz,2H),2.10-0.76(m,51H);LC/MS:m/z计算值:765.5,实测值:766.5(M+1)+。实施例44:化合物854-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-2-((3-氯苄基)(2-(二甲基氨基)乙基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。按照类似于实施例33的方式,制备标题化合物。试验性地指定立体化学为绘图形式,但没有利用光谱方法充分证实。1HNMR(400MHz,甲醇-d4)δ=7.57-7.31(m,4H),4.50(dd,J=5.0,11.0Hz,1H),4.28(br.s.,1H),4.02-3.69(m,2H),3.53-3.36(m,1H),3.32-3.07(m,4H),3.08-2.85(m,2H),2.78(s,6H),2.73-2.51(m,3H),2.45(d,J=18.3Hz,1H),2.13-0.75(m,46H);LC/MS:m/z计算值:808.5,实测值:809.5(M+1)+。实施例45:化合物864-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-((3-氯苄基)(2-(二甲基氨基)乙基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。按照类似于实施例33的方式,制备标题化合物。试验性地指定立体化学为绘图形式,但没有利用光谱方法充分证实。1HNMR(400MHz,甲醇-d4)δ=7.46-7.23(m,4H),4.49(dd,J=5.1,10.9Hz,1H),4.19(d,J=10.0Hz,1H),3.95-3.78(m,1H),3.78-3.66(m,1H),3.41-3.33(m,1H),3.27-3.00(m,3H),2.87(s,6H),2.70-2.50(m,3H),2.37(br.s.,1H),2.34-2.16(m,3H),2.08-0.82(m,46H);LC/MS:m/z计算值:808.5,实测值:809.5(M+1)+。实施例46:化合物874-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-(N-(3-氯苄基)乙酰胺基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。按照类似于实施例33的方式,由化合物81制备标题化合物。试验性地指定立体化学为绘图形式,但没有利用光谱方法充分证实。该化合物以旋转异构体的混合物形态存在。1HNMR(400MHz,甲醇-d4)δ=7.42-7.04(m,4H),5.42-3.97(m,3H),3.55-3.00(m,3H),2.82-0.79(m,53H);LC/MS:m/z计算值:779.5,实测值:780.3(M+1)+。实施例47:化合物884-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-2-(N-(3-氯苄基)乙酰胺基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。按照类似于实施例33的方式,由化合物80制备标题化合物。试验性地指定立体化学为绘图形式,但没有利用光谱方法充分证实。1HNMR(400MHz,甲醇-d4)δ=7.36-6.99(m,4H),4.89-3.88(m,4H),3.39-2.83(m,3H),2.73-0.66(m,53H);LC/MS:m/z计算值:779.5,实测值:780.3(M+1)+。实施例48和49化合物89和904-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-1-乙酰氧基-2-((2-氯苄基)(2-(二甲基氨基)乙基)氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸(89)和4-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-((2-氯苄基)(乙基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸(90)。按照类似于实施例42和43的方式,制备标题化合物。试验性地指定立体化学为绘图形式,但没有利用光谱方法充分证实。对于89:1HNMR(400MHz,氯仿-d)δ=7.42-7.18(m,4H),5.70-5.56(m,1H),4.57-4.42(m,1H),3.83-3.51(m,2H),3.21-2.85(m,3H),2.79(s,6H),2.74-2.54(m,3H),2.54-2.23(m,4H),2.15-0.65(m,50H);LC/MS:m/z计算值:850.5,实测值:851.4(M+1)+。对于90:1HNMR(400MHz,甲醇)δ=7.77-7.43(m,4H),4.69-4.27(m,4H),3.62-3.37(m,2H),3.26-3.10(m,1H),2.97-2.82(m,1H),2.61(q,J=16.0Hz,2H),2.27-2.10(m,1H),2.10-0.77(m,51H);LC/MS:m/z计算值:765.5,实测值:766.3(M+1)+。实施例50:化合物914-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-((2-氯苄基)(2-(二甲基氨基)乙基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。按照类似于实施例33的方式,制备标题化合物。试验性地指定立体化学为绘图形式,但没有利用光谱方法充分证实。1HNMR(400MHz,甲醇-d4)δ=7.55-7.42(m,2H),7.42-7.32(m,2H),4.49(dd,J=5.5,11.0Hz,1H),4.43-4.30(m,1H),4.00-3.89(m,1H),3.87-3.76(m,1H),3.42-3.34(m,1H),3.24-2.91(m,3H),2.91-2.51(m,10H),2.52-2.17(m,4H),2.11-1.84(m,2H),1.84-0.78(m,44H);LC/MS:m/z计算值:808.5,实测值:809.4(M+1)+。实施例51:化合物924-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-2-((2-氯苄基)(2-(二甲基氨基)乙基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。按照类似于实施例33的方式,制备标题化合物。试验性地指定立体化学为绘图形式,但没有利用光谱方法充分证实。1HNMR(400MHz,甲醇)δ=7.57-7.45(m,2H),7.39(dd,J=3.6,5.6Hz,2H),4.56-4.40(m,2H),4.02(d,J=12.8Hz,1H),3.81(d,J=12.8Hz,1H),3.46-3.23(m,2H),3.13-2.89(m,4H),2.81-2.41(m,10H),2.15-1.91(m,3H),1.89-0.82(m,44H);LC/MS:m/z计算值:808.5,实测值:809.5(M+1)+。实施例52:化合物934-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-1-乙酰氧基-2-(苄基氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。按照类似于实施例16的方式,制备标题化合物的TFA盐。试验性地指定立体化学为绘图形式,但没有利用光谱方法充分证实。1HNMR(500MHz,DMSO-d6)δ=12.17(br.s.,1H),9.49(br.s.,1H),9.19(br.s.,1H),7.66-7.28(m,5H),5.86-5.53(m,1H),4.49-3.97(m,3H),3.16-2.84(m,2H),2.68-2.55(m,1H),2.55-2.47(m,2H),2.41(d,J=19.5Hz,1H),2.11(s,3H),2.04-0.67(m,47H);LC/MS:m/z计算值:745.5,实测值:746.5(M+1)+。实施例53:化合物944-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-1-乙酰氧基-2-(苄基氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。按照类似于实施例16的方式,制备标题化合物的TFA盐。试验性地指定立体化学为绘图形式,但没有利用光谱方法充分证实。1HNMR(500MHz,氯仿-d)δ=7.41(br.s.,5H),5.81(d,J=10.1Hz,1H),4.48(dd,J=5.5,10.2Hz,1H),4.25(d,J=13.2Hz,1H),4.06(d,J=13.2Hz,1H),3.27(d,J=12.3Hz,1H),3.14(dt,J=6.8,13.6Hz,1H),3.08-2.85(m,2H),2.74-2.62(m,1H),2.62-2.54(m,1H),2.36(d,J=18.0Hz,1H),1.99-0.63(m,49H);LC/MS:m/z计算值:745.5,实测值:746.5(M+1)+。实施例54:化合物954-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-((3-氯-2-氟苄基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。按照类似于实施例14的方式,制备标题化合物的TFA盐。试验性地指定立体化学为绘图形式,但没有利用光谱方法充分证实。LC/MS:m/z计算值:755.4,实测值:756.3(M+1)+。实施例55:化合物964-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-2-((3-氯-2-氟苄基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。按照类似于实施例14的方式,制备标题化合物的TFA盐。试验性地指定立体化学为绘图形式,但没有利用光谱方法充分证实。LC/MS:m/z计算值:755.4,实测值:756.2(M+1)+。实施例56:化合物974-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-((3-氯-2-氟苄基)(2-(二甲基氨基)乙基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。按照类似于实施例18的方式,制备标题化合物的TFA盐。试验性地指定立体化学为绘图形式,但没有利用光谱方法充分证实。1HNMR(500MHz,氯仿-d)δ=7.49-7.35(m,2H),7.15(t,J=7.7Hz,1H),4.46(dd,J=6.1,9.9Hz,1H),4.22(d,J=10.4Hz,1H),4.05(d,J=13.9Hz,1H),3.90(d,J=13.6Hz,1H),3.48(br.s.,1H),3.32-3.02(m,4H),2.85(br.s.,6H),2.74-2.40(m,4H),2.40-2.15(m,3H),1.99-0.58(m,43H);LC/MS:m/z计算值:826.5,实测值:827.3(M+1)+。实施例57:化合物984-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-2-((3-氯-2-氟苄基)(2-(二甲基氨基)乙基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。按照类似于实施例18的方式,制备标题化合物的TFA盐。试验性地指定立体化学为绘图形式,但没有利用光谱方法充分证实。1HNMR(500MHz,氯仿-d)δ=7.56-7.32(m,2H),7.16(t,J=7.7Hz,1H),4.53-4.38(m,1H),4.28(d,J=9.1Hz,1H),4.13-3.87(m,2H),3.44(br.s.,1H),3.33-2.91(m,5H),2.93-2.21(m,11H),2.09-1.95(m,1H),1.95-0.65(m,45H);LC/MS:m/z计算值:826.5,实测值:827.3(M+1)+。实施例58:化合物994-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-1-羟基-2-(异丙胺基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。按照类似于实施例18的方式,制备标题化合物的TFA盐。试验性地指定立体化学为绘图形式,但没有利用光谱方法充分证实。1HNMR(400MHz,氯仿-d)δ=10.30(br.s.,1H),4.71-4.26(m,2H),3.49-2.98(m,2H),2.87-2.42(m,6H),2.42-2.21(m,1H),2.07-0.68(m,53H);LC/MS:m/z计算值:655.5,实测值:656.5(M+1)+。实施例59:化合物1004-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-(环己基氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。按照类似于实施例18的方式,制备标题化合物的TFA盐。试验性地指定立体化学为绘图形式,但没有利用光谱方法充分证实。1HNMR(400MHz,氯仿-d)δ=10.25(br.s.,1H),7.12(br.s.,1H),4.67-4.34(m,2H),3.29-3.03(m,1H),2.92(br.s.,1H),2.83-2.42(m,6H),2.42-2.26(m,1H),2.11-0.72(m,55H);LC/MS:m/z计算值:695.5,实测值:696.4(M+1)+。实施例60和61:化合物111和1124-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-3-(1-(5-氯嘧啶-2-基)环丙基)-2-氧代噁唑烷-5-基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸(111)和4-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-3-(1-(5-氯嘧啶-2-基)环丙基)-2-氧代噁唑烷-5-基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸(112)。步骤A:中间体101(3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((1,3-二噻烷-2-基)(羟基)甲基)-9-羟基-1-异丙基-5a,5b,8,8,11a-五甲基-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-2-酮。在氮气氛围中,在-40℃,向1,3-二噻烷(5.7g,47.4mmol)的无水四氢呋喃(THF,60mL)溶液中慢慢地加入n-BuLi溶液(27mL,67.5mmol)。将该反应混合物在-20℃下再搅拌2小时之后,在氮气氛围中,在-70℃,慢慢地加入中间体6(4.2g,8.46mmol)的无水THF(40mL)溶液。然后,将该反应在-78℃下搅拌1小时,而后用饱和NaHCO3溶液淬灭。用EtOAc提取,用水(50mL)、饱和盐水(50mL)洗涤有机相,用硫酸钠干燥,减压蒸发,提供粗品,将粗品用硅胶柱色谱纯化(PE:EtOAc=8:1至4:1),得到中间体101(3.0g,5.22mmol,61.7%)。LC/MS:m/z计算值:574.4,实测值:575.0(M+1)+。步骤B:中间体102乙酸(3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(乙酰氧基(1,3-二噻烷-2-基)甲基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基酯。在室温下,向中间体101(3.5g,6.09mmol)、Et3N(2.55mL,18.26mmol)和DMAP(0.149g,1.218mmol)的DCM(40mL)溶液中加入Ac2O(3.45mL,36.5mmol)。在50℃下搅拌2小时之后,用水淬灭该反应混合物。用水(100mL)洗涤有机相,用硫酸钠干燥,减压蒸发,提供中间体102(3.41g,85%)。LC/MS:m/z计算值:658.4,实测值:659.1(M+1)+。步骤C:中间体103乙酸(3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((1,3-二噻烷-2-基)(羟基)甲基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基酯。在室温下,将102(6.7g,10.17mmol)和氢氧化钾(1.141g,20.33mmol)在1:1甲苯和乙醇的混合物(100ml)中的溶液强力搅拌1小时。用1NHCl水溶液将该反应混合物中和至pH7,并减少体积至干燥。将残余物在硅胶上纯化,使用石油醚/EtOAc(5:1),得到乙酸(3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((1,3-二噻烷-2-基)(羟基)甲基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基酯(103)(3.4g,5.01mmol,49%)浅黄色化合物。LC/MS:m/z计算值:616.4,实测值:617.3(M+1)+。步骤D:中间体104乙酸(3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(1-羟基-2-氧代乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基酯。向在空气氛围中、在室温下搅拌的103(1.2g,1.945mmol)的乙腈(20mL)和水(5.00mL)溶液中一次性加入NBS(1.385g,778mmol)。将该反应混合物在室温下搅拌0.5小时,然后用Na2SO3(固体)淬灭,浓缩,并用EtOAc提取残余物。用水和饱和盐水洗涤有机相,用硫酸钠干燥,真空浓缩,得到乙酸(3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(1-羟基-2-氧代乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基酯(104)(1.09g,1.083mmol,55.7%产率)浅黄色固体,其不用进一步纯化就使用。步骤E:中间体106乙酸(3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-((1-(5-氯嘧啶-2-基)环丙基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基酯。向乙酸(3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(1-羟基-2-氧代乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基酯(104)(545mg,1.035mmol)和1-(5-氯嘧啶-2-基)环丙胺盐酸盐(105)(213mg,1.035mmol)的甲醇(5mL)和1,2-二氯乙烷(5mL)溶液中加入氯化锌(141mg,1.035mmol)。将该反应混合物在室温下搅拌过夜,而后加入氰基硼氢化钠(65.0mg,1.035mmol)。将该反应混合物搅拌1小时,然后将硅胶加入到该混合物中,真空除去溶剂,得到残余物-硅胶粉末,将其在硅胶柱上纯化,使用石油醚/EtOAc(5:1至3:1),得到非对映体混合物形式的(3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-((1-(5-氯嘧啶-2-基)环丙基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基乙酸酯(105)(200mg,0.166mmol,16.04%产率)黄色泡沫体。LC/MS:m/z计算值:679.4,实测值:680.3(M+1)+。步骤F:中间体107(3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(3-(1-(5-氯嘧啶-2-基)环丙基)-2-氧代噁唑烷-5-基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基乙酸酯。向在室温下搅拌的乙酸(3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-((1-(5-氯嘧啶-2-基)环丙基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基酯(106)(400mg,0.588mmol)的二氯甲烷(15mL)溶液中加入BOC2O(1.365mL,5.88mmol)。将该反应混合物在室温下搅拌过夜,然后减压蒸发,并对残余物进行硅胶色谱,使用石油醚/EtOAc(6:1至3:1),得到乙酸(3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(3-(1-(5-氯嘧啶-2-基)环丙基)-2-氧代噁唑烷-5-基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基酯(107)(350mg,0.496mmol,84%产率)白色固体。步骤G:中间体1083-(1-(5-氯嘧啶-2-基)环丙基)-5-((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-9-羟基-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-3a-基)噁唑烷-2-酮。向乙酸(3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(3-(1-(5-氯嘧啶-2-基)环丙基)-2-氧代噁唑烷-5-基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7ja,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基酯(107)(350mg,0.496mmol)的1,4-二噁烷(10mL)和甲醇(5mL)溶液中加入盐酸(5mL,165mmol)。将该反应混合物在40℃搅拌过夜。减压除去溶剂,并接纳在DCM(100mL)中,用饱和NaHCO3(20mL)、水(20mL)和盐水(20mL)洗涤,用硫酸钠干燥,过滤,浓缩,得到残余物,对其进行硅胶柱处理,用石油醚/EtOAc(6:1至3:1)洗脱,得到3-(1-(5-氯嘧啶-2-基)环丙基)-5-((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-9-羟基-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-3a-基)噁唑烷-2-酮(130mg,0.087mmol,17%)白色固体。LC/MS:m/z计算值:663.4,实测值:664.3(M+1)+。步骤H:中间体109和1102,2-二甲基琥珀酸1-叔丁基4-((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-3-(1-(5-氯嘧啶-2-基)环丙基)-2-氧代噁唑烷-5-基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)酯(109)和2,2-二甲基琥珀酸1-叔丁基4-((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-3-(1-(5-氯嘧啶-2-基)环丙基)-2-氧代噁唑烷-5-基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)酯(110)。将4-叔丁氧基-3,3-二甲基-4-氧代丁酸10(119mg,0.587mmol)、3-(1-(5-氯嘧啶-2-基)环丙基)-5-((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-9-羟基-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-3a-基)噁唑烷-2-酮(108)(130mg,0.196mmol)、EDC(188mg,0.978mmol)和DMAP(71.7mg,0.587mmol)的混合物在DCM(5mL)中、在室温下搅拌过夜。反应完成之后,用DCM(25ml)稀释该混合物,用水(2x15ml)和盐水(20ml)洗涤,用硫酸钠干燥,过滤,减压浓缩。用硅胶色谱纯化残余物,使用石油醚/EtOAc(6:1至3:1)作为洗脱液,得到两个非对映产物2,2-二甲基琥珀酸1-叔丁基4-((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-3-(1-(5-氯嘧啶-2-基)环丙基)-2-氧代噁唑烷-5-基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)酯(109)和2,2-二甲基琥珀酸1-叔丁基4-((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-3-(1-(5-氯嘧啶-2-基)环丙基)-2-氧代噁唑烷-5-基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)酯(110)白色固体,数量为:(80mg,45%)和(50mg,22%)。没有指定每个非对映体的立体化学。化合物A(试验性地指定为109):LC/MS:m/z计算值:847.5,实测值:848.3(M+1)+。化合物B(试验性地指定为110):LC/MS:m/z计算值:847.5,实测值:848(M+1)+。步骤I:化合物1114-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-3-(1-(5-氯嘧啶-2-基)环丙基)-2-氧代噁唑烷-5-基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。向2,2-二甲基琥珀酸1-叔丁基4-((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-3-(1-(5-氯嘧啶-2-基)环丙基)-2-氧代噁唑烷-5-基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)酯(109)(80mg,0.094mmol)的DCM(10mL)溶液中加入TFA(1mL,0.094mmol)。将该反应混合物在室温下搅拌过夜,然后用DCM(20ml)稀释,用水(2x15ml)、饱和碳酸氢钠溶液(20ml)和盐水(20ml)洗涤,用硫酸钠干燥,过滤,浓缩,得到残余物。将残余物在硅胶上纯化,使用石油醚/EtOAc(4:1至1:1)作为洗脱液,得到产物4-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-3-(1-(5-氯嘧啶-2-基)环丙基)-2-氧代噁唑烷-5-基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸(111)(50mg,67%)白色固体。将该物质冷冻干燥,得到白色粉末。试验性地指定立体化学为绘图形式,但没有利用光谱方法充分证实。1HNMR(400MHz,氯仿-d)δ=8.58(s,2H),5.04(t,J=8.5Hz,1H),4.51(dd,J=4.6,10.9Hz,1H),3.41-3.04(m,4H),2.75-2.44(m,3H),2.36(d,J=13.3Hz,1H),2.12-0.72(m,49H);LC/MS:m/z计算值:791.4,实测值:792.3(M+1)+。步骤J:化合物1124-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-3-(1-(5-氯嘧啶-2-基)环丙基)-2-氧代噁唑烷-5-基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。按照类似于化合物111所描述的方式,制备标题化合物。试验性地指定立体化学为绘图形式,但没有利用光谱方法充分证实。1HNMR(400MHz,氯仿-d)δ=8.59(s,2H),5.10(t,J=8.8Hz,1H),4.52(dd,J=5.3,10.8Hz,1H),3.70-3.54(m,2H),3.28-3.10(m,2H),3.08-2.92(m,2H),2.77-2.53(m,2H),2.14-0.58(m,49H);LC/MS:m/z计算值:791.4,实测值:792.3(M+1)+。实施例62:化合物1244-(((3aS,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-2-((4-氯苄基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。步骤A:中间体113乙酸(3aS,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(羟甲基)-1-异丙基-5a,5b,8,8,11a-五甲基-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基酯。向中间体3(5g,7.59mmol)的EtOH(100mL)和甲苯(100mL)溶液中加入KOH(0.51g,9.11mmol)。在室温下搅拌4小时之后,将该反应混合物在水(500mL)和EtOAc(500mL)之间分配。用水(200mLx3)、盐水(100mL)洗涤有机相,并用硫酸钠干燥。除去溶剂,提供残余物,将其用硅胶柱色谱纯化(Hex:EtOAc=6:1至4:1),得到中间体113(2.5g,67.9%)白色固体。1HNMR(400Hz,CDCl3)δppm4.50-4.67(1H,m),3.68(1H,d,J=10.4Hz),3.32(1H,d,J=10.4Hz),3.23-3.15(1H,m),2.42-2.28(3H,m),2.05(3H,s),2.02-1.89(2H,m),1.77-0.83(40H,m)。步骤B:中间体114乙酸(3aS,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-甲酰基-1-异丙基-5a,5b,8,8,11a-五甲基-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基酯。在室温下,向中间体113(3g,6.19mmol)的DCM(75mL)溶液中加入PCC(4g,18.57mmol)和硅胶(3.0g)。在室温下搅拌2小时之后,用水(100mL)淬灭该反应。分离有机相,用饱和碳酸氢钠(50mL)洗涤,用硫酸钠干燥,真空浓缩,提供残余物,将其用硅胶柱色谱纯化(Hex:EtOAc=10:1),得到中间体114(3g,100%)白色固体。1HNMR(400Hz,CDCl3)δppm9.43(1H,s),4.50-4.46(1H,m),3.25-3.21(1H,m),2.43-2.02(5H,m),2.04(3H,m),2.00-1.93(1H,m),1.75-0.81(38H,m)。步骤C:中间体115乙酸(3aS,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(1-羟基-2-硝基乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基酯。向中间体114(5g,10.36mmol)的MeNO2(128mL,2382mmol)溶液中加入Et3N(10.11mL,72.5mmol)。在60℃搅拌过夜之后,将该反应混合物在水和EtOAc(各自100mL)之间分配。用水(20mLx3)、盐水(20mL)洗涤有机相,并用硫酸钠干燥。除去溶剂,提供残余物,将其用硅胶柱色谱纯化(Hex:EtOAc=10:1至6:1),得到中间体115(2.8g,49.7%)白色粉末。LC/MS:m/z计算值:543.4,实测值:566.3(M+Na+)+。步骤D:中间体116乙酸(3aS,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-氨基-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基酯。在0℃,向中间体115(2.8g,5.15mmol)的MeOH(166mL)溶液中加入氯化镍(II)(1.67g,12.87mmol)和硼氢化钠(4.87g,129mmol)。在0℃下搅拌10分钟之后,将该反应混合物在水和EtOAc(各自200mL)之间分配,并将有机相用水(100mLx3)、盐水(50mL)洗涤,用硫酸钠干燥。除去溶剂,提供中间体116(2.65g,100%)固体。LC/MS:m/z计算值:513.4,实测值:514.3(M+1)+。步骤E:中间体118乙酸(3aS,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-((叔丁氧羰基)(4-氯苄基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基酯。向中间体116(350mg,0.613mmol)和4-氯苯甲醛(86mg,0.613mmol)的MeOH(15mL)和二氯乙烷(DCE,15mL)溶液中加入氯化锌(50.1mg,0.368mmol)。将该反应混合物在80℃下搅拌1小时并冷却至室温之后,加入氰基硼氢化钠(57.8mg,0.92mmol)。将得到的混合物在室温下再搅拌1小时,提供中间体117。向上面获得的反应混合物中加入Et3N(0.18mL,1.38mmol)和二碳酸二叔丁基酯(0.157mL,0.674mmol)。在室温下搅拌30分钟之后,将该反应混合物在水(20mL)和EtOAc(100mL)之间分配。用水(30mLx3)、盐水(20mL)洗涤有机相,并用硫酸钠干燥。除去溶剂,提供残余物,将其用硅胶柱色谱纯化(Hex:EtOAc=15:1),得到中间体118(125mg,27.6%)白色固体。步骤F:中间体119乙酸(3aS,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-((叔丁氧羰基)(4-氯苄基)氨基)乙酰基)-1-异丙基-5a,5b,8,8,11a-五甲基-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基酯。向中间体118(120mg,0.162mmol)的DCM(10mL)溶液中加入PCC(35mg,0.162mmol)和硅胶(100mg)。在室温下搅拌2小时之后,过滤除去不溶性物质,并将滤液浓缩,得到中间体119(110mg,92%)白色固体。步骤G:中间体1204-氯苄基(2-((3aS,5aR,5bR,7aR,9S,11aR,11bR,13aS)-9-羟基-1-异丙基-5a,5b,8,8,11a-五甲基-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-3a-基)-2-氧代乙基)氨基甲酸叔丁基酯。向NaOH(597mg,14.94mmol)的MeOH(1mL)、THF(1mL)和水(0.5mL)溶液中加入中间体119(110mg,0.149mmol)。在室温下搅拌1小时之后,用水(20mL)稀释该反应,并用EtOAc(50mL)提取。用盐水(20mL)洗涤有机相,用硫酸钠干燥,真空蒸发,得到中间体120(100mg,96%)白色固体。步骤H:中间体1212,2-二甲基琥珀酸4-((3aS,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-((叔丁氧羰基)(4-氯苄基)氨基)乙酰基)-1-异丙基-5a,5b,8,8,11a-五甲基-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)1-叔丁基酯。向在室温下搅拌的4-叔丁氧基-3,3-二甲基-4-氧代丁酸10(1.648g,8.15mmol)、DMAP(0.995g,8.15mmol)的DCM(15ml)溶液中加入EDCl(2.60g,13.58mmol)。将该反应混合物在室温下搅拌2小时。然后,将4-氯苄基(2-((3aS,5aR,5bR,7aR,9S,11aR,11bR,13aS)-9-羟基-1-异丙基-5a,5b,8,8,11a-五甲基-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-3a-基)-2-氧代乙基)氨基甲酸叔丁基酯120(1.886g,2.72mmol)加入到该反应中。将该反应混合物在室温下搅拌过夜。完成后,用水(25mLx2)和盐水洗涤该混合物,用硫酸钠干燥,通过短硅胶柱过滤,真空蒸发,得到粗品,将粗品在硅胶柱上进一步纯化,使用石油醚/EtOAc(50:1至10:1),得到中间体121(2.37g,99%)白色泡沫体。步骤I:中间体122和1232,2-二甲基琥珀酸4-((3aS,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-2-((叔丁氧羰基)(4-氯苄基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)1-叔丁基酯(122)和2,2-二甲基琥珀酸4-((3aS,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-((叔丁氧羰基)(4-氯苄基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)1-叔丁基酯(123)。向在0℃搅拌的2,2-二甲基琥珀酸4-((3aS,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-((叔丁氧羰基)(4-氯苄基)氨基)乙酰基)-1-异丙基-5a,5b,8,8,11a-五甲基-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)1-叔丁基酯(121)(791mg,0.90mmol)的MeOH(10mL)和THF(10.00mL)溶液中加入NaBH4(170mg,4.50mmol)。将该反应混合物在室温下搅拌2小时,直到起始原料消失为止。完成后,加入硅胶,并将该混合物蒸干,用硅胶色谱纯化(石油醚/EtOAc,40:1至10:1),得到两个非对映的产物:2,2-二甲基琥珀酸4-((3aS,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-2-((叔丁氧羰基)(4-氯苄基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)1-叔丁基酯和2,2-二甲基琥珀酸4-((3aS,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-((叔丁氧羰基)(4-氯苄基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)1-叔丁基酯。没有证实立体化学,但制备的非对映体白色泡沫体的数量为:410mg,52%,试验性地指定为化合物122,以及77mg,10%,试验性地指定为化合物123。步骤J:化合物1244-(((3aS,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-2-((4-氯苄基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。向122(410mg,0.466mmol)的DCM(10mL)溶液中加入TFA(2mL,26.0mmol)。将该反应混合物在室温下搅拌2小时。将该反应混合物浓缩至干,用制备HPLC纯化,得到4-(((3aS,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-2-((4-氯苄基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸三氟乙酸盐(124)(185mg,0.221mmol,47.4%产率)白色固体。1HNMR(500MHz,氯仿-d)δ=7.36(q,J=8.5Hz,4H),4.58-4.41(m,1H),4.41-4.31(m,1H),4.20-3.97(m,2H),3.23-3.05(m,2H),2.85-2.66(m,2H),2.56(d,J=16.1Hz,1H),2.51-2.38(m,1H),2.34-2.19(m,2H),1.93-1.82(m,1H),1.83-0.67(m,46H);LC/MS:m/z计算值:723.5,实测值:724.3(M+1)+。实施例63:化合物1324-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-(3,4-二氢异喹啉-2(1H)-基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。步骤A:中间体125乙酸(3aS,5aR,5bR,7aR,9S,11aR,11bR,13aS)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3a-乙烯基-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基酯。向冷的(-78℃)甲基三苯基溴化鏻(8.63g,24.16mmol)的THF(30mL)溶液中逐滴加入二(三甲硅烷基)氨基锂(4.4g,24.1mmol)/THF。将该反应在-78℃下搅拌1小时,然后加入6(10.0g,20.1mmol)/THF(60ml)。将该混合物升温至室温,搅拌1小时。TLC显示反应完成。将2NHCl加入到该混合物中,并用乙酸乙酯提取,用水和盐水洗涤。用Na2SO4干燥有机相,而后过滤,浓缩,而后用5%EtOAc/石油醚沉淀出目标产物(10g,85%纯度,85%化学产率)。步骤B:中间体126(3aS,5aR,5bR,7aR,9S,11aR,11bR,13aS)-9-羟基-1-异丙基-5a,5b,8,8,11a-五甲基-3a-乙烯基-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-2-酮。向在室温下搅拌的125(16g,32.3mmol)的1,4-二噁烷(300mL)和MeOH(30ml)溶液中加入HCl(37%)(150mL,32.3mmol)。将该反应混合物在60℃下搅拌3小时。TLC和LCMS显示起始原料完全耗尽。加入水,并将挥发物浓缩,过滤所得到的沉淀,并用水洗涤。干燥滤饼,得到126(14g,81%)。步骤C:中间体1272,2-二甲基琥珀酸1-叔丁基4-((3aS,5aR,5bR,7aR,9S,11aR,11bR,13aS)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3a-乙烯基-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)酯。向10(14.52g,71.8mmol)、DMAP(10.52g,86mmol)和126(13g,28.7mmol)的二氯甲烷(150mL)溶液中加入EDC(27.5g,144mmol)。将该混合物在室温下搅拌2小时,此时,TLC显示反应完成。用2NHCl和盐水洗涤该反应。用Na2SO4干燥有机物,过滤,浓缩。用硅胶色谱纯化残余物,得到127(9.5g,49%),以及额外的4g不纯产物,其需要再纯化,而后再使用。步骤D:中间体128和1292,2-二甲基琥珀酸1-叔丁基4-((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-1-异丙基-5a,5b,8,8,11a-五甲基-3a-((S)-氧杂环丙烷-2-基)-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)酯(128)和2,2-二甲基琥珀酸1-叔丁基4-((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-1-异丙基-5a,5b,8,8,11a-五甲基-3a-((R)-氧杂环丙烷-2-基)-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)酯(129)。在室温下,向127(8.5g,13.34mmol)的DCM(90mL)溶液中加入m-CPBA(5.42g,26.7mmol)。将该反应混合物在室温下搅拌过夜。将该混合物用150mlDCM进一步稀释,然后用饱和NaHCO3、水和盐水洗涤(由于安全原因应注意,应该中和过量的过氧化物,但不是在该特定方法中进行)。浓缩有机相,用硅胶色谱纯化(EtOAc/PE,5%至15%),得到128(2.0g,21%)和129(800mg,8%)以及2.4g回收的起始原料。对于128:1HNMR(500MHz,氯仿-d)=4.51(dd,J=5.4,11.3Hz,1H),3.26-3.12(m,3H),2.66(t,J=4.4Hz,1H),2.54(s,2H),2.35(dd,J=2.7,4.6Hz,1H),2.18(d,J=18.3Hz,1H),2.12-1.93(m,3H),1.91-0.74(m,52H);LC/MS:m/z计算值:652.5,实测值:653.3(M+1)+。对于129:1HNMR(500MHz,氯仿-d)δ=4.51(dd,J=5.0,11.3Hz,1H),3.26-3.07(m,2H),3.00(dd,J=3.2,12.6Hz,1H),2.69(t,J=4.3Hz,1H),2.59-2.41(m,3H),2.21-0.76(m,56H);LC/MS:m/z计算值:652.5,实测值:653.3(M+1)+。步骤E:中间体1312,2-二甲基琥珀酸1-叔丁基4-((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-(3,4-二氢异喹啉-2(1H)-基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)酯。向2,2-二甲基琥珀酸1-叔丁基4-((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-1-异丙基-5a,5b,8,8,11a-五甲基-3a-((R)-氧杂环丙烷-2-基)-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)酯(0.2g,0.306mmol)的叔丁醇(3mL)溶液中加入1,2,3,4-四氢异喹啉(0.408g,3.06mmol)。将该反应混合物在100℃下搅拌5小时。完成后,冷却,加入EtOAc,并将该混合物用4NHCl和盐水洗涤,然后用Na2SO4干燥,过滤,浓缩,得到132(200mg,66%),其不用进一步纯化就使用。LC/MS:m/z计算值:785.6,实测值:786.5(M+1)+。步骤F:化合物1324-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-(3,4-二氢异喹啉-2(1H)-基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。向131(0.2g,0.254mmol)的DCM(2mL)溶液中加入TFA(1mL,12.98mmol)。将该反应混合物在室温下搅拌1小时,然后浓缩。用制备HPLC纯化残余物,得到标题化合物的TFA盐(106mg,48%)白色固体。1HNMR(500MHz,甲醇-d4)δ=7.43-7.15(m,4H),4.66-4.41(m,4H),3.28-3.05(m,3H),3.05-2.83(m,2H),2.73-2.52(m,3H),2.30(d,J=13.9Hz,1H),2.16-2.03(m,1H),2.00-0.72(m,48H);LC/MS:m/z计算值:729.5,实测值:730.5(M+1)+。按照类似于上述实施例的方式,或通过所述方法的组合或再排序,和/或,使用本领域技术人员熟知的其它方法,制备下面的实施例。实施例64:化合物1334-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-2-(3,4-二氢异喹啉-2(1H)-基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。试验性地指定立体化学为绘图形式,但没有利用光谱方法充分证实。LC/MS:m/z计算值:729.5,实测值:730.5(M+1)+。实施例65:化合物1344-(((3aS,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-1-羟基-2-(4-甲基哌嗪-1-基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。分离为非对映体的混合物。LC/MS:m/z计算值:682.53,实测值:683.5(M+1)+。实施例66:化合物1354-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-((4-氯苄基)氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:707.5,实测值:708.3(M+1)+。实施例67:化合物1364-(((3aS,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-2-((环己基甲基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。试验性地指定立体化学为绘图形式,但没有利用光谱方法充分证实。LC/MS:m/z计算值:695.6,实测值:696.5(M+1)+。实施例68:化合物1374-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-2-(环己基氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。试验性地指定立体化学为绘图形式,但没有利用光谱方法充分证实。LC/MS:m/z计算值:695.5,实测值:696.5(M+1)+。实施例69:化合物1384-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-2-(苄基(2-(二甲基氨基)乙基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。试验性地指定立体化学为绘图形式,但没有利用光谱方法充分证实。LC/MS:m/z计算值:774.6,实测值:775.5(M+1)+。实施例70:化合物1394-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-1-乙酰氧基-2-((2-(二甲基氨基)乙基)(4-氟苄基)氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。试验性地指定立体化学为绘图形式,但没有利用光谱方法充分证实。LC/MS:m/z计算值:834.6,实测值:835(M+1)+。实施例71:化合物1404-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-1-乙酰氧基-2-((2-(二甲基氨基)乙基)(4-氟苄基)氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。试验性地指定立体化学为绘图形式,但没有利用光谱方法充分证实。LC/MS:m/z计算值:834.6,实测值:835(M+1)+。实施例72:化合物1415-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-((4-氯苄基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-3,3-二甲基-5-氧代戊酸。试验性地指定立体化学为绘图形式,但没有利用光谱方法充分证实。LC/MS:m/z计算值:751.5,实测值:752.3(M+1)+。实施例73:化合物1425-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-2-((4-氯苄基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-3,3-二甲基-5-氧代戊酸。试验性地指定立体化学为绘图形式,但没有利用光谱方法充分证实。LC/MS:m/z计算值:751.5,实测值:752.3(M+1)+。实施例74:化合物1434-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-2-((2,4-二氯苄基)(2-(二甲基氨基)乙基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。试验性地指定立体化学为绘图形式,但没有利用光谱方法充分证实。LC/MS:m/z计算值:842.5,实测值:843.3(M+1)+。实施例75:化合物1444-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-(苄基(2-(二甲基氨基)乙基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。试验性地指定立体化学为绘图形式,但没有利用光谱方法充分证实。LC/MS:m/z计算值:774.6,实测值:775.4(M+1)+。实施例76:化合物1454-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-((2-(二甲基氨基)乙基)(4-氟苄基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。试验性地指定立体化学为绘图形式,但没有利用光谱方法充分证实。LC/MS:m/z计算值:792.5,实测值:793.5(M+1)+。实施例77:化合物1464-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-((4-氟苄基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。试验性地指定立体化学为绘图形式,但没有利用光谱方法充分证实。LC/MS:m/z计算值:721.5,实测值:722.3(M+1)+。实施例78:化合物1474-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-2-((2-(二甲基氨基)乙基)(4-氟苄基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。试验性地指定立体化学为绘图形式,但没有利用光谱方法充分证实。LC/MS:m/z计算值:792.5,实测值:793.5(M+1)+。实施例79:化合物1484-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-2-((4-氟苄基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。试验性地指定立体化学为绘图形式,但没有利用光谱方法充分证实。LC/MS:m/z计算值:721.5,实测值:722.3(M+1)+。实施例80:化合物1494-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-((2,4-二氯苄基)(2-(二甲基氨基)乙基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。试验性地指定立体化学为绘图形式,但没有利用光谱方法充分证实。LC/MS:m/z计算值:842.5,实测值:843.5(M+1)+。实施例81:化合物1504-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-(4-氯-N-(2-(二甲基氨基)乙基)苯甲酰胺基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。试验性地指定立体化学为绘图形式,但没有利用光谱方法充分证实。LC/MS:m/z计算值:822.5,实测值:823.4(M+1)+。实施例82:化合物1514-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-((2-氯苄基)氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:721.5,实测值:722.3(M+1)+。实施例83:化合物1524-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-苯甲酰胺基乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:701.5,实测值:702.5(M+1)+。实施例84:化合物1534-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((((R)-1-(4-氯苯基)乙基)氨基)甲基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:721.5,实测值:722.3(M+1)+。实施例85:化合物1544-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((N-(4-氯苄基)乙酰胺基)甲基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:749.4,实测值:750.3(M+1)+。实施例86:化合物1554-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(((4-氯苄基)氨基)甲基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:707.4,实测值:708.3(M+1)+。实施例87:化合物1564-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((N-(4-氯代苯乙基)乙酰胺基)甲基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:763.5,实测值:764.3(M+1)+。实施例88:化合物1574-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(((4-氯代苯乙基)氨基)甲基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:721.5,实测值:722.3(M+1)+。实施例89:化合物1584-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-((4-氯苄基)(3-甲氧基丙基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:809.50,实测值:810.7(M+1)+。实施例90:化合物1594-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-2-((4-氯苄基)(3-甲氧基丙基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:809.5,实测值:810.4(M+1)+。实施例91:化合物1604-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-((4-氯苄基)(2-甲氧基乙基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:795.5,实测值:796.3(M+1)+。实施例92:化合物1614-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-2-((4-氯苄基)(2-甲氧基乙基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:795.5,实测值:796.3(M+1)+。实施例93:化合物1624-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-2-(4-氯-N-(2-(二甲基氨基)乙基)苯甲酰胺基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:822.5,实测值:823.5(M+1)+。实施例94:化合物1634-(((3aS,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-((4-氯苄基)(2-(二甲基氨基)乙基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:794.5,实测值:795.5(M+1)+。实施例95:化合物1644-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-((4-氯苄基)((R)-吡咯烷-2-基甲基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:820.5,实测值:821.5(M+1)+。实施例96:化合物1654-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-2-((4-氯苄基)((R)-吡咯烷-2-基甲基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:820.5,实测值:821.5(M+1)+。实施例97:化合物1664-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-((4-氯苄基)(2-羟乙基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:781.5,实测值:782.5(M+1)+。实施例98:化合物1674-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-4-(4-氯苄基)-5,6-二氧代吗啉-2-基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:791.4,实测值:792.5(M+1)+。实施例99:化合物1684-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-2-(((5-氯代吡啶-2-基)甲基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:738.4,实测值:739.5(M+1)+。实施例100:化合物1694-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-4-(4-氯苄基)-5-氧代吗啉-2-基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:777.4,实测值:778.6(M+1)+。实施例101:化合物1704-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-4-(4-氯苄基)-6-氧代吗啉-2-基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:777.4,实测值:777.9(M+1)+。实施例102:化合物1714-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-4-(4-氯苄基)-5-氧代吗啉-2-基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:777.4,实测值:777.9(M+1)+。实施例103:化合物1724-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-(((5-氯代吡啶-2-基)甲基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:737.4,实测值:739.4(M+1)+。实施例104:化合物1734-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-2-((4-氯苄基)(2-羟乙基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:781.5,实测值:782.3(M+1)+。实施例105:化合物1744-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(((4-氯苄基)(2-(二甲基氨基)乙基)氨基)甲基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:778.5,实测值:779.5(M+1)+。实施例106:化合物1754-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(((4-氯代苯乙基)(2-(二甲基氨基)乙基)氨基)甲基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:792.5,实测值:793.5(M+1)+。实施例107:化合物1764-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-2-(N-(4-氯苄基)-2-(二甲基氨基)乙酰胺基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:822.5,实测值:823.5(M+1)+。实施例108:化合物1774-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-(N-(4-氯苄基)-2-(二甲基氨基)乙酰胺基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:822.5,实测值:823.5(M+1)+。实施例109:化合物1784-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-((4-氯苄基)(2-(吡咯烷-1-基)乙基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:834.5,实测值:835.5(M+1)+。实施例110:化合物1794-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-2-((4-氯苄基)(2-(吡咯烷-1-基)乙基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:834.5,实测值:835.5(M+1)+。实施例111:化合物1804-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-((4-氯苄基)(2-(甲基氨基)乙基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:794.5,实测值:795.4(M+1)+。实施例112:化合物1814-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-2-((2-氨基乙基)(4-氯苄基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:780.5,实测值:781.4(M+1)+。实施例113:化合物1824-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-((2-氨基乙基)(4-氯苄基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:780.5,实测值:781.4(M+1)+。实施例114:化合物1834-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-2-((4-氯苄基)(2-(甲基氨基)乙基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:794.5,实测值:795.5(M+1)+。实施例115:化合物1844-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-((4-氯苄基)(2-(N-甲基乙酰胺基)乙基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:836.5,实测值:837.5(M+1)+。实施例116:化合物1854-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-2-((4-氯苄基)(2-(N-甲基乙酰胺基)乙基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:836.5,实测值:837.5(M+1)+。实施例117:化合物1864-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-2-(((S)-1-(5-氯代吡啶-2-基)乙基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:752.5,实测值:753.4(M+1)+。实施例118:化合物1874-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-(((S)-1-(5-氯代吡啶-2-基)乙基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:752.5,实测值:753.4(M+1)+。实施例119:化合物1884-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-((2-(二甲基氨基)乙基)(苯乙基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:788.6,实测值:789.5(M+1)+。实施例120:化合物1894-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-2-(环己基(2-(二甲基氨基)乙基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:766.6,实测值:767.6(M+1)+。实施例121:化合物1904-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-(环己基(2-(二甲基氨基)乙基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:766.6,实测值:767.6(M+1)+。实施例122:化合物1914-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-2-(((5-氯代吡啶-2-基)甲基)(2-(二甲基氨基)乙基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:809.5,实测值:810.5(M+1)+。实施例123:化合物1924-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-(N-(4-氯苄基)-2-(二甲基氨基)乙酰胺基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:806.5,实测值:807.4(M+1)+。实施例124:化合物1934-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-(2-氨基-N-(4-氯苄基)乙酰胺基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:778.5,实测值:779.4(M+1)+。实施例125:化合物1944-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-(N-(4-氯苄基)-2-(甲基氨基)乙酰胺基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:792.5,实测值:793.4(M+1)+。实施例126:化合物1954-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-2-(((S)-2-(二甲基氨基)-1-苯基乙基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:760.5,实测值:761.5(M+1)+。实施例127:化合物1964-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-(((R)-2-(二甲基氨基)-1-苯基乙基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:760.5,实测值:761.5(M+1)+。实施例128:化合物1974-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-(((R)-2-(二甲基氨基)-1-苯基乙基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:760.5,实测值:761.5(M+1)+。实施例129:化合物1984-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-((4-氯苄基)(3-(二甲基氨基)丙基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:822.5,实测值:823.5(M+1)+。实施例130:化合物1994-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-2-((4-氯苄基)(3-(二甲基氨基)丙基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:822.5,实测值:823.5(M+1)+。实施例131:化合物2004-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3a-(2-(苯乙基氨基)乙基)-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:701.5,实测值:702.5(M+1)+。实施例132:化合物2014-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-((2-(二甲基氨基)乙基)(异丙基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:726.5,实测值:727.5(M+1)+。实施例133:化合物2022-(((R)-2-((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-9-((3-羧基-3-甲基丁酰基)氧基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-3a-基)-2-羟乙基)(4-氯苄基)氨基)-N,N,N-三甲基乙铵三氟乙酸盐。LC/MS:m/z计算值:823.5,实测值:823.5(M)+。实施例134:化合物2034-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-4-(4-氯苄基)-6-氧代吗啉-2-基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:777.4,实测值:778.4(M+1)+。实施例135:化合物2044-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-(((S)-2-(二甲基氨基)-1-苯基乙基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:760.5,实测值:761.4(M+1)+。实施例136:化合物2054-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-2-((2-(二甲基氨基)乙基)(异丙基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:726.6,实测值:727.5(M+1)+。实施例137:化合物2064-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-(((5-氯代吡啶-2-基)甲基)(2-(二甲基氨基)乙基)氨基)-1-羟乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:809.5,实测值:810.5(M+1)+。实施例138:化合物2074-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-1-羟基-2-(异丙胺基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:655.5,实测值:656.4(M+1)+。实施例139:化合物2084-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-(((R)-2-(二甲基氨基)-1-苯基乙基)氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:744.5,实测值:745.5(M+1)+。实施例140:化合物2094-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-(2-(((S)-2-(二甲基氨基)-1-苯基乙基)氨基)乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:744.5,实测值:745.5(M+1)+。实施例141:化合物2102-(((S)-2-((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-9-((3-羧基-3-甲基丁酰基)氧基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-3a-基)-2-羟乙基)(4-氯苄基)氨基)-N,N,N-三甲基乙铵三氟乙酸盐。LC/MS:m/z计算值:823.5,实测值:823.5(M)+。实施例142:化合物2114-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-4-(4-氯苄基)-6-氧代哌嗪-2-基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:776.5,实测值:777.4(M+1)+。实施例143:化合物2124-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-4-(4-氯苄基)-1-甲基-6-氧代哌嗪-2-基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:790.5,实测值:791.4(M+1)+。实施例144:化合物2134-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((R)-2-((4-氯苄基)(2-(二甲基氨基)乙基)氨基)-1-甲氧基乙基)-1-异丙基-5a,5b,8,8,11a-五甲基-2-氧代-3,3a,4,5,5a,5b,6,7,7a,8,9,10,11,11a,11b,12,13,13a-十八氢-2H-环戊二烯并[a]-9-基)氧基)-2,2-二甲基-4-氧代丁酸。LC/MS:m/z计算值:822.5,实测值:823.5(M+1)+。实施例145:化合物2144-(((3aR,5aR,5bR,7aR,9S,11aR,11bR,13aS)-3a-((S)-1-羟基-2-(哌啶-1-基)乙基)-1-异丙基-5a,5b,8,8,1...
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1