具有增强的碳水化合物的高强度酸性Α‑葡糖苷酶的制作方法
相关申请的交叉引用
本申请要求2014年9月30日提交的美国临时62/057,842、2014年9月30日提交的美国临时62/057,847、2015年2月5日提交的美国临时62/112,463、以及2015年3月19日提交的美国临时62/135,345的优先权的权益,其中每个通过引用以其全部内容结合。
发明背景
发明领域
本发明涉及医学、遗传学和重组糖蛋白生物化学领域,并且具体地涉及重组人α葡糖苷酶(rhgaa)组合物,这些组合物具有较高总含量的带有甘露糖6-磷酸的聚糖,这些聚糖有效靶向肌细胞上的cimpr并随后将rhgaa递送至溶酶体,在该溶酶体中该rhgaa可分解异常高水平的累积的糖原。与常规rhgaa产品相比,本发明的rhgaa表现出优秀的对肌细胞的靶向和随后向溶酶体的递送,并且表现出使其对患有庞贝氏病(pompedisease)的受试者的酶替代疗法特别有效的其他药代动力学性质。
相关技术说明
针对庞贝氏病的现有酶替代疗法使用常规rhgaa产品,这些常规rhgaa产品具有低总含量的带有m6p和双-m6p的聚糖。已知
庞贝氏病是由于酸性α-葡糖苷酶(gaa)活性缺乏导致的遗传性溶酶体贮积症。患有庞贝氏病的人没有或具有降低水平的酸性α-葡糖苷酶(gaa),该酶分解糖原和身体用作能量源的物质。这种酶缺乏导致溶酶体中过量的糖原累积,这些溶酶体是包含通常分解糖原和其他细胞碎片或废物的酶的内细胞器。患有庞贝氏病的受试者的某些组织(尤其是肌肉)中的糖原累积损害了细胞正常运行的能力。在庞贝氏病中,在溶酶体中,特别是在骨骼肌细胞中,糖原没有适当地代谢并逐渐累积,并且在该疾病的婴儿发病形式中,在心肌细胞中,糖原没有适当地代谢并逐渐累积。糖原的积累损害肌细胞和神经细胞以及其他受影响的组织中的那些肌细胞和神经细胞。
传统上,取决于发病年龄,庞贝氏病在临床上被确认为是早期婴儿形式或晚期发病形式。发病年龄倾向于与导致庞贝氏病的遗传突变的严重性相应。最严重的基因突变导致gaa活性的完全丧失,显现为婴儿期的早发性疾病。减少gaa活性但不完全消除gaa活性的遗传突变与具有延迟发病和进展的庞贝氏病的形式相关。婴儿发病的庞贝氏病在出生后不久显现,并且其表征为肌无力、呼吸功能不全和心力衰竭。未经治疗,它通常在两年内是致命的。儿童和成人发病的庞贝氏病在生命晚期显现,并且通常进展比婴儿发病更慢。这种形式的疾病,虽然它通常不影响心脏,但由于骨骼肌和参与呼吸的那些肌肉的弱化,也可以导致死亡。
当前庞贝氏病的非姑息治疗涉及使用重组人gaa(rhgaa)如
发生这种状况是因为常规rhgaa缺乏高总含量的带有m6p和双-m6p的聚糖,这些聚糖将rhgaa分子靶向靶肌细胞上的cimpr,随后在这些靶肌细胞中将该rhgaa转运到细胞的溶酶体中。这种用于酶替代疗法的rhgaa的细胞摄取通过专门的碳水化合物(甘露糖-6-磷酸(m6p))进行促进,该m6p结合至存在于细胞表面上的阳离子非依赖性甘露糖6-磷酸受体(cimpr),用于随后将外源酶递送至溶酶体。
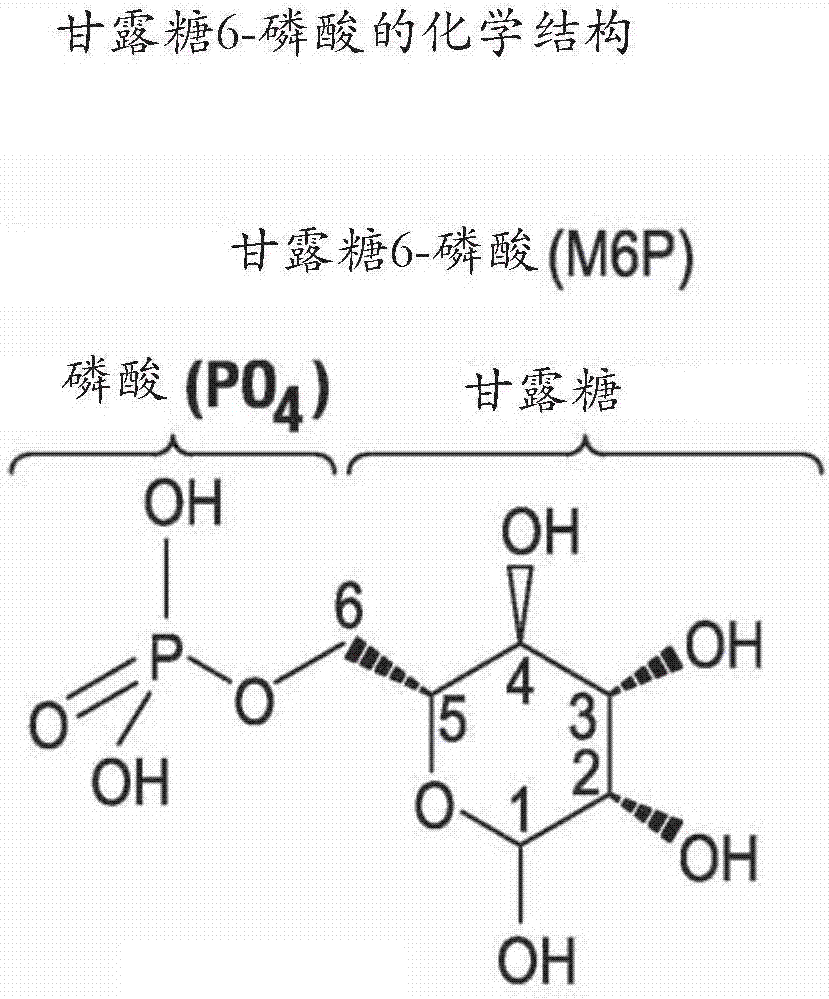
在rhgaa上存在七个潜在的n-联糖基化位点。由于每个糖基化位点在存在的n-联寡糖(n-聚糖)的类型中是异质的,所以rhgaa由具有n-聚糖的蛋白的复杂混合物组成,这些n-聚糖对m6p受体和其他碳水化合物受体具有不同结合亲和力。包含具有一个m6p基团(单-m6p)的高甘露糖n-聚糖的rhgaa以低(约6,000nm)亲和力结合至cimpr,而在相同n-聚糖上包含两个m6p基团(双-m6p)的rhgaa以高(约2nm)亲和力来结合。非磷酸化的、单-m6p、和双-m6p聚糖的代表性结构如图1a所示。甘露糖-6-p基团如图1b所示。一旦在溶酶体内,rhgaa可以酶促降解累积的糖原。然而,常规rhgaa具有低总水平的带有m6p和双-m6p的聚糖,并且因此靶向肌细胞很差,导致rhgaa至溶酶体的较差递送。这些常规产品中的大多数rhgaa分子不具有磷酸化的n-聚糖,从而缺乏对cimpr的亲和力。非磷酸化的高甘露糖聚糖也可以被甘露糖受体清除,该甘露糖受体导致ert的非生产性清除(图2)。
包含半乳糖和唾液酸的其他类型的n-聚糖、复合碳水化合物,也存在于rhgaa上。由于复合的n-聚糖没有被磷酸化,所以它们对cimpr没有亲和力。然而,具有暴露的半乳糖残基的复合型n-聚糖对肝脏肝细胞上的脱唾液酸糖蛋白受体具有中度至高度亲和力,这导致rhgaa的快速非生产性清除(图2)。
gaa或rhgaa的糖基化可以通过磷酸转移酶和坎菲尔德(canfield)等人,美国专利号6,534,300所描述的揭酶(uncoveringenzyme)在体外进行酶促修饰以产生m6p基团。酶糖基化不能被充分控制,并且产生具有不期望的免疫学性质和药理学性质的rhgaa。酶促修饰的rhgaa可以仅包含高-甘露糖n-聚糖,这些高甘露糖n-聚糖全部可以用磷酸转移酶/揭酶在体外潜在地进行酶促磷酸化,并且可以每个gaa包含平均5-6个m6p基团。通过对gaa进行体外酶处理而产生的糖基化模式是有问题的,因为额外的末端甘露糖残基,特别是非磷酸化的末端甘露糖残基负面影响经修饰的rhgaa的药代动力学。当在体内给予此类酶促修饰的产物时,这些甘露糖基团增加了gaa的非生产性清除,增加了免疫细胞对酶促修饰的gaa的摄取,并且由于更少的gaa到达靶组织(如心肌细胞或骨骼肌肌细胞)而降低了rhgaa治疗功效。例如,末端非磷酸化甘露糖残基是肝和脾中的甘露糖受体的已知配体,其导致酶促修饰的rhgaa的快速清除和rhgaa对靶组织的靶向降低。此外,具有含末端非磷酸化甘露糖残基的高甘露糖n-聚糖的酶促修饰的gaa的糖基化模式类似于酵母、霉菌和功能中产生的糖蛋白上的糖基化模式,这些酵母、霉菌和功能增加了引发对酶促修饰的rhgaa的免疫或过敏反应(如危及生命的严重过敏(过敏性)或超敏反应)的风险。
如上所解释的,常规rhgaa产品如
由于向溶酶体递送常规酶替代疗法的低效性,这些疗法通常与其他问题(包括产生对gaa的免疫反应)相关。大部分常规rhgaa中的gaa不包含带有单或双-m6p的聚糖,该单-或双-m6p使rhgaa靶向肌细胞。受试者的免疫系统暴露于这种过量的非磷酸化gaa,并且可以产生识别gaa的有害免疫反应。诱导对未进入靶组织并递送至溶酶体的非磷酸化gaa的免疫应答增加了由于给予的rhgaa的免疫失活而导致的治疗失败的风险,并增加了患者经历对rhgaa治疗的有害的自身免疫或过敏反应的风险。根据本发明所述的rhgaa包含显著更少的这种非靶向的、非磷酸化的rhgaa,从而减少患者的免疫系统对其的暴露。
在逻辑上,较大的剂量对受试者以及治疗受试者的医学专业人员施加额外的负担,如延长静脉内给予rhgaa所需的输注时间。这是因为常规rhgaa包含更高含量的非磷酸化rhgaa,其不靶向肌细胞上的cimpr。不结合肌细胞上的cimpr并且然后进入溶酶体的rhgaa不会在那里酶促降解糖原。当给予相等剂量的常规rhgaa和根据本发明所述的rhgaa时,根据本发明的组合物中的更多rhgaa结合肌细胞上的cimpr,并且然后递送至溶酶体。本发明的rhgaa为医生提供了给予较低量的rhgaa同时将相同或更多的rhgaa递送至溶酶体的选择。
用于制备常规rhgaa(如
发明概述
响应于与靶向和给予常规形式的rhgaa相关的问题以及响应于与产生这种良好靶向形式的rhgaa相关的困难,诸位发明人已调研并开发了用于制备更有效靶向cimpr并将rhgaa递送至肌肉组织中的溶酶体的rhgaa的程序,因为它比常规rhgaa组合物具有更高含量的m6p-聚糖和双-m6p聚糖。此外,本发明的rhgaa具有经过良好加工的复合型n-聚糖,其最小化非靶组织对rhgaa的非生产性清除。
考虑到与使用常规rhgaa产品(如
通过该方法产生的rhgaa凭借其总糖基化模式也具有有利的药代动力学性质,该模式增加靶组织摄取并且在向患有庞贝氏病的受试者给予后降低非生产性清除。诸位发明人显示,本发明的rhgaa,如通过命名为atb-200的rhgaa所例示的,在靶向骨骼肌组织方面比常规rhgaa(如
根据本发明的优异rhgaa可以被进一步完成或与分子伴侣组合或与靶向肌肉组织中的cimpr的其他基团(例如,结合该受体的igf2的部分)缀合。以下实例显示,与使用常规rhgaa产品
附图简要说明
本申请文件包含至少一幅彩绘的附图。
图1图1a示出非磷酸化高甘露糖聚糖、单-m6p聚糖、和双-m6p聚糖。图1b示出m6p基团的化学结构。
图2图2a描述了rhgaa经由带有m6p的聚糖对靶组织(例如,具有庞贝氏病的受试者的肌肉组织)的生产性靶向。图2b描述了对非靶组织(例如,肝和脾)或通过非m6p聚糖与非靶组织的结合的非生产性药物清除。
图3图3a图示了cimpr受体(又称igf2受体)和该受体的结构域。图3b是一张表,该表示出了带有双-和单-m6p的聚糖对cimpr的结合亲和力(纳摩尔)、高甘露糖型聚糖与甘露糖受体的结合亲和力、以及脱唾液酸化复合聚糖对去唾液酸糖蛋白受体的结合亲和力。具有带有m6p和双-m6p的聚糖的rhgaa可以生产性地结合至肌肉靶细胞上的cimpr。具有高甘露糖聚糖和脱唾液酸化聚糖的rhgaa可以非生产性地结合至带有相应受体的非靶细胞。
图4图4a和4b分别示出了
图5用于用编码rhgaa的dna转化cho细胞的dna构建体。用编码rhgaa的dna构建体(seqidno:4)转化cho细胞。
图6图6a和6b示出了myozyme和atb-200rhgaa的cimpr亲和色谱法的结果。如图6b所示,atb-200rhgaa中约70%的rhgaa包含m6p。
图7atb-200rhgaa纯化,实施例1和2。
图8
图9相比鉴定为bp-rhgaa、atb200-1和atb200-2的atb200rhgaa的三种不同的制剂,
图10图10a比较了atb-200rhgaa(左轨迹线)和
图11图11a比较了不同gaa浓度下,正常成纤维细胞内的atb-200rhgaa活性(左轨迹线)与
图12图12a示出在与载体(阴性对照),与20mg/ml阿葡糖苷酶α或与5mg/kg、10mg/kg或20mg/kgatb-200rhgaa接触后,相对于心肌中的蛋白的糖原的量。图12b示出在与载体(阴性对照),与20mg/ml
图13在分子伴侣at2221的存在下,atb-200rhgaa稳定性得到改进。图13a中的第一条左轨迹线示出在ph7.4(血液ph)下在各种温度下未折叠的atb-200rhgaa蛋白的百分比。最后一条右轨迹线示出在ph5.2(溶酶体ph)下在各种温度下未折叠的atb-200rhgaa蛋白的百分比。三个中间轨迹示出10μg、30μg或100μg的at2221分子伴侣对蛋白折叠的影响。这些数据示出与对照样品相比,在血液ph下,at2221防止atb-200rhgaa的解折叠。在中性ph下通过at2221的tm的改进总结在图13b中。
图14该表显示atb-200rhgaa和分子伴侣at2221的组合在gaa敲除小鼠中比用
图15在用lumizyme、atb-200rhgaa、或atb-200rhgaa以及各种浓度的at2221分子伴侣处理后的四头肌中的残留糖原。
图16用atb200+麦格司他(miglustat)(at2221)处理的小鼠的骨骼肌病理学的改进超过单独用ert处理的那些。来自用常规rhgaa或atb-200rhgaa和麦格司他(at-2221)处理的gaako小鼠的肌肉组织的pas糖原染色(图16a)和em(图16b)。图16c;通过lamp-1标志物进行的溶酶体增殖的评估。图16di型和ii型肌纤维的鉴定。
图17.用atb-200+麦格司他(at2221)处理的小鼠的骨骼肌病理学的改进超过单独用ert处理的那些。来自用常规rhgaa或atb-200rhgaa和麦格司他(at-2221)处理的gaako小鼠的肌肉组织的pas糖原染色(图17a)。图17b;通过lamp-1标志物进行的溶酶体增殖的评估。
发明详述
定义:在本发明的上下文中以及在每个术语使用的特定上下文中,在本说明书中使用的术语通常具有其在本领域中的一般含义。某些术语在下文或说明书中的其他地方讨论,以向从业者提供描述本发明的组合物和方法以及如何制作和使用它们的另外指导。
术语“gaa”是指人酸性α-葡糖苷酶(gaa)(催化溶酶体糖原的α-1,4-糖苷键和α-1,6-糖苷键的水解的酶),以及是指gaa氨基酸序列的插入、相关或取代变体以及发挥酶活性的更长gaa序列的片段。术语“rhgaa”用于区分内源性gaa与合成或重组产生的gaa,如通过用编码gaa的dna转化cho细胞产生的gaa。编码gaa的示例性dna序列是np_000143.2(seqidno:4),将其通过引用结合。gaa和rhgaa可以存在于一种组合物中,该组合物包含具有不同糖基化模式的gaa分子混合物,如在其聚糖上带有单-m6p或双-m6p基团的rhgaa分子和不带有m6p或双-m6p的gaa分子的混合物。也可以用其他化合物(如分子伴侣)完成gaa和rhgaa,或者可以与gaa或rhgaa缀合物中的其他部分结合,如结合到将该缀合物靶向cimpr并随后将其递送至溶酶体的igf2部分。
“受试者”或“患者”优选地是人,尽管也可以治疗患有涉及糖原累积的病症的其他哺乳动物和非人动物。受试者可以是患有庞贝氏病或其他糖原贮积或积累障碍的胎儿、新生儿、幼儿、儿童或成人。被治疗个体的一个实例是患有gsd-ii(例如婴儿gsd-ii、儿童gsd-ii、或成人发病gsd-ii)的个体(胎儿、新生儿、幼儿、儿童、青少年或成年人)。该个体可以具有残留的gaa活性,或没有可测量的活性。例如,患有gsd-ii的个体可以具有小于约1%正常gaa活性(婴儿gsd-ii)的gaa活性、约1%-10%正常gaa活性(儿童gsd-ii)的gaa活性、或约10%-40%正常gaa活性(成人gsd-ii)的gaa活性。
如本文所用的术语“治疗”(treat或treatment)是指与疾病相关的一种或多种症状的改善,预防或延迟疾病的一种或多种症状的发病,和/或减轻疾病的一种或多种症状的严重性或频率。例如,治疗可以是指心脏状况的改进(例如,舒张末期和/或收缩末期容积的增加,或者通常在gsd-ii中发现的进行性心肌病的减少、改善或预防)或肺功能的改进(例如,超过基线能力的啼哭肺活量的增加,和/或在啼哭期间氧脱饱和的正常化);神经发育和/或运动技能的改进(例如,aims评分的增加);受疾病影响的个体的组织中的糖原水平的降低;或这些效应的任何组合。在一个优选实施例中,治疗包括改进心脏状况,具体是减少或预防gsd-ii相关性心肌病。
如本文所用的术语“改进”、“增加”或“减少”表示相对于基线测量的值,该基线测量如在开始本文所述的治疗之前在相同个体中的测量,或在本文所述的治疗的不存在下在一个对照个体(或多个对照个体)中的测量。对照个体是患有与被治疗个体相同形式的gsd-ii(婴儿、儿童或成人发病)的个体,该对照个体与所治疗个体的年龄大约相同(以确保在治疗的个体和对照个体中的疾病阶段是可比较的)。
如本文所用的术语“纯化的”是指在减少或消除不相关材料即污染物(包括从中获得材料的天然材料)的存在的条件下分离的材料。例如,纯化的蛋白优选地是基本上不含与其在细胞中结合的其他蛋白或核酸,纯化的核酸分子优选地是基本上不含可以在细胞内与其一起发现的蛋白或其他不相关的核酸分子。如本文所用,在材料的分析测试的上下文中,在操作上使用术语“基本上不含”。优选地,基本上不含污染物的纯化材料是至少95%纯的;更优选地至少97%纯的,更优选地仍然至少99%纯的。可以通过色谱法、凝胶电泳、免疫测定、组合物分析、生物测定、酶法测定以及本领域已知的其他方法评估纯度。在具体实施例中,纯化的意指污染物水平低于管理机构可接受的用于对人或非人动物安全给予的水平。可以使用本领域已知的方法,包括通过色谱尺寸分离、亲和色谱法或阴离子交换色谱法,从cho细胞中分离或纯化重组蛋白。
术语“遗传修饰的”或“重组的”是指在引入包括编码基因产物的编码序列的核酸、连同控制编码序列表达的调节元件后,表达特定基因产物(如rhgaa或atb-200rhgaa)的细胞(如cho细胞)。核酸的引入可以通过本领域已知的任何方法来完成,包括基因靶向和同源重组。如本文所用,该术语还包括已经工程化(例如通过基因激活技术)以表达或过表达通常由这种细胞不能正常表达的内源基因或基因产物的细胞。
“庞贝氏病”是指以缺乏酸性α葡糖苷酶(gaa)活性为特征的常染色体隐性lsd,该常染色体隐性lsd损害溶酶体糖原代谢。酶缺乏导致溶酶体糖原累积,并导致进行性骨骼肌无力、心脏功能降低、呼吸功能不全、和/或疾病晚期的cns损伤。gaa基因中的遗传突变导致较低的表达或产生具有改变的稳定性和/或最终导致疾病的生物活性的酶的突变体形式。(通常参见,赫希霍恩(hirschhorn)r,1995,糖原贮积症ii型:酸性α-葡糖苷酶(酸性麦芽糖酶)缺乏(glycogenstoragediseasetypeii:acidα-glucosidase(acidmaltase)deficiency),遗传疾病的代谢和分子基础(themetabolicandmolecularbasesofinheriteddisease),斯克里维尔(scriver)等人编辑,麦格劳希尔出版社(mcgraw-hill),纽约,第7版,第2443-2464页)。庞贝氏病(婴儿、儿童和成人)的三种公认的临床形式与残留的α-葡糖苷酶活性水平相关(雷乌谢尔(reuser)aj等人,1995,糖原贮积病ii型(酸性麦芽糖酶缺乏症),肌肉和神经补充(muscle&nervesupplement)3,s61-s69)。婴儿庞贝氏病(i型或a型)是最常见和最严重的,特征是在生命的第二年内不能茁壮成长、全身性低渗、心脏肥大和心肺功能衰竭。儿童庞贝氏病(ii型或b型)的严重程度是中等的,并且特征在于没有心脏肥大的肌肉症状的优势。儿童庞贝氏病个体通常由于呼吸衰竭而在达到20岁之前死亡。成人庞贝氏病(iii型或c型)通常在青春期或最晚至第六十年呈现为缓慢进展性肌病(费利西亚(felicia)kj等人,1995,成人发病酸性麦芽糖酶缺乏症的临床变异:受影响同胞的报告和文学评论(clinicalvariabilityinadult-onsetacidmaltasedeficiency:reportofaffectedsibsandreviewoftheliterature),医学(medicine)74,131-135)。在庞贝中,已经显示α-葡糖苷酶在翻译后通过糖基化、磷酸化、以及蛋白水解加工而被大幅修饰。通过溶酶体中的蛋白水解将110千道尔顿(小孩)前体转化为76个和70个小孩成熟形式是最佳糖原催化所需的。如本文所用的,术语“庞贝氏病”是指所有类型的庞贝氏病。本申请中公开的配制品和给药方案可用于治疗例如i型、ii型或iii型庞贝氏病。
本发明的非限制性实施例
一种源自cho细胞的rhgaa组合物,该rhgaa组合物包含比通过
该rhgaa的氨基酸序列可以与seqidno:1、3或4所描述的氨基酸序列具有至少70%、75%、80%、85%、95%或99%一致性,或对于seqidno:1、3或4所描述的氨基酸序列包含1、2、3、4、5、6、7、8、9、10个或更多个缺失、取代或添加。在本发明的gaa或rhgaa的一些实施例中,如在atb-200rhgaa中,gaa或rhgaa将包括野生型gaa氨基酸序列,如seqidno:1或3的氨基酸序列。在其他非限制性实施例中,该rhgaa包括存在于野生型gaa中的氨基酸残基的子集,其中该子集包括野生型gaa的氨基酸残基,其形成用于底物结合和/或底物减少的活性位点。在一个实施例中,该rhgaa是葡糖苷酶α,其是人酶酸性α-葡糖苷酶(gaa),由该基因的最主要的九个观察到的单倍型编码。本发明的rhgaa,包括atb-200rhgaa,可以包括与人α葡糖苷酶的氨基酸序列有90%、95%、96%、97%、98%或99%一致的氨基酸序列,如通过登录号ahe24104.1(gi:568760974)(seqidno:1)给出的并且将其通过对美国专利号8,592,362或对np_000143.2的氨基酸序列(seqidno:4)的引用而结合的氨基酸序列。还分别通过seqidno:2和3给出gaa的核苷酸和氨基酸序列。该氨基酸序列的变体还包括对以下gaa氨基酸序列具有1、2、3、4、5、6、7、8、9、10、11、12个或更多个氨基酸缺失、插入或取代的那些。还考虑编码gaa和此类变体人gaa的多核苷酸序列,并且可以用于重组表达根据本发明所述的rhgaa。
可以使用不同比对算法和/或程序来计算两个序列之间的一致性,包括可用作gcg序列分析包(威斯康辛大学,麦迪逊市,威斯康辛州)的一部分的fasta或blast,并且可以与例如,默认设置一起使用。例如,考虑与本文所述的特定多肽具有至少70%、85%、90%、95%、98%或99%一致性,并且优选地表现出基本相同功能的多肽,连同编码此类多肽的多核苷酸。除非另有说明,相似性分数将基于blosum62的使用。当使用blastp时,相似性百分比是基于blastp阳性得分,并且序列一致性百分比是基于blastp一致性得分。blastp“一致性”示出相同的高分序列对中总残基的数量和分数;并且blastp“阳性”示出比对分数具有正值并且彼此相似的残基的数量和分数。本披露考虑和涵盖具有与本文披露的氨基酸序列具有这些程度的一致性或相似性或任何中间程度的一致性或相似性的氨基酸序列。使用遗传密码推导出的相似多肽的多核苷酸序列,并且可以通过常规手段(具体地通过使用遗传密码来逆转录其氨基酸序列)获得。
优选地,根据本发明的组合物中不超过70%、65%、60%、55%、45%、40%、35%、30%、25%、20%、15%、10%或5%的总rhgaa缺乏带有m6p或双-m6p的n-聚糖或缺乏结合阳离子非依赖性甘露糖-6-磷酸受体(cimpr)的能力。可替代地,组合物中30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%、99%、<100%或更多的rhgaa包括至少一个带有m6p和/或双-m6p的n-聚糖或具有结合cimpr的能力。
本发明的rhgaa组合物中的rhgaa分子可以在其聚糖上具有1、2、3或4个m6p基团。例如,在rhgaa分子上的唯一一个n-聚糖可以带有m6p(单-磷酸化的),单个n-聚糖可以带有两个m6p基团(双-磷酸化的),或在相同rhgaa分子上的两个不同n-聚糖可以带有单个m6p基团。rhgaa组合物中的rhgaa分子还可以具有不带有m6p基团的n-聚糖。在另一个实施例中,平均来说,这些n-聚糖包含大于3mol/mol的m6p和大于4mol/mol的唾液酸。平均来说,在rhgaa上的至少约3%、4%、5%、6%、7%、8%、9%,或10%的总聚糖可以处于单-m6p聚糖形式,例如,约6.25%的总聚糖可以携带单个m6p基团,并且平均来说,在rhgaa上的至少约0.5%、1%、1.5%、2.0%、2.5%、3.0%的总聚糖是处于双-m6p聚糖形式,并且平均来说,少于25%的本发明的总rhgaa不包含结合至cimpr的磷酸化的聚糖。
根据本发明所述的rhgaa组合物可以具有平均含量的携带m6p的n-聚糖,该平均含量范围从0.5至7.0mol/molrhgaa,或子范围的任何中间值,该子范围包括0.5、1.0、1.5、2.0、2.5、3.0、3.5、4.0、4.5、5.0、5.5、6.0、6.5或7.0mol/molrhgaa。如实例中所示,可以将本发明的rhgaa分级以提供在rhgaa上具有不同平均数量的带有m6p或带有双-m6p的聚糖的rhgaa组合物,从而通过选择特定级分或通过选择性地组合不同级分来允许进一步定制靶向靶组织中溶酶体的rhgaa。
可以将在rhgaa上高达60%的n-聚糖完全唾液酸化,例如,可以将高达10%、20%、30%、40%、50%或60%的n-聚糖完全唾液酸化。在一些实施例中,将rhgaa组合物中从4%至20%的总n-聚糖完全唾液酸化。
在其他实施例中,rhgaa上不多于5%、10%、20%或30%的n-聚糖携带唾液酸和末端gal。该范围包括所有中间值和子范围,例如组合物中rhgaa上的7%至30%的总n-聚糖可以携带唾液酸和末端gal。
在又其他实施例中,在rhgaa上不多于5%、10%、15%、16%、17%、18%、19%或20%的n-聚糖仅具有末端gal并且不包含唾液酸。该范围包括所有中间值和子范围,例如组合物中rhgaa上的从8%至19%的总n-聚糖可以仅具有末端gal并且不包含唾液酸。
在本发明的其他实施例中,组合物中rhgaa上的40%、45%、50%、55%至60%的总n-聚糖是复合型n-聚糖;或者组合物中rhgaa上的不多于1%、2%、3%、4%、5%、6%、7%的总n-聚糖是杂合型n-聚糖;组合物中rhgaa上的不多于5%、10%或15%的高甘露糖型n-聚糖是非磷酸化的;组合物中rhgaa上的至少5%或10%的高甘露糖型n-聚糖是单-m6p磷酸化的;和/或组合物中rhgaa上的至少1%或2%的高甘露糖型n-聚糖是双-m6p磷酸化的。这些值包括所有的中间值和子范围。根据本发明所述的rhgaa组合物可以满足上述的一个或多个含量范围。
在一些实施例中,本发明的rhgaa组合物将平均带有2.0至8.0个唾液酸残基/molrhgaa。该范围包括所有中间值和子范围,包括2.0、2.5、3.0、3.5、4.0、4.5、5.0、5.5、6.0、6.5、7.0、7.5和8.0个残基/molrhgaa。唾液酸残基可以防止脱唾液酸糖蛋白受体的非生产性清除。
本发明的rhgaa组合物优选地由cho细胞,如cho细胞系ga-atb-200,或由此类cho细胞培养物的次代培养物或衍生物产生。表达gaa的等位基因变体或其他变体gaa氨基酸序列(如与seqidno:1具有至少90%、95%或99%一致性的那些)的dna构建体可以在cho细胞中构建并表达。本领域普通技术人员可以选择适合于转化cho细胞用于产生此类dna构建体的替代载体。
诸位发明人已经发现,可以使用中国仓鼠卵巢(cho)细胞产生具有靶向cimpr和细胞溶酶体的优异能力的rhgaa以及降低其体内非生产性清除的糖基化模式。这些细胞可以被诱导以表达具有比常规rhgaa产品显著更高水平的总m6p和双-m6p的rhgaa。由这些细胞产生的重组人gaa,例如,如实例中描述的rhgaaatb-200所例示的,具有比常规gaa(如
根据本发明的rhgaa可以配制成药物组合物或用于生产用于治疗庞贝氏病或与缺乏gaa相关的其他病症的药物。这些组合物可以用生理学上可接受的载体或赋形剂来配制。该载体和组合物可以是无菌的,并且另外适合给予方式。
适合的药学上可接受的载体包括但不限于水、盐溶液(例如,nacl)、盐水、缓冲盐水、醇、甘油、乙醇、阿拉伯树胶、植物油、苄甲醇、聚乙二醇、明胶、碳水化合物(如乳糖、直链淀粉或淀粉)、糖(如甘露醇、蔗糖、或其他)、葡萄糖、硬脂酸镁、滑石、硅酸、脂肪酸酯、羟甲基纤维素、聚乙烯吡咯烷酮等、及其组合。如果需要,可以将该药物制剂与助剂,例如表面活性剂(如聚山梨醇酯,像聚山梨醇酯80)、润滑剂、防腐剂、稳定剂、润湿剂、乳化剂、用于影响渗透压的盐、缓冲液、着色剂、调味剂和/或芳香族物质等进行混合,这些助剂不与活性组合物发生有害反应。在优选实施例中,使用适合于静脉给予的水溶性载体。
如果需要,该组合物或药物还可以包含少量的润湿剂或乳化剂、或ph缓冲剂。该组合物可以是液体溶液、悬浮液、乳剂、片剂、丸剂、胶囊剂、缓释配制品或粉剂。还可利用常规粘合剂和载体如甘油三酯将该组合物配制为栓剂。口服配制品可以包括标准载体如药物级甘露醇、乳糖、淀粉、硬脂酸镁、聚乙烯吡咯烷酮、糖精钠、纤维素、碳酸镁等。在优选实施例中,通过静脉内输注给予该rhgaa。
可以根据常规程序将该组合物或药物配制为适合向人类给予的药物组合物。例如,在优选的实施例中,用于静脉内给予的组合物是在无菌等渗水缓冲液中的溶液。必要时,该组合物还可以包括增溶剂和局部麻醉剂以缓解注射部位的疼痛。通常,成分以单位剂量形式分开或混合在一起提供,例如,作为在气密封容器中的干燥冻干粉或无水浓缩物,气密封容器如指明活性剂的量的安瓿或小药囊。在通过输注给予组合物时,可以用包含无菌药用级的水,盐水或右旋糖/水的输液瓶进行分配。在通过注射给予组合物时,可以提供无菌注射用水或盐水的安瓿,这样使得可以在给予前将这些成分混合。
可以将该rhgaa配制成为中性或盐的形式。药学上可接受的盐包括与游离氨基基团形成的盐如源自盐酸、磷酸、乙酸、草酸、酒石酸等的那些,以及与游离羧基基团形成的盐如源自氢氧化钠、氢氧化钾、氢氧化铵、氢氧化钙、氢氧化铁、异丙胺、三乙胺、2-乙氨基乙醇、组氨酸、普鲁卡因等的那些。
通过适当的途径给予rhgaa(或包含gaa的组合物或药物)。在一个实施例中,静脉内给予该gaa。在其他实施例中,通过直接给予至靶组织(如至心脏或骨骼肌(例如,肌内))或神经系统(例如,直接注射到脑中;脑室内;鞘内)来给予gaa。如果需要,可以同时使用多于一个途径。
将该rhgaa(或包含gaa的组合物或药物)以治疗有效量给予(例如,当以规律间隔给予时,足以治疗疾病的剂量,如上文所述通过减轻与与疾病相关的症状,预防或延迟疾病的发病,和/或还减轻疾病的症状的严重性或频率)。在治疗疾病中治疗有效的量将取决于疾病影响的性质和程度,并且可以通过标准临床技术来确定。另外,可以任选地使用体外或体内测定来帮助鉴定最佳剂量范围。所使用的精确剂量还将取决于给予途径和疾病的严重程度,并且应根据从业者的判断和每个患者的情况来决定。有效剂量可以从源自体外或动物模型测试系统的剂量-反应曲线外推。在优选的实施例中,治疗有效量等于或小于20mg酶/kg个体体重,优选地在约1-10mg酶/kg体重的范围内,并且甚至更优选地是约10mg酶/kg体重或约5mg酶/kg体重。对具体个体的有效剂量可以是随着时间变化的(例如,增加的或减少的),这取决于该个体的需要。例如,在生理疾病或躯体应激的时候,或如果抗gaa抗体存在或增加,或如果疾病症状恶化,该量可以增加。
以规律的间隔给予治疗有效量的gaa(或包含gaa的组合物或药物),这取决于疾病影响的性质和程度,以及持续进行的基础。如本文中所使用,以“规律的间隔,”给予表示,将该治疗有效量定期地给予(如区别于一次性剂量)。该间隔可以通过标准临床技术来确定。在优选的实施例中,每月、每两个月;每周;每周两次;或每日给予gaa。单个个体的给予间隔不需要是固定的间隔,但是可以是随时间变化的,其取决于该个体的需要。例如,在生理疾病或躯体应激的时候,如果抗gaa抗体存在或增加,或如果疾病症状恶化,可以减小剂量之间的间隔。在一些实施例中,将5、10、20、50、100、或200mg酶/kg体重的治疗有效量以每周两次、每周或每隔一周,伴有或不伴有分子伴侣来给予。
本发明的gaa或rhgaa可以制备用于以后使用,如在单位剂量小瓶或注射器中,或在用于静脉给予的瓶或袋中。包含gaa或rhgaa的试剂盒连同任选的赋形剂或其他活性成分,如分子伴侣或或其他药物,可以封装在包装材料中,并且附有用于复水、稀释或定量给药的说明书,用于治疗对其有需要的受试者,如患有庞贝氏病的患者。
gaa(或包含gaa的组合物或药物)可以单独给予,或与其他试剂(如分子伴侣)联合给予。可以给予具有与单-m6p或双-m6p的不同糖基化程度的rhgaa或者给予具有不同程度的m6p或双-m6p糖基化的rhgaa的组合。
在一些实施例中,本发明的rhgaa组合物将与分子伴侣(例如at-2220或at-2221)复合或混合。分子伴侣,有时称为“药理分子伴侣”是当与rhgaa复合或共给予时改变其药代动力学和其他药理学性质的化合物。本文所例示的代表性分子伴侣包括at2221(麦格司他,n-丁基-脱氧野尻霉素)和at2220(duvoglustathcl,1-脱氧野尻霉素)。这种复合或混合可以发生在身体外部或身体内部,例如,其中给予单独剂量的rhgaa和分子伴侣。例如,可以通过将其与duvoglustat-hcl(at2220,脱氧野尻霉素,at2220)或麦格司他(at2221,n-丁基-脱氧野尻霉素)组合来改进本发明的活性rhgaa、其级分或衍生物对cimpr以及随后对细胞溶酶体的靶向。以下实例示出接受了与分子伴侣组合的本发明的良好靶向的rhgaa的敲除gaa的小鼠的关键骨骼肌中显著的糖原底物减少。
本发明的另一方面涉及产生根据本发明所述的rhgaa的cho细胞或其衍生物或其他等效物。此类cho细胞系的一个实例是产生如本文所述的rhgaa组合物的ga-atb-200或其次代培养物。此类cho细胞系可以包含编码gaa的多核苷酸的基因的多个拷贝,例如5、10、15或20或更多个拷贝。
本发明的高m6p和双-m6prhgaa(如atb-200rhgaa)可以通过用编码gaa的dna构建体转化cho细胞(中国仓鼠卵巢细胞)来产生。尽管cho细胞之前被用于制备rhgaa,但是没有意识到转化的cho细胞可以按产生具有高含量的靶向cimpr的m6p和双-m6p聚糖的rhgaa的方式进行培养和选择。
出人意料地,诸位发明人发现可以转化cho细胞系,选择产生rhgaa的转化体,该rhgaa包含高含量的带有靶向cimpr的m6p或双-m6p的聚糖,并稳定表达该高-m6prhgaa。因此,本发明的相关方面涉及用于制备这些cho细胞系的方法。该方法涉及用编码gaa或gaa变体的dna转化cho细胞,选择将编码gaa的dna稳定整合到其一个或多个染色体中并稳定表达gaa的cho细胞,并且选择表达具有高含量的带有m6p或双-m6p的聚糖的gaa的cho细胞,以及任选地选择具有含高唾液酸含量的n-聚糖,和/或具有含低非磷酸化的高-甘露糖含量的n-聚糖的cho细胞。
可以通过培养该cho细胞系,并且从cho细胞培养中回收所述的组合物,使用这些cho细胞系来产生根据本发明所述的rhgaa和rhgaa组合物。
通过给予该rhgaa组合物,有利地使用本发明的rhgaa组合物或其级分或衍生物来治疗患有与溶酶体gaa不足相关的病症、障碍或疾病的受试者。对治疗有需要的受试者包括患有糖原贮积症ii型(庞贝氏病)以及将受益于给予rhgaa的其他病症、障碍或疾病的那些。
以下实例示出当以比常规rhgaa产品显著更低的剂量给予时,本发明的rhgaa(atb-200)被骨骼肌细胞摄取,结合至cimpr,并且,有效地从骨骼肌细胞去除糖原。在敲除gaa小鼠中使用静脉内给予atb-200的每两周一次的方案,获得骨骼肌成肌细胞中高达75%的糖原的减少。这些减少超过由相同量的
它可用于降解、减少或去除来自心肌、平滑肌、或横纹肌的糖原。经受治疗的骨骼肌或横纹肌对象的实例包括选自下组的至少一种肌肉,该组由以下各项组成:小趾展肌(脚)、小指展肌(手)、拇展肌、拇短展肌、拇长展肌、内收短肌、跼收肌、长收肌、大收肌、拇收肌、肘肌、肘关节肌、膝关节肌、杓会厌肌(aryepiglotticus)、aryjordanicus、耳肌、肱二头肌、股二头肌、肱肌、肱桡肌、颊肌、球海绵体肌、咽下缩肌、咽中缩肌、咽上缩肌、喙肱肌、皱眉肌、提睾肌、环甲肌、肉膜、深横断会阴、三角肌、降口角肌、降下唇肌、膈肌、二腹肌、二腹肌(前视)、竖脊肌-棘肌、竖脊肌-髂肋肌、竖脊肌-最长肌、桡侧伸腕短肌、桡侧伸腕长肌、尺侧伸腕肌、小指伸肌(手)、指伸肌(手)、趾伸短肌(脚)、趾伸长肌(脚)、大拇趾伸长肌、食指伸肌(extensorindicis)、拇短伸肌、拇长伸肌、腹外斜肌、桡侧腕屈肌、尺侧腕屈肌、小趾短屈肌(脚)、小指短屈肌(手)、趾短屈肌、趾长屈肌(脚)、指深屈肌、指浅屈肌、屈姆短肌、屈姆长肌、拇短屈肌、拇长屈肌、额肌、腓肠肌、下孖肌、上孖肌、颏舌肌、颏舌骨肌、臀大肌、臀中肌、臀小肌、股薄肌、舌骨舌肌、髂肌、下斜肌、下直肌、冈下肌、肋间外肌、肋间深肌、肋间内肌、腹内斜肌、手背(interossei-dorsalofhand)、脚背(interossei-dorsaloffoot)、手掌、脚掌、横突间肌、舌的内附肌、坐骨海绵体肌、环杓侧肌、翼外肌、外直肌、背阔肌、提口角肌、肛提肌-尾骨肌、肛提肌-髂尾肌、肛提肌-耻尾肌、肛提肌-耻骨直肠肌、肛提肌-耻骨阴道肌、提上唇肌、提上唇肌、鼻翼(alaequenasi)、上睑提肌、肩胛提肌、腭帆提肌(levatorvelipalatine)、肋提肌、头长肌、颈长肌、脚蚓状肌(4)、手蚓状肌、咬肌、翼内肌、内直肌、颏肌、腭垂肌(m.uvulae)、下颌舌骨肌、鼻肌、杓斜肌、头下斜肌、头上斜肌、闭孔外肌、闭孔内肌(a)、闭孔内肌(b)、肩胛舌骨肌、小指对掌肌(手)、拇对掌肌、眼轮匝肌、口轮匝肌、腭舌肌、腭咽肌、掌短肌、掌长肌、耻骨肌、胸大肌、胸小肌、腓骨短肌、腓骨长肌、第三腓骨肌、梨状肌(a)、梨状肌(b)、跖肌、颈阔肌、腘肌、环杓后肌、降眉间肌、旋前方肌、旋前圆肌、腰大肌、腰小肌、锥状肌、股方肌、腰方肌、跖方肌、腹直肌、头前直肌(rectuscapitusanterior)、头后直肌、头后大直肌、头后小直肌、股直肌、大菱形肌、小菱形肌、笑肌、咽鼓管咽肌、缝匠肌、前斜角肌、中斜角肌、小斜角肌、后斜角肌、半膜肌、半腱肌、前锯肌、下后锯肌、上后锯肌、比目鱼肌、肛门括约肌、尿道括约肌、头夹肌、颈夹肌、镫骨肌、胸锁乳突肌、胸骨舌骨肌、胸骨甲状肌、茎突舌肌、茎突舌骨肌、茎突舌骨肌(前视)、茎突咽肌、锁骨下肌、肋下肌(subcostalis)、肩胛下肌、会阴浅横肌(superficialtransverseperinei)、上斜肌、上直肌、旋后肌、冈上肌、颞肌、颞顶肌、阔筋膜张肌、鼓膜张肌、腭帆张肌、大圆肌、小圆肌、甲杓肌和声带肌、甲状会厌肌(thyro-epiglotticus)、甲状舌骨肌、胫骨前肌、胫骨后肌、杓横肌、横向脊椎肌-多裂肌、横向脊椎肌-回旋肌、横向脊椎肌-半棘肌、腹横肌、胸横肌、斜方肌、三头肌、股中间肌、股外侧肌、股内侧肌、颧大肌、以及颧大肌。
本发明的gaa组合物还可以给予至或用于治疗1型(慢缩)肌纤维或2型(快缩)肌纤维或在这些肌纤维中累积糖原的受试者。i型,慢缩或“红”肌,富集毛细血管,并富含线粒体和肌红蛋白,这给出肌肉组织其特有的红色。它可以携带更多的氧气,并使用脂肪或碳水化合物作为燃料来维持需氧活动。慢缩肌纤维长时间收缩,但几乎没有力。ii型,快缩肌具有三种在收缩速度和产生的力两者方面都不同的主要亚型(iia、iix和iib)。快缩纤维快速并有力地收缩,但疲劳非常迅速,仅短暂维持,在肌肉收缩变得痛苦之前厌氧的活动爆发。它们最有助于肌肉强度,并且具有更大的质量增加的潜力。iib型是厌氧的、糖酵解的、是在线粒体和肌红蛋白方面密度最小的“白”肌。在小动物(例如,啮齿动物)中,这是主要快肌型,这解释了它们的肉的苍白的颜色。
可以系统性给予本发明的rhgaa组合物、其级分或衍生物,例如通过静脉内(iv)输注,或直接给予至所需部位,如进入心肌或骨骼肌(如四头肌、三头肌、或膈肌)。可以将它给予至肌细胞、特定肌肉组织、肌肉或肌肉群。例如,此类治疗可以将该rhgaa组合物肌肉内直接给予至受试者的四头肌或三头肌或膈肌。
如以上所提到的,可以将本发明的rhgaa组合物、其级分或衍生物与分子伴侣如at-2220(duvoglustathcl,1-脱氧野尻霉素)或at-2221(麦格司他,n-丁基-脱氧野尻霉素)或其盐进行复合或混合,以改进该rhgaa给予的药代动力学。该rhgaa和分子伴侣可以一起或分开地给予。当同时给予时,可以将该组合物中的gaa与分子伴侣一起预先装载。可替代地,该gaa和分子伴侣可以在同一时间或在不同时间分开给予。
at2221的代表性剂量范围是从0.25至400mg/kg,优选地是从0.5-200mg/kg,并且最优选是从2至50mg/kg。at2221的具体剂量包括1、2、3、4、5、10、15、20、25、30、35、40、45和50mg/kg。可以将这些剂量与rhgaa(如atb-200rhgaa)以范围从15:1至150:1的at2221与rhgaa的摩尔比进行组合。具体的比率包括15:1、20:1、25:1、50:1、60:1、65:1、70:1、75:1、80:1、85:1、90:1、100:1、125:1、和150:1。可以按这些量或摩尔比同时地、顺序地或分开地共同给予rhgaa和at2221。上述范围包括所有中间子范围和值,如范围端点之间的所有整数值。
at2220的代表性剂量范围是从0.1至120mg/kg,优选地是0.25至60mg/kg,并且最优选地是从0.6至15mg/kg。at2220的具体剂量包括1、2、3、4、5、6、7、8、9、10、15、20、25和30mg/kg。可以将这些剂量与rhgaa(如atb-200rhgaa)以范围从15:1至150:1的at2220与rhgaa的摩尔比进行组合。具体的比率包括15:1、20:125:1、50:1、60:1、65:1、70:1、75:1、80:1、85:1、90:1、100:1、125:1、和150:1。可以按这些量或摩尔比同时地、顺序地或分开地共同给予rhgaa和at2220。上述范围包括所有中间子范围和值,如范围端点之间的所有整数值。
还可以将本发明的rhgaa组合物、其级分或衍生物用于代谢、降解、去除或以其他方式减少组织、肌肉、肌肉纤维、肌细胞、溶酶体、细胞器、细胞区室、或细胞质中的糖原。通过向受试者给予该rhgaa组合物,任选地与分子伴侣或降低对rhgaa的免疫反应的药物一起给予。
在其使用方法的另一个实施例中,本发明的rhgaa可以通过将其、其级分或衍生物给予至需要这种调节的细胞、组织、或受试者来用于调节细胞中的溶酶体增殖、自噬或胞吐,任选与分子伴侣组合或任选地作为与另一靶向部分的缀合物。自噬是一种分解代谢机制,该机制允许细胞通过其溶酶体的作用降解糖原或其他不必要的或机能障碍的细胞组分。该方法还可涉及向需要治疗的受试者系统或局部给予该gaa组合物。
还可以将根据本发明所述的rhgaa(与
实例
以下非限制性实例例证了本发明的各个方面。
部分i:atb-200rhgaa及其性质
现有
为了评估rhgaa在
图5描述了与常规ert(
产生具有高含量的带有单-m6p或双-m6p的n-聚糖的atb-200rhgaa的cho细胞的制备。
用表达rh-gaa的dna转染cho细胞,随后选择产生rhgaa的转化体。用于用编码rh-gaa的dna转化cho细胞的dna构建体在图5中示出。用表达rh-gaa的dna转染cho细胞,随后选择产生rhgaa的转化体。
转染后,用次黄嘌呤/胸苷缺陷(-ht)培养基来选择包含稳定整合的gaa基因的dg44cho(dhfr-)细胞。通过甲氨蝶呤处理(mtx,500nm)来诱导在这些细胞中的gaa表达的扩增。通过gaa酶活性测定来鉴定表达大量gaa的细胞池,并用来建立产生rhgaa的单个克隆。在半固体培养基板上产生单个克隆,通过clonepix系统挑选,并且转移至24深孔板。针对gaa酶活性测定单个克隆,以鉴定表达高水平gaa的克隆。用于确定gaa活性的条件培养基使用了4-mu-α-葡糖苷酶底物。针对生存力、生长能力、gaa生产率、n-聚糖结构和稳定的蛋白表达来进一步评估如通过gaa酶测定所测量的产生更高水平的gaa的克隆。使用这一程序分离cho细胞系,包括表达具有增强的单-m6p或双-m6pn-聚糖的rhgaa的cho细胞系ga-atb-200。
rhgaaatb-200rhgaa的纯化
在摇瓶中产生根据本发明所述的多批次的rhgaa,并且在灌注生物反应器中使用cho细胞系ga-atb-200和cimpr来测量结合。针对来自不同生产批次的经纯化的atb-200rhgaa,观察到与在图6b和图7中所示那些相似的cimpr受体结合(约70%),表明可以一致地产生atb-200rhgaa。如图6a和6b所示,与atb200rhgaa相比,
atb-200与lumizyme的分析比较
根据末端磷酸根,使用弱阴离子交换(“wax”)液相色谱法,进行atb-200rhgaa的分级。通过用递增量的盐洗脱ert来产生洗脱曲线。通过uv(a280nm)监测该曲线。从cho细胞获得atb-200rhgaa,并且进行纯化。
atb-200rhgaa的寡糖表征
通过maldi-tof来评估经纯化的atb-200rhgaa和
atb-200的cimpr亲和力的表征
除了具有可以结合至cimpr的更大百分比的rhgaa之外,重要的是理解该相互作用的质量。使用cimpr板结合测定来确定
图10b示出了lumizyme、常规rhgaa、以及根据本发明所述的atb-200中的双-m6p聚糖的相对含量。对于
atb-200rhgaa比lumizyme更有效地被成纤维细胞内化。
使用正常的和庞贝氏成纤维细胞细胞系来比较atb-200和
还示出atb-200rhgaa在细胞中有效内化(图11a和11b),分别地示出atb-200rhgaa内化到正常的和庞贝氏成纤维细胞中,并且其比常规的
部分ii:临床前研究
具有优异的糖基化的atb-200rhgaa显著优于用于gaako小鼠的骨骼肌中的糖原清除的护理ert标准
如上所解释的,使用重组人gaa(rhgaa)的酶替代疗法(ert)是可用于庞贝氏病的唯一批准的治疗。该ert需要专门的碳水化合物甘露糖6-磷酸(m6p)用于细胞摄取并随后经由细胞表面阳离子非依赖性m6p受体(cimpr)递送至溶酶体。然而,目前的rhgaaert包含少量的m6p,这限制在疾病相关组织中的药物靶向和功效。诸位发明人开发了生产细胞系和制造方法,它们产生具有比常规rhgaa更优异的糖基化和更高的m6p含量(具体是高亲和力的双-m6pn-聚糖结构)的rhgaa(命名为atb-200rhgaa),用于改进药物靶向。atb-200rhgaa以高亲和力(kd约2-4nm)结合ci-mpr,并且被庞贝成纤维细胞和骨骼肌成肌细胞有效内化(k摄取约7-14nm)。
atb-200rhgaa在骨骼肌中清除糖原显著好于
atb-200rhgaa与at2221共同给予的基本原理(chart技术)
分子伴侣结合至rhgaaert并使rhgaaert稳定,增加活性酶摄取到组织中,改进耐受性并潜在地减轻免疫原性。如上所示,使用charttm,充分改进在不利条件下ert的蛋白稳定性。chart:分子伴侣高级替代疗法,参见http://_www.amicusrx.com/chaperone.aspx(2015年9月22日最后访问),将其通过引用来结合。如图13a和13b所示,通过at2221(麦格司他,n-丁基-脱氧野尻霉素)显著改进了atb-200的稳定性。在37℃下,通过在中性(ph7.4-血浆环境)或酸性(ph5.2-溶酶体环境)缓冲液中的热变性监测rhgaa蛋白的折叠。在中性ph缓冲液中,经24小时,at2220使rhgaa蛋白稳定。
与atb-200rhgaa与麦格司他的共给予相比的
将12周龄gaako小鼠用
用与药理分子伴侣at2221(麦格司他)共同给予的atb-200rhgaa减少组织糖原。
发现药理分子伴侣和atb-200rhgaa的组合在体内增强糖原清除。将gaako小鼠每隔一周以20mg/kg进行两次rhgaa的iv推注给予。在rhgaa之前30分钟以0、1、2和10mg/kg的剂量口服给予药理分子伴侣at2221。在最后剂量的ert之后两周收获组织,并分析gaa活性、糖原含量细胞特异性糖原以及溶酶体增殖。
如图15所示,接受atb200+分子伴侣at2221的动物表现出从四头肌的增强的糖原清除。atb-200rhgaa(20mg/kg)降低糖原超过相同剂量的
如图16a和16b所示,不像显示有限糖原减少(由丰富的点状pas信号指示)的常规rhgaa,单独的atb-200rhgaa显示pas信号显著降低。与10mg/kg麦格司他共同给予导致底物实质性的进一步减少。tem揭示了大多数溶酶体中的糖原为膜结合的、对应于点状pas信号的电子致密材料。atb-200rhgaa与麦格司他的共同给予减少了包含底物的溶酶体的数量、大小和密度,这表明将atb-200rhgaa靶向递送至肌细胞并随后递送至溶酶体。
从以上所示的研究(每隔一周注射2次iv推注)看出,使用lamp1标志物处理组织用于溶酶体增殖,上调是庞贝氏病的另一个标志。lamp:溶酶体相关膜蛋白。从以上所示的研究(2次iv推注eow注射)看出,在相邻切片中处理比目鱼肌组织用于lamp1染色,并且在相邻切片中加入i型纤维特异性抗体(noq7.5.4d)(图16c和16d)。与常规rhgaa相比,atb-200rhgaa导致更大幅的lamp1减少,这些减少导致在wt动物中看到的水平(图16c)。
此外,不像rhgaa(其中该效应主要受限于i型纤维(慢缩,用星号标记)),atb-200rhgaa也导致在一部分ii型(快缩)纤维(红色箭头)中的lamp1信号显著减少(图16d)。重要的是,与麦格司他共同给予进一步改进大多数ii型纤维中atb-200介导的lamp1增殖的减少(图16c和16d)。其结果是,看来似乎在lamp1信号水平上没有出现显著的纤维类型特异性差异。从四头肌和膈肌获得了类似的结论(数据未显示)。
在一个单独的和类似设计的研究中,在较长时期内用4次每两周一次iv推注注射检查atb-200±at2221的作用。在心脏中,通过重复给予rhgaa或atb-200至在野生型(wt)动物中所看到的水平,容易地清除了心肌细胞中的主要糖原贮积(图17a)。然而,心脏平滑肌细胞中的底物似乎优选地通过atb-200rhgaa来清除,这表明与rhgaa相比(星号标记心脏血管的腔),atb-200的潜在更广的生物分布。重要的是,与麦格司他的共同给予进一步改进atb-200介导的lamp1增殖的减少。
这些结果表明atb-200rhgaa(其在其n-聚糖上具有更高水平的m6p和双-m6p)有效靶向骨骼肌中的cimpr。atb-200rhgaa还具有经过良好加工的复合型n-聚糖(其最小化体内非生产性清除),具有有利于其在体内使用的药代动力学性质,并且在体内表现出对关键肌肉组织的良好靶向。他们还表明,针对减少肌肉组织中的糖原,atb-200rhgaa优于常规的护理标准lumizyme,并且atb-200rhgaa和分子伴侣at2221的组合进一步改进从靶组织中去除糖原并改进肌肉病理。
序列表
<110>阿米库斯治疗学公司(amicustherapeutics,inc.)
<120>具有增强的碳水化合物的高强度酸性α-葡糖苷酶
<130>twlb7360-17p8
<150>us62/135,345
<151>2015-03-19
<150>us62/112,643
<151>2015-02-05
<150>us62/057,847
<151>2014-09-30
<150>us62/057,842
<151>2014-09-30
<160>4
<170>patentin3.5版本
<210>1
<211>952
<212>prt
<213>智人
<220>
<221>尚未归类的特征
<222>(1)..(952)
<223>来自专利us8592362基因库的序列4:ahe24104.1
<400>1
metglyvalarghisproprocysserhisargleuleualavalcys
151015
alaleuvalserleualathralaalaleuleuglyhisileleuleu
202530
hisasppheleuleuvalproarggluleuserglyserserproval
354045
leuglugluthrhisproalahisglnglnglyalaserargprogly
505560
proargaspalaglnalahisproglyargproargalavalprothr
65707580
glncysaspvalproproasnserargpheaspcysalaproasplys
859095
alailethrglngluglncysglualaargglycyscystyrilepro
100105110
alalysglnglyleuglnglyalaglnmetglyglnprotrpcysphe
115120125
pheproprosertyrprosertyrlysleugluasnleuserserser
130135140
glumetglytyrthralathrleuthrargthrthrprothrphephe
145150155160
prolysaspileleuthrleuargleuaspvalmetmetgluthrglu
165170175
asnargleuhisphethrilelysaspproalaasnargargtyrglu
180185190
valproleugluthrproargvalhisserargalaproserproleu
195200205
tyrservalgluphesergluglupropheglyvalilevalhisarg
210215220
glnleuaspglyargvalleuleuasnthrthrvalalaproleuphe
225230235240
phealaaspglnpheleuglnleuserthrserleuproserglntyr
245250255
ilethrglyleualagluhisleuserproleumetleuserthrser
260265270
trpthrargilethrleutrpasnargaspleualaprothrprogly
275280285
alaasnleutyrglyserhisprophetyrleualaleugluaspgly
290295300
glyseralahisglyvalpheleuleuasnserasnalametaspval
305310315320
valleuglnproserproalaleusertrpargserthrglyglyile
325330335
leuaspvaltyrilepheleuglyprogluprolysservalvalgln
340345350
glntyrleuaspvalvalglytyrprophemetproprotyrtrpgly
355360365
leuglyphehisleucysargtrpglytyrserserthralailethr
370375380
argglnvalvalgluasnmetthrargalahispheproleuaspval
385390395400
glntrpasnaspleuasptyrmetaspserargargaspphethrphe
405410415
asnlysaspglypheargasppheproalametvalglngluleuhis
420425430
glnglyglyargargtyrmetmetilevalaspproalaileserser
435440445
serglyproalaglysertyrargprotyraspgluglyleuargarg
450455460
glyvalpheilethrasngluthrglyglnproleuileglylysval
465470475480
trpproglyserthralapheproaspphethrasnprothralaleu
485490495
alatrptrpgluaspmetvalalagluphehisaspglnvalprophe
500505510
aspglymettrpileaspmetasngluproserasnpheilearggly
515520525
sergluaspglycysproasnasngluleugluasnproprotyrval
530535540
proglyvalvalglyglythrleuglnalaalathrilecysalaser
545550555560
serhisglnpheleuserthrhistyrasnleuhisasnleutyrgly
565570575
leuthrglualailealaserhisargalaleuvallysalaarggly
580585590
thrargprophevalileserargserthrphealaglyhisglyarg
595600605
tyralaglyhistrpthrglyaspvaltrpsersertrpgluglnleu
610615620
alaserservalprogluileleuglnpheasnleuleuglyvalpro
625630635640
leuvalglyalaaspvalcysglypheleuglyasnthrsergluglu
645650655
leucysvalargtrpthrglnleuglyalaphetyrprophemetarg
660665670
asnhisasnserleuleuserleuproglngluprotyrserpheser
675680685
gluproalaglnglnalametarglysalaleuthrleuargtyrala
690695700
leuleuprohisleutyrthrleuphehisglnalahisvalalagly
705710715720
gluthrvalalaargproleupheleuglupheprolysaspserser
725730735
thrtrpthrvalasphisglnleuleutrpglyglualaleuleuile
740745750
thrprovalleuglnalaglylysalagluvalthrglytyrphepro
755760765
leuglythrtrptyraspleuglnthrvalproileglualaleugly
770775780
serleuproproproproalaalaproarggluproalailehisser
785790795800
gluglyglntrpvalthrleuproalaproleuaspthrileasnval
805810815
hisleuargalaglytyrileileproleuglnglyproglyleuthr
820825830
thrthrgluserargglnglnprometalaleualavalalaleuthr
835840845
lysglyglyglualaargglygluleuphetrpaspaspglygluser
850855860
leugluvalleugluargglyalatyrthrglnvalilepheleuala
865870875880
argasnasnthrilevalasngluleuvalargvalthrserglugly
885890895
alaglyleuglnleuglnlysvalthrvalleuglyvalalathrala
900905910
proglnglnvalleuserasnglyvalprovalserasnphethrtyr
915920925
serproaspthrlysvalleuaspilecysvalserleuleumetgly
930935940
gluglnpheleuvalsertrpcys
945950
<210>2
<211>3624
<212>dna
<213>智人
<220>
<221>cds
<222>(220)..(3078)
<223>溶酶体α-葡糖苷酶(酸性麦芽糖酶)的智人gaamrna;基因库:y00839.1
<400>2
cagttgggaaagctgaggttgtcgccggggccgcgggtggaggtcggggatgaggcagca60
ggtaggacagtgacctcggtgacgcgaaggaccccggccacctctaggttctcctcgtcc120
gcccgttgttcagcgagggaggctctgggcctgccgcagctgacggggaaactgaggcac180
ggagcgggcctgtaggagctgtccaggccatctccaaccatgggagtgaggcac234
metglyvalarghis
15
ccgccctgctcccaccggctcctggccgtctgcgccctcgtgtccttg282
proprocysserhisargleuleualavalcysalaleuvalserleu
101520
gcaaccgctgcactcctggggcacatcctactccatgatttcctgctg330
alathralaalaleuleuglyhisileleuleuhisasppheleuleu
253035
gttccccgagagctgagtggctcctccccagtcctggaggagactcac378
valproarggluleuserglyserserprovalleuglugluthrhis
404550
ccagctcaccagcagggagccagcagaccagggccccgggatgcccag426
proalahisglnglnglyalaserargproglyproargaspalagln
556065
gcacaccccggccgtcccagagcagtgcccacacagtgcgacgtcccc474
alahisproglyargproargalavalprothrglncysaspvalpro
70758085
cccaacagccgcttcgattgcgcccctgacaaggccatcacccaggaa522
proasnserargpheaspcysalaproasplysalailethrglnglu
9095100
cagtgcgaggcccgcggctgctgctacatccctgcaaagcaggggctg570
glncysglualaargglycyscystyrileproalalysglnglyleu
105110115
cagggagcccagatggggcagccctggtgcttcttcccacccagctac618
glnglyalaglnmetglyglnprotrpcysphepheproprosertyr
120125130
cccagctacaagctggagaacctgagctcctctgaaatgggctacacg666
prosertyrlysleugluasnleuserserserglumetglytyrthr
135140145
gccaccctgacccgtaccacccccaccttcttccccaaggacatcctg714
alathrleuthrargthrthrprothrphepheprolysaspileleu
150155160165
accctgcggctggacgtgatgatggagactgagaaccgcctccacttc762
thrleuargleuaspvalmetmetgluthrgluasnargleuhisphe
170175180
acgatcaaagatccagctaacaggcgctacgaggtgcccttggagacc810
thrilelysaspproalaasnargargtyrgluvalproleugluthr
185190195
ccgcgtgtccacagccgggcaccgtccccactctacagcgtggagttc858
proargvalhisserargalaproserproleutyrservalgluphe
200205210
tccgaggagcccttcggggtgatcgtgcaccggcagctggacggccgc906
sergluglupropheglyvalilevalhisargglnleuaspglyarg
215220225
gtgctgctgaacacgacggtggcgcccctgttctttgcggaccagttc954
valleuleuasnthrthrvalalaproleuphephealaaspglnphe
230235240245
cttcagctgtccacctcgctgccctcgcagtatatcacaggcctcgcc1002
leuglnleuserthrserleuproserglntyrilethrglyleuala
250255260
gagcacctcagtcccctgatgctcagcaccagctggaccaggatcacc1050
gluhisleuserproleumetleuserthrsertrpthrargilethr
265270275
ctgtggaaccgggaccttgcgcccacgcccggtgcgaacctctacggg1098
leutrpasnargaspleualaprothrproglyalaasnleutyrgly
280285290
tctcaccctttctacctggcgctggaggacggcgggtcggcacacggg1146
serhisprophetyrleualaleugluaspglyglyseralahisgly
295300305
gtgttcctgctaaacagcaatgccatggatgtggtcctgcagccgagc1194
valpheleuleuasnserasnalametaspvalvalleuglnproser
310315320325
cctgcccttagctggaggtcgacaggtgggatcctggatgtctacatc1242
proalaleusertrpargserthrglyglyileleuaspvaltyrile
330335340
ttcctgggcccagagcccaagagcgtggtgcagcagtacctggacgtt1290
pheleuglyprogluprolysservalvalglnglntyrleuaspval
345350355
gtgggatacccgttcatgccgccatactggggcctgggcttccacctg1338
valglytyrprophemetproprotyrtrpglyleuglyphehisleu
360365370
tgccgctggggctactcctccaccgctatcacccgccaggtggtggag1386
cysargtrpglytyrserserthralailethrargglnvalvalglu
375380385
aacatgaccagggcccacttccccctggacgtccaatggaacgacctg1434
asnmetthrargalahispheproleuaspvalglntrpasnaspleu
390395400405
gactacatggactcccggagggacttcacgttcaacaaggatggcttc1482
asptyrmetaspserargargaspphethrpheasnlysaspglyphe
410415420
cgggacttcccggccatggtgcaggagctgcaccagggcggccggcgc1530
argasppheproalametvalglngluleuhisglnglyglyargarg
425430435
tacatgatgatcgtggatcctgccatcagcagctcgggccctgccggg1578
tyrmetmetilevalaspproalaileserserserglyproalagly
440445450
agctacaggccctacgacgagggtctgcggaggggggttttcatcacc1626
sertyrargprotyraspgluglyleuargargglyvalpheilethr
455460465
aacgagaccggccagccgctgattgggaaggtatggcccgggtccact1674
asngluthrglyglnproleuileglylysvaltrpproglyserthr
470475480485
gccttccccgacttcaccaaccccacagccctggcctggtgggaggac1722
alapheproaspphethrasnprothralaleualatrptrpgluasp
490495500
atggtggctgagttccatgaccaggtgcccttcgacggcatgtggatt1770
metvalalagluphehisaspglnvalpropheaspglymettrpile
505510515
gacatgaacgagccttccaacttcatcagaggctctgaggacggctgc1818
aspmetasngluproserasnpheileargglysergluaspglycys
520525530
cccaacaatgagctggagaacccaccctacgtgcctggggtggttggg1866
proasnasngluleugluasnproprotyrvalproglyvalvalgly
535540545
gggaccctccaggcggccaccatctgtgcctccagccaccagtttctc1914
glythrleuglnalaalathrilecysalaserserhisglnpheleu
550555560565
tccacacactacaacctgcacaacctctacggcctgaccgaagccatc1962
serthrhistyrasnleuhisasnleutyrglyleuthrglualaile
570575580
gcctcccacagggcgctggtgaaggctcgggggacacgcccatttgtg2010
alaserhisargalaleuvallysalaargglythrargpropheval
585590595
atctcccgctcgacctttgctggccacggccgatacgccggccactgg2058
ileserargserthrphealaglyhisglyargtyralaglyhistrp
600605610
acgggggacgtgtggagctcctgggagcagctcgcctcctccgtgcca2106
thrglyaspvaltrpsersertrpgluglnleualaserservalpro
615620625
gaaatcctgcagtttaacctgctgggggtgcctctggtcggggccgac2154
gluileleuglnpheasnleuleuglyvalproleuvalglyalaasp
630635640645
gtctgcggcttcctgggcaacacctcagaggagctgtgtgtgcgctgg2202
valcysglypheleuglyasnthrserglugluleucysvalargtrp
650655660
acccagctgggggccttctaccccttcatgcggaaccacaacagcctg2250
thrglnleuglyalaphetyrprophemetargasnhisasnserleu
665670675
ctcagtctgccccaggagccgtacagcttcagcgagccggcccagcag2298
leuserleuproglngluprotyrserphesergluproalaglngln
680685690
gccatgaggaaggccctcaccctgcgctacgcactcctcccccacctc2346
alametarglysalaleuthrleuargtyralaleuleuprohisleu
695700705
tacacactgttccaccaggcccacgtcgcgggggagaccgtggcccgg2394
tyrthrleuphehisglnalahisvalalaglygluthrvalalaarg
710715720725
cccctcttcctggagttccccaaggactctagcacctggactgtggac2442
proleupheleuglupheprolysaspserserthrtrpthrvalasp
730735740
caccagctcctgtggggggaggccctgctcatcaccccagtgctccag2490
hisglnleuleutrpglyglualaleuleuilethrprovalleugln
745750755
gccgggaaggccgaagtgactggctacttccccttgggcacatggtac2538
alaglylysalagluvalthrglytyrpheproleuglythrtrptyr
760765770
gacctgcagacggtgccaatagaggcccttggcagcctcccaccccca2586
aspleuglnthrvalproileglualaleuglyserleupropropro
775780785
cctgcagctccccgtgagccagccatccacagcgaggggcagtgggtg2634
proalaalaproarggluproalailehissergluglyglntrpval
790795800805
acgctgccggcccccctggacaccatcaacgtccacctccgggctggg2682
thrleuproalaproleuaspthrileasnvalhisleuargalagly
810815820
tacatcatccccctgcagggccctggcctcacaaccacagagtcccgc2730
tyrileileproleuglnglyproglyleuthrthrthrgluserarg
825830835
cagcagcccatggccctggctgtggccctgaccaagggtggagaggcc2778
glnglnprometalaleualavalalaleuthrlysglyglygluala
840845850
cgaggggagctgttctgggacgatggagagagcctggaagtgctggag2826
argglygluleuphetrpaspaspglygluserleugluvalleuglu
855860865
cgaggggcctacacacaggtcatcttcctggccaggaataacacgatc2874
argglyalatyrthrglnvalilepheleualaargasnasnthrile
870875880885
gtgaatgagctggtacgtgtgaccagtgagggagctggcctgcagctg2922
valasngluleuvalargvalthrsergluglyalaglyleuglnleu
890895900
cagaaggtgactgtcctgggcgtggccacggcgccccagcaggtcctc2970
glnlysvalthrvalleuglyvalalathralaproglnglnvalleu
905910915
tccaacggtgtccctgtctccaacttcacctacagccccgacaccaag3018
serasnglyvalprovalserasnphethrtyrserproaspthrlys
920925930
gtcctggacatctgtgtctcgctgttgatgggagagcagtttctcgtc3066
valleuaspilecysvalserleuleumetglygluglnpheleuval
935940945
agctggtgttagccgggcggagtgtgttagtctctccagagggaggctggtt3118
sertrpcys
950
ccccagggaagcagagcctgtgtgcgggcagcagctgtgtgcgggcctgggggttgcatg3178
tgtcacctggagctgggcactaaccattccaagccgccgcatcgcttgtttccacctcct3238
gggccggggctctggcccccaacgtgtctaggagagctttctccctagatcgcactgtgg3298
gccggggcctggagggctgctctgtgttaataagattgtaaggtttgccctcctcacctg3358
ttgccggcatgcgggtagtattagccacccccctccatctgttcccagcaccggagaagg3418
gggtgctcaggtggaggtgtggggtatgcacctgagctcctgcttcgcgcctgctgctct3478
gccccaacgcgaccgcttcccggctgcccagagggctggatgcctgccggtccccgagca3538
agcctgggaactcaggaaaattcacaggacttgggagattctaaatcttaagtgcaatta3598
ttttaataaaaggggcatttggaatc3624
<210>3
<211>952
<212>prt
<213>智人
<400>3
metglyvalarghisproprocysserhisargleuleualavalcys
151015
alaleuvalserleualathralaalaleuleuglyhisileleuleu
202530
hisasppheleuleuvalproarggluleuserglyserserproval
354045
leuglugluthrhisproalahisglnglnglyalaserargprogly
505560
proargaspalaglnalahisproglyargproargalavalprothr
65707580
glncysaspvalproproasnserargpheaspcysalaproasplys
859095
alailethrglngluglncysglualaargglycyscystyrilepro
100105110
alalysglnglyleuglnglyalaglnmetglyglnprotrpcysphe
115120125
pheproprosertyrprosertyrlysleugluasnleuserserser
130135140
glumetglytyrthralathrleuthrargthrthrprothrphephe
145150155160
prolysaspileleuthrleuargleuaspvalmetmetgluthrglu
165170175
asnargleuhisphethrilelysaspproalaasnargargtyrglu
180185190
valproleugluthrproargvalhisserargalaproserproleu
195200205
tyrservalgluphesergluglupropheglyvalilevalhisarg
210215220
glnleuaspglyargvalleuleuasnthrthrvalalaproleuphe
225230235240
phealaaspglnpheleuglnleuserthrserleuproserglntyr
245250255
ilethrglyleualagluhisleuserproleumetleuserthrser
260265270
trpthrargilethrleutrpasnargaspleualaprothrprogly
275280285
alaasnleutyrglyserhisprophetyrleualaleugluaspgly
290295300
glyseralahisglyvalpheleuleuasnserasnalametaspval
305310315320
valleuglnproserproalaleusertrpargserthrglyglyile
325330335
leuaspvaltyrilepheleuglyprogluprolysservalvalgln
340345350
glntyrleuaspvalvalglytyrprophemetproprotyrtrpgly
355360365
leuglyphehisleucysargtrpglytyrserserthralailethr
370375380
argglnvalvalgluasnmetthrargalahispheproleuaspval
385390395400
glntrpasnaspleuasptyrmetaspserargargaspphethrphe
405410415
asnlysaspglypheargasppheproalametvalglngluleuhis
420425430
glnglyglyargargtyrmetmetilevalaspproalaileserser
435440445
serglyproalaglysertyrargprotyraspgluglyleuargarg
450455460
glyvalpheilethrasngluthrglyglnproleuileglylysval
465470475480
trpproglyserthralapheproaspphethrasnprothralaleu
485490495
alatrptrpgluaspmetvalalagluphehisaspglnvalprophe
500505510
aspglymettrpileaspmetasngluproserasnpheilearggly
515520525
sergluaspglycysproasnasngluleugluasnproprotyrval
530535540
proglyvalvalglyglythrleuglnalaalathrilecysalaser
545550555560
serhisglnpheleuserthrhistyrasnleuhisasnleutyrgly
565570575
leuthrglualailealaserhisargalaleuvallysalaarggly
580585590
thrargprophevalileserargserthrphealaglyhisglyarg
595600605
tyralaglyhistrpthrglyaspvaltrpsersertrpgluglnleu
610615620
alaserservalprogluileleuglnpheasnleuleuglyvalpro
625630635640
leuvalglyalaaspvalcysglypheleuglyasnthrsergluglu
645650655
leucysvalargtrpthrglnleuglyalaphetyrprophemetarg
660665670
asnhisasnserleuleuserleuproglngluprotyrserpheser
675680685
gluproalaglnglnalametarglysalaleuthrleuargtyrala
690695700
leuleuprohisleutyrthrleuphehisglnalahisvalalagly
705710715720
gluthrvalalaargproleupheleuglupheprolysaspserser
725730735
thrtrpthrvalasphisglnleuleutrpglyglualaleuleuile
740745750
thrprovalleuglnalaglylysalagluvalthrglytyrphepro
755760765
leuglythrtrptyraspleuglnthrvalproileglualaleugly
770775780
serleuproproproproalaalaproarggluproalailehisser
785790795800
gluglyglntrpvalthrleuproalaproleuaspthrileasnval
805810815
hisleuargalaglytyrileileproleuglnglyproglyleuthr
820825830
thrthrgluserargglnglnprometalaleualavalalaleuthr
835840845
lysglyglyglualaargglygluleuphetrpaspaspglygluser
850855860
leugluvalleugluargglyalatyrthrglnvalilepheleuala
865870875880
argasnasnthrilevalasngluleuvalargvalthrserglugly
885890895
alaglyleuglnleuglnlysvalthrvalleuglyvalalathrala
900905910
proglnglnvalleuserasnglyvalprovalserasnphethrtyr
915920925
serproaspthrlysvalleuaspilecysvalserleuleumetgly
930935940
gluglnpheleuvalsertrpcys
945950
<210>4
<211>952
<212>prt
<213>智人
<220>
<221>尚未归类的特征
<222>(1)..(952)
<223>溶酶体α-葡糖苷酶前原蛋白[智人];ncbi参考序列:np_000143.2
<400>4
metglyvalarghisproprocysserhisargleuleualavalcys
151015
alaleuvalserleualathralaalaleuleuglyhisileleuleu
202530
hisasppheleuleuvalproarggluleuserglyserserproval
354045
leuglugluthrhisproalahisglnglnglyalaserargprogly
505560
proargaspalaglnalahisproglyargproargalavalprothr
65707580
glncysaspvalproproasnserargpheaspcysalaproasplys
859095
alailethrglngluglncysglualaargglycyscystyrilepro
100105110
alalysglnglyleuglnglyalaglnmetglyglnprotrpcysphe
115120125
pheproprosertyrprosertyrlysleugluasnleuserserser
130135140
glumetglytyrthralathrleuthrargthrthrprothrphephe
145150155160
prolysaspileleuthrleuargleuaspvalmetmetgluthrglu
165170175
asnargleuhisphethrilelysaspproalaasnargargtyrglu
180185190
valproleugluthrprohisvalhisserargalaproserproleu
195200205
tyrservalgluphesergluglupropheglyvalilevalargarg
210215220
glnleuaspglyargvalleuleuasnthrthrvalalaproleuphe
225230235240
phealaaspglnpheleuglnleuserthrserleuproserglntyr
245250255
ilethrglyleualagluhisleuserproleumetleuserthrser
260265270
trpthrargilethrleutrpasnargaspleualaprothrprogly
275280285
alaasnleutyrglyserhisprophetyrleualaleugluaspgly
290295300
glyseralahisglyvalpheleuleuasnserasnalametaspval
305310315320
valleuglnproserproalaleusertrpargserthrglyglyile
325330335
leuaspvaltyrilepheleuglyprogluprolysservalvalgln
340345350
glntyrleuaspvalvalglytyrprophemetproprotyrtrpgly
355360365
leuglyphehisleucysargtrpglytyrserserthralailethr
370375380
argglnvalvalgluasnmetthrargalahispheproleuaspval
385390395400
glntrpasnaspleuasptyrmetaspserargargaspphethrphe
405410415
asnlysaspglypheargasppheproalametvalglngluleuhis
420425430
glnglyglyargargtyrmetmetilevalaspproalaileserser
435440445
serglyproalaglysertyrargprotyraspgluglyleuargarg
450455460
glyvalpheilethrasngluthrglyglnproleuileglylysval
465470475480
trpproglyserthralapheproaspphethrasnprothralaleu
485490495
alatrptrpgluaspmetvalalagluphehisaspglnvalprophe
500505510
aspglymettrpileaspmetasngluproserasnpheilearggly
515520525
sergluaspglycysproasnasngluleugluasnproprotyrval
530535540
proglyvalvalglyglythrleuglnalaalathrilecysalaser
545550555560
serhisglnpheleuserthrhistyrasnleuhisasnleutyrgly
565570575
leuthrglualailealaserhisargalaleuvallysalaarggly
580585590
thrargprophevalileserargserthrphealaglyhisglyarg
595600605
tyralaglyhistrpthrglyaspvaltrpsersertrpgluglnleu
610615620
alaserservalprogluileleuglnpheasnleuleuglyvalpro
625630635640
leuvalglyalaaspvalcysglypheleuglyasnthrsergluglu
645650655
leucysvalargtrpthrglnleuglyalaphetyrprophemetarg
660665670
asnhisasnserleuleuserleuproglngluprotyrserpheser
675680685
gluproalaglnglnalametarglysalaleuthrleuargtyrala
690695700
leuleuprohisleutyrthrleuphehisglnalahisvalalagly
705710715720
gluthrvalalaargproleupheleuglupheprolysaspserser
725730735
thrtrpthrvalasphisglnleuleutrpglyglualaleuleuile
740745750
thrprovalleuglnalaglylysalagluvalthrglytyrphepro
755760765
leuglythrtrptyraspleuglnthrvalprovalglualaleugly
770775780
serleuproproproproalaalaproarggluproalailehisser
785790795800
gluglyglntrpvalthrleuproalaproleuaspthrileasnval
805810815
hisleuargalaglytyrileileproleuglnglyproglyleuthr
820825830
thrthrgluserargglnglnprometalaleualavalalaleuthr
835840845
lysglyglyglualaargglygluleuphetrpaspaspglygluser
850855860
leugluvalleugluargglyalatyrthrglnvalilepheleuala
865870875880
argasnasnthrilevalasngluleuvalargvalthrserglugly
885890895
alaglyleuglnleuglnlysvalthrvalleuglyvalalathrala
900905910
proglnglnvalleuserasnglyvalprovalserasnphethrtyr
915920925
serproaspthrlysvalleuaspilecysvalserleuleumetgly
930935940
gluglnpheleuvalsertrpcys
945950
- 还没有人留言评论。精彩留言会获得点赞!