检测VKORC1基因分型的引物探针组及试剂盒的制作方法
本发明涉及体外核酸检测
技术领域:
,尤其涉及一种检测VKORC1基因分型的引物探针组及试剂盒。
背景技术:
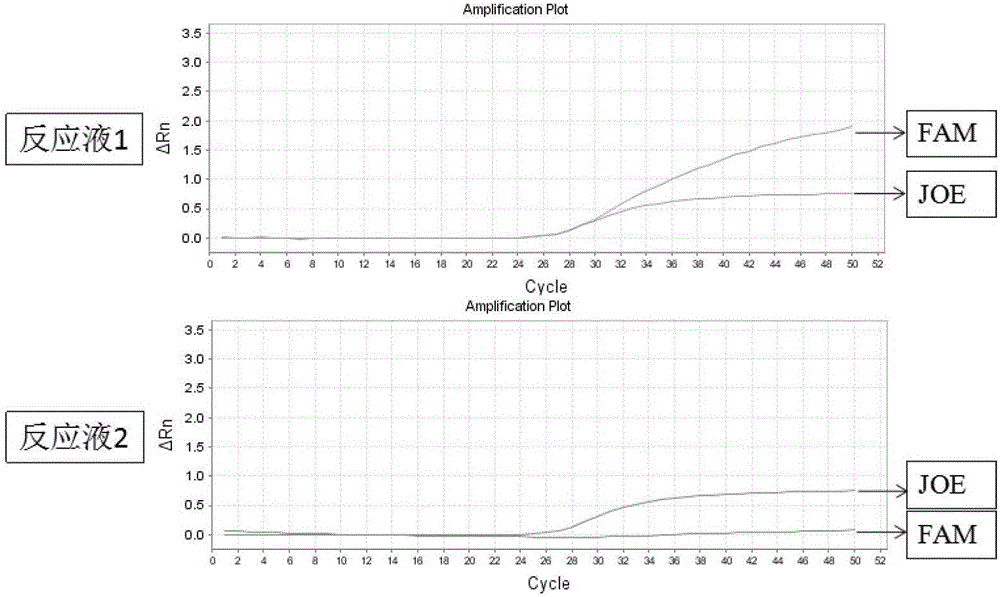
:华法林是一种双香豆素衍生物,是目前临床上应用最广泛的口服抗凝药物之一,用于预防和治疗深静脉血栓、肺栓塞、心脏瓣膜置换术及房颤导致的血栓形成。华法林治疗窗较窄,很小的剂量都可能导致不良反应的发生,且在不同个体达到相同作用效果,高低剂量者之间可相差10倍以上。维生素K环氧化物还原酶复合体1(Vitaminkepoxidereductasesubunit1,VKORC1)是维生素K循环中的关键酶,华法林因抑制该酶而阻断维生素K以辅因子形式参与羧化酶的催化反应,抑制了凝血因子Ⅱ、Ⅶ、Ⅸ、Ⅹ的功能活性,从而产生抗凝作用。国内外大量研究发现:VKORC1基因突变会增加该酶对华法林的敏感性,从而增强抗凝效果,其中比较常见的突变有启动子区的G-1639A突变及1号内含子的C1173T突变。目前研究已经证实1639G>A和1173C>T两个位点是完全连锁的。VKORC1-1693AA(1173TT)基因型患者需要的华法林剂量显著低于1693GA或GG(1173TC或CC)。美国食品药品监督管理局(FDA)明确指出:在使用华法林时,建议检测VKORC1基因型。目前医院用于VKORC1基因检测的“金标准”是PCR-直接测序法,但直接测序法的操作程序较复杂,敏感性不高,仅能检测出20-30%以上的突变株等。相比于直接测序法,ARMS-TaqMan法的灵敏性更高、成本更低。ARMS也称作等位基因特异性PCR(AlleleSpecificPCR,AS-PCR),其原理是PCR引物的3’端末位碱基与其模板DNA存在错配时,一般将导致扩增效率急剧下降,设计等位基因特异性PCR扩增引物,在严格的条件下,只有在引物3’碱基与模板配对时才能出现PCR扩增信号,从而检测出突变。实时荧光定量PCR(Real-timeQuantitativePCR,QPCR)技术于1996年由美国AppliedBiosystems公司推出,由于该技术不仅实现了PCR从定性到定量的飞跃,而且与常规PCR相比,它具有特异性更强、有效解决PCR污染问题、自动化程度高等特点,目前已得到广泛应用。QPCR技术一般分为探针法和染料法,本试剂盒采用的是TaqMan荧光探针:PCR扩增时在加入一对引物的同时加入一个特异性的荧光探针,该探针为一寡核苷酸,两端分别标记一个报告荧光基团和一个淬灭荧光基团。探针完整时,报告基团发射的荧光信号被淬灭基团吸收;PCR扩增时,Taq酶的5'-3'外切酶活性将探针酶切降解,使报告荧光基团和淬灭荧光基团分离,从而荧光监测系统可接收到荧光信号,即每扩增一条DNA链,就有一个荧光分子形成,实现了荧光信号的累积与PCR产物形成完全同步。目前市场上还没有利用ARMS结合QPCR技术进行VKORC1的基因多态性检测的产品。技术实现要素:为了解决上述方法检测VKORC1基因分型过程中存在敏感性不高、检测周期长、操作繁琐及成本高的技术问题,本发明提供一种敏感性高、特异性强、检测周期短、操作简单并有效满足临床检验要求的检测VKORC1基因分型的引物探针组及试剂盒。本发明提供了一种检测VKORC1基因分型的引物探针组,所述VKORC1基因检测的多态性位点为G1639A,所述引物探针组包括:扩增VKORC1野生型和突变型的通用下游引物:5’-GCCAGGCTTGTCTTAAACTCC-3’(SEQIDNO.1);扩增VKORC1野生型和突变型的通用探针:5’FAM-ACCTCAAGTGATCCACCCACCTCGGC-TAMRA3’(SEQIDNO.2);扩增VKORC1野生型的上游引物:5’-CCTGAAAAACAACCATTGGACG-3’(SEQIDNO.3);扩增VKORC1突变型的上游引物:5’-CCTGAAAAACAACCATTGGACA-3’(SEQIDNO.4);及扩增内控GAPDH基因的上游引物:5’-CACATGGCCTCCAAGGAGTAA-3’(SEQIDNO.5);扩增内控GAPDH基因的下游引物:5’-TGAGGGTCTCTCTCTTCCTCTTGT-3’(SEQIDNO.6);扩增内控GAPDH基因的探针:5’JOE-CTGGACCACCAGCCCCAGCAAG-TAMRA3’(SEQIDNO.7)。本发明还提供了一种检测VKORC1基因分型的试剂盒,所述VKORC1基因检测的多态性位点为G1639A,所述试剂盒包括:PCR反应液1,所述PCR反应液1含有SEQIDNO.1、SEQIDNO.2、SEQIDNO.3、SEQIDNO.5、SEQIDNO.6及SEQIDNO.7所示的扩增引物及探针;PCR反应液2,所述PCR反应液2含有SEQIDNO.1、SEQIDNO.2、SEQIDNO.4、SEQIDNO.5、SEQIDNO.6及SEQIDNO.7所示的扩增引物及探针。在本发明提供的所述试剂盒的一种较佳实施例中,所述试剂盒还包括阳性对照品,其为插有SEQIDNO.1和SEQIDNO.3扩增产物的VKORC1野生纯合子质粒,插有SEQIDNO.1和SEQIDNO.4扩增产物的VKORC1突变纯合子质粒,插有SEQIDNO.5和SEQIDNO.6扩增产物的内控GAPDH质粒的上述三种质粒组成的质粒混合物;其中,质粒载体为pMD18-T质粒;所述质粒混合物中VKORC1突变纯合子质粒、VKORC1野生纯合子质粒和内控GAPDH质粒的数量比为1:1:2。在本发明提供的所述试剂盒的一种较佳实施例中,所述试剂盒还包括空白对照品,所述空白对照品为超纯水。在本发明提供的所述试剂盒的一种较佳实施例中,所述PCR反应液1-2中其他组分为常规的2xMixBuffer和H2O,PCR反应参数及体系为:95℃30s;95℃10s,60℃30s(采集荧光),进行50个循环,原料名称加入量(μL)2xMixBuffer(含ROX)12.5上游引物0.5下游引物0.5探针0.5内控上游引物0.5内控下游引物0.5内控探针0.5DNA模板1去离子水8.5总体积25本发明还提供了如上所述的引物探针组在制备用于检测VKORC1基因分型的试剂中的应用。相较于现有技术,本发明提供的检测VKORC1基因分型的引物探针组及试剂盒具有以下有益效果:一、通过利用ARMS技术结合QPCR技术设计了灵敏度高和特异性好的引物探针组及其试剂盒,使得所述试剂盒在检测VKORC1基因分型时,具有定性准确,灵敏度高及特异性强的优点;此外,还具有样品处理简单、测序步骤简单、测序速度快、一个小时完成一次上机反应、直接给出检测位点荧光曲线及结果直观的优点;二、通过利用ARMS技术结合QPCR技术设计了灵敏度高和特异性好的引物探针组及其试剂盒,使得所述试剂盒在检测VKORC1基因分型时,可实时监测反应进程、反应时间短、操作简便及高通量样品检测,PCR反应同时进行荧光采集,并比金标准方法,即毛细管电泳测序法灵敏度更高,更适合用于突变分析及临床检验;三、通过在所述试剂盒中设置了空白对照品和阳性对照品,使得所述试剂盒在检测VKORC1基因分型时,可以更好的确保检测结果的准确性。附图说明图1为华法林作用机制及VKORC1效应示意图;图2为临床样品VKORC1野生型的荧光扩增曲线图;图3为临床样品VKORC1突变杂合型的荧光扩增曲线图;图4为临床样品VKORC1突变纯合型的荧光扩增曲线图;图5为临床VKORC1阳性对照品的荧光扩增曲线图;图6为临床VKORC1空白对照品的荧光扩增曲线图;图7至图8为VKORC1多组设计引物的荧光扩增曲线图;其中图7的测序结果不准确,图8的测序结果真实可靠。具体实施方式为了使本发明的目的、技术方案及优点更加清楚明白,下面结合附图及实施例,对本发明进行进一步的详细说明。应当理解,此处所描述的具体实施例仅用以解释本发明,并不用于限定本发明。实施例1:试剂盒的制备一、引物和探针的设计与合成针对人VKORC1基因的多态性位点G1639A等位基因,选择特异的突变位点,选用的引物和探针设计在VKORC1突变位点和附近的保守区,避免在引物结合区域出现有SNP(通过在线NCBI网站对靶基因序列的SNP进行检索),通过在线NCBI网站进行PrimerBlast,确认引物对的特异性扩增。探针位于一对引物之间的区域,且避免其结合区域出现有SNP;其中扩增引物和荧光探针先经过PAGE纯化,再经HPLC纯化,其中目的探针SEQIDNO.2的5’端采用荧光报告基团(FAM)标记,内控探针SEQIDNO.7的5’端采用荧光报告基团(JOE)标记,3’端均采用荧光淬灭基团(TAMRA)标记。表1.突变位点与类型MutationBasechangeVKORC1(1639)G>A扩增序列如表2:表2.特异性扩增引物与探针序列二、对照品选择阳性对照品由3种质粒的混合物组成,所述质粒混合物中VKORC1突变纯合子质粒、VKORC1野生纯合子质粒和内控GAPDH质粒的数量比为1:1:2;DNase/RNase-Free水为空白对照品。三、PCR反应液组成表3.PCR反应液1组成表4.PCR反应液2组成原料名称加入量(μL)2xMixBuffer(含ROX)12.5SEQIDNO.40.5SEQIDNO.10.5SEQIDNO.20.5SEQIDNO.50.5SEQIDNO.60.5SEQIDNO.70.5去离子水8.5总体积24通过2种不同的PCR反应液,对VKORC1G1639A位点进行分型检测。实施例2:试剂盒的使用一、样品检测溶解引物探针干粉(引物溶解后有效期为1个月)。按照模板数配制体系:取PCR反应液,加入溶好的引物、探针,分装体系,加入样品DNA、空白对照品或阳性对照品为模板,组成PCR反应体系。按照PCR反应程序进行PCR扩增。VKORC1体系各主要成分如下:表5.PCR反应液1组成原料名称加入量(μL)2xMixBuffer(含ROX)12.5SEQIDNO.30.5SEQIDNO.10.5SEQIDNO.20.5SEQIDNO.50.5SEQIDNO.60.5SEQIDNO.70.5DNA模板1去离子水8.5总体积25表6.PCR反应液2组成原料名称加入量(μL)2xMixBuffer(含ROX)12.5SEQIDNO.40.5SEQIDNO.10.5SEQIDNO.20.5SEQIDNO.50.5SEQIDNO.60.5SEQIDNO.70.5DNA模板1去离子水8.5总体积25该体系反应程序如下:表7.PCR反应程序二、ABI7500荧光定量PCR按下右端开机键,启动ABI7500。开机后机器左端“power”指示灯长亮。打开仓门,将配好的试剂放入仓内,记好自己摆放的位置。1)双击“7500Softwarev2.0.5”图标打开软件。在弹出的窗口中点击“OK”进入程序。2)单击“NewExperiment”,在弹出的“ExperimentProperties”界面中依次选中“7500(96wells)”、“Quantitaion-StandadCurve”、“Reagents”图标使其变亮。3)点击“PlateSetup”,在“Reporter”栏内的下拉选框里选择“FAM”,在“Quencher”栏内的下拉选框里选择“TAMRA”,点击“AddNewTarget”,在“Reporter”栏内的下拉选框里选择“JOE”,在“Quencher”栏内的下拉选框里选择“TAMRA”;反复点击“AddNewSample”,使“SampleName”下方弹出足够数量的方框,在这些方框内输入各样本的唯一编号。4)点击“AssignTargetsandSamples”,在“PassiveReference”栏内的下拉选框里选择“ROX”,选中试剂所放的孔位,确认与仪器相对应,在“Assignsample(s)totheselectedwells”栏内的方框里打“√”,在“Assigntarget(s)totheselectedwells”栏内的方框里打“√”,并点击对应的图标使其变亮:“U”(待测样本)、“S”(阳性对照)、“N”(空白对照)。5)反应条件设置:单击“RunMethod”进入反应条件设置面板,制定所需的扩增程序,在“HoldingStage”栏内设置95℃30秒,将光标移至“CyclingStage”栏,在第1节“Step1”中设置95℃10秒,在“Step2”中设置60℃30秒,并在该节中点击荧光采集图标使其变亮,在“NumberofCycles”栏内输入50,并在“ReactionVolumePerWell”栏内输入25。6)确认无误后,点击“STARTR…”对当次PCR编号并保存在对应的文件夹,点击确定,开始运行。开始后会有一段预热,正式开始循环时“INUSE”指示灯闪烁。7)运行完后,打开仓门,将产物倒入垃圾桶,填写仪器使用记录。三、结果判断反应结束后,进行自动调整基线和阈值。设定之后,点击“Analyse”(分析)按键,即可从“ViewWellTable”窗口的“Ct”处得到各样本的Ct值。四、质控标准对于VKORC1:配有PCR反应液1的反应管Ct值定为Ct1,配有PCR反应液2的反应管Ct值定为Ct2,△Ct=Ct2-Ct1。阳性对照的Ct≤32,-2≤△Ct≤2;空白对照无S型扩增曲线或无Ct值显示。以上条件必须在同一次实验中全部满足,否则本次实验结果无效。五、结果报告:对于待检样本:1)若Ct﹥32,说明DNA质量太低,需要重新提取DNA或更换样本;2)若Ct-≤32,即对于ΔCT绝对值>12的样本定义为相应的纯合子,-2≤ΔCT≤2的样本定义为VKORC1的杂合型。而2≤|ΔCT|≤12的样本则需要重做试验进行复核,重做结果一致,则认定为取样过程或样本处理过程存在污染,需要重新取样。图1为华法林作用机制及VKORC1效应示意图;图2显示的是临床样品检测结果中VKORC1的野生型;图3显示的是临床样品检测结果中VKORC1的杂合型;图4显示的是临床样品检测结果中VKORC1的突变纯合型;图5及图6分别显示的是临床检测结果中阳性对照品和空白对照品的荧光扩增曲线图。其中,图2反应液1中FAM曲线Ct1值为25.69,反应液2中FAM曲线无Ct1值,△Ct>12判定为野生型。图3反应液1中FAM曲线Ct1值为26.8,反应液2中FAM曲线Ct2值为26.44,△Ct=26.8-26.44=0.36-2≤ΔCT≤2判定为杂合型。图4反应液1中FAM曲线无Ct1值,反应液2中FAM曲线Ct2值为25.22,△Ct>12判定为突变纯合型。图5反应液1和2的FAM曲线均有CT值,JOE曲线也均有CT值。图6反应液1和2的FAM曲线均无CT值,JOE曲线也均无CT值。图7至图8显示的是设计的VKORC1多组引物的荧光扩增曲线图,其中图8的引物为最佳,是我们产品中选定的引物。本发明提供的检测VKORC1基因分型的引物探针组及试剂盒具有以下有益效果:一、通过利用ARMS技术结合QPCR技术设计了灵敏度高和特异性好的引物探针组及其试剂盒,使得所述试剂盒在检测VKORC1基因分型时,具有定性准确,灵敏度高及特异性强的优点;此外,还具有样品处理简单、测序步骤简单、测序速度快、一个小时完成一次上机反应、直接给出检测位点荧光曲线及结果直观的优点;二、通过利用ARMS技术结合QPCR技术设计了灵敏度高和特异性好的引物探针组及其试剂盒,使得所述试剂盒在检测VKORC1基因分型时,可实时监测反应进程、反应时间短、操作简便及高通量样品检测,PCR反应同时进行荧光采集,并比金标准方法,即毛细管电泳测序法灵敏度更高,更适合用于突变分析及临床检验;三、通过在所述试剂盒中设置了空白对照品和阳性对照品,使得所述试剂盒在检测VKORC1基因分型时,可以更好的确保检测结果的准确性。以上所述仅为本发明的实施例,并非因此限制本发明的专利范围,凡是利用本发明说明书内容所作的等效流程变换,或直接或间接运用在其它相关的
技术领域:
,均同理包括在本发明的专利保护范围内。SEQUENCELISTING<110>长沙三济生物科技有限公司<120>检测VKORC1基因分型的引物探针组及试剂盒<130>2016<160>7<170>PatentInversion3.3<210>1<211>21<212>DNA<213>人工序列<400>1gccaggcttgtcttaaactcc21<210>2<211>26<212>DNA<213>人工序列<400>2acctcaagtgatccacccacctcggc26<210>3<211>22<212>DNA<213>人工序列<400>3cctgaaaaacaaccattggacg22<210>4<211>22<212>DNA<213>人工序列<400>4cctgaaaaacaaccattggaca22<210>5<211>21<212>DNA<213>人工序列<400>5cacatggcctccaaggagtaa21<210>6<211>24<212>DNA<213>人工序列<400>6tgagggtctctctcttcctcttgt24<210>7<211>22<212>DNA<213>人工序列<400>7ctggaccaccagccccagcaag22当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1