肝癌早期诊断试剂或试剂盒及用途的制作方法
本发明涉及疾病诊断试剂领域,更具体地,涉及一种UBE2J2、ATP6V0D1和STXBP2中的至少一种作为肝癌早期诊断分子标识物的用途,以及一种肝癌早期诊断试剂或试剂盒。
背景技术:
肝癌是人类最常见的恶性肿瘤之一,其发病率在全世界范围内位居第四,每年约有74.5万人死于肝癌。目前临床上对于肝细胞肝癌(Hepatocellular carcinoma HCC)的常规监测方法是超声扫描和血清甲胎蛋白(alpha-fetoprotein AFP)水平的测定。腹部超声扫描对于HbsAg携带者的诊断灵敏度可达71%,特异度可达93%,但其阳性预测值只有14%,AFP诊断肝癌的敏感度、特异度和阳性预测值并不十分理想,分别只有39%-64%、76%-91%和9%-32%。约40%的肝癌患者AFP并不升高,亟需找到更加简单可靠的方法来提高早期HCC的检出率。
肿瘤标识物由恶性肿瘤细胞合成、分泌并释放,能在机体组织或体液中用生化或免疫组化等方法进行定量测定的生物分子(通常为蛋白质),可以给临床提供恶性肿瘤的诊断、预后或治疗监测等信息。但是,目前诊断治疗肝癌的特异性肿瘤标识物寥寥无几,急需找到更多肝癌标识物,为早期肝癌诊断和治疗提供新靶点和新途径。
肿瘤转移是造成大于90%癌症患者死亡的主要原因。肿瘤的转移扩散,需要肿瘤细胞对其周围环境进行侵润,在这过程,细胞突出起着关键的牵引和探测作用。通过分离肝癌细胞突出,对总mRNA进行测序(DRS)分析,找到新的肝癌特异性靶点,对早期肝癌诊断和治疗,具有重要意义。
技术实现要素:
本发明的目的是提供新的肝癌早期诊断的分子标识物和药物治疗的基因靶标,以及提供肝癌早期诊断试剂或试剂盒。
根据本发明的第一方面,提供UBE2J2、ATP6V0D1和STXBP2中的至少一种作为肝癌早期诊断分子标识物的用途。
根据本发明的第二方面,提供一种肝癌早期诊断试剂,所述试剂或试剂盒包括用于检测UBE2J2、ATP6V0D1和STXBP2中至少一种的试剂。
根据本发明的第三方面,提供一种肝癌早期诊断试剂盒,所述试剂盒包括上述肝癌早期诊断试剂。
实验表明,UBE2J2、ATP6V0D1和STXBP2均在高转移肝癌细胞突出中高表达。多个肝癌及癌旁标本测试证明,它们在大部分的肝癌标本中的表达要比癌旁高。细胞侵袭实验证明,它们能够调控肝癌细胞侵袭能力。因此,它们可作为肝癌诊断和治疗的新靶标,具有潜在的临床应用前景。
本发明的其它特征和优点将在随后具体实施方式部分予以详细说明。
附图说明
通过结合附图对本发明示例性实施方式进行更详细的描述。
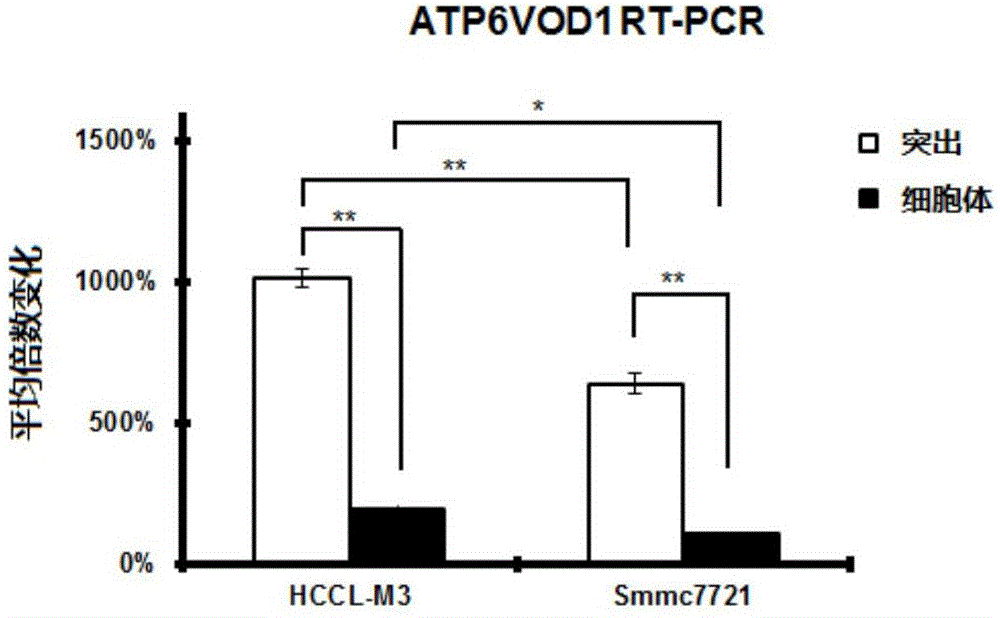
图1A、图1B和图1C分别示出了UBE2J2、ATP6V0D1和STXBP2在高转移细胞株HCCLM3和低转移细胞株smmc17721的细胞突出和细胞体中进行RT-PCR的结果。
图2A和图2B为细胞侵袭实验结果,验证UBE2J2具有调控HCCLM3肝癌细胞侵袭能力,其中,con表示对照组。
图3A-图3D为免疫组化实验结果,验证UBE2J2在转移性肝癌组织中高表达,其中,图3A和图3C表示肝癌组织,图3B和图3D表示癌旁组织。
具体实施方式
下面将参照附图更详细地描述本发明的优选实施方式。虽然附图中显示了本发明的优选实施方式,然而应该理解,可以以各种形式实现本发明而不应被这里阐述的实施方式所限制。
根据本发明的第一方面,提供UBE2J2、ATP6V0D1和STXBP2中的至少一种作为肝癌早期诊断分子标识物的用途。
其中,所述UBE2J2、ATP6V0D1和STXBP2的基因序列已被公开报道,可通过公开途径查询。具体地,
UBE2J2
http://asia.ensembl.org/Homo_sapiens/Transcript/Sequence_cDNA?db=cor e;g=ENSG00000160087;r=1:1254985-1273855;t=ENST00000400929
ATP6V0D1
http://asia.ensembl.org/Homo_sapiens/Transcript/Sequence_cDNA?db=cor e;g=ENSG00000159720;r=16:67438019-67481237;t=ENST00000290949
STXBP2
http://asia.ensembl.org/Homo_sapiens/Transcript/Sequence_cDNA?db=cor e;g=ENSG00000076944;r=19:7637119-7647873;t=ENST00000221283
优选地,所述肝癌为转移性肝癌。
根据本发明的第二方面,提供一种肝癌早期诊断试剂,所述试剂为用于检测UBE2J2、ATP6V0D1和STXBP2中至少一种的试剂。
优选地,所述试剂为用于扩增UBE2J2、ATP6V0D1和STXBP2中至少一种的引物。
根据本发明,本领域技术人员可以通过常规分子生物学手段设计合适的引物。
根据本发明一种实施方式,所述引物的序列为:
UBE2J2正向引物:5’-ATGACCCCTTATGAAGGTGG-3’(SEQ ID NO:1);
UBE2J2反向引物:5’-TCACTCCTGCGCGATGCT-3’(SEQ ID NO:2)。
根据本发明一种实施方式,所述引物的序列为:
ATP6V0D1正向引物:5’-CGGAGCTTTACTTTAACGT-3’(SEQ ID NO:3);
ATP6V0D1反向引物:5’-AGGGATGTAGTTGTCGATTTT-3’(SEQ ID NO:4)。
根据本发明一种实施方式,所述引物的序列为:
STXBP2正向引物:5’-TGAAGGCGGTGGTGGGGGA-3’(SEQ ID NO:5);
STXBP2反向引物:5’-AATGTCCTCCAGCTTCTTGT-3’(SEQ ID NO:6)。
根据本发明,优选地,所述肝癌为转移性肝癌。
根据本发明的第三方面,提供一种肝癌早期诊断试剂盒,所述试剂盒包括上述肝癌早期诊断试剂。
所述试剂盒还可以包括用于扩增的其他常规试剂,包括但不限于:扩增用酶、dNTP和PCR反应缓冲液。
下面通过具体实施例对本发明进行说明,但本发明并不局限于此。
下述实施例中所述实验方法,如无特殊说明,均为常规方法;所述试剂和生物材料,如无特殊说明,均可从商业途径获得。
实施例1
Boyden改良法分离高转移肝癌细胞突出和细胞体的mRNA,进行RNA-seq测序。
把高转移HCCLM3和低转移smmcl7721肝癌细胞转移到孵有I型胶原蛋白的1.0μm孔径悬挂式细胞培养皿上,37℃静置24~30小时。用1×PBS洗涤,倒立Boyden培养皿,用移液枪吸去Boyden培养皿上侧的残留培养基,接着用浸有Trizol的细胞刮铲来搜刮Boyden培养皿上侧的细胞突出。当分离细胞体中的RNA时,平放Boyden培养皿,用移液枪吸去Boyden培养皿里的培养基,然后用浸有Trizol的细胞刮铲来搜刮Boyden培养皿内侧的细胞体。
提取得到的mRNA,进行总mRNA测序(DRS)分析。按照在HCCLM3细胞突出/细胞体表达比值从高到低对五千多种基因进行排序,尚未有细胞侵袭相关报道的前20位基因如下表1所示:
表1高转移肝癌细胞突出中高表达的基因
注:H表示高转移细胞株,S表示低转移细胞株,P表示细胞突出,B表示细胞体,/表示未检测到表达。
所述RT-PCR中,UBE2J2正向引物:5’-ATGACCCCTTATGA AGGTGG-3’(SEQ ID NO:1);
UBE2J2反向引物:5’-TCACTCCTGCGCGATGCT-3’(SEQ ID NO:2)。
ATP6V0D1正向引物:5’-CGGAGCTTTACTTTAACGT-3’(SEQ ID NO:3);
ATP6V0D1反向引物:5’-AGGGATGTAGTTGTCGATTTT-3’(SEQ ID NO:4)。
STXBP2正向引物:5’-TGAAGGCGGTGGTGGGGGA-3’(SEQ ID NO:5);
STXBP2反向引物:5’-AATGTCCTCCAGCTTCTTGT-3’(SEQ ID NO:6)。
RT-PCR结果如图1A、图1B和图1C所示。可见,UBE2J2、ATP6V0D1和STXBP2在高转移肝癌细胞突出和低转移肝癌细胞突出中均表现出高表达。
实施例2
细胞侵袭实验。
高转移HCCLM3肝癌细胞预先用UBE2J2siRNA转染24小时,然后转移到孵有I型胶原蛋白的8.0μm孔径悬挂式细胞培养皿上,37℃静置24小时。用1×PBS洗涤,3%福尔马林固定15分钟后用棉签把上层未穿透小孔的细胞轻轻擦拭掉,PBS洗干净后用结晶紫染色,拍照,统计穿透的细胞数目。
结果如图2A-图2B所示,说明UBE2J2具有调控HCCLM3肝癌细胞侵袭能力,其中,con表示对照组。ATP6V0D1和STXBP2也表现出相似的细胞侵袭能力。
实施例3
免疫组化实验。
从福永人民医院收集45例转移性肝癌标本及癌旁组织,石蜡包埋切片,将切片依次放入二甲苯-二甲苯-100%酒精-100%酒精-95%酒精-90%酒精-80%酒精-70%酒精中浸泡10分钟进行脱蜡。加入3%H2O2浸泡10分钟,再加入柠檬酸缓冲液,放入微波炉中蒸煮3分钟进行抗原修复。冷却至室温,加入PBS稀释10倍的血清37℃封闭半小时。再加入UBE2J2一抗4度过夜结合,PBS洗3次,每次5分钟,加入二抗37℃结合半小时,DAB显色1分钟,最后滴加哈氏苏木素(SIGMA)1分钟,在0.25%的盐酸酒精中浸没不少于2秒,用自来水冲洗大于2分钟,室温晾干后封片。显微镜拍照,统计染上颜色的切片数量。
其中一例检测结果如图3A-图3D所示。其中,图3A和图3C表示肝癌组织,图3B和图3D表示癌旁组织,图3C和图3D分别为图3A和图3B的局部放大图。可见,肝癌组织为阳性染色,癌旁组织为阴性染色。
45例的肝癌组织中,42例是阳性染色,癌旁组织全部都是阴性染色,验证了UBE2J2在肝癌中高表达,可作为肝癌诊断和治疗的新靶标,具有潜在的临床应用前景。
以上已经描述了本发明的各实施例,上述说明是示例性的,并非穷尽性的,并且也不限于所披露的各实施例。在不偏离所说明的各实施例的范围和精神的情况下,对于本技术领域的普通技术人员来说许多修改和变更都是显而易见的。
SEQUENCE LISTING
<110> 深圳市坤健创新药物研究院
<120> 肝癌早期诊断试剂或试剂盒及用途
<130> ILC160686SKJ
<160> 6
<170> PatentIn version 3.3
<210> 1
<211> 20
<212> DNA
<213> 人工序列
<400> 1
atgacccctt atgaaggtgg 20
<210> 2
<211> 18
<212> DNA
<213> 人工序列
<400> 2
tcactcctgc gcgatgct 18
<210> 3
<211> 19
<212> DNA
<213> 人工序列
<400> 3
cggagcttta ctttaacgt 19
<210> 4
<211> 21
<212> DNA
<213> 人工序列
<400> 4
agggatgtag ttgtcgattt t 21
<210> 5
<211> 19
<212> DNA
<213> 人工序列
<400> 5
tgaaggcggt ggtggggga 19
<210> 6
<211> 20
<212> DNA
<213> 人工序列
<400> 6
aatgtcctcc agcttcttgt 20
- 还没有人留言评论。精彩留言会获得点赞!