检测样品中KRAS基因的突变的方法与流程
本发明通常涉及基因突变检测领域,具体地涉及检测kras基因的突变的方法。
背景技术:
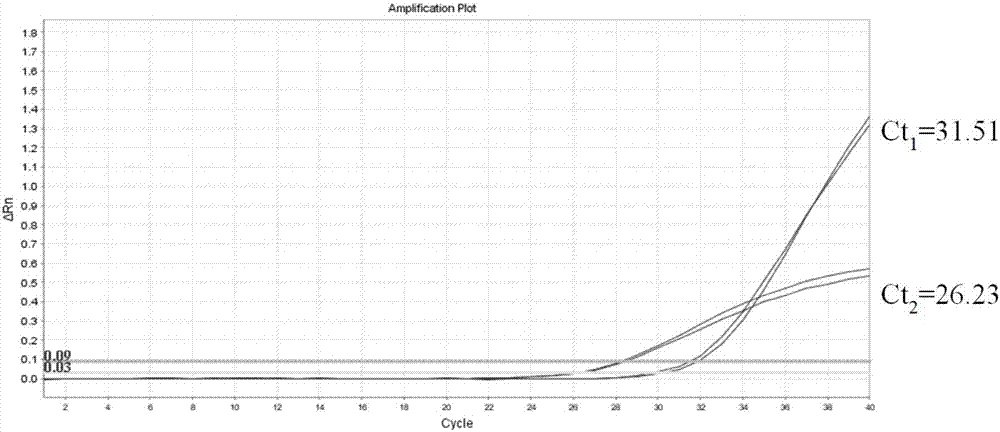
:kras(k-ras)基因是最重要的肿瘤致病基因之一,其参与egfr信号传导过程。k-ras基因突变导致egfr信号通路持续激活进而加速肿瘤细胞增殖,常见的突变包括k-ras基因的第2外显子的12和13密码子、第3外显子的61密码子。研究表明,k-ras基因突变状态与非小细胞肺癌对易瑞沙(吉非替尼)、特罗凯(厄洛替尼)等靶向治疗药物的原发性耐药有关。另外,对于结直肠癌患者,k-ras基因突变检测用于决定患者是否适用egfr单抗药物如爱必妥(西妥昔单抗)、维克替比(帕尼单抗)的治疗。美国国立综合癌症网络(nccn)2015年版临床治疗指南指出:k-ras基因突变是egfr酪氨酸激酶抑制剂疗效的预测指标,肿瘤患者在接受egfr靶向药物治疗前必须进行k-ras基因突变检测,以帮助决定患者是否接受egfr酪氨酸激酶抑制剂类药物治疗。目前检测kras基因第二外显子的密码子12、密码子13突变的金标准是arms-qpcr。arms-qpcr(amplificationrefractorymutationsystem)即扩增阻滞突变系统,又名等位基因特异性pcr(allelespecificpcr)。arms技术针对引物3’端进行等位基因特异性区分野生型和突变型两种形式,具有高特异性、高灵敏性(1%)、耗时短、结果易于判读等优点。目前arms-qpcr检测kras突变的实现形式如下所述:需要对kras基因第二外显子的密码子12和密码子13中每个位点构建arms-qpcr反应体系,即一个样本的检测须在八个反应管中同时进行,其中七个反应管分别检测g12d、g12v、g13d、g12c、g12a、g12s、g12r七种突变,第八孔作为试剂有效性判断的阳性质控孔存在。现有技术中,一个待检测样本需要通过七个反应孔来检测这其中是否存在基因突变,七个反应孔所需要的模板dna量比较多,这样就使得在dna量较少的情况下,无法判断待检测样本中是否存在基因突变。目前肿瘤组织活检是靶向基因检测极其重要的dna来源,但在很多情况下,存在肿瘤组织获得比较困难、dna获得量较小的情况。因此,针对某些突变对应同种靶向用药的情况,使用有限量的dna实现这些突变的同时检测就变得很有意义。技术实现要素:为了解决至少部分上述技术问题,本发明的发明人发现,通过使用能够特异性识别并点对点结合至野生型kras基因靶序列的结合物,并通过调整作为引物的检测核苷酸和结合物的识别区域的位置关系,并同时调整反应体系中结合物和检测核苷酸的浓度比例可以一次性快速确定靶序列中是否存在基因突变,而无需多次检测反应,且提高了用于cfdna检测的灵敏度。至少基于上述内容完成了本发明。具体地,本发明包括以下内容。本发明的一方面,提供检测样品中kras基因的突变的方法,其包括:构建dna扩增反应体系,所述dna扩增反应体系包含能够特异性识别并结合至野生型kras基因的待测靶序列的结合物,和检测核苷酸;利用所述dna扩增反应体系进行dna扩增反应;判断是否获得包含所述待测靶序列的扩增产物,若获取所述扩增产物,则所述靶序列中存在突变,反之,则所述靶序列中不存在突变;其中所述结合物由下式(1)的重复单元构成,其中,n为6-20的整数,b为选自由a、t、g和c组成的组;且所述结合物与所述野生型kras基因的待测靶序列结合后的解链温度为70℃及以上,当所述待测靶序列中包含突变时,则所述结合物不能与所述待测靶序列结合;其中所述检测核苷酸能够特异性识别并结合kras基因,且其结合序列与所述待测靶序列中突点位点对应的位置不重叠。在某些实施方案中,所述检测样品中kras基因的突变的方法,式(1)中n=14,且沿从左到右的方向各重复单元中的b依次为tacgccaccagctc。在某些实施方案中,所述检测样品中kras基因的突变的方法中,所述野生型kras基因的待测靶序列包含甘氨酸密码子。在某些实施方案中,所述检测样品中kras基因的突变的方法中,所述待测靶序列包含所述野生型kras基因上第二外显子中密码子12和密码子13所对应的序列。在某些实施方案中,所述检测样品中kras基因的突变的方法中,所述检测核苷酸包括第一核苷酸、第二核苷酸和第一探针;其中所述第一核苷酸的结合序列位于所述待测靶序列的上游,和所述第二核苷酸的结合序列位于所述待测靶序列的下游。在某些实施方案中,所述检测样品中kras基因的突变的方法中,其中所述反应体系还包括用于扩增内参序列的第三核苷酸、第四核苷酸和第二探针。优选地,所述第三核苷酸和所述第四核苷酸的结合序列分别位于kras基因上。更优选地,所述第三核苷酸和所述第四核苷酸的结合序列各自们于所述待测靶序列的上游,或者各自位于所述待测靶序列的下游。在某些实施方案中,所述检测样品中kras基因的突变的方法中,所述dna扩增反应为荧光定量pcr,且判断是否获得所述扩增产物的步骤包括:获取与所述待测靶序列对应的所述第一荧光探针的循环数值ct1;获得与第三核苷酸和第四核苷酸列对应的所述第二荧光探针的循环数值ct2;当ct1≤35,ct2≤31,且δct1=|ct1-ct2|≤8时,所述dna扩增反应中产生所述扩增产物,否则所述dna扩增反应中未产生所述扩增产物。在某些实施方案中,所述检测样品中kras基因的突变的方法中,所述荧光定量pcr的反应体系基于20ul总体积包含7-8ng模板,且反应条件如下:95℃10min95℃15s,70℃15s,60℃1min,40个循环。在某些实施方案中,所述检测样品中kras基因的突变的方法中,所述突变为点突变。在某些实施方案中,所述检测样品中kras基因的突变的方法中,所述样品为组织或血液样品,例如血浆和/或血清。在某些实施方案中,所述检测样品中kras基因的突变的方法中,所述kras基因来源于gdna或cfdna。有益效果:本发明的检测方法可以一次性同时检测kras基因上多种点突变,本方法中利用能够特异性识别并结合至野生型kras基因待测靶序列的结合物,对待测靶序列进行dna扩增反应,通过是否获得待测靶序列的扩增产物判断待测靶序列中是否存在突变。进一步,本方法中仅需要少量待检测dna,便可以判断待测靶序列中是否存在突变,且灵敏度高(0.5%),准确、快速。附图说明图1是本发明其中一个实施例以组织dna为样本检测kras基因的突变的荧光定量pcr扩增曲线;图2是本发明其中一个实施例以组织dna为样本检测kras基因的突变的荧光定量pcr扩增曲线;图3是本发明其中一个实施例以组织dna为样本检测kras基因的突变的荧光定量pcr扩增曲线;图4是本发明其中一个实施例以组织dna为样本检测kras基因的突变的荧光定量pcr扩增曲线;图5是本发明其中一个实施例以组织dna为样本检测kras基因的突变的荧光定量pcr扩增曲线;图6是本发明其中一个实施例以组织dna为样本检测kras基因的突变的荧光定量pcr扩增曲线;图7是本发明其中一个实施例以组织dna为样本检测kras基因的突变的荧光定量pcr扩增曲线;图8是本发明其中一个实施例以血液cfdna为样本检测kras基因的突变的荧光定量pcr扩增曲线;图9是本发明其中一个实施例以血液cfdna为样本检测kras基因的突变的荧光定量pcr扩增曲线;图10是本发明其中一个实施例以血液cfdna为样本检测kras基因的突变的荧光定量pcr扩增曲线;图11是本发明其中一个实施例以血液cfdna为样本检测kras基因的突变的荧光定量pcr扩增曲线;图12是本发明所述的检测kras基因上多种点突变的方法的流程图。具体实施方式现详细说明本发明的多种示例性实施方式,该详细说明不应认为是对本发明的限制,而应理解为是对本发明的某些方面、特性和实施方案的更详细的描述。应理解本发明中所述的术语仅仅是为描述特别的实施方式,并非用于限制本发明。另外,对于本发明中的数值范围,应理解为具体公开了该范围的上限和下限值以及它们之间的每个中间值。在任何陈述值或陈述范围内的中间值以及任何其他陈述值或在所述范围内的中间值之间的每个较小的范围也包括在本发明内。这些较小范围的上限和下限可独立地包括或排除在范围内。除非另有说明,否则本文使用的所有技术和科学术语具有本发明所述领域的常规技术人员通常理解的相同含义。虽然本发明仅描述了优选的方法和材料,但是在本发明的实施或测试中也可以使用与本文所述相似或等同的任何方法和材料。本说明书中提到的所有文献通过引用并入,用以公开和描述与所述文献相关的方法和/或材料。在与任何并入的文献冲突时,以本说明书的内容为准。本发明中,名词术语既包括单数形式,也包括复数形式,除非上下文另行明确指出。本发明中所述的“至少一种”不仅仅指包含“一个”或“一种”的情况,更重要的还包含“多个”或“多种”的情况。本发明中,术语“结合物”是指可以通过化学键、亲和性或碱基互补等方式与基因相结合的任何物质。优选地,所述结合物为由单体经固相合成。优选地,所述结合物由重复单元构成。优选地,结合物具有不带电荷的骨架结构,以便于结合物以碱基配对的方式与dna结合。优选地,所述结合物不易被已知的蛋白酶和核酸酶降解,其与dna结合后具有极强的特异性和热稳定性。在示例性实施方案中,所述结合物与dna具有极强的稳定性,优选地,其解链温度tm值比dna-dna、dna-rna的tm高1-10℃,例如,高2、3、4、5、6、7、8或9℃。在示例性实施方案中,所述结合物与所述野生型kras基因的待测靶序列结合后的解链温度为70℃以上,进一步优选,所述解链温度为80℃以上;更优选,所述解链温度为85℃以上;还优选所述解链温度为90℃以下。例如70±5℃,优选71±3℃。在示例性实施方案中,在所述结合物的骨架结构引入修饰基团,以改善结合物与dna序列结合的亲和力和序列的选择性。在结合物进行修饰的方法包括在骨架结构中引入修饰或引入碱基衍生结构的修饰,例如,在骨架结构上引入手性和非手性基团以获得与dna的特定方向结合性;提高骨架结构的强度;在骨架结构上直接引入阳离子功能基团;或与特定的分子结合使其能够穿透目标细胞。在示例性实施方案中,在结合物的骨架结构中主要通过引入五元或六元环结构,进一步在骨架结构中接上反-1,2-环己烷二胺、吡咯烷或顺-环戊烷;进一步地,在结合物重复单元上插入碱基修饰,进一步地,碱基修饰包括:引入能够进行荧光标记的类碱基;对胸腺嘧啶和胞嘧啶进行杂环化修饰;引入胞嘧啶,如,2,6-二氨基嘌呤等天然的碱基类似物;在尿嘧啶的5位引入功能基团。本发明中,所述的结合物的重复单元中b依次为tacgccaccagctc,在结合物的碱基中插入修饰-tacgcc*1a*2ccagctc-,其中,c*1表示在胞嘧啶进行杂环修饰,a*2表示在腺嘌呤被二氨基嘌呤替代,提高结合物稳定性和tm值;进一步地,在结合物的序列中至少有一个腺嘌呤被二氨基嘌呤替代;进一步地,在结合物的碱基中插入修饰-t*3acgcc*1a*2ccagctc-,其中,t*1表示胸腺嘧啶由巯基嘧啶替代。本发明检测样品中kras基因的突变的方法中,构建dna扩增反应体系,所述dna扩增反应体系包含能够特异性识别并结合至野生型kras基因的待测靶序列的结合物;利用所述dna扩增反应体系进行dna扩增反应;判断是否获得包含所述待测靶序列的扩增产物,若获取所述扩增产物,则所述靶序列中存在点突变,反之,则所述靶序列中不存在点突变。其中,所述结合物由下式(1)的重复单元构成,其中,n为6-20的整数,b为选自由a、t、g和c组成的组;且所述结合物与所述野生型kras基因的待测靶序列结合后的解链温度为70℃以上,当所述待测靶序列中包含点突变时,则所述结合物不能与所述待测靶序列结合。进一步地,所述结合物中n=14,且沿从左到右的方向各重复单元中的b依次为tacgccaccagctc。进一步其中,至少有一个腺嘌呤被二氨基嘌呤替代,所述解链温度为70℃;进一步地,所述解链温度为72℃、74℃、75℃等;进一步地,所述解链温度为80℃;进一步地,所述解链温度为85℃;进一步地,所述解链温度为90℃。在某些实施方案中,需要调整反应体系中的结合物和检测核苷酸的浓度比例为3:1-5:1,优选4:1,由此可进一步提高检测灵敏度。在某些实施方案中,所述野生型kras基因的待测靶序列包含甘氨酸密码子。进一步地,所述野生型kras基因的待测靶序列包含所述野生型kras基因上第二外显子密码子中12和密码子13所对应的序列。在某些实施方案中,所述dna扩增反应体系中包括检测核苷酸,所述检测核苷酸包括第一核苷酸、第二核苷酸、第一探针。优选地,反应体系进一步包括用于扩增内参的第三核苷酸、第四核苷酸和第二探针。在某些实施方案中,第一核苷酸和/或第二核苷酸的结合序列与所述待测靶序列不重叠,例如,所述第一核苷酸的结合序列位于所述待测靶序列的上游,和所述第二核苷酸的结合序列位于所述待测靶序列的下游。在某些实施方案中,第一核苷酸的结合序列不包含待测靶序列中突点位点对应的位置。优选地,第一核苷酸的结合序列距待测靶序列中突变位点的位置为1-20bp,更优选为1-10bp,例如2、3、4、5、6、7、8、9bp。优选地,第二核苷酸位于待测靶序列的下游。本发明的发明人发现,重叠区域的长度在特定范围内具有优异的技术效果。因为如果重叠区域过短,则噪音过大,灵敏度大大降低,甚至降至5%以上。另一方面,如果重叠区域过长,则本发明的结合物影响到作为引物的检测核苷酸的结合,不利于pcr中的扩增反应顺利进行,最终也会影响到检测的灵敏度。使用本发明的结合物与核苷酸,特别是检测核苷酸的组合可使灵敏度提高至例如约0.5%,相比现有技术提高约50%。如果重叠区域的长度进一步延长,例如包含了突变位置的序列,甚至一个碱基,则不能通过一次反应特定位点所有类型的突变,可能仅仅检测一种类型的突变,这是本发明所不期望的。在某些实施方案中,第一核苷酸的结合序列与待测靶序列具有至少重叠区域,所述重叠区域的长度为1-10bp,优选1-8bp,例如,1、2、3、4、5、6、7bp等。在某些实施方案中,所述第一探针和所述第二探针均为荧光探针,且所述第一探针和所述第二探针的荧光报告基团不同;第三核苷酸和第四核苷酸组成内参引物,通过第三核苷酸和第四核苷酸对其对应的序列的扩增,以判断待检测dna序列的完整性。进一步地,所述第一探针的荧光报告基团为fam或vic,相对应地,所述第二探针的荧光报告基团为vic或fam,所述第一探针和/所述第二探针上还包括mgb-nfq猝灭基团。在某些实施方案中,所述第一核苷酸序列为:-aattagctgtatcgtcaaggcactctt-,所述第二核苷酸序列为-cattatttttattataaggcctgctgaa-;进一步地,所述第三核苷酸序列为-gatgattcgaaagcttcattaatttgt-,所述第四核苷酸序列为-ggtgcatgcagttgattacttcttatt-;进一步地,所述第一探针序列为-tgactgaatataaacttg-,第一探针的荧光报告基团为fam,所述第一探针的猝灭基团为mgb-nfq;所述第二探针序列为-cacaccaacattca-第二探针的荧光报告基团为vic,所述第二探针的猝灭基团为mgb-nfq。在某些实施方案中,所述检测样品中kras基因的突变的方法中,所述dna扩增反应为荧光定量pcr,且判断是否获得所述扩增产物的步骤包括:获取与所述待测靶序列对应的所述第一荧光探针的循环数值ct1;获得与第三核苷酸和第四核苷酸列对应的所述第二荧光探针的循环数值ct2;当ct1≤35,ct2≤31,且δct1=|ct1-ct2|≤8时,则所述dna扩增反应中产生所述扩增产物,否则所述dna扩增反应中未产生所述扩增产物。所述荧光定量pcr的反应体系基于20ul总体积包含7-8ng模板,且反应条件如下:95℃10min95℃15s,70℃15s,60℃1min,40个循环。在60℃采集荧光。实施例在没有特别说明的情况下,本发明中使用的任何试剂均为市场购买的一般试剂。1.样本提取使用dna提取试剂对组织dna进行提取,从7个不同的组织样本中分别提取dna,分别为样品1、样品2、样品3、样品4、样品5、样品6、和样品7,其中样品7为野生型样品;dna提取主要步骤如下:将组织样本暂存于4℃的冰箱中,采用美国qiagen公司的组织dna提取试剂盒进行提取,具体步骤参见试剂盒附带的使用说明书,在此不再赘述。首先对新鲜血液进行血浆分离,然后使用qiagen公司的提取试剂盒提取血浆中的cfdna,从4个不同的血液样本中分别提取血液dna,分别为样品8、样品9、样品10和样品11,其中,样品11为健康人样品。dna提取主要步骤如下:将全血样本暂存于4℃的冰箱中,采用美国qiagen公司的游离dna提取试剂盒进行提取,具体步骤参见试剂盒附带的使用说明书,在此不再赘述。2.配置荧光定量pcr的反应体系,如表1所示:表1dna2.00μm第一核苷酸和第二核苷酸0.25μm第一探针0.25μm结合物0.90μm第三核苷酸和第四核苷酸0.25μm第二探针0.25μmdntp2.00μmmgcl20.40μmtaq酶10.00μm去离子水3.70μm总计20.00μm3.荧光定量pcr取出预先保存在-20℃环境中的dntp、mgcl2、taq酶,和表2所示的结合物、第一核苷酸、第二核苷酸、第三核苷酸、第四核苷酸、第一探针和第二探针。按照下述pcr反应程序,分别对样品1、样品2和样品3进行荧光定量pcr实验。表2序列名称序列结合物tacgccaccagctc第一核苷酸序列aattagctgtatcgtcaaggcactctt第二核苷酸序列cattatttttattataaggcctgctgaa第三核苷酸序列gatgattcgaaagcttcattaatttgt第四核苷酸序列ggtgcatgcagttgattacttcttatt第一探针荧光报告基团为famtgactgaatataaacttg第二探针荧光报告基团为viccacaccaacattcapcr反应程序:在60℃采集荧光。ct值表示每个反应管内的荧光信号到达所设定的阈值所经历的循环数。其中,样片1至样品11的检测结果如下:样品1的反应管内ct1=29.49,ct2=25.95,δct1=ct1-ct2=3.54≤8表明样品1进行荧光定量pcr时,获得扩增产物,则结合物没有与kras基因相结合,kras基因上的特异位点中至少存在一种突变;样品2的反应管内ct1=31.51,ct2=26.23,δct1=ct1-ct2=5.28≤8表明样品2进行荧光定量pcr时,获得扩增产物,则结合物没有与kras基因相结合,kras基因上的特异位点中至少存在一种突变;样品3的反应管内ct1=31.03,ct2=26.25,δct1=ct1-ct2=4.78≤8表明样品3进行荧光定量pcr时,获得扩增产物,则结合物没有与kras基因相结合,kras基因上的特异位点中至少存在一种突变;样品4的反应管内ct1=31.81,ct2=26.26,δct1=ct1-ct2=7.55≤8表明样品4进行荧光定量pcr时,没有获得扩增产物,则结合物与kras基因相结合,kras基因上的特异位点中不存在突变;样品5的反应管内ct1=31.11,ct2=26.48,δct1=ct1-ct2=4.63≤8表明样品5进行荧光定量pcr时,获得扩增产物,则结合物没有与kras基因相结合,kras基因上的特异位点中至少存在一种突变;样品6的反应管内ct1=33.70,ct2=26.20,δct1=ct1-ct2=7.5≤8表明样品6进行荧光定量pcr时,没有获得扩增产物,则结合物与kras基因相结合,kras基因上的特异位点中不存在突变;样品7的反应管内ct1于小于阈值,无ct1,ct2=26.27;样品8的反应管内ct1=31.50,ct2=27.63,δct1=ct1-ct2=3.87≤8表明样品8进行荧光定量pcr时,获得扩增产物,则结合物没有与kras基因相结合,kras基因上的特异位点中至少存在一种突变;样品9的反应管内ct1=34,ct2=27.69,δct1=ct1-ct2=6.31≤8表明样品9进行荧光定量pcr时,获得扩增产物,则结合物没有与kras基因相结合,kras基因上的特异位点中至少存在一种突变;样品10的反应管内ct1=34.72,ct2=27.69,δct1=ct1-ct2=7.03≤8表明样品10进行荧光定量pcr时,获得扩增产物,则结合物没有与kras基因相结合,kras基因上的特异位点中至少存在一种突变;样品11的反应管内无ct1,ct2=25.68;4.验证为了验证本方法的准确性,利用二代测序技术(nsg)对样品1至样品11进行测序,结果发现:样品1中kras基因存在g12d点突变,且突变概率为5%;样品2中kras基因存在g12d点突变,且突变概率为1%;样品3中kras基因存在g12v点突变,且突变概率为5%;样品4中kras基因存在g12v点突变,且突变概率为1%;样品5中kras基因存在g13d点突变,且突变概率为5%;样品6中kras基因存在g13d点突变,且突变概率为1%;样品7中kras基因第二外显子中密码子12和密码子13所对应的序列上无突变;样品8中kras基因存在g12d点突变,且突变概率为5%;样品9中kras基因存在g12d点突变,且突变概率为1%;样品10中kras基因存在g12d点突变,且突变概率为0.5%;样品11中kras基因第二外显子中密码子12和密码子13所对应的序列上无突变。且同时通过数字pcr技术对上述样品进行验证试验。通过上述验证,利用本发明可以快速检测出kras基因上的多个点突变,且检测灵敏度0.5%。在不背离本发明的范围或精神的情况下,可对本发明说明书的具体实施方式做多种改进和变化,这对本领域技术人员而言是显而易见的。由本发明的说明书得到的其他实施方式对技术人员而言是显而易见得的。本申请说明书和实施例仅是示例性的。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1