转换共刺激受体的制作方法
本申请是发明名称为“转换共刺激受体”、申请号为“201280041432.6”、申请日为2012年7月27日的申请的分案申请。
相关申请的交叉引用
本申请要求于2011年7月29日提交的美国专利申请系列号61/513,259的优先权,该申请的内容整体通过引用并入本文。
本发明背景
免疫系统的一般原理是t细胞感知其微环境,然后取决于它们所感知的信号,或是被激活或是被抑制。cd28基因家族由传递阳性信号的2个基因(cd28和icos),以及递送阴性信号的3个基因(ctla4、pd-1和btla)组成(riley等人,2005,blood105:13-21)。pd-1的配体是pdl1和pdl2。众所周知,pd-1配体经常在肿瘤微环境中表达,并且t细胞上的pd-1与pdl1或pdl2的接合可以导致t细胞失活。
此时,防止由pd-1或btla配体递送的阴性信号的仅有方式是得到与pd-1或btla结合的拮抗性抗体或融合蛋白,这是一种现在正在早期临床试验中测试的方式(cheever等人,2008,immunolrev222:357-68)。另一方式将是得到可能抑制pd-1信号转导或btla信号转导的小分子化合物。当前防止pd-1灭活t细胞的方式是用pd-1拮抗性抗体对患者进行全身治疗。
上述方式两者均具有局限性,因为驻留在肿瘤微环境以及整个免疫系统中的t细胞都免于所述全身治疗所导致的灭活,并且预期这会在一些患者中导致自身免疫或全身炎症反应综合征(beck等人,2006,jclinoncol24:2283-9;blansfield等人,2005,jimmunother28:593-8;dougan等人,2009,annualreviewofimmunology27:83-117)。
因此,在本领域中对于用于过继疗法的有效形式的组合物和方法存在迫的需求。本发明解决了这种需求。
发明概述
本发明提供了这样的融合蛋白,其包含第一结构域和第二结构域,其中第一结构域是与阴性信号相关联的多肽,第二结构域是与阳性信号相关联的多肽。
在一个实施方案中,第一结构域是与阴性信号相关联的多肽的胞外结构域的至少一部分,第二结构域是与阳性信号相关联的多肽的胞内结构域的至少一部分。
在一个实施方案中,所述融合蛋白还包含跨膜结构域。在另一个实施方案中,所述跨膜结构域是与阴性信号相关联的多肽的跨膜结构域或与阳性信号相关联的多肽的跨膜结构域。
在一个实施方案中,与阴性信号相关联的多肽选自ctla4、pd-1和btla。
在一个实施方案中,与阳性信号相关联的多肽选自cd28和icos。
本发明还提供了被改造以表达融合蛋白的细胞,所述融合蛋白包含第一结构域和第二结构域,其中所述结构域是与阴性信号相关联的多肽,所述第二结构域是与阳性信号相关联的多肽。
在一个实施方案中,所述细胞还包含嵌合抗原受体(car),其中所述car包含特异性抗体的抗原识别结构域和cd3-ζ链的胞内结构域。
本发明还提供了这样的载体,其包含第一结构域和第二结构域,其中所述第一结构域是与阴性信号相关联的多肽,所述第二结构域是与阳性信号相关联的多肽。
本发明提供了治疗癌症患者的方法。在一个实施方案中,方法包括向所述患者施用被遗传改造以表达融合蛋白的t细胞,融合蛋白包含第一结构域和第二结构域,其中第一结构域是与阴性信号相关联的多肽,且第二结构域是与阳性信号相关联的多肽。
在一个实施方案中,t细胞被进一步遗传改造以表达car,其中所述car包含特异性抗体的抗原识别结构域和cd3-ζ链的胞内结构域。
在一个实施方案中,t细胞是自体t细胞。
附图简述
当结合附图阅读时,下面对本发明的优选实施方案的详述将得到更好的理解。为了说明本发明,在附图中显示了目前优选的实施方案。然而,应当理解,本发明不限于在附图中所示的实施方案的准确配置和手段。
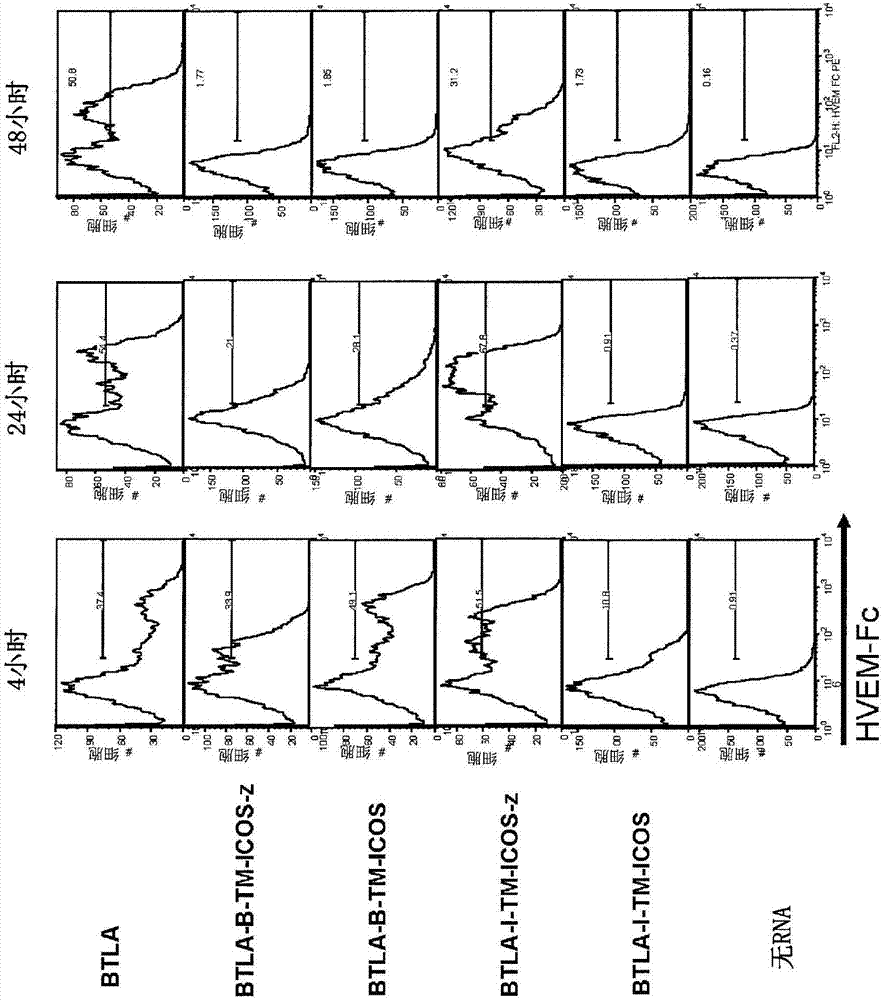
图1,包括图1a至1c,是证明btla信号可以以嵌合共刺激受体(ccr)或另外地称为转换受体的形式被转变成其他信号的一系列图像。图1a是描绘嵌合转换受体的示意性图示的图像。图1b是证明在所指示的不同时刻通过hvem-fc融合蛋白检测到btla的表面表达的图像。图1c是描绘由电穿孔的t细胞产生的il-2的图像,所述t细胞用btla配体阴性细胞系(ktplocd86a2)或btla配体hvem阳性细胞系(ktplocd86a2hvem)刺激。刺激后24小时,通过elisa测定il的产生。结果显示通过将btla胞外结构域与icos和cd3ζ两者的胞内结构域融合,t细胞可以通过刺激表达btla配体的hvem的细胞系而被激活,表明btla信号可以以嵌合共刺激受体的形式转变成其它信号。
图2,包括图2a至2c,是证明btla信号可以通过btla-cd28ccr被转变成cd28信号的一系列图像。
图3,包括图3a和3b,是证明btla信号可以通过btla-icosccr转变成icos信号的一系列图像。结果显示,由btla-icos转变的icos信号增加th17细胞产生。
图4,包括图4a至4d,是证明pd1信号可以转变成cd28信号的一系列图像。
图5,包括图5a和5c,是证明由于pd1-cd28ccr共同引入逆转pd1抑制的一系列图像。
图6,包括图6a至6c,是证明pd1信号转变成icos信号的一系列图像。
图7是证明pd1wt对细胞因子产生的抑制性作用被pd1嵌合构建物拯救的图像。
图8是证明pd-1嵌合受体不影响粒酶b产生的图像。
图9是证明在存在或不存在pd1时观察到cd8t细胞的杀伤活性的最小差异的图像。
图10是显示pd-1嵌合受体对t细胞增殖的作用的图像。
图11是显示pd1-cd28嵌合受体增加cd8t细胞的数目的图像。
详述
本发明大体上涉及融合蛋白受体,当展示在细胞上时其可以将传输至细胞的阴性信号转变成阳性信号。该融合蛋白是嵌合蛋白,其中所述蛋白包含至少两个结构域,其中第一结构域是与阴性信号相关联的多肽以及第二结构域是与阳性信号相关联的多肽。在一个实施方案中,第一结构域结合抑制性因子并且激活所述融合蛋白,其中信号通过第二结构域发送,产生传输至细胞的阳性信号。以此方式,融合蛋白能够将细胞中另外的阴性信号转变成阳性信号。因此,本发明可以被认为涵盖转换受体,所述转换受体能够将阴性信号转换为阳性信号以增强免疫应答。免疫应答的增强可以治疗与免疫应答不足相关的疾病。
本发明基于下列的发现:t细胞可以被改造以表达转换受体以便利用这样的事实:t细胞能够感知其微环境从而根据它们所感知的信号被激活或抑制。例如,本发明利用这样的事实:在肿瘤微环境中存在抑制t细胞活性的配体。t细胞被改造以表达转换受体,其中第一结构域能够被肿瘤微环境中的抑制性配体激活,并且借助于通过转换受体的第二结构域的信号将传输至t细胞的另外的抑制性信号转换为阳性信号。因此,本发明提供了一种疗法,其提供改善的治疗指数,具有较少的毒性以及提供有效的一次治疗的能力,并且避免了继续施用抗体的需要。
在一些情况下,细胞在被施用于需要其的患者之前被遗传修饰。优选地,细胞可以被遗传修饰以稳定地表达本发明所需的转换受体。在其他情况下,细胞可以被进一步修饰以在其表面上表达抗体结合结构域,赋予新的抗原特异性,所述抗原特异性是mhc非依赖性的(例如,嵌合抗原受体(car))。car将特异性抗体的抗原识别结构域与cd3-ζ链或fcγri蛋白的胞内结构域组合成单一嵌合蛋白质。在此背景下,细胞被改造以表达转换受体和car两者。
本发明的修饰细胞能够在体内复制,产生长期持久性,可以形成持续的肿瘤控制。
本发明还提供了制备本发明的转换受体的方法,以及在癌症的研究和治疗中使用这些转换受体的方法。
定义
除非另有定义,本文中使用的所有技术和科学术语具有与本发明所述领域的普通技术人员通常理解的相同含义。尽管可在测试本发明的实践中使用类似于或等于本文描述的那些的任何方法和材料,但优选的材料和方法在本文中进行描述。在描述和要求保护本发明中,将使用以下术语。
也应理解本文使用的术语仅是为了描述具体实施方式的目的,并不意欲是限制性的。
本文使用冠词“一(a)”和“一(an)”,指的是该冠词语法对象的一个或多于一个(即,指的是至少一个)。以例子说明,“一元件”表示一个元件或多于一个的元件。
如本文使用的“大约”,当指的是可测量的值诸如量、时间持续时间等时,意指涵盖从指定值±20%或±10%的变化,更优选±5%,甚至更优选±1%,和还要更优选±0.1%的变化,只要这种变化适于实施公开的方法。
术语“抗体”,如本文所用的,指的是与抗原特异性结合的免疫球蛋白分子。抗体可为源于天然来源或源于重组来源的完整的免疫球蛋白,并可为完整免疫球蛋白的免疫反应部分。抗体通常为免疫球蛋白分子的四聚物。本发明中的抗体可以以多种形式存在,包括例如,多克隆抗体、单克隆抗体、fv、fab和f(ab)2,以及单链抗体和人源化抗体(harlow等人,1999,见:usingantibodies:alaboratorymanual(使用抗体:实验室手册),coldspringharborlaboratorypress,ny;harlow等人,1989,见:antibodies:alaboratorymanual(抗体:实验室手册),coldspringharbor,newyork;houston等人,1988,proc.natl.acad.sci.usa85:5879-5883;bird等人,1988,science242:423-426)。
如本文所用的术语“抗原”或“ag”被定义为激发免疫应答的分子。该免疫应答可涉及抗体产生,或特异性免疫竞争细胞的激活,或两者。技术人员将理解任何大分子,实际上包括所有的蛋白质或肽,可用作抗原。此外,抗原可源自重组或基因组dna。技术人员将理解任何dna(包括编码引起免疫应答的蛋白质的核苷酸序列或部分核苷酸序列)因此编码“抗原”,如该术语在本文中使用那样。此外,本领域技术人员将理解抗原不必仅由基因的全长核苷酸序列编码。容易显而易见的是,本发明包括但不限于,多于一个的基因的部分核苷酸序列的用途,并且这些核苷酸序列以各种各样的组合进行排列,以引起所需的免疫应答。此外,技术人员将理解,抗原根本不必由“基因”编码。容易显而易见的是,抗原可被产生、合成或可源自生物学样品。这种生物学样品可包括但不限于组织样品、肿瘤样品、细胞或生物学流体。
如本文所用的术语“抗肿瘤效应”,指的是生物学效应,其可由肿瘤体积的减小、肿瘤细胞数的减少、转移灶数目的减少、预期寿命的增加或与癌性病症相关的各种生理症状的改善来显示。“抗肿瘤效应”也可由本发明的肽、多核苷酸、细胞和抗体在预防肿瘤在首发位置出现的能力来显示。
如本文所用的,术语“自体”可以用来指源自相同个体、随后被再次引入该个体的任何物质。
“同种异体的(allogeneic)”指的是源自相同物种的不同动物的移植物。
“异种的(xenogeneic)”指的是源自不同物种的动物的移植物。
如本文所用的,“生物学活性或免疫学活性”是指根据本发明的融合蛋白,其具有与作为本发明的融合蛋白的结构单元的单一野生型蛋白相似的结构功能(但不一定达到相同程度),和/或相似的调控功能(但不一定达到相同程度),和/或相似的生物化学功能(但不一定达到相同程度)和/或免疫学活性(但不一定达到相同程度)。
如本文所用的术语“癌症”被定义为以畸变细胞的快速和失控生长为特征的疾病。癌症细胞可局部播散或通过血流和淋巴系统播散至身体的其他部分。各种癌症的例子包括但不限于乳腺癌、前列腺癌、卵巢癌、子宫颈癌、皮肤癌、胰腺癌、结肠直肠癌、肾癌、肝癌、脑癌、淋巴瘤、白血病、肺癌等等。
“嵌合蛋白”是指任何单一多肽单元,其包含两个不同的多肽结构域,其中所述两个结构域不是该相同多肽单元内天然存在的。典型地,此嵌合蛋白通过表达cdna构建体来制备,但可以通过本领域中已知的蛋白合成方法制备。
如本文所用的术语“衍生物”就氨基酸序列而言是指本发明的融合蛋白的化学修饰。
“编码”指的是多核苷酸诸如基因、cdna或mrna中用作用于合成生物学过程中的其他多聚体和大分子的模板的核苷酸的特异性序列的固有性质,所述多聚体和大分子具有定义的核苷酸序列(即,rrna、trna和mrna)或定义的氨基酸序列中的任一个以及由其得到的生物学性质。因此,如果对应于编码蛋白的基因的mrna的转录和翻译在细胞或其他生物学系统中产生蛋白质,则该基因编码所述蛋白质。其核苷酸序列与mrna序列相同并通常提供在序列表中的编码链,和用作转录基因或cdna的模板的非编码链两者,都可被称为编码该基因或cdna的蛋白质或其他产物。
除非另有规定,“编码氨基酸序列的核苷酸序列”包括为彼此的简并形式并编码相同的氨基酸序列的所有的核苷酸序列。编码蛋白质或rna的核苷酸序列可包括内含子。
“有效量”或“治疗有效量”在本文中可互换使用,并且指的是如本文所述有效实现特定生物学结果的化合物、制剂、材料或组合物的量。这种结果可以包括,但不限于,如通过本领域中合适的任何方式测定的对病毒感染的抑制。
如本文所用的“内源的”指的是来自生物体、细胞、组织或系统的或在生物体、细胞、组织或系统内产生的任何物质。
如本文所用的,术语“外源的”指的是从生物体、细胞、组织或系统外引入的或在生物体、细胞、组织或系统外产生的任何物质。
如本文所用的术语“表达”被定义为由它的启动子驱动的特定核苷酸序列的转录和/或翻译。
“表达载体”指的是包含重组多核苷酸的载体,所述重组多核苷酸包含可操作地连接至待表达的核苷酸序列的表达控制序列。表达载体包含足够的用于表达的顺式作用元件;用于表达的其他元件可由宿主细胞供应或在体外表达系统中供应。表达载体包括所有本领域己知的那些,诸如整合了重组多核苷酸的粘粒、质粒(例如,裸露的或包含在脂质体中)和病毒(例如,慢病毒、逆转录病毒、腺病毒和腺相关病毒)。
如本文所用的,术语“融合蛋白”指的是包含两个或更多个不同蛋白质的氨基酸序列的嵌合蛋白。典型地,由本领域中熟知的体外重组技术获得融合蛋白。
“同源的”,如本文所用的,指的是两个聚合分子之间,例如,两个核酸分子诸如两个dna分子或两个rna分子之间,或两个多肽分子之间的亚单位序列同一性。当两个分子两者中的亚单位位置被相同的单体亚单位占据时;例如,如果两个dna分子的每一个中的位置被腺嘌呤占据,则它们在那个位置处是同源的。两个序列之间的同源性是匹配或同源的位置数的直接函数;例如,如果两个序列中的位置的一半(例如,多聚体10个亚单位长度中的5个位置)是同源的,则两个序列是50%同源的;如果所述位置的90%(例如10个中的9个)是匹配的或同源的,则两个序列是90%同源的。
术语“免疫反应”,如本文中所用的,是指刺激和/或激活免疫细胞的可检测结果。
“免疫应答”,如该术语在本文中使用那样,指的是导致激活和/或引起t细胞、b细胞、自然杀伤(nk)细胞和/或抗原递呈细胞的任一个中的效应器功能的过程。因此,免疫应答,如技术人员将要理解的那样,包括,但不限于,辅助t细胞或细胞毒性t细胞应答的任何可检测到抗原特异性或同种异体激活、抗体产生、t细胞介导的同种异体反应的激活,等等。
“免疫细胞”,如该术语在本文中使用那样,指的是参与免疫应答的发起的任何细胞。此类细胞包括,但不限于,t细胞、b细胞、nk细胞、抗原递呈细胞,等。
如本文所用的,“指导材料”包括出版物、记录、图表或任何其他可用于传达本发明组合物和方法的有用性的表达媒介。本发明的试剂盒的指导材料可例如被附加在包含本发明的核酸、肽和/或组合物的容器上,或与包含所述核酸、肽和/或组合物的容器一起运送。可选地,指导材料可与容器分开地运送,目的是指导材料和化合物由接受者配合使用。
“分离的”指从自然状态改变或移出。例如,天然存在于活动物中的核酸或肽不是“分离的”,但与它的自然状态的共存物质部分或完全分离的同一核酸或肽是“分离的”。分离的核酸或蛋白质可以以基本上纯化的形式存在,或例如,可存在于非自然环境,诸如宿主细胞中。
在本发明的内容中,对于通常存在的核酸碱基使用以下缩写。“a”指的是腺苷,“c”指的是胞嘧啶,“g”指的是鸟苷,“t”指的是胸苷,和“u”指的是尿苷。
除非另有规定,“编码氨基酸序列的核苷酸序列”包括为彼此的简并版本并编码相同的氨基酸序列的所有的核苷酸序列。短语编码蛋白质或rna的核苷酸序列也可包括内含子,其程度为编码该蛋白质的核苷酸序列可在某些版本中包含(一个或多个)内含子。
如本文所用的“慢病毒”指的是逆转录病毒科的属。在逆转录病毒中慢病毒是唯一能够感染非分裂细胞的;它们可传递显著量的遗传信息进入宿主细胞的dna,以便它们是基因传递载体的最有效的方法之一。hiv、siv和fiv是慢病毒的所有例子。源自慢病毒的载体提供了实现显著水平的体内基因转移的工具。
术语“调节”免疫应答,如本文所用的,是指与缺少治疗或化合物的哺乳动物中的免疫应答水平相比,和/或与在其他方式相同但未治疗的哺乳动物中的免疫应答水平相比,介导哺乳动物中免疫应答水平的可检测到的增加或减少。该术语涵盖扰乱和/或影响天然信号或应答,由此介导哺乳动物,优选人中的有益的治疗性应答。
“阴性信号”,如本文所使用的,是指诱发与减少增殖、减少激活、减少细胞处理等相关的胞内事件的经典级联的信号。
“阳性信号”,如本文所使用的,是指诱发与增加增殖、增加激活、增加细胞处理等相关的胞内事件的经典级联的信号。
术语“可操作地连接”指的是调控序列和异源核酸序列之间的功能性连接,其导致后者的表达。例如,当第一核酸序列被放置以与第二核酸序列具有功能关系时,第一核酸序列与第二核酸序列可操作地连接。例如,如果启动子影响编码序列的转录或表达,则启动子被可操作地连接至编码序列。通常地,可操作地连接的dna序列是连续的,并且在必要时在相同的阅读框中连接两个蛋白编码区。
免疫原性组合物的“肠胃外”施用包括例如皮下(s.c.)、静脉内(i.v.)、肌肉内(i.m.)或胸骨内注射,或输注技术。
如本文所用的术语“多核苷酸”被定义为核苷酸链。此外,核酸为核苷酸的多聚体。因此,如本文所用的核酸和多核苷酸是可互换的。本领域技术人员具有核酸为可被水解成单体“核苷酸”的多核苷酸的一般常识。单体核苷酸可被水解成核苷。如本文所用的多核苷酸包括但不限于通过本领域中可用的任何手段获得的所有的核酸序列,所述手段包括但不限于重组手段,即,利用普通克隆技术和pcrtm等等从重组文库或细胞基因组克隆核酸序列,和通过合成手段。
如本文所用的,术语“肽”、“多肽”和“蛋白质”可互换使用,并指的是由肽键共价连接的氨基酸残基组成的化合物。蛋白或肽必须包含至少两个氨基酸,和对可包括蛋白质或肽的序列的氨基酸最大数目没有限制。多肽包括任何肽或蛋白质,所述肽或蛋白质包括通过肽键相互连接的两个或更多个氨基酸。如本文所用的,该术语指的是短链和较长链,短链在本领域中也例如通常被称为肽、寡肽和寡聚体;较长链在本领域中通常被称为蛋白质,其具有很多类型。“多肽”包括例如生物学活性片段、基本上同源的多肽、寡肽、同二聚体、异二聚体、多肽的变体、修饰多肽、衍生物、类似物、融合蛋白等等。多肽包括天然肽、重组肽、合成肽或其组合。
如本文所用的术语“启动子”被定义为启动多核苷酸序列的特异性转录需要的,由细胞的合成机器或引入的合成机器识别的dna序列。
如本文所用的,术语“启动子/调控序列”指可操作地连接至启动子/调控序列的基因产物表达所需的核酸序列。在一些例子中,该序列可为核心启动子序列,并且在其他例子中,该序列也可包括基因产物表达所需的增强子序列和其他调控元件。启动子/调控序列可例如为以组织特异方式表达基因产物的序列。
“组成型”启动子为这样的核苷酸序列,其当与编码或指定基因产物的多核苷酸可操作地连接时,使得在细胞的大多数或所有生理学条件下在细胞中产生基因产物。
“诱导型”启动子为这样的核苷酸序列,其当与编码或指定基因产物的多核苷酸可操作地连接时,使得在基本上仅当对应于启动子的诱导物存在于细胞中时,在细胞中产生基因产物。
“组织特异性”启动子为这样的核苷酸序列,其当与编码基因或由基因指定的多核苷酸可操作地连接时,使得基本上只要细胞为对应于启动子的组织类型的细胞,则在细胞中产生基因产物。
术语“对象”意欲包括在其内可引起免疫应答的活生物体(例如,哺乳动物)。
如本文所用的“基本上纯化的”细胞为基本上不含其他细胞类型的细胞。基本上纯化的细胞也指的是已经与在其天然存在状态下与其正常相关联的其他细胞类型分离的细胞。在一些例子中,基本上纯化的细胞群指的是均质细胞群。在其他例子中,该术语简单地指的是已经与在其天然状态下与其正常相关联的细胞分离的细胞。在一些实施方案中,在体外培养细胞。在其他实施方案中,不在体外培养细胞。
如本文所用的术语“治疗性的”是指治疗和/或预防。治疗性效果通过疾病状态的抑制、缓和或根除获得。
如本文所用的术语“转染的”或“转化的”或“转导的”指的是这样的过程,通过该过程外源的核酸被转移或引入宿主细胞中。“转染的”或“转化的”或“转导的”细胞是已经用外源核酸转染、转化或转导的细胞。该细胞包括原代对象细胞和它的子代。
如本文所用的短语“转录控制下”或“可操作地连接”指启动子处于与多核苷酸有关的正确的位置和定向,以控制通过rna聚合酶进行的转录和多核苷酸的表达的起始。
“载体”为物质的组合物,其包含分离的核酸,并且其可用于递送分离的核酸至细胞内部。很多载体在本领域中是己知的,包括但不限于线性多核苷酸、与离子或两性分子化合物相关的多核苷酸、质粒和病毒。因此,术语“载体”包括自主复制的质粒或病毒。该术语也应被解释为包括便于将核酸转移入细胞的非质粒和非病毒化合物,诸如例如聚赖氨酸化合物、脂质体等等。病毒载体的例子包括但不限于,腺病毒载体、腺相关病毒载体、逆转录病毒载体等等。
术语“刺激”是指通过刺激分子(例如,tcr/cd3复合物)与它的关联配体结合,由此介导信号转导事件,诸如但不限于,经由tcr/cd3复合物的信号转导,来诱导的初级应答。刺激可介导某些分子的改变的表达,诸如tgf-β的下调和/或细胞骨架结构的再组织等等。
“激活”,如本文所用的,指的是已经被充分刺激以诱导可检测到的细胞增殖的t细胞的状态。激活也可与诱导的细胞因子产生和可检测到的效应器功能相关联。术语“激活的t细胞”指的是正在经历细胞分裂的t细胞等。激活也可以与下列相关联:产生免疫应答(例如,有丝分裂原诸如cona或pha),可检测地上调表面标志物,诸如cd25,即,il2受体,起始涉及p56lck的磷酸化级联,导致细胞因子和白介素的释放,增加dna合成(所述dna合成可以通过评估3h-胸苷掺入至新生dna链中的水平的方法等来评估),和使细胞增殖。
如本文所用的术语“特异性结合”是指识别并结合样品中存在的关联结合伴侣(例如,t细胞上存在的刺激和/或共刺激分子)蛋白的抗体或配体,但所述抗体或配体基本上不识别或结合样品中的其他分子。
范围:在此公开中,本发明的多个方面可以以范围形式示出。应当理解,以范围形式的描述仅是为了方便和简洁,并不应被解释为对本发明范围的刻板限制。因此,对范围的描述应被考虑为具有具体公开的所有可能的子范围以及处于那个范围内的单个数值。例如,对范围诸如从l至6的描述应被考虑为具有具体公开的子范围诸如从l至3、从l至4、从1至5、从2至4、从2至6、从3至6等,以及该范围内的单个数字,例如,1、2、2.7、3、4、5、5.3和6。不管范围的宽度如何,这均是适用的。
描述
本发明涉及这样的发现:嵌合转换受体可以被设计为将阴性信号转导信号转变为阳性信号。在一个实施方案中,转换受体是嵌合蛋白,所述嵌合蛋白包含与阴性信号相关联的第一蛋白质或其片段,和与阳性信号相关联的第二蛋白质或其片段。与阴性信号相关联的蛋白质的实例包括但不限于ctla-4、pd-1、btla等。与阳性信号相关联的蛋白质的实例包括但不限于cd28、icos等。
本发明涉及嵌合转换受体和相关的融合蛋白,以及利用这些蛋白质治疗癌症的方法。
在一个实施方案中,本发明提供了被改造以表达嵌合转换受体的细胞(例如,t细胞或自然杀伤细胞),其中被改造的细胞表现出抗肿瘤性质。在一些例子中,被改造的细胞还被改造以表达嵌合抗原受体(car)。在一些例子中,本发明的被改造的细胞表现出增强的il-2和ifn-γ产生。在一些例子中,本发明的被改造的细胞被极化以分泌il-17。因此,本发明的被改造的细胞当输注到患者中时可以在患者体内清除肿瘤细胞。
组合物
本发明在一个方面中提供了转换受体,所述转换受体当在细胞中表达时将细胞中的阴性信号转变成阳性信号。例如,此转换受体具有第一结构域和第二结构域,所述第一结构域包含递送阴性信号的多肽;所述第二结构域包含递送阳性信号的多肽。
在一个实施方案中,具有递送阴性信号能力的多肽包括但不限于ctla4、pd-1、btla等。在一个实施方案中,具有递送阳性信号能力的多肽包括但不限于icos、cd28等。
在递送阴性信号的多肽的情况下,合适的第一结构域包括野生型ctla4的变体或衍生物。优选地,此实施方案的转换受体的第一结构域是ctla蛋白的胞外结构域的至少一部分,具体地,所述细胞外结构域的该部分对于与ctla的天然配体结合是必不可少的。胞外结构域的野生型形式的变体,或负责与ctla的天然配体结合的胞外结构域部分也包括在本发明中,只要所述变体提供与野生型蛋白类似的生物学活性水平即可。
在递送阴性信号的多肽的情况下,合适的第一结构域包括野生型pd-1的变体或衍生物。优选地,此实施方案的转换受体的第一结构域是pd-1蛋白的胞外结构域的至少一部分,具体地,所述胞外结构域的该部分对于与pd-1的天然配体结合是必不可少的。胞外结构域的野生型形式的变体,或负责与pd-1的天然配体结合的胞外结构域部分也包括在本发明中,只要所述变体提供与野生型蛋白类似的生物学活性水平即可。
在递送阴性信号的多肽的情况下,合适的第一结构域包括野生型btla的变体或衍生物。优选地,此实施方案的转换受体的第一结构域是btla蛋白的胞外结构域的至少一部分,具体地,所述胞外结构域的该部分对于与btla的天然配体结合是必不可少的。胞外结构域的野生型形式的变体,或负责与btla的天然配体结合的胞外结构域部分也包括在本发明中,只要所述变体提供与野生型蛋白类似的生物学活性水平即可。
在递送阳性信号的多肽的情况下,合适的第二结构域包括icos蛋白的变体或衍生物。优选地,此实施方案中的转换受体的第二结构域是icos蛋白的胞内结构域(也称为内结构域)的至少一部分,具体地,该部分对于触发到达细胞的细胞内成分的信号是必不可少的。icos蛋白的胞内结构域的野生型形式的变体,或负责信号传导的胞内结构域的部分也包括在本发明中,只要所述变体提供与野生型蛋白类似的的生物学活性水平即可。
在递送阳性信号的多肽的情况下,合适的第二结构域包括cd28蛋白的变体或衍生物。优选地,此实施方案中的转换受体的第二结构域是cd28蛋白的胞内结构域(也称为内结构域或胞质的)的至少一部分,具体地,该部分对于触发到达细胞的胞内成分的信号是必不可少的。cd28蛋白的胞内结构域的野生型形式的变体,或负责信号传导的胞内结构域的部分也包括在本发明中,只要所述变体提供与野生型蛋白类似的的生物学活性水平即可。
本发明的转换受体包括对应于胞质的、跨膜的和胞外结构域的多肽,以及对应于胞质的、跨膜的和胞外结构域的较小部分的多肽。在一个实施方案中,所述转换受体包含递送阴性信号的第一多肽的跨膜结构域。在另一个实施方案中,所述转换受体包含递送阳性信号的第二多肽的跨膜结构域。
在本发明的又另一方面中,递送本文所述的任一转换受体的阴性信号成分的第一多肽可以用另一抑制性蛋白(即,防止免疫应答的激活和/或诱导t细胞或其他细胞类型,诸如b细胞、天然杀伤(nk)细胞、nkt细胞、淋巴系祖细胞、树突细胞、单核细胞/巨噬细胞、具有抗原递呈能力的基于组织的巨噬细胞谱系细胞以及许多非专业抗原递呈细胞中的任一种,例如,内皮细胞中的凋亡)替代。抑制性蛋白的实例包括但不限于pd-1、ctla-4、btla、cd160、cd161和cd94的配体;lag-3和cd244(参见2011,wherry,natimmunol.131:492-9)。
根据本发明可以使用任何合适的递送阴性信号的第一多肽,条件是所述多肽结合相应的配体,并且通过此结合事件导致转换受体的激活。根据本发明的一个实施方案,转换受体的递送阴性信号的第一多肽与其相应配体的接合导致该转换受体的递送阳性信号的第二多肽的激活。以此方式,阴性信号可以转变成阳性信号。即,本发明的转换受体的第一多肽可以触发胞内信号传导途径,从而使得本发明的第二多肽的激活导致阴性信号转变成阳性信号。因此,本发明的转换受体的第一多肽的独特特征是其将天然地将引起到达细胞的阴性信号的天然转导信号转变成诱导细胞表现出抗肿瘤特征的阳性信号。
类似地,可以使用任何合适的第二多肽,条件是所述蛋白质可以向细胞发送阳性信号,该阳性信号不同于与转换受体的第一多肽成分相关联的转导信号。第二多肽可以是发送阳性信号或激活信号的蛋白质。本发明的第二多肽的优选实例包括但不限于cd28、cd27、icos、cd137(4-1bb)和tcrζ。
在一个实施方案中,本发明利用了其中存在有大量抑制免疫系统的配体或蛋白质的微环境,其中免疫系统的抑制导致不合乎需要的疾病状态。即,该转换受体可以被改造以包含第一结构域,所述第一结构域结合微环境中的免疫抑制因子并且将正常与所述免疫抑制因子相关联的信号转变成阳性信号,其中所述阳性信号激活细胞以表现出增强的免疫应答。
本发明的优选嵌合蛋白是btla:icos。btla与icos序列的遗传嵌合和重组表达产生嵌合的btla:icos“转换受体”,其显示了归因于btla和icos两者的结构和功能特征。被改造以表达btla:icos的细胞可以将抑制性信号传导重新定向为刺激信号并且由此增强t细胞功能。在一些情况下,细胞被改造以表达btla:icos转换受体以及car。
本发明的另一优选嵌合蛋白是pd1:cd28。pd1与cd28序列的遗传嵌合和重组表达产生嵌合的pd1:cd28“转换受体”,其显示了归因于pd1和cd28两者的结构和功能特征。被改造以表达pd1:cd28的细胞可以将抑制性信号传导重新定向为刺激信号并且由此增强t细胞功能。在一些情况下,细胞被改造以表达pd1:cd28转换受体以及car。
本发明的另一优选嵌合蛋白是ctla4:cd28。ctla4与cd28序列的遗传嵌合和重组表达产生嵌合的ctla4:cd28“转换受体”,其显示了归因于ctla4和cd28两者的结构和功能特征。被改造以表达ctla4:cd28的细胞可以将抑制性信号传导重新定向为刺激信号并且由此增强t细胞功能。在一些情况下,细胞被改造以表达ctla4:cd28转换受体以及car。
本发明的蛋白质可以以大量形式存在。例如,本发明的蛋白质可以是直链或支链多肽的形式。直链的嵌合蛋白可以通过重组dna技术产生。例如,嵌合转录盒可以使用限制性内切酶位点重叠或基于聚合酶链式反应(pcr)的重叠延伸拼接来组装。
支链的多肽嵌合蛋白可以容易地通过模板组装合成肽(tasp)技术来制备(mutter,trendsbiochem.sci.13:260-265(1988))。通过此方法,肽单元被单独合成并且使用化学偶联剂将其共价偶联至多功能载体,诸如核心肽。例如,短杆菌肽s的环状十肽类似物可以用作核心肽,其中两个反向平行的β-片区段(lys-ala-lys)通过两个β-转角连接。可以使用区段缩合策略来将第一和第二蛋白质附接到4个赖氨酸侧链的ε-氨基。
本发明的蛋白质还可以作为通过桥诸如化学键,连接在一起的两个或更多个独立蛋白质存在。例如,在支链结构中使用化学交联剂诸如二硫代-双(丙酸琥珀酰亚胺酯)(dsp),两个或更多个蛋白质成分可以彼此直接共价连接。例如,通过此方法,第一和第二蛋白质可以直接连接。
本发明的嵌合转换受体的特定第一和第二多肽可以根据被治疗的疾病而变化。例如,典型地,当治疗癌症或病毒感染时,使用刺激免疫细胞应答的第二多肽。当治疗其中存在致病性免疫应答的免疫系统病症时,使用抑制性第二多肽。因此,对于癌症和病毒疾病,将抑制性免疫信号转变成激活免疫激活信号的转换受体是合乎需要的。相反,对于自身免疫病,将激活免疫信号转变成抑制性免疫信号的嵌合转换受体是合乎需要的。在此情况下,免疫-抑制性第二蛋白成分可以针对不同的致病免疫效应器,包括t细胞、b细胞、自然杀伤细胞和抗原递呈细胞。
因此,本发明提供了一种转换受体,其当在细胞中表达时将细胞中的阳性信号转变为阴性信号。例如,此转换受体包含第一结构域和第二结构域,所述第一结构域包含递送阳性信号的多肽;所述第二结构域包含在细胞中递送阴性信号的多肽。
遗传修饰
本发明涵盖用慢病毒载体(lv)转导的细胞(例如,t细胞)。在一个实施方案中,lv编码本发明的转换受体,所述转换受体包含第一结构域和第二结构域,所述第一结构域包含递送阳性信号的多肽;所述第二结构域包含递送阴性信号的多肽。
在一个实施方案中,细胞可以进一步用编码嵌合抗原受体(car)的lv转导,所述嵌合抗原受体将特异性抗体的抗原识别结构域与cd3-ζ链或fcγri蛋白的胞内结构域组合成单一嵌合蛋白。
源于逆转录病毒诸如慢病毒的载体是实现长期基因转移的合适工具,因为它们允许转基因长期、稳定的整合并且其在子细胞中传播。慢病毒载体具有超过源自致癌逆转录病毒诸如鼠白血病病毒的载体的额外优点,因为它们可转导非增殖的细胞,诸如肝细胞。它们还具有低免疫原性的额外优点。
简单概括,典型地通过可操作地连接编码所需多肽或其部分的核酸至启动子,并将构建体结合入表达载体,实现本发明的天然或合成核酸的表达。该载体可以适合于复制和整合真核细胞。典型的克隆载体包含可用于调控所需核酸序列表达的转录和翻译终止子、初始序列和启动子。
该核酸可被克隆入许多类型的载体中。例如,该核酸可被克隆入这样的载体中,所述载体包括但不限于质粒、噬菌粒、噬菌体衍生物、动物病毒和粘粒。特定的感兴趣载体包括表达载体、复制载体、探针产生载体和测序载体。
进一步地,表达载体可以以病毒载体形式提供给细胞。病毒载体技术在本领域中是公知的并在例如sambrook等人,molecularcloning:alaboratorymanual(分子克隆,实验室手册),volumes1-3(第三版,coldspringharborpress,ny2001),和其他病毒学和分子生物学手册中进行了描述。可用作载体的病毒包括但不限于逆转录病毒、腺病毒、腺相关病毒、疱疹病毒和慢病毒。通常,合适的载体包含在至少一种生物体中起作用的复制起点、启动子序列、方便的限制性核酸内切酶位点和一个或多个可选择标记(例如,wo01/96584;wo01/29058;和美国专利号6,326,193)。
额外的启动子元件,例如,增强子,调控转录起始的频率。典型地,这些位于起始位点上游的30-110bp区域中,尽管最近已经显示许多启动子也包含起始位点下游的功能元件。启动子元件之间的间隔经常是可变的,以便当元件相对于另一个被倒置或移动时,保持启动子功能。在胸苷激酶(tk)启动子中,启动子元件之间的间隔可被增加至隔开50bp,之后活性才开始下降。取决于启动子,表现出单个元件可协作或独立地起作用,以激活转录。
启动子的一个实例是即刻早期巨细胞病毒(cmv)启动子序列。该启动子序列为能够驱动可操作地连接至其上的任何多核苷酸序列的高水平表达的强组成型启动子序列。然而,也可使用其他组成型启动子序列,包括但不限于类人猿病毒40(sv40)早期启动子、小鼠乳腺肿瘤病毒(mmtv)、人免疫缺陷病毒(hiv)长末端重复(ltr)启动子、momulv启动子、鸟类白血病病毒启动子、epstein-barr病毒即刻早期启动子、rous肉瘤病毒启动子、以及人基因启动子,诸如但不限于肌动蛋白启动子、肌球蛋白启动子、血红蛋白启动子和肌酸激酶启动子。进一步地,本发明不应被限于应用组成型启动子。诱导型启动子也被考虑为本发明的一部分。诱导型启动子的使用提供了分子开关,其当这样的表达是期望的时,能够打开可操作地连接诱导型启动子的多核苷酸序列的表达,或当表达是不期望的时关闭所述表达。诱导型启动子的实例包括但不限于金属硫蛋白启动子、糖皮质激素启动子、孕酮启动子和四环素启动子。
为了评估car多肽或其部分的表达,被引入细胞的表达载体也可包含可选择标记基因或报道基因中的任一个或两者,以便于从寻求通过病毒载体被转染或感染的细胞群中鉴定和选择表达细胞。在其他方面,可选择标记可被携带在单独一段dna上并用于共转染程序。可选择标记和报道基因两者的侧翼都可具有适当的调控序列,以便能够在宿主细胞中表达。有用的可选择标记包括例如抗生素抗性基因,诸如neo等等。
报道基因用于鉴定潜在转染的细胞并用于评价调控序列的功能性。通常地,报道基因为以下基因:其不存在于受体生物体或组织中或由受体生物体或组织表达,并且其编码多肽,该多肽的表达由一些可容易检测到的性质例如酶活性来清楚表示。在dna已经被引入受体细胞后,报道基因的表达在合适的时间进行测定。合适的报道基因可包括编码萤光素酶、β-半乳糖苷酶、氯霉素乙酰基转移酶、分泌型碱性磷酸酶或绿色荧光蛋白基因的基因(例如,ui-tei等人,2000febsletters479:79-82)。合适的表达系统是公知的并可利用己知技术制备或从商业上获得。通常,显示最高水平的报道基因表达的具有最少的5’侧翼区的构建体被鉴定为启动子。这样的启动子区可被连接至报道基因并用于评价试剂的调节启动子-驱动转录的能力。
将基因引入细胞和将基因表达入细胞的方法在本领域中是己知的。在表达载体的情况下,载体可通过在本领域中的任何方法容易地引入宿主细胞,例如,哺乳动物、细菌、酵母或昆虫细胞。例如,表达载体可通过物理、化学或生物学手段转移入宿主细胞。
将多核苷酸引入宿主细胞的物理方法包括磷酸钙沉淀、脂质转染法、粒子轰击、微注射、电穿孔等等。生产包含载体和/或外源核酸的细胞的方法在本领域中是公知的。参见,例如,sambrook等人,molecularcloning:alaboratorymanual(分子克隆:实验室手册)volumes1-3(第三版,coldspringharborpress,ny2001)。
将感兴趣的多核苷酸引入宿主细胞的生物学方法包括使用dna和rna载体。病毒载体,特别是逆转录病毒载体,已经成为最广泛使用的将基因插入哺乳动物例如人细胞中的方法。其他病毒载体可源自慢病毒、痘病毒、单纯疱疹病毒i、腺病毒和腺相关病毒等等。参见,例如美国专利号5,350,674和5,585,362。
将多核苷酸引入宿主细胞的化学手段包括胶体分散系统,诸如大分子复合物、纳米胶囊、微球、珠、和基于脂质的系统,包括水包油乳剂、胶束、混合胶束和脂质体。用作体外和体内递送工具的示例性胶体系统为脂质体(例如,人造膜囊)。
在使用非病毒递送系统的情况下,示例性递送工具为脂质体。考虑使用脂质制剂,以将核酸引入宿主细胞(体外、离体或体内)。在另一方面,核酸可与脂质相缔合。与脂质相缔合的核酸可被封装入脂质体的水性内部中,散布在脂质体的脂双层内,经由与脂质体和寡核苷酸两者都相缔合的连接分子附接至脂质体,陷入脂质体内,与脂质体复合,分散在包含脂质的溶液中,与脂质混合,与脂质合并,作为悬浮液包含在脂质中,包含在胶束中或与胶束复合,或以其他方式与脂质相缔合。脂质、脂质/dna或脂质/表达载体缔合的组合物不限于溶液中的任何具体结构。例如,它们可以双分子层结构,作为胶束存在或具有“坍塌的(collapsed)”结构。它们也可简单地被散布在溶液中,可能形成大小或形状不均一的聚集体。脂质为脂肪物质,其可为天然存在或合成的脂质。例如,脂质包括脂肪小滴,其天然存在于细胞质以及包含长链脂肪族烃和它们的衍生物诸如脂肪酸、醇类、胺类、氨基醇类和醛类的该类化合物中。
适于使用的脂质可从商业来源中获得。例如,二肉豆蔻酰磷脂酰胆碱(“dmpc”)可从sigma,st.louis,mo获得;磷酸二鲸蜡酯(“dcp”)可从k&klaboratories(plainview,ny)获得;胆固醇(“choi”)可从calbiochem-behring获得;二肉豆蔻酰磷脂酰甘油(“dmpg”)和其他脂质可从avantipolarlipids,inc.(birmingham,al)获得。脂质在氯仿或氯仿/甲醇中的原液可在大约-20℃保存。氯仿用作唯一的溶剂,因为它比甲醇更容易蒸发。“脂质体”为通用术语,其包括通过产生封闭的脂质双分子层或聚集体而形成的多种单一和多层脂质载体。脂质体可以以具有含有磷脂双分子层膜和内部水性介质的囊泡结构为特征。多层脂质体具有由水性介质分开的多个脂质层。当磷脂悬浮在过量的水性溶液中时,它们自发形成。在形成密闭的结构并使水和溶解的溶质陷入脂质双分子层之间前,该脂质成分经历自身重排(ghosh等人,1991glycobiology5;505-10)。然而,也包括与正常的囊泡结构相比具有溶液中的不同结构的组合物。例如,脂质可呈现胶束结构或仅作为脂质分子的非均一聚集体而存在。同样考虑的是脂质转染胺-核酸复合物。
治疗性应用
本发明包括这种类型的细胞疗法,其中t细胞被遗传修饰以表达转换受体并且被改造的t细胞被输注至需要其的受体。输注的细胞能够杀死受体中的肿瘤细胞。不像抗体疗法,本发明的被改造的t细胞能够体内复制,产生长期持久性,可以引起持续的肿瘤控制。
本发明还涉及用于治疗患者的疾病的方法,包括向患者施用有效量的本发明的被改造的转换受体。根据本发明的方法可以治疗多种疾病,包括但不限于癌症,诸如卵巢癌、乳腺癌、结肠癌、多形性胶质母细胞瘤、前列腺癌和白血病;病毒感染,诸如hbv、hcv、htlv-1、htlv-ii、ebv、hsv-i、hsv-ii和kshv的慢性病毒感染;和自身免疫病,诸如关节炎、哮喘、移植物抗宿主病、器官排斥、银屑病、系统性红斑狼疮、特应性变态反应、炎性肠病、多发性硬化症、变应性皮炎、斯耶格伦氏综合征、进行性系统性硬化症、自身免疫性甲状腺炎、自身免疫性糖尿病、自身免疫性肝病和骨髓增生异常综合征。
癌症的实例包括但不限于,癌,淋巴瘤,母细胞瘤,肉瘤和白血病或恶性淋巴增殖性疾病。此类癌症的更具体的例子包括肾癌或肾脏癌症,乳腺癌,结肠癌,直肠癌,结肠直肠癌,肺癌包括小细胞肺癌、非小细胞肺癌,肺的腺癌和肺的鳞状癌,鳞状细胞癌(例如上皮鳞状细胞癌),宫颈癌,卵巢癌,前列腺癌,肝癌,膀胱癌,腹膜癌,肝细胞癌,胃癌或胃癌症——包括胃肠癌,胃肠道间质瘤(gist),胰腺癌,头颈癌,胶质母细胞瘤,视网膜母细胞瘤,星形细胞瘤,卵泡膜细胞瘤(thecomas),男性细胞瘤(arrhenoblastomas),肝细胞瘤,血液学恶性肿瘤(包括非霍奇金淋巴瘤(nhl),多发性骨髓瘤和急性血液学恶性肿瘤,子宫内膜癌或子宫癌,子宫内膜异位症,纤维肉瘤,绒毛膜癌,唾液腺癌,外阴癌,甲状腺癌,食管癌,肝癌,肛门癌,阴茎癌,鼻咽癌,喉癌,卡波西肉瘤,黑素瘤,皮肤癌,许旺氏细胞瘤(schwannoma),少突神经胶质瘤,成神经细胞瘤,横纹肌肉瘤,骨源性肉瘤,平滑肌肉瘤,尿道癌,甲状腺癌,肾母细胞瘤(wilm'stumor),以及b细胞淋巴瘤(包括低度/滤泡性非霍奇金淋巴瘤(nhl);小淋巴细胞性(sl)nhl;中度/滤泡性nhl;中度弥漫性nhl;高度免疫母细胞性nhl;高度淋巴母细胞性nhl;高度小无核裂细胞性nhl;巨大肿块nhl;外套细胞淋巴瘤;aids相关淋巴瘤;和瓦尔登斯特伦氏巨球蛋白血症(waldenstrom'smacroglobulinemia));慢性淋巴细胞性白血病(cll);急性成淋巴细胞性白血病(all);毛细胞性白血病,慢性成髓细胞性白血病;和移植后淋巴增殖性病症(ptld),以及与斑痣性错构瘤病(phakomatoses)、水肿(诸如与脑肿瘤有关的)、和meigs综合征有关的异常血管增殖。“肿瘤”,如本文所使用的,指所有赘生性细胞生长和增殖,无论是恶性的或者是良性的,以及所有癌前的和癌性的细胞和组织。
在本发明的内容中,“肿瘤抗原”或“过度增生性病症抗原”或“与过度增生性病症相关的抗原”指的是特定过度增生性病症常见的抗原。在某些方面,本发明的过度增生性病症抗原源自癌症,包括但不限于,原发性或转移性黑素瘤,胸腺瘤,淋巴瘤,肉瘤,肺癌,肝癌,非霍奇金淋巴瘤,霍奇金淋巴瘤,白血病,子宫癌,宫颈癌,膀胱癌,肾癌和腺癌诸如乳腺癌,前列腺癌,卵巢癌,胰腺癌,等。
在一个实施方案中,本发明的肿瘤抗原包括一种或多种被源自哺乳动物癌肿瘤的肿瘤浸润淋巴细胞(til)免疫识别的抗原癌症表位(antigeniccancerepitopes)。
恶性肿瘤表达可用作免疫攻击的靶抗原的许多蛋白。这些分子包括但不限于组织特异性抗原诸如mart-1、黑素瘤中的酪氨酸酶和gp100和前列腺癌中的前列腺酸性磷酸酶(pap)和前列腺特异性抗原(psa)。其他靶分子属于转化相关分子的组,诸如癌基因her-2/neu/erbb-2。而另一组的靶抗原为癌性胚胎抗原,诸如癌胚抗原(cea)。在b-细胞淋巴瘤中,肿瘤特异性独特型免疫球蛋白构成对个体肿瘤独特的真正的肿瘤特异性免疫球蛋白抗原。b-细胞分化抗原诸如cd19、cd20和cd37是b-细胞淋巴瘤中靶抗原的其他候选物。这些抗原中的一些(cea、her-2、cd19、cd20、独特型)已经有限成功地用作利用单克隆抗体的被动免疫疗法的靶标。
在癌症治疗的情况下,本发明的转换受体可以任选地联合其他化疗剂施用于患者。合适的化疗剂包括,例如,烷化剂诸如塞替派和环磷酰胺;磺酸烷基酯类诸如白消安(busulfan)、英丙舒凡(improsulfan)和哌泊舒凡(piposulfan);氮丙啶类(aziridines)诸如苯佐替派(benzodepa)、卡波醌(carboquone)、美妥替派(meturedepa)和乌瑞替派(uredepa);乙撑亚胺类(ethylenimines)和甲基蜜胺类(methylameiamines),包括六甲蜜胺(altretamine)、三乙撑蜜胺(triethylenemelamine)、三乙撑磷酰胺(triethylenephosphoramide)、三乙撑硫代磷酰胺(triethylenethiophosphoramide)和三羟甲蜜胺(trimethylolomelamine);氮芥类(nitrogenmustards)诸如苯丁酸氮芥(chlorambucil)、萘氮芥(chlornaphazine)、胆磷酰胺(cholophosphamide)、雌莫司汀(estramustine)、异环磷酰胺(ifosfamide)、氮芥(mechlorethamine)、盐酸氧化氮芥(mechlorethamineoxidehydrochloride)、美法仑(melphalan)、新氮芥(novembichin)、苯芥胆甾醇(phenesterine)、泼尼莫司汀(prednimustine)、曲磷胺(trofosfamide)、尿嘧啶氮芥(uracilmustard);亚硝基脲类(nitrosoureas)诸如卡莫司汀(carmustine)、氯脲菌素(chlorozotocin)、福莫司汀(fotemustine)、洛莫司汀(lomustine)、尼莫司汀(nimustine)、雷莫司汀(ranimustine);抗生素类,诸如阿克拉霉素(aclacinomysin)、放线菌素(actinomycin)、氨茴霉素(anthramycin)、偶氮丝氨酸(azaserine)、博来霉素(bleomycin)、放线菌素c(cactinomycin)、卡奇霉素(calicheamicin)、carabicin、洋红霉素(carminomycin)、嗜癌霉素(carzinophilin)、色霉素(chromomycin)、放线菌素d(dactinomycin)、柔红霉素(daunorubicin)、地托比星(detorubicin)、6-二偶氮-5-氧代-l-正亮氨酸、多柔比星(doxorubicin)、表柔比星(epirubicin)、依索比星(esorubicin)、伊达比星(idarubicin)、麻西罗霉素(marcellomycin)、丝裂霉素类(mitomycins)、霉酚酸(mycophenolicacid)、诺拉霉素(nogalamycin)、橄榄霉素(olivomycin)、培洛霉素(peplomycin)、potfiromycin、嘌呤霉素(puromycin)、三铁阿霉素(quelamycin)、罗多比星(rodorubicin)、链黑霉素(streptonigrin)、链佐星(streptozocin)、杀结核菌素(tubercidin)、乌苯美司(ubenimex)、净司他丁(zinostatin)、佐柔比星(zorubicin);抗代谢物类,诸如甲氨蝶呤和5-氟尿嘧啶(5-fu);叶酸类似物,诸如二甲叶酸(denopterin)、甲氨蝶呤、蝶罗呤(pteropterin)、三甲曲沙(trimetrexate);嘌呤类似物,诸如氟达拉滨(fludarabine)、6-巯基嘌呤(mercaptopurine)、硫咪嘌呤(thiamiprine)、硫鸟嘌呤(thioguanine);嘧啶类似物,诸如安西他滨(ancitabine)、阿扎胞苷(azacitidine)、6-氮杂尿苷(6-azauridine)、卡莫氟(carmofur)、阿糖胞苷(cytarabine)、双脱氧尿苷(dideoxyuridine)、去氧氟尿苷(doxifluridine)、依诺他滨(enocitabine)、氟尿苷(floxuridine),5-fu;雄激素类,诸如卡普睾酮(calusterone)、丙酸屈他雄酮(dromostanolonepropionate)、环硫雄醇(epitiostanol)、美雄烷(mepitiostane)、睾内酯(testolactone);抗肾上腺类,诸如氨鲁米特(aminoglutethimide)、米托坦(mitotane)、曲洛司坦(trilostane);叶酸补充剂,诸如亚叶酸(folinicacid);醋葡醛内酯(aceglatone);醛磷酰胺糖苷(aldophosphamideglycoside);氨基酮戊酸(aminolevulinicacid);安吖啶(amsacrine);bestrabucil;比生群(bisantrene);依达曲沙(edatraxate);defofamine;地美可辛(demecolcine);地吖醌(diaziquone);elformthine;依利醋铵(elliptiniumacetate);依托格鲁(etoglucid);硝酸镓;羟基脲(hydroxyurea);香菇多糖(lentinan);氯尼达明(lonidamine);米托胍腙(mitoguazone);米托蒽醌(mitoxantrone);莫哌达醇(mopidamol);硝氨丙吖啶(nitracrine);喷司他丁(pentostatin);蛋氨氮芥(phenamet);吡柔比星(pirarubicin);鬼臼酸(podophyllinicacid);2-乙基酰肼(2-ethylhydrazide);丙卡巴肼(procarbazine);psktm;雷佐生(razoxane);西左非兰(sizofiran);螺锗(spirogermanium);替奴佐酸(tenuazonicacid);三亚胺醌(triaziquone);2,2’,2”-三氯三乙胺;乌拉坦(urethan);长春地辛(vindesine);达卡巴嗪(dacarbazine);甘露醇氮芥(mannomustine);二溴甘露醇(mitobronitol);二溴卫矛醇(mitolactol);哌泊溴烷(pipobroman);gacytosine;阿糖胞苷(arabinoside)(“ara-c”);环磷酰胺;塞替派(thiotepa);紫杉烷类(taxanes),例如,紫杉醇(taxoltm,bristol-myerssquibboncology,princeton,n.j.)和多烯紫杉醇(taxoteretm,rhone-poulencrorer,antony,france);苯丁酸氮芥(chlorambucil);吉西他滨(gemcitabine);6-硫鸟嘌呤(6-thioguanine);巯基嘌呤(mercaptopurine);甲氨蝶呤(methotrexate);铂类似物,诸如顺铂(cisplatin)和卡铂(carboplatin);长春碱(vinblastine);铂;依托泊甙(etoposide)(vp-16);异环磷酰胺(ifosfamide);丝裂霉素c(mitomycinc);米托蒽醌(mitoxantrone);长春新碱(vincristine);长春瑞滨(vinorelbine);诺维本(navelbine);能灭瘤(novantrone);替尼泊甙(teniposide);道诺霉素(daunomycin);氨基蝶呤(aminopterin);希罗达(xeloda);伊班膦酸钠(ibandronate);cpt-11;拓扑异构酶抑制剂rfs2000;二氟甲基鸟氨酸(dmfo);维甲酸(retinoicacid);埃斯波霉素(esperamicins)、卡培他滨(capecitabine);和上述任一种的药学上可接受的盐、酸或衍生物。
还包括能起作用以调节或抑制激素对肿瘤的作用的抗激素剂,诸如抗雌激素剂包括例如,他莫昔芬(tamoxifen),雷洛昔芬(raloxifene),芳香酶抑制剂4(5)-咪唑,4-羟基他莫昔芬,曲沃昔芬(trioxifene),keoxifene,ly117018,奥那司酮(onapristone),和托瑞米芬(法乐通,fareston);和抗雄激素剂诸如氟他胺(flutamide),尼鲁米特(nilutamide),比卡鲁胺(bicalutamide),亮丙瑞林(leuprolide)和戈舍瑞林(goserelin);和上述任一种的药学上可接受的盐、酸或衍生物。
还包括能够使肿瘤细胞对trail敏感并克服trail抗性的化疗剂,诸如蛋白酶体抑制剂和组蛋白脱乙酰基酶(hdac)抑制剂,放线菌酮,甲磺酸伊马替尼和其他蛋白酪氨酸激酶抑制剂,17-烯丙基氨基-17-去甲氧基格尔德霉素,三氧化二砷和凋亡蛋白x-连锁抑制剂小分子拮抗剂;和这些中任一种的药学上可接受的盐、酸或衍生物。
关于癌症治疗方法的额外信息在美国专利号7,285,522中提供,该专利整体通过引用并入。
因此,在优选的实施方案中,本发明的转换受体可以用于治疗乳腺癌。在另一个优选的实施方案中,本发明的转换受体可以用于治疗结肠癌。在另一个实施方案中,本发明的转换受体可以用于治疗肝癌。在另一个优选的实施方案中,本发明的转换受体可以用于治疗卵巢癌。在另一个实施方案中,本发明的转换受体可以用于治疗白血病。在另一个实施方案中,本发明的转换受体可以用于治疗黑素瘤。在进一步的实施方案中,本发明的转换受体可以用于治疗自身免疫病,例如,移植物排斥,或移植物抗宿主或宿主抗移植物疾病。
典型地,对于每种疾病应用,可以生成候选转换受体的小“文库”并且该文库可以在适宜的和公认的离体和体内模型中进行比较评价以确定相对功效和毒性。
在方法中使用的具体的第一和第二蛋白质将根据被治疗的疾病而变化。通常,对于癌症,将抑制性免疫转导激活信号转变成激活免疫转导激活信号的转换受体是合乎需要的。不希望受限于任何特殊理论,由本发明的被改造的细胞引起的抗肿瘤免疫应答可以是主动或被动免疫应答。所述应答可以是过继免疫疗法方式的部分。
关于离体免疫,以下中的至少一项在将细胞施用进入哺乳动物前在体外发生:i)扩充细胞,ii)将编码本发明的转换受体的核酸引入细胞中,和/或iii)冷冻保存细胞。
离体程序在本领域中是公知的,并在以下更完全地进行讨论。简单地说,细胞从哺乳动物(优选人)中分离并用表达本发明的转换受体的载体进行遗传修饰(即,体外转导或转染)。被改造的细胞可被施用给哺乳动物受者,以提供治疗益处。哺乳动物受者可为人,并且被改造的细胞可相对于受者为自体的。可选地,细胞可相对于受者为同种异体的、同基因的(syngeneic)或异种的。
在此通过引用并入的美国专利号5,199,942中描述的造血干细胞和祖细胞的离体扩充程序,可被应用至本发明的细胞。其他合适的方法在本领域中是己知的,因此本发明不限于细胞离体扩充的任何具体方法。简单地说,t细胞的离体培养和扩充包括:(1)从外周血收获物或骨髓外植体收集来自哺乳动物的cd34+造血干细胞和祖细胞;和(2)离体扩充这样的细胞。除了美国专利号5,199,942中描述的细胞生长因子,其他因子诸如flt3-l、il-1、il-3和c-kit配体,也可用于培养和扩充细胞。
除了就离体免疫而言使用基于细胞的疫苗之外,本发明还提供了体内免疫以引起针对患者中抗原的免疫应答的组合物和方法。
通常地,如本文所述激活和扩充的细胞可用于治疗和预防免疫受损的个体中产生的疾病。特别地,本发明的被改造的细胞用于治疗癌症。在某些实施方案中,本发明的细胞用于治疗处于发展癌症风险中的患者。因此,本发明提供了治疗或预防癌症的方法,其包括施用给需要其的对象以治疗有效量的本发明的被改造的t细胞。
本发明的被改造的t细胞可被单独施用或作为药物组合物与稀释剂和/或与其他组分诸如il-2或其他细胞因子或细胞群联合施用。简单地说,本发明的药物组合物可包含如本文所述的靶细胞群,与一种或多种药学或生理学上可接受的载体、稀释剂或赋形剂联合。这样的组合物可包含缓冲液诸如中性缓冲盐水、磷酸盐缓冲盐水等;碳水化合物诸如葡萄糖、甘露糖、蔗糖或葡聚糖、甘露醇;蛋白质;多肽或氨基酸诸如甘氨酸;抗氧化剂;螯合剂诸如edta或谷胱甘肽;佐剂(例如,氢氧化铝);和防腐剂。本发明的组合物优选配制用于静脉内施用。
本发明的药物组合物可以以适于待治疗(或预防)的疾病的方式施用。施用的数量和频率将由这样的因素确定,如患者的病症、以及患者疾病的类型和严重度,尽管适当的剂量可通过临床实验来确定。
当表示“免疫学上的有效量”、“抗肿瘤有效量”、“肿瘤抑制有效量”或“治疗量”时,待施用的本发明组合物的精确量可由医师考虑患者(对象)的年龄、体重、肿瘤大小、感染或转移程度以及病症的个体差异来确定。可通常指出:包含本文描述的t细胞的药物组合物可以以104至109个细胞/kg体重的剂量,优选105至106个细胞/kg体重的剂量(包括那些范围内的所有整数值)施用。t细胞组合物也可以以这些剂量多次施用。细胞可通过使用免疫疗法中公知的输注技术(参见,例如,rosenberg等人,neweng.j.ofmed.319:1676,1988)施用。对于具体患者的最佳剂量和治疗方案可通过监测患者的疾病体征并因此调整治疗而由医学领域技术人员容易地确定。
在某些实施方案中,可期望向对象施用激活的t细胞,并随后重新抽取血液(或实施单采血液成分术),根据本发明激活来自其中的t细胞,和用这些激活和扩充的t细胞再输入至该患者。该过程可每几周进行多次。在某些实施方案中,t细胞可从10cc至400cc的抽取血液中进行激活。在一些实施方案中,t细胞从20cc、30cc、40cc、50cc、60cc、70cc、80cc、90cc或100cc的抽取血液中进行激活。不被理论所束缚,利用此多次血液抽取/多个再输注方案,可选出某些t细胞群。
对对象施用组合物可以以任何方便的方式进行,包括通过雾化吸入法、注射、摄入、输液、植入或移植。本文描述的组合物可经皮下、皮内、瘤内、结内、髓内、肌肉内、通过静脉内(i.v.)注射或腹膜内施用给患者。在一个实施方案中,本发明的t细胞组合物通过皮内或皮下注射被施用给患者。在另一个实施方案中,本发明的t细胞组合物优选通过静脉内注射施用。t细胞的组合物可被直接注入肿瘤、淋巴结或感染部位。
在本发明的某些实施方案中,利用本文描述的方法或本领域己知的将t细胞扩充至治疗性水平的其他方法激活和扩充的细胞,与任何数量的相关治疗模式结合(例如,之前、同时或之后)施用给患者,所述治疗模式包括但不限于用以下试剂进行的治疗:所述试剂诸如抗病毒疗法,西多福韦和白介素-2、针对ms患者的阿糖胞苷(也已知为ara-c)或那他珠单抗治疗,或对银屑病患者的依法利珠单抗治疗或对pml患者的其他治疗。在进一步的实施方案中,本发明的t细胞可与以下各项联合使用:化疗、辐照、免疫抑制剂,诸如,环孢菌素、硫唑嘌呤、甲氨喋呤、麦考酚酯和fk506,抗体,或其他免疫消融剂诸如campath、抗-cd3抗体或其他抗体疗法、细胞毒素、氟达拉滨、环孢菌素、fk506、雷帕霉素、麦考酚酸、类固醇类、fr901228、细胞因子和照射。这些药物抑制钙依赖性磷酸酶钙调磷酸酶(环孢菌素和fk506)或抑制对生长因子诱导的信号传导重要的p70s6激酶(雷帕霉素)。(liu等人,cell66:807-815,1991;henderson等人,immun.73:316-321,1991;bierer等人,curr.opin.immun.5:763-773,1993;isoniemi(见前))。在进一步的实施方案中,本发明的细胞组合物与骨髓移植、利用化疗剂诸如氟达拉滨、外部光束放射疗法(xrt)、环磷酰胺、或抗体诸如okt3或campath的t细胞消融疗法结合(例如,之前、同时或之后)而施用给患者。在另一个实施方案中,本发明的细胞组合物在b-细胞消融疗法诸如与cd20反应的试剂,例如美罗华(rituxan)后进行施用。例如,在一个实施方案中,对象可经历高剂量化疗的标准治疗,之后进行外周血干细胞移植。在特定实施方案中,在移植后,对象接受本发明的扩充的免疫细胞的输注。在一个额外的实施方案中,扩充的细胞在外科手术前或外科手术后施用。
待施用给患者的以上治疗的剂量将随着被治疗状况的精确属性和治疗的受者而变化。人施用的剂量换算可根据本领域接受的实践实施。例如,campath的剂量对于成人患者将通常在1至大约100mg的范围内,通常每天施用一次,持续1至30天之间的时期。尽管在一些例子中可使用高至每天40mg的较大剂量(美国专利号6,120,766中描述),但优选的日剂量为每天l至10mg。
实验实施例
本发明通过参考以下实验实施例进一步详细地进行描述。这些实施例仅出于说明性的目的提供,并不意欲为限制性的,除非另有规定。因此,本发明决不应被解释为限于以下实施例,而是应被解释为包括由于本文提供的教导变得显而易见的任何和全部的变化形式。
没有进一步的描述,相信利用先前的描述和以下的说明性实施例,本领域普通技术人员可制造和利用本发明的化合物,并实践请求保护的方法。以下工作实施例因此具体指出本发明的优选实施方案,并不解释为以任何方式限制本公开的剩余部分。
实施例1:转换受体
本文给出的结果证明了,嵌合受体可以被改造从而将t细胞上的阴性信号转变成阳性信号。设计实验以开发出系统性地避免肿瘤抑制因子的抑制并且因此避免整个免疫系统的抑制的方法。简言之,t细胞被改造以表达嵌合受体,所述嵌合受体编码pd-1胞外结构域(没有抑制性pd-1结构域)和刺激性cd28或icos信号传导结构域。嵌合受体的定向将pd-1胞外结构域置于细胞外并将cd28或icos刺激性结构域置于t细胞内。因此,t细胞与肿瘤抗原在肿瘤微环境中的相互作用在pd-1配体的接合后被正性地影响,因为细胞中的信号通过cd28或icos信号传导内结构域而不是天然的抑制性pd-1内结构域递送。
现在描述这些实验中采用的材料和方法。
材料和方法
转换受体的产生
设计构建体用于测试btla转换受体。下面是每个构建体的序列,所述构建体被克隆进基于pgem.64a的ivt载体中。
btla;seqidno:1
atgaagacattgcctgccatgcttggaactgggaaattattttgggtcttcttcttaatcccatatctggacatctggaacatccatgggaaagaatcatgtgatgtacagctttatataaagagacaatctgaacactccatcttagcaggagatccctttgaactagaatgccctgtgaaatactgtgctaacaggcctcatgtgacttggtgcaagctcaatggaacaacatgtgtaaaacttgaagatagacaaacaagttggaaggaagagaagaacatttcatttttcattctacattttgaaccagtgcttcctaatgacaatgggtcataccgctgttctgcaaattttcagtctaatctcattgaaagccactcaacaactctttatgtgacagatgtaaaaagtgcctcagaacgaccctccaaggacgaaatggcaagcagaccctggctcctgtatagtttacttcctttggggggattgcctctactcatcactacctgtttctgcctgttctgctgcctgagaaggcaccaaggaaagcaaaatgaactctctgacacagcaggaagggaaattaacctggttgatgctcaccttaagagtgagcaaacagaagcaagcaccaggcaaaattcccaagtactgctatcagaaactggaatttatgataatgaccctgacctttgtttcaggatgcaggaagggtctgaagtttattctaatccatgcctggaagaaaacaaaccaggcattgtttatgcttccctgaaccattctgtcattggaccgaactcaagactggcaagaaatgtaaaagaagcaccaacagaatatgcatccatatgtgtgaggagttaa
btla-btm-cd28;seqidno:2
aagcttgccgccatgaagacattgcctgccatgcttggaactgggaaattattttgggtcttcttcttaatcccatatctggacatctggaacatccatgggaaagaatcatgtgatgtacagctttatataaagagacaatctgaacactccatcttagcaggagatccctttgaactagaatgccctgtgaaatactgtgctaacaggcctcatgtgacttggtgcaagctcaatggaacaacatgtgtaaaacttgaagatagacaaacaagttggaaggaagagaagaacatttcatttttcattctacattttgaaccagtgcttcctaatgacaatgggtcataccgctgttctgcaaattttcagtctaatctcattgaaagccactcaacaactctttatgtgacagatgtaaaaagtgcctcagaacgaccctccaaggacgaaatggcaagcagaccctggctcctgtatagtttacttcctttggggggattgcctctactcatcactacctgtttctgcctgttctgctgcctggaggagtaagaggagcaggctcctgcacagtgactacatgaacatgactccccgccgccccgggcccacccgcaagcattaccagccctatgccccaccacgcgacttcgcagcctatcgctcctgataagcggccgca
btla-btm-cd27;seqidno:3
aagcttgccgccatgaagacattgcctgccatgcttggaactgggaaattattttgggtcttcttcttaatcccatatctggacatctggaacatccatgggaaagaatcatgtgatgtacagctttatataaagagacaatctgaacactccatcttagcaggagatccctttgaactagaatgccctgtgaaatactgtgctaacaggcctcatgtgacttggtgcaagctcaatggaacaacatgtgtaaaacttgaagatagacaaacaagttggaaggaagagaagaacatttcatttttcattctacattttgaaccagtgcttcctaatgacaatgggtcataccgctgttctgcaaattttcagtctaatctcattgaaagccactcaacaactctttatgtgacagatgtaaaaagtgcctcagaacgaccctccaaggacgaaatggcaagcagaccctggctcctgtatagtttacttcctttggggggattgcctctactcatcactacctgtttctgcctgttctgctgcctggaaggaaatatagatcaaacaaaggagaaagtcctgtggagcctgcagagccttgtcgttacagctgccccagggaggaggagggcagcaccatccccatccaggaggattaccgaaaaccggagcctgcctgctccccctgataagcggccgca
btla-itm-cd28;seqidno:4
aagcttgccgccatgaagacattgcctgccatgcttggaactgggaaattattttgggtcttcttcttaatcccatatctggacatctggaacatccatgggaaagaatcatgtgatgtacagctttatataaagagacaatctgaacactccatcttagcaggagatccctttgaactagaatgccctgtgaaatactgtgctaacaggcctcatgtgacttggtgcaagctcaatggaacaacatgtgtaaaacttgaagatagacaaacaagttggaaggaagagaagaacatttcatttttcattctacattttgaaccagtgcttcctaatgacaatgggtcataccgctgttctgcaaattttcagtctaatctcattgaaagccactcaacaactctttatgtgacagatgtaaaaagtgcctcagaacgaccctccaaggacgaaatggcaagcagaccctggctcctgtatagtttctggttacccataggatgtgcagcctttgttgtagtctgcattttgggatgcatacttattgaggagtaagaggagcaggctcctgcacagtgactacatgaacatgactccccgccgccccgggcccacccgcaagcattaccagccctatgccccaccacgcgacttcgcagcctatcgctcctgataagcggccgca
btla-itm-cd27;seqidno:5
aagcttgccgccatgaagacattgcctgccatgcttggaactgggaaattattttgggtcttcttcttaatcccatatctggacatctggaacatccatgggaaagaatcatgtgatgtacagctttatataaagagacaatctgaacactccatcttagcaggagatccctttgaactagaatgccctgtgaaatactgtgctaacaggcctcatgtgacttggtgcaagctcaatggaacaacatgtgtaaaacttgaagatagacaaacaagttggaaggaagagaagaacatttcatttttcattctacattttgaaccagtgcttcctaatgacaatgggtcataccgctgttctgcaaattttcagtctaatctcattgaaagccactcaacaactctttatgtgacagatgtaaaaagtgcctcagaacgaccctccaaggacgaaatggcaagcagaccctggctcctgtatagtttctggttacccataggatgtgcagcctttgttgtagtctgcattttgggatgcatacttattgaaggaaatatagatcaaacaaaggagaaagtcctgtggagcctgcagagccttgtcgttacagctgccccagggaggaggagggcagcaccatccccatccaggaggattaccgaaaaccggagcctgcctgctccccctgataagcggccgca
btla-btm-icos;seqidno:6
aagcttgccgccatgaagacattgcctgccatgcttggaactgggaaattattttgggtcttcttcttaatcccatatctggacatctggaacatccatgggaaagaatcatgtgatgtacagctttatataaagagacaatctgaacactccatcttagcaggagatccctttgaactagaatgccctgtgaaatactgtgctaacaggcctcatgtgacttggtgcaagctcaatggaacaacatgtgtaaaacttgaagatagacaaacaagttggaaggaagagaagaacatttcatttttcattctacattttgaaccagtgcttcctaatgacaatgggtcataccgctgttctgcaaattttcagtctaatctcattgaaagccactcaacaactctttatgtgacagatgtaaaaagtgcctcagaacgaccctccaaggacgaaatggcaagcagaccctggctcctgtatagtttacttcctttggggggattgcctctactcatcactacctgtttctgcctgttctgctgcctgtgttggcttacaaaaaagaagtattcatccagtgtgcacgaccctaacggtgaatacatgttcatgagagcagtgaacacagccaaaaaatctagactcacagatgtgaccctataagcggccgca
btla-btm-icos-z;seqidno:7
aagcttgccgccatgaagacattgcctgccatgcttggaactgggaaattattttgggtcttcttcttaatcccatatctggacatctggaacatccatgggaaagaatcatgtgatgtacagctttatataaagagacaatctgaacactccatcttagcaggagatccctttgaactagaatgccctgtgaaatactgtgctaacaggcctcatgtgacttggtgcaagctcaatggaacaacatgtgtaaaacttgaagatagacaaacaagttggaaggaagagaagaacatttcatttttcattctacattttgaaccagtgcttcctaatgacaatgggtcataccgctgttctgcaaattttcagtctaatctcattgaaagccactcaacaactctttatgtgacagatgtaaaaagtgcctcagaacgaccctccaaggacgaaatggcaagcagaccctggctcctgtatagtttacttcctttggggggattgcctctactcatcactacctgtttctgcctgttctgctgcctgtgttggcttacaaaaaagaagtattcatccagtgtgcacgaccctaacggtgaatacatgttcatgagagcagtgaacacagccaaaaaatctagactcacagatgtgaccctatgcagagtgaagttcagcaggagcgcagacgcccccgcgtaccagcagggccagaaccagctctataacgagctcaatctaggacgaagagaggagtacgatgttttggacaagagacgtggccgggaccctgagatggggggaaagccgagaaggaagaaccctcaggaaggcctgtacaatgaactgcagaaagataagatggcggaggcctacagtgagattgggatgaaaggcgagcgccggaggggcaaggggcacgatggcctttaccagggtctcagtacagccaccaaggacacctacgacgcccttcacatgcaggccctgccccctcgctaagcggccgca
btla-itm-icos;seqidno:8
aagcttgccgccatgaagacattgcctgccatgcttggaactgggaaattattttgggtcttcttcttaatcccatatctggacatctggaacatccatgggaaagaatcatgtgatgtacagctttatataaagagacaatctgaacactccatcttagcaggagatccctttgaactagaatgccctgtgaaatactgtgctaacaggcctcatgtgacttggtgcaagctcaatggaacaacatgtgtaaaacttgaagatagacaaacaagttggaaggaagagaagaacatttcatttttcattctacattttgaaccagtgcttcctaatgacaatgggtcataccgctgttctgcaaattttcagtctaatctcattgaaagccactcaacaactctttatgtgacagatgtaaaaagtgcctcagaacgaccctccaaggacgaaatggcaagcagaccctggctcctgtatagtttctggttacccataggatgtgcagcctttgttgtagtctgcattttgggatgcatacttatttgttggcttacaaaaaagaagtattcatccagtgtgcacgaccctaacggtgaatacatgttcatgagagcagtgaacacagccaaaaaatctagactcacagatgtgaccctataagcggccgca
btla-itm-icos-z;seqidno:9
aagcttgccgccatgaagacattgcctgccatgcttggaactgggaaattattttgggtcttcttcttaatcccatatctggacatctggaacatccatgggaaagaatcatgtgatgtacagctttatataaagagacaatctgaacactccatcttagcaggagatccctttgaactagaatgccctgtgaaatactgtgctaacaggcctcatgtgacttggtgcaagctcaatggaacaacatgtgtaaaacttgaagatagacaaacaagttggaaggaagagaagaacatttcatttttcattctacattttgaaccagtgcttcctaatgacaatgggtcataccgctgttctgcaaattttcagtctaatctcattgaaagccactcaacaactctttatgtgacagatgtaaaaagtgcctcagaacgaccctccaaggacgaaatggcaagcagaccctggctcctgtatagtttacttcctttggggggattgcctctactcatcactacctgtttctgcctgttctgctgcctgtgttggcttacaaaaaagaagtattcatccagtgtgcacgaccctaacggtgaatacatgttcatgagagcagtgaacacagccaaaaaatctagactcacagatgtgaccctatgcagagtgaagttcagcaggagcgcagacgcccccgcgtaccagcagggccagaaccagctctataacgagctcaatctaggacgaagagaggagtacgatgttttggacaagagacgtggccgggaccctgagatggggggaaagccgagaaggaagaaccctcaggaaggcctgtacaatgaactgcagaaagataagatggcggaggcctacagtgagattgggatgaaaggcgagcgccggaggggcaaggggcacgatggcctttaccagggtctcagtacagccaccaaggacacctacgacgcccttcacatgcaggccctgccccctcgctaagcggccgca
t细胞的转导
已经描述了利用包被有抗-cd3和抗-cd28单克隆抗体的顺磁聚苯乙烯珠的t细胞制备方法(laport等人,2003,blood102:20042013)。慢病毒转导如所述的那样进行(levine等人,2006,procnatlacadsciusa103:17372-17377)。利用rna电穿孔t细胞已经被描述为(2010,zhao等人,cancerres70:9062)表达这些受体的方法。已经描述了腺病毒载体的应用(2004,schroers等人,exphematol32:536)。已经描述了许多其他的在t细胞中表达蛋白质的方式(2009,june等人,natrevimmunol9:704)。
细胞因子分析
可溶性细胞因子的量化利用从lifetechnologies(invitrogen)购买的luminex珠阵列技术和试剂盒实施。按照制造商的实验方案,利用3倍系列稀释产生的8点标准曲线实施测定。
现在描述实验结果。
本文给出的结果证明了,嵌合受体可以被改造并在t细胞上表达,其中所述嵌合受体将t细胞上的阴性信号转变成阳性信号。因此,本发明提供了一种类型的过继t细胞或nk细胞疗法,所述疗法利用已经被遗传修饰以表达t细胞受体(tcrs)或嵌合抗原受体(cars)的细胞。
设计实验以开发出系统性避免pd-1的抑制并且因此避免整个免疫系统的抑制的靶向方法。该靶向方法包括施用表达嵌合受体的t细胞,所述嵌合受体编码例如pd-1胞外结构域,和t细胞的细胞内部分上的刺激性cd28或icos信号传导结构域而非抑制性pd-1结构域。因此,t细胞与肿瘤抗原在肿瘤微环境中的相互作用在pd-1配体的接合后被正性地影响,因为细胞中的信号通过cd28或icos信号传导内结构域而不是天然的抑制性pd-1内结构域递送。
转变btla信号
以相似的方式,已经构建了编码btla的嵌合受体。btla,与pd-1一起都是cd28家族的成员。btla具有数个配体,包括hvem,hvem在肿瘤细胞和其他细胞上表达,经常在肿瘤微环境内。众所周知,btla与细胞上的天然配体的相互作用负性地调控t-细胞免疫应答(paulos等人,2010,jclininvest120:76-80;derré等人,2010,jclininvest120:157-67;chemnitz等人,2006,jimmunol176:6603-14)。为了规避,构建了由btla胞外结构域和包含cd28或icos结构域的胞内信号传导内结构域组成的嵌合受体。
简言之,使用分子克隆来构建图1中所绘的示例性嵌合受体。为了测试t细胞表面上表达的btlaccr的连接是否可以正确地被表达并且通过icos胞内结构域向cd3ζ转导信号,编码btlaccr的ivtmrna如指示的那样被电穿孔进被刺激的t细胞并且在如指示的不同时间通过hvem-fc融合蛋白检测btla的表面表达(图1b)。被电穿孔的t细胞用btla配体阴性细胞系(ktpolcd86a2)或btla配体hvem阳性细胞系(ktcd86fluhvem)刺激。刺激后24小时,通过elisa测定由t细胞产生的il-2(图1c)。结果显示,通过将btla胞外结构域与icos和cd3ζ两者的胞内结构域融合,t细胞可以被表达btla配体hvem的细胞系的刺激所激活,指示btla信号可以以嵌合共刺激受体(ccr)的形式转变成其他信号。
设计下一组实验以评估btla抑制信号是否可以通过btla-cd28ccr转变成cd28共刺激信号。为了发现可以显示cd28信号传导的适宜窗口,将不同剂量的rna(ug/0.1mlt细胞)电穿孔进t细胞中并通过facs检测car(cd19z、cd19-28z)表达。上图显示了直方图和转基因表达的百分比,并且下图显示了转基因表达的mfi(图2a)。如图2a中所述的rna电穿孔的t细胞的il2产生被cd19阳性细胞系k562-cd19刺激,并且如图2b中所示通过elisa测定il-2产生。上图显示了ifn-γ并且下图显示了il-2产生。结果显示,在1.5ug的rna剂量下,不像cd19-28zrna电穿孔的t细胞(其显示超过300pg/mlil-2产生),对于cd19zrna电穿孔的t细胞没有可检测的il-2产生。以1.5ug的rna剂量对于cd19z和cd19-28z电穿孔的t细胞两者,可以以相似的水平检测到ifn-γ产生。因此,使用1.5ugrna作为rna剂量来测试转变btla-cd28信号的多肽。
t细胞用1.5ugcd19z和btlaccr如指示的那样共同电穿孔并用表达cd19(k562cd19)或cd19和hvem两者(k562cd19/hvem)的k562刺激。表达间皮素的k562细胞系(具有或不具有hvem)用作对照(图2c)。结果显示,全长(野生型)btla抑制il2和ifn-γ两者产生。对于仅用cd19z电穿孔的t细胞,当用cd19/hvem双阳性细胞系刺激时没有可检测到的il-2产生,而用cd19-28z电穿孔并用cd19/hvem双阳性细胞系刺激的t细胞产生超过400pg/ml的il-2。然而,当t细胞用cd19z和btla-cd28ccrrna两者共同电穿孔时,当用cd19/hvem双阳性细胞系刺激时,il-2产生比cd19-28z电穿孔的t细胞高4倍。当用cd19/hvem双阳性细胞系或表达低水平的hvem的cd19阳性k562刺激(图2c)时,用cd19z和btla-cd28ccrrna两者共同电穿孔的t细胞与cd19z或cd19-28z电穿孔的t细胞相比产生更高的ifn-γ。本文给出的结果证明,btla抑制信号可以通过btla-cd28ccr转变成cd28信号。
设计下一组实验以测试是否抑制性btla信号可以通过btla-icosccr转变成共刺激icos信号。简言之,在如图3a中显示的,在th17极化系统中测试将btla转变成icos信号。静息cd4t细胞用cd19z和btlaccr如指示的那样(处理)共同电穿孔并用cd19/hvem双阳性细胞系(1组和2组,一式两份)刺激,或t细胞用btla-icos单独电穿孔并用板结合的hvem-fc和okt3刺激(第3组)。如所述的那样(2010,paulos等人,sciencetranslationalmedicine),cd3/icos珠或cd3/cd28珠分别用作阳性和阴性对照。所有培养在th17细胞因子混合物的存在下进行。在刺激后不同的天数(如指示的那样)时,t细胞用pma/离子霉素(ionomycin)刺激,并且通过细胞内细胞因子染色检测il-17a和ifn-γ(图3b)。结果显示,由btla-icos转变的icos信号在hvem抑制信号的存在下增强th17细胞产生。
将pd-1转变成cd28信号
为了测试t细胞表面上表达的pd1ccr的连接是否可以被功能表达以通过cd28或cd27或icos胞内结构域转导信号,使用编码pd1ccr的ivtrna(序列显示在下面)。
pd1-i-icos;seqidno.10
atgcagatcccacaggcgccctggccagtcgtctgggcggtgctacaactgggctggcggccaggatggttcttagactccccagacaggccctggaacccccccaccttctccccagccctgctcgtggtgaccgaaggggacaacgccaccttcacctgcagcttctccaacacatcggagagcttcgtgctaaactggtaccgcatgagccccagcaaccagacggacaagctggccgccttccccgaggaccgcagccagcccggccaggactgccgcttccgtgtcacacaactgcccaacgggcgtgacttccacatgagcgtggtcagggcccggcgcaatgacagcggcacctacctctgtggggccatctccctggcccccaaggcgcagatcaaagagagcctgcgggcagagctcagggtgacagagagaagggcagaagtgcccacagcccaccccagcccctcacccaggccagccggccagttccaaaccctggtgttctggttacccataggatgtgcagcctttgttgtagtctgcattttgggatgcatacttatttgttggcttacaaaaaagaagtattcatccagtgtgcacgaccctaacggtgaatacatgttcatgagagcagtgaacacagccaaaaaatctagactcacagatgtgaccctataa
pd1-28-cd28;seqidno.11
atgcagatcccacaggcgccctggccagtcgtctgggcggtgctacaactgggctggcggccaggatggttcttagactccccagacaggccctggaacccccccaccttctccccagccctgctcgtggtgaccgaaggggacaacgccaccttcacctgcagcttctccaacacatcggagagcttcgtgctaaactggtaccgcatgagccccagcaaccagacggacaagctggccgccttccccgaggaccgcagccagcccggccaggactgccgcttccgtgtcacacaactgcccaacgggcgtgacttccacatgagcgtggtcagggcccggcgcaatgacagcggcacctacctctgtggggccatctccctggcccccaaggcgcagatcaaagagagcctgcgggcagagctcagggtgacagagagaagggcagaagtgcccacagcccaccccagcccctcacccaggccagccggccagttccaaaccctggtgttttgggtgctggtggtggttggtggagtcctggcttgctatagcttgctagtaacagtggcctttattattttctgggtgaggagtaagaggagcaggctcctgcacagtgactacatgaacatgactccccgccgccccgggcccacccgcaagcattaccagccctatgccccaccacgcgacttcgcagcctatcgctcctaa
pd1-cd27;seqidno.12
atgcagatcccacaggcgccctggccagtcgtctgggcggtgctacaactgggctggcggccaggatggttcttagactccccagacaggccctggaacccccccaccttctccccagccctgctcgtggtgaccgaaggggacaacgccaccttcacctgcagcttctccaacacatcggagagcttcgtgctaaactggtaccgcatgagccccagcaaccagacggacaagctggccgccttccccgaggaccgcagccagcccggccaggactgccgcttccgtgtcacacaactgcccaacgggcgtgacttccacatgagcgtggtcagggcccggcgcaatgacagcggcacctacctctgtggggccatctccctggcccccaaggcgcagatcaaagagagcctgcgggcagagctcagggtgacagagagaagggcagaagtgcccacagcccaccccagcccctcacccaggccagccggccagttccaaaccctggtgatccttgtgatcttctctggaatgttccttgttttcaccctggccggggccctgttcctccatcaacgaaggaaatatagatcaaacaaaggagaaagtcctgtggagcctgcagagccttgtcgttacagctgccccagggaggaggagggcagcaccatccccatccaggaggattaccgaaaaccggagcctgcctgctccccctaa
如指示的pd1ccr和cd19zrna被共同电穿孔进刺激的t细胞中,并且在如指示的时间点通过抗-pd1和抗-carab检测转基因(图4a)。如图4a中所述共同电穿孔的t细胞与表达pd-l1或作为对照的gfp的nalm6(人b细胞白血病细胞系)或表达pd-l1或作为对照的icosl的k562-cd19共培养。在共培养后24h测定ifn-γ产生。用cd19z和pd1-cd28(pd1-28)共引入的t细胞与用cd19z单独电穿孔或与具有截短的细胞质结构域的pd1,或pd1-cd27(pd1-27)共同电穿孔的t细胞相比显示显著较高的ifn-γ产生。当与cd19/pd-l1双阳性细胞系共培养时,当t细胞用cd19z和全长(野生型)pd1共同电穿孔并用cd19/pd-l1双阳性细胞系刺激时,看到强烈的t细胞抑制(图4b)。
如图4a中所述共同电穿孔的t细胞与表达pd-l1或作为对照的gfp的nalm6(人b细胞白血病细胞系)或表达pd-l1或作为对照的icosl的k562-cd19共培养。在共培养后24h测定il-2产生。共引入cd19z和pd1-cd28(pd1-28)的t细胞与用cd19z单独电穿孔或与具有截短的细胞质结构域的pd1,或pd1-cd27(pd1-27)共同电穿孔的t细胞相比显示显著较高的il-2产生。当与cd19/pd-l1双阳性细胞系共培养时,当t细胞用cd19z和全长pd1共同电穿孔并用cd19/pd-l1双阳性细胞系刺激时,看到强烈的t细胞抑制(图4c)。
如图4a中所述共同电穿孔的t细胞在基于流动的ctl测定中测试。用cd19z和pd1共同引入的t细胞显示显著减少的针对nalm6-pd-l1靶标的杀伤能力,而当使用nalm6-pd1作为靶标时,对于用pd1ccr共同电穿孔的t细胞,与用cd19z单独电穿孔的t细胞相比,没有看到显著的差异。当pd1配体阴性nalm6用作靶标时,对于所有t细胞组,包括用cd19z和pd1共同电穿孔的t细胞,均未发现显著的差异。
设计下一组实验来通过pd1-cd28ccr共同引入以逆转pd1抑制。为了模拟肿瘤微环境或处于其中t细胞为pd1阳性的慢性感染的情况,t细胞用cd3/cd28珠或okt3/pbmc/il2刺激,并用cd19z(10ug)和pd1(5ug)与另外的pd1ccr(10ug)如指示的那样共同电穿孔。电穿孔后1天通过facs检测car和pd1和/或pd1ccr表达(图5a)。
如图5a中所示电穿孔的t细胞与nalm6或表达pd-l1的k562-cd19共培养。共培养过夜后测定il-2产生。结果显示,与不含pd-l1的cd19阳性细胞系共培养的相同t细胞相比,用cd19z单独电穿孔的t细胞产生il-2的量减少。然而,在pd1的存在下,当与pd-l1阳性细胞系共培养时,il-2产生完全被阻断,例外是与pd1-cd28(pd1-28)共同电穿孔的t细胞,后者显示比单独cd19z的t细胞产生高得多的il-2,而当t细胞与pd-l1阴性细胞系共培养时,t细胞上的pd1表达对t细胞的影响最小(图5b)。
如图5a中所示电穿孔的t细胞与nalm6或表达pd-l1的k562-cd19共培养。共培养过夜后测定ifn-γ产生(图5c)。看到与图5b中所示的il-2产生相似的细胞因子产生曲线。本文给出的结果证明,pd1-cd28ccr可以逆转pd1的抑制效应并且促进t细胞效应器功能。
将pd1转变成icos信号
cd4t细胞用pd1(或pd1变体)和cd19-zcarmrna(每种10ug)电穿孔。电穿孔后4小时(第0天),t细胞与表达pd-l1和cd19的k562细胞在r10培养基中在il1(10ng/ml)、il6(10ng/ml)、il23(20ng/ml)以及针对il4和ifnγ的中和抗体(10μg/ml)的存在下混合(0.5:1=k562:t细胞)。在指示的天数(电穿孔后5、9和12天)时,细胞与pma(3ug/ml)和离子霉素(1ug/ml)和用于细胞内细胞因子染色的golgistop温育4小时。进行cd4的表面染色,然后进行ifn-γ,il17和il2的细胞内染色。用抗-cd28/cd3珠和抗-icos/cd3珠刺激的cd4t细胞用作对照(图6a)。与pd1野生型或无尾pd1相比,在表达pd1-icos的细胞中,细胞因子产生增加,特别是在第9天时。刺激的t细胞的细胞增殖显示在图6c中。
pd-1嵌合受体
pd-1在患有慢性病毒感染的患者中的cd8耗竭的t细胞的表面上上调。阻断pd-1:pd-l1信号恢复表达pd-1的cd8耗竭的t细胞的功能。许多肿瘤表达pd-l1,提供了免疫抑制性的微环境。
下面实验的目的是通过将pd-1嵌合受体引入至肿瘤部位来指引过继转移的t细胞以克服抑制性肿瘤微环境。
观察到pd1wt对细胞因子产生的抑制效应被pd1嵌合构建体挽救(图7)。然而,pd1嵌合受体不影响粒酶b产生(图8)。类似地,在存在或缺少pd1的情况下,观察到cd8t细胞的杀伤活性的差异最小(图9)。
设计下一组实验以评价pd-1嵌合受体对t细胞增殖的作用(图10)。观察到pd1-cd28嵌合受体增加cd8t细胞的数目(图11)。
总之,本文给出的结果证明,pd-1嵌合构建体没有表现出由pd-1wt显示的抑制效应。pd1-cd28似乎增加cd4t细胞中tnfα、il2和ifnγ的产生。pd-1嵌合受体不显示高于表达cd19carz的t细胞本身的增加的细胞毒性。pd1-cd28增加cd8t细胞数高于表达cd19carz的t细胞本身的数目。
将共抑制信号传导重新定向为阳性共刺激
本文给出的结果证明,转换受体通过电穿孔或采用慢病毒载体在t细胞中表达。观察到car和转换受体可以在相同的t细胞中表达。当表达car或tcr和转换受体的细胞暴露于具有btla或pd-1的配体的肿瘤细胞时,t细胞显示具有阳性免疫应答,而不是通常的抑制性应答。
当这些嵌合受体在t细胞中表达时,在btla转换受体的情况下,在与肿瘤细胞上它们的天然配体hvem相互作用后,观察到t细胞被刺激,然后表达与阳性抗肿瘤效应相关的功能,包括分泌ifn-γ。
来自这些研究的另一重要结果是,hvem:btla与嵌合受体的相互作用导致增强的il-17分泌。这是th17细胞的标志物,th17细胞已知是可用于肿瘤免疫疗法的细胞(martin-orozco等人,2009,immunity31:787-98;paulos等人,2010,sciencetranslationalmedicine2:55-78;garaude等人,2010,scitranslmed2(55):55ps2)。例如,本文给出的结果证明,表达car和具有icos信号传导结构域的btla转换受体的t细胞被极化以分泌大量的il-17。
另外,本文给出的结果显示,如果表达car和具有cd28和缺失的结构域的pd1转换受体的t细胞表达pd-1转换受体,则防止它们具有抑制作用,而是杀死肿瘤细胞并分泌细胞因子(il-2和ifn-γ)。
不希望受限于任何特定理论,据信通过在t细胞上表达具有pd-1或btla转换受体的嵌合抗原受体(cars),然后将该t细胞引入至肿瘤微环境中,所述t细胞具有增强的抗肿瘤效应并且表现出th17表型。用于本发明的肿瘤免疫疗法的过继t细胞转移的类型在疫苗疗法的领域中也适用,诸如对于慢性病毒感染包括hiv或其他病毒诸如ebv、hcv或cmv。此技术也可以容易地结合到其他目前正在使用用tcr遗传修饰的t细胞的临床试验中。例如,在具有对癌症抗原诸如mage-a3和ny-eso-1特异的tcr的t细胞的情况下,可以使用本发明的转换受体,并且据信这些t细胞加入转换受体将增加t细胞的功效。
本文引用的各个和每个专利、专利申请和出版物的公开内容在此都通过引用全文并入。尽管已经参考具体实施方案公开了本发明,但显而易见的是可由本领域技术人员设计本发明的其他实施方案和变化形式,而不脱离本发明的真实精神和范围。权利要求意欲被解释为包括所有这样的实施方案和等同变化形式。
序列表
<110>宾夕法尼亚大学董事会
c.h.琼
y.赵
<120>转换共刺激受体
<130>046483-6010-00-wo.601501
<150>us61/513,259
<151>2011-07-29
<160>12
<170>patentinversion3.5
<210>1
<211>870
<212>dna
<213>人工的
<220>
<223>化学合成的
<400>1
atgaagacattgcctgccatgcttggaactgggaaattattttgggtcttcttcttaatc60
ccatatctggacatctggaacatccatgggaaagaatcatgtgatgtacagctttatata120
aagagacaatctgaacactccatcttagcaggagatccctttgaactagaatgccctgtg180
aaatactgtgctaacaggcctcatgtgacttggtgcaagctcaatggaacaacatgtgta240
aaacttgaagatagacaaacaagttggaaggaagagaagaacatttcatttttcattcta300
cattttgaaccagtgcttcctaatgacaatgggtcataccgctgttctgcaaattttcag360
tctaatctcattgaaagccactcaacaactctttatgtgacagatgtaaaaagtgcctca420
gaacgaccctccaaggacgaaatggcaagcagaccctggctcctgtatagtttacttcct480
ttggggggattgcctctactcatcactacctgtttctgcctgttctgctgcctgagaagg540
caccaaggaaagcaaaatgaactctctgacacagcaggaagggaaattaacctggttgat600
gctcaccttaagagtgagcaaacagaagcaagcaccaggcaaaattcccaagtactgcta660
tcagaaactggaatttatgataatgaccctgacctttgtttcaggatgcaggaagggtct720
gaagtttattctaatccatgcctggaagaaaacaaaccaggcattgtttatgcttccctg780
aaccattctgtcattggaccgaactcaagactggcaagaaatgtaaaagaagcaccaaca840
gaatatgcatccatatgtgtgaggagttaa870
<210>2
<211>685
<212>dna
<213>人工的
<220>
<223>化学合成的
<400>2
aagcttgccgccatgaagacattgcctgccatgcttggaactgggaaattattttgggtc60
ttcttcttaatcccatatctggacatctggaacatccatgggaaagaatcatgtgatgta120
cagctttatataaagagacaatctgaacactccatcttagcaggagatccctttgaacta180
gaatgccctgtgaaatactgtgctaacaggcctcatgtgacttggtgcaagctcaatgga240
acaacatgtgtaaaacttgaagatagacaaacaagttggaaggaagagaagaacatttca300
tttttcattctacattttgaaccagtgcttcctaatgacaatgggtcataccgctgttct360
gcaaattttcagtctaatctcattgaaagccactcaacaactctttatgtgacagatgta420
aaaagtgcctcagaacgaccctccaaggacgaaatggcaagcagaccctggctcctgtat480
agtttacttcctttggggggattgcctctactcatcactacctgtttctgcctgttctgc540
tgcctggaggagtaagaggagcaggctcctgcacagtgactacatgaacatgactccccg600
ccgccccgggcccacccgcaagcattaccagccctatgccccaccacgcgacttcgcagc660
ctatcgctcctgataagcggccgca685
<210>3
<211>701
<212>dna
<213>人工的
<220>
<223>化学合成的
<400>3
aagcttgccgccatgaagacattgcctgccatgcttggaactgggaaattattttgggtc60
ttcttcttaatcccatatctggacatctggaacatccatgggaaagaatcatgtgatgta120
cagctttatataaagagacaatctgaacactccatcttagcaggagatccctttgaacta180
gaatgccctgtgaaatactgtgctaacaggcctcatgtgacttggtgcaagctcaatgga240
acaacatgtgtaaaacttgaagatagacaaacaagttggaaggaagagaagaacatttca300
tttttcattctacattttgaaccagtgcttcctaatgacaatgggtcataccgctgttct360
gcaaattttcagtctaatctcattgaaagccactcaacaactctttatgtgacagatgta420
aaaagtgcctcagaacgaccctccaaggacgaaatggcaagcagaccctggctcctgtat480
agtttacttcctttggggggattgcctctactcatcactacctgtttctgcctgttctgc540
tgcctggaaggaaatatagatcaaacaaaggagaaagtcctgtggagcctgcagagcctt600
gtcgttacagctgccccagggaggaggagggcagcaccatccccatccaggaggattacc660
gaaaaccggagcctgcctgctccccctgataagcggccgca701
<210>4
<211>685
<212>dna
<213>人工的
<220>
<223>化学合成的
<400>4
aagcttgccgccatgaagacattgcctgccatgcttggaactgggaaattattttgggtc60
ttcttcttaatcccatatctggacatctggaacatccatgggaaagaatcatgtgatgta120
cagctttatataaagagacaatctgaacactccatcttagcaggagatccctttgaacta180
gaatgccctgtgaaatactgtgctaacaggcctcatgtgacttggtgcaagctcaatgga240
acaacatgtgtaaaacttgaagatagacaaacaagttggaaggaagagaagaacatttca300
tttttcattctacattttgaaccagtgcttcctaatgacaatgggtcataccgctgttct360
gcaaattttcagtctaatctcattgaaagccactcaacaactctttatgtgacagatgta420
aaaagtgcctcagaacgaccctccaaggacgaaatggcaagcagaccctggctcctgtat480
agtttctggttacccataggatgtgcagcctttgttgtagtctgcattttgggatgcata540
cttattgaggagtaagaggagcaggctcctgcacagtgactacatgaacatgactccccg600
ccgccccgggcccacccgcaagcattaccagccctatgccccaccacgcgacttcgcagc660
ctatcgctcctgataagcggccgca685
<210>5
<211>701
<212>dna
<213>人工的
<220>
<223>化学合成的
<400>5
aagcttgccgccatgaagacattgcctgccatgcttggaactgggaaattattttgggtc60
ttcttcttaatcccatatctggacatctggaacatccatgggaaagaatcatgtgatgta120
cagctttatataaagagacaatctgaacactccatcttagcaggagatccctttgaacta180
gaatgccctgtgaaatactgtgctaacaggcctcatgtgacttggtgcaagctcaatgga240
acaacatgtgtaaaacttgaagatagacaaacaagttggaaggaagagaagaacatttca300
tttttcattctacattttgaaccagtgcttcctaatgacaatgggtcataccgctgttct360
gcaaattttcagtctaatctcattgaaagccactcaacaactctttatgtgacagatgta420
aaaagtgcctcagaacgaccctccaaggacgaaatggcaagcagaccctggctcctgtat480
agtttctggttacccataggatgtgcagcctttgttgtagtctgcattttgggatgcata540
cttattgaaggaaatatagatcaaacaaaggagaaagtcctgtggagcctgcagagcctt600
gtcgttacagctgccccagggaggaggagggcagcaccatccccatccaggaggattacc660
gaaaaccggagcctgcctgctccccctgataagcggccgca701
<210>6
<211>672
<212>dna
<213>人工的
<220>
<223>化学合成的
<400>6
aagcttgccgccatgaagacattgcctgccatgcttggaactgggaaattattttgggtc60
ttcttcttaatcccatatctggacatctggaacatccatgggaaagaatcatgtgatgta120
cagctttatataaagagacaatctgaacactccatcttagcaggagatccctttgaacta180
gaatgccctgtgaaatactgtgctaacaggcctcatgtgacttggtgcaagctcaatgga240
acaacatgtgtaaaacttgaagatagacaaacaagttggaaggaagagaagaacatttca300
tttttcattctacattttgaaccagtgcttcctaatgacaatgggtcataccgctgttct360
gcaaattttcagtctaatctcattgaaagccactcaacaactctttatgtgacagatgta420
aaaagtgcctcagaacgaccctccaaggacgaaatggcaagcagaccctggctcctgtat480
agtttacttcctttggggggattgcctctactcatcactacctgtttctgcctgttctgc540
tgcctgtgttggcttacaaaaaagaagtattcatccagtgtgcacgaccctaacggtgaa600
tacatgttcatgagagcagtgaacacagccaaaaaatctagactcacagatgtgacccta660
taagcggccgca672
<210>7
<211>1011
<212>dna
<213>人工的
<220>
<223>化学合成的
<400>7
aagcttgccgccatgaagacattgcctgccatgcttggaactgggaaattattttgggtc60
ttcttcttaatcccatatctggacatctggaacatccatgggaaagaatcatgtgatgta120
cagctttatataaagagacaatctgaacactccatcttagcaggagatccctttgaacta180
gaatgccctgtgaaatactgtgctaacaggcctcatgtgacttggtgcaagctcaatgga240
acaacatgtgtaaaacttgaagatagacaaacaagttggaaggaagagaagaacatttca300
tttttcattctacattttgaaccagtgcttcctaatgacaatgggtcataccgctgttct360
gcaaattttcagtctaatctcattgaaagccactcaacaactctttatgtgacagatgta420
aaaagtgcctcagaacgaccctccaaggacgaaatggcaagcagaccctggctcctgtat480
agtttacttcctttggggggattgcctctactcatcactacctgtttctgcctgttctgc540
tgcctgtgttggcttacaaaaaagaagtattcatccagtgtgcacgaccctaacggtgaa600
tacatgttcatgagagcagtgaacacagccaaaaaatctagactcacagatgtgacccta660
tgcagagtgaagttcagcaggagcgcagacgcccccgcgtaccagcagggccagaaccag720
ctctataacgagctcaatctaggacgaagagaggagtacgatgttttggacaagagacgt780
ggccgggaccctgagatggggggaaagccgagaaggaagaaccctcaggaaggcctgtac840
aatgaactgcagaaagataagatggcggaggcctacagtgagattgggatgaaaggcgag900
cgccggaggggcaaggggcacgatggcctttaccagggtctcagtacagccaccaaggac960
acctacgacgcccttcacatgcaggccctgccccctcgctaagcggccgca1011
<210>8
<211>672
<212>dna
<213>人工的
<220>
<223>化学合成的
<400>8
aagcttgccgccatgaagacattgcctgccatgcttggaactgggaaattattttgggtc60
ttcttcttaatcccatatctggacatctggaacatccatgggaaagaatcatgtgatgta120
cagctttatataaagagacaatctgaacactccatcttagcaggagatccctttgaacta180
gaatgccctgtgaaatactgtgctaacaggcctcatgtgacttggtgcaagctcaatgga240
acaacatgtgtaaaacttgaagatagacaaacaagttggaaggaagagaagaacatttca300
tttttcattctacattttgaaccagtgcttcctaatgacaatgggtcataccgctgttct360
gcaaattttcagtctaatctcattgaaagccactcaacaactctttatgtgacagatgta420
aaaagtgcctcagaacgaccctccaaggacgaaatggcaagcagaccctggctcctgtat480
agtttctggttacccataggatgtgcagcctttgttgtagtctgcattttgggatgcata540
cttatttgttggcttacaaaaaagaagtattcatccagtgtgcacgaccctaacggtgaa600
tacatgttcatgagagcagtgaacacagccaaaaaatctagactcacagatgtgacccta660
taagcggccgca672
<210>9
<211>1011
<212>dna
<213>人工的
<220>
<223>化学合成的
<400>9
aagcttgccgccatgaagacattgcctgccatgcttggaactgggaaattattttgggtc60
ttcttcttaatcccatatctggacatctggaacatccatgggaaagaatcatgtgatgta120
cagctttatataaagagacaatctgaacactccatcttagcaggagatccctttgaacta180
gaatgccctgtgaaatactgtgctaacaggcctcatgtgacttggtgcaagctcaatgga240
acaacatgtgtaaaacttgaagatagacaaacaagttggaaggaagagaagaacatttca300
tttttcattctacattttgaaccagtgcttcctaatgacaatgggtcataccgctgttct360
gcaaattttcagtctaatctcattgaaagccactcaacaactctttatgtgacagatgta420
aaaagtgcctcagaacgaccctccaaggacgaaatggcaagcagaccctggctcctgtat480
agtttacttcctttggggggattgcctctactcatcactacctgtttctgcctgttctgc540
tgcctgtgttggcttacaaaaaagaagtattcatccagtgtgcacgaccctaacggtgaa600
tacatgttcatgagagcagtgaacacagccaaaaaatctagactcacagatgtgacccta660
tgcagagtgaagttcagcaggagcgcagacgcccccgcgtaccagcagggccagaaccag720
ctctataacgagctcaatctaggacgaagagaggagtacgatgttttggacaagagacgt780
ggccgggaccctgagatggggggaaagccgagaaggaagaaccctcaggaaggcctgtac840
aatgaactgcagaaagataagatggcggaggcctacagtgagattgggatgaaaggcgag900
cgccggaggggcaaggggcacgatggcctttaccagggtctcagtacagccaccaaggac960
acctacgacgcccttcacatgcaggccctgccccctcgctaagcggccgca1011
<210>10
<211>690
<212>dna
<213>人工的
<220>
<223>化学合成的
<400>10
atgcagatcccacaggcgccctggccagtcgtctgggcggtgctacaactgggctggcgg60
ccaggatggttcttagactccccagacaggccctggaacccccccaccttctccccagcc120
ctgctcgtggtgaccgaaggggacaacgccaccttcacctgcagcttctccaacacatcg180
gagagcttcgtgctaaactggtaccgcatgagccccagcaaccagacggacaagctggcc240
gccttccccgaggaccgcagccagcccggccaggactgccgcttccgtgtcacacaactg300
cccaacgggcgtgacttccacatgagcgtggtcagggcccggcgcaatgacagcggcacc360
tacctctgtggggccatctccctggcccccaaggcgcagatcaaagagagcctgcgggca420
gagctcagggtgacagagagaagggcagaagtgcccacagcccaccccagcccctcaccc480
aggccagccggccagttccaaaccctggtgttctggttacccataggatgtgcagccttt540
gttgtagtctgcattttgggatgcatacttatttgttggcttacaaaaaagaagtattca600
tccagtgtgcacgaccctaacggtgaatacatgttcatgagagcagtgaacacagccaaa660
aaatctagactcacagatgtgaccctataa690
<210>11
<211>717
<212>dna
<213>人工的
<220>
<223>化学合成的
<400>11
atgcagatcccacaggcgccctggccagtcgtctgggcggtgctacaactgggctggcgg60
ccaggatggttcttagactccccagacaggccctggaacccccccaccttctccccagcc120
ctgctcgtggtgaccgaaggggacaacgccaccttcacctgcagcttctccaacacatcg180
gagagcttcgtgctaaactggtaccgcatgagccccagcaaccagacggacaagctggcc240
gccttccccgaggaccgcagccagcccggccaggactgccgcttccgtgtcacacaactg300
cccaacgggcgtgacttccacatgagcgtggtcagggcccggcgcaatgacagcggcacc360
tacctctgtggggccatctccctggcccccaaggcgcagatcaaagagagcctgcgggca420
gagctcagggtgacagagagaagggcagaagtgcccacagcccaccccagcccctcaccc480
aggccagccggccagttccaaaccctggtgttttgggtgctggtggtggttggtggagtc540
ctggcttgctatagcttgctagtaacagtggcctttattattttctgggtgaggagtaag600
aggagcaggctcctgcacagtgactacatgaacatgactccccgccgccccgggcccacc660
cgcaagcattaccagccctatgccccaccacgcgacttcgcagcctatcgctcctaa717
<210>12
<211>720
<212>dna
<213>人工的
<220>
<223>化学合成的
<400>12
atgcagatcccacaggcgccctggccagtcgtctgggcggtgctacaactgggctggcgg60
ccaggatggttcttagactccccagacaggccctggaacccccccaccttctccccagcc120
ctgctcgtggtgaccgaaggggacaacgccaccttcacctgcagcttctccaacacatcg180
gagagcttcgtgctaaactggtaccgcatgagccccagcaaccagacggacaagctggcc240
gccttccccgaggaccgcagccagcccggccaggactgccgcttccgtgtcacacaactg300
cccaacgggcgtgacttccacatgagcgtggtcagggcccggcgcaatgacagcggcacc360
tacctctgtggggccatctccctggcccccaaggcgcagatcaaagagagcctgcgggca420
gagctcagggtgacagagagaagggcagaagtgcccacagcccaccccagcccctcaccc480
aggccagccggccagttccaaaccctggtgatccttgtgatcttctctggaatgttcctt540
gttttcaccctggccggggccctgttcctccatcaacgaaggaaatatagatcaaacaaa600
ggagaaagtcctgtggagcctgcagagccttgtcgttacagctgccccagggaggaggag660
ggcagcaccatccccatccaggaggattaccgaaaaccggagcctgcctgctccccctaa720
- 还没有人留言评论。精彩留言会获得点赞!
- 作为5-HT<sub>2A</sub>血清素受体调节剂适用于治疗与其相关的病症的3-苯基-吡唑衍生物的制作方法
- 作为5-HT<sub>2A</sub> 血清素受体调节剂适用于治疗与其相关的病症的3-苯基-吡唑衍生物的制作方法
- 用于诊断表达her2受体或其截短形式的癌症的方法
- 人T2R受体hT2R50的新单体型及其在鉴定人苦味调节剂的测定法中的用途的制作方法
- 一种新的多肽——嗅觉受体27.61 和编码这种多肽的多核苷酸的制作方法
- 一种新的多肽——t1/st2受体结合蛋白10.23和编码这种多肽的多核苷酸的制作方法
- 一种新的多肽——人嘌呤受体9.46和编码这种多肽的多核苷酸的制作方法
- 一种新的多肽——人嘌呤受体13.75和编码这种多肽的多核苷酸的制作方法
- 一种新的多肽——人sigma受体15.07和编码这种多肽的多核苷酸的制作方法
- 一种新的多肽——补体受体12和编码这种多肽的多核苷酸的制作方法