检测鲤春病毒血症病毒的试剂盒及其检验方法与流程
本发明是有关一种核酸的测定和检验方法,特别是有关于一种利用聚合酶连锁反应检测鲤春病毒血症病毒的试剂盒及其检验方法。
背景技术:
鲤春病毒血症(springviraemiaofcarp,svc)又称鲤鱼传染性腹水症,是由鲤春病毒血症病毒(springviremiaofcarpvirus,svcv)引起的急性、出血性并伴有高度传染的流行病,会严重危害渔业生产并能造成毁灭性打击。
鲤春病毒血症病毒分类于棒状病毒科(rhabdoviridae),疱病毒属(vesiculovirus)。由单链、负股rna组成,基因组包含11019个核苷酸,可转译出5个结构蛋白质,分别为核蛋白(nucleoprotein,n)、磷蛋白(phosphoprotein,p)、基质蛋白(matrixprotein,m)、醣蛋白(glycoprotein,g)及核醣核酸相关聚合酶(rna-dependentrnapolymerase,l)。有一层囊膜,病毒大小约为180×70nm,在cscl中的浮密度为1.195-1.200g/ml。根据其结构蛋白组分可把鲤春病毒血症病毒列入水泡性口炎类,且目前研究证明鲤春病毒血症病毒只有一种血清型。
鲤春病毒血症病毒通常感染鲤科鱼类,在鲤、锦鲤、草鱼、鲢、鳙、黑鲫和鲫等鱼中可发生明显的症状,但鲤是其中最敏感的宿主。鲤春病毒血症以全身出血及腹水、发病急、死亡率高为特征,常常于春季暴发并引起幼鱼和成鱼死亡。在急性感染时,染病鱼体的肝、肾、脾、鳃、及脑为高力价病毒存在器官。鲤春病毒血症最早流行于欧洲、中东和俄罗斯,近年来传播到美洲和亚洲。世界动物卫生组织(oie)将其列为必报的重要疫病。也为2008年我国新颁布的动物疫病名录中将其列为一类动物疫病。因此开发快速、方便及准确检测鲤春病毒血症病毒的试剂盒及其检验方法,以方便鲤春病毒血症的现场或实验室检测至为关键。
技术实现要素:
有鉴于此,本发明的一目的是在提供一种检测鲤春病毒血症病毒的试剂盒及其检测方法,可以快速且特异性地自待测样本中检测鲤春病毒血症病毒。
本发明的一方式是在提供一种检测鲤春病毒血症病毒的试剂盒,包含一引物对,所述引物对包含一序列辨识编号1所示的正向引物以及一序列辨识编号2所示的反向引物。
依据前述的检测鲤春病毒血症病毒的试剂盒,可更包含一如序列辨识编号3所示的荧光探针。
依据前述的检测鲤春病毒血症病毒的试剂盒,可更包含一反转录聚合酶连锁反应所需的试剂。
本发明的另一方式是在提供一种检测鲤春病毒血症病毒的检验方法,包含以下步骤。提供一待测样本作为一模版。将所述模板进行一反转录聚合酶连锁反应,以获得一cdna模板。将cdna模板以前段所述的检测鲤春病毒血症病毒的试剂盒进行聚合酶连锁反应,以获得一聚合酶连锁反应产物,而所述检测鲤春病毒血症病毒的试剂盒包含一引物对,所述引物对包含序列辨识编号1所示的正向引物以及序列辨识编号2所示的反向引物。最后侦测所述聚合酶连锁反应产物的分子量大小是否为98bp。
依据前述的检测鲤春病毒血症病毒的检验方法,其中所述聚合酶连锁反应产物可具有如序列辨识编号4所示的序列。
依据前述的检测鲤春病毒血症病毒的检验方法,其中侦测所述聚合酶连锁反应产物可以胶体电泳系统进行。
本发明的又一方式是在提供一种检测鲤春病毒血症病毒的检验方法,包含以下步骤。提供一待测样本作为一模版。将所述模板进行一反转录聚合酶连锁反应,以获得一cdna模板。将cdna模板以前段所述的检测鲤春病毒血症病毒的试剂盒进行一荧光探针式聚合酶连锁反应,而所述检测鲤春病毒血症病毒的试剂盒包含一引物对和一荧光探针,所述引物对包含序列辨识编号1所示的正向引物和序列辨识编号2所示的反向引物,所述荧光探针具有如序列辨识编号3所示的序列。最后检测是否具有一荧光信号值。
依据前述的检测鲤春病毒血症病毒的检验方法,其中所述荧光探针式聚合酶连锁反应可为实时聚合酶连锁反应(real-timepcr)或隔绝恒温式聚合酶连锁反应(insulatedisothermalpcr,iipcr)。
本发明的再一方式是在提供一种检测鲤春病毒血症病毒的检验方法,包含以下步骤。提供一待测样本作为一模版。将所述模板以前段所述的检测鲤春病毒血症病毒的试剂盒依序进行一反转录聚合酶连锁反应和一dna扩增反应。所述检测鲤春病毒血症病毒的试剂盒为预混形式,其包含一引物对、一反转录聚合酶连锁反应所需的试剂和/或一荧光探针,所述引物对包含序列辨识编号1所示的正向引物和序列辨识编号2所示的反向引物,所述荧光探针具有如序列辨识编号3所示的序列。而所述dna扩增反应为一聚合酶连锁反应或一荧光探针式聚合酶连锁反应。最后侦测是否具有一预期聚合酶连锁反应产物。dna扩增反应为聚合酶连锁反应时,当一聚合酶连锁反应产物的分子量大小为98bp时,为具有预期聚合酶连锁反应产物的表征。dna扩增反应为荧光探针式聚合酶连锁反应时,一荧光信号值为具有预期聚合酶连锁反应产物的表征。
依据前述的检测鲤春病毒血症病毒的检验方法,其中所述荧光探针式聚合酶连锁反应可为实时聚合酶连锁反应或隔绝恒温式聚合酶连锁反应。
由此,本发明的检测鲤春病毒血症病毒的试剂盒及其检验方法,能快速、特异、方便且准确地检测待测样本中是否存在鲤春病毒血症病毒,显示待测样本已感染鲤春病毒血症病毒。本发明的检测鲤春病毒血症病毒的试剂盒及其检验方法的检测结果除了可经由一般常规跑胶确认结果外,也可进行荧光聚合酶连锁反应及隔绝恒温式聚合酶连锁反应确认结果,其中尤其隔绝恒温式聚合酶连锁反应的检测结果不需复杂的资料判读,即使未受过专业训练的人员,也能利用本发明的试剂盒及检验方法进行鲤春病毒血症病毒的检测,搭配可携式的荧光核酸分析仪可用于田野间水产养殖渔业的检测,能快速且准确的诊断病原感染以供提早防治。
上述发明内容旨在提供本揭示内容的简化摘要,以使阅读者对本揭示内容具备基本的理解。此发明内容并非本揭示内容的完整概述,且其用意并非在指出本发明实施例的重要/关键组件或界定本发明的范围。
附图说明
为让本发明的上述和其他目的、特征、优点与实施例能更明显易懂,所附图式的说明如下:
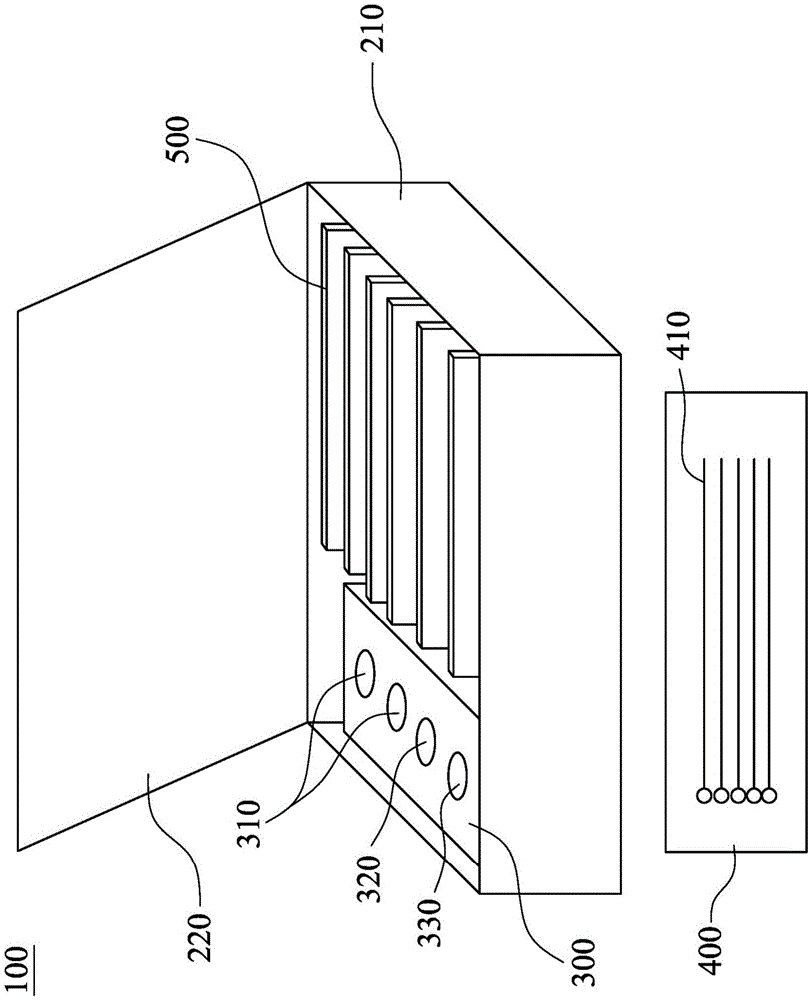
图1表示依照本发明的一实施方式的检测鲤春病毒血症病毒的试剂盒的结构示意图。
图2表示本发明的另一实施方式的检测鲤春病毒血症病毒的检验方法的步骤流程图。
图3表示本发明的又一实施方式的检测鲤春病毒血症病毒的检验方法的步骤流程图。
图4表示本发明的又一实施方式的检测鲤春病毒血症病毒的检验方法的步骤流程图。
图5为本发明的检测鲤春病毒血症病毒的试剂盒的检测特异性分析结果图。
图6为本发明的检测鲤春病毒血症病毒的试剂盒的检测灵敏度分析结果图。
图7为本发明的检测鲤春病毒血症病毒的试剂盒进行隔绝恒温式聚合酶连锁反应的胶体电泳分析图。
其中,附图符号的说明如下:
100:检测鲤春病毒血症病毒的试剂盒;
210:盒体;
220:盒盖;
300:内衬;
310:预混缓冲溶液模块;
320:阳性对照模块;
330:核酸缓冲溶液模块;
400:接样环组件;
410:接样环;
500:预混试剂组件;
600:检测鲤春病毒血症病毒的检验方法;
610、620、630、640:步骤;
700:检测鲤春病毒血症病毒的检验方法;
710、720、730、740:步骤;
800:检测鲤春病毒血症病毒的检验方法;
810、820、830:步骤。
具体实施方式
本说明书揭露内容提供一种快速检测鲤春病毒血症病毒的试剂盒以及其检验方法。其以鲤春病毒血症病毒的高度保留区设计特异性引物对,以包含引物对的试剂盒与待测样本进行聚合酶连锁反应,当有预期聚合酶连锁反应产物时,为待测样本中存在鲤春病毒血症病毒的表征,显示待测样本已感染鲤春病毒血症病毒。并可进一步地设计与鲤春病毒血症病毒具有特异性的荧光探针,以包含引物对及荧光探针的试剂盒,与待测样本进行荧光探针式聚合酶连锁反应,当有荧光讯号时,为待测样本中存在鲤春病毒血症病毒的表征,显示待测样本已感染鲤春病毒血症病毒。
本发明前述所称的“荧光探针”指一包含连续至少8个核苷酸的分子,其为选取pcr上下游引物之间的一段序列作为探针,并在探针的5`-端标记上荧光基团(reporter),3`-端标记上相应的荧光抑制染剂(quencher),由于两个基团靠得很近,构成荧光能量传递的关系,没有荧光信号产生,在每一个循环的退火(annealing)过程中,该探针可以与模板相结合,随后的延伸反应中,当引物合成至探针与模板结合处时,taq酶的5`-外切酶活性可以降解探针的5`-端,并因此使荧光基团与荧光抑制染剂上的淬灭基团分离,让荧光基团释放出荧光。例如荧光探针的5'端荧光基团可使用fam(520nm)或joe、vic(550nm)等,而荧光探针的3'端荧光抑制染剂可使用黑洞淬灭剂(blackholequencher)(bhq1)或是非荧光淬灭剂(nonfluorescentquencher)(nfq)等,然其仅为示例不作为本发明的限定。
本发明前述所称的“隔绝恒温式聚合酶连锁反应(insulatedisothermalpcr,iipcr)”为一新的荧光检测技术,以单点温度控制并利用热对流的原理,完成聚合酶连锁反应过程中解离dna双股结构的反应(denaturing)、引物退火反应(annealing)和延长反应(extension)等三步骤的循环。因只需底部单一温度控制,且以自然的温度梯度取代机械式的升降温,可使机器更轻量化、避免机器因反复升降温造成机械故障,以及省下升降温所需的时间。因检测结果不需资料判读,即使未受过专业训练的人员,也能利用本发明的检测鲤春病毒血症病毒的试剂盒及检测方法进行鲤春病毒血症病毒的检测。
下列实验例用于示范说明本发明,用以有利于本发明所属技术领域通常知识者,可在不需过度解读的情形下完整利用并实践本发明,而不应将这些实验例视为对本发明范围的限制,但用于如何实施本发明的材料及方法。
[检测鲤春病毒血症病毒的试剂盒]
本发明的检测鲤春病毒血症病毒的试剂盒,包含一引物对,所述引物对包含一序列辨识编号1所示的正向引物以及一序列辨识编号2所示的反向引物。较佳地,本发明的检测鲤春病毒血症病毒的试剂盒可更包含如序列辨识编号3所示的荧光探针。更佳地,本发明的检测鲤春病毒血症病毒的试剂盒可更包含一反转录聚合酶连锁反应所需的试剂,用以将待测样本中的模板经由反转录聚合酶连锁反应反转录为cdna模板,使得本发明的检测鲤春病毒血症病毒的试剂盒为预混形式,可于同一试验管中依序进行反转录聚合酶连锁反应和dna扩增反应。
请参照图1,表示依照本发明的一实施方式的检测鲤春病毒血症病毒的试剂盒100的结构示意图。检测鲤春病毒血症病毒的试剂盒100包含盒体210、盒盖220、内衬300、接样环组件400和预混试剂组件500。
盒盖220用于盖合盒体210,盒盖220的内表面设置有海绵缓冲层。内衬300、接样环组件400和预混试剂组件500依序设置于盒体210内。
内衬300包含预混缓冲溶液模块310、阳性对照模块320和核酸缓冲溶液模块330。预混缓冲溶液模块310设有相应的孔位,用以放置溶解混合引物的第一缓冲溶液。阳性对照模块320用以放置阳性核酸干粉。核酸缓冲溶液模块330用以放置溶解阳性核酸干粉的第二缓冲溶液。
接样环组件400包括至少一袋独立包装的接样环包,每袋接样环包内放置有若干个接样环410。
预混试剂组件500包括至少一袋独立包装的预混试剂包,每袋预混试剂包内有若干管预混试剂管,预混试剂管内放置冻干粉末,冻干粉末包括dntps、引物对、荧光探针、反转录酶和dna聚合酶。其中引物对包含序列辨识编号1所示的正向引物以及序列辨识编号2所示的反向引物。荧光探针的序列如序列辨识编号3所示,于此实施例,荧光探针的3’端具有nfq荧光抑制染剂,5’端具有fam荧光基团修饰。
检测鲤春病毒血症病毒的试剂盒100中预混试剂管为预先混好的预混形式,未添加rox参比染料,使用时只需依据待测样本数取出对应量的预混试剂管,将预混试剂管的冻干颗粒、预混缓冲溶液模块310内的第一缓冲溶液混合,并以接样环410将待测样本转移至预混试剂管中,即可开始反应。如需要加入荧光染料校正real-timepcr仪器,可依照各实验室的标准试验流程加入rox参比染料即可。检测鲤春病毒血症病毒的试剂盒100简单、方便携带,可常温携带和保存。并且,如果对检测鲤春病毒血症病毒的试剂盒100进行铝箔包装密封,冷冻保存于-20℃则可存放1年以上效能不变。
[检测鲤春病毒血症病毒的检验方法]
请参照图2,表示本发明的另一实施方式的检测鲤春病毒血症病毒的检验方法600的步骤流程图。检测鲤春病毒血症病毒的检验方法600包含步骤610、步骤620、步骤630和步骤640。
步骤610为提供一待测样本作为一模版。所述待测样本可为鱼的鱼鳃样本、脾脏样本及消化道器官样本。并可进一步利用商业萃取试剂盒或其他习知方法萃取待测样本中的核酸,其步骤及原理被相关领域中具有通常知识者所知悉,因而此处不再详细赘述。
步骤620为将所述模板进行反转录聚合酶连锁反应,以获得一cdna模板。
步骤630为将所述cdna模板以包含序列辨识编号1所示的正向引物以及序列辨识编号2所示的反向引物的引物对进行聚合酶连锁反应,以获得一聚合酶连锁反应产物。
步骤640为侦测所述聚合酶连锁反应产物的分子量大小是否为98bp。若聚合酶连锁反应产物的分子量大小为98bp,则表示待测样本中存在鲤春病毒血症病毒,显示待测样本已感染鲤春病毒血症。较佳地,聚合酶连锁反应产物具有如序列辨识编号4所示的序列。而聚合酶连锁反应产物可以胶体电泳系统进行侦测。
请参照图3,表示本发明的另一实施方式的检测鲤春病毒血症病毒的检验方法700的步骤流程图。检测鲤春病毒血症病毒的检验方法700包含步骤710、步骤720、步骤730和步骤740。
步骤710为提供一待测样本作为一模版。所述待测样本可为鱼的鱼鳃样本、脾脏样本及消化道器官样本,并可进一步利用商业萃取试剂盒或其他习知方法萃取待测样本中的核酸。
步骤720为将所述模板进行反转录聚合酶连锁反应,以获得一cdna模板。
步骤730为将所述cdna模板以序列辨识编号1所示的正向引物、序列辨识编号2所示的反向引物以及序列辨识编号3所示的荧光探针进行一荧光探针式聚合酶连锁反应。较佳地,荧光探针式聚合酶连锁反应可为实时聚合酶连锁反应(real-timepcr)或隔绝恒温式聚合酶连锁反应(insulatedisothermalpcr,iipcr)。
步骤740为检测是否具有一荧光信号值,若具有荧光信号值,则表示待测样本中存在鲤春病毒血症病毒,显示待测样本已感染鲤春病毒血症。
请参照图4,表示本发明的又一实施方式的检测鲤春病毒血症病毒的检验方法800的步骤流程图。检测鲤春病毒血症病毒的检验方法800包含步骤810、步骤820和步骤830。
步骤810为提供一待测样本作为一模版。所述待测样本可为鱼的鱼鳃样本、脾脏样本及消化道器官样本,并可进一步利用商业萃取试剂盒或其他习知方法萃取代测样本中的核酸。
步骤820为将所述模板于同一试验管中以本发明的检测鲤春病毒血症病毒的试剂盒依序进行一反转录聚合酶连锁反应和一dna扩增反应。所述检测鲤春病毒血症病毒的试剂盒包含一引物对、一反转录聚合酶连锁反应所需的试剂和/或一荧光探针,所述引物对包含序列辨识编号1所示的正向引物和序列辨识编号2所示的反向引物,所述荧光探针具有如序列辨识编号3所示的序列。而所述dna扩增反应为一聚合酶连锁反应或一荧光探针式聚合酶连锁反应。而荧光探针式聚合酶连锁反应可为实时聚合酶连锁反应或隔绝恒温式聚合酶连锁反应。
步骤830为侦测是否具有一预期聚合酶连锁反应产物。dna扩增反应为聚合酶连锁反应时,当一聚合酶连锁反应产物的分子量大小为98bp时,为具有预期聚合酶连锁反应产物的表征。dna扩增反应为荧光探针式聚合酶连锁反应时,一荧光信号值为具有预期聚合酶连锁反应产物的表征。
[试验例]
1.实时聚合酶连锁反应
请参照图1和图4,详细地,若以检测鲤春病毒血症病毒的试剂盒100进行实时聚合酶连锁反应以检测鲤春病毒血症病毒为例。
先以100μl的第二缓冲溶液溶解阳性对照组核酸干粉,以获得浓度为4×10-5ng/μl的阳性对照,并将回溶后的阳性对照保存于4℃备用。再打开预混试剂包,并根据待测样本数取出对应量的预混试剂管。
而预混试剂管中冻干颗粒回溶方式如下列步骤。若不需添加rox参比染料,打开管盖,每一管预混试剂管加入50μl的第一缓冲溶液回溶冻干颗粒,即获得实时聚合酶连锁反应混合液。实时聚合酶连锁反应混合液中,dntps的浓度为0.5mm、序列辨识编号1所示的正向引物酸和序列辨识编号2所示的反向引物的浓度分别为0.5μm、荧光探针的浓度为0.05μm、反转录酶的浓度为16u以及dna聚合酶的浓度为13u。若需添加rox参比染料校正real-timepcr仪器,每一管预混试剂管加入49μl的第一缓冲溶液和1μl的rox参比染料回溶冻干颗粒。
将回溶好的冻干颗粒溶液每管取23μl分装到0.2ml的荧光pcr专用反应管中。取2μl的待测样本、阳性对照或阴性对照,加入含有23μl冻干颗粒溶液的荧光pcr专用反应管。其中,阴性对照不含有靶标基因的核酸。
再依据反应条件进行扩增反应。探针检测模式设置为:reporterdye-fam、quencherdye-mgb或none,依机型而定。反应条件设定为42℃反应30分钟,然后进入40次循环,每次的循环条件为93℃反应15秒、60℃反应60秒。
反应结束后保存检测数据文件,并进一步进行结果判定。分析条件设置为先设定标准曲线中阳性标准品的量。再点击程序的自动分析功能,获得分析结果。其中阳性标准品的ct值<32,即表示整组试剂效能及反应正常。若在fam信道扩增曲线有明显对数增长,则为阳性结果,表示待测样本中存在鲤春病毒血症病毒,显示待测样本已感染鲤春病毒血症病毒。若在fam信道扩增曲线无对数增长,则为阴性结果,表示待测样本中不存在鲤春病毒血症病毒,或是存在低于检测灵敏度的病毒量。
首先,本试验例对本发明的检测鲤春病毒血症病毒的试剂盒及其检验方法进行检测特异性分析,所使用的待测样本包含鲤春病毒血症病毒(svcv)、病毒性出血性败血病病毒(vhsv)、传染性造血器官坏死病病毒(ihnv)、传染性胰腺坏死病毒(ipnv)、鲑传染性贫血病毒(isav)、鲑甲病毒(sav)的核酸。
请参照图5,为本发明的检测鲤春病毒血症病毒的试剂盒的检测特异性分析结果图。结果显示,本发明的检测鲤春病毒血症病毒的试剂盒及其检验方法只对鲤春病毒血症病毒有特异性扩增,而其它供试毒株则未见扩增曲线,显示本发明的检测鲤春病毒血症病毒的试剂盒及其检验方法具有良好的特异性。
本试验例进一步地对本发明的检测鲤春病毒血症病毒的试剂盒及其检验方法进行检测灵敏度分析。首先构筑一内含鲤春病毒血症病毒的目标基因的质体,再以此质体利用试管内反转录rna作为正控制组的模板,之后利用紫外分光亮度计测定反转录rna模板的浓度和纯度,根据测定的浓度计算拷贝数。再以depc水将反转录rna模板进行10倍序列稀释,稀释成3.2×107复本至3.2×100复本,作为标准品以测试灵敏度,并将前述序列稀释后的标准品以本发明的检测鲤春病毒血症病毒的试剂盒及其检验方法进行检测,详细的检测步骤如前所述,在此不再赘述。
请参照图6,为本发明的检测鲤春病毒血症病毒的试剂盒的检测灵敏度分析结果图,其中由左至右的曲线依序为3.2×107复本、3.2×106复本、3.2×105复本、3.2×104复本、3.2×103复本、3.2×102复本、3.2×101复本的检测曲线,而3.2×100复本没有扩增曲线。结果显示,本发明的检测鲤春病毒血症病毒的试剂盒及其检验方法对鲤浮肿病毒的检测灵敏度高达32个复本。
2.隔绝恒温式聚合酶连锁反应
若以检测鲤春病毒血症病毒的试剂盒100进行隔绝恒温式聚合酶连锁反应以检测鲤春病毒血症病毒为例,先以100μl的第二缓冲溶液溶解阳性对照组核酸干粉,以获得浓度为4×10-5ng/μl的阳性对照,并将回溶后的阳性对照保存于4℃备用。再打开预混试剂包,并根据待测样本数取出对应量的预混试剂管,而预混试剂管中冻干颗粒回溶方式如下列步骤。打开管盖,每一管预混试剂管加入50μl的第一缓冲溶液回溶冻干颗粒,即获得隔绝恒温式聚合酶连锁反应混合液,将溶液混合后移至隔绝恒温式聚合酶连锁反应管中,以隔绝恒温式聚合酶连锁反应装置进行等温扩增。反应条件为反转录42℃反应10分钟,底部加热95℃30分钟即可得的反应结果。
为了了解本发明的检测鲤春病毒血症病毒的试剂盒进行隔热同温聚合酶连锁反应增幅98bp的聚合酶连锁反应产物的稳定性,将试管内反转录rna依序稀释成复本数目为100作为阳性对照组,接着以对本发明的检测鲤春病毒血症病毒的试剂盒及其检验方法进行检测分析,隔绝恒温式聚合酶连锁反应产物另以胶体电泳分离,以确保本发明的精确性。
请参照图7和表一,图7为本发明的检测鲤春病毒血症病毒的试剂盒进行隔绝恒温式聚合酶连锁反应的胶体电泳分析图,其中m为核酸的分子量标记,n为不含有靶标基因核酸的阴性对照组。表一为本发明的检测鲤春病毒血症病毒的试剂盒进行隔绝恒温式聚合酶连锁反应的荧光讯号分析结果。
表一、隔绝恒温式聚合酶连锁反应的荧光分析结果
由图7的结果显示,在复本数目为100的阳性对照组,利用本发明的检测鲤春病毒血症病毒的试剂盒,即序列辨识编号1所示的正向引物、如序列辨识编号2所示的反向引物,以及序列辨识编号3所示的荧光探针,于3个独立试验管中皆能稳定增幅出大小为98bp的聚合酶连锁反应产物。于表一的荧光讯号分析中,将进行iipcr后的520nm讯号值,除以进行iipcr前的520nm讯号值可得一信噪比(signal-to-noiseratio),当信噪比超过反应器预设的阈值时,判读为具有荧光讯号(以+表示)。阳性对照组皆于波长520nm可侦测到荧光讯号,而未加模板的阴性组则无荧光讯号。结果显示,无论以荧光侦测或是胶体电泳分析反应结果,本发明的检测鲤春病毒血症病毒的试剂盒,皆能检验待测样本中是否具有鲤春病毒血症病毒。
综上所述,本发明的检测鲤春病毒血症病毒的试剂盒及其检验方法能够灵敏、特异性好、快速且操作简单方便的对鲤春病毒血症病毒进行检测。检测鲤春病毒血症病毒的试剂盒不仅能够特异、灵敏的对鲤春病毒血症病毒进行检测,而且检测鲤春病毒血症病毒的试剂盒若搭配轻便、易携带,结合便携式的荧光核酸分析仪,例如pockit智能型手提式核酸分析仪(金瑞鸿捷),在池塘边就可以对鲤春病毒血症病毒进行现场检测,为鲤春病毒血症病毒的快速检测和防控提供了有效的科学手段和重要依据,对保障我国鲤科鱼类的进出口贸易以及国内生产养殖安全具有重要意义。
本发明已以实施方式揭露如上,然其并非用以限定本发明,任何熟习此技艺者,在不脱离本发明的精神和范围内,当可作各种的更动与润饰,因此本发明的保护范围当以后附的权利要求书所界定者为准。
序列表(sequencelisting)
<110>深圳出入境检验检疫局食品检验检疫技术中心
金瑞鸿捷(厦门)生物科技有限公司
<120>检测鲤春病毒血症病毒的试剂盒及其检验方法
<160>4
<170>patentinversion3.3
<210>1
<211>23
<212>dna
<213>人工序列(artificialsequence)
<220>
<221>
<222>
<223>引物(primer),增幅鲤春病毒血症病毒的正向引物
<400>1
gtagtaccccattctgttcattt23
<210>2
<211>23
<212>dna
<213>人工序列(artificialsequence)
<220>
<221>
<222>
<223>引物(primer),增幅鲤春病毒血症病毒的反向引物
<400>2
ttcatttcgcacactttttctct23
<210>3
<211>20
<212>dna
<213>人工序列(artificialsequence)
<220>
<221>
<222>
<223>引物(primer),荧光探针
<400>3
tgatcgatccagtgtcctcc20
<210>4
<211>98
<212>dna
<213>鲤春病毒血症(springviraemiaofcarp)
<220>
<221>
<222>
<223>cds,增幅的鲤春病毒血症病毒脱氧核醣核酸片段
<400>4
gtagtaccccattctgttcatttagagccatatggaggacattggatcgatcacgaattt60
aatgggggcgaatgcagagaaaaagtgtgcgaaatgaa98
- 还没有人留言评论。精彩留言会获得点赞!