用于抑制NPC1基因表达的siRNA的应用的制作方法
本发明属于生物医药技术领域,尤其涉及用于抑制npc1基因表达的sirna的应用。
背景技术:
结直肠癌是常见的消化道恶性肿瘤,占胃肠道肿瘤的第二位。结直肠癌好发部位为直肠与乙状结肠交界处,占60%;发病多在40岁以后。5-氟尿嘧啶可在细胞内转化成不同的细胞毒性代谢产物,作用与s期,属于抗代谢类抗肿瘤药。
然而,5-氟尿嘧啶的药性有限,还有必要研发出用于治疗结直肠癌的新药物。
技术实现要素:
本发明目的在于克服现有技术存在的不足,而提供抑制npc1基因表达的sirna的应用,抑制npc1基因表达的sirna可降低结肠癌对5-氟尿嘧啶的耐药性。
为实现上述目的,本发明采取的技术方案为:用于抑制npc1基因表达的sirna,其特征在于,至少为以下两条sirna中一种:
npc1-sirna-1,其正义链的核苷酸序列如seqidno.1所示,其反应链的核苷酸序列如seqidno.2所示;
npc1-sirna-3,其正义链的核苷酸序列如seqidno.3所示,其反应链的核苷酸序列如seqidno.4所示。
npc1蛋白是一个由1278个氨基酸组成并含有13次跨膜螺旋的膜蛋白,npc1蛋白是胆固醇在人体细胞内不可或缺的搬运工,npc1异常是c型niemann-pick疾病的主要致病因素。
另外,本发明还提供npc1-sirna-1在制备用于治疗结直肠癌药物中的应用,npc1-sirna-1正义链的核苷酸序列如seqidno.1所示,其反应链的核苷酸序列如seqidno.2所示。
另外,本发明还提供npc1-sirna-1和5-氟尿嘧啶在制备用于治疗结直肠癌药物中的应用,npc1-sirna-1正义链的核苷酸序列如seqidno.1所示,其反应链的核苷酸序列如seqidno.2所示。
另外,本发明还提供一种用于治疗结直肠癌药物,其包括npc1-sirna-1和5-氟尿嘧啶,npc1-sirna-1正义链的核苷酸序列如seqidno.1所示,其反应链的核苷酸序列如seqidno.2所示。
另外,本发明还提供npc1-sirna-3在制备用于治疗结直肠癌药物中的应用,npc1-sirna-3正义链的核苷酸序列如seqidno.3所示,其反应链的核苷酸序列如seqidno.4所示。
另外,本发明还提供npc1-sirna-3和5-氟尿嘧啶在制备用于治疗结直肠癌药物中的应用,npc1-sirna-1正义链的核苷酸序列如seqidno.3所示,其反应链的核苷酸序列如seqidno.4所示。
另外,本发明还提供一种用于治疗结直肠癌药物,其包括npc1-sirna-3和5-氟尿嘧啶,npc1-sirna-1正义链的核苷酸序列如seqidno.3所示,其反应链的核苷酸序列如seqidno.4所示。
本发明有益效果:本发明提供抑制npc1基因表达的sirna的应用,本发明设计的npc1-sirna-1、npc1-sirna-3在hct-116和hct-8细胞中均能良好地抑制npc1基因的表达;在npc1-sirna-1、npc1-sirna-3转染下,敲低npc1的hct-116和hct-8肿瘤细胞对5-fu的耐药作用得到降低。
附图说明
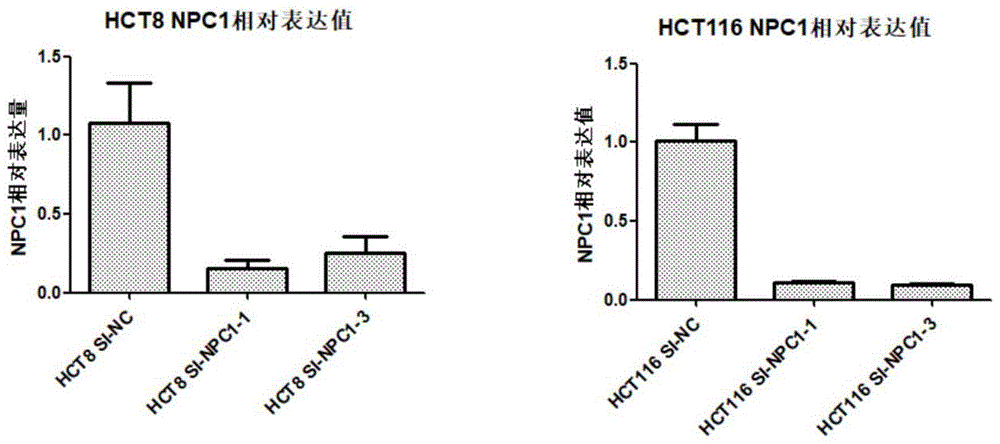
图1显示npc1-sirna转染hct-116和hct-8细胞后,细胞中npc1蛋白的表达量;其中,nc表示阴性对照,npc1-1表示采用npc1-sirna-1进行转染,npc1-2表示采用npc1-sirna-2进行转染,npc1-3表示采用npc1-sirna-3进行转染;
图2显示npc1-sirna对hct-116和hct-8细胞耐药性的影响;其中,gapdh表示阳性对照,nc-si表示阴性对照,npc1-si01表示采用npc1-sirna-1进行转染,npc1-si03表示采用npc1-sirna-3进行转染。
具体实施方式
为更好地说明本发明的目的、技术方案和优点,下面将结合具体实施例和附图对本发明作进一步说明。
npc1-sirna的设计
本发明设计了3个npc1-sirna,npc1-sirna的核苷酸序列如表1所示。
表1npc1-sirna的核苷酸序列
涉及的实验方法
细胞的培养
结直肠癌细胞系hct-116,hct8由中山大学胃肠病学研究所保存,hct-116用含10%胎牛血清(invitrogen,grandisland,ny,usa)的dmem(gibco,china)培养基,hct8用含10%胎牛血清(invitrogen,grandisland,ny,usa)的rpmi1640(gibco,china)培养基,置于含5%二氧化碳、37℃恒温潮湿的培养箱中培养。
瞬时转染细胞
用npc1-sirna瞬时转染hct-116,hct8。当细胞接种于6孔板24小时细胞密度达到50%后,按照生产商说明以脂质体lipofectamine2000(invitrogen,usa)为载体用npc1-sirna和nc-sirna瞬时转染hct-116,hct8,npc1-sirna和nc-sirna模拟物最终浓度为10nm。转染8小时后更换含10%fbs的新鲜培养基。为了验证转染效果,提取转染后三天总rna并通过实时定量pcr验证npc1敲低的表达效果。
npc1表达水平的检测
按照trizol试剂(invitrogen,usa)的生产商说明书中的步骤提取细胞总rna。步骤如下:(1)吸弃培养基,用1ml的pbs冲洗两次,每孔加入trizol试剂0.5ml,室温放置5min;(2)将细胞裂解液全部转移到1.5ml的ep管中,加入0.1ml氯仿,剧烈震荡15s,室温下静置5min,12,000g,4℃离心15min;(3)取上层水相转移到另外一个新的无rnase的离心管内,加入等体积的异丙醇,轻柔混匀,室温放置10min,12,000g,4℃离心15min;(4)弃上清,加入75%乙醇洗涤rna沉淀,7,500g,4℃离心10min,弃上清,空气干燥rna沉淀10min,用depc水溶解rna。用all-in-onemirnaqrt-pcrdetectionkit(genecopoeia,china)试剂盒进行rt-pcr扩增。所得定量数据由7500softwarev2.0.6(appliedbiosystems)导出,每个样品的thresholdcycle(ct)值代表所测基因的表达水平,由δδct方法计算出来的值代表npc1与内参基因的差异,最后由2-δδct方法处理数据,得出数据代表npc1的表达水平。
5-fu耐药试验
将5-fu(sigma,china)粉剂用dmso配制成浓度为1m的储存液备用。细胞以106个/孔的密度接种于6孔板后培养24小时,加入5-fu使得终浓度分别为0.01μm,0.1μm,1μm,10μm,100μm,1000μm,分别培养96小时。
细胞存活率的测试(mts)
按照celltiter96@aqneousonesolutionreagent试剂的生产商说明书中的步骤测细胞存活率。步骤如下:(1)室温溶解,往每个96孔板加入20ul,于37℃培养箱避光孵育2小时;(2)取出培养板,490nm测量细胞吸光度,并统计处理。
实验结果
如图1所示,本发明设计的npc1-sirna-1、npc1-sirna-2和npc1-sirna-3在hct-116和hct8细胞中均能良好地抑制npc1基因的表达。
如图2所示,在一系列5-fu浓度下(0μm,1μm,5μm,10μm,20μm,50μm,100μm,200μm),敲低npc1的hct-116和hct-8肿瘤细胞对5-fu的耐药作用得到降低。
实施例1
本实施例提供一种用于治疗结直肠癌药物,其包括npc1-sirna-1和5-氟尿嘧啶,npc1-sirna-1正义链的核苷酸序列如seqidno.1所示,其反应链的核苷酸序列如seqidno.2所示。
实施例2
本实施例提供一种用于治疗结直肠癌药物,其包括npc1-sirna-3和5-氟尿嘧啶,npc1-sirna-1正义链的核苷酸序列如seqidno.3所示,其反应链的核苷酸序列如seqidno.4所示。
最后所应当说明的是,以上实施例用以说明本发明的技术方案而非对本发明保护范围的限制,尽管参照较佳实施例对本发明作了详细说明,本领域的普通技术人员应当理解,可以对本发明的技术方案进行修改或者同等替换,而不脱离本发明技术方案的实质和范围。
sequencelisting
<110>中山大学附属第六医院
<120>用于抑制npc1基因表达的sirna的应用
<130>2019.6.24
<160>4
<170>patentinversion3.3
<210>1
<211>19
<212>rna
<213>人工序列
<400>1
ggagccacguacuucauga19
<210>2
<211>19
<212>rna
<213>人工序列
<400>2
ucaugaaguacguggcucc19
<210>3
<211>19
<212>rna
<213>人工序列
<400>3
ccauguuccuuucggauaa19
<210>4
<211>19
<212>rna
<213>人工序列
<400>4
uuauccgaaaggaacaugg19
- 还没有人留言评论。精彩留言会获得点赞!