一种结核分枝杆菌RNA/DNA同步定量分析方法与流程
本发明属于生物工程检测技术领域,具体涉及临床标本中结核分枝杆菌的荧光定量检测方法。
背景技术:
结核病(TB)是一种危害严重的慢性传染病,全球有约20亿人被感染,每年新增结核病患者达800-1000万,每年因结核病死亡人数为200-300万。我国结核病情况同样较为严峻,年发病人数约为130万,因结核病死亡人数每年达13万,超过其它传染病死亡人数的总和。我国是全球22个结核病流行严重的国家之一,同时也是全球27个耐多药结核病流行严重的国家之一。我国结核病患病人数居世界第二位,仅次于印度。20世纪90年代以来,结核病群或高危人群的流动或移民以及结核病控制放松及艾滋病病毒(HIV)与结核分枝杆菌双重感染蔓延等因素使结核病在全球的传播有“死灰复燃”的趋势。同时,耐药、耐多药(MDR)及超耐药(XDR)结核病占结核病比率提高,导致多种一、二线抗结核药物治疗效果下降,诊断及治疗成本上升,许多国家不同程度地出现了疫情下降缓慢或严重反弹的局面,发病率以每年1.1%的速度增长,结核病再次成为威胁人类健康的主要传染病,带来严重的公共卫生问题和重大的经济社会问题。据世界卫生组织报道,目前全球有近1/3的人感染了结核杆菌,即20亿人口感染了结核杆菌,其中活动性肺结核病人约2000万,每年新增结核病人约800~1000万,每年约有300万人死于结核病。结核病已成为导致全世界成人因传染病而死亡的主要疾病之一。我国是全球22个结核病高发国家之一,活动性肺结核病人数居世界第二位。结核病在我国流行的特点为“四高一低”:高患病率、高耐药率、高死亡率、高感染率和低递降率。据2000年全国结核病流行病学抽样调查估计,全国现有活动性肺结核病人450万,其中传染性肺结核病人150万。因此结核病防治是我国乃至全球疾病防治的重要课题。近年来世界各地结核分枝杆菌的多耐药菌株逐渐增多,甚至引起暴发流行。结核分枝杆菌的耐药可由自发突变产生(原发性耐药)或由于用药不当经突变选择产生(继发性耐药)。目前滥用抗生素、过渡治疗的现象很普遍,如何准确快速判断药物治疗的药效是目前急需解决的问题。临床诊断肺结核的主要依据是检测痰中结核分枝杆菌,其中,涂片法简单易行,但阳性率较低;罗氏培养法虽然是金标准,但检测周期长,均难以满足临床需要。因此提供敏感、特异、快速、可靠、简便、适合临床应用的实验室检查技术已成为国内外研究的重点。其中实时荧光PCR因其技术成熟,具有较高的灵敏性和特异性,已逐步应用到临床中。实时荧光定量PCR技术,是指在PCR反应体系中加入一对引物的同时加入一个特异性荧光探针(TaqMan探针),目前常用的TaqMan探针5′端标记有报告基团(Reporter,R),如FAM、VIC等,3′端标记有荧光淬灭基团(Quencher,Q),如TAMRA等。对于完整的TaqMan探针,报告基团所发射的荧光能量被淬灭基团吸收,仪器检测不到信号。随着PCR的进行,Taq酶在链延伸过程中遇到与模板结合的探针,其3′→5′外切核酸酶活性就会将探针切断,报告基团远离淬灭基团,其能量不能被吸收,即产生荧光信号。每经过一个PCR循环,荧光信号随着目的片段的扩增而指数增长,检测每个循环结束后的荧光强度,整个反应结束后,便可得到一条扩增曲线,由已知浓度标准样品的扩增曲线可以得到一条标准曲线,根据该标准曲线以及未知模板的扩增曲线可对未知模板进行定量分析。目前已有的检测方法是单独检测样本DNA或者RNA,但还没有在同一管反应中同步检测RNA和DNA的报道。在前期工作基础上,本发明提出在同一管反应中同时检测RNA和DNA的方法,具体为:分别以结核分枝杆菌复合群的16SrRNA基因和23SrRNA基因为靶目标,对16SrRNA设计一条逆转录引物、一对PCR引物以及一条Taqman探针,对23SrDNA设计另一对PCR引物以及另一条Taqman探针,在一个反应体系中同时进行RT-qPCR(16srRNA+16srDNA)和qPCR(23SrDNA)。分别测定总核酸(DNA+RNA)、以及DNA的绝对浓度,并算出(DNA+RNA)/DNA比值。具体地,通过分别比较16SrRNA和23SrDNA的Ct值以及5个绝对浓度已知的定量内参做出的标准曲线,可以求得待测标本中结核分枝杆菌(RNA+DNA)和DNA的绝对浓度,作为待测标本中结核分枝杆菌核酸定量检测结果,判断结核分枝杆菌的有无及丰度;通过比较16SrRNA总核酸与23SrDNA的Ct值(分别对应FAM和HEX检测通道),可以算出(DNA+RNA)/DNA比值,作为判定标本中细菌生长活性的标准:当该比值大于200时,待测标本中结核分枝杆菌为活跃生长的活菌,当比值在2-200之间,为生长较慢的活菌,比值小于2时,为不生长的死菌。此方法的优势:(1)可以比较结核分枝杆菌中RNA和DNA的相对量,从而判断细菌的生长状态;(2)样本需求量变少,加上(DNA+RNA)的量一般比DNA量大数十倍甚至更多,可以提高检测灵敏度;(3)方法更简便,两管PCR反应,合并到一管,节约成本和工作量;(4)由于在同一管中进行PCR,反应效率一致,DNA与RNA的比值更加精确。
技术实现要素:
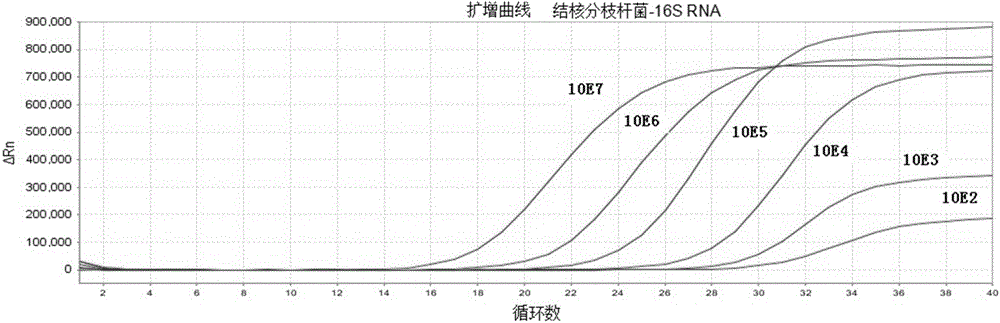
本发明的目的是克服现有技术中存在的缺陷,提供一种检测灵敏度高、且操作简单的结核分枝杆菌DNA与RNA同步检测的荧光定量PCR分析方法。本发明提供的结核分枝杆菌的荧光定量PCR检测方法,通过对RDP(RibosomalDatabaseProject)中结核分枝杆菌复合群的16SrRNA和23SrDNA全序列进行生物信息学比对分析,选取序列保守片段为靶目标,应用primerexpress软件和primerpremier5.0软件,设计一条逆转录引物和两对PCR引物以及两条Taqman探针。本发明方法所用的结核分枝杆菌复合群特异性定量检测试剂包含一条逆转录引物和两对特异性PCR引物以及两条特异性荧光探针,扩增目的扩增片段长度分别为100bp(16SrRNA基因)和67bp(23SrDNA)。具体来说,本发明提供的结核分枝杆菌RNA/DNA同步定量分析方法,具体步骤如下:1、通过生物信息学分析,选择结核分支杆菌的16SrRNA基因的保守片段为靶目标,其基因片段的扩增目标核苷酸序列为:GGGATGCATGTCTTGTGGTGGAAAGCGCTTTAGCGGTGTGGGATGAGCCCGCGGCCTATCAGCTTGTTGGTGGGGTGACGGCCTACCAAGGCGACGACGG(SEQIDNO.5)选择结核分支杆菌的23SrRNA基因的保守片段为靶目标,其基因片段的扩增目标核苷酸序列为:TGGGTCCTGAGGCAACACTCGGACTTGTTCCAGGTGTTGTCCCACCGCCTTGGTGGTGGGGTGTGGT(SEQIDNO.9)2、应用primerexpress软件和primerpremier5.0软件,设计一条结核分支杆菌的逆转录引物和两对PCR引物以及两条Taqman探针,具体地:16SrRNA引物和探针序列为:逆转录引物MTBC-RT:5’-CCGTATCTCAGTCCCAGTGT-3’(SEQIDNO.1)上游引物:MTBC-16SF:5’-GGGATGCATGTCTTGTGGTG-3’(SEQIDNO.2)下游引物:MTBC-16SR:5’-CCGTCGTCGCCTTGGTAG-3’(SEQIDNO.3)Taqman探针序列MTBC-16SP:5'-FAM-CGGGCTCATCCCACACCGCTA-TAMRA-3’(SEQIDNO.4);23SrRNA引物和探针序列为:上游引物:MTBC-23SF:5’-CCTCTGCTGCCAAGAAAAGC-3’(SEQIDNO.6)下游引物:MTBC-23SR:5’-GTTATCTCGTACGCCTTGGTATGC-3’(SEQIDNO.7)Taqman探针序列MTBC-23SP:5'-HEX-TCTAGCGAGCACACACACGGCCC-TAMRA-3';(SEQIDNO.8);3、构建和制备质粒定量标准品根据本发明中的PCR产物,利用DNA重组技术将包含目的扩增片段的基因克隆到质粒载体pGEM-TEasyVector中,构建的重组质粒作为检测结核杆菌RNA/DNA同步定量分析的定量标准品;4、分离样本中结核分枝杆菌,提取总核酸,使提取的样本中同时含有DNA与RNA成分;5、分别以结核分枝杆菌复合群的16SrRNA和23SrDNA为靶目标,对16SrRNA,使用设计的一条逆转录引物、一对PCR引物以及一条Taqman探针;对23SrDNA,使用设计的另一对PCR引物以及另一条Taqman探针,对提取的同一例样本同时进行RT-qPCR,其中,RT(Reversetranscription)部分为单重的只针对16SrRNA的逆转录反应,qPCR(QuantitativePCR)部分为两重(针对16SrRNA和23SrRNA)的实时定量PCR反应。通过比较16SrRNA和23SrDNA的Ct值以及5个绝对浓度已知的定量内参(105-101copies/ul)做出的标准曲线,求得待测标本中结核分枝杆菌DNA的绝对浓度,作为待测标本中结核分枝杆菌DNA定量检测结果;通过比较16SrRNA与23SrDNA的Ct值(分别对应FAM和HEX检测通道),算出(DNA+RNA)/DNA比值,作为判定标本中结核分枝杆菌生长活性的标准,即根据FAM通道或HEX通道的Ct值,计算FAM通道Ct值/HEX通道Ct值,也就是(16SrRNA+16SrDNA)/23SrDNA,代表了总核酸(RNA和DNA)与DNA的拷贝数比值;当该比值大于200时,待测标本中结核分枝杆菌为活跃生长的活菌,当比值在2-200之间,为生长较慢的活菌,比值小于2时,为不生长的死菌。结核分枝杆菌RNA/DNA同步定量分析方法进一步分析(1)结核分枝杆菌DNA、RNA同步抽提本发明利用新的核酸抽提方法,同时提取结核分支杆菌中的DNA与RNA,此类提取方法的难点是如何提高核酸的质与量。为了保证提取过程中DNA与RNA的完整性,方法1中提取液同时含有异硫氰酸胍与酚:氯仿:异戊醇(25:24:1),方法2中提取液则含有PH值7.8的TE缓冲液。另外,上述两种方法都利用了MiniBeadbeater-1研磨珠均质器对结核分支杆菌进行物理破壁,极大的提高了核酸抽提的量。分别以两种方法提取相同菌量的总核酸作为模板进行R/P分析,方法1所得扩增曲线的Ct值较大,R/Pratio比值为0.6,说明模板中存在抑制剂。方法2所得扩增曲线的Ct值较小,R/Pratio比值为1.1,说明模板量损失少,提取效率较高。由于方法2通过纯化试剂盒对提取的核酸进行了纯化,故PCR反应抑制作用不明显,完全可以保证模板总核酸的准确扩增。另外方法2的步骤简单、需时少,成本较低、适合大样本的处理。因此,在后续试验中采用方法2进行模板总核酸的提取。(2)引物与探针的特异性分析NCBI数据库的现有序列中,只有结核杆菌复合群的基因序列与提交的一对引物及一条探针具有高度同源性,其中正向引物与探针的特异性较反向引物好。与其他细菌及人的序列没有同源性,引物与探针的特异性好。为了进一步验证引物与探针在实际检测中的特异性,运用本课题反应体系对人基因组DNA和大肠杆菌基因组DNA分别进行了检测,结果均为阴性,其Ct值在36左右,与无模板阴性对照一致,PCR产物电泳未见100bp条带。而结核杆菌复合群DNA标准品经上述方法检测则显示为阳性,其Ct值为22。将PCR产物电泳可以得到大小为100bp的目的条带,且无引物二聚体。说明本课题引物和探针与人及大肠杆菌基因组DNA无交叉反应,特异性较强,扩增曲线见图1。(3)荧光定量PCR反应条件的优化通过对反应体系中不同浓度的定量PCR引物、Taqman探针、以及退火温度等实验结果进行比较,最终选择反应灵敏度高、本底荧光信号低、具有典型S型扩增荧光信号曲线、扩增效率接近于1的最优反应体系。引物浓度的优化:在反应体系中其他条件相同的情况下,将MTBC的PCR引物浓度从0.1umol/L至0.5umol/L以0.05umol/L递增,均可行。通过试验结果分析比较,确定较佳的引物终浓度为0.2-0.4umol/L,最佳的引物终浓度为0.3umol/L。探针浓度优化:在反应体系中其他条件相同的情况下,将MTBC的探针浓度分别从0.1umol/L至0.8umol/L做倍比连续稀释后进行检测,均可行。通过试验结果分析比较,确定较佳的引物终浓度为0.3-0.6umol/L,最佳的引物终浓度为0.4umol/L。退火温度优化:通过比较退火温度的优化试验结果后,选定较佳退火温度为55℃-65℃,最佳退火温度为60℃。(4)绝对定量标准曲线重组质粒标准品pGEM-TEasy-16srRNA首先运用紫外线分光光度计进行浓度测定,并根据其分子量计算出相关的拷贝数。然后将原始质粒标准品依次进行10倍梯度稀释,分别生成101、102、103、104、105、106、107拷贝/微升等不同浓度的质粒标准品。每个浓度进行3个重复,并设阴性空白对照,进行实时荧光定量PCR(图2,图3)。利用平均CT值作图可得到标准曲线(图4)。从图4分析可得出标准曲线的检测极限是10拷贝/微升,相关系数是0.999,通过标准曲线的斜率(S=-3.39)可以计算出扩增效率E(E=10-1/斜率-1)是0.97。说明该反应的检测结果可靠性高。(5)定量检测结果判定标准1)检测样本中1×108copies/ml≥TBDNA(HEX通道)≥5×102copies/ml,测定结果有效,可直接报告相应的拷贝量;2)检测样本中TBDNA(HEX通道)≥1×108copies/ml,既可直接报告为≥1×108copies/ml,也可用生理盐水按10倍梯度做相应稀释,使其拷贝量落在1×105~5×107copies/ml范围内再重新测定,测定结果应以稀释倍数进行校正;3)检测样本TBDNA(HEX通道)的拷贝量为<5×102copies/ml时,报告拷贝数为<5×102copies/ml;4)Ct值不显示时,报告该样本TBDNA小于检测极限。(6)死活菌检测结果判定标准1)若DNA+RNA(FAM通道)及DNA(HEX通道)的CT值均≤35,且DNA+RNA(FAM通道)/DNA(HEX通道)的拷贝数比值>200,则判断该检测样本含有大量活菌,该患者为活动性肺结核,有极大传染性;2)若DNA+RNA(FAM通道)及DNA(HEX通道)的CT值均≤35,且DNA+RNA(FAM通道)/DNA(HEX通道)的拷贝数比值在2-200之间,则判断该检测样本含有部分活菌或者可能为患者治疗后体内的结核菌活力比正常低有一定传染性;3)若DNA+RNA(FAM通道)及DNA(HEX通道)的CT值均≤35,且DNA+RNA(FAM通道)/DNA(VIC通道)的拷贝数比值在0-2之间,则判断该检测样本是无活力的死菌,治疗有效。本发明方法评价经过大量的反应条件优化、对比试验和验证试验,并经过临床样本的检测应用评估。对建立的方法进行灵敏度、稳定性、特异性以及对临床样本的有效性进行综合评价:(1)灵敏度:用TE分别将质粒定量标准品pGEM-TEasy-23SrRNA稀释至1010、109、108、107、106、105、104、103、102、101、100copies/ul,采用经优化后的体系进行检测,验证所建立的方法的灵敏度。本检测方法在1010-102copies/reaction数量级范围内具有良好的线性关系,相关系数R=0.9937,其检测范围可达9个数量级。(2)稳定性:从批间重复和批内重复两个方面进行评价。批内重复性:选取同一份样本设5个平行反应管同时进行反应,检测其CT值及比值的变异系数。批间重复性:选取同一份样本,一周内重复检测5次,检测其CT值及比值的变异系数。(3)特异性:本发明选取了5个人的基因组DNA样本进行检测,结果只有结核分支杆菌样本呈阳性结果,5份人的基因组DNA均为阴性结果。本发明采用的荧光定量PCR技术巧妙的利用了PCR技术的高效扩增、探针技术的高特异性和光谱技术的敏感性及实时定量的优点,克服了常规PCR定性检测的一些不足,极大地提高了检测的敏感性和特异性,检测灵敏度可达102数量级;并且缩短了实验时间,简化了实验操作,而且荧光检测的结果由电脑软件分析,避免了产物后处理过程所致的污染,较常规PCR更为客观、灵敏、准确。同时,本发明中采用的阳性对照是根据结核分支杆菌的保守序列设计构建的标准质粒,使得阳性标准品德来源可靠,避免了阳性毒株在每次实验中的使用。本发明方法可进行大批量的样本分析,并对结核分枝杆菌复合群进行定量,从而为结核分支杆菌的检测和监控提供有效方法。附图说明图1.荧光定量PCR方法的特异性分析结果。从左至右,依次为结核分枝杆菌质粒标准品、阴性对照、人基因组DNA、大肠杆菌DNA。图2.结核分枝杆菌16SrRNA基因不同浓度的标准品实时荧光定量PCR的扩增曲线。图3.结核分枝杆菌23SrRNA基因不同浓度的标准品实时荧光定量PCR的扩增曲线。图4.绝对定量标准曲线,横坐标是DNA拷贝数,纵坐标是平均CT值。图5.病人的R/P比值与治疗天数之间的关系,病人1(A),2(B),3(C),4(D)。横坐标是治疗天数,纵坐标是R/P比值。具体实施方式下面结合具体实施例详细说明本发明,但不以任何形式限制本发明要求保护的范围。实施例1:肺内临床标本的检测总共检测了207份肺内标本,在总的207份肺内标本中,30份是培养阳性标本(其中24份是涂片阳性,6份涂片阴性),另外177份则是培养阴性(其中27份涂片阳性,150份涂片阴性)。24份培养和涂片同时阳性的标本,R/P检测结果都为阳性;其余6份培养阳性涂片阴性的样本中,只有4份样本R/P检测结果阳性;而177份培养阴性样本中,其中156份样本R/P检测结果阴性,只有21份样本R/P检测结果阳性。在所有肺内样本中,一共有23份样本的培养和R/P结果之间是存在分歧的:其中21份样本是R/P阳性而培养阴性的,另外2份样本则是R/P阴性而培养阳性(如表1)。基于表1,计算出肺内标本的灵敏度、特异度、阳性预测值、阴性预测值分别为93.3%、88.1%、57.1%、98.7%。为了更好的解决上述23例分歧标本,我们回顾性的查看了病人的临床证据,发现17份分歧样本可以得到解决。另外4份未得到解决的样本,我们则进行了样本重新检测。调整后的肺内标本检测结果(如表2),其中45份样本是真阳性,157份样本是真阴性,4份样本是假阳性,1份样本是假阴性。基于表2,计算得出临床灵敏度、特异度、阳性预测值、阴性预测值分别为97.8%、97.5%、91.8%、99.4%。实施例2:评价肺外标本的结核分枝杆菌的活动性在总的28份肺外标本中,4份样本同时涂片和培养阳性,2份样本涂片阴性而培养阳性。另外的22份培养阴性样本中,有5份涂片阳性,17份涂片阴性。4份培养和涂片同时阳性的标本,R/P检测结果都为阳性;其余2份培养阳性涂片阴性的样本中,R/P检测结果也都为阳性。而22份培养阴性样本中,18份样本R/P检测结果阴性,另外4份样本R/P检测结果阳性,即4份分歧样本(如表1)。基于这些数据,计算出总的肺外标本的灵敏度为100%,特异度为81.8%,阳性预测值为60%,阴性预测值为100%。通过查看分歧样本的临床证据之后,其中10份样本是真阳性,17份样本是真阴性,1份样本是假阳性。基于表2,计算得出临床肺外标本灵敏度、特异度、阳性预测值、阴性预测值则分别为100%、94.4%、91.0%、100%。表1.运用R/P分析检测临床样本MTBC的结果+:阳性;—:阴性;n:样本量。表2.调整R/P分析与培养结果之间分歧数据之后的临床样本MTBC检测结果n:样本量。在总的235份临床样本中,当分歧样本解决后,以培养结果和临床评估为参考标准,R/P分析中55份样本是真阳性,1份样本是假阴性,5份样本是假阳性,174份样本是真阴性。而荧光定量PCR分析中,47份样本是真阳性,9份样本是假阴性,18份样本是假阳性,161份样本是真阴性。R/P分析的灵敏度(98.2%vs83.9%,p<0.05)和特异度(97.2%vs89.9%,p<0.05)都比荧光定量PCR高,且具有统计学差异(如表3)。R/P分析的阳性预测值和阴性预测值分别为91.7%,99.4%,比荧光定量PCR的好很多(91.7%vs72.3%,p<0.05;99.4%vs94.7%,p<0.05)(如表3)。表3.基于分歧数据调整之后,R/P分析与荧光定量PCR之间的比较*:有统计学差异(p<0.05);n:样本量。实施例3:新药临床试验治疗效果的监测为了对某种新型的抗结核分枝杆菌的药物临床效果进行评估,我们收集了4例结核病患者多份临床样本(标本数≥2)。这4例病人我们一直监测其治疗效果,直至他们的样本培养阴性为止,样本的R/P结果和培养及临床证据结果始终一致,但是荧光定量PCR的检测结果则一直保持阳性(如表4)。表4.运用培养、涂片、荧光定量PCR、R/P分析等方法监测结核患者治疗效果的比较这4例结核患者初始抗结核治疗(0天)的R/P分析比值,比治疗一段时间之后的比值要高很多。经过抗结核治疗之后,病人1的R/P分析比值从第0天的6.2降低到第75天的1.23;病人2的R/P分析比值从第0天的4降低到第50天的1.4;病人3的R/P分析比值从第0天的4.5降低到第63天的0.9;病人4的R/P分析比值从第0天的3.8降低到第40天的1.2。4例结核病人经过治疗之后的R/P比值都小于1.51,即都转为阴性(如图5)。SEQIDNO.1:ccgtatctcagtcccagtgtSEQIDNO.2:gggatgcatgtcttgtggtgSEQIDNO.3:ccgtcgtcgccttggtagSEQIDNO.4:cgggctcatcccacaccgctaSEQIDNO.5:gggatgcatgtcttgtggtggaaagcgctttagcggtgtgggatgagcccgcggcctatcagcttgttggtggggtgacggcctaccaaggcgacgacggSEQIDNO.6:CCTCTGCTGCCAAGAAAAGCSEQIDNO.7:GTTATCTCGTACGCCTTGGTATGCSEQIDNO.8:TCTAGCGAGCACACACACGGCCCSEQIDNO.9:TGGGTCCTGAGGCAACACTCGGACTTGTTCCAGGTGTTGTCCCACCGCCTTGGTGGTGGGGTGTGGT
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1
- 一种敲除c‑di‑AMP分解酶的重组耻垢分枝杆菌株及其应用的制造方法与工艺
- 检测结核分枝杆菌感染的抗原多肽池及其应用的制造方法与工艺
- 一种猕猴桃分枝定位器的制造方法与工艺
- 一种xanthone类化合物及其单晶的制备方法与作为抗海分枝杆菌药物的应用与制造工艺
- 一种糖肽类抗生素耐药基因检测试剂盒的制造方法与工艺
- 分枝杆菌快速分离培养方法与制造工艺
- 一种用于检测潜在结核的特异性标志物及其应用的制造方法与工艺
- 结核分枝杆菌抗原蛋白Rv2941及其T细胞表位肽的应用的制造方法与工艺
- 一种微流控芯片上基于荧光量子点磁性富集并分离结核分枝杆菌TB的方法及装置与制造工艺
- 二肽meso‑DAP‑D‑Ala和/或四肽L‑Ala‑D‑Glu‑L‑Lys‑D‑Ala的新用途的制造方法与工艺