基于超支化聚醚胺的两亲性高分子夺氢型光引发剂及其制备方法与流程
本发明涉及一种基于超支化聚醚胺的两亲性高分子夺氢型光引发剂及其制备方法,属于光化学技术领域。
背景技术:
紫外光固化技术具有固化速度快,经济高效,节能环保,环境友好等特点,使其在涂料,油墨,光刻胶,微电子,光致抗蚀剂,齿科材料,粘合剂,光盘复制等工业领域有着广泛的应用。而光引发剂作为光固化体系中的关键组成部分,它关系到配方体系在光照射下低聚物以及稀释剂能否快速有效的由液态转化为固态,因此对光引发剂的研究有着非常重要的意义。而传统的小分子光引发剂容易挥发和发生迁移,一方面会降低光聚合引发效率,另一方面导致产品出现气味和毒性,使得光固化体系的应用有很大的局限性。将小分子光引发剂接枝到超支化聚醚胺大分子链上,制备出基于超支化聚醚胺的两亲性高分子光引发剂,不仅克服了小分子易迁移黄变的缺点大大提高了引发性能,还使得聚合体系更加环保经济。(中国专利,CN 1594370A,CN1887913A,CN102432699A)
近年来,由于技术的快速发展,对光引发剂的性能要求越来越高。不仅要求光引发剂有优越的引发性能,而且要求其与光固化体系相容性好,毒性小,环境兼容性好,稳定性好等特点。随着经济的发展,对环保问题的逐渐重视,实用环保的水性光引发剂逐渐成为研究的焦点,并且成为光引发的发展趋势,具有极大的发展前景。彭欢等人(中国专利,CN 104558630A)开发了一种硫杂蒽酮改性树枝形聚酰胺-胺水溶性光引发剂,可在水性系中使用,具有优异的引发性能。聂俊等人(中国专利,CN1887913A)研发了一种高分子性二苯甲酮光引发剂,可在油性体系中使用。但是在水性体系和油性体系中同时具有优异引发性能,并且含有共引发剂胺的基于超支化聚醚胺的两亲性高分子夺氢型光引发剂却没有报道。
技术实现要素:
本发明的目的在于针对目前现有技术的不足,提供一种基于超支化聚醚胺的两亲性高分子夺氢型光引发剂及其制备方法。该引发剂引发效率高,与水以及油性溶剂相容性好,毒性低,环境兼容性好,制备方法简单,应用广泛。
为实现上述目的,本发明通过简单的方法将小分子光引发剂接枝到具有共引发剂胺的超支化聚醚胺的链上,制备出一种新型的两亲性高分子夺氢型光引发剂。具体技术方案介绍如下。
本发明提供一种基于超支化聚醚胺的两亲性高分子夺氢型光引发剂,结构如式(1)所示:
其中,X表示聚醚链,Y表示共引发剂胺分子残基,P表示光引发剂分子残基;其中:
所述共引发剂胺单体分子残基Y具有式(3)所示结构:
其中,R2为C2-C10直链或支链烷基,C2-C10烷氧基,环烷基或被烷基取代氢的哌嗪;R3为氢、C1-C10直链或支链烷基、C1-C10烷氧基、羟基、羧基、酯基、环烷基、苯基、萘基或杂环式基。
本发明中,所述X具有如式(2)所示结构:
其中,R1为C1-C20直链或支链烷基,C1-C20烷氧基,环烷基,苯基,萘基,杂环式基或这些基团氢原子被取代基取代的产物,0<n<20;
本发明中,所述光引发剂分子残基P选自如式(4)所列结构的一种:
其中,R6、R7、R8、R9、R10和R11分别独立地选自氢、卤素、C1-C20直链或支链烷基、C1-C20烷氧基、硝基、氨基、羟基、羧基、腈基、磺酸基、酯基、环烷基、苯基或萘基;R4、R5和R12分别独立地选自芳香基或芳香基上的氢原子被任意取代基取代的产物;X1为亚甲基,氧,硫或氮原子;n1,2,3,4,5,6为整数,0<n1,2,,4,5,6<5,0<n3<3;
本发明还提供一种上述基于超支化聚醚胺的两亲性高分子夺氢型光引发剂的制备方法,具体步骤如下:
①按照摩尔比为0.95:1~1:0.95,将含有伯胺和仲胺的共引发剂和含双环氧基团的聚醚在有机溶剂中混和,在惰性气体的保护下,冰水浴搅拌混合1.5~2.5天后,75~85℃温度下反应,反应结束后,将有机溶剂旋蒸除去,干燥,得到超支化聚醚胺;
②按照摩尔比为0.9:1~1:0.9,将超支化聚醚胺与带有官能团的小分子光引发剂溶于有机溶剂中,75~85℃温度下反应,反应结束后,旋蒸除去有机溶剂,在沉淀剂中进行沉淀,干燥,得到基于超支化聚醚胺的两亲性高分子夺氢型光引发剂;其中:
步骤①中,所述含有伯胺和仲胺的共引发剂单体的结构如式(5)所示:
其中,R2为C2-C10直链或支链烷基,C2-C10烷氧基,环烷基或被烷基取代氢的哌嗪;R3为氢、C1-C10直链或支链烷基、C1-C10烷氧基、羟基、羧基、酯基、环烷基、苯基、萘基或杂环式基;
本发明中,步骤①中,所述含双环氧基团的聚醚的结构如式(6)所示:
其中,R1为C1-C20直链或支链烷基,C1-C20烷氧基,环烷基,苯基,萘基,杂环式基或这些基团氢原子被取代基取代的产物,0<n<20。
本发明中,步骤①和②中,所述超支化聚醚胺的结构如式(8)所示:
本发明中,步骤②中,所述带有官能团的小分子光引发剂,结构如式(7)所示:
P-L-R13 (7)
其中,P为式(4)中任一引发剂残基,L为C1-C20直链或支链烷基,C1-C20烷氧基,环烷基或苯基,R13为环氧基团,羧基或酯基。
本发明中,步骤①和②中,所述有机溶剂为甲苯,醇类,二氯甲烷,氯仿,1,4-二氧六环,酮类,二甲基亚砜或N,N-二甲基甲酰胺。
本发明中,步骤②中,所述沉淀剂为正己烷或石油醚。
本发明中,步骤②中,所述惰性气体为氮气或氩气。
本发明的优点如下:所得的基于超支化聚醚胺的两亲性高分子夺氢型光引发剂,其分子中含有夺氢型光引发剂和共引发剂胺,有利于俩者之间的能量转移,能够更快更多的产生自由基,提高引发效率:另外,作为一种高分子光引发剂,其克服了传统小分子光引发剂易挥发,迁移,黄变,稳定性差,有残留等缺陷;同时其主链超支化聚醚胺与水,油性溶剂和商业性单体相容性都有很好的相容性,不仅提高的引发性能,而且使得光引发剂不易迁移到表面,降低了光引发剂的毒性,并且其环境相容性好,使用环保,尤其作为水性光引发剂符合环保使用的发展趋势,因此其在涂料,油墨,微电子,齿科材料,光致抗蚀剂,光盘复制,光刻胶,粘合剂,电子封装材料等光固化领域有广阔的应用前景。
本发明的核磁H谱图是通过(VarianMercuryPlus400MHz)核磁谱仪测得的。
本发明的红外谱图是通过实时红外仪器(Thermo IS10傅里叶红外光谱仪器,)测得的。
本发明的固化动力学谱图是通过光致差示量热计(Photo-DSC)(DSC6200,Seiko Instrument Inc)测得的。本发明所有固化动力学实验的光源为带有365nm光栅的高压汞灯,光强范围50mW/cm2,氮气保护为50ml/min。
附图说明
图1是实施案例1所合成的基于超支化聚醚胺的两亲性高分子夺氢型光引发剂(hPEA101-TX)的红外谱图。
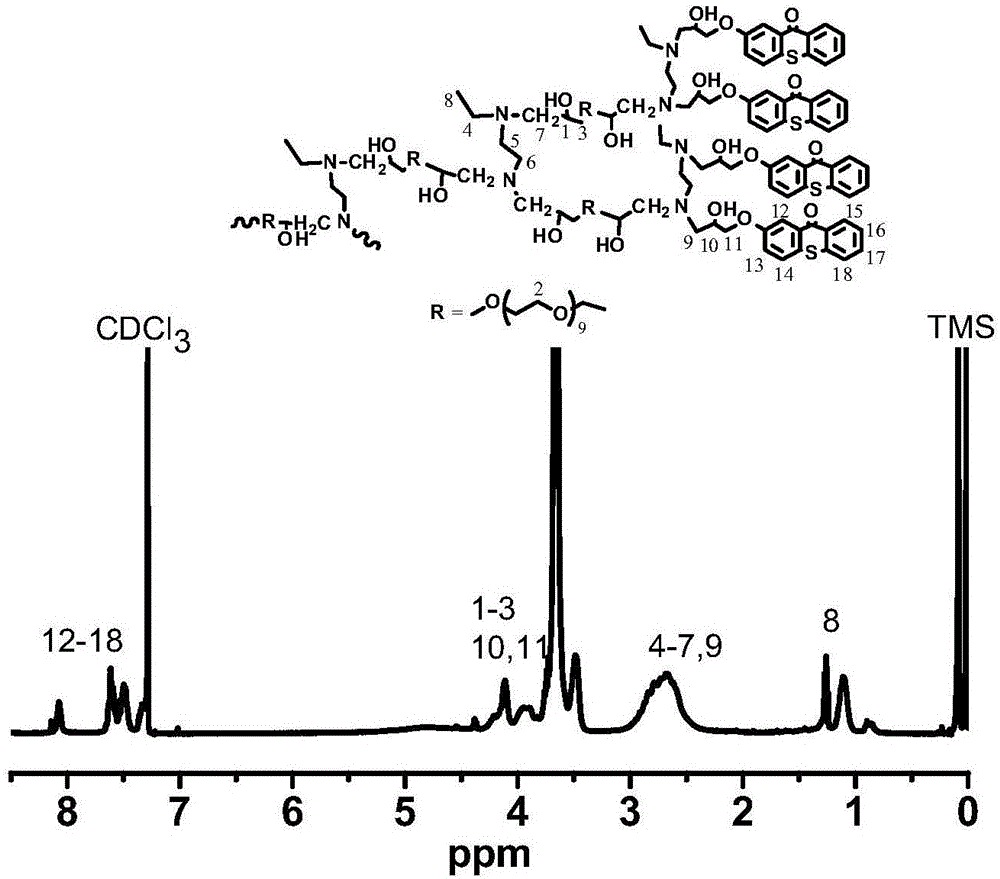
图2是实施例1所合成的基于超支化聚醚胺的两亲性高分子夺氢型光引发剂(hPEA101-TX)的结构图及其在氘代氯仿溶液中的核磁氢谱谱图。
图3是实施例2所合成的基于超支化聚醚胺的两亲性高分子夺氢型光引发剂(hPEA101-BP)的结构图及其在氘代氯仿溶液中的核磁氢谱谱图。
图4为实施例1合成的hPEA101-TX,实施例3合成的hPEA211-TX与相应的小分子光引发剂模型化合物MGA-TX和小分子共引发剂三乙醇胺(TEOA)以及商业性水性光引发剂2959引发水溶性单体丙烯酰胺(AM)的双键在紫外光照下里面随曝光时间的固化动力学谱图。
图5为实施例1合成的hPEA101-TX,实施例3合成的hPEA211-TX,实施例5合成的hPEA110-TX与相应的小分子光引发剂模型化合物MGA-TX和小分子共引发剂三乙醇胺(TEOA)以及商业性油性光引发剂ITX引发油溶性单体1,6-己二醇二丙烯酸酯(HDDA)的双键在紫外光照下里面随曝光时间的固化动力学谱图。
具体实施方式
下面,用实施例来进一步说明本发明内容,但本发明的保护范围并不受限制于实施例。对本领域的技术人员在不背离本发明精神和保护范围的情况下做出的其他的变化和修改,仍包括在本发明保护范围之内。
实施例1
(1)17.5g(0.035mol)聚乙二醇二缩水甘油醚(PEGDA)和3.1g(0.035mol)N-乙基乙二胺(NEED)溶解在乙醇中,加入到三口烧瓶中,在磁子搅拌,氮气保护下,冰水浴中混合2天,然后换为油浴80℃下反应24h,反应结束后将溶液旋蒸剩20mL,在正己烷中沉淀三次,于60℃恒温真空烘箱中干燥得到第一种超支化聚醚胺(hPEA101)。
(2)4.5g(7.7mmol)hPEA101和1.96g(6.9mmol)2-(2,3环氧丙氧基)硫杂蒽酮(ETX)溶解在乙醇中,加入到三口烧瓶中,在磁子搅拌,氮气保护下,在避光条件下油浴80℃下反应24h,反应结束后,将溶液旋蒸剩10mL,在正己烷中沉淀,于60℃恒温真空烘箱干燥得到超支化聚醚胺的两亲性硫杂蒽酮光引发剂(hPEA101-TX)。
图1是目标产物的结构图和核磁氢谱,图2是目标产物的红外谱图。1HNMR(CDCl3400MHz):8.66-7.29(芳香基),4.42-3.39(-OCH,-OCH2),2.66(-NH2),0.96-1.30(-CH3)。FT-IR(KBr):3448cm-1(O-H),2876cm-1(C-H),1646cm-1(C=O),1465cm-1(C-N)。
实施例2
(1)17.5g(0.035mol)聚乙二醇二缩水甘油醚和3.1g(0.035mol)N-乙基乙二胺溶解在乙醇中,加入到三口烧瓶中,在磁子搅拌,氮气保护下,冰水浴中混合2天,然后换为油浴80℃下反应24h,反应结束后将溶液旋蒸剩20mL,在正己烷中沉淀三次,于60℃恒温真空烘箱中干燥得到第一种超支化聚醚胺(hPEA101)。
(2)3.5g(6.0mmol)hPEA101和1.36g(5.4mmol)2-(2,3环氧丙氧基)二苯甲酮(EBP)溶解在乙醇中,加入到三口烧瓶中,在磁子搅拌,氮气保护下,在避光条件下油浴80℃下反应24h,反应结束后,将溶液旋蒸剩10mL,在正己烷中沉淀,于60℃恒温真空烘箱干燥得到超支化聚醚胺的两亲性二苯甲酮光引发剂(hPEA101-BP)。
图1是目标产物的结构图和核磁氢谱。1HNMR(CDCl3 400MHz):7.85-6.96(芳香基),4.20-3.38(-OCH,-OCH2),2.65(-NH2),0.98-1.89(-CH3)。FT-IR(KBr):3486cm-1(O-H),2847cm-1(C-H),1646cm-1(C=O),1455cm-1(C-N)。
实施例3
(1)20g(0.04mol)聚乙二醇二缩水甘油醚,6.96g(0.04mol)乙二醇二缩水甘油醚7.04g(0.08mol)N-乙基乙二胺溶解在乙醇中,加入到三口烧瓶中,在磁子搅拌,氮气保护下,冰水浴中混合2天,然后换为油浴80℃下反应24h,反应结束后将溶液旋蒸剩20mL,在正己烷中沉淀三次,于60℃恒温真空烘箱中干燥得到第二种超支化聚醚胺(hPEA211)。
(2)2.1g(5mmol)hPEA211和1.1g(4.5mmol)2-(2,3环氧丙氧基)硫杂蒽酮溶解在乙醇中,加入到三口烧瓶中,在磁子搅拌,氮气保护下,在避光条件下油浴80℃下反应24h,反应结束后,将溶液旋蒸剩10mL,在正己烷中沉淀,于60℃恒温真空烘箱干燥得到超支化聚醚胺的两亲性硫杂蒽酮光引发剂(hPEA211-TX)。
1HNMR(CDCl3 400MHz):8.68-7.28(芳香基),4.20-3.42(-OCH,-OCH2),2.64(-NH2),0.82-1.29(-CH3)。FT-IR(KBr):3439cm-1(O-H),2876cm-1(C-H),1646cm-1(C=O),1465cm-1(C-N)。
实施例4
(1)20g(0.04mol)聚乙二醇二缩水甘油醚,6.96g(0.04mol)乙二醇二缩水甘油醚7.04g(0.08mol)N-乙基乙二胺溶解在乙醇中,加入到三口烧瓶中,在磁子搅拌,氮气保护下,冰水浴中混合2天,然后换为油浴80℃下反应24h,反应结束后将溶液旋蒸剩20mL,在正己烷中沉淀三次,于60℃恒温真空烘箱中干燥得到第二种超支化聚醚胺(hPEA211)。
(2)4.0g(9.4mmol)hPEA211和2.2g(8.5mmol)2-(2,3环氧丙氧基)二苯甲酮(EBP)溶解在乙醇中,加入到三口烧瓶中,在磁子搅拌,氮气保护下,在避光条件下油浴80℃下反应24h,反应结束后,将溶液旋蒸剩10mL,在正己烷中沉淀,于60℃恒温真空烘箱干燥得到超支化聚醚胺的两亲性二苯甲酮光引发剂(hPEA211-BP)。
1HNMR(CDCl3 400MHz):6.92-7.86(芳香基),4.29-3.31(-OCH,-OCH2),2.64(-NH2),0.84-1.29(-CH3)。FT-IR(KBr):3448cm-1(O-H),2857cm-1(C-H),1656cm-1(C=O),1455cm-1(C-N)。
实施例5
(1)10.63g(0.06mol)乙二醇二缩水甘油醚和5.37g(0.06mol)N-乙基乙二胺溶解在乙醇中,加入到三口烧瓶中,在磁子搅拌,氮气保护下,冰水浴中混合2天,然后换为油浴80℃下反应24h,反应结束后将溶液旋蒸剩20mL,在正己烷中沉淀三次,于60℃恒温真空烘箱中干燥得到第三种超支化聚醚胺(hPEA110)。
(2)0.72g(2.5mmol)hPEA110和0.63g(2.2mmol)2-(2,3环氧丙氧基)硫杂蒽酮溶解在乙醇中,加入到三口烧瓶中,在磁子搅拌,氮气保护下,在避光条件下油浴80℃下反应24h,反应结束后,将溶液旋蒸剩10mL,在正己烷中沉淀,于60℃恒温真空烘箱干燥得到超支化聚醚胺的两亲性硫杂蒽酮光引发剂(hPEA110-TX)。
1HNMR(CDCl3 400MHz):8.69-7.28(芳香基),4.40-3.39(-OCH,-OCH2),2.69(-NH2),0.82-1.31(-CH3)。FT-IR(KBr):3458cm-1(O-H),2838cm-1(C-H),1646cm-1(C=O),1465cm-1(C-N)。
实施例6
(1)10.63g(0.06mol)乙二醇二缩水甘油醚和5.37g(0.06mol)N-乙基乙二胺溶解在乙醇中,加入到三口烧瓶中,在磁子搅拌,氮气保护下,冰水浴中混合2天,然后换为油浴80℃下反应24h,反应结束后将溶液旋蒸剩20mL,在正己烷中沉淀三次,于60℃恒温真空烘箱中干燥得到第三种超支化聚醚胺(hPEA110)。
(2)2.67g(10mmol)hPEA110和2.33g(9.2mmol)2-(2,3环氧丙氧基)二苯甲酮溶解在乙醇中,加入到三口烧瓶中,在磁子搅拌,氮气保护下,在避光条件下油浴80℃下反应24h,反应结束后,将溶液旋蒸剩10mL,在正己烷中沉淀,于60℃恒温真空烘箱干燥得到超支化聚醚胺的两亲性二苯甲酮光引发剂(hPEA110-BP)。
1HNMR(CDCl3 400MHz):7.88-6.95(芳香基),4.32-3.41(-OCH,-OCH2),2.69(-NH2),0.81-1.29(-CH3)。FT-IR(KBr):3467cm-1(O-H),2847cm-1(C-H),1646cm-1(C=O),1455cm-1(C-N)。
应用案例1
本发明的基于超支化聚醚胺的两亲性高分子夺氢型光引发剂可通过紫外光快速引发丙烯酰胺或其他烯烃类单体快速固化成型,而且与小分子光引发剂相比,其固化时间更短,转化率达到100%时,时间缩短140s,引发效率更高,最高引发速率提高了0.03s-1。与商业性水性光引发剂2959相比,体现出明显的优势,在40s时超支化聚醚胺的两亲性高分子夺氢型光引发剂比2959的双键转化率高50%,说明超支化聚醚胺的两亲性高分子夺氢型光引发剂在水溶剂中具有优异的引发效率。
图4是分别使用本发明的基于超支化聚醚胺的两亲性高分子夺氢型光引发剂与相应小分子光引发剂模型化合物以及商业水性光引发剂2959作为光引发剂在氮气氛围下引发水溶性单体丙烯酰胺的固化动力学谱图。具体说,图4为实施例1合成的hPEA101-TX,实施例3合成的hPEA211-TX与相应的小分子光引发剂模型化合物MGA-TX和小分子共引发剂TEOA以及商业水性光引发剂作为光引发剂在氮气氛围下引发丙烯酰胺的双键在紫外光照下里面随曝光时间的转化率谱图,测试方法如下所述:将一定量的光固化单体(丙烯酰胺)和光引发剂(hPEA101-TX,hPEA211-TX与相应的小分子光引发剂模型化合物MGA-TX和小分子共引发剂TEOA以及商业水性光引发剂2959)按照一定比例溶解在水中作为试样。称取2mg试样放入铝制坩埚中,参比物为空坩埚,试样与参比物在50ml/min的氮气保护下恒温紫外光照,固化反应放出热量随时间变化由计算机记录,由于固化反应放出热量与参加反应双键的量成正比,故通过积分放热曲线的峰面积得到固化反应的热量,从而求出双键转化率以及固化反应速率。单体中双键最终转化率代表着聚合反应完成的程度和光引发剂的引发效率,双键转化的速率代表着光引发剂引发聚合反应的快慢。
从图4中可以看出,超支化聚醚胺的两亲性高分子夺氢型光引发剂hPEA101-TX,hPEA211-TX引发的双键转化速率远大于小分子引发剂体系和商业水性引发剂2959的效果,在引发时间为40s时,hPEA101-TX,hPEA211-TX的转化率达到90%以上,而小分子引发体系为80%左右,2959为40%左右,并且高分子引发剂在40s时转化率达到在水溶液中引发单体时引发效率明显优于小分子光引发剂和商业水性光引发剂2959。主要原因在于本发明的基于超支化聚醚胺的两亲性高分子夺氢型光引发剂将光引发剂分子接枝在含有共引发剂胺的超支化聚醚胺链上既克服了传统小分子光引发剂易迁移、黄变、稳定性差、有残留等缺陷,又有利于两者之间的能量转移,从而更快更多地产生自由基活性种,提高了光引发效率。同时说明了基于超支化聚醚胺的两亲性高分子夺氢型光引发剂在水溶剂中具有优异的引发性能。
应用案例2
本发明的基于超支化聚醚胺的两亲性高分子夺氢型光引发剂可通过紫外光快速引发丙烯酸酯或其他烯烃类单体快速固化成型,而且与小分子光引发剂以及商业性油性光引发剂(ITX)相比,单体双键最终转化率提高10%-25%,即光引发剂的引发效率提高了10%~25%,说明超支化聚醚胺的两亲性高分子夺氢型光引发剂在油性溶剂中具有优异的引发效率。
图5是分别使用本发明的基于超支化聚醚胺的两亲性高分子夺氢型光引发剂与相应的小分子光引发剂模型化合物以及商业油性光引发剂ITX作为光引发剂在氮气氛围下引发油溶性单体1,6-己二醇二丙烯酸酯(HDDA)的固化动力学谱图。具体来说,图5为实施例1合成的hPEA101-TX,实施例3合成的hPEA211-TX,实施例5合成的hPEA110-TX与相应的小分子光引发剂模型化合物MGA-TX和小分子共引发剂TEOA以及商业油性光引发剂作为光引发剂在氮气氛围下引发HDDA的双键在紫外光照下里面随曝光时间的转化率谱图,测试方法如下所述:将一定量的光固化单体(丙烯酸酯)和光引发剂(hPEA101-TX,hPEA211-TX,hPEA110-TX与相应的小分子光引发剂模型化合物MGA-TX和小分子共引发剂TEOA以及商业油性光引发剂ITX)按照一定比例溶解在1,4-二氧六环中作为试样。称取2mg试样放入铝制坩埚中,参比物为空坩埚,试样与参比物在50ml/min的氮气保护下恒温紫外光照,固化反应放出热量随时间变化由计算机记录,由于固化反应放出热量与参加反应双键的量成正比,故通过积分放热曲线的峰面积得到固化反应的热量,从而求出双键转化率以及固化反应速率。单体中双键最终转化率代表着聚合反应完成的程度和光引发剂的引发效率,双键转化的速率代表着光引发剂引发聚合反应的快慢。
从图5中可以看出,超支化聚醚胺的两亲性高分子夺氢型光引发剂hPEA101-TX,hPEA211-TX,hPEA110-TX引发的双键转化速率远大于小分子引发剂体系和商业油性引发剂ITX的效果,单体最终转化率提高10%-25%(hPEA110-TX,hPEA211-TX,hPEA101-TX,MGA-TX/TEOA,ITX/TEOA引发单体最终转化率为100%,100%,87%,79%,75%)。这说明基于超支化聚醚胺的两亲性高分子夺氢型光引发剂在油性溶剂中引发效率高,引发速率快。主要原因在于本发明的基于俩亲性超支化聚醚胺高分子夺氢型光引发剂将光引发剂分子接枝在含有共引发剂胺的超支化聚醚胺链上既克服了传统小分子光引发剂易迁移、黄变、稳定性差、有残留等缺陷,又有利于两者之间的能量转移,从而更快更多地产生自由基活性种,提高了光引发效率。同时说明了基于超支化聚醚胺的两亲性高分子夺氢型光引发剂在油性溶剂中具有优异的引发性能。
- 还没有人留言评论。精彩留言会获得点赞!