高灵敏的乙型肝炎病毒核酸定量检测试剂盒的制作方法
本发明属于分子生物技术和基因检测领域,具体是一种新型高灵敏的乙型肝炎病毒核酸定量检测试剂盒。
背景技术:
据世界卫生组织报道,世界上有超过20亿人感染过乙肝病毒,其中有4亿人患有慢性乙型肝炎(HBV),HBV感染已成为最显著的公共健康问题。目前在中国,约有9300万人携带乙肝病毒,其中慢性乙肝患者约2000万例。HBV属于肝脱氧核糖核酸病毒科,在电子显微镜下显示为直径42nm的小圆颗粒,称为丹氏颗粒。丹氏颗粒由包膜和核心两部分组成,包膜含有表面蛋白、糖蛋白和细胞脂肪;核心含核心蛋白、HBV基因组DNA和HBV DNA多聚酶。HBV基因组为部分双链环状DNA,较长链通常含有3182个核苷酸而较短链含1700-2800个核苷酸。HBV全基因组DNA包含四个相互重叠的开放阅读框,编码四种具有特殊结构和功能的蛋白质。
HBV病毒侵入人体后,与宿主细胞上的特异性受体结合,脱去包膜,进入宿主细胞质内,脱去核衣壳,部分病毒基因组DNA进入并整合至宿主细胞核内,进一步反转录成mRNA进入宿主细胞质,,并在HBV DNA逆转录酶的作用下逆转录合成病毒负链DNA,负链DNA在HBV DNA聚合酶作用下合成正链DNA,这样就完成了HBV基因组DNA的复制,形成了子代的部分双链环状DNA;最后和相关蛋白装配成完整的病毒颗粒,释放至宿主细胞外,由此完成病毒粒子的复制。在基因复制过程中会自发地或由免疫诱导产生突变,突变会随着时间累积,因此相对于其他DNA病毒而言,HBV基因组变异程度更大。
目前,世界上主要存在8种HBV亚型,即HBV基因型A-H,不同基因型之间全基因组序列差异不少于8%或S基因差异不少于4%。在中国人群中出现的主要是A-D型HBV,其中以B、C、D型为主,A型较少见,且存在地区分布差异性。对于长期感染HBV的患者来说,若不加以干预,在慢性HBV患者几十年的发展历程中,有15%-40%的患者会发展成为肝硬化、晚期肝脏疾病、肝细胞癌或需要进行肝脏移植。在输血过程产生的漏检也是HBV感染的重要途径,因此,乙肝病毒的检测对于乙肝病毒感染的预防、诊断和治疗具有举足轻重的关键作用。
HBV病毒核酸遗传基因序列中的主要有四个开放阅读框(ORF),分别称为S(ORF S)、C(ORF Core)、P(ORF P)及X(ORF X),能编码全部已知的HBV蛋白质。S区可分为S基因和前S基因,其中S基因能编码主要表面蛋白,前S基因能编码PreS1和PreS2蛋白。C区基因包括:前C基因,编码e抗原(HBeAg);C基因,编码核心抗原(HBcAg)。其中S基因和C基因是保守型较高的序列区域,因此在检测中常以此序列为目标进行检测,已达到覆盖不同分型的目的。
本方法中分别针对乙型肝炎病毒核酸的S基因和C基因的两段保守序列作为靶序列,并通过引入内定量参考品(QS),无需制备标曲即可实现样本的准确定量,可实现对HBV DNA的高灵敏实时荧光定量检测,不仅避免了实际临床样本中由于S基因或者C基因的丢失造成的假阴性结果,还能够通过高度一致内定量参考品(QS)对检测样本进行定量,无需外对照,避免了检测反应管间的差异,使整个检测过程更加便捷。目前尚无一种方式采用该方式完成乙型肝炎病毒核酸高灵敏定量检测。
技术实现要素:
基于此,本发明的目的之一为提供一种更为简单、更有保证的高灵敏乙型肝炎病毒核酸荧光定量PCR检测试剂盒,以实现避免实际临床样本中由于S基因和/或者C基因的丢失造成的假阴性结果。
实现上述目的的技术方案如下。
一种乙型肝炎病毒核酸荧光定量PCR检测试剂盒,包括有针对S基因的引物和探针,所述引物为SEQ ID NO.1和SEQ ID NO.2,所述探针为SEQ ID NO.5,SEQ ID NO.7,SEQ ID NO.8,SEQ ID NO.9,和SEQ ID NO.11,其中,碱基组成如SEQ ID NO.7,SEQ ID NO.8或其反向互补序列所示探针的末端标记有荧光。
一种乙型肝炎病毒核酸荧光定量PCR检测试剂盒,包括有针对C基因的引物和探针,所述引物为SEQ ID NO.3和SEQ ID NO.4,所述探针为SEQ ID NO.6,SEQ ID NO.7,SEQ ID NO.8,SEQ ID NO.10,和SEQ ID NO.12,其中,碱基组成如SEQ ID NO.7和SEQ ID NO.8,或其反向互补序列所示探针的末端标记有荧光。
一种乙型肝炎病毒核酸荧光定量PCR检测试剂盒,包括有针对S和C基因的引物和探针,所述引物为:SEQ ID NO.1和SEQ ID NO.2,SEQ ID NO.3和SEQ ID NO.4;所述探针为SEQ ID NO.5至SEQ ID NO.12,或分别为SEQ ID NO.5至SEQ ID NO.10的反向互补序列;其中,碱基组成如SEQ ID NO.7,SEQ ID NO.8,或其反向互补序列所示探针的末端标记有荧光。
在其中一个实施例中,还包括有内定量参考品,优选地,所述内定量参考品的碱基组成如SEQ ID NO.13所示。有该定量参考品(外对照),可实现不需要标准曲线就能对临床样本实现定量检测。
本发明新型高灵敏的乙型肝炎病毒核酸定量检测试剂盒,分别针对乙型肝炎病毒核酸的S基因和C基因的两段保守序列作为靶序列,并通过引入内定量参考品(QS),无需制备标曲即可实现样本的准确定量,可实现对HBV DNA的高灵敏实时荧光定量检测。
优先地,所述内定量参考品(QS)是人为设计合成的质粒,针对HBV基因组中S基因和C基因上的两段保守序列分别设计相应的QS序列,使QS序列与靶标序列仅有一个碱基差异,保证了QS扩增效率与靶序列高度一致,因此保证了定量的准确性。所选靶序列同时包含了乙型肝炎病毒核酸的S基因和C基因的两段保守序列,避免了实际临床样本中由于S基因或者C基因的丢失造成的假阴性结果。
本发明利用了PCR扩增和核酸侵入反应的结合方法,用于高灵敏定量检测HBV核酸分子。该方法的具体原理是:通过设计一对PCR引物对目标模板进行扩增,并针对扩增产物设计一对上下游探针,它们可与模板退火杂交,形成一个单碱基重叠侵入结构,该结构可被Afu酶特异性识别,从而切割下游探针与模板互补的第一碱基的化学键,产生信号分子。由于设计的下游探针与模板结合部分的Tm值接近反应温度,新的完整的下游探针会再次与模板退火,形成新一轮的切割,从而实现信号分子的扩增。产生的信号分子可以与相应的标记有荧光基团和淬灭基团的荧光探针结合,再次形成核酸侵入结构,被Afu酶识别并切割,将荧光基团与淬灭基团分离,产生荧光信号。同样,游离出来的信号分子可再次与荧光探针杂交从而产生切割,实现荧光信号的放大。如此实现对目标物的检测。
分别通过检测乙型肝炎病毒核酸的S基因和C基因的两段保守序列,并采用内定量参考品(QS)实现样本的准确定量,从而实现对HBV DNA的高灵敏实时荧光定量检测。这一方式不仅避免了实际临床样本中由于S基因或者C基因的丢失造成的假阴性结果,还避免了检测反应管间的差异,使整个检测过程更加便捷。
本发明具有以下有益效果:
本发明中的新型高灵敏的乙型肝炎病毒核酸定量检测试剂盒建立了基于S基因和C基因的HBV定量检测HBV核酸的方法,避免了临床样本因个别基因特征缺失导致的假阴性结果。
采用本发明中的新型高灵敏的乙型肝炎病毒核酸定量检测试剂盒对HBV基因组DNA分子进行检测,具有很高的定量范围,可定量检测低至10拷贝/管反应的HBV DNA。
本发明中的新型高灵敏的乙型肝炎病毒核酸定量检测试剂盒引入了QS内标体系,不仅能够质控样本和试剂的有效性,还能够作为定量参考品定量待测样本的拷贝数,无需另外做定量标准曲线。
利用本发明中的新型高灵敏的乙型肝炎病毒核酸定量检测试剂盒可实现短时间高灵敏度的闭管核酸检测,能够有效的避免扩增产物的交叉污染。
附图说明
下列附图用于说明本发明的具体实施方案,不用于限定有权利要求所界定的本发明范围。
图1是实施例1中乙型肝炎病毒核酸定量检测试剂盒原理示意图。
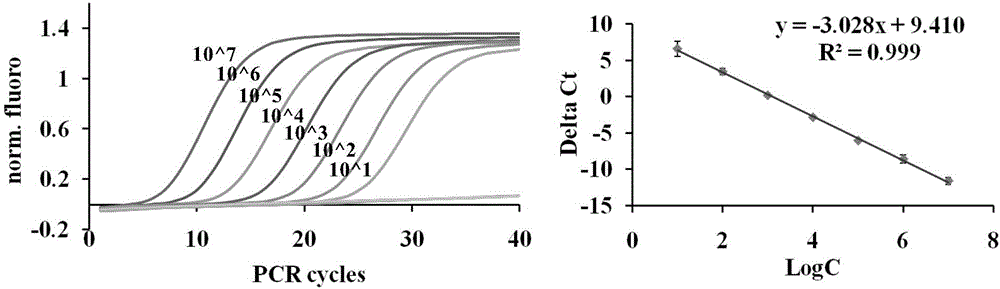
图2是实施例2中新型高灵敏的乙型肝炎病毒核酸定量检测试剂盒的灵敏度。
图3是实施例3中乙型肝炎病毒核酸定量检测试剂盒的模拟样本检测结果。
图4是实施例6中乙型肝炎病毒核酸定量检测试剂盒的单体系验证结果。
具体实施方式
除非另有定义,本发明所使用的所有的技术和科学术语与属于本发明的技术领域的技术人员通常理解的含义相同。本发明的说明书中所使用的术语只是为了描述具体的实施例的目的,不用于限制本发明。本发明所使用的术语“和/或”包括一个或多个相关的所列项目的任意的和所有的组合。
下列实施例中未注明具体条件的实验方法,通常按照常规条件,例如Sambrook等人,分子克隆:实验室手册(New York:Cold Spring Harbor Laboratory Press,1989)中所述的条件,或按照制造厂商所建议的条件。实施例中所用到的各种常用化学试剂,均为市售产品。
为了便于理解本发明,下面将参照相关附图对本发明进行更全面的描述。附图中给出了本发明的较佳实施例。但是,本发明可以以许多不同的形式来实现,并不限于本文所描述的实施例。相反地,提供这些实施例的目的是使对本发明的公开内容的理解更加透彻全面。
实施例1新型高灵敏的乙型肝炎病毒核酸定量检测试剂盒
建立一种PCR结合级联核酸侵入反应的方法进行HBV DNA的实时定量检测,原理如图1所示。通过设计一对PCR引物对目标模板进行扩增,并针对扩增产物设计一对上下游探针,它们可与模板退火杂交,形成一个单碱基重叠侵入结构,该结构可被内切酶特异性识别,从而切割探针、产生信号分子而被荧光PCR仪器所检测。
采用加入内定量参考品(QS)进行HBV DNA的定量检测。QS是人工设计合成的质粒模板,含有与HBV目标DNA序列完全相同的PCR引物和上游探针结合区域及一个特异的探针结合区域,探针结合区域可用于HBV DNA和QS扩增子的区分。通过设计两种不同的信号分子探针,检测PCR每个循环中的荧光信号分别实现对HBV DNA和QS的实时检测。
所述新型高灵敏的乙型肝炎病毒核酸定量检测试剂盒,包含4条引物、6条探针、反应液、酶液。
引物、探针和纳米金探针序列如引物1-引物4、探针1-探针6,或为上述序列的互补序列:
引物1:CTG GAT GTG TCT GCG GCG;SEQ ID NO.1
引物2:TAG AGG ACA AAC GGG CAA CAT;SEQ ID NO.2
引物3:TGG TCT GYK YAC CAK CAY CAT;SEQ ID NO.3
引物4:AGC CAY CCA AGG CAC AGC;SEQ ID NO.4
探针1:CT GCT ATG CCT CAT;SEQ ID NO.5
探针2:GAG GCT TGA ACA GTR GGA;SEQ ID NO.6
探针3:FAM-ACG GAC GCG GAG TCT TGT TGG TTC-BHQ;SEQ ID NO.7
探针4:VIC-ACG GAC GCG GAG TGA TTA GGC AGA-BHQ;SEQ ID NO.8
探针5:ACG GAC GCG GAG TCT TGT TGG TTC TTC;SEQ ID NO.9
探针6:ACG GAC GCG GAG TG ATT ACG GAG;SEQ ID NO.10
探针7:CGC GCC GAG GAC TTC TTG GTT GTT C;SEQ ID NO.11
探针8:CGC GCC GAG GAG ATT ACG GAG;SEQ ID NO.12
QS模板:CTG GAT GTG TCT GCG GCG TTT TAT CAT CTT CCT CTT CAT CCT GCT GCT ATG CCT CAT CTA CTT CTT GGT TGT TCT GGA CTA TCA AGG TAT GTT GCC CGT TTG TCC TCT AGG AGG CTG TAG GCA TAA ATT GGT CTG TTC ACC AGC AGC ATG CAA CTT TTT CAC CTC TCC GTA ATC TTC TCT TGT TCA TGT CCT ACT GTT CAA GCC TCC AAG CTG TGC CTT GGG TGG CTT TG SEQ ID NO.13
注:混合碱基Y表示C+T,K表示G+T
实施例2新型高灵敏的乙型肝炎病毒核酸定量检测试剂盒的灵敏度
本实施例应用所述的新型高灵敏的乙型肝炎病毒核酸定量检测试剂盒检测了不同浓度的HBV DNA模板,用来验证本发明所述的检测方法的灵敏度。
反应条件:
20μL扩增体系包括:2μL 10×buffer,250μmol/L dNTP,500nmol/L PCR上下游引物(SEQ ID NO.1至SEQ ID NO.4),250nmol/L探针(SEQ ID NO.5至SEQ ID NO.12),1U Taq DNA聚合酶,8U Afu酶,1μL模板(模板浓度分别为:107、106、105、104、103、102、10以及1拷贝/μL)和1μL QS模板(103拷贝/μL),加水补充至40μL。扩增反应程序:95℃,3min;95℃20s,67℃,30s,70℃,20s,预扩增5个循环;95℃,20s,63℃,1min,70℃,20s,扩增40个循环,每个循环结束读一次荧光信号。
结果示于图2中,结果显示新型高灵敏的乙型肝炎病毒核酸定量检测试剂盒能够定量检测低至10拷贝的HBV DNA分子。
实施例3新型高灵敏的乙型肝炎病毒核酸定量检测试剂盒的模拟样本检测
本实施例应用所述的新型高灵敏的乙型肝炎病毒核酸定量检测试剂盒检测了混合于人血清样本中的不同浓度HBV DNA模板(卫生部临检中心标准品样本),用来验证本发明所述的检测方法在检测模拟样本时情况。
反应条件:
20μL扩增体系包括:2μL 10×buffer,250μmol/L dNTP,500nmol/L PCR上下游引物(SEQ ID NO.1至SEQ ID NO.4),250nmol/L探针(SEQ ID NO.5至SEQ ID NO.12),1U Taq DNA聚合酶,8U Afu酶,1μL人血清样本(标准品样本)提取的基因组DNA模板(模板浓度分别为:105、104、103、102、40以及20IU/mL)和1μL QS模板(103拷贝/μL),加水补充至40μL。扩增反应程序:95℃,3min;95℃20s,67℃,30s,70℃,20s,预扩增5个循环;95℃,20s,63℃,1min,70℃,20s,扩增40个循环,每个循环结束读一次荧光信号。
结果示于图3中,结果显示新型高灵敏的乙型肝炎病毒核酸定量检测试剂盒能够定量检测低至40IU/mL的HBV DNA分子。
实施例4新型高灵敏的乙型肝炎病毒核酸定量检测试剂盒的检测限
本实施例应用所述的新型高灵敏的乙型肝炎病毒核酸定量检测试剂盒检测了混合于人血清样本中的不同浓度HBV DNA模板(标准品样本),用来验证本发明所述的检测方法的检测限。
反应条件:
20μL扩增体系包括:2μL 10×buffer,250μmol/L dNTP,500nmol/L PCR上下游引物(SEQ ID NO.1至SEQ ID NO.4),250nmol/L探针(SEQ ID NO.5至SEQ ID NO.12),1U Taq DNA聚合酶,8U Afu酶,1μL人血清样本(标准品样本)提取的基因组DNA模板(模板浓度分别为:40IU/mL、30IU/mL、20IU/mL以及10IU/mL 4个浓度,分别检测5次)和1μL QS模板(103拷贝/μL),加水补充至40μL。扩增反应程序:95℃,3min;95℃20s,67℃,30s,70℃,20s,预扩增5个循环;95℃,20s,63℃,1min,70℃,20s,扩增40个循环,每个循环结束读一次荧光信号。
结果示于表1中,结果显示新型高灵敏的乙型肝炎病毒核酸定量检测试剂盒能够检测低至10IU/mL的HBV DNA分子。
表1
实施例5新型高灵敏的乙型肝炎病毒核酸定量检测试剂盒的精密度
本实施例应用所述的新型高灵敏的乙型肝炎病毒核酸定量检测试剂盒检测了混合于人血清样本中的不同浓度HBV DNA模板(标准品样本),用来验证本发明所述的检测方法的精密度。
反应条件:
20μL扩增体系包括:2μL 10×buffer,250μmol/L dNTP,500nmol/L PCR上下游引物(SEQ ID NO.1至SEQ ID NO.4),250nmol/L探针(SEQ ID NO.5至SEQ ID NO.12),1U Taq DNA聚合酶,8U Afu酶,1μL人血清样本(标准品样本)提取的基因组DNA模板(模板浓度分别为:2×104IU/mL、2×103IU/mL和2×102IU/mL,每个浓度检测20次,分别检测4批)和1μL QS模板(103拷贝/μL),加水补充至40μL。扩增反应程序:95℃,3min;95℃20s,67℃,30s,70℃,20s,预扩增5个循环;95℃,20s,63℃,1min,70℃,20s,扩增40个循环,每个循环结束读一次荧光信号。
结果示于表2-表3中,结果显示新型高灵敏的乙型肝炎病毒核酸定量检测试剂盒的精密度较为理想,各浓度批内重复性变异系数5.6%-34.6%,批间重复性变异系数为26.0%-35.7%;批内重复性对数标准差为0.03-0.13,批间重复性对数标准差为0.10-0.15;批内重复性对数变异系数为0.64%-4.2%,批间重复性对数变异系数为2.5%-5.2%。
表2
表3
实施例6
本实施例应用所述的检测方法单独扩增S基因体系或者C基因体系,以证实S和C基因体系的优势。
反应条件:
20μL扩增体系包括:2μL 10×buffer,250μmol/L dNTP,500nmol/L PCR上下游引物(SEQ ID NO.1和SEQ ID NO.2或SEQ ID NO.3和SEQ ID NO.4),250nmol/L探针(SEQ ID NO.5、SEQ ID NO.7、SEQ ID NO.8、SEQ ID NO.9和SEQ ID NO.11或SEQ ID NO.6、SEQ ID NO.7、SEQ ID NO.8、SEQ ID NO.10和SEQ ID NO.12),1U Taq DNA聚合酶,8U Afu酶,1μL人血清样本(标准品样本)提取的基因组DNA模板(2×103IU/mL和20IU/mL)和1μL QS模板(103拷贝/μL),加水补充至40μL。扩增反应程序:95℃,3min;95℃20s,67℃,30s,70℃,20s,预扩增5个循环;95℃,20s,63℃,1min,70℃,20s,扩增40个循环,每个循环结束读一次荧光信号,与双体系进行比较。
结果如图4所示,根据结果,单独S体系或者C体系检测的Ct值较S+C双体系检测Ct值高,说明双体系检测结果优于S体系或者C体系检测结果。
实施例7
本实施例应用所述的检测方法检测实际样本验证定量的准确性。
反应条件:
20μL扩增体系包括:2μL 10×buffer,250μmol/L dNTP,500nmol/L PCR上下游引物(SEQ ID NO.1-SEQ ID NO.4),250nmol/L探针(SEQ ID NO.5-SEQ ID NO.12),1U Taq DNA聚合酶,8U Afu酶,1μL人血清样本提取的基因组DNA模板,加水补充至40μL。扩增反应程序:95℃,3min;95℃20s,67℃,30s,70℃,20s,预扩增5个循环;95℃,20s,63℃,1min,70℃,20s,扩增40个循环,每个循环结束读一次荧光信号,与双体系进行比较。
结果如表4所示,根据结果,对于三个真实浓度分别为2×104IU/mL、2×103IU/mL和2×102IU/mL模板,定量值均符合预期,这说明本试剂盒通过QS内定量可以实现样本的准确定量。
表4
以上所述实施例的各技术特征可以进行任意的组合,为使描述简洁,未对上述实施例中的各个技术特征所有可能的组合都进行描述,然而,只要这些技术特征的组合不存在矛盾,都应当认为是本说明书记载的范围。
以上所述实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。
SEQUENCE LISTING
<110> 广州市宝创生物技术有限公司
<120> 高灵敏的乙型肝炎病毒核酸定量检测试剂盒
<160> 13
<170> PatentIn version 3.3
<210> 1
<211> 18
<212> DNA
<213> 人工序列
<400> 1
ctggatgtgt ctgcggcg 18
<210> 2
<211> 21
<212> DNA
<213> 人工序列
<400> 2
tagaggacaa acgggcaaca t 21
<210> 3
<211> 21
<212> DNA
<213> 人工序列
<400> 3
tggtctgyky accakcayca t 21
<210> 4
<211> 18
<212> DNA
<213> 人工序列
<400> 4
agccayccaa ggcacagc 18
<210> 5
<211> 14
<212> DNA
<213> 人工序列
<400> 5
ctgctatgcc tcat 14
<210> 6
<211> 18
<212> DNA
<213> 人工序列
<400> 6
gaggcttgaa cagtrgga 18
<210> 7
<211> 24
<212> DNA
<213> 人工序列
<400> 7
acggacgcgg agtcttgttg gttc 24
<210> 8
<211> 24
<212> DNA
<213> 人工序列
<400> 8
acggacgcgg agtgattagg caga 24
<210> 9
<211> 27
<212> DNA
<213> 人工序列
<400> 9
acggacgcgg agtcttgttg gttcttc 27
<210> 10
<211> 23
<212> DNA
<213> 人工序列
<400> 10
acggacgcgg agtgattacg gag 23
<210> 11
<211> 25
<212> DNA
<213> 人工序列
<400> 11
cgcgccgagg acttcttggt tgttc 25
<210> 12
<211> 21
<212> DNA
<213> 人工序列
<400> 12
cgcgccgagg agattacgga g 21
<210> 13
<211> 230
<212> DNA
<213> 人工序列
<400> 13
ctggatgtgt ctgcggcgtt ttatcatctt cctcttcatc ctgctgctat gcctcatcta 60
cttcttggtt gttctggact atcaaggtat gttgcccgtt tgtcctctag gaggctgtag 120
gcataaattg gtctgttcac cagcagcatg caactttttc acctctccgt aatcttctct 180
tgttcatgtc ctactgttca agcctccaag ctgtgccttg ggtggctttg 230
- 还没有人留言评论。精彩留言会获得点赞!