多重PCR引物、试剂盒及用途的制作方法
本申请是申请日为2015年11月4日,名称为“一种基于下一代测序技术检测EGFR/KRAS/BRAF基因突变位点的多重PCR引物和方法及应用”的中国专利申请201510740906.1的分案。
技术领域:
本发明属于分子生物学领域,特别是涉及一种基于下一代测序技术检测EGFR、KRAS和/或BRAF基因突变位点的多重PCR引物和方法及应用。
背景技术:
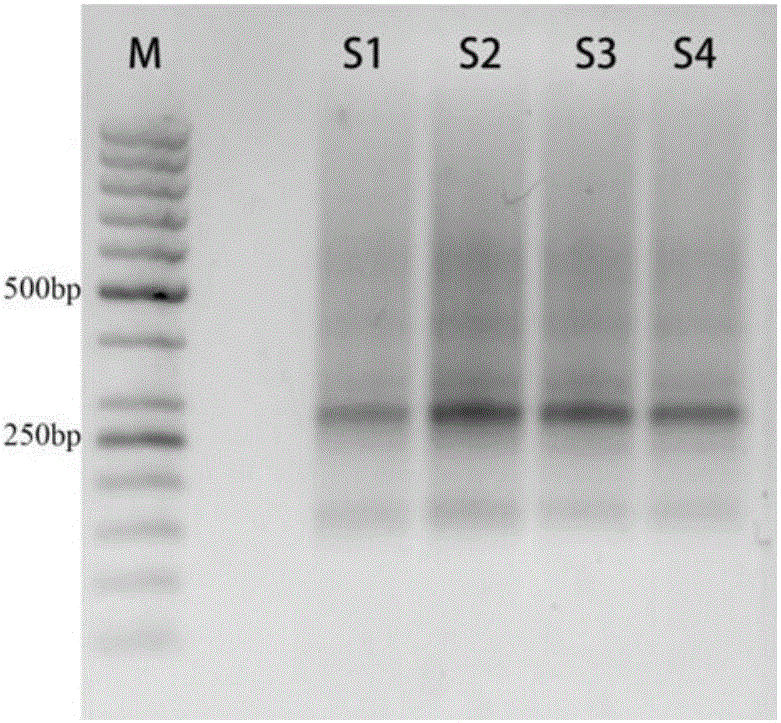
:表皮生长因子受体(epidermalgrowthfactorreceptor,EGFR)是位于7号染色体短臂上的原癌基因C-erbB-1(HER-1)的表达产物,是表皮生长因子受体家族(HER)中的4个成员之一,HER家族在细胞生理过程中发挥重要的调节作用。EGFR酪氨酸激酶区域的突变主要发生在18~21号外显子,其中19和21号外显子突变占总突变的90%。EGFR信号传导的异常是导致多种肿瘤发生的原因。研究表明,EGFR在多种肿瘤中都有表达,如结直肠癌、乳腺癌、胰腺癌、前列腺癌和非小细胞肺癌等。K-ras基因是一种原癌基因,长约35kb,位于12号染色体短臂上,是ras基因家族成员之一,编码KRAS蛋白。K-ras基因常见的突变位点位于2号外显子的12号密码子和13号密码子上、3号外显子的6l号密码子,其中有7个突变热点:G12C、G12R、G12S、G12V、G12D、G12A、G13V/D,占K-ras基因总突变的98%以上。研究表明体细胞K-ras基因突变与多种人类恶性肿瘤,如肺癌、白血病、黏蛋白腺癌、胰腺癌、结直肠癌有关,而生殖细胞K-ras基因突变与努南综合征和心脏-面部-皮肤(cardio-facio-cutaneous,CFC)综合征相关。BRAF基因是一种原癌基因,定位于7号染色体上,编码丝/苏氨酸特异性激酶。约90%的BRAF基因突变发生在外显子15的1799位核苷酸上,T突变为A,导致缬氨酸被谷氨酸取代(V600E)。BRAF基因突变在黑色素瘤、结直肠癌、神经胶质瘤、肉瘤、卵巢癌、乳腺癌以及肺癌等肿瘤细胞系中的发生率依次为59%、18%、11%、9%、14%、2%、3%;此外,BRAFV600E在甲状腺乳头状癌中的发生率高达35.8%。BRAF基因突变是晚期及复发性结直肠癌最重要的预后指标之一,与患者较差的总体生存期密切相关。目前常见的检测这三个基因突变的方法有Sanger测序法和荧光定量PCR法。Sanger测序法中,单对引物可检测多个突变,但对多个基因、或同一基因的不同外显子上的突变位点就需分别进行扩增测序,操作繁琐,并且灵敏度较低约20%,假阴性率较高。荧光定量PCR法虽然灵敏度高,但每对引物只能检测一种突变,且每种突变需单独建立一个PCR反应体系,同时检测多个样本多个突变位点操作繁琐。这两种方法对样本的需要量都较大,不适合同时检测多个基因突变位点。技术实现要素:鉴于此,本发明提供了一种多重PCR引物及应用。第一方面,本发明提供了一种多重PCR引物。该多重PCR引物由以下引物对组成:SEQIDNO:3和SEQIDNO:4所示引物对,SEQIDNO:7和SEQIDNO:8所示引物对,SEQIDNO:11和SEQIDNO:12所示引物对,SEQIDNO:17和SEQIDNO:18所示引物对,SEQIDNO:23和SEQIDNO:24所示引物对,以及SEQIDNO:27和SEQIDNO:28所示引物对。发明人基于目标序列特点多次设计,以及多次组合试验筛选,确定了这一组多重PCR引物,利用该多重PCR引物,能够一次性高效检测EGFR/KRAS/BRAF基因突变位点,可同时覆盖EGFR18~21号外显子、KRAS2号外显子和BRAF15号外显子。其中的SEQIDNO:3和SEQIDNO:4引物对能够在同一反应体系中不受其它引物对影响地实现EGFR基因的外显子18的区域的扩增,SEQIDNO:7和SEQIDNO:8引物对能够在同一反应体系中不受其它引物对影响地实现扩增EGFR基因的外显子19的区域,SEQIDNO:11和SEQIDNO:12引物对能够在同一反应体系中不受其它引物对影响地实现扩增EGFR基因的外显子20的区域,SEQIDNO:17和SEQIDNO:18引物对能够在同一反应体系中不受其它引物对影响地实现扩增EGFR基因的外显子21的区域,SEQIDNO:23和SEQIDNO:24引物对能够在同一反应体系中不受其它引物对影响地实现扩增KRAS基因的外显子2的区域,SEQIDNO:27和SEQIDNO:28引物对能够在同一反应体系中不受其它引物对影响地实现扩增BRAF基因的外显子15的区域。根据本发明的实施例,上述多重PCR引物还可以进一步包括如下附加技术特征至少之一:根据本发明的实施例,该多重PCR引物还包括以下引物对中的至少一对:SEQIDNO:1和SEQIDNO:2所示引物对,SEQIDNO:5和SEQIDNO:6所示引物对,SEQIDNO:9和SEQIDNO:10所示引物对,SEQIDNO:13和SEQIDNO:14所示引物对,SEQIDNO:15和SEQIDNO:16所示引物对,SEQIDNO:19和SEQIDNO:20所示引物对,SEQIDNO:21和SEQIDNO:22所示引物对,以及SEQIDNO:25和SEQIDNO:26所示引物对。其中,SEQIDNO:1和SEQIDNO:2引物对能够在同一反应体系中不受其它引物对影响地实现EGFR基因的外显子18的区域的扩增,SEQIDNO:5和SEQIDNO:6引物对能够在同一反应体系中不受其它引物对影响地实现扩增EGFR基因的外显子19的区域,SEQIDNO:9和SEQIDNO:10引物对以及SEQIDNO:13和SEQIDNO:14引物对能够在同一反应体系中不受其它引物对影响地实现扩增EGFR基因的外显子20的区域,SEQIDNO:17和SEQIDNO:18引物对以及SEQIDNO:19和SEQIDNO:20引物对能够在同一反应体系中不受其它引物对影响地实现扩增EGFR基因的外显子21的区域,SEQIDNO:21和SEQIDNO:22引物对能够在同一反应体系中不受其它引物对影响地实现扩增KRAS基因的外显子2的区域,SEQIDNO:25和SEQIDNO:26引物对能够在同一反应体系中不受其它引物对影响地实现BRAF基因的外显子15的区域的扩增。根据本发明的实施例,所述多重PCR引物中,至少包括扩增EGFR、KRAS和BRAF基因中任意两个基因的引物对,所述引物对能够用于扩增所述基因的至少一个外显子区域。本领域技术人员可以理解,若多次设计摸索以及多次试验筛选确定的多重PCR引物组能够在同一反应体系中、同时互不干扰地实现目标片段的扩增,其中的任一部分引物组合也能于同一反应体系中发挥各自的功能,即互不影响地同时实现相应目标区域的扩增。根据本发明的实施例,所述多重PCR引物为SEQIDNO:1~SEQIDNO:28所示的核苷酸序列组成的引物组。本领域技术人员可以理解,若多次设计摸索以及多次试验筛选确定的多重PCR引物组(比如,SEQIDNO:1~SEQIDNO:28所示的核苷酸序列组成的引物组)获得了较佳的扩增效果,一般情况下,设计引物的时候,适当的将多重PCR引物组中任一一条引物的长度延长或截短0~3个碱基,也可以获得不错的多重PCR扩增效果,也应纳入本发明保护范围。第二方面,本发明提供了前面本发明一方面或者任一实施例中的多重PCR引物在获得和/或检测EGFR、KRAS和/或BRAF基因序列中的用途。上述对本发明一方面或者任一实施例中的多重PCR引物的技术特征和效果的描述,同样适用本发明这一方面的用途,在此不再赘述。第三方面,本发明提供了一种试剂盒。该试剂盒包含前面本发明一方面或者任一实施例中的多重PCR引物。上述对本发明一方面或者任一实施例中的多重PCR引物的技术特征和效果的描述,同样适用本发明这一方面的试剂盒,在此不再赘述。第四方面,本发明提供了前面任一实施例中的试剂盒在获得和/或检测EGFR、KRAS和/或BRAF基因序列中的用途。第五方面,本发明提供了一种扩增基因序列目标区域的方法。根据本发明的实施例,所述方法包括利用前面所述的多重PCR引物进行所述扩增。根据本发明的实施例,上述方法还可以进一步包括如下附加技术特征至少之一:根据本发明的具体实施例,所述多重PCR反应的体系中,各引物等摩尔混合。根据本发明的再一具体实施例,所述多重PCR反应的体系中,模板量为50ng~1μg/50μl体系。根据本发明的再一具体实施例,所述多重PCR反应的程序为:上述程序具体为:95℃预变性15min,95℃变性15s,60℃退火2min,72℃延伸3min,循环30~40次(优选为35次),最后72℃后延伸10min。根据本发明的具体示例,所述多重PCR反应结束后,电泳,割胶回收片段长度为150bp的DNA片段。第六方面,本发明提供了一种EGFR、KRAS和/或BRAF基因检测的方法。根据本发明的实施例,所述方法包括:(1)利用前面所述的方法对待样品中的至少一部分核酸进行扩增,获得扩增产物;(2)分析所述扩增产物,以获得EGFR、KRAS和/或BRAF基因检测结果。根据本发明的实施例,上述EGFR、KRAS和/或BRAF基因检测的方法还可以进一步包括如下附加技术特征至少之一:根据本发明的实施例,所述核酸为DNA和/或RNA。根据本发明的实施例,所述RNA为(优选采用RNA试剂盒)提取人外周血单个核细胞获得的总RNA。根据本发明的实施例,所述核酸为RNA,步骤(1)包括:(1-1)利用所述多重PCR引物中的上游或下游引物将所述RNA反转录为cDNA;以及(1-2)利用所述多重PCR引物中相应的下游或上游引物对所述cDNA进行扩增,获得扩增产物。根据本发明的具体实施例,当所述核酸为RNA,步骤(1)包括:先以下游引物组为反转录引物合成cDNA;然后以合成的cDNA为模板,加入上游引物组,进行多重PCR,扩增cDNA,获得多重PCR产物。根据本发明的再一具体实施例,当所述核酸为RNA,步骤(1)包括:先以上游引物组为反转录引物合成cDNA;然后以合成的cDNA为模板,加入下游引物组,进行多重PCR,扩增cDNA,获得多重PCR产物。根据本发明的实施例,步骤(2)包括:(2-1)对所述扩增产物进行测序;以及(2-2)将测序结果分别与EFGR、KRAS和/或BRAF基因野生型序列比对,以确定EFGR、KRAS和/或BRAF基因突变位点。如本发明所述的,所述“EGFR、KRAS和/或BRAF基因突变位点”或“EGFR/KRAS/BRAF基因突变位点”表示EGFR、KRAS、BRAF三个基因中的一个或多个。第八方面,本发明提出了一种检测癌症的方法,根据本发明的实施例,所述方法包括:利用前面所述的EGFR、KRAS和/或BRAF基因检测的方法进行EFGR、KRAS和/或BRAF基因检测,获得检测结果,所述待测样品来自受检者;以及依据检测结果,评估受检者的患癌风险。根据本发明的实施例,上述检测癌症的方法还可以进一步包括如下附加技术特征至少之一:根据本发明的实施例,所述检测结果包含以下突变中的至少之一:EGFRc.2156G>A、EGFRc.2235_2249del15、EGFRc.2240_2257del18、EGFRc.2369C>T、EGFRc.2573T>G、EGFRc.2582T>A、EGFRc.34G>T、KRASc.34G>T、KRASc.34G>A、KRASc.34G>C、KRASc.35G>T、KRASc.35G>A、KRASc.35G>C、KRASc.38G>A和BRAFc.1799T>A,则指示受检者患有癌症。上述突变是根据HGVS等命名法标注该位点在参考cDNA上的位置来表示的,一个突变位点还可以有其它表示方式,如GenBankSNP数据库的命名方法,是以“rs”开头的SNP位点表示方式,rs671与ALDH2基因c.1510G>A(G1510A)表示同一个位点。本领域普通技术人员知道,采用其它命名方式比如以该突变在参考gDNA上的位置来标注指代与本发明一样的突变也属于本发明范围。根据本发明的实施例,所述癌症包括选自结直肠癌、乳腺癌、胰腺癌、前列腺癌、非小细胞肺癌、白血病、黏蛋白腺癌、黑色素瘤、神经胶质瘤、肉瘤、卵巢癌和乳腺癌的至少之一。本发明提供的基于下一代测序技术检测EGFR/KRAS/BRAF基因突变位点的多重PCR引物及方法的有益效果为:本发明提供了检测EGFR、KRAS和BRAF基因突变位点的多重PCR引物,包含了分别扩增这三个基因的一个或多个外显子区域的引物对,能够覆盖EGFR18~21号外显子、KRAS2号外显子和BRAF15号外显子,包括了EGFR、KRAS和BRAF基因的主要突变位点。所设计的目标序列在每个DNA样品中均得到有效的扩增,在所设计的KRAS、EGFR和BRAF基因的各个外显子中均能真实的检测出突变,从而反映出所提供的检测方案具有较好的特异性和适用性。本发明的附加方面和优点将在下面的描述中部分给出,部分将从下面的描述中变得明显,或通过本发明的实践了解到。附图说明本发明的上述和/或附加的方面和优点从结合下面附图对实施例的描述中将变得明显和容易理解,其中:图1为本发明实施例提供的单独引物PCR的琼脂糖凝胶电泳图;图2为本发明实施例提供的多重PCR的琼脂糖凝胶电泳图;以及图3为本发明实施例提供的测序深度的生物信息学分析结果。具体实施方式下面详细描述本发明的实施例,所述实施例的示例在附图中示出,其中自始至终相同或类似的标号表示相同或类似的元件或具有相同或类似功能的元件。下面通过参考附图描述的实施例是示例性的,仅用于解释本发明,而不能理解为对本发明的限制。材料及试剂说明:癌症(如肺癌、结直肠癌等)患者:来源于深圳第六人民医院,患者知情同意。非特殊说明,本发明实施例采用的试剂均为市售商品,本发明实施例采用的数据库均为公开的在线数据库。具体地,本发明引物如表1所示。表1:多重PCR引物序列设计引物:采用Oligo7.0和MFEprimer-2.0对引物二聚体以及茎环错配进行分析,在包含突变位点的外显子两端设计引物,扩增的序列平均长度在150bp左右,且14对引物的退火温度基本一致。本实施例提供的引物组覆盖了EGFR18~21号外显子、KRAS2号外显子和BRAF15号外显子基因突变位点。由于很小的序列变化将导致引物扩增效果显著降低,发明人分别针对不同目的区域的不同区段设计了多组多重PCR引物组,在经过预实验筛选后,综合产物片段长度和点突变覆盖范围,本发明选取了扩增效果最佳的引物组,如上表1所示。表1各对引物单独PCR结果如图1所示。其中,表1中14对引物分别进行扩增验证的PCR体系及PCR参数如下:反应体系如表2所示:参照QIAGEN公司MultiplexPCR试剂盒(货号:206143)配置。表2:多重PCR缓冲液(MultiplexBuffer,2×)25μlQ溶剂(Qsolution,5×)10μl引物5μlDNA10μlTotal50μl循环参数:实施例1本发明实施例1提供了一种待测DNA样品的制备方法,包括如下步骤:从医院获取包含癌细胞的组织,采用QIAampDNAMiniKit(51304)试剂盒提取基因组DNA,并用Nanodrop2000(Thermo)测定DNA的浓度及纯度,然后保存基因组DNA。实施例2本发明实施例2提供了一种采用检测EGFR/KRAS/BRAF基因突变位点的多重PCR引物构建EGFR/KRAS/BRAF基因突变测序文库的方法,包括如下步骤:1、多重PCR:以实施例1所得基因组DNA为扩增模板采用SEQIDNO:1~SEQIDNO:28所示14对引物对,再采用QIAGEN公司MultiplexPCR试剂盒(货号:206143),按试剂盒说明书配置两管多重PCR体系,多重PCR体系如表3所示。表3:反应体系:多重PCR缓冲液(MultiplexBuffer,2×)25μlQ溶剂(Qsolution,5×)10μl引物5μlDNA10μlTotal50μl各引物分两组进行等摩尔混合,引物总浓度是10微摩尔。第一组引物包括:引物编号1、2、5、6、9、10、13、14、15、16、21、22、25和26;第二组引物包括:引物编号3、4、7、8、11、12、17、18、19、20、23、24、27和28。模板量可以调整,本实施例中采用200ng。再按下述多重PCR的条件设置PCR仪器程序,进行多重PCR:PCR结束后,4℃保存PCR产物并电泳检测,在紫外下切下约150bp左右的目的片段。将第一组引物和第二组引物的PCR产物合在一起回收,得到32uL纯化后的产物,胶回收步骤采用QIAGEN公司QIAquick胶纯化试剂盒,按常规实验室操作进行。2、加尾:取纯化后的PCR产物,在产物3’末端加A尾,配置体系如表4所示(其中,Klenowexo-购自NEB,货号:M0212):表4:将该体系置于37℃下30min。利用QIAGEN公司QIAquick胶纯化试剂盒纯化加A尾的PCR产物。3、加接头:在DNA两端加上测序用的接头,配置体系如表5所示(其中,Quickligase购自NEB,M2200L)。表5:5×quickligasebuffer10μlAdaptor1μlQuickligase5μl加A尾的PCR产物25μlH2O9μlTotal50μl其中,Adaptor的序列SEQIDNO:29所示:5’-/5Phos/GATCGGAAGAGCACACGTCTGAACTCCAGTC/ideoxyU/ACACTCTTTCCCTACACGACGCTCTTCCGATC*T-3’(SEQIDNO:29)。随后将该体系置于20℃下15min。然后加入3μL的USER,37℃放置15min。最后通过QIAGEN公司QIAquick胶回收试剂盒纯化连接产物。4、产物上加入测序用的标签序列,配置体系如表6所示(具体步骤参照illumina高通量测序文库构建说明书)。表6:5×Q5Solutionbuffer10μldNTP(10mM)1μlP1(P5序列+common序列+接头序列)1μlIndex(P7序列+标签序列Index+接头序列)1μlQ5酶0.5μl纯化后的连接产物36.5ulTotal50μl将配置的体系按下述程序进行PCR反应:PCR结束后,用1.5%琼脂糖凝胶电泳验证PCR产物富集片段的大小,选取270bp的目的片段进行切胶回收,并纯化至30μL。琼脂糖凝胶电泳结果图2所示。在图2中,S1~S4(分别代表不同的样本)泳道可以明显看到在250bp-300bp之间有一条带,为加上接头的片段(270bp,箭头所指处),与理论相符。5、将步骤4获得的纯化产物直接用Miseq平台测序进行测序。测序结果是fastq格式的数据,通过生物信息学分析获得EGFR、BRAS和KRAF三个基因多突变位点情况。测序深度见图3。本实施例使用PE150试剂盒进行测序,即片段两端各测序150bp。生物信息学分析测序深度如图3所示,横坐标是EGFR、BRAS和KRAF每对引物得到的扩增产物,纵坐标是测序深度。由图3可知,本实施例测序结果中覆盖了所有引物对的扩增产物,并且分布比较平均。效果实施例1参照实施例2的方法,对100例肺癌癌症样品(包含癌细胞的样品)分别进行多重PCR、加A尾、加接头、加标签序列、高通量测序及生物信息学分析,获得如下结果,如表7所示:表7:癌症样品基因突变位点检测如表7所示,在测试的100例癌症样品中,三个基因的主要突变位点均有检测到。特别值得注意的是,经过对样品测序的数据分析,证实所设计的目标序列在每个DNA样品中均得到有效的扩增,从突变结果中也可看出,在所设计的KRAS、EGFR和BRAF基因的各个外显子中均检测到了突变,从而反映出所提供的检测方案具有较好的特异性和适用性。在本发明的描述中,除非另有说明,“多个”的含义是两个或两个以上。在本说明书的描述中,参考术语“一个实施例”、“一些实施例”、“示意性实施例”、“示例”、“具体示例”、或“一些示例”等的描述意指结合该实施例或示例描述的具体特征、结构、材料或者特点包含于本发明的至少一个实施例或示例中。在本说明书中,对上述术语的示意性表述不一定指的是相同的实施例或示例。而且,描述的具体特征、结构、材料或者特点可以在任何的一个或多个实施例或示例中以合适的方式结合。尽管已经示出和描述了本发明的实施例,本领域的普通技术人员可以理解:在不脱离本发明的原理和宗旨的情况下可以对这些实施例进行多种变化、修改、替换和变型,本发明的范围由权利要求及其等同物限定。SEQUENCELISTING<110>深圳市瀚海基因生物科技有限公司<120>多重PCR引物、试剂盒及用途<130>PI2015017_1<160>29<170>PatentInversion3.3<210>1<211>20<212>DNA<213>Artificial<220><223>多重PCR引物(EGFR-18-No.1-F)<400>1cccttgtctctgtgttcttg20<210>2<211>19<212>DNA<213>Artificial<220><223>多重PCR引物(EGFR-18-No.1-R)<400>2cttatacaccgtgccgaac19<210>3<211>20<212>DNA<213>Artificial<220><223>多重PCR引物(EGFR-18-No.2-F)<400>3gagaagctcccaaccaagct20<210>4<211>18<212>DNA<213>Artificial<220><223>多重PCR引物(EGFR-18-No.2-R)<400>4agaccatgagaggccctg18<210>5<211>19<212>DNA<213>Artificial<220><223>多重PCR引物(EGFR-19-No.3-F)<400>5gcagcatgtggcaccatct19<210>6<211>20<212>DNA<213>Artificial<220><223>多重PCR引物(EGFR-19-No.3-R)<400>6ttccttgttggctttcggag20<210>7<211>20<212>DNA<213>Artificial<220><223>多重PCR引物(EGFR-19-No.4-F)<400>7tctctctgtcatagggactc20<210>8<211>21<212>DNA<213>Artificial<220><223>多重PCR引物(EGFR-19-No.4-R)<400>8cacagcaaagcagaaactcac21<210>9<211>20<212>DNA<213>Artificial<220><223>多重PCR引物(EGFR-20-No.1-F)<400>9atgcgaagccacactgacgt20<210>10<211>18<212>DNA<213>Artificial<220><223>多重PCR引物(EGFR-20-No.1-R)<400>10gatgagctgcacggtgga18<210>11<211>18<212>DNA<213>Artificial<220><223>多重PCR引物(EGFR-20-No.2-F)<400>11ctccctccaggaagccta18<210>12<211>21<212>DNA<213>Artificial<220><223>多重PCR引物(EGFR-20-No.2-R)<400>12attgtctttgtgttcccggac21<210>13<211>17<212>DNA<213>Artificial<220><223>多重PCR引物(EGFR-20-No.3-F)<400>13gcagctcatgcccttcg17<210>14<211>21<212>DNA<213>Artificial<220><223>多重PCR引物(EGFR-20-No.3-R)<400>14cgtatctcccttccctgatta21<210>15<211>20<212>DNA<213>Artificial<220><223>多重PCR引物(EGFR-21-No.1-F)<400>15tgaactacttggaggaccgt20<210>16<211>20<212>DNA<213>Artificial<220><223>多重PCR引物(EGFR-21-No.1-R)<400>16ccttactttgcctccttctg20<210>17<211>20<212>DNA<213>Artificial<220><223>多重PCR引物(EGFR-21-No.2-F)<400>17aaacaccgcagcatgtcaag20<210>18<211>21<212>DNA<213>Artificial<220><223>多重PCR引物(EGFR-21-No.2-R)<400>18aaatgctggctgacctaaagc21<210>19<211>21<212>DNA<213>Artificial<220><223>多重PCR引物(EGFR-21-No.4-F)<400>19attcggatgcagagcttcttc21<210>20<211>19<212>DNA<213>Artificial<220><223>多重PCR引物(EGFR-21-No.4-R)<400>20gatcttgacatgctgcggt19<210>21<211>20<212>DNA<213>Artificial<220><223>多重PCR引物(KRAS-2-No.1-F)<400>21cgtcaaggcactcttgccta20<210>22<211>21<212>DNA<213>Artificial<220><223>多重PCR引物(KRAS-2-No.1-R)<400>22ggtactggtggagtatttgat21<210>23<211>20<212>DNA<213>Artificial<220><223>多重PCR引物(KRAS-2-No.4-F)<400>23ggtcctgcaccagtaatatg20<210>24<211>25<212>DNA<213>Artificial<220><223>多重PCR引物(KRAS-2-No.4-R)<400>24aatataaacttgtggtagttggagc25<210>25<211>22<212>DNA<213>Artificial<220><223>多重PCR引物(BRAF-15-No.1-F)<400>25gactttctagtaactcagcagc22<210>26<211>21<212>DNA<213>Artificial<220><223>多重PCR引物(BRAF-15-No.1-R)<400>26cagtgaaatctcgatggagtg21<210>27<211>23<212>DNA<213>Artificial<220><223>多重PCR引物(BRAF-15-No.2-F)<400>27ccagacaactgttcaaactgatg23<210>28<211>22<212>DNA<213>Artificial<220><223>多重PCR引物(BRAF-15-No.2-R)<400>28gctctgataggaaaatgagatc22<210>29<211>65<212>DNA<213>Artificial<220><223>adaptor序列<220><221>misc_feature<222>(1)..(1)<223>磷酸化修饰<220><221>misc_feature<222>(32)..(32)<223>脱氧修饰<220><221>misc_feature<222>(65)..(65)<223>硫代磷酸酯修饰<400>1gatcggaagagcacacgtctgaactccagtcuacactctttccctacacgacgctcttcc60gatct当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1