一种5型磷酸二酯酶抑制剂的甲磺酸盐多晶物及其制备方法和应用与流程
本发明涉及晶型化合物技术领域,具体涉及一种5型磷酸二酯酶抑制剂的甲磺酸盐多晶物及其制备方法和应用。
背景技术:
勃起功能障碍(erectiledysfunction,简称:ed),是指持续不能达到和(或)维持充分勃起以获得满意性生活。根据统计目前全球范围内约1.5亿男性患有不同程度的ed症状,预计到2025年该患病人数将会增加一倍。pde5(5型磷酸二酯酶)抑制剂,是目前研究最为成熟的ed治疗药物。如今已批准上市的该类药物有五种分别为西地那非(sildenafil)、他达那非(tadanafil)、伐地那非(vardenafil)、乌地那非(udenafil)和米罗那非(mirodenafil)。据文献报道,此类化合物具有较强的选择性抑制磷酸二酯酶的作用,已引起广泛关注,成为新的研究热点。相关研究对这类化合物进行了大量的结构修饰,以期能提高其活性和对磷酸二酯酶5的选择性。
目前有文献报道合成一系列西地那非类似物,其中,笪远锋等(一种西地那非类似物的合成工艺研究,中国当代医药,2014年2月第21卷第5期)合成了一种西地那非类似物(简称wg001),其化学名称是5-[2-乙氧基-5-(4-甲基哌嗪-1-基硫代羰基)苯基]-1-甲基-3-正丙基-1,6-二氢-吡唑并[4,3-d]嘧啶-7-硫酮,结构式如下:
中国专利“一种西地那非类似物的合成方法”(cn104650093a)对上述西地那非类似物的合成方法进行了改进,该专利详细介绍了该西地那非类似物的制备方法。
晶型是化合物分子或原子在晶格空间排列不同而形成的不同固体状态。同一药物的不同晶型,其稳定性以及生物利用度等方面可能会存在明显差异,从而影响药物的疗效。因此,对于药物晶型研究是进行药物物质基础研究的重要组成部分,但是目前尚未有5-[2-乙氧基-5-(4-甲基哌嗪-1-基硫代羰基)苯基]-1-甲基-3-正丙基-1,6-二氢-吡唑并[4,3-d]嘧啶-7-硫酮甲磺酸盐药物晶型的相关报道。并且该西地那非类似物在药物代谢方面还存在一定不足,生物利用度有待进一步提高。
技术实现要素:
针对上述现有技术,本发明的目的是提供一种5型磷酸二酯酶抑制剂的甲磺酸盐多晶物及其制备方法和应用,使其能提高药物活性和改善药物生物利用度。
为实现上述目的,本发明采用如下技术方案:
本发明的第一方面,提供一种5型磷酸二酯酶抑制剂的甲磺酸盐多晶物,所述5型磷酸二酯酶抑制剂的结构如式a所示:
所述的5型磷酸二酯酶抑制剂的甲磺酸盐多晶物,其x射线粉末衍射图如图1所示。
所述的5型磷酸二酯酶抑制剂的甲磺酸盐多晶物在x射线粉末衍射图谱中包含以下2θ反射角测定的衍射峰:7.1750°±0.2°,7.6299°±0.2°,8.8588°±0.2°,13.2310°±0.2°,14.3754°±0.2°,14.8440±0.2°,15.2941°±0.2°,17.1838°±0.2°,20.0314°±0.2°,20.8507°±0.2°,21.2839°±0.2°,21.7890°±0.2°,22.2594°±0.2°,23.0373±0.2°,25.1243°±0.2°,25.4244°±0.2°,26.1530°±0.2°,28.1210°±0.2°,30.0135°±0.2°,31.4809°±0.2°,32.3619°±0.2°,37.2410°±0.2°,37.6388°±0.2°,40.8286°±0.2°。
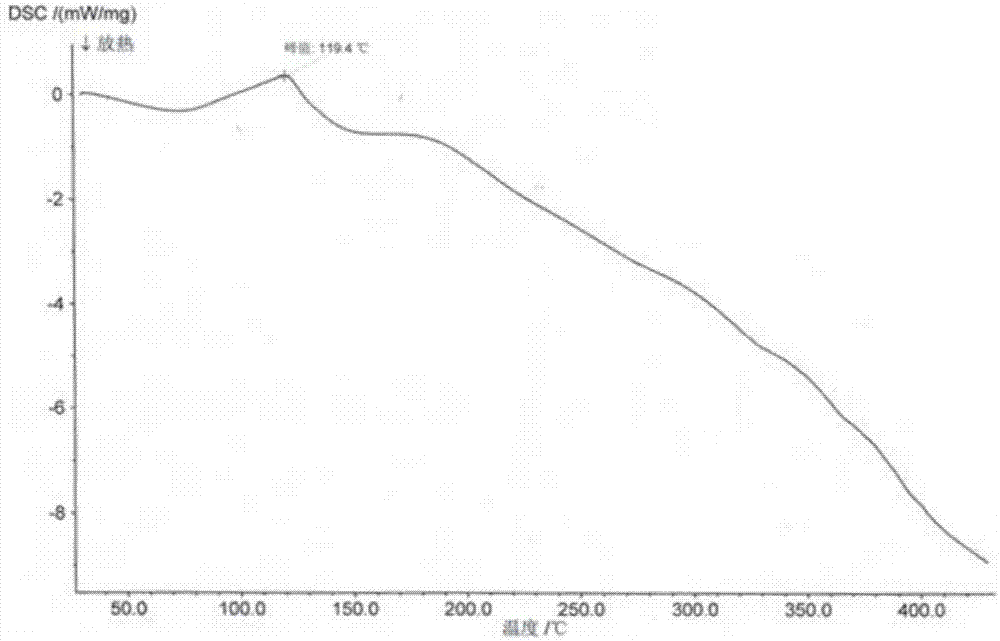
此外,本发明还通过差示扫描量热法和红外光谱技术对所述5型磷酸二酯酶抑制剂的甲磺酸盐多晶物进行分析,其差示扫描量热分析图如图2所示;红外光谱图如图3所示。
本发明的第二方面,提供上述5型磷酸二酯酶抑制剂的甲磺酸盐多晶物的制备方法,包括:制备5型磷酸二酯酶抑制剂的甲磺酸盐的步骤;和将5型磷酸二酯酶抑制剂的甲磺酸盐溶于无水乙醇中,待固体料完全溶解后,压滤,滤液冷却至20℃以下静置结晶的步骤。
上述制备方法中,所述制备5型磷酸二酯酶抑制剂的甲磺酸盐的步骤,具体为:将式a所示的化合物加入到无水乙醇中,搅拌均匀,缓慢加入5%naoh,搅拌,待固体物质完全溶解后,在10℃以下的温度条件下抽滤,滤液中加入甲磺酸与无水乙醇的混合液,调节ph至7-8,搅拌结晶,析出固体料;抽滤,将固体料加入到无水乙醇中,升温至30-35℃,用甲磺酸调ph至3-4,升温至80℃回流,回流完毕后稍冷却至70℃,趁热抽滤,滤液先自然冷至室温,后再用冰水冷却至15℃以下,放置结晶,抽滤,固体料80-90摄氏度烘干,得5型磷酸二酯酶抑制剂的甲磺酸盐。
上述制备方法中,将5型磷酸二酯酶抑制剂的甲磺酸盐溶于3倍重量的无水乙醇中,加热升温至50-60℃,甲磺酸调节ph至3-4,再升温至70-75℃,使固体料完全溶解。
本发明的第三方面,提供上述5型磷酸二酯酶抑制剂的甲磺酸盐多晶物在制备治疗或预防男性勃起功能障碍的药物的用途。
进一步的,本发明还提供上述5型磷酸二酯酶抑制剂的甲磺酸盐多晶物在制备治疗或预防与5型磷酸二酯酶有关疾病的药物的用途。
所述的与5型磷酸二酯酶有关的疾病包括:男性性功能障碍、女性性功能障碍、良性前列腺增生、膀胱阻塞、失禁、心绞痛、高血压、肺高压、充血性心衰、动脉硬化、中风、外周循环系统疾病、哮喘、支气管炎、阿尔茨海默症、急性呼吸系统衰竭等。
本发明的第四方面,提供一种治疗或预防男性勃起功能障碍的药物组合物,其包含有效量的上述5型磷酸二酯酶抑制剂的甲磺酸盐多晶物。
上述药物组合物可以制成固体口服制剂,如片剂、胶囊、丸剂和粉末剂;也可以制成液体口服制剂,如悬浮剂、溶解剂、乳剂和糖浆剂。这些制剂可以含有常规的功能性赋形剂,如润湿剂、增甜剂、芳香剂、防腐剂等,也可以含有常规的功能性赋形剂,如填充剂、粘合剂、分散剂、稀释剂、吸收促进剂、吸收剂和润滑剂;也可以制成膏剂外用;同样适合于制成静脉注射剂。
本发明的第五方面,提供一种治疗或预防与5型磷酸二酯酶有关疾病的药物组合物,其包含有效量的上述的5型磷酸二酯酶抑制剂的甲磺酸盐多晶物。
上述技术方案具有如下有益效果:
本发明以式a所示的5型磷酸二酯酶抑制剂为研究对象,首先与甲磺酸成盐,制备得到5型磷酸二酯酶抑制剂的甲磺酸盐,再通过溶剂结晶,进而获得治疗男性勃起功能障碍和与5型磷酸二酯酶相关疾病效果更佳的5型磷酸二酯酶抑制剂的甲磺酸盐多晶物,不仅提高了药物的活性,而且还提高了其水溶性和生物利用度,弥补了其晶型药物研究的空白。
附图说明
构成本申请的一部分的说明书附图用来提供对本申请的进一步理解,本申请的示意性实施例及其说明用于解释本申请,并不构成对本申请的不当限定。
图1:式a所示化合物的甲磺酸盐多晶物的x-射线粉末衍射图;
图2:式a所示化合物的甲磺酸盐多晶物的热法分析图;
图3:式a所示化合物的甲磺酸盐多晶物的ir谱图;
图4:式a所示化合物的甲磺酸盐多晶物的液相色谱图;
图5:参比制剂组与受试制剂组分别灌胃给予b与c胶囊内容物后,平均血药浓度-时间曲线;
图6:参比制剂组sd大鼠灌胃给予b胶囊内容物后,个体血药浓度-时间曲线;
图7:受试制剂组sd大鼠灌胃给予c胶囊内容物后,个体血药浓度-时间曲线。
具体实施方式
应该指出,以下详细说明都是示例性的,旨在对本发明提供进一步的说明。除非另有指明,本文使用的所有技术和科学术语具有与本发明所属技术领域的普通技术人员通常理解的相同含义。
需要注意的是,这里所使用的术语仅是为了描述具体实施方式,而非意图限制根据本发明的示例性实施方式。如在这里所使用的,除非上下文另外明确指出,否则单数形式也意图包括复数形式,此外,还应当理解的是,当在本说明书中使用术语“包含”和/或“包括”时,其指明存在特征、步骤、操作和/或它们的组合。
正如背景技术所介绍的,目前尚未有5-[2-乙氧基-5-(4-甲基哌嗪-1-基硫代羰基)苯基]-1-甲基-3-正丙基-1,6-二氢-吡唑并[4,3-d]嘧啶-7-硫酮甲磺酸盐药物晶型的相关报道;并且该西地那非类似物在药物代谢方面还存在一定不足,生物利用度有待进一步提高。基于此,本发明提出了一种5型磷酸二酯酶抑制剂的甲磺酸盐多晶物及其制备方法和应用。
在本申请的一种实施方案中,给出了5型磷酸二酯酶抑制剂的甲磺酸盐多晶物,该甲磺酸盐多晶物是一种新晶型结构,能够改善5型磷酸二酯酶抑制剂的水溶性和生物利用度。
该5型磷酸二酯酶抑制剂的甲磺酸盐多晶物,其x射线粉末衍射图如图1所示。所述的新晶型各详细粉末x射线衍射参数见表1。
表1本发明所述新晶型的粉末x射线衍射峰值
此外,本发明还通过差示扫描量热法和红外光谱技术对所述5型磷酸二酯酶抑制剂的甲磺酸盐多晶物进行分析,其差示扫描量热分析图如图2所示,图谱中存在1个吸热峰,在119.4℃处。
红外光谱图如图3所示,其在3477.67cm-1,3262.83cm-1,2959.82cm-1,2933.09cm-1,2872.82cm-1,2722.42cm-1,,1637.94cm-1,1606.16cm-1,1573.35cm-1,1544.76cm-1,1518.00cm-1,1498.31cm-1,1468.97cm-1,1304.10cm-1,1262.09cm-1,1195.75cm-1,1112.81cm-1,1080.28cm-1,1042.16cm-1,976.02cm-1,919.02cm-1,887.55cm-1,816.81cm-1,776.56cm-1,643.60cm-1,610.94cm-1,555.50cm-1,536.73cm-1,508.15cm-1处存在红外光谱特征峰在本发明的另一种实施方案中,将有效量的本发明的5型磷酸二酯酶抑制剂的甲磺酸盐多晶物与药学上可接受的辅料一起组成药物组合物。
本发明中所述的有效量是指能够达到治疗作用的药理剂剂量。所述药学上可接受的辅料可以为常规的功能性赋形剂,如润湿剂、增甜剂、芳香剂、防腐剂等;也可以为常规的功能性赋形剂,如填充剂、粘合剂、分散剂、稀释剂、吸收促进剂、吸收剂和润滑剂。
为了使得本领域技术人员能够更加清楚地了解本发明的技术方案,以下将结合具体的实施例详细说明本发明的技术方案。
本发明实施例中使用的式a所示的化合物,其为现有技术已有的化合物,可以按“一种西地那非类似物的合成工艺研究”,(中国当代医药,2014年2月第21卷第5期)的方法合成;也可以按专利“一种西地那非类似物的合成方法”(cn104650093a)的方法合成。
实施例1:5-[2-乙氧基-5-(4-甲基哌嗪-1-基硫代羰基)苯基]-1-甲基-3-正丙基-1,6-二氢-吡唑并[4,3-d]嘧啶-7-硫酮甲磺酸盐多晶物的制备
具体制备方法如下:
于洗净干燥的反应瓶中先投入200g无水乙醇和100g式a所示的化合物,搅拌均匀后,缓慢投入200g5%naoh。投毕,搅拌下使式a所示化合物完全溶解。待固体完全溶解后,于10℃以下(此条件必须满足10℃以下)抽滤,滤液中加入20g甲磺酸与80g无水乙醇的混合液调ph值7-8偏8(注意需用冰水降温),固体料重新析出,搅拌结晶2h。抽滤,固体料投入到320g无水乙醇中,升温至30-35℃,用甲磺酸(约22g)调ph值,固体料逐渐溶解且温度上升,然后固体料完全溶解,保持溶液ph值3-4偏3(不超过60摄氏度),调毕,搅拌10min,测ph值3-4偏3稳定后,升温至80℃回流1h,回流完毕。稍冷却至70℃,趁热抽滤。滤液先自然冷至室温,后再用冰水冷却至15℃以下。放置结晶2h,抽滤,固体料80-90摄氏度烘干,得式a所示化合物的甲磺酸盐。
将式a所示化合物的甲磺酸盐投入3倍的乙醇中,加热升温至50-60℃,甲磺酸调ph值3-4偏3,再升温至70-75℃,固体料完全溶解后,趁热压滤,滤液冷却至20℃以下静置结晶10h,离心,固体料烘干。得精品式a所示化合物的甲磺酸盐多晶物。
将得到的式a所示化合物的甲磺酸盐多晶物采用荷兰panalyticalb.v(帕纳科)公司的锐影x射线衍射仪(empyreanx-raydiffractometer)于室温检测,2θ角扫描从5°到40°,cu-ka,扫描速度:2°/分钟。管电压:40kv,管电流:40ma.
该多晶型物的x-射线粉末衍射图如图1所示。该多晶型物2θ值处的衍射峰包括:7.1750°±0.2°,7.6299°±0.2°,8.8588°±0.2°,13.2310°±0.2°,14.3754°±0.2°,14.8440±0.2°,15.2941°±0.2°,17.1838°±0.2°,20.0314°±0.2°,20.8507°±0.2°,21.2839°±0.2°,21.7890°±0.2°,22.2594°±0.2°,23.0373±0.2°,25.1243°±0.2°,25.4244°±0.2°,26.1530°±0.2°,28.1210°±0.2°,30.0135°±0.2°,31.4809°±0.2°,32.3619°±0.2°,37.2410°±0.2°,37.6388°±0.2°,40.8286°±0.2°。
将得到的式a所示化合物的甲磺酸盐多晶物采用德国耐驰公司,型号为sta449f3的差示扫描热量热仪,气体为高氩,加热速度为10℃/分钟,扫描温度范围30℃-400℃。
该多晶型物的热法分析图如图2所示,其吸热最大值在119.4℃。
将得到的式a所示化合物的甲磺酸盐多晶物采用德国布鲁克公司vertex70红外光谱仪,于室温检测,光谱范围4000-400cm-1的波数。
该多晶型物的红外光谱图如图3所示。
采用液相色谱法对式a所示化合物的甲磺酸盐多晶物的含量进行检测,检测的条件为:
(1)样品处理:将样品用甲醇溶解,制得样品浓度为500μg/ml。
(2)色谱条件:检测波长为285nm;流动相组成为:乙腈:0.1%磷酸;洗脱条件为:梯度洗脱,0-15min由20:80渐变至25:75,15-20min由25:75渐变至40:60。柱温:30.1℃;流速1ml/min;进样量20μl。
含量测定的色谱图如图4所示。色谱分析数据见表2。
表2:色谱分析数据
经计算,其摩尔收率:90%,纯度:99.51%。
试验例1:溶解性试验
以中国药典2010版二部标准凡例中关于溶解度的规定作为判断依据
称取研成细粉的样品(样品b:式a所示的化合物;样品c:实施例1制备的式a所示化合物的甲磺酸盐多晶物),置于25℃±2℃一定容量的溶剂中,每隔5分钟强力振摇30秒钟;观察30分钟内的溶解情况,如看不见溶质颗粒或液滴时,即视为完全溶解。
1g样品b10000g水中不溶,所以判定其几乎不溶于水。
1g样品c在800g水中完全溶解,所以判定其微溶于水。
1g样品b在10000g95%的乙醇中不能完全溶解,所以判其几乎不溶于95乙醇。
1g样品c在90g95%乙醇中能完全溶解,所以判定其略溶于95乙醇。
试验例2:生物利用度试验
通过测定sd大鼠灌胃给予b(参比制剂,以式a所示的化合物为有效成分)或c(受试制剂,以实施例1制备的式a所示化合物的甲磺酸盐多晶物为有效成分)胶囊内容物后的血药浓度,统计主要药代动力学参数,计算两种制剂的相对生物利用度(f)。
1.试验方法:
将12只雄性sd大鼠按体重随机分成2组,每组6只。禁食约12h后,2组动物分别灌胃给予50mg/只b与c胶囊内容物溶液(以式a所示的化合物含量计)。各组药前采血,并于药后0.5、1、2、3、4、6、8、24、32、48h眼眦采血约0.5ml,置于肝素钠抗凝的离心管中,4℃12000r/min离心5min,制备血浆。采用hplc-ms/ms法检测大鼠血浆中a含量。a血药浓度-时间数据经das3.2.6程序处理,计算各组药动学参数。
2.试验结果:
sd大鼠分别灌胃给予参比制剂b、受试制剂c胶囊内容物后,式a所示的化合物平均血药浓度-时间曲线及个体血药浓度-时间曲线见图5-7;平均血药浓度及个体血药浓度见表3-6。
参比制剂、受试制剂组式a所示的化合物的主要药动学参数见表7、8。两组药动学参数经双单侧t检验分析结果见表9。
表3:参比制剂组sd大鼠灌胃给予b胶囊内容物后,式a所示化合物平均血药浓度(μg/l)-时间(h)数据
-,检测值低于最低定量限(1μg/l)。
表4受试制剂组sd大鼠灌胃给予c胶囊内容物后,平均血药浓度(μg/l)-时间(h)数据
-,检测值低于最低定量限(1μg/l)。
表5参比制剂组sd大鼠灌胃给予b胶囊内容物后,式a所示化合物血药浓度(μg/l)-时间(h)数据
-,检测值低于最低定量限(1μg/l)。
表6受试制剂组sd大鼠灌胃给予c胶囊内容物后,式a所示化合物血药浓度(μg/l)-时间(h)数据
-,检测值低于最低定量限(1μg/l)。
表7参比制剂组sd大鼠灌胃给予b胶囊内容物后,式a所示化合物主要药动学参数
表8受试制剂组sd大鼠灌胃给予c胶囊内容物后,式a所示化合物主要药动学参数
表9:主要药动学参数结果
**p<0.01vs参比制剂组
由上述结果可以看出,sd大鼠灌胃给予b与c胶囊内容物后,相比于参比制剂组,受试制剂组暴露量更高,auc(0-∞)是参比组的3.1倍,cmax是参比组的2.9倍,f值为310.66%。
结论:sd大鼠灌胃给予c胶囊后,与b胶囊比较,式a所示的化合物更多分布于体液,清除速率更低,在大鼠体内的暴露量是b胶囊的3.1倍,吸收明显高于b胶囊制剂。
上述实施例为本发明较佳的实施方式,但本发明的实施方式并不受上述实施例的限制,其他的任何未背离本发明的精神实质与原理下所作的改变、修饰、替代、组合、简化,均应为等效的置换方式,都包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!