一种外周血氧化型低密度脂蛋白自身抗体的检验方法与流程
本发明涉及一种医用抗体的检验方法,特别是涉及一种外周血氧化型低密度脂蛋白自身抗体的检验方法。
背景技术:
动脉粥样硬化性心血管疾病是西方国家死亡及致残的首要原因,被称为发达国家的“头号杀手”,在发展中国家发病率也越来越高。《2010年中国心血管病年报》公布数据显示,据估计我国心血管病现患人数2.3亿,每5个成年人中有1人是心血管病;中国人总死亡中,每死亡3个人中就有1人是死于心血管病。大量的临床随机对照试验也发现,通过目前的治疗和预防措施,仅能够将心肌梗死、卒中等并发症的降低不足50%。因此,发展更新的诊断及治疗策略去补充及替代现有的诊断技术将是未来发展的方向。
低密度脂蛋白(ldl)在内皮下的滞留及其氧化修饰是触发动脉粥样硬化形成的始动环节,继之引起炎症细胞的浸润和激活,并且促进巨噬细胞转化为泡沫细胞。无论是在体内还是体外,ldl的氧化都是一个复杂的过程。它可能通过以下途径导致内皮细胞功能不全:通过氧化、糖基化及与糖基化高级产物或mda的结合使ldl颗粒进行了修饰,从而在动脉粥样硬化形成过程起到十分重要的作用。而适应性免疫系统可在动脉粥样硬化形成过程中被激活,通过特异性免疫反应不断加重动脉粥样硬化的病理变化过程,最终导致斑块脱落,发生心肌梗死或脑梗死。
众所周知,修饰的ldl分子在氧化进程末期具有了趋化性、细胞毒性及免疫原性,能够刺激免疫系统产生针对氧化型低密度脂蛋白(oxldl)的特异性抗体。oxldl分子含有大量的抗原表位,并且针对这些产物由hdl和ldl多形性变而产生了很多的多克隆抗体。这些抗oxldl抗体要么直接表达在内膜损坏部位,要么形成循环中的免疫复合物。这些抗体可在血清中检测到。因此,oxldl的剂量仅仅反应了某一时刻的氧化状态,可以受到很多因素的影响(如饮食、吸烟、生活习惯等),而血清中的抗oxldl抗体的出现表明了体内一个长期脂质过氧化反应的存在。
大量的近期研究表明,局部及全身免疫系统的激活可能与动脉粥样硬化斑块的不稳定性相关。已经有作者发现,急性冠脉综合征(acutecoronarysyndrome,acs)患者存在短暂的t细胞激活增加,认为其可能在急性并发症的病理生理学机制中起到决定性作用。有研究发现,acs患者中抗oxldligg抗体平均滴度明显高于慢性冠心病患者,而此差异明显独立于已知心血管危险因素,如高血压、吸烟、糖尿病及血脂异常等。很多研究对比了acs患者与没有临床事件的冠心病患者,发现其对于oxldl的免疫反应具有明显差异。由于血中高浓度抗氧化物质的存在,导致循环中的oxldl水平非常低,而且,他们可能与动脉硬化斑块内氧化的脂蛋白水平不完全一致。在健康个体中,估测血浆平均oxldl浓度大约是0.1ng/µgldl蛋白。所以,对于oxldl抗体的评估能够更可靠地反应体内氧化应激水平。已经发现,这些抗体与动脉粥样硬化的程度相关,并且能够预测心肌梗死的发生风险。也有研究表明,在acs患者中抗oxldligg抗体水平明显高于对照组,尤其在那些存在不稳定临床并发症的患者中(如循环功能不全、恶性心律失常、复发的缺血性胸痛、运动试验阳性、需要急诊冠脉介入治疗或心源性猝死等),说明抗oxldligg抗体在不稳定斑块的诊断方面具有潜在作用。因此,抗oxldl抗体水平的检测可加强传统冠脉危险因素的预测作用。
技术实现要素:
本发明的目的在于提供一种外周血氧化型低密度脂蛋白自身抗体的检验方法,本发明采用优化的双抗体夹心elisa法检测患者外周血中抗oxldligg和igm抗体,比较急性冠脉综合征患者外周血自身抗体水平与健康人之间的差异,分析oxldl抗体水平与动脉粥样硬化性疾病发生、发展乃至预后的相关性,确定冠状动脉粥样硬化性疾病早期诊断的标志物。
本发明的目的是通过以下技术方案实现的:
一种外周血氧化型低密度脂蛋白自身抗体的检验方法,所述方法包括以下过程:
a.首先进行抗原设计,利用生物信息学数据库和在线工具对中国人oxldl蛋白的结构进行分析,预测蛋白的ph值、亲水性、柔性、表面可及性、抗原性,并进行评分。遵循以上表位设计原则和方法选择oxldl的apob成分设计多肽抗原;
b.抗体的检测,elisa法原理是将抗原或抗体固相化,用过氧化酶标记已知抗体。结合在固相载体表面的抗原或抗体仍保持其免疫学活性,酶标记的抗体既保留其免疫学活性,又保留酶的活性;
c.抗体检测流程包括材料与试剂的准备、抗原准备、样本稀释、加入酶标抗体、显色、测定od值、抗体水平计算与质量控制、质控。
所述的一种外周血氧化型低密度脂蛋白自身抗体的检验方法,所述抗体检测,针对中国人mhc基因型特征,选择心血管相关抗原oxldl中的apob片段,设计了最具特异性的20个多肽抗原片段。
所述的一种外周血氧化型低密度脂蛋白自身抗体的检验方法,所述材料与试剂的准备包括有包被液、显色液、抗体、包被板。
所述的一种外周血氧化型低密度脂蛋白自身抗体的检验方法,所述抗原包被包括抗原储存液,人源抗原和玉米抗原。
所述的一种外周血氧化型低密度脂蛋白自身抗体的检验方法,所述样本稀释包括,冻存血浆从﹣20℃或﹣80℃移到4℃融解,稀释时血浆应放在冰上操作。
所述的一种外周血氧化型低密度脂蛋白自身抗体的检验方法,所述加入酶标抗体包括,取甘油(1:1)稀释的羊抗人抗体5ul(浓度稀释为1:2倍),加入分析液45ul(浓度稀释为1:20倍)。
所述的一种外周血氧化型低密度脂蛋白自身抗体的检验方法,所述显色用前2小时取适量底物显色液tmb,置于室温(18-22℃)。
所述的一种外周血氧化型低密度脂蛋白自身抗体的检验方法,所述测定od值包括,提前将酶标仪打开,预热10分钟,将波长设定为450nm(标准波长)和620-650nm(参考波长),在终止反应后十分钟内,完成光密度(od)的测定。
所述的一种外周血氧化型低密度脂蛋白自身抗体的检验方法,所述抗体水平计算与质量控制特异结合指数(sbi)公式计算:
sbi=[hag(od)-nc(od)]/[mag(od)-nc(od)]。
所述的一种外周血氧化型低密度脂蛋白自身抗体的检验方法,所述质控包括,各样本设双复孔,取平均od值。od值离散度判定:离散度=od1-od2/od1+od2,离散度≤0.1,为有效结果;离散度>0.1,为无效结果。
本发明的优点与效果是:
本发明利用免疫信息学数据库和免疫学软件,根据中国人主要组织相容复合体(mhc或hla)基因型分布,在ox-ldl分子中的主要组成部分apob蛋白序列上设计特异性线性多肽抗原,该抗原将覆盖95%以上的中国人群,每个抗原可携带约10个重叠表位。本发明采用优化的双抗体夹心elisa法检测患者外周血中抗oxldligg和igm抗体,比较急性冠脉综合征患者外周血自身抗体水平与健康人之间的差异,并比较不同类型、不同时期急性冠脉综合征患者血清抗oxldl自身抗体水平的变化。分析oxldl抗体水平与动脉粥样硬化性疾病发生、发展乃至预后的相关性,以确定冠状动脉粥样硬化性疾病早期诊断的标志物。
附图说明
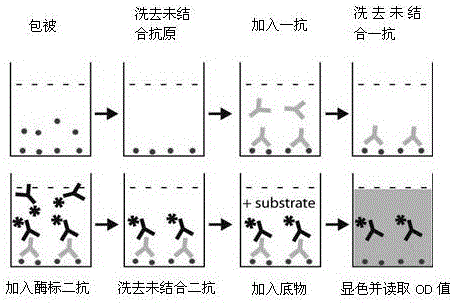
图1为双抗体夹心法测抗体的原理和操作步骤示意图。
具体实施方式
下面结合实施例对本发明进行详细说明。
首先进行抗原设计,利用生物信息学数据库和在线工具对中国人oxldl蛋白的结构进行分析,预测蛋白的ph值、亲水性、柔性、表面可及性、抗原性,并进行评分。遵循以上表位设计原则和方法选择oxldl的apob成分设计多肽抗原:a.尽可能是在蛋白表面;b.保证抗原片段序列不形成α-helix;c.n端和c端的肽段比中间的肽段更好;d.避免蛋白内部重复或接近重复段的序列;e.避免同源性太强的肽段;f.交联可以交联在n,c两端,选择依据就是交联在对产生抗体不太重要的一端;g.序列中不能有太多的脯氨酸(pro),但有1~2个pro有好处,可以使肽链结构相对稳定一些,对产生特异性抗体有益。
抗体的检测,elisa法原理是将抗原或抗体固相化,用过氧化酶标记已知抗体。结合在固相载体表面的抗原或抗体仍保持其免疫学活性,酶标记的抗体既保留其免疫学活性,又保留酶的活性。在测定时,受检标本(测定其中的抗体或抗原)与固相载体表面的抗原或抗体起反应。洗涤去除液体中的其他物质后,再加入酶标记的已知抗体。合酶反应的底物,底物被酶催化成为有色产物,其含量与标本中受检物质的量直接相关,故可根据呈色的深浅进行定性或定量分析。由于酶的催化效率很高,间接地放大了免疫反应的结果,使测定方法达到很高的敏感度。elisa方法包括双抗体夹心法、间接法、竞争法、捕获包被法以及亲和素-生物素系统。测抗体的方法是双抗体夹心法,其基本原理和操作步骤见图1。
本发明利用生物信息学数据库及软件综合分析蛋白结构和性质,针对中国人mhc基因型特征,选择心血管相关抗原oxldl中的apob片段,设计了最具特异性的20个多肽抗原片段。利用优化的elisa法检测400例不同时期acs患者外周血清中20种不同抗原序列的相应抗体水平,并选择健康体检者为对照组,以100例健康体检者的混合血为质控样本,采用spss18.0软件进行x2检验和roc曲线分析。
抗体检测流程如下:
(1)材料与试剂包括,包被液:磷酸盐缓冲液(pbs),含0.1%叠氮钠,ph为7.4。分析液:pbs含1.5%纯度大于98%的牛血清白蛋白bsa。洗液:tris盐缓冲液(tbs)含tween®20,ph8.0。显色液:四甲基联苯胺。终止液:配制10.9%的硫酸溶液为终止液。二抗:过氧化物酶标记的羊抗人(iga,igg,igm)抗体。包被板:96孔平底透明微量滴定板。人工合成多肽抗原:溶解于67%的乙酸,储存液浓度为5mg/ml,放置﹣20℃冰箱中可保存12个月。
(2)抗原包被包括,取适量抗原储存液(5mg/ml),包括人源抗原(hag)和玉米抗原(mag),用包被液稀释至10µg/ml,每孔加样0.1ml。摇匀后用膜封闭,4℃孵育过夜,或存放1-2周。
4.2.3使用前吸除包被液,用洗涤液洗板3次,然后加样。
(3)样本稀释(一抗)包括,冻存血浆从﹣20℃或﹣80℃移到4℃融解,稀释时血浆应放在冰上操作。用分析液按1:150倍稀释血浆样品,每孔加样0.1ml。室温(18-22℃)孵育1.5小时。用洗涤液洗板3次。
(4)加入酶标抗体(二抗)包括,取甘油(1:1)稀释的羊抗人抗体5ul(浓度稀释为1:2倍),加入分析液45ul(浓度稀释为1:20倍),充分混合后取适量体积,再用分析液稀释1500倍,达到1:30000的稀释倍数。每孔加样0.1ml。室温(18-22℃)孵育1小时。洗涤,同上。
(5)显色包括,用前2小时取适量底物显色液tmb,置于室温(18-22℃)。每孔加入tmb100ul,置于水平摇床。室温避光显色20-30分钟,随时观察颜色变化。每孔加入50ul终止液。
(6)测定od值包括,提前将酶标仪打开,预热10分钟,将波长设定为450nm(标准波长)和620-650nm(参考波长),在终止反应后十分钟内,完成光密度(od)的测定。
(7)抗体水平计算与质量控制包括,用特异结合指数(sbi)表示血浆中的抗体水平,sbi值可用以下公式计算:
sbi=[hag(od)-nc(od)]/[mag(od)-nc(od)]。
(8)质控包括,各样本设双复孔,取平均od值。od值离散度判定:离散度=od1-od2/od1+od2,离散度≤0.1,为有效结果;离散度>0.1,为无效结果。取100份健康人血清等体积混合作为质控血(qualitycontrol,qc),代表人群的普遍情况,每板均设2个qc血浆孔,以qc血浆孔的od值变异水平判定结果的稳定性,批间变异cv=所有批次qc孔sd/所有批次qc孔od均值<20%。批内变异cv=每日各板qc孔sd/每日各板qc孔均值<10%。
- 还没有人留言评论。精彩留言会获得点赞!