他汀类化合物治疗缺血性疾病的用途的制作方法
本发明涉及医药技术领域,更具体地说,涉及HMG-CoA还原酶抑制剂(他汀类化合物)治疗缺血性疾病的新用途。
背景技术:
心脑血管疾病是危及人类健康的头号杀手,缺血性心脑血管疾病引起的致残率和致死率很高。伴随着人口老龄化和发病年龄的下降,问题越来越严重。目前缺血性心、脑血管的治疗方法主要有药物、支架置入和血运重建。支架置入一度受到追捧,甚至出现过度治疗的热潮。而当前的一些RCT研究表明,积极的药物治疗能取得同样的甚至比介入治疗更好的效果(Lampropoulos CE,Papaioannou I,D'Cruz DP.Osteoporosis--a risk factor for cardiovascular disease?Nature reviews Rheumatology.2012;8:587-98)。这引发了人们对介入治疗的反思和对血运重建治疗的探索。
外周动脉疾病(Peripheral Arterial Disease,PAD)是由心脏以外的血管粥样硬化闭塞引起的周围组织缺血性疾病,50-60岁人群PAD的患病率为6%,70岁以上则高达10–20%,几乎等于冠状动脉疾病总患病率;严重缺血并发坏疽的患者往往需要截肢,致死致残率高,严重危害人们的健康(Annex BH.Therapeutic angiogenesis for critical limb ischaemia.Nature Reviews Cardiology.2013;10:387–396.)。血管成形或搭桥手术可以实现闭塞血管的再通,以实现血液流向肢体远端,但中远期再闭塞率高,而且对于流出道广泛闭塞的患者根本无法手术治疗。
骨髓来源的内皮祖细胞(Endothelial Progenitor Cells,EPCs)在血管新生和内皮功能稳态中具有重要的作用。治疗性血管新生又称“药物搭桥”,利用外源性血管生长因子及骨髓源性EPCs,促进缺血组织血管新生(Annex BH.Therapeutic angiogenesis for critical limb ischaemia.Nature Reviews Cardiology.2013;10:387–396.)。治疗性血管新生的瓶颈在于循环EPCs数量少,衰老、糖尿病、高血脂等循环EPCs更少(Yao L,et al.Bone marrow endothelial progenitors augment atherosclerotic plaque regression in a mouse model of plasma lipid lowering.Stem Cells.2012;30:2720–2731.)(Adler BJ,et al.Obesity-driven disruption of haematopoiesis and the bone marrow niche.Nature Reviews Endocrinology.2014;10:737–748.)。通过促进内源性EPCs动员以增加外周血EPCs的数量是一个重要治疗策略(Liu Y,et al.Beneficial effects of statins on endothelial progenitor cells.Am J Med Sci.2012;344:220–226.)。
传统观念认为骨骼是储藏钙磷、保护内脏的惰性器官。近年来研究发现骨骼还是重要的内分泌器官,被视为整合生理学的典范,不仅是靶器官,还是重要的调控器官(Karsenty G,Ferron M.The contribution of bone to whole-organism physiology.Nature.2012;481:314–320.)(Karsenty G,Oury F.Biology without walls:the novel endocrinology of bone.Annu Rev Physiol.2012;74:87–105.),并以“骨-血管轴”影响血管功能(Thompson B,Towler DA.Arterial calcification and bone physiology:role of the bone–vascular axis.Nature Reviews Endocrinology.2012;8:529–543.)。骨骼不仅包含成骨细胞、破骨细胞和骨细胞,还有丰富的内皮细胞、巨噬细胞、神经和脂肪组织等,更富集大量造血干细胞、骨髓基质干细胞。骨骼通过造血干细胞龛(Niche),即骨龛和血管龛协同调控造血干细胞的增殖、动员和分化(Bianco P.Bone and the hematopoietic niche:a tale of two stem cells.Blood.2011;117:5281–5288.)(Morrison SJ,Scadden DT.The bone marrow niche for haematopoietic stem cells.Nature.2014;505:327–334.)。
近年来,他汀类药物降脂外的多效作用广受关注。但他汀类药物作为肝脏中胆固醇合成的限速酶HMG-CoA还原酶的抑制剂,口服后不到5%能够进入血液循环,骨骼中的浓度更低。本发明人在中国专利申请(CN201210596032.3、CN201210512630.8)局部施用他汀类药物,结果发现局部骨骼单次注射小剂量辛伐他汀,可以促进胰岛素分泌、增强胰岛素的敏感性;并且增加骨量、提高骨密度、改善骨组织微结构、增强骨骼力学性能。
既往有研究发现,长期口服大剂量口服瑞舒伐他汀(20mg/kg/d,连续10周)可增加外周血内皮祖细胞数目(Thum T,Fraccarollo D,Galuppo P,et al.Bone marrow molecular alterations after myocardial infarction:impact on endothelial progenitor cells.Cardiovasc Res 2006;70:50–60.),即使最短也需要连续口服至少4周以上(Liu Y,Wei J,Hu S,Hu L.Beneficial effects of statins on endothelial progenitor cells.Am J Med Sci.2012;344:220–226.)。治疗依从性低,且一旦发生缺血性损伤,再行口服他汀难以救急。
但是,骨骼内施用他汀类药物动员内源性内皮祖细胞、促进血管新生,治疗缺血性疾病未见文献报道。
技术实现要素:
整合生理学的新进展、骨骼也是内分泌器官的新发现,也许提供了这样的可能:通过局部骨骼干预,达到治疗系统性疾病的目的。而骨骼内丰富的骨小梁间隙、骨髓腔为局部干预提供了绝佳的干预/给药腔隙。
本发明人令人惊奇地发现了骨骼内单次应用小剂量他汀类化合物可长期显著地促进系统性血管新生,治疗缺血性疾病。
本发明的目的是提供他汀类化合物作为局部施用药物、优选骨骼内施用药物用于治疗缺血性疾病的新用途。
具体地说,本发明提供了他汀类化合物作为治疗缺血性疾病的骨骼内施用药物的新用途。
在本发明的一种具体实施方案中,本发明提供了他汀类化合物作为治疗缺血性疾病的骨骼内施用药物的用途,其中,所述的缺血性疾病是指外周缺血性疾病,优选糖尿病肢端缺血性疾病。
在本发明的一种具体实施方案中,本发明提供了他汀类化合物作为治疗缺血性疾病的骨骼内施用药物的用途,其中,所述的缺血性疾病是指心脑血管缺血性疾病。
在本发明的一种具体的实施方案中,本发明提供了他汀类化合物作为治疗缺血性疾病的骨骼内施用药物的用途,这里,所述的骨骼内施用药物包括药理学上有效量的他汀类化合物或其药学上可接受的盐和药学上可接受的辅料。
在本发明的实施方案中,所述的他汀类化合物选自但不限于辛伐他汀、阿托伐他汀、氟伐他汀、洛伐他汀、普伐他汀、瑞舒伐他汀、匹伐他汀、柏伐他汀、西立伐他汀、克伐他汀、达伐他汀、美伐他汀、或替伐他汀等HMG-CoA还原酶抑制剂。
他汀类化合物也可以是药学上可接受盐的形式,包括但不限于盐酸盐、氢溴酸盐、氢碘酸盐、硫酸盐、硝酸盐、磷酸盐、柠檬酸盐、甲磺酸盐、三氟醋酸盐或乙酸盐、钠盐、钾盐、钙盐或镁盐。
在本发明的一种优选的实施方案中,所述的他汀类化合物选自辛伐他汀、阿托伐他汀、氟伐他汀、洛伐他汀、普伐他汀、瑞舒伐他汀、或匹伐他汀,而且它们可以是药学上可接受盐的形式,例如盐酸盐、氢溴酸盐、硫酸盐、硝酸盐、磷酸盐、柠檬酸盐、甲磺酸盐、钠盐、钾盐、钙盐或镁盐,更优选地,辛伐他汀、阿托伐他汀钙或阿托伐他汀钠、氟伐他汀钠、普伐他汀钠、瑞舒伐他汀钙、或匹伐他汀钙。
另一方面,本发明提供了一种用于预防或治疗缺血性疾病的局部应用的药物组合物,其特征在于含有治疗有效量的他汀类化合物或其药学上可接受盐和任选的药学可接受的载体、稀释剂或赋形剂。
在本发明的一种具体的实施方案中,一种治疗或预防哺乳动物缺血性疾病、病症或症状的药物组合物,其特征在于,包括向所述哺乳动物骨骼内施用的他汀类化合物或其药学上可接受盐;优选地,其具有上述任一项技术方案中所述的特征。
在本发明的实施方案中,所述他汀类骨骼内施用药物(或组合物)优选为骨骼内注射或埋入给药,本发明所述的他汀类骨骼内施用药物可以注射剂的形式存在,所述的注射剂包括但不限于注射溶液、注射用混悬液、注射用乳剂、注射用凝胶、注射用固体形式,或者它们的缓释或控释形式,或内植物形式。这里,所述的注射用固体形式是指在使用时与注射用溶媒例如注射用水、注射用生理盐水或注射用葡萄糖溶液等中一种相混合,以便注射应用。
在本发明的一种具体实施方案中,所述的他汀类骨骼内施用药物(或组合物)包括他汀类化合物或其药学上可接受的盐与药学上可接受的辅料。这里,所述药学上接受的辅料选自水溶性溶媒或油性溶媒、分散剂、等渗剂、防腐剂、增溶剂或者稳定剂中的一种或两种以上,其中,水溶性溶媒可选自蒸馏水、生理盐水、格林氏溶液或者磷酸盐缓冲溶液(PBS)等;油溶性溶媒可选自植物油,例如橄榄油、蓖麻油、芝麻油、棉籽油或者玉米油等;分散剂可选自吐温20或吐温80、聚乙二醇、羧甲基纤维素、或者海藻酸钠等;等渗剂可选自氯化钠、甘油、山梨醇、或者葡萄糖等;增溶剂可选自水杨酸钠、帕洛沙姆或者醋酸钠等;防腐剂可选自尼泊金甲酯、尼泊金丙酯、苯甲醇、氯丁醇、苯甲酸钠、或者苯酚等;稳定剂可选自白蛋白等,如人血清白蛋白、牛血清白蛋白等。此外,所述药学上可接受的辅料还可选自生物可降解的材料,例如聚乳酸、聚丙交酯-乙交酯、聚天冬氨酸等。对于本领域的技术人员而言,可以应用已知的制剂技术来制备本发明的他汀类局部用药物(或组合物),例如,将他汀类化合物或其药学上可接受的盐与分散剂、和/或等渗剂、和/或防腐剂、和/或增溶剂、和/或稳定剂一起溶解、悬浮或乳化在水溶性溶媒或油性溶媒中(这里,引入Remington:the science and practice of pharmacy,第21版,Lippincott Williams&Wilkins出版社,2005年,作为参考)。
在本发明实施方案中,对哺乳动物骨骼内施用他汀类药物,给药间隔为7天至600天一次,优选地10天至500天一次,更优选地20天至400天一次,特别优选地30天至300天一次。
对哺乳动物骨骼内施用药物,剂量为每次他汀类化合物0.1mg至50mg,优选地为0.1mg至10mg。对于临床医师而言,在本发明的教导下,其可根据临床治疗效果的需要,调整或者修改给药的次数和剂量。
在本发明的实施方案中,所述的哺乳动物优选地为人类。
经实验证明,本发明的他汀类局部单次用组合物经骨髓腔内给药可显著动员内源性内皮祖细胞,促进糖尿病大鼠后肢缺血、糖尿病大鼠皮肤缺损及大鼠大脑中动脉栓塞造成脑缺血模型的血管新生,有效减缓ApoE-/-小鼠动脉粥样硬化;并且,治疗缺血性疾病、改善微循环。
附图说明
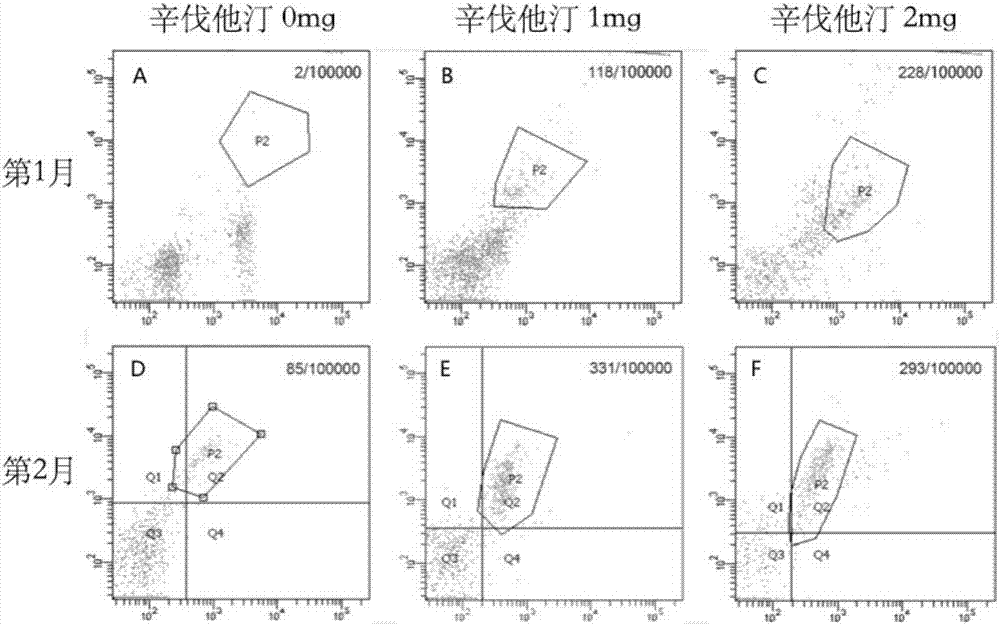
图1表示1型糖尿病大鼠胫骨内单次注射辛伐他汀长期动员内源性EPCs;A,B,C分别表示胫骨单次注射辛伐他汀(0,1,2mg)1个月后外周血中EPCs数目,D,E,F分别表示胫骨单次注射辛伐他汀(0,1,2mg)2个月后外周血中EPCs数目。
图2表示1型糖尿病大鼠后肢缺血模型胫骨内单次注射小剂量辛伐他汀动员内源性EPCs;
图3表示1型糖尿病大鼠后肢缺血模型口服大剂量辛伐他汀不能动员内源性EPCs;
图4表示1型糖尿病大鼠胫骨骨髓腔内局部单次注射小量辛伐他汀30天后,大鼠微循环显著改善;
图5表示1型糖尿病大鼠胫骨骨髓腔内局部单次注射小量辛伐他汀30天后,胰腺血管新生增多,侧枝循环显著改善;
图6表示1型糖尿病大鼠胫骨骨髓腔内局部单次注射小量辛伐他汀,系统性血管新生增加;
图7-1表示骨内注射辛伐他汀后血流恢复图;
图7-2表示骨内注射辛伐他汀后血流恢复比率统计图;
图8-1表示口服辛伐他汀后血流恢复图;
图8-2表示口服辛伐他汀后血流恢复比率统计图;
图9表示股动脉血管造影(A为骨内给药干预部分,B为口服给药干预部分);
图10表示腓肠肌相对湿重恢复比率;
图11表示胫骨内注射辛伐他汀促进1型糖尿病大鼠皮肤创面愈合;
图12表示ApoE-/-小鼠髓腔内单次注射辛伐他汀减少动脉粥样硬化斑块;图13表示胫骨内注射辛伐他汀改善成年大鼠MACo脑缺血。
具体实施方式
下面通过实施例来进一步说明本发明的可实施性,对于本领域的技术人员而言,根据现有技术的教导,在本发明实施方案的指导下,对其中的技术特征进行等同性修改或替换是显而易见的,仍然属于本发明请求保护的范围内。
制备例
辛伐他汀骨骼内用注射剂制备
将辛伐他汀1000mg溶解于PBS磷酸盐缓冲液10ml(购自北京中杉金桥生物技术有限公司),PBS溶液中含2%的二甲基亚砜(Dimethyl Sulfoxide,DMSO,购自Sigma公司)和0.1%牛血清白蛋白(Bovine Serum Albumin,BSA,购自Sigma公司),将所得到溶液均质,即得。
辛伐他汀骨骼内用温敏性水凝胶制备
泊洛沙姆407(BASF,Ludwigshafen,Germany)溶解于4℃预冷的磷酸盐缓冲液中(PBS,pH 7.4,4),最终泊洛沙姆的浓度为25%(w/w)。4℃静置过夜后形成澄清溶液。
辛伐他汀(National Institutes for Food and Drug Control,Beijing,China)加入已配制好的泊洛沙姆溶液中(4℃),搅拌均匀,得辛伐他汀最终浓度为0mg/ml、0.5mg/ml、1mg/ml。辛伐他汀/泊洛沙姆溶液(4℃)升高温度至室温即可得到水凝胶。
实施例1
1型糖尿病大鼠胫骨内单次注射辛伐他汀长期动员内源性EPCs
STZ诱导的1型糖尿病大鼠胫骨髓腔内单次局部单次注射辛伐他汀0mg、1mg、2mg,1月及2月后FACS检测外周血中EPCs数量,结果显示辛伐他汀组外周血EPCs数量显著增加(结果参见图1)。
实施例2
1型糖尿病大鼠后肢缺血模型胫骨内单次注射小剂量辛伐他汀与口服大剂量辛伐他汀动员内源性EPCs的比较
链脲佐菌素(STZ)诱导的1型糖尿病大鼠,将大鼠右侧股动脉切除1.0cm造后肢缺血模型。在大鼠左侧胫骨内分别注射0、0.5、1mg辛伐他汀,利用FACS动态观察EPCs数量。结果显示:胫骨内注射辛伐他汀后,与糖尿病后肢缺血模型组(T1DM Con)和载体组(SIM 0mg)相比,可以显著增加外周血中的EPCs数量(P<0.01)(结果参见图2)。但每天灌胃给予20mg/kg辛伐他汀,利用FACS动态观察EPCs数量结果显示,口服辛伐他汀后并没有显著增加外周血中的EPCs数量(结果参见图3)。结果提示骨内注射辛伐他汀可能与口服辛伐他汀引起的作用不同。
实施例2
糖尿病大鼠全身血管新生作用
链脲佐菌素(STZ)诱导的1型糖尿病大鼠胫骨骨髓腔内局部单次注射辛伐他汀0mg、1mg、2mg,干预后30天活体观察大鼠耳部血管,显示辛伐他汀组耳局部血管显著增多,侧枝循环增多(结果参见图4)。
大鼠处死前灌注12h后扫描micro-CT以观察胰腺局部血管数量,结果显示辛伐他汀组胰腺局部血管数量明显增多,侧枝循环增多,而糖尿病胰腺的血管新生将保护胰岛细胞(结果参见图5)。
C57小鼠胫骨内局部注射辛伐他汀0、1mg,4周后尾静脉注射Osteosense和Angiosense荧光探针,12h后利用小动物活体成像仪检测。结果显示:局部注射辛伐他汀4周后,注射部位成骨依然活跃,并且在肝脏、脾脏、肾脏及胰腺部位检测到较强的成血管信号(结果参见图6).
实施例3
胫骨内注射辛伐他汀促进1型糖尿病大鼠对侧后肢缺血的血管新生:
链脲佐菌素(STZ)诱导的1型糖尿病大鼠,将大鼠右侧股动脉切除1.0cm造后肢缺血模型。大鼠左侧胫骨内分别注射0,0.5,1mg辛伐他汀,利用超声多普勒血流仪动态观察血流恢复情况。结果显示:胫骨内注射辛伐他汀后,与糖尿病后肢缺血模型组(T1DM Con)和载体组(SIM 0mg)相比,显著加快血流恢复速度(P<0.01),最早可在第3天即可观测到血流部分恢复(结果参见图7-1,2)。
糖尿病大鼠后肢缺血模型每天灌胃给予0mg/kg或20mg/kg/d辛伐他汀,连续3周,口服辛伐他汀在观察时间内并没有显著加快血流恢复速度(结果参见图8-1,2)。
3周后灌注灌注micro-CT扫描,辛伐他汀骨内注射后股动脉两断端之间侧支循环明显增多,而口服辛伐他汀后股动脉两断端之间并没有观察到小血管生成(结果参见图9)。
实施例4
缺血侧腓肠肌湿重恢复比率检测
链脲佐菌素(STZ)诱导的1型糖尿病大鼠,将大鼠右侧股动脉切除1.0cm造后肢缺血模型。大鼠左侧胫骨内分别注射0,0.5,1mg辛伐他汀,4周后取腓肠肌称重。缺血侧腓肠肌湿重显示:糖尿病后肢缺血模型组及SIM 0mg对照组腓肠肌显著性萎缩(P<0.05),而局部注射辛伐他汀组腓肠肌未见明显萎缩(结果参见图10)。
实施例5
胫骨内注射辛伐他汀促进1型糖尿病大鼠皮肤创面愈合:
链脲佐菌素(STZ)诱导的1型糖尿病大鼠,利用皮肤取材器于大鼠背部造成直径12mm皮肤缺损。大鼠左侧胫骨内分别注射0,0.5mg辛伐他汀,利用数码相机隔天拍照观察缺损处恢复情况。结果显示:胫骨内注射辛伐他汀后,与糖尿病模型组(T1DM Con)和载体组(SIM 0mg)相比,可以显著加快皮肤缺损恢复速度(P<0.01),且效果明显优于口服大剂量辛伐他汀(20mg/kg/d)。免疫荧光进行新生血管染色也表明骨内注射辛伐他汀能明显增加缺损处的血管新生(结果参见图11)。
实施例6
ApoE-/-小鼠髓腔内单次注射辛伐他汀治疗动脉粥样硬化实验:
ApoE-/-小鼠高脂饲料诱导的动脉粥样硬化模型,在其左侧胫骨内单次注射辛伐他汀(0、0.5、1mg),在给药后8周后处死取材。对ApoE-/-小鼠的主动脉整体和主动脉根部连续切片油红O染色,图像分析软件计算比较斑块大小;血脂浓度进行检测;ELISA检测血中一氧化氮,骨桥蛋白及超敏C反应蛋白水平变化;FACS检测外周血EPCs数量。结果显示:ApoE-/-小鼠主动脉整体及主动脉根部油红O染色显示斑块显著减小;小鼠总胆固醇,甘油三酯及低密度脂蛋白胆固醇显著降低;血清一氧化氮浓度显著增加,骨桥蛋白及超敏C反应蛋白浓度均显著降低;外周血EPC数量显著增加(结果参见图12)。
实施例7
大鼠大脑动脉栓塞实验
在大鼠大脑中动脉栓塞(Middle Cerebral Artery Occlusion,MCAO)造成脑缺血的动物实验中,MCAO术后4小时大鼠胫骨单次注射辛伐他汀500ug,3天后microfill灌注,micro-CT扫描即可见实验组的侧枝循环血运重建明显高于对照组,TTC染色显示梗死面积明显小于对照组(结果参见图13)。
- 还没有人留言评论。精彩留言会获得点赞!