一种卤化II型聚酮类抗生素化合物、制备方法及其应用与流程
本发明涉及微生物领域,具体涉及一种卤化II型聚酮类抗生素化合物、制备方法及其应用。
背景技术:
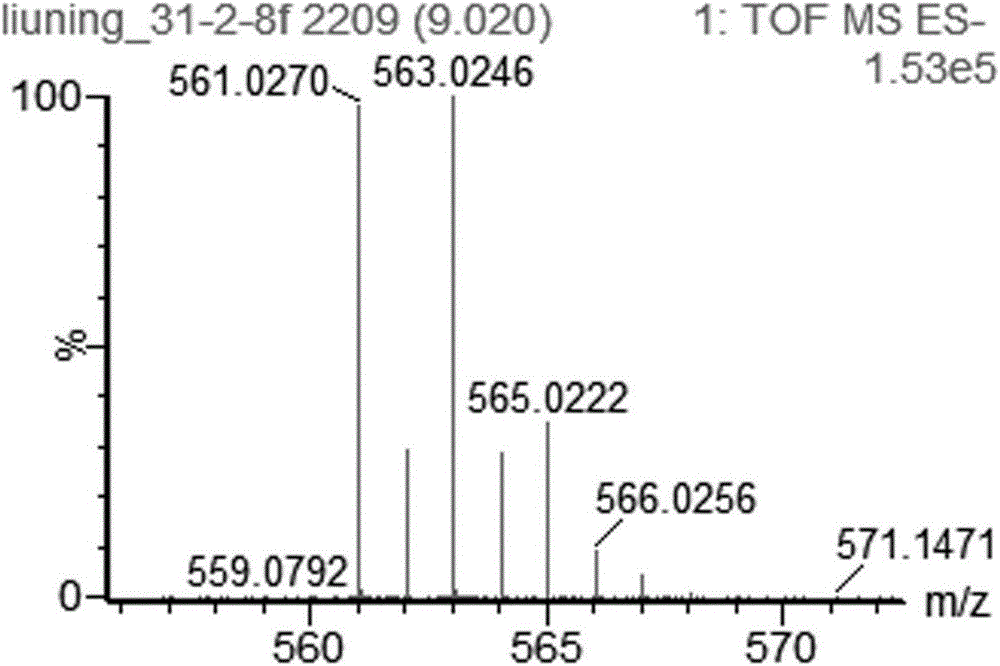
:随着抗生素的频繁使用和滥用导致许多微生物致病菌对抗生素产生耐药性,为许多疾病的治疗与预防带来极大困难,严重威胁人类的健康和生命的安全。世界卫生组织发布了抗生素耐药监测报告《抗生素耐药:全球检测报告》(AntimicrobialResistanceGlobalReportonSurveillance2014)客观阐述全球范围抗生素耐药情况,分析当前严峻形势,根据2014年报告数据显示:当下抗生素耐药情况十分严峻,一些耐药菌已经出现“无药可医”状况。2013年美国政府发布的《美国2013年抗生素耐药性威胁》(AntimicrobialResistanceThreatsintheUnitedStates,2013)的报告数据指出,耐碳青霉烯类肠杆菌每年导致至少9000人住院治疗,600人死亡;艰难梭菌引发严重的腹泻,每年导致25万的美国人住院,1.4万人死亡。因此,鉴于当前日益严峻的抗菌形势,加大抗生素研发力度,探索和研发新抗生素成为当务之急。技术实现要素:本发明要解决的技术问题是提供一种较强的抗耐药金黄色葡萄球菌的卤化II型聚酮类抗生素化合物。为了解决上述技术问题,本发明提供如下技术方案:卤化II型聚酮类抗生素化合物,结构为:该化合物具有ABX型的结构骨架类型。该化合物通过对链霉菌Streptomycessp.菌株(菌株保藏号:CGMCCNo.4.7321)发酵并分离得到,对革兰氏阳性细菌如金黄色葡萄球菌及其耐药菌具有很高的抑制活性,有望成为抗耐药金黄色葡萄球菌药物及其先导化合物而具有良好的药用开发前景。本发明提供的另一技术方案,卤化II型聚酮类抗生素化合物的制备方法,包括有CGMCC登记号码为CGMCCNo.4.7321的链霉菌。本发明提供的另一技术方案,卤化II型聚酮类抗生素化合物的应用,用作抗耐药金黄色葡萄球菌。附图说明图1为本发明化合物的红外光谱图;图2为本发明化合物的高分辨质谱图;图3为本发明化合物在MeOH-d4中的1H-NMR谱图;图4为本发明化合物在MeOH-d4中的13C-NMR谱图;图5为本发明化合物在MeOH-d4中的DEPT谱图;图6为本发明化合物在MeOH-d4中的HSQC谱图;图7为本发明化合物在MeOH-d4中的HMBC谱图;图8为本发明化合物在MeOH-d4中的H-HCOSY谱图;图9为本发明化合物在MeOH-d4中的ROESY谱图;图10为本发明化合物在MeOH-d4中的CD谱图;图11为化合物的抗耐药金黄色葡萄球菌活性实物图。所用链霉菌的保藏单位:北京的中国微生物菌种保藏管理委员会普通微生物中心(CGMCC);保藏编号:CGMCCNo.4.7321;保藏时间:2016年06月02日。具体实施方式链霉菌是产活性天然产物的主要来源,目前临床应用的抗生素约2/3来源于该属。特别是卤化天然产物具有结构新颖的特点,使卤化产物成药潜力增大,已经发现已经有6000余种具有结构多样的卤化天然产物。它们中很大一部分具有抗生素的活性。由于卤化产物在对抗耐药菌感染方面有较大的临床应用潜力,如临床上抗感染的万古霉素,替考拉宁以及2014年美国FDA批准上市的抗耐药菌感染抗生素新药达巴万星,奥利万星及泰地唑胺,它们都属于卤化天然产物。本发明人从一株CGMCC4.7321链霉菌Streptomycessp.次级代谢产物中分离一个Anthrabenzoxocinones类抗生素,经紫外光谱、红外光谱、高分辨质谱、圆二色谱及核磁共振等波谱数据仔细分析,确定为Anthrabenzoxocinones类的新氯化产物。对Anthrabenzoxocinones新氯化物进行活性评价,该化合物具有较强的抗耐药金黄色葡萄球菌。因此,该化合物有望成为抗耐药金黄色葡萄球菌药物及其先导化合物而具有良好的药用开发前景。CGMCCNo.4.7321链霉菌:1)、生物学命名、分类依据:经16SrRNA保守引物(27f/1492r)扩增,测序并在线比对分析和参考菌株StreptomycessparsogenesstrainNBRC13086的同源性为99%,初步分类为链霉菌。命名为:链霉菌Streptomycessp.2)、保藏单位:北京的中国微生物菌种保藏管理委员会普通微生物中心(CGMCC);3)、保藏编号:CGMCCNo.4.7321;4)、保藏时间:2016年06月02日;5)、保藏地点:北京市朝阳区北辰西路1号院3号:中国科学院微生物研究所;6)、特征:i.气生菌丝发达,米黄色菌落,边缘粗糙,有皱褶;孢子数目偏少;mol%G+C=73%。分离培养基:ii.固体GYM(ISP2):葡萄糖4g,麦芽抽提物4g,酵母粉10g,碳酸钙2g,琼脂粉18g,加水至1000毫升,灭菌。iii.建议培养条件:固体GYM培养基:最适培养温度28℃,建议培养时间:4天。iv.16sRNA序列为:TGCAGTCGAACGATGAAGCCGCTTCGGTGGTGGATTAGTGGCGAACGGGTGAGTAACACGTGGGCAATCTGCCCTGCACTCTGGGACAAGCCCTGGAAACGGGGTCTAATACCGGATATGACCTGGTGAGGCATCTTACTGGGTGGAAAGCTCCGGCGGTGCAGGATGAGCCCGCGGCCTATCAGCTTGTTGGTGGGGTGATGGCCTACCAAGGCGACGACGGGTAGCCGGCCTGAGAGGGCGACCGGCCACACTGGGACTGAGACACGGCCCAGACTCCTACGGGAGGCAGCAGTGGGGAATATTGCACAATGGGCGAAAGCCTGATGCAGCGACGCCGCGTGAGGGATGACGGCCTTCGGGTTGTAAACCTCTTTCAGCAGGGAAGAAGCGCAAGTGACGGTACCTGCAGAAGAAGCGCCGGCTAACTACGTGCCAGCAGCCGCGGTAATACGTAGGGCGCAAGCGTTGTCCGGAATTATTGGGCGTAAAGAGCTCGTAGGCGGCTTGTCACGTCGGATGTGAAAGCCCGGGGCTTAACCCCGGGTCTGCATTCGATACGGGCAGGCTAGAGTTCGGTAGGGGAGATCGGAATTCCTGGTGTAGCGGTGAAATGCGCAGATATCAGGAGGAACACCGGTGGCGAAGGCGGATCTCTGGGCCGATACTGACGCTGAGGAGCGAAAGCGTGGGGAGCGAACAGGATTAGATACCCTGGTAGTCCACGCCGTAAACGTTGGGAACTAGGTGTGGGCGACATTCCACGTTGTCCGtGCCGCAGCTAACGCATTAAGTTCCCCGCCTGGGGAGTACGGCCGCAAGGCTAAAACTCAAaGgAATTGACGGGGGCCCGCACAAGCGGCGGAGCATGTGGCTTAATTCGACGCAACGCGAAGAACCTTACCAAGGCTTGACATACATCGGAAACATCCAGAGATGGGTGCCCCCTTGTGGTCGGTGTACAGGTGGTGCATGGCTGTCGTCAGCTCGTGTCGTGAGATGTTGGGTTAAGTCCCGCAACGAGCGCAACCCTTGTTCTGTGTTGCCAGCATGCCCTTCGGGGTGATGGGGACTCACAGGAGACTGCCGGGGTCAACTCGGAGGAAGGTGGGGACGACGTCAAGTCATCATGCCCCTTATGTCTTGGGCTGCACACGTGCTACAATGGCCGGTACAATGAGCTGCGATACCGCGAGGTGGAGCGAATCTCAAAAAGCCGGTCTCAGTTCGGATTGGGGTCTGCAACTCGACCCCATGAAGTCGGAGTCGCTAGTAATCGCAGATCAGCATTGCTGCGGTGAATACGTTCCCGGGCCTTGTACACACCGCCCGTCACGTCACGAAAGTCGGTAACACCCGAAGCCGGTGGCCCAACCCCTTGTGGAGGGAGTC。7)、分离地点:贵州省梵净山自然保护区(海拔高度800m,东经108°47′50″,北纬27°56′32″)。以下为本发明抗生素化合物的具体制备方法、化合物的确认及其应用的确定。一、本发明的抗生素化合物的制备方法为:1、发酵培养将生长斜面的链霉菌Streptomycessp.菌株接种于种子培养基,种子培养基为GYM固体培养基,(GYM固体培养基的制备方法为:用葡萄糖4g、麦芽抽提物4g、酵母粉10g、碳酸钙2g、微量元素预混液0.5mL和1.8%琼脂粉(w/v),加入去离子水定容到1.0L,121℃高压灭菌30min制成),28℃培养48小时,然后接种到发酵培养基(配方与种子培养基相同),在28℃培养17天。2、提取分离将上述的发酵培养基连同菌体捣碎,加入乙酸乙酯在旋转摇床(160rpm)提取24小时,连续提取三次,利用旋转蒸发仪在45℃回收乙酸乙酯溶剂,得到发酵物粗提物32g。发酵物粗提物32g,正相硅胶柱层(硅胶100-200目,1.5Kg硅胶颗粒),洗脱溶剂氯仿:丙酮(100%、95%、90%、80%、67%、50%、33%、0%)依次洗脱,将氯仿-丙酮为80%(v/v)的洗脱部分再经过葡聚糖凝胶SephadexLH-20柱层析,100%甲醇洗脱得到的组分Ⅰ再经过硅胶柱层析(100-200目),石油醚:乙酸乙酯(v/v)洗脱,依次按以上顺序洗脱,石油醚:乙酸乙酯(v/v)=10:1的洗脱部分再经过HPLC95%甲醇等度洗脱制备得化合物。二、化合物的结构鉴定为浅黄色粉末,易溶于甲醇,二甲亚砜等有机溶剂,如图1所示,化合物的红外光谱显示,其红外吸收3442cm-1和1680cm-1表明该化合物有羟基及羰基基团存在,此外红外吸收峰1603-1cm及1548cm-1,该化合物还含有苯环结构。如图2所示,化合物的高分辨质谱显示,其高分辨负离子峰荷质比561.0270和563.0246,暗示该化合物有分子式为C27H21Cl3O7。如图4、图5、图6所示,在13CNMR和DEPT谱以及HSQC谱中显示,化合物具有三个苯环,其碳质子吸收信号分别为159.6,157.4,157.1,153.0,152.6,150.7,146.4,142.4,133.4,122.1,117.9,115.6,113.6,112.3,109.7,107.9,107.8和101.7;此外该化合物还含有一个羰基基团,其信号在190.8;一个亚甲基(δC:39.7);四级碳原子(δC:39.4,98.3);结合13HNMR核磁谱中化合物具有2个苯环单峰氢质子信号[δH:6.86(1H,s),6.27(1H,s)];四个甲基峰信号[2.49(3H,s),1.79(3H,s),1.69(3H,s),1.60(3H,s)];结合文献调研表明该化合物具有ABX聚型骨架。该化合物与ABX骨架不同在于,它苯环上的三个氢质子被氯原子取代。如图7、图8和图9所示,HMBC谱、H-HCOSY谱图和ROSEY谱图上,氢信号6.86(1H,s)与碳信号112.3和122.1相关,证明该质子连接在ABX骨架的C-8位;δH6.17(1H,s)与δC113.6,115.7,133.4,150.7和152.6相关,证明了质子6.17(1H,s)连接在C-4位上;最后质子信号6.13(1H,s)有一个关键相关信号,它与碳信号98.4相关确定该质子连接在C-16位上。综合以上信息,可以确定氯原子在苯环上取代位置,3个氯原子分别取代了4,10以及12位上的氢原子,综合上述信息可以推断出该化合物的平面结构。如图10所示,通过CD谱图可以确定化合物的绝对构型,CD谱图显示在239nm及282nm具有明显的正科顿效应,根据陈海燕等人的报道,表明该化合物C-16及C-6构型为S,由此确定该化合物的结构为:和化合物在MeOH-d4中的NMR数据如表1所示。系统命名该化合物为:(6s,16s)-4,10,12-trichloroanthrabenzoxocinone,由于此化合物为本发明人的首次发现,因此,发明人将次化合物命名为zunyimycinC。其二维立体表示为:表1NO.1H13C1133.426.27(1H,s)101.73150.74113.64a152.65698.373.04-3.11(2H,m)39.77a142.486.86(1H,s)117.98a146.4939.49a153.010107.911159.612107.813157.413a109.714190.814a112.315157.115a122.1166.10(1H,s)65.716a115.61-CH32.49(3H,s)15.86-CH31.60(3H,s)26.29-CH31.79(3H,s)27.59-CH31.69(3H,s)27.8三、化合物的应用确定采用纸片法对命名为zunyimycinB的该化合物进行抗菌活性测试,以耐药鲍曼不动杆菌、耐药大肠杆菌、耐药肺炎克雷伯杆菌、耐药金黄色葡萄球菌为测活菌,甲醇和丙酮为阴性对照。结果如图11所示,3为本发明的化合物,1、2为其他两种化合物;4为丙酮;5为甲醇,表明,本发明的化合物均对耐药金黄色葡萄球菌具有抑制作用,抑菌圈直径为1.8mm。对于本领域的技术人员来说,在不脱离本发明技术方案的前提下,还可以作出若干变形和改进,这些也应该视为本发明的保护范围,这些都不会影响本发明实施的效果和专利的实用性。当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1