检测白血病CDX2基因表达水平的引物和方法与流程
本发明涉及一种临床检验用途的基因检测方法和分子检测引物,采用探针实时荧光定量PCR技术,能够对人类白血病中的CDX2表达水平进行检测,可有效的节约检测时间,提高检测精度。
背景技术:
白血病是一类造血干细胞发育异常的恶性克隆性疾病,随着我国经济的发展,环境污染的加剧及生活方式的改变,白血病的发生率呈现升高的趋势,尤其是在35岁以下中青年人群及儿童中白血病的发病率和死亡率居高不下。白血病的预后一般较差,没有较好的预防和控制措施,病死率高。目前认为,白血病微小残留病灶(minimal residual disease,MRD)是白血病复发及治疗失败的根本原因。MRD作为独立的预后因素,不仅对评价化疗的疗效、监测白血病复发的意义重大,在指导危险分层后的个体化治疗中亦发挥重要作用。
尾侧型同源盒基因CDX2(caudal-related homeodomin transcription factor2,CDX2)基因是CDX基因家族的一员,作为一种原癌基因,CDX2全长共22kb,定位于13号染色体q12.13,由2个内含子和3个外显子构成,其下游表达的CDX2蛋白通过螺旋环螺旋形式与相应的DNA区域结合,共含有311个单个氨基酸,作为转录因子来调控DNA的表达。正常情况下,CDX2在胎儿期广泛表达,在整个成人期则仅在肠道腺上皮中表达。研究证实CDX2的异常表达与肠化生Barrett食管及胃癌的发生、发展及预后有关,并具有抑制结肠肿瘤的作用。CDX2并不局限于在消化道表达,在泌尿生殖、妇科、头颈部等也显示不同程度的表达。近年来的研究发现CDX2基因参与了干细胞自我更新和白血病转化,通过影响HOX基因表达调控促成白血病的发生,是与白血病发生、发展密切相关的致白血病基因,在大多数的AML、ALL患者中CDX2有不同程度的异常表达。
在实际应用中,用于检测CDX2表达的方法主要为免疫组化,尽管该法原理简单,但是试验过程过于繁琐,需要的试剂种类繁多,且试验结果需要经验丰富的专家来判读,判读结果存在较大的主观性,一定程度上限制了该法的应用。正是因为免疫组化法存在这些问题,才促使我们探索新的方法来检测CDX2表达水平。
实时荧光定量PCR法具有较高的灵敏度和特异性,而且能对PCR进行实时在线检测,反应CDX2在组织中的初始含量,试验节约了大量的检测时间,还避免了遗留污染的发生。常见的方法有SYBR Green I染料法,双探针杂交法以及Taqman技术等。其中SYBR Green I由于是非饱和染料,特异性不如双探针杂交法以及Taqman法,必须通过观察溶解曲线来判断其特异性;而双探针法杂交法成本又较为昂贵。因此本研究采用实时荧光PCR技术结合Taqman探针法应用于CDX2基因检测。
技术实现要素:
本发明设计了利用内参/目的基因用引物、探针序列,用荧光定量PCR技术检测CDX2基因。通过调整两个基因的引物探针浓度及比例,优化PCR的反应体系和反应条件,并以正常人的CDX2表达量作为参照,开发了一种新型的CDX2基因表达水平检测方法。用于白血病辅助诊断及MRD监测的检验方法,主要包括红细胞裂解液;TRIzol;氯仿;异丙醇;无水乙醇;QIAGEN RNeasy FFPE Kit。
本发明提供了一种检测CDX2基因相对表达量的引物和探针,包括:扩增覆盖CDX2基因的上下游引物CDX2-F、CDX2-R和探针CDX2-Probe,检测内参基因Abl用引物Abl-F、Abl-R和探针Abl-Probe;其碱基序列为:
CDX2-F:GAACCTGTGCGAGTGGAT
CDX2-R:TGATGTAGCGACTGTAGTGA
CDX2-Probe:FAM-CAGTCCCTCGGCAGCCAAGTGA-TAMRA
Abl-F:GATACGAAGGGAGGGTGTACCA
Abl-R:CTCGGCCAGGGTGTTGAA
Abl-Probe:FAM-TGCTTCTGATGGCAAGCTCTACGTCTCCT-TAMRA。
本发明还提供了一种检测CDX2基因相对表达量的方法,其包括如下步骤:
(1)提取血液中的总RNA;
(2)将RNA反转为cDNA;
(3)利用CDX2基因扩增的上下游引物CDX2-F、CDX2-R和探针CDX2-Probe,检测内参基因Abl用引物Abl-F、Abl-R和探针Abl-Probe对步骤(2)中的cDNA分别进行扩增;
其中检测CDX2基因的引物和探针,分别为:
CDX2-F:GAACCTGTGCGAGTGGAT
CDX2-R:TGATGTAGCGACTGTAGTGA
CDX2-Probe:FAM-CAGTCCCTCGGCAGCCAAGTGA-TAMRA
检测Abl内参基因的引物和探针,分别为:
Abl-F:GATACGAAGGGAGGGTGTACCA
Abl-R:CTCGGCCAGGGTGTTGAA
Abl-Probe:FAM-TGCTTCTGATGGCAAGCTCTACGTCTCCT-TAMRA。
进一步的,还包括阳性对照品的扩增和阴性对照品的扩增。
本发明还提供一种检测CDX2基因相对表达量的试剂盒,包括PCR反应液,其特征在于,所述PCR反应液包括CDX2基因扩增的上、下游引物CDX2-F、CDX2-R和探针CDX2-Probe,检测内参基因Abl用引物Abl-F、Abl-R和探针Abl-Probe;
其中检测CDX2基因的引物和探针,分别为:
CDX2-F:GAACCTGTGCGAGTGGAT
CDX2-R:TGATGTAGCGACTGTAGTGA
CDX2-Probe:FAM-CAGTCCCTCGGCAGCCAAGTGA-TAMRA
检测Abl内参基因的引物和探针,分别为:
Abl-F:GATACGAAGGGAGGGTGTACCA
Abl-R:CTCGGCCAGGGTGTTGAA
Abl-Probe:FAM-TGCTTCTGATGGCAAGCTCTACGTCTCCT-TAMRA。
进一步的还包括红细胞裂解液、TRIzol;氯仿;异丙醇;无水乙醇等试剂、逆转录试剂试剂及阳性对照品和阴性对照品。
本发明的有益效果:本发明将实时荧光PCR技术结合采用Tapman探针,利用双标准曲线的方法,分别构建内参基因ABL和CDX2目的基因的定量标准曲线,检测受测者体内CDX2的相对于内参基因的表达水平。相比于以往的免疫组化方法和现今流行的△△CT法,该试剂方法和试剂盒具有精度高,结果便于判读等优点。加之该试剂盒将反应体系所需的引物、探针进行合理配比和优化,使实验条件达到最佳,从而省去了繁琐的条件摸索环节,大大提升了实验效率。该试剂盒经测试特异性好,灵敏度高,操作简便。有助于临床上白血病的早期诊断及微小残留病灶(MRD)的监测,对于及时干预治疗、调整治疗方案、评价治疗效果、预测预后、预防临床复发都具有重要意义。
附图说明
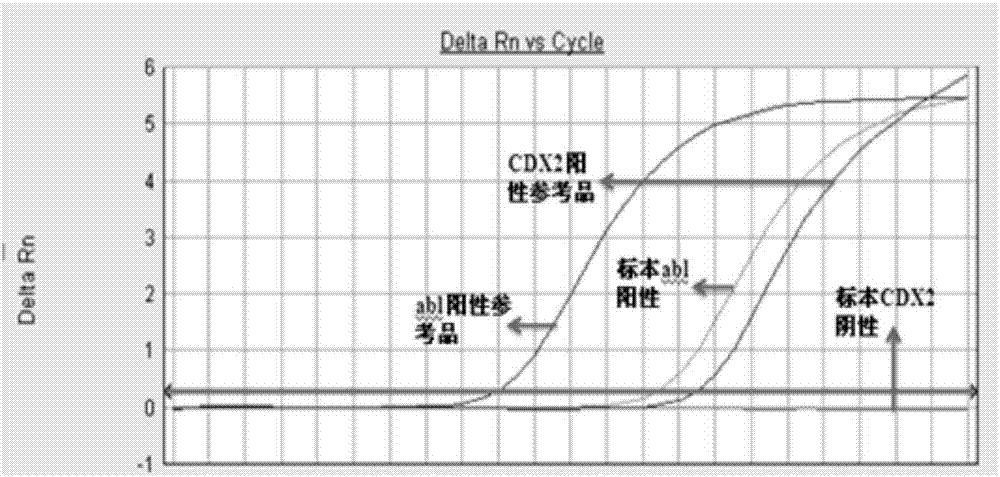
图1是灵敏度检测结果图。
图2是阴性样品的结果图。
图3是阳性样品的结果图。
具体实施方式
下面结合具体实施例和附图,进一步阐述本发明。应当注意的是,实施例中未说明的常规条件和方法,通常按照所属领域实验人员常规采用方法:譬如,奥斯柏和金斯顿主编的《精编分子生物学实验指南》第四版,或者按照制造厂商所建议的步骤和条件。
本发明用于辅助临床上白血病(leukemia)的早期诊断、早期预防及高危人群筛选的方法。主要包括以下试剂:红细胞裂解液;TRIzol;氯仿;异丙醇;无水乙醇;QIAGEN RNeasy FFPE Kit。
检测体系PCR反应液:THUNDERBIRD qPCR MIX(TOYOBO,QPS-101)、检测目的基因用上下游引物CDX2-F,CDX2-R,探针为CDX2-Probe,检测内参基因Abl用引物为Abl-F,Abl-R,探针为Abl-Probe以及阳性对照品和阴性对照品。
其中检测CDX2基因的引物和探针,分别为:
CDX2-F:GAACCTGTGCGAGTGGAT
CDX2-R:TGATGTAGCGACTGTAGTGA
CDX2-Probe:FAM-CAGTCCCTCGGCAGCCAAGTGA-TAMRA
检测Abl内参基因的引物和探针,分别为:
Abl-F:GATACGAAGGGAGGGTGTACCA
Abl-R:CTCGGCCAGGGTGTTGAA
Abl-Probe:FAM-TGCTTCTGATGGCAAGCTCTACGTCTCCT-TAMRA
阳性对照品:含CDX2基因组的溶液;
阴性对照品:不含CDX2基因组的溶液。
所述上游引物定位于该基因第一外显子,下游引物定位于第二两个外显子,探针跨越第一、第二两个外显子,对目的基因的扩增及检测具有极高的特异性;此外这段引物的PCR产物长度为146bp,片段长度小,探针法检测可得到较好的结果。
实施例2
本发明方法的操作流程:
(1)抽提血液中的总RNA:在洁净的1.5ml的离心管中加入1ml红细胞裂解液,取抗凝血0.5ml混匀。室温静置10min;1500rpm离心5min,弃上清,收集底部的细胞;再次加入0.5ml红细胞裂解液,1500rpm离心5min,弃上清,收集底部的细胞;向细胞中加入1ml TRIzol,反复吹打直至沉淀完全溶解,室温静止5min;加入0.2ml氯仿,震荡均匀;14000rpm 4℃离心10min,吸取上清层转移至另一新的离心管中;加入等体积的异丙醇,上下充分混匀,室温静置10min;14000rpm 4℃离心10min,弃上清,加入75%乙醇1ml,轻轻上下颠倒洗涤管壁;14000rpm 4℃离心5min,弃乙醇;室温干燥10-15min,加入20ulRNase-free水溶解沉淀。
(2)参考TOYOBO公司的Rever Tra Ace qPCR RT Kit试剂盒说明书,将RNA反转为cDNA。
(3)试剂配置:按检测人份数配置检测体系PCR反应液各XμL,每人份23μL分装:
X=23μL反应液×(8份内参(标准曲线)+8份目的基因(标准曲线)+n份标本+1份阳性对照+1份阴性对照+1份空白对照);
(4)加样:加入检测体系PCR反应液中2μL cDNA;阳性对照和阴性对照直接加2μL阳性对照品和阴性对照品;空白对照加2μL生理盐水或不加任何物质。
(5)检测:检测在实时荧光PCR仪上进行,可用仪器包括ABI7300,7500(美国Applied Biosystems公司)等。反应条件:95℃预变性1min;95℃15s,58℃35sec40个循环,荧光信号于58℃35sec时采集。
(6)结果判断:将阈值线调整至背景信号及阴性扩增线以上,系统根据标准曲线和CT值自动计算出拷贝数。
1)内参阳性时,检测结果才认为有效;
2)阳性判断标准:Ct<36,为阳性;35≤Ct≤38,为疑似阳性,需要再次验
证;Ct>38,为阴性。
实施例3本发明灵敏度检测
以质粒浓度为100、10、1copies/μL作为模板进行实验,每个浓度重复10次,同时设置一个空白对照。结果发现本发明的检测下线为10copies,具体见表1和图1。
表1本发明灵敏度检测结果
实施例4采用本发明所述检测方法检测健康人群标本
取待检的健康体检样品20例,按实施例2所述方法提取基因组、配制试剂并检测。
每份样品加入检测体系PCR反应液中2μL。同时做阳性,阴性,空白对照,内参基因/目的基因的标准曲线各一份。一台96孔的荧光PCR仪可同时检测20份样品,每个样本2次重复,一份阳性对照,一份阴性对照和一份空白对照,检测时间仅为100分钟。20例筛查样本中所有样本的abl均起线,但CDX2未有标本出现起线。结果如表2所示,样品1的检测结果图见图2。
表2 20例健康体检样本CDX2mRNA表达水平
实施例5采用本发明所述检测方法检测临床标本
取待检的临床样品20例,按实施例2所述方法提取基因组、配制试剂并检测。
每份样品加入检测体系PCR反应液中2μL。同时做阳性,阴性,空白对照,内参基因/目的基因的标准曲线各一份。一台96孔的荧光PCR仪可同时检测20份样品,每个样本2次重复,一份阳性对照,一份阴性对照和一份空白对照,检测时间仅为100分钟。20例筛查样本中所有样本的abl均起线,其中有6例出现CDX2阳性表达。实验结果如下表3所示,样品3的检测结果见图3。
表3 20例临床样本CDX2mRNA表达水平
SEQUENCE LISTING
<110> 福州艾迪康医学检验所有限公司
<120> 检测白血病CDX2基因表达水平的引物和方法
<130>
<160> 6
<170> PatentIn version 3.5
<210> 1
<211> 18
<212> DNA
<213> 人工序列
<400> 1
gaacctgtgc gagtggat 18
<210> 2
<211> 20
<212> DNA
<213> 人工序列
<400> 2
tgatgtagcg actgtagtga 20
<210> 3
<211> 22
<212> DNA
<213> 人工序列
<400> 3
cagtccctcg gcagccaagt ga 22
<210> 4
<211> 22
<212> DNA
<213> 人工序列
<400> 4
gatacgaagg gagggtgtac ca 22
<210> 5
<211> 18
<212> DNA
<213> 人工序列
<400> 5
ctcggccagg gtgttgaa 18
<210> 6
<211> 29
<212> DNA
<213> 人工序列
<400> 6
tgcttctgat ggcaagctct acgtctcct 29
- 还没有人留言评论。精彩留言会获得点赞!
- 玉米低镁条件下特异性转运镁离子基因ZmMGT10及其应用的制造方法与工艺
- CRISPR‑Cas9特异性敲除猪SLA‑3基因的方法及用于特异性靶向SLA‑3基因的sgRNA与制造工艺
- 毛酸浆的分子特异性标记引物及鉴别方法与制造工艺
- 一种检测CYP2C9基因多态性的ARMS引物的制造方法与工艺
- 构建在海马体区域特异性敲除IKKα基因的小鼠模型的方法及打靶载体和试剂盒与制造工艺
- 使用重叠非等位基因特异性引物和等位基因特异性阻断剂寡核苷酸的组合物进行等位基因特异性扩增的制造方法与工艺
- 一种利用线粒体D-loop区特异区域鉴定鼋的标记引物及方法
- 一种用于检测大豆拟茎点种腐病菌的特异性lamp引物组合物及其应用
- 一种针对膨胀污泥中Eikelboom Type 0092型丝状菌群特异性引物和方法
- 脯氨酸特异性蛋白酶基因及其应用
- 一组小熊猫基因的微卫星引物的制作方法与工艺
- 羊肚菌交配型决定基因鉴定专用引物及出菇能力预测方法与流程
- 一种KRAS基因的检测引物组、其构成的反应体系及应用的制作方法与工艺
- MTHFR‑A1298C基因多态性快速检测引物、分子信标、试剂盒及检测方法与流程
- 用于检测人类VKORC1与CYP2C9基因多态性的引物、探针、试剂盒及方法与流程
- 一种牛卷毛基因快速筛选的引物、方法及试剂盒与流程
- KCNQ1OT1基因、aHIF基因及其引物的应用以及用于诊断冠心病的试剂盒的制作方法与工艺
- 用于检测人类ALDH2基因多态性的引物、探针、试剂盒及方法与流程
- 一种检测耳聋基因的引物及其应用的制造方法与工艺
- 海岛棉跨膜蛋白基因、引物及其应用的制造方法与工艺
- 一种KRAS基因的检测引物组、其构成的反应体系及应用的制作方法与工艺
- MTHFR‑A1298C基因多态性快速检测引物、分子信标、试剂盒及检测方法与流程
- 用于检测人类VKORC1与CYP2C9基因多态性的引物、探针、试剂盒及方法与流程
- 一种牛卷毛基因快速筛选的引物、方法及试剂盒与流程
- KCNQ1OT1基因、aHIF基因及其引物的应用以及用于诊断冠心病的试剂盒的制作方法与工艺
- 用于检测人类ALDH2基因多态性的引物、探针、试剂盒及方法与流程
- 一种检测耳聋基因的引物及其应用的制造方法与工艺
- 海岛棉跨膜蛋白基因、引物及其应用的制造方法与工艺
- 区分动物肌肉蛋白TNNC1基因的引物及其应用的制造方法与工艺
- MTRR基因多态性快速检测的引物、分子信标、试剂盒及其检测方法与流程