抗HCV广谱中和抗体的制备、检测以及应用的制作方法
本发明本发明属于细胞免疫学、基因工程领域,涉及一种抗hcv广谱中和抗体的制备、检测以及应用。
背景技术:
:丙型肝炎病毒(hepatitiscvirus,hcv)为单股正链rna包膜病毒,属于黄病毒科、噬肝病毒属,主要经血液传播,可造成急、慢性病毒性肝炎、肝硬化,继而发展成肝细胞癌。据报道病史20年以上的慢性丙型肝炎患者,肝硬化的年发生率为10%~15%,而每年约有1-7%的肝硬化患者发展为肝癌。hcv感染呈全球性分布,我国属hcv中度感染区。中国2016年最新报告的丙型肝炎的发病人数约为20万,发病率为15%。因此,加强hcv的基础研究,开发治疗hcv药物及诊断试剂,为保障我国人民的身体健康具有重要的意义。丙型肝炎病毒感染后可在机体内合成及复制自身成分,不断形成新的子代病毒,从而导致机体针对hcv感染产生特异性免疫应答。丙型肝炎病毒感染的实验室诊断主要包括血清学诊断、hcv核酸诊断。其中,hcv血清学诊断包括hcv抗体诊断和hcv抗原诊断;hcv核酸诊断主要是hcvrna的定性和定量检测。在临床上,主要是根据临床表现和实验室检查进行hcv确诊hcv抗病毒治疗的目的是清除或持续抑制体内的hcv,以降低肝损伤,恢复肝功能,阻止其进展为肝纤维化、肝硬化、肝功能衰竭或肝癌,并提高患者的生活质量。目前世界多国广为使用的治疗方案是乙二醇干扰素α与利巴韦林的联合治疗,但其对基因2型和3型的svr率为75%~90%,但对基因1型和4型的svr率很低,仅为45%和52%。这两种药联合治疗有很多严重的副作用和禁忌症,复发率较高,并且价格昂贵。因此,对现有治疗方案的改进和对新的安全有效的药物的开发对于临床治疗就尤为必要和重要了。近年来,抗体在hcv感染中的作用开始受到重视,研究表明,抗体在阻断hcv颗粒与受体分子的结合、或通过中和抑制病毒进入细胞方面表现出极大的潜力。虽然有hcv抗体类药物正在进行临床或临床前实验,但是目前进入临床前研究的抗体数量还很少。有必要开展更多的研究,尽可能的挖掘抗hcv抗体的治疗潜力,为丙肝患者的抗病毒治疗提供更多的选择。技术实现要素:为了弥补现有技术的不足,本发明的目的在于,提供一种全人源的抗hcv的广谱中和抗体,以及所述抗体在检测hcv和制备治疗hcv感染引起的疾病的药物中的应用。为了实现上述目的,本发明采用如下技术方案:本发明提供了一种抗hcv广谱中和抗体,所述抗体重链可变区包含至少一个含有三个cdr的重链可变区和至少一个含有三个cdr的轻链可变区;其中所述重链可变区包含:(1)vhcdr1,其氨基酸序列为seqidno.1;(2)vhcdr2,其氨基酸序列为seqidno.2;(3)vhcdr2,其氨基酸序列为seqidno.3;其中所述轻链可变区包含:(4)vlcdr1,其氨基酸序列为seqidno.5;(5)vlcdr2,其氨基酸序列为seqidno.6;(6)vlcdr2,其氨基酸序列为seqidno.7。进一步,所述抗体具有seqidno.4所示的vh结构域,和/或seqidno.8所示的vl结构域。进一步,所述抗体包含抗体重链恒定区和/或抗体轻链恒定区的全部或者部分。进一步,所述抗体是抗体的抗原结合片段。进一步,所述抗体被附着到至少第二诊断剂或治疗剂。本发明提供了一种组合物,所述组合物包括上面所述的抗体或上面所述抗体的免疫轭合物。所述免疫轭合物包括上面所述的抗体,所述免疫轭合物附着到至少第二治疗剂或诊断剂。其中,所述抗体被附着到至少放疗药剂、化疗药剂、抗-血管生成药剂、细胞凋亡-诱导药剂、抗-微管蛋白药剂、抗-细胞或者细胞毒性药剂、类固醇、细胞因子拮抗剂、细胞因子表达抑制剂、趋化因子拮抗剂、趋化因子表达抑制剂、三磷酸腺苷酶抑制剂、抗炎药剂、信号传导途径抑制剂、抗-癌症药剂、其它抗体、凝血剂或抗病毒剂。所述抗病毒剂选自由核苷、核苷逆转录酶抑制剂、非核苷逆转录酶抑制剂和蛋白酶抑制剂。进一步,所述组合物是药学上可接受的组合物。本发明提供了一种克隆或表达载体,所述克隆或表达载体包含一种或多种dna序列,所述dna序列编码上面所述的抗体的重链和/或轻链。本发明的dna序列可包括例如通过化学处理产生的合成dna、cdna、基因组dna或其任何组合。编码本发明的抗体分子的dna序列可由本领域技术人员熟知的方法来获得。例如,编码部分或全部抗体重链和轻链的dna序列可按需要从确定的dna序列或基于对应的氨基酸序列来合成。编码受体框架序列的dna对于本领域技术人员是广泛可得的并且可基于其已知的氨基酸序列来容易地合成。分子生物学的标准技术可用于制备编码本发明的抗体分子的dna序列。所需dna序列可完全或部分地利用寡核苷酸合成技术合成。可适当地采用定点诱变和聚合酶链式反应(pcr)技术。本发明提供了一种宿主细胞,所述宿主细胞包括上面所述的抗体的重链和/或轻链的dna序列或上面所述的克隆或表达载体。在本发明中,任何适当的宿主细胞/载体系统可用于编码本发明的抗体分子的dna序列的表达。可使用细菌(例如大肠杆菌)及其它微生物系统,或还可使用真核生物(例如哺乳动物)宿主细胞表达系统。适当的哺乳动物宿主细胞包括cho、、293细胞、骨髓瘤或杂交瘤细胞。本发明提供了上面所述的抗体在制备治疗hcv引起的疾病的药物组合物或检测hcv的工具中的应用。所述疾病包括(但不限于)肝炎、肝硬化、肝功能衰竭或肝癌。进一步,所述工具包括试剂盒、试纸、芯片等。其中,所述芯片包括蛋白质芯片;所述蛋白质芯片包括固相载体以及固定在固相载体的上述单克隆抗体;所述蛋白免疫检测试剂盒;所述蛋白免疫检测试剂盒包括上述单克隆抗体。如所属领域的技术人员应理解的,术语“抗体”包括的免疫结合试剂扩展到所有抗体和其抗原结合片段,包括整个抗体、二聚、三聚和多聚抗体;双特异性抗体;嵌合抗体;重组和工程抗体,和其片段。术语“抗体”因此用于指任何具有抗原结合区的抗体类分子,并且该术语包括组成抗原结合域的抗体片段,例如fab’,fab,f(ab’)2,单域抗体(dab),tandabs二聚体、fv,scfv(单链fv),dsfv,ds-scfv,fd,线性抗体,微型抗体(minibodies),二价抗体(diabodies),双特异性抗体片段,二抗体(bibody),三抗体(tribody)(scfv-fab融合,分别为双特异性或三特异性);sc-二价抗体(sc-diabody);κ(λ)抗体(kappa(lamda)bodies)(scfv-cl融合);双特异性t细胞衔接器(engager(bite))(scfv串联以吸引t细胞);双可变区(dvd)-ig(双特异性格式);小的免疫蛋白(sip)(一类微型抗体);smip(“小模块化免疫药物”)scfv-fc二聚体;dart(双链稳定二价抗体“双亲和力再靶向”);包含一个或多个cdr的小抗体拟似物等等。抗体可以使用常规技术片段化。例如,可以通过胃蛋白酶处理抗体生成f(ab’)2片段。由此产生的f(ab’)2片段可以被处理来降低二硫键从而生产fab′的碎片。木瓜蛋白酶消化可导致fab片段的形成。fab,fab’和f(ab’),scfv,fv,dsfv,fd,dabs,tandabs,ds-scfv,二聚体,微型抗体,二价抗体,双特异性抗体片段和其它片段也可以由重组技术合成或可以化学合成。生产抗体片段的技术在该领域是被众所周知和描述的。本领域技术人员还将理解的是,本发明涵盖所述hcv抗体的氨基酸序列修饰。举例而言,可需要改良抗体之结合亲和力及/或其它生物学特性。抗hcv抗体之氨基酸序列变体是由向抗hcv抗体核酸中引入适当核苷酸变化或由肽合成制备。该等修饰包括(例如)抗hcv抗体氨基酸序列内之残基缺失及/或插入及/或取代。进行缺失、插入及取代之任何组合以达成最终构建体,其限制条件为该最终构建体具有所要特征。氨基酸变化亦可改变抗hcv抗体之转译后过程,诸如改变糖基化位点之数目或位置。氨基酸序列插入物包括长度为一个残基至含有一百个或更多残基之多肽之氨基及/或羧基末端融合体,以及具有单个或多个氨基酸残基之序列内插入物。末端插入物之实例包括具有n末端甲硫氨酰基残基的抗hcv抗体或与细胞毒性多肽融合之抗体。抗hcv抗体分子的其它插入变体包括抗hcv抗体的n末端或c末端与酶(例如,对于adept而言)或增加抗体之血清半衰期之多肽的融合体。另一类型的变体为氨基酸取代变体。此等变体在抗hcv抗体分子中具有至少一个经不同残基置换之氨基酸残基。最引人关注之取代诱变位点包括高变区,但亦涵盖fr或恒定区的变化。fr或恒定区的氨基酸取代,优选为1~5个氨基酸,更优选为1个或2个氨基酸的取代。具有这样的氨基酸取代的卡尼优选与未取代抗体在功能上同等。因此,氨基酸取代优选为保守性氨基酸取代,这是电荷、侧链、极性、芳香性等的性质类似的氨基酸间的取代。性质类似的氨基酸例如可分类为:碱性氨基酸(精氨酸、赖氨酸、组氨酸)、酸性氨基酸(天冬氨酸、谷氨酸)、无电荷极性氨基酸(甘氨酸、天冬酰胺、谷氨酰胺、丝氨酸、苏氨酸、半胱氨酸、酪氨酸)、无极性氨基酸(亮氨酸、异亮氨酸、丙氨酸、缬氨酸、脯氨酸、苯丙氨酸、色氨酸、甲硫氨酸)、支链氨基酸(苏氨酸、缬氨酸、异亮氨酸)、芳香族氨基酸(苯丙氨酸、酪氨酸、色氨酸、组氨酸)等。通过将框架区内的氨基酸残基取代成半胱氨酸的氨基酸取代而导入二硫键,由此可以制作稳定化的抗体和抗原结合性抗体片段(dsfv等),这样的抗体和抗原结合性抗体片段也包含在本发明的范围内。在此,“在功能上同等”是指,具有氨基酸取代的抗体与取代前的抗体具有同样的生物学或生化学活性、特别是具有hcv感染抑制活性。一般亦可用丝氨酸取代与维持抗hcv抗体之适当构形无关的任何半胱氨酸残基以改良分子之氧化稳定性及防止异常交联。相反,可将半胱氨酸键添加至抗体中以改良其稳定性(尤其其中抗体为诸如fv片段之抗体片段)。本发明还涵盖了抗体的其它修饰。举例而言,可将抗体与多种非蛋白聚合物中之一者(例如,聚乙二醇、聚丙二醇、聚环氧烷或聚乙二醇与聚丙二醇之共聚物)连接。抗体亦可包裹于例如由凝聚技术或界面聚合制备之微胶囊(例如,分别为羟甲基纤维素或明胶微胶囊及聚-(甲基丙烯酸甲酯)微胶囊)中,包裹于胶状药物传递系统(例如,脂质粒、白蛋白微球体、微乳液、奈米颗粒及奈米胶囊)或巨乳液中。本发明涵盖与所述抗体的氨基酸序列或者编码该抗体的任何核苷酸序列具有一定程度的序列一致性或序列同源性的序列,术语“同系物”意即与个体氨基酸序列及个体核苷酸序列具有某些同源性之实体。本文中,术语“同源性”可等同于“一致性”。在本发明中,同源序列用于包括可与个体氨基酸至少75、85或90%一致性,优选至少95%或98%一致性之氨基酸序列。通常,同系物将包含与个体氨基酸序列相同之活性位点等。尽管亦可关于相似性(亦即,具有类似化学特性/功能之氨基酸残基)考虑同源性,但在本
发明内容中,优选关于序列一致性表达同源性。在本发明中,同源序列用于包括可与编码本发明之多肽的核苷酸序列(个体序列)至少75%、85%或90%一致性,优选至少95%或98%一致性的核苷酸序列。通常,同系物将包含与个体序列编码相同活性位点等之序列。尽管亦可关于相似性(亦即,具有类似化学特性/功能之氨基酸残基)考虑同源性,但在本
发明内容中,优选关于序列一致性表达同源性。在本发明中,本领域所熟知的免疫组化技术可用于对抗体与细胞或样品的结合进行评分。这种试验可用于测试具体抗体的特异性,或检测hcv在组织样品中的表达。简而言之,例如抗体可在一个高密度阵列的人体组织上测试,该组织包括阳性对照物(已知是hcv-阳性的细胞)和阴性对照(已知是hcv-阴性的细胞)。膜染色强度可以4级标准(0,1,2,3)通过肉眼观察评估。对于hcv+组织,优选的抗体得分为微弱或强烈(如0以上的分数),优选的是强烈免疫组化得分。本发明的药物可以是含有药学上可接受的载体的药物组合物。“药学上可接受的载体”是指可在制剂的
技术领域:
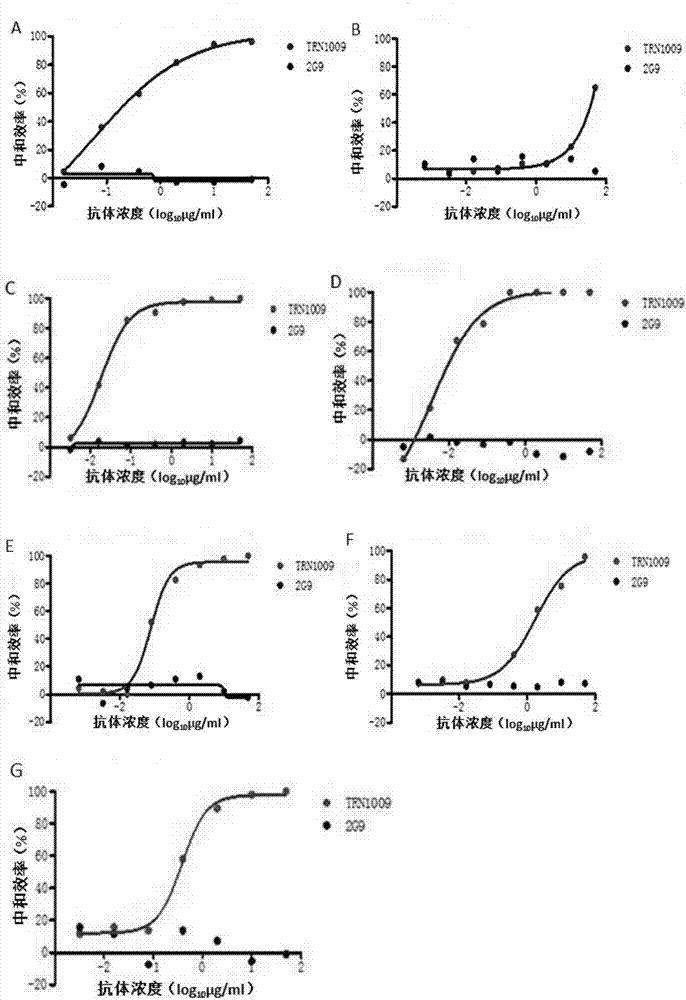
中常规使用的溶剂和/或添加剂。药学上可接受的溶剂包括(但不限于)水、药学上可接受的有机溶剂(如乙醇、丙二醇、乙氧基化乙硬脂醇、聚氧化异硬脂醇、聚氧乙烯山梨坦脂肪酸酯类)。这些溶剂优选进行灭菌,根据需要,优选调整为与血液等渗。另外,药学上可接受的添加剂包括(但不限于)胶原、聚乙烯醇、聚乙烯基吡咯烷酮、羧基乙烯基聚合物、羧基甲基纤维素钠、聚丙烯酸钠、海藻酸钠、水溶性糊精、羧甲基淀粉钠、果胶、甲基纤维素、乙基纤维素、黄原胶、阿拉伯树胶、琼脂、聚乙二醇、二甘油、甘油、丙二醇、凡士林、石蜡、硬酯醇、硬脂酸、人血清蛋白、甘露醇、山梨糖醇、乳糖、作为药物添加物可接受的表面活性剂等。关于药学上可接受的添加剂,除此之外,根据需要,还可包含赋形剂、粘合剂、崩解剂、填充剂、乳化剂、流动添加调节剂、润滑剂、矫味矫臭剂、助溶剂(可溶化剂)、助悬剂、稀释剂、表面活性剂、稳定剂、吸收促进剂、増量剤、赋湿剂、保湿剂(例如甘油、淀粉)、吸附剂、崩解抑制剂、包衣剂、着色剂、保存剂、抗氧化剂、香料、风味剂、甜味剂、缓冲剂等。关于溶剂和添加剂,根据剂型可以单独或适当组合使用。例如,作为注射用制剂使用时,可以将经纯化的抗体溶解于溶剂(例如生理盐水、缓冲液、葡萄糖溶液)中,向其中添加吸附防止剂(例如,吐温80、吐温20、明胶、人血清蛋白)而得的制剂。或者,为了在使用前进行溶解而制成再构成的剂型,可以是冻干制品。例如,为了进行冻干可以使用赋形剂(例如甘露醇、葡萄糖等的糖醇或糖类)本发明的抗体或抗原结合性抗体片段或药物可以通过口服给予、组织内给予(例如皮下给予、肌肉给予、静脉内给予)、局部给予(例如,经皮给予)或经直肠给予来进行给予。剂型优选为适合于给予方法的形态。例如组织内给予时,优选经由血流的注射,此时的剂型,代表性的是液体。进行注射时,对注入部位没有特别限定。包括(但不限于)静脉内、动脉内、肝脏内、肌肉内、关节内、骨髓内、髓腔内、心室内、经皮、皮下、皮内、腹腔内、鼻腔内、肠内或舌下等。优选为静脉内注射或动脉内注射等血管内注射。经由血流可使本发明的药物直接到达全身,而且侵袭性比较低,给病人等对象带来的负担小。或者,还可注射到肝脏内或肝门静脉,使本发明的药物直接作用于hcv所在部位。将本发明的抗体或抗原结合性抗体片段或药物给予对象者(病人等)时,优选每一给予单位中含有可发挥hcv感染抑制活性的有效量的本发明的抗体抗原结合性抗体片段。“有效量”是指就有效成分发挥其功能所必要的量,即本发明中是指抑制hcv感染所必要的量,且是指对所给予的对象者几乎或完全不产生有害副作用的量。该有效量可根据对象者(病人等)的信息、剂型和给予途径等的各种条件而发生变化。“对象者(病人等)的信息”包含:疾病的进展程度或重症程度、全身的健康状态、年龄、体重、性别、饮食生活、药物敏感性、有无并用药物、以及对治疗的耐性等。本发明药物的最终给予量和有效量,基于每个对象者的信息等,通过医师的判断进行确定。在获得hcv感染抑制效果方敏,有必要大量给予本发明药物时,为了减轻对于对象者的负担,还可分成数次进行给予。为了补充或增强本发明药物的治疗或预防效果、或者降低给予量,还可以将本发明药物与其它药物适量混合使用或并用使用。作为并用的药物,可举出:现有的抗病毒剂,例如干扰素、病毒唑等。对成为本发明的抗体或抗原结合性抗体片段或药物给予对象的对象者没有限定,优选为人等的灵长类、家畜、宠物、实验(试验)动物等的哺乳动物,特别优选为人等的灵长类。对象者可以是罹患丙型肝炎、或者可以是未罹患丙型肝炎但有罹患丙型肝炎风险的对象者。对象可以是接受肝脏移植的慢性丙型肝炎病人、或者可以是接受需要输血的手术的病人。本发明的抗体或抗原结合性抗体片段可用作试样中的hcv检测用试剂。试样是指,可包含hcv(hcv颗粒或其薄膜蛋白)的各种试样。例如为:培养细胞、培养细胞破碎液、培养液上清、或来自对象者的试样、例如人试样。人试样是指,采自人的组织(例如,术后采取的组织)、或血液、血清、血清、尿、骨髓液、唾液、淋巴液、精液等的体液等所有的来自人的活体试样,优选为血液、血清、血浆或尿。另外,不仅可以是液体试样,也可以是固体试样。例如也可以是器官移植的捐献者器官或组织切片标本等。hcv的检测可以通过elisa法、eia法、荧光免疫测定法、放射免疫测定法、或发光免疫测定法等的使用标记抗体的公知的免疫学检测方法、表面等离子体共振法(spr法)或石英晶体微量天平测定法进行实施,但优选通过使用标记抗体的免疫学检测方法进行实施。另外,上述的免疫学测定方法还可以如下实施:将免疫比浊法、胶乳凝集反应、胶乳比浊法、红细胞凝集反应或颗粒凝集反应等的免疫复合物凝集物的生成,通过光学方法测定其透射光或散射光,或者通过目视测定的测定法来实施。此时,可以使用磷酸缓冲液、甘氨酸缓冲液、tris缓冲液或good缓冲液等作为溶剂,并且可包含聚乙二醇等的反应促进剂或非特异性反应抑制剂。本发明所公开的抗hcv中和抗体编号为trn1009。本发明的优点和有益效果:本发明提供了一种抗hcv中和抗体,该抗体具有抗体效价高、特异性强、亲和力、稳定性好、无免疫原性、完全人源性蛋白结构的特点。本发明提供了一种药物组合物,该药物组合物可用于hcv引起的疾病(如丙型肝炎、肝硬化、肝癌等)的治疗。本发明提供的抗体可用于制备检测hcv病毒的工具,发现有效中和抗原表位及开发丙型肝炎重组蛋白及亚单位疫苗。附图说明图1为抗体trn1009表达纯化图,其中,图a显示了trn1009抗体的sds-page检测图,图b显示了trn1009抗体的western-blot检测图。图2为抗体trn1009与不同的hcv病毒株的中和活性检测图;其中,图a显示了抗体trn1009与病毒株h77的中和活性图;图b显示了抗体trn1009与病毒株con1的中和活性图;图c显示了抗体trn1009与病毒株jfh1的中和活性;图d显示了抗体trn1009与病毒株s52的中和活性;图e显示了抗体trn1009与病毒株ed43的中和活性;图f显示了抗体trn1009与病毒株sa13的中和活性;图g显示了抗体trn1009与病毒株hk6a的中和活性图。图3为抗体trn1009与不同基因型的抗原的结合活性检测图。图4为抗体trn1009与不同hcv病毒抗原e2-core蛋白的亲和活性检测图,其中,图a为抗体trn1009与e2-core-2a基因型蛋白亲和活性检测图;图b为抗体trn1009与e2-core-4a基因型蛋白亲和活性检测图;图c为抗体trn1009e2-core-6a基因型蛋白亲和活性检测图;图d为抗体trn1009与e2-core-7a基因型蛋白亲和活性检测图。具体的实施方式下面结合附图和实施例对本发明作进一步详细的说明。以下实施例仅用于说明本发明而不用于限制本发明的范围。实施例中未注明具体条件的实验方法,通常按照常规条件,例如sambrook等人,分子克隆:实验室手册(newyork:coldspringharborlaboratorypress,1989)中所述的条件,或按照制造厂商所建议的条件。实施例1淋巴细胞分离与单个记忆性b细胞分选一、材料:1.试剂:ficoll淋巴细胞分离液为cedarlane公司产品。cd3-apc、cd14-apc、cd16-pe、cd20-apc、cd27-pe、igd-fitc等均为invirogen公司产品等。二、方法结果1、样本获取:hcv感染者抗凝外周血采自云南省昆明市,该患者确认感染时间为2010年。2、淋巴细胞分离与单个记忆性b细胞分选采集hcv-i002血液样本100ml,用淋巴细胞分离管分离外周血单个核细胞(peripheralbloodmononuclearcell,pbmc),利用bdfacsria流式细胞仪(bdbiosciences,sanjose,ca)进行细胞分选,首先去除细胞碎片、黏连细胞和死细胞,通过荧光抗体染色得到cd3-/cd14-/cd16-/igm-的细胞,选择表达cd235a-/igd-/cd20+的b细胞,圈出cd27all记忆b细胞,用特异性标记荧光素的抗原得到e2双荧光标记的靶细胞。实施例2单细胞rt-pcr分离抗体可变区基因一、材料1.试剂:引物(invitrogen合成),superscriptiii反转录酶、hotstartaqplus酶(invitrogen,carlsbad,ca)、琼脂等。二、方法结果1.单细胞rt-pcr将含有单个b淋巴细胞的96孔板的pcr预测混液中加入0.5μm的各亚型重链与轻链的恒定区引物与superscriptiv逆转录酶(invitrogen,carlsbad,ca),同时设置阳性及阴性对照;逆转录pcr条件:55℃60min,降至4℃。合成cdna第一条链,产物cdna-20℃长期保存。2.抗体可变区目的基因的扩增采用巢式pcr方法,以逆转录产物(cdna)为模板,加入amplitaqgold360mastermix(invitrogen,carlsbad,ca),及0.5μm的各亚型重链与轻链抗体的特异性引物。反应条件:预变性95℃5min,然后进行35个pcr循环:95℃×30s,55℃×60s,72℃×90s,最后用72℃延伸7min。pcr产物用1.2%的琼脂糖凝胶电泳进行鉴定。3.dna凝胶电泳鉴定使用2%琼脂糖凝胶进行电泳实验进行鉴定。取2μlpcr反应产物与18μl0.1%的loadingbuffer混匀后上样,在e-base电泳系统的eg模式下进行电泳12min。凝胶成像系统检测pcr产物大小。实施例3重组抗体的表达载体的构建一、材料1.试剂:琼脂糖、tris,lb、氨苄青霉素,polyfect(qiagen,valencia,ca),fcs、dmem、pbs等。2.载体:pcdna3.3载体3.菌株:大肠杆菌dh5α二、方法结果1.pcr产物纯化克隆鉴定取2μl扩增产物经2%琼脂糖凝胶电泳检测,轻链约800bp和重链约1500bp的目的片段。将凝胶电泳鉴定为阳性,且重链与轻链可匹配成对的抗体可变区基因pcr产物利用ta克隆的方法连接到pcdna3.3载体上(已经改造并含有抗体leader与恒定区),将连接产物转化dh5α感受态细菌中,在含有氨苄青霉素的平板上37℃培养过夜,随即挑取10个单菌落用特异性引物进行pcr,反应条件:94℃预变性3min,94℃变性30s,55℃退火30s,72℃延伸1min40s,28个循环,最后72℃再延伸5min。2.结果取2μlpcr产物在1%琼脂糖凝胶上进行电泳检测,选取pcr鉴定为阳性的菌落进行基因测序,比对结果正确的即为抗体重链和轻链的重组表达质粒。实施例4目的基因的表达与抗体的筛选检测一、材料1.试剂:polyfect(qiagen,valencia,ca),fbs、dmem、pbs,luciferase,igg抗体,bsa,pbst,硫酸钠,丙酮等。2.细胞:293t,cho、huh7。3.病毒:hcv假病毒(hcvpp)。二、方法1.目的基因的表达在大肠杆菌dh5α中大量扩增表达阳性抗体重链和轻链基因的质粒,无内毒素抽提试剂盒抽提。用转染试剂polyetherimide共转染cho细胞,转染后4-6h添加新鲜无血清培养基,置于37℃,8%co2恒温培养箱中培养96h,收集细胞上清进行检测。2.抗体的筛选检测筛选:培养72h后细胞上清采用直接竞争elisa检测目的基因表达的抗体。elisa筛选:以不同的hcv包膜糖蛋白为抗原,并用包被液将抗原稀释浓度为100ng/ml,包被于elisa96孔板,每孔100μl,4℃过夜。封闭液37℃封闭2h。封闭后加一抗,抗体起始浓度为25μg/ml,3倍梯度稀释,每孔体积为100μl,37℃孵育1h,同时用hcv阳性病人血清作为阳性对照,狂犬抗体为阴性对照。用hrp标记的羊抗人igg(1:2000稀释)作为二抗37℃孵育1h。加入底物显色液(tmb),37℃避光放置5min后,用2m硫酸中止反应,用450nm波长进行比色。检测:将elisa筛选到的有结合活性的抗体命名为trn1009,并进行中和实验:将不同的hcv包膜糖蛋白的包装成质粒,加入荧光素luciferase基因转染293t细胞用于包装hcv假病毒(hcvpp),收取上清用于感染。铺huh7细胞于96孔板中,每孔细胞约1×104个,每孔体积为100μl,过夜培养,感染时细胞约30%铺满。hcvpp与抗体混合,室温放置30min。加入hcvpp与抗体混合液于96孔板,感染huh7细胞。对照组仅加入hcvpp,感染24h后换液,继续培养1-2天。感染后2-3天后测定luciferase活性,测量方法为去掉细胞上清,每孔用30μl裂解液,充分裂解后取20μl细胞裂解液加30μl底物,读取荧光值。比较抗体与对照组,计算中和效率。3.结果elisa实验筛选到的有结合活性的抗体具有非常好的中和效率。实施例5抗体大量表达与纯化一、材料1.试剂:polyfect(qiagen,valencia,ca),pbs,fbs,dmem(gibco),pro293a-cdm培养基(lonza),protein-a亲和层析柱(amersham),sds-page电泳试剂盒(invitrogen),低分子量蛋白标准,溴酚蓝,考马斯亮蓝r250。2.细胞:cho。二、方法1.trn1009抗体大量表达与纯化将中和实验鉴定出的有中和活性的编号为trn1009的抗体重链与轻链的表达载体(其中,重链可变区的氨基酸序列如seqidno.4所示;抗体轻链可变区的氨基酸序列如seqidno.8所示)共转染cho细胞(细胞融合度达到90%以上),转染后6-8h补培养基,37℃,8%co2培养箱中培养96h。然后收集转染上清,4000rp,4℃,离心1h,弃沉淀,利用蛋白(protein)a亲和层析法进行纯化获得trn1009抗体。2.sds-page和western-blot检验采用利用十二烷基硫酸钠-聚丙稀酰胺凝胶电泳(polyacrylamidegelelectrophoresis,sds-page)和蛋白质印迹法(免疫印迹试验,即westernblot)检验trn1009抗体的表达与纯化的结果:制备样品(200-800ng/w)、上样(10%的预制胶)、电泳、固定、染色、脱色;或进行westernblot分析。3.结果结果如图1所示,纯化后得到纯度非常高的蛋白成分,抗体trn1009的分子量超过120kd,并可清晰观察到解链后的抗体重链、轻链,重链约为70kd,轻链约为30kd。实施例6trn1009抗体的结合特异性检测一、材料1.试剂:pbs,luciferase,igg抗体,bsa,pbst,硫酸钠,丙酮等。2.病毒:hcv假病毒(hcvpp)。二、方法结果1.用实施例4提到的elisa方法对表达纯化的抗体的结合结合特异性进行检测:将不同的hcv包膜糖蛋白的包装成质粒,加入荧光素luciferase基因转染293t细胞用于包装hcv假病毒(hcvpp),收取上清用于感染。铺huh7细胞于96孔板中,每孔细胞约1×104个,过夜培养。hcvpp与不同浓度的抗体trn1009混合,起始浓度75μg/ml,3倍稀释,室温放置30min。加入hcvpp与抗体trn1009混合液于96孔板,感染huh7细胞。对照组仅加入hcvpp,感染24h后换液,继续培养1-2天。感染后2-3天后测定luciferase活性,测量方法为去掉细胞上清,每孔用30μl裂解液,充分裂解后取20μl细胞裂解液加30μl底物,读取荧光值。2.结果:荧光值降低,表明trn1009抗体与hcv包膜糖蛋白100%特异性结合。实施例7trn1009抗体的中和活性检测一、材料1.试剂:dmem,bsa,pbst,硫酸钠等。2.病毒:hcv病毒株(h77、con1、jfh1、s52、ed43、sa13、hk6a)。二、方法结果1.铺huh7细胞于96孔板中,过夜培养,感染时细胞约30%铺满。hcv真病毒株(h77、con1、jfh1、s52、ed43、sa13、hk6a)与不同浓度的抗体混合,起始浓度25μg/ml,3倍稀释,室温放置30min。加入hcv病毒株(h77、con1、jfh1、s52、ed43、sa13、hk6a)与抗体混合液于96孔板,感染huh7细胞。对照组仅加入hcv病毒株2g9,感染24h后换液,继续培养1-2天。感染后2-3天后测定活性,读取荧光值。比较抗体与对照组,计算中和效率。2.结果trn1009抗体与7株hcv病毒株的中和活性检测结果如图2所示;trn1009抗体与不同的hcv病毒株的中和效率如表1所示,较低浓度的trn1009抗体与hcv病毒株的中和效率即达到100%。表1trn1009抗体与不同的hcv病毒株的中和效率实施例8trn1009抗体的结合活性检测一、材料试剂:igg,pbst,tmb,硫酸等。二、方法结果1.以不同的hcv亚病毒株(hcv1a、hcv1b、hcv2、hcv3、hcv4、hcv5、hcv6、hcv7)的包膜蛋白作为抗原,并用包被液将抗原稀释浓度为100ng/ml,包被于elisa96孔板,每孔100μl,4℃过夜。封闭液37℃封闭2h。封闭后加一抗,trn1009起始浓度为25μg/ml,3倍梯度稀释,每孔体积为100μl,37℃孵育1h,同时用hcv阳性病人血清作为阳性对照,狂犬抗体为阴性对照。用hrp标记的羊抗人igg(1:2000稀释)作为二抗37℃孵育1h。加入底物显色液(tmb)100μl/孔,37℃避光放置5min后,用2m硫酸中止反应,用450nm波长进行比色。3.结果结果如图3所示,把表达纯化的抗体trn1009进行大于2000倍稀释后trn1009抗体依然可以与抗原结合,具有极强的结合活性。实施例9trn1009抗体的亲和活性检测一、材料1.试剂:igg抗体,biacore偶联试剂盒等。2.芯片:cm5。二、方法结果1.使用biacore分析仪的偶联捕获法进行亲和活性检测,利用biacorex-100system软件进行分析。2.结果trn1009抗体与4种不同基因型的hcv的包膜糖蛋白e2-core(e2-core-2a、e2-core-4a、e2-core-6a和e2-core-7a)的亲和活性如图4所示;具体结果如下面表2所示,trn1009抗体与4种不同基因型的hcv的包膜糖蛋白的亲和力高,平衡解离常数均达1*10-11kd(m)以上。表2trn1009抗体与hcv病毒抗原的亲和力动力学结果参数表ligandka(1/ms)kd(1/s)kd(m)e2-core-2a4.88e+046.25e-071.28e-11e2-core-4a4.25e+048.24e-081.94e-12e2-core-6a2.81e+044.97e-071.77e-11e2-core-7a9.85e+045.80e-095.88e-14上述实施例的说明只是用于理解本发明的方法及其核心思想。应当指出,对于本领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以对本发明进行若干改进和修饰,这些改进和修饰也将落入本发明权利要求的保护范围内。sequencelisting<110>广州泰诺迪生物科技有限公司珠海泰诺麦博生物技术有限公司暨南大学<120>抗hcv广谱中和抗体的制备、检测以及应用<160>8<170>patentinversion3.5<210>1<211>8<212>prt<213>人源<400>1glyglyasnpheasnasntyrpro15<210>2<211>8<212>prt<213>人源<400>2ileileproleuvalasnvalgly15<210>3<211>23<212>prt<213>人源<400>3alaargglyglyglyglyargglythrvallyshisleuglygluval151015leuasntyrglymetaspval20<210>4<211>130<212>prt<213>人源<400>4glnvalglnleuvalglnserglyalagluvallyslysproglyser151015servallysvalsercyslysglyserglyglyasnpheasnasntyr202530proiletyrtrpvalargglnalaproglyglnglypheglutrpleu354045glyargileileproleuvalasnvalglygluhisalaglnlysphe505560glnaspargvalthrilethralaasplysserthrserthralatyr65707580metgluleuserserleuargsergluaspthralavaltyrtyrcys859095alaargglyglyglyglyargglythrvallyshisleuglygluval100105110leuasntyrglymetaspvaltrpglyglnglythrthrvalthrval115120125serser130<210>5<211>6<212>prt<213>人源<400>5glnserileserasnser15<210>6<211>3<212>prt<213>人源<400>6alaalaser1<210>7<211>9<212>prt<213>人源<400>7glnglnseraspserileprohisthr15<210>8<211>107<212>prt<213>人源<400>8aspilevalmetthrglnserproproserleuseralaservalgly151015aspargvalthrilethrcysargalaserglnserileserasnser202530leuasntrptyrglnglnlysproglylysproprolysleuleuile354045tyralaalaserserleuglnasnglyvalproserargphethrala505560serglyserglythraspphethrleuthrileserserleuglnpro65707580gluaspphealaalatyrtyrcysglnglnseraspserileprohis859095thrpheglyglnglythrlysleugluilelys100105当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1