金属配合物及其制备方法、含有所述金属配合物的用于烯烃聚合的催化剂组分和用于烯烃聚合的催化剂,以及使用所述用于烯烃聚合的催化剂制备α-烯烃聚合物和共聚物的方法与流程
本发明涉及可用于制备α-烯烃聚合物和α-烯烃共聚物的金属配合物,以及使用所述金属配合物制备α-烯烃聚合物和α-烯烃共聚物的新型方法。
背景技术:
α-烯烃和含极性基团的单体的共聚物是工业上有用的聚合物。为了通过直接聚合获得所述共聚物,通常使用高压自由基方法。然而,该方法的缺点在于不能聚合更高级的α-烯烃如丙烯。工业上难以通过除高压自由基方法之外的方法制备所述共聚物,并且在使用齐格勒催化剂或茂金属催化剂的情况下,催化剂失活是不可避免的。
然后,在茂金属催化剂领域,通过有机稀土金属配合物基茂金属催化剂能够实现乙烯和甲基丙烯酸甲酯的共聚合。自20世纪90年代以来,已经深入研究了乙烯与含极性基团的共聚单体通过后过渡金属配合物催化剂的共聚合。例如,brookhart等人报道的(α-二亚胺)钯配合物和grubbs等人报道的(水杨酰脒基)镍催化剂是已知的。在使用这些催化剂的情况下,采用低聚合温度来抑制链转移的频率;因此,通常会导致低的共聚物生产性和低分子量。近年来,通过诸如(磷磺酸盐)钯配合物((phosphorussulfonate)palladiumcomplex)(参见专利文献1)和(磷苯酚盐)镍配合物((phosphorusphenolate)nickelcomplex)(参见专利文献2至4、非专利文献1和2等)等的发现解决了乙烯与含极性基团的单体共聚的问题,这些是所谓的基于shop的催化剂。
如上所述,(磷苯酚盐)镍配合物作为用于乙烯与含极性基团的单体共聚合的共聚催化剂是有效的。但是,没有关于(磷苯酚盐)镍配合物在α-烯烃与含极性基团的单体的共聚合中的有效性的报道。
引文列表
专利文献
专利文献1:日本专利申请特开(jp-a)号2010-150246
专利文献2:国际公开号wo2010/050256
专利文献3:美国专利号6559326
专利文献4:jp-a号2005-307021
非专利文献
非专利文献1:j.heinickeetal.,"chem.eur.j.",2003,9,6093.
非专利文献2:j.heinickeetal.,"europeanjournalofinorganicchemistry",2000,3,431.
技术实现要素:
发明要解决的问题
鉴于现有技术的问题,本发明的目的是提供一种具有优异聚合活性的新型催化剂组分,其用于制备α-烯烃聚合物和α-烯烃共聚物、特别是用于制备高分子量的聚合物,以及使用所述催化剂组分制备α-烯烃聚合物和α-烯烃共聚物的方法。
用于解决问题的方案
为了实现上述目的,本发明的发明人进行了研究,并且发现一种具有磷苯酚盐配体结构的新型过渡金属配合物,其不同于现有的(磷苯酚盐)过渡金属配合物,他们发现α-烯烃的均聚或与含极性基团的单体的共聚合是可以的。此外,他们发现能够获得具有更高分子量的(共)聚合物,并且他们完成了本发明。
在本发明的第一实施方式中,提供:
[1-1]一种金属配合物,其是通过使下述通式[i]或[ii]表示的化合物与含有属于元素周期表中第9、10或11族的过渡金属的过渡金属化合物接触而得到的:
其中,所述通式[i]和[ii]中的r1至r6、e1和x1如下:
r1、r2、r3和r4各自独立地表示选自由下述(i)至(iv)组成的组的原子或基团:
(i)氢,
(ii)卤素,
(iii)具有1至30个碳原子的直链状烷基、具有3至30个碳原子的支链非环状烷基、具有2至30个碳原子的烯基、具有3至30个碳原子且任选具有侧链的环烷基、具有6至30个碳原子的芳基、具有7至30个碳原子的芳烷基、或具有7至30个碳原子的烷芳基,每个所述基团任选具有选自由杂原子和含有杂原子的基团组成的组的成员,和
(iv)or9、co2r9、co2m’、c(o)n(r8)2、c(o)r9、sr9、so2r9、sor9、oso2r9、p(o)(or9)2-y(r8)y、cn、nhr9、n(r9)2、si(or8)3-x(r8)x、osi(or8)3-x(r8)x、no2、so3m’、po3m’2、p(o)(or2)2m’或含环氧基的基团,其中r8表示氢或具有1至20个碳原子的烃基;r9表示具有1至20个碳原子的烃基;m’表示碱金属、碱土金属、铵、季铵或鏻;x表示0至3的整数;和y表示0至2的整数;
适当地选自r1、r2、r3和r4的多个基团任选彼此结合以形成脂环、芳环或含有选自氧、氮和硫组成的组的杂原子的杂环,并且在这种情况下,环成员的数量为5至8,和所述环任选在其上具有取代基;
r5和r6各自独立地表示具有7至30个碳原子的直链状烷基、具有7至30个碳原子的支链非环状烷基、具有7至30个碳原子的烯基、具有7至30个碳原子且任选具有侧链的环烷基、或具有7至30个碳原子的芳烷基,每个所述基团任选具有选自由杂原子和含有杂原子的基团组成的组的成员;
e1表示磷、砷或锑;和
x1表示氧或硫,和
其中,在所述通式[i]中,
z表示氢或离去基团,和
m表示z的化合价。
[1-2]一种由下述通式[iii]表示的金属配合物:
其中,所述通式[iii]中的r1至r7、e1、x1、m和l1如下:
r1、r2、r3和r4各自独立地表示选自由下述(i)至(iv)组成的组的原子或基团:
(i)氢,
(ii)卤素,
(iii)具有1至30个碳原子的直链状烷基、具有3至30个碳原子的支链非环状烷基、具有2至30个碳原子的烯基、具有3至30个碳原子且任选具有侧链的环烷基、具有6至30个碳原子的芳基、具有7至30个碳原子的芳烷基、或具有7至30个碳原子的烷芳基,每个所述基团任选具有选自由杂原子和含有杂原子的基团组成的组的成员,和
(iv)or9、co2r9、co2m’、c(o)n(r8)2、c(o)r9、sr9、so2r9、sor9、oso2r9、p(o)(or9)2-y(r8)y、cn、nhr9、n(r9)2、si(or8)3-x(r8)x、osi(or8)3-x(r8)x、no2、so3m’、po3m’2、p(o)(or2)2m’或含环氧基的基团,其中r8表示氢或具有1至20个碳原子的烃基;r9表示具有1至20个碳原子的烃基;m’表示碱金属、碱土金属、铵、季铵或鏻;x表示0至3的整数;和y表示0至2的整数;
适当地选自r1、r2、r3和r4的多个基团任选彼此结合以形成脂环、芳环或含有选自氧、氮和硫组成的组的杂原子的杂环,并且在这种情况下,环成员的数量为5至8,和所述环任选在其上具有取代基;
r5和r6各自独立地表示具有7至30个碳原子的直链状烷基、具有7至30个碳原子的支链非环状烷基、具有7至30个碳原子的烯基、具有7至30个碳原子且任选具有侧链的环烷基、或具有7至30个碳原子的芳烷基,每个所述基团任选具有选自由杂原子和含有杂原子的基团组成的组的成员;
e1表示磷、砷或锑;
x1表示氧或硫;
m表示属于元素周期表中第9、10或11族的过渡金属;
r7表示氢或具有1至20个碳原子且任选具有选自由杂原子和含有杂原子的基团组成的组的成员的烃基;
l1表示配位至m的配体;和
r7和l1任选彼此结合以形成环。
[1-3]根据[1-2]所述的金属配合物,其中m为属于元素周期表中第10族的过渡金属。
[1-4]根据[1-1]至[1-3]任一项所述的金属配合物,其中r3是氢。
[1-5]一种由上述[1-2]的通式[iii]表示的金属配合物的制备方法,其中将由上述[1-1]的通式[i]或[ii]表示的化合物与含有属于元素周期表中第9、10或11族的过渡金属的过渡金属化合物接触:
[1-6]一种用于烯烃聚合的催化剂组分,其包含[1-1]至[1-4]任一项限定的金属配合物或通过[1-5]限定的制备方法得到的金属配合物。
[1-7]一种用于烯烃聚合的催化剂,其包含下述组分(a)和(b),和根据需要的下述组分(c):
组分(a):[1-1]至[1-4]任一项限定的金属配合物或通过[1-5]限定的制备方法得到的金属配合物
组分(b):可与组分(a)反应形成离子对的化合物,或离子交换性层状硅酸盐
组分(c):有机铝化合物。
[1-8]根据[1-7]所述的用于烯烃聚合的催化剂,其中所述组分(b)为铝氧烷。
[1-9]一种α-烯烃聚合物的制备方法,其中(a)α-烯烃在[1-7]或[1-8]限定的所述用于聚合的催化剂存在下聚合或共聚合。
[1-10]一种α-烯烃共聚物的制备方法,其中(a)α-烯烃和(b)(甲基)丙烯酸酯单体、乙烯基单体或烯丙基单体在[1-7]或[1-8]限定的所述用于聚合的催化剂存在下共聚合。
在本发明的第二实施方式中,提供:
[2-1]一种金属配合物,其是通过使下述通式[i]或[ii]表示的化合物与含有属于元素周期表中第9、10或11族的过渡金属的过渡金属化合物接触而得到的:
其中,所述通式[i]和[ii]中的r1至r6、e1和x1如下:
r2、r3和r4各自独立地表示选自由下述(i)至(iv)组成的组的原子或基团:
(i)氢,
(ii)卤素,
(iii)具有1至30个碳原子的直链状烷基、具有3至30个碳原子的支链非环状烷基、具有2至30个碳原子的烯基、具有3至30个碳原子且任选具有侧链的环烷基、具有6至30个碳原子的芳基、具有7至30个碳原子的芳烷基、或具有7至30个碳原子的烷芳基,每个所述基团任选具有选自由杂原子和含有杂原子的基团组成的组的成员,和
(iv)or9、co2r9、co2m’、c(o)n(r8)2、c(o)r9、sr9、so2r9、sor9、oso2r9、p(o)(or9)2-y(r8)y、cn、nhr9、n(r9)2、si(or8)3-x(r8)x、osi(or8)3-x(r8)x、no2、so3m’、po3m’2、p(o)(or2)2m’或含环氧基的基团,其中r8表示氢或具有1至20个碳原子的烃基;r9表示具有1至20个碳原子的烃基;m’表示碱金属、碱土金属、铵、季铵或鏻;x表示0至3的整数;和y表示0至2的整数;
r1表示选自由下述(v)和(vi)组成的组的基团:
(v)具有1至30个碳原子的直链状烷基、具有3至30个碳原子的支链非环状烷基、具有2至30个碳原子的烯基、具有3至30个碳原子且任选具有侧链的环烷基、具有6至30个碳原子的芳基、具有7至30个碳原子的芳烷基、或具有7至30个碳原子的烷芳基,每个所述基团具有选自由杂原子和含有杂原子的基团组成的组的成员,和
(vi)or9、co2r9、co2m’、c(o)n(r8)2、c(o)r9、sr9、so2r9、sor9、oso2r9、p(o)(or9)2-y(r8)y、cn、nhr9、n(r9)2、si(or8)3-x(r8)x、osi(or8)3-x(r8)x、no2、so3m’、po3m’2、p(o)(or2)2m’或含环氧基的基团,其中r8、r9、m’、x和y如上所述;
适当地选自r1、r2、r3和r4的多个基团任选彼此结合以形成脂环、芳环或含有选自由氧、氮和硫组成的组的杂原子的杂环,并且在这种情况下,环成员的数量为5至8,和所述环任选在其上具有取代基;
r5和r6各自独立地表示具有1至6个碳原子的直链状烷基、具有3至6个碳原子的支链非环状烷基、或具有2至6个碳原子的烯基,每个所述基团任选具有选自由杂原子和含有杂原子的基团组成的组的成员;
r5和r6任选彼此结合以形成脂环、芳环或含有选自由氧、氮和硫组成的组的杂原子的杂环,并且在这种情况下,环成员的数量为5至8,和所述环任选在其上具有取代基;
e1表示磷、砷或锑;和
x1表示氧或硫,和
其中,在所述通式[i]中,
z表示氢或离去基团,和
m表示z的化合价。
[2-2]一种由下述通式[iii]表示的金属配合物:
其中,所述通式[iii]中的r1至r7、e1、x1、m和l1如下:
r2、r3和r4各自独立地表示选自由下述(i)至(iv)组成的组的原子或基团:
(i)氢,
(ii)卤素,
(iii)具有1至30个碳原子的直链状烷基、具有3至30个碳原子的支链非环状烷基、具有2至30个碳原子的烯基、具有3至30个碳原子且任选具有侧链的环烷基、具有6至30个碳原子的芳基、具有7至30个碳原子的芳烷基、或具有7至30个碳原子的烷芳基,每个所述基团任选具有选自由杂原子和含有杂原子的基团组成的组的成员,和
(iv)or9、co2r9、co2m’、c(o)n(r8)2、c(o)r9、sr9、so2r9、sor9、oso2r9、p(o)(or9)2-y(r8)y、cn、nhr9、n(r9)2、si(or8)3-x(r8)x、osi(or8)3-x(r8)x、no2、so3m’、po3m’2、p(o)(or2)2m’或含环氧基的基团,其中r8表示氢或具有1至20个碳原子的烃基;r9表示具有1至20个碳原子的烃基;m’表示碱金属、碱土金属、铵、季铵或鏻;x表示0至3的整数;和y表示0至2的整数;
r1表示选自由下述(v)和(vi)组成的组的基团:
(v)具有1至30个碳原子的直链状烷基、具有3至30个碳原子的支链非环状烷基、具有2至30个碳原子的烯基、具有3至30个碳原子且任选具有侧链的环烷基、具有6至30个碳原子的芳基、具有7至30个碳原子的芳烷基、或具有7至30个碳原子的烷芳基,每个所述基团具有选自由杂原子和含有杂原子的基团组成的组的成员,和
(vi)or9、co2r9、co2m’、c(o)n(r8)2、c(o)r9、sr9、so2r9、sor9、oso2r9、p(o)(or9)2-y(r8)y、cn、nhr9、n(r9)2、si(or8)3-x(r8)x、osi(or8)3-x(r8)x、no2、so3m’、po3m’2、p(o)(or2)2m’或含环氧基的基团,其中r8、r9、m’、x和y如上所述;
适当地选自r1、r2、r3和r4的多个基团任选彼此结合以形成脂环、芳环或含有选自由氧、氮和硫组成的组的杂原子的杂环,并且在这种情况下,环成员的数量为5至8,和所述环任选在其上具有取代基;
r5和r6各自独立地表示具有1至6个碳原子的直链状烷基、具有3至6个碳原子的支链非环状烷基、或具有2至6个碳原子的烯基,每个所述基团任选具有选自由杂原子和含有杂原子的基团组成的组的成员;
r5和r6任选彼此结合以形成脂环、芳环或含有选自由氧、氮和硫组成的组的杂原子的杂环,并且在这种情况下,环成员的数量为5至8,和所述环任选在其上具有取代基;
e1表示磷、砷或锑;
x1表示氧或硫;
m表示属于元素周期表中第9、10或11族的过渡金属;
r7表示氢或具有1至20个碳原子且任选具有选自由杂原子和含有杂原子的基团组成的组的成员的烃基;
l1表示配位至m的配体;和
r7和l1任选彼此结合以形成环。
[2-3]根据[2-2]所述的金属配合物,其中m为属于元素周期表中第10族的过渡金属。
[2-4]根据[2-1]至[2-3]任一项所述的金属配合物,其中r1为具有6至30个碳原子且具有选自由杂原子和含有杂原子的基团组成的组的成员的芳基,或si(or8)3-x(r8)x。
[2-5]根据[2-1]至[2-4]任一项所述的金属配合物,其中r3为氢或具有1至30个碳原子且具有含有杂原子的基团的直链状烷基。
[2-6]根据[2-5]所述的金属配合物,其中r3是氢。
[2-7]一种由上述[2-2]的通式[iii]表示的金属配合物的制备方法,其中将由上述[2-1]的通式[i]或[ii]表示的化合物与含有属于元素周期表中第9、10或11族的过渡金属的过渡金属化合物接触。
[2-8]一种用于烯烃聚合的催化剂组分,其包含[2-1]至[2-6]任一项限定的金属配合物或通过[2-7]限定的制备方法得到的金属配合物。
[2-9]一种用于烯烃聚合的催化剂,其包含下述组分(a)和(b),和根据需要的下述组分(c):
组分(a):[2-1]至[2-6]任一项限定的金属配合物或通过[2-7]限定的制备方法得到的金属配合物
组分(b):可与组分(a)反应形成离子对的化合物,或离子交换性层状硅酸盐
组分(c):有机铝化合物。
[2-10]根据[2-9]所述的用于烯烃聚合的催化剂,其中所述组分(b)为铝氧烷。
[2-11]一种α-烯烃聚合物的制备方法,其中(a)α-烯烃在[2-9]或[2-10]限定的所述用于聚合的催化剂存在下聚合或共聚合。
[2-12]一种α-烯烃共聚物的制备方法,其中(a)α-烯烃和(b)(甲基)丙烯酸酯单体、乙烯基单体或烯丙基单体在[2-9]或[2-10]限定的所述用于聚合的催化剂存在下共聚合。
在本发明的第三实施方式中,提供:
[3-1]一种金属配合物,其是通过使下述通式[i]或[ii]表示的化合物与含有属于元素周期表中第9、10或11族的过渡金属的过渡金属化合物接触而得到的:
其中,所述通式[i]和[ii]中的r1至r6、e1和x1如下:
r1表示具有1至30个碳原子的直链状烷基、具有3至30个碳原子的支链非环状烷基、具有2至30个碳原子的烯基、具有3至30个碳原子且任选具有侧链的环烷基、具有6至30个碳原子的芳基、具有7至30个碳原子的芳烷基、或具有7至30个碳原子的烷芳基;
r2、r3和r4各自独立地表示选自由下述(i)至(iv)组成的组的原子或基团:
(i)氢,
(ii)卤素,
(iii)具有1至30个碳原子的直链状烷基、具有3至30个碳原子的支链非环状烷基、具有2至30个碳原子的烯基、具有3至30个碳原子且任选具有侧链的环烷基、具有6至30个碳原子的芳基、具有7至30个碳原子的芳烷基、或具有7至30个碳原子的烷芳基,每个所述基团任选具有选自由杂原子和含有杂原子的基团组成的组的成员,和
(iv)or9、co2r9、co2m’、c(o)n(r8)2、c(o)r9、sr9、so2r9、sor9、oso2r9、p(o)(or9)2-y(r8)y、cn、nhr9、n(r9)2、si(or8)3-x(r8)x、osi(or8)3-x(r8)x、no2、so3m’、po3m’2、p(o)(or2)2m’或含环氧基的基团,其中r8表示氢或具有1至20个碳原子的烃基;r9表示具有1至20个碳原子的烃基;m’表示碱金属、碱土金属、铵、季铵或鏻;x表示0至3的整数;和y表示0至2的整数;
适当地选自r2、r3和r4的多个基团任选彼此结合以形成脂环、芳环或含有选自由氧、氮和硫组成的组的杂原子的杂环,并且在这种情况下,环成员的数量为5至8,和所述环任选在其上具有取代基;
r5和r6各自独立地表示具有4至6个碳原子的直链状烷基、具有4至6个碳原子的仲烷基、具有4至6个碳原子的叔烷基、或具有4至6个碳原子的烯基,每个所述基团任选具有选自由杂原子和含有杂原子的基团组成的组的成员;
e1表示磷、砷或锑;和
x1表示氧或硫,和
其中,在所述通式[i]中,
z表示氢或离去基团,和
m表示z的化合价。
[3-2]一种由下述通式[iii]表示的金属配合物:
其中,所述通式[iii]中的r1至r7、e1、x1、m和l1如下:
r1表示具有1至30个碳原子的直链状烷基、具有3至30个碳原子的支链非环状烷基、具有2至30个碳原子的烯基、具有3至30个碳原子且任选具有侧链的环烷基、具有6至30个碳原子的芳基、具有7至30个碳原子的芳烷基、或具有7至30个碳原子的烷芳基;
r2、r3和r4各自独立地表示选自由下述(i)至(iv)组成的组的原子或基团:
(i)氢,
(ii)卤素,
(iii)具有1至30个碳原子的直链状烷基、具有3至30个碳原子的支链非环状烷基、具有2至30个碳原子的烯基、具有3至30个碳原子且任选具有侧链的环烷基、具有6至30个碳原子的芳基、具有7至30个碳原子的芳烷基、或具有7至30个碳原子的烷芳基,每个所述基团任选具有选自由杂原子和含有杂原子的基团组成的组的成员,和
(iv)or9、co2r9、co2m’、c(o)n(r8)2、c(o)r9、sr9、so2r9、sor9、oso2r9、p(o)(or9)2-y(r8)y、cn、nhr9、n(r9)2、si(or8)3-x(r8)x、osi(or8)3-x(r8)x、no2、so3m’、po3m’2、p(o)(or2)2m’或含环氧基的基团,其中r8表示氢或具有1至20个碳原子的烃基;r9表示具有1至20个碳原子的烃基;m’表示碱金属、碱土金属、铵、季铵或鏻;x表示0至3的整数;和y表示0至2的整数;
适当地选自r2、r3和r4的多个基团任选彼此结合以形成脂环、芳环或含有选自由氧、氮和硫组成的组的杂原子的杂环,并且在这种情况下,环成员的数量为5至8,和所述环任选在其上具有取代基;
r5和r6各自独立地表示具有4至6个碳原子的直链状烷基、具有4至6个碳原子的仲烷基、具有4至6个碳原子的叔烷基、或具有4至6个碳原子的烯基,每个所述基团任选具有选自由杂原子和含有杂原子的基团组成的组的成员;
e1表示磷、砷或锑;
x1表示氧或硫;
m表示属于元素周期表中第9、10或11族的过渡金属;
r7表示氢或具有1至20个碳原子且任选具有选自由杂原子和含有杂原子的基团组成的组的成员的烃基;
l1表示配位至m的配体;和
r7和l1任选彼此结合以形成环。
[3-3]根据[3-2]所述的金属配合物,其中m为属于元素周期表中第10族的过渡金属。
[3-4]根据[3-1]至[3-3]任一项所述的金属配合物,其中r5和r6各自为叔丁基。
[3-5]根据[3-1]至[3-4]任一项所述的金属配合物,其中r1为叔丁基。
[3-6]一种由上述[3-2]的通式[iii]表示的金属配合物的制备方法,其中将由上述[3-1]的通式[i]或[ii]表示的化合物与含有属于元素周期表中第9、10或11族的过渡金属的过渡金属化合物接触。
[3-7]一种用于烯烃聚合的催化剂组分,其包含[3-1]至[3-5]任一项限定的金属配合物或通过[3-6]限定的制备方法得到的金属配合物。
[3-8]一种用于烯烃聚合的催化剂,其包含下述组分(a)和(b),和根据需要的下述组分(c):
组分(a):[3-1]至[3-5]任一项限定的金属配合物或通过[3-6]限定的制备方法得到的金属配合物
组分(b):可与组分(a)反应形成离子对的化合物,或离子交换性层状硅酸盐
组分(c):有机铝化合物。
[3-9]根据[3-8]所述的用于烯烃聚合的催化剂,其中所述组分(b)为铝氧烷。
[3-10]一种α-烯烃聚合物的制备方法,其中(a)α-烯烃在[3-8]或[3-9]限定的所述用于聚合的催化剂存在下聚合。
[3-11]一种α-烯烃共聚物的制备方法,其中(a)α-烯烃和(b)(甲基)丙烯酸酯单体、乙烯基单体或烯丙基单体在[3-8]或[3-9]限定的所述用于聚合的催化剂存在下共聚合。
[3-12]根据[3-10]所述的α-烯烃聚合物的制备方法或根据[3-11]所述的α-烯烃共聚物的制备方法,其中所述(a)α-烯烃为丙烯。
发明的效果
通过本发明,可以通过比以前更高的聚合活性获得具有更高分子量的α-烯烃均聚物;此外,可以实现通过优异的聚合活性的α-烯烃与含极性基团的单体的共聚合。
附图说明
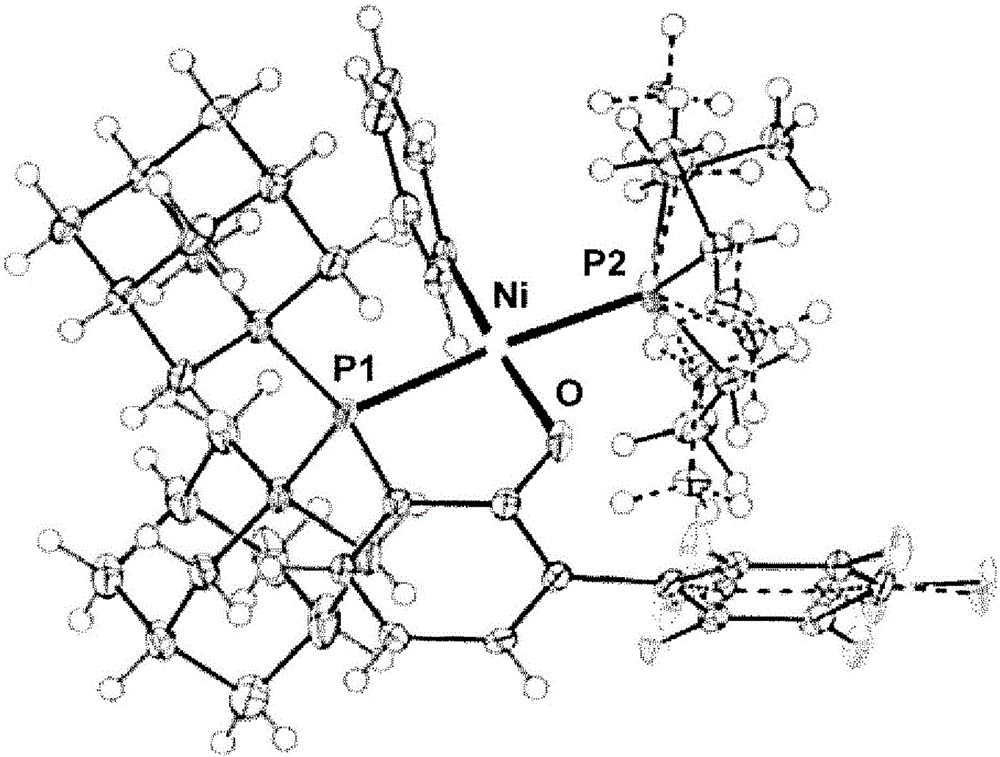
图1是配合物(b-350)niph(pet3)的ortep图。
具体实施方式
1.第一实施方式
在本发明的第一实施方式中,提供可通过将由通式[i]或[ii]表示的化合物与含有属于元素周期表中第9、10或11族的过渡金属如镍、钯、钴、铜或铑的过渡金属化合物接触得到的反应产物,即由通式[iii]表示的金属配合物(以下可称为金属配合物[iii]),并且还提供使用所述反应产物作为催化剂组分的方法,即在作为催化剂组分的所述金属配合物存在下制备(a)α-烯烃的聚合物或共聚物的方法,以及在作为催化剂组分的所述金属配合物存在下制备(a)α-烯烃和(b)(甲基)丙烯酸酯单体、乙烯基单体或烯丙基单体的共聚物的方法。
在本发明中,"聚合"是一种单体的均聚和多种单体的共聚合的统称,并且这两种情况简单地描述为"聚合",特别是当两种情况都不需要区分时。此外,在本发明中,"(甲基)丙烯酸酯"包括丙烯酸酯和甲基丙烯酸酯。
1-1.金属配合物
本发明的第一实施方式的金属配合物是可通过使下述通式[i]或[ii]表示的化合物与含有属于元素周期表中第9、10或11族的过渡金属的过渡金属化合物接触得到的:
在本发明中,"接触"表示由通式[i]和[ii]表示的化合物(以下,它们可统称为磷苯酚盐化合物)和过渡金属化合物彼此非常接近的存在,以使得通式[i]或[ii]中的e1可与所述过渡金属形成配位键,和/或通式中的x1可与所述过渡金属形成单键。此外,使磷苯酚盐化合物与过渡金属化合物接触表示将这些化合物混合以使得这些化合物彼此非常接近地存在并且可以形成所述两种键中的至少一种。
混合磷苯酚盐化合物和过渡金属化合物的条件没有特别限制。这些化合物可以直接混合或使用溶剂进行混合。特别是从实现均匀混合的观点,优选使用溶剂。
在如此得到的金属配合物中,所述磷苯酚盐化合物变成配体。因此,所述磷苯酚盐化合物与过渡金属化合物之间的反应通常是配体交换反应。当如此得到的金属配合物在热力学上比过渡金属化合物更稳定时,通过在室温(15℃至30℃)下混合磷苯酚盐化合物和过渡金属化合物来进行配体交换反应。另一方面,当如此得到的金属配合物在热力学上不如过渡金属化合物稳定时,优选适当地加热所述混合物以致配体交换反应充分地进行。
据估计,可通过使由通式[i]或[ii]表示的化合物与含有属于元素周期表中第9、10或11族的过渡金属的过渡金属化合物接触得到的金属配合物具有由下述通式[iii]表示的结构。
然而,当所述磷苯酚盐化合物与含有属于元素周期表中第9、10或11族的过渡金属的过渡金属化合物接触时,存在会生成具有不同于通式[iii]表示的结构的结构的金属配合物的可能性,这是因为由通式[i]或[ii]表示的化合物是二齿配体。例如,可能是下述情形:其中仅通式[i]或[ii]中的x1与过渡金属形成键,或其中仅该式中的e1可与过渡金属形成键。由通式[iii]表示的金属配合物是所述磷苯酚盐化合物与过渡金属化合物的1:1反应产物。取决于过渡金属的类型,可能有其中得到具有不同组成比例的反应产物的情形。例如,可能有其中磷苯酚盐化合物的一个或多个分子与一个过渡金属形成配合物的情形,或可能有其中磷苯酚盐化合物的一个分子与两个或多个过渡金属反应以合成多核配合物的情形。
在本发明中,没有否认具有不同于由通式[iii]表示的结构的结构的金属配合物可用于与由通式[iii]表示的金属配合物一样制备α-烯烃(共)聚合物。
以下,将描述通式[i]和[ii]中的r1至r6、e1和x1以及通式[i]中的z和m。
r1、r2、r3和r4各自独立地表示(i)氢、(ii)卤素、(iii)任选具有选自由杂原子和含有杂原子的基团组成的组中的成员的特定基团,或(iv)含有杂原子的取代基。
作为(ii)卤素,实例包括氟原子、氯原子、溴原子和碘原子。其中,氟原子是优选的。
作为(iii)中使用的杂原子,实例包括氧、氮、磷、硫、硒、硅、卤素和硼。这些杂原子中,氟和氯是优选的。
作为(iii)中使用的"含有杂原子的基团",特别是,可提及与以下描述的(iv)含有杂原子的取代基类似的基团。作为"含有杂原子的基团",提供烷氧基(or9)、酯基(co2r9)等。r9如下所述。
对于(iii),对应于r1至r4的取代基的碳原子总数优选为1至30,更优选为2至25,还更优选为4至20。
按照上述,(iii)"任选具有选自由杂原子和含有杂原子的基团组成的组中的成员的特定基团"表示(iii-a)具有1至30个碳原子的直链状烷基、具有3至30个碳原子的支链非环状烷基、具有2至30个碳原子的烯基、具有3至30个碳原子且任选具有侧链的环烷基、具有6至30个碳原子的芳基、具有7至30个碳原子的芳烷基、和具有7至30个碳原子的烷芳基;(iii-b)其中一个或两个或更多杂原子通过取代与(iii-a)中的各基团结合的基团;(iii-c)其中一个或两个或更多上述"含有杂原子的基团"通过取代与(iii-a)中的各基团结合的基团;和(iii-d)其中一个或两个或更多的上述杂原子和一个或两个或更多的上述"含有杂原子的基团"通过取代与(iii-a)中的各基团结合的基团。对于(iii-c),实例包括通过取代结合了烷氧基的烷基,和通过取代结合了酯基的芳基,等等。
特别是,(iv)含有杂原子的取代基表示or9、co2r9、co2m’、c(o)n(r8)2、c(o)r9、sr9、so2r9、sor9、oso2r9、p(o)(or9)2-y(r8)y、cn、nhr9、n(r9)2、si(or8)3-x(r8)x、osi(or8)3-x(r8)x、no2、so3m’、po3m’2、p(o)(or2)2m’或含环氧基的基团。r8表示氢或具有1至20个碳原子的烃基。r9表示具有1至20个碳原子的烃基。m’表示碱金属、碱土金属、铵、季铵或鏻。此外,x表示0至3的整数,和y表示0至2的整数。
适当地选自r1、r2、r3和r4的多个基团任选彼此结合以形成脂环、芳环或含有选自由氧、氮和硫组成的组的杂原子的杂环。在这种情况下,环成员的数量为5至8,和所述环任选在其上具有取代基。
r1中含有的多个基团可以彼此结合以形成在r1上的环。即使r2、r3和r4中任一个含有多个基团时,这也同样适用。
优选r1、r2、r3和r4各自独立地表示(i)氢原子;(ii)氟原子、氯原子、溴原子;(iii)甲基、乙基、异丙基、丁基、苯基、三氟甲基、五氟苯基、咔唑基、萘基、蒽基;(iv)甲氧基、乙氧基、苯氧基、腈基、三甲基甲硅烷基、三乙基甲硅烷基、二甲基苯基甲硅烷基、三甲氧基甲硅烷基、三乙氧基甲硅烷基、三甲基甲硅烷基氧基、三甲氧基甲硅烷氧基、环己基氨基、磺酸钠、磺酸钾、磷酸钠、磷酸钾等。
特别是对于r1,优选的是(i)氢原子;(iii)叔丁基、五氟苯基、咔唑基;(iv)甲氧基、三甲基甲硅烷基、三甲基甲硅烷基氧基、环己基氨基等。对于r3,优选的是(i)氢原子或(iii)叔丁基等。
r5和r6各自独立地表示具有7至30个碳原子的直链状烷基、具有7至30个碳原子的支链非环状烷基、具有7至30个碳原子的烯基、具有7至30个碳原子且任选具有侧链的环烷基、或具有7至30个碳原子的芳烷基,每个所述基团任选具有选自由杂原子和含有杂原子的基团组成的组的成员。r5和r6可彼此结合以形成环。
对于所述直链状烷基、支链非环状烷基、烯基、任选具有侧链的环烷基和芳烷基中每一个,碳原子数优选是7至25,更优选8至20,仍更优选10至15。
r5和r6位于金属m的附近,并且通过空间和/或电子相互作用影响m。为了具有这种效果,r5和r6优选是体积大的。
r5和r6的优选的具体实例包括5-三环[3.3.1.13,7]癸烷-1-基(1-金刚烷基)、5-甲基-2-(丙烷-2-基)环己基(
作为用作r5和r6的杂原子,实例包括氧、氮、磷、硫、硒、硅、卤素和硼。这些杂原子中,氟和氯是优选的。此外,含有这些杂原子的基团包括:包括烷氧基、芳氧基、酰基和酯基的含氧基团;包括氨基和酰胺基的含氮基团;包括硫代烷氧基和硫代芳氧基的含硫基团;包括膦基的含磷取代基;包括甲硒烷基的含硒基团;包括三烷基甲硅烷基、二烷基芳基甲硅烷基和烷基二芳基甲硅烷基的含硅基团;包括氟烷基和氟芳基的含氟基团;和包括烷基硼基和芳基硼基的含硼基团。这些含有杂原子的基团之中,烷氧基或芳氧基是最优选的。
作为上述含有杂原子的基团中含有的杂原子,能够与过渡金属配位的杂原子是优选的。含有这种能够与过渡金属配位的杂原子的含有杂原子的基团的具体实例包括下述基团。
即,可提及含氧基团,包括烷氧基如甲氧基、乙氧基、正丙氧基、异丙氧基、正丁氧基和叔丁氧基,芳氧基如苯氧基、对甲基苯氧基和对甲氧基苯氧基,酰基如乙酰基和苯甲酰基,和酯基如乙酰氧基、羧基乙基、羧基叔丁基和羧基苯基;含氮基团,包括二烷基氨基如二甲基氨基、二乙基氨基、二正丙基氨基和环己基氨基;含硫基团,包括硫代烷氧基如硫代甲氧基、硫代乙氧基、硫代正丙氧基、硫代异丙氧基、硫代正丁氧基、硫代叔丁氧基和硫代苯氧基,和硫代芳氧基如对甲基硫代苯氧基和对甲氧基硫代苯氧基;含磷取代基,包括二烷基膦基如二甲基膦基、二乙基膦基、二正丙基膦基和环己基膦基;和含硒基团,包括甲硒烷基如甲基甲硒烷基、乙基甲硒烷基、正丙基甲硒烷基、正丁基甲硒烷基、叔丁基甲硒烷基和苯基甲硒烷基。
e1表示磷、砷或锑。它们之中,e1优选是磷。
x1表示氧或硫。它们之中,x1优选是氧。
z表示氢或离去基团。z的具体实例包括氢原子、r9so2基团(其中r9如上所述)、cf3so2基团等。
此外,m表示z的化合价。
通式[ii]以阴离子形式示出。作为其抗衡阳离子,可以使用任何阳离子,只要该阳离子不抑制与本发明的过渡金属化合物的反应即可。所述抗衡阳离子的具体实例包括铵、季铵或鏻,以及元素周期表中第1至14族的金属离子。这些阳离子之中,nh4+、r94n+(其中r9如上所述,四个r9可以彼此相同或不同(以下同样适用))、r94p+、li+、na+、k+、mg2+、ca2+和al3+是优选的,r94p+、li+、na+和k+是更优选的。
下述表1-1示出本发明的通式[i]和[ii]中取代基的具体组合等。z和m仅涉及通式[i]。然而,具体实例不限于下述实例。
为了理解化合物的结构,示出了上表1-1中列出的化合物1的结构式和名称。由所述结构式表示的化合物将称为2-二金刚烷基膦基-6-五氟苯基苯酚。
由通式[i]和[ii]表示的化合物可以通过已知的合成法来合成。
由下述通式[iii]表示的本发明的金属配合物包括在由通式[i]或[ii]表示的化合物与含有属于元素周期表中第9、10或11族的过渡金属的过渡金属化合物的反应产物中。然而,如上所述,通过所述制备方法得到的金属配合物的结构不限于由通式[iii]表示的结构。
在通式[iii]中,r1至r6、e1和x1如上所述。如上所述,就含有苯环和这些取代基(r1至r6、e1和x1)的主骨架而言,反应产物中的金属配合物的配合结构与由通式[iii]表示的金属配合物的配合结构之间存在相似性。
以下,将描述通式[iii]中的m、r7和l1。
在本发明中,m为属于元素周期表中第9、10或11族的过渡金属。m优选是第10族中的镍、钯和铂,第9族中的钴和铑,和第11族中的铜,更优选第10族中的镍、钯和铂,最优选第10族中的镍或钯。
m的化合价优选是二价。m的化合价是指有机金属化学中使用的形式氧化数。即,当包括某些元素的键中的电子对分配给具有更大电负性的元素时,化合价是指残留在所述元素原子上的电荷数。例如,在本发明的通式[iii]中,当e1是磷,x1是氧,m是镍,r7是苯基,l1是三乙基膦以及镍与磷、氧、苯基的碳和三乙基膦的磷形成键时,镍的形式氧化数即镍的化合价变成二价。理由如下:根据上述定义,在这些键中,电子对分配给具有比镍更大的电负性的两个磷、氧和碳,磷的电荷变成0,氧的电荷变成-1,苯基的电荷变成-1,所述配合物整体上是电中性的;因此,残留在镍上的电荷变成+2。
作为二价过渡金属,例如,镍(ii)、钯(ii)、铂(ii)和钴(ii)是优选的。作为除二价过渡金属以外的过渡金属,铜(i)或铑(iii)也是优选的。
在本发明中,r7表示氢原子或具有1至20个碳原子且任选具有选自由杂原子和含有杂原子的基团组成的组的成员的烃基。本发明中的聚合或共聚合被认为是通过将本发明的组分(a)或组分(b)插入到m和r7的键中来引发。因此,当r7的碳原子数过大时,倾向于抑制该引发反应。为此,不包括取代基中含有的碳原子的r7的碳原子数优选是1至16,更优选1至10。
r7的具体实例包括氢化物基团、甲基、乙基、正丙基、异丙基、正丁基、异丁基、正己基、正辛基、正癸基、正十二烷基、环戊基、环己基、苄基、苯基、对甲基苯基、三甲基甲硅烷基、三乙基甲硅烷基、三苯基甲硅烷基等。
在本发明中,l1表示配位至m的配体。本发明中的配体l1是具有1至20个碳原子且具有作为能够形成配位键的原子的氧、氮或硫的烃化合物。此外,作为l1,可使用具有能够与过渡金属形成配位键的碳碳不饱和键(并且任选含有杂原子)的烃化合物。l1的碳原子数优选是1至16,更优选1至10。此外,作为与通式[iii]中的m形成配位键的l1,没有电荷的化合物是优选的。
在本发明中,优选作为l1的是环状不饱和烃、膦、吡啶、哌啶、烷基醚、芳基醚、烷基芳基醚、环状醚、烷基腈衍生物、芳基腈衍生物、醇、酰胺、脂族酯、芳族酯、胺等。更优选作为l1的是环烯烃、膦、吡啶、环状醚、脂族酯、芳族酯等。特别优选作为l1的是三烷基膦、吡啶、卢剔啶(二甲基吡啶)、皮考啉(甲基吡啶)和r9co2r8(r8和r9的定义如上所述)。
r7和l1可以彼此结合形成环。这种实例是环辛-1-烯基,该基团也是本发明中优选的实施方式。
下表1-2示出本发明的通式[iii]中的取代基的具体组合。然而,具体实例不限于下述实例。
为了理解金属配合物的结构,示出了上表1-2中列出的配合物1b的结构式和名称。由所述结构式表示的配合物将称为(2-二金刚烷基膦基-6-五氟苯基苯酚盐)苯基(三乙基膦)镍(ii)。
此外,举例说明表1-2中列出的化合物的中心金属m从镍变成钯的化合物。
对于本发明中使用的过渡金属化合物,使用能够与由通式[i]或[ii]表示的化合物反应形成具有聚合能力的配合物的那些。它们有时称为前驱体。
例如,作为含有镍的过渡金属化合物,可使用双(1,5-环辛二烯)镍(0),由通式ni(ch2cr13ch2)2表示的配合物[其中r13表示氢原子、卤素原子、具有1至30个碳原子且任选含有杂原子的烃基、or8、co2r8、co2m’、c(o)n(r9)2、c(o)r8、sr8、so2r8、sor8、oso2r8、p(o)(or8)2-y(r9)y、cn、nhr8、n(r8)2、si(or9)3-x(r9)x、osi(or9)3-x(r9)x、no2、so3m’、po3m’2、p(o)(or8)2m’或含环氧基的基团,其中r8表示具有1至20个碳原子的烃基;r9表示氢原子或具有1至20个碳原子的烃基;m’表示碱金属、碱土金属、铵、季铵或鏻;x表示0至3的整数;和y表示0至2的整数)],双(环戊二烯基)镍(ii),由通式ni(ch2sir133)2l12表示的配合物(其中r13和l1如上所述),由通式nir132l12表示的配合物(其中r13和l1如上所述)等。
此外,作为含有属于第9、10或11族的过渡金属的过渡金属化合物,可使用通式mr13pl1q(其中m表示第9、10或11族的过渡金属;r13和l1如上所述;p和q各自是满足m的化合价的0或更大的整数)。
这些过渡金属化合物之中,优选使用的是双(1,5-环辛二烯)镍(0)、niphcl(pet3)2、niphcl(pph3)2、由通式ni(ch2cr13ch2)2表示的配合物(其中r13如上所述)、由通式ni(ch2sir133)2l12表示的配合物(其中r13和l1如上所述)、由通式nir132l12表示的配合物(其中r13和l1如上所述)、pd(dba)2、pd2(dba)3、pd3(dba)4(其中dba表示二苄叉基丙酮)、pd(ococh3)2和(1,5-环辛二烯)pd(甲基)(氯化物)。
特别优选的是双(1,5-环辛二烯)镍(0)、niphcl(pet3)2、niphcl(pph3)2、ni(ch2chch2)2、ni(ch2cmech2)2、ni(ch2sime3)2(py)2(以下,py表示吡啶)、ni(ch2sime3)2(lut)2(以下,lut表示2,6-卢剔啶))、niph2(py)2、niph2(lut)2、pd(dba)2、pd2(dba)3、pd3(dba)4(其中dba表示二苄叉基丙酮))、pd(ococh3)2、和(1,5-环辛二烯)pd(甲基)(氯化物)。
本发明的反应产物可以通过将由通式[i]或[ii]表示的上述化合物与上述过渡金属化合物[iv]例如以[i]+[ii]:[iv]=[1:99]至[99:1]的摩尔比在有机溶剂如甲苯或苯中,在0℃至100℃下,在减压至加压下接触1至86400秒来获得。当双(1,5-环辛二烯)镍(0)(ni(cod)2)在甲苯或苯中的溶液用作所述过渡金属化合物时,可以通过溶液从黄色至例如红色的变色来确认形成所述反应产物。
在本反应之后,构成过渡金属化合物但不是所述化合物的过渡金属的组分被除z以外的通式[i]的一部分或由通式[ii]表示的化合物取代,从而形成由本发明的通式[iii]表示的金属配合物。该取代反应优选定量进行;然而,在有些情况下,其可以进行不完全。在反应完成之后,除由通式[iii]表示的配合物之外,还存在衍生自通式[i]和[ii]以及所述过渡金属化合物的其他组分。当进行本发明的聚合反应或共聚合反应时,可以除去或保留这些其他组分。通常,优选除去这些其他组分,因为可以获得更高的活性。
当进行反应时,本发明的l1可以一起存在。当镍或钯用作本发明的m时,纯化的由通式[iii]表示的配合物的稳定性有时通过在体系中共存具有路易斯碱性质的l1而得到改善。在这种情况下,l1的共存是优选的,只要l1不抑制本发明的聚合反应或共聚合反应。
在本发明中,所述反应可以预先在不同于用于α-烯烃聚合或α-烯烃与(甲基)丙烯酸酯的共聚合的反应器的容器中进行,然后如此得到的由通式[iii]表示的配合物可用于α-烯烃的聚合或α-烯烃与(甲基)丙烯酸酯的共聚合,或所述反应可以在这些单体存在下进行。此外,所述反应可以在用于α-烯烃聚合或α-烯烃与(甲基)丙烯酸酯的共聚合的反应器中进行。在这种情况下,这些单体可以存在或不存在。作为由通式[i]和[ii]表示的每种组分,可以使用单一组分,或者可以组合使用多种组分。特别是,为了拓宽分子量分布或共聚单体含量分布,这种多种组分的组合使用是有用的。
1-2.金属配合物的制备方法
在本发明的第一实施方式的制备方法中,如上所述,由通式[iii]表示的金属配合物可以通过使由通式[i]或[ii]表示的化合物与含有属于元素周期表中第9、10或11族的过渡金属的过渡金属化合物接触来制备。
1-3.用于烯烃聚合的催化剂组分
根据本发明的第一实施方式的用于烯烃聚合的催化剂组分包含上述金属配合物或可通过上述制备方法得到的金属配合物。
在本发明的第一实施方式中,由通式[iii]表示的金属配合物可用作用于聚合或共聚合的催化剂组分。如以上所述,由通式[iii]表示的金属配合物可以通过使通式[i]或[ii]与所述过渡金属配合物组分反应来形成。当由通式[iii]表示的金属配合物用作催化剂组分时,可以使用分离的金属配合物,或者可以使用负载在载体上的金属配合物。这种负载可以在用于α-烯烃聚合或α-烯烃与(甲基)丙烯酸酯共聚合的反应器中,在这些单体存在或不存在下进行,或者可以在不同于所述反应器的容器中进行。
作为可使用的载体,可使用任何载体,只要所述载体不损害本发明的范围即可。通常,可适当地使用无机氧化物和聚合物载体。特别是,可提及sio2、al2o3、mgo、zro2、tio2、b2o3、cao、zno、bao、tho2等,或它们的混合物。此外,可使用混合氧化物如sio2-al2o3、sio2-v2o5、sio2-tio2、sio2-mgo和sio2-cr2o3,并且可使用无机硅酸盐、聚乙烯载体、聚丙烯载体、聚苯乙烯载体、聚丙烯酸载体、聚甲基丙烯酸载体、聚丙烯酸酯载体、聚酯载体、聚酰胺载体、聚酰亚胺载体等。对于这些载体,粒径、粒径分布、孔容积、比表面积等没有特别限制,可使用任何载体。
作为无机硅酸盐,可使用粘土、粘土矿物、沸石、硅藻土等。对于这些物质,可以使用合成材料,或可以使用天然存在的矿物。粘土和粘土矿物的具体实例包括水铝英石类如水铝英石;高岭土类如地开石、珍珠陶土、高岭土和钙长石;埃洛石类如变埃洛石和埃洛石;蛇纹石类如纤蛇纹石、利蛇纹石和叶蛇纹石;蒙脱石类如蒙脱土、锌蒙脱石、贝得石、绿脱石、皂石和锂蒙脱石;蛭石矿物如蛭石;云母矿物如伊利石、绢云母和海绿石;绿坡缕石;海泡石;坡缕石;膨润土(bentonite);木节土(kibushiclay);gaerome粘土;硅铁石;叶蜡石;和绿泥石类。这些物质可形成混合层。人造化合物包括合成云母、合成锂蒙脱石、合成皂石和合成带云母。这些具体实例之中,优选的是高岭土类如地开石、珍珠陶土、高岭土和钙长石;埃洛石类如变埃洛石和埃洛石;蛇纹石类如纤蛇纹石、利蛇纹石和叶蛇纹石;蒙脱石类如蒙脱土、zaukonite、贝得石、绿脱石、皂石和锂蒙脱石;蛭石矿物如蛭石;云母矿物如伊利石、绢云母和海绿石;合成云母;合成锂蒙脱石;合成皂石;和合成带云母。特别优选的是蒙脱石类如蒙脱土、zaukonite、贝得石、绿脱石、皂石和锂蒙脱石;蛭石矿物如蛭石;合成云母;合成锂蒙脱石;合成皂石;和合成带云母。
这些载体可以原样使用,或者可以用盐酸、硝酸、硫酸等进行酸处理,和/或使用licl、nacl、kcl、cacl2、mgcl2、li2so4、mgso4、znso4、ti(so4)2、zr(so4)2、al2(so4)3等进行盐处理。所述处理可以通过将相应的酸和碱混合以在反应体系中形成盐来进行。此外,可以进行如粉碎和造粒等形状控制或干燥处理。
1-4.用于烯烃聚合的催化剂
根据本发明的第一实施方式的用于烯烃聚合的催化剂包含下述组分(a)和(b),和根据需要的下述组分(c):
组分(a):上述金属配合物或可通过上述制备方法得到的金属配合物
组分(b):可与组分(a)反应形成离子对的化合物,或离子交换性层状硅酸盐
组分(c):有机铝化合物。
所述组分(a)是上述金属配合物或可通过上述制备方法得到的金属配合物。可单独使用一种金属配合物,或可组合使用两种或多种金属配合物。
所述组分(b)的实例是有机铝氧化合物。所述有机铝氧化合物在分子中具有al-o-al键,和所述键的数量在通常1至100的范围内,优选1至50。这种有机铝氧化合物通常是可通过使有机铝化合物与水反应得到的产物。
有机铝与水的反应通常在惰性烃类(溶剂)中进行。作为惰性烃类,可使用脂族烃、脂环族烃或芳族烃如戊烷、己烷、庚烷、环己烷、甲基环己烷、苯、甲苯和二甲苯。优选使用脂族烃或芳族烃。
作为用于制备所述有机铝氧化合物的有机铝化合物,可使用由下述通式表示的化合物。优选使用三烷基铝。
(rx)tal(x3)(3-t)
(其中rx表示烃基如各自具有1至18个碳原子、优选1至12个碳原子的烷基、烯基、芳基和芳烷基;x3表示氢原子或卤素原子;和t表示1≤t≤3的整数。)
所述三烷基铝中的烷基可以是甲基、乙基、丙基、异丙基、丁基、异丁基、戊基、己基、辛基、癸基、十二烷基等中任何烷基。优选的是甲基和异丁基,特别优选的是甲基。可混合和使用两种或多种所述有机铝化合物。
水与有机铝化合物的反应比例(水/al的摩尔比)优选是0.25/1至1.2/1,特别优选0.5/1至1/1。反应温度通常在-70℃至100℃的范围内,优选-20℃至20℃。通常在5分钟至24小时、优选10分钟至5小时的范围内选择反应时间。作为反应所需的水,不仅可以使用简单的水,而且可以使用硫酸铜水合物、硫酸铝水合物等中含有的水合水,以及可以在反应体系中产生水的组分。
上述有机铝氧化合物之中,可通过烷基铝与水反应得到的有机铝氧化合物通常称为铝氧烷。甲基铝氧烷(包括基本上由甲基铝氧烷(mao)组成的那些)特别优选作为所述有机铝氧化合物。此外,固体形式的干燥甲基铝氧烷(dmao),其通过将溶剂从mao溶液中去除而得到,是优选的。
作为所述有机铝氧化合物,可以组合使用两种或多种上述有机铝氧化合物,或者可以使用溶解或分散在上述惰性烃溶剂中的有机铝氧化合物的溶液。
所述组分(b)的具体实例是离子交换性层状硅酸盐。离子交换性层状硅酸盐(以下可简称为"硅酸盐")是具有其中由离子键合等形成的平面彼此平行定位并由结合力堆叠的晶体结构且其中所含有的离子可交换的硅酸盐化合物。作为所述硅酸盐,各种硅酸盐是已知的,所述硅酸盐详细描述在"nendokobutsugaku",haruoshirozu,asakurapublishingco.,ltd.(1995)中。
在本发明中,作为组分(b),优选使用属于蒙脱石类的那些。其具体实例包括蒙脱土、锌蒙脱石、贝得石、绿脱石、皂石、锂蒙脱石、镁皂石等。它们之中,从增大共聚物部分的聚合活性和分子量的观点,优选蒙脱土。
大多数硅酸盐主要作为天然粘土矿物的主要成分生产。因此,经常含有除所述离子交换性层状硅酸盐以外的夹杂物(如石英和方英石)。用于本发明的蒙脱石类的硅酸盐可以含有夹杂物。
所述硅酸盐可以进行酸处理和/或盐处理。所述处理可以通过将相应的酸和碱混合以在反应体系中形成盐来进行。
作为组分(b),可以使用上述有机铝氧化合物和离子交换性层状硅酸盐的混合物。此外,作为所述有机铝氧化合物和离子交换性层状硅酸盐,可以使用一种所述化合物和硅酸盐,或两种或多种所述化合物和硅酸盐。
用作组分(c)的有机铝化合物的实例由下述通式表示:
al(rp)ax(3-a)
其中rp表示具有1至20个碳原子的烃基;x表示氢、卤素、烷氧基或甲硅烷氧基;和a为大于0且等于或小于3的数。
由所述通式表示的有机铝化合物的具体实例包括三烷基铝如三甲基铝、三乙基铝、三丙基铝、三异丁基铝等,和含有卤素或烷氧基的烷基铝如二乙基铝一氯化物、二乙基铝单甲醚等。
它们之中,三异丁基铝是优选的。此外,可以组合使用两种或多种上述有机铝化合物。此外,上述铝化合物可以用醇、苯酚等改性来使用。作为改性剂,例举甲醇、乙醇、1-丙醇、异丙醇、丁醇、苯酚、2,6-二甲基苯酚、2,6-二叔丁基苯酚等。优选的具体实例是2,6-二甲基苯酚和2,6-二叔丁基苯酚。
在根据本发明的第一实施方式的用于烯烃聚合的催化剂的制备方法中,所述组分(a)、组分(b)和根据需要的组分(c)的接触方法没有特别限制。例如,可提供下述方法。
方法(i):组分(a)和组分(b)彼此接触,然后添加组分(c)。
方法(ii):组分(a)和组分(c)彼此接触,然后添加组分(b)。
方法(iii):组分(b)和组分(c)彼此接触,然后添加组分(a)。
方法(iv):组分(a)、(b)和(c)彼此同时接触。
此外,每种组分可以通过将其与不同种类的组分混合而作为混合物使用,或者可以以不同的顺序单独接触。所述接触不仅可以在催化剂制备时进行,也可以在使用烯烃进行预聚合时或烯烃聚合时进行。
另外,可以将一种组分分开并与每种组分接触,例如,以使组分(b)和组分(c)彼此接触,然后添加组分(a)和组分(c)的混合物的方式。
所述组分(a)、(b)和(c)的接触优选在惰性气体气氛如氮气等和在惰性烃溶剂如戊烷、己烷、庚烷、甲苯、二甲苯等中进行。所述接触可以在-20℃至溶剂的沸点之间的温度下进行,特别优选在室温至溶剂的沸点之间的温度下进行。
1-5.α-烯烃聚合物的制备方法
本发明的第一实施方式的α-烯烃聚合物的制备方法的实施方式是(a)α-烯烃在所述用于聚合的催化剂存在下聚合或共聚合。
本发明中的组分(a)是由通式ch2=chr10表示的α-烯烃。r10是氢原子或具有1至20个碳原子的烃基,其可具有支链、环和/或不饱和键。当r10的碳原子数大于20时,倾向于较少显示聚合活性。为此,它们之中,r10是氢原子或具有1至10个碳原子的烃基的α-烯烃优选作为组分(a)。
更优选作为组分(a)的那些包括乙烯、丙烯、1-丁烯、1-戊烯、1-己烯、1-辛烯、1-癸烯、3-甲基-1-丁烯、4-甲基-1-戊烯、乙烯基环己烯和苯乙烯。作为组分(a),可以使用单一组分,或者可以组合使用多种组分。
本发明的α-烯烃聚合物的制备方法的另一实施方式是(a)α-烯烃和(b)(甲基)丙烯酸酯单体、乙烯基单体或烯丙基单体在上述用于聚合的催化剂存在下共聚合。
本发明中的(甲基)丙烯酸酯单体由通式ch2=c(r11)co2(r12)表示。r11是氢原子或具有1至10个碳原子的烃基,其可具有支链、环和/或不饱和键。r12是具有1至30个碳原子的烃基,其可具有支链、环和/或不饱和键。此外,r12可在其中任何位置含有杂原子。
当r11的碳原子数是11以上时,倾向于较少显示聚合活性。因此,r11是氢原子或具有1至10个碳原子的烃基,优选的(甲基)丙烯酸酯包括其中r11是氢原子或具有1至5个碳原子的烃基的(甲基)丙烯酸酯。更优选的(甲基)丙烯酸酯单体包括r11是甲基的甲基丙烯酸酯或r11是氢原子的丙烯酸酯。类似地,当r12的碳原子数大于30时,倾向于较少显示聚合活性。因此,r12的碳原子数是1至30,优选是1至12,更优选1至8。
此外,作为r12中任选含有的杂原子,提供氧、硫、硒、磷、氮、硅、氟、硼等。这些杂原子之中,氧、硅和氟是优选的,并且氧是更优选的。另外,不含杂原子的r12也是优选的。
更优选的(甲基)丙烯酸酯单体包括(甲基)丙烯酸甲酯、(甲基)丙烯酸乙酯、(甲基)丙烯酸正丙酯、(甲基)丙烯酸异丙酯、(甲基)丙烯酸正丁酯、(甲基)丙烯酸异丁酯、(甲基)丙烯酸叔丁酯、(甲基)丙烯酸戊酯、(甲基)丙烯酸己酯、(甲基)丙烯酸环己酯、(甲基)丙烯酸辛酯、(甲基)丙烯酸2-乙基己酯、(甲基)丙烯酸壬酯、(甲基)丙烯酸癸酯、(甲基)丙烯酸十二烷基酯、(甲基)丙烯酸苯酯、(甲基)丙烯酸甲苯酰酯、(甲基)丙烯酸苄基酯、(甲基)丙烯酸羟乙酯、(甲基)丙烯酸二甲基氨基乙酯、(甲基)丙烯酸二乙基氨基乙酯、(甲基)丙烯酸-2-氨基乙酯、(甲基)丙烯酸2-甲氧基乙酯、(甲基)丙烯酸-3-甲氧基丙酯、(甲基)丙烯酸缩水甘油基酯、(甲基)丙烯酸环氧乙烷酯、(甲基)丙烯酸三氟甲基酯、(甲基)丙烯酸2-三氟甲基乙基酯、(甲基)丙烯酸全氟乙基酯、(甲基)丙烯酰胺、(甲基)丙烯酰基二甲基酰胺、(甲基)丙烯酸2-羟基丁酯、(甲基)丙烯酸4-羟基丁酯等。(甲基)丙烯酸酯可以单独使用,或多种(甲基)丙烯酸酯可以组合使用。
本发明中的乙烯基单体是含有极性基团的乙烯基单体,如含卤素、含氮、含氧和含硫的乙烯基单体。特别是,其是含有卤素、羟基、氨基、硝基、羧基、醛基、酯基、环氧基、腈基等的乙烯基单体。其具体实例包括5-己烯-1-醇、2-甲基-3-丁烯-1-醇、10-十一碳烯酸乙酯、10-十一碳烯-1-醇、12-十三碳烯-2-醇、10-十一烷酸、甲基-9-癸烯酸酯、叔丁基-10-十一碳烯酸酯、1,1-二甲基-2-丙烯-1-醇、9-癸烯-1-醇、3-丁烯酸、3-丁烯-1-醇、n-(3-丁烯-1-基)邻苯二甲酰亚胺、5-己烯酸、5-己烯酸甲酯、5-己烯-2-酮、丙烯腈、甲基丙烯腈、醋酸乙烯酯等。它们之中,3-丁烯-1-醇、10-十一碳烯酸乙酯和10-十一碳烯-1-醇是特别优选的。
作为本发明中的烯丙基单体,实例包括具有3个碳原子的烯丙基单体(丙烯基单体)和作为具有4个或更多碳原子的含烯丙基单体的烯丙基系单体。所述烯丙基单体是含有极性基团的烯丙基单体,如含卤素、含氮、含氧和含硫的烯丙基单体。特别是,其是含有卤素、羟基、氨基、硝基、羧基、醛基、酯基、环氧基、腈基等的乙烯基单体。其优选的具体实例包括乙酸烯丙酯、烯丙醇、烯丙胺、n-烯丙基苯胺、n-叔丁氧基羰基-n-烯丙胺、n-苄氧基羰基-n-烯丙胺、n-烯丙基-n-苄胺、烯丙基氯、烯丙基溴、烯丙基醚、二烯丙基醚等。它们之中,乙酸烯丙酯和烯丙醇是更优选的,乙酸烯丙酯、烯丙基醚和二烯丙基醚是再更优选的。
本发明中的聚合反应是在存在或不存在液体下进行的,所述液体可以是:烃溶剂如丙烷、正丁烷、异丁烷、正己烷、正庚烷、甲苯、二甲苯、环己烷和甲基环己烷;或液化的α-烯烃;或极性溶剂如二乙基醚、乙二醇二甲醚、四氢呋喃、二氧杂环己烷、醋酸乙酯、苯甲酸甲酯、丙酮、甲基乙基酮、甲酰胺、乙腈、甲醇、异丙醇和乙二醇。此外,在此描述的液体化合物的混合物可用作溶剂。此外,离子液体也可以用作溶剂。更优选上述烃溶剂和离子液体以获得更高的聚合活性和高分子量。
在本发明中,所述聚合反应可在已知的添加剂存在或不存在下进行。作为添加剂,抑制自由基聚合的聚合抑制剂和具有稳定制备的共聚物的作用的添加剂是优选的。优选的添加剂的实例包括醌衍生物、受阻酚衍生物等。具体地,可使用氢醌单甲醚、2,6-二叔丁基-4-甲基苯酚(bht)、三甲基铝和bht的反应产物、钛(iv)醇盐和bht的反应产物等。此外,所述聚合可以在无机和/或有机填料存在下通过使用这种填料作为添加剂进行。此外,涉及本发明的l1或离子液体可以用作添加剂。
本发明中优选的添加剂包括路易斯碱。通过选择适合的路易斯碱,可以改善活性、分子量和丙烯酸酯的共聚合反应性。相对于聚合体系中存在的催化剂组分中的过渡金属m,路易斯碱的量为0.0001至1000当量、优选0.1至100当量、更优选0.3至30当量。将路易斯碱添加至聚合体系的方法没有特别限制,可使用任何技术。例如,路易斯碱可以通过与本发明的催化剂组分混合来添加,或可以通过与单体混合来添加,或可以独立于催化剂组分和单体添加到聚合体系中。此外,可以组合使用多种路易斯碱。此外,可以使用与本发明相关的l1相同的路易斯碱,或者可以使用不同的路易斯碱。
路易斯碱包括芳族胺、脂族胺、烷基醚、芳基醚、烷基芳基醚、环状醚、烷基腈、芳基腈、醇、酰胺、脂族酯、芳族酯、磷酸酯、亚磷酸酯、噻吩、噻蒽、噻唑、噁唑、吗啉、环状不饱和烃等。它们之中,优选的路易斯碱是芳族胺、脂族胺、环状醚、脂族酯和芳族酯,特别优选的路易斯碱是吡啶衍生物、嘧啶衍生物、哌啶衍生物、咪唑衍生物、苯胺衍生物、哌啶衍生物、三嗪衍生物、吡咯衍生物和呋喃衍生物。
具体的路易斯碱化合物包括吡啶、五氟吡啶、2,6-卢剔啶、2,4-卢剔啶、3,5-卢剔啶、嘧啶、n,n-二甲基氨基吡啶、n-甲基咪唑、2,2'-二吡啶、苯胺、哌啶、1,3,5-三嗪、2,4,6-三(三氟甲基)-1,3,5-三嗪、2,4,6-三(2-吡啶基)-s-三嗪、喹啉、8-甲基喹啉、吩嗪、1,10-菲咯啉、n-甲基吡咯、1,8-二氮杂双环-[5.4.0]-十一碳-7-烯、1,4-二氮杂双环-[2.2.2]-辛烷、三乙胺、苄腈、皮考啉、三苯胺、n-甲基-2-吡咯烷酮、4-甲基吗啉、苯并噁唑、苯并噻唑、呋喃、2,5-二甲基呋喃、二苯并呋喃、呫吨、1,4-二氧杂环己烷、1,3,5-三氧杂环己烷、二苯并噻吩、噻蒽、三苯基鏻环戊二烯、三苯基亚磷酸酯、三苯基磷酸酯、三吡咯烷基膦、三(吡咯烷基)硼烷等。
在本发明中,聚合方式没有特别限制。优选使用其中生成的聚合物的至少一部分在介质中呈淤浆形式的淤浆聚合;其中液化单体本身用作介质的本体聚合;其中聚合在汽化单体中进行的气相聚合;或其中生成的聚合物的至少一部分溶解在高温高压下液化的单体中的高压离子聚合;等。此外,可以使用任何类型的间歇聚合、半间歇聚合和连续聚合。此外,可以进行活性聚合或与链转移一起发生的聚合。此外,链穿梭或配位链转移聚合(cctp)可以通过组合使用所谓的链转移剂(csa)来进行。
未反应的单体和介质可以通过将它们与制备的共聚物分离并回收它们来使用。在回收时,这些单体和介质可以在纯化或不纯化的情况下重复使用。为了将制备的共聚物与未反应的单体和介质分离,可以使用迄今已知的方法。例如,可以使用诸如过滤、离心、溶剂萃取或用不良溶剂再沉淀等的方法。
聚合温度、聚合压力和聚合时间没有特别限制。通常,考虑到生产性和加工能力,可以从以下范围进行最佳设定。即,聚合温度可选自通常-20℃至290℃、优选0℃至250℃的范围内;共聚合压力可选自0.1mpa至300mpa、优选0.3mpa至250mpa的范围;和聚合时间可选自0.1分钟至10小时、优选0.5分钟至7小时、更优选1分钟至6小时的范围。
在本发明中,聚合通常在惰性气体气氛中进行。例如,可使用氮气气氛、氩气气氛或二氧化碳气氛,优选使用氮气气氛。允许混入少量氧气或空气。
向聚合反应器中供给催化剂和单体也没有特别限制,可以根据各自目的采用各种供给方法。例如,在间歇聚合的情况下,可以采用这样的技术:预先将预定量的单体供给到聚合反应器中,然后供给催化剂。在这种情况下,可以将额外的单体或额外的催化剂供给到聚合反应器。在连续聚合的情况下,可以采用这样的技术:将预定量的单体和催化剂连续或间歇地供给到聚合反应器中,以连续地进行聚合反应。
关于共聚物组成的控制,通常可以使用这样的方法:将多种单体供给到反应器中,并改变供给单体的比例。此外,提供了通过利用取决于催化剂结构的差异的单体竞聚率的差异来控制共聚组成的方法,以及通过利用单体竞聚率的聚合温度依赖性来控制共聚组成的方法。
对于控制聚合物的分子量,可使用迄今已知的方法。即,提供了通过控制聚合温度来控制分子量的方法,通过控制单体浓度来控制分子量的方法,通过使用链转移剂控制分子量的方法,通过控制过渡金属配合物中的配体结构来控制分子量的方法等。当使用链转移剂时,可使用迄今已知的链转移剂。例如,可使用氢气、烷基金属等。
此外,当组分(b)本身作为一种链转移剂起作用时,通过控制组分(b)与组分(a)的比例或控制组分(b)的浓度,可以进行分子量调节。当通过控制过渡金属配合物中的配体结构进行分子量调节时,可以利用这样的趋势:通常通过控制上述r2和r3中含杂原子的基团的类型、数量和构型,通过在金属m周围设置体积大的取代基,或通过将杂原子引入上述r6中来提高分子量。优选设置给电子基团如芳基和含杂原子的取代基,以使得给电子基团可与金属m具有相互作用。通过使用分子模型或分子轨道计算测量给电子基团与金属m之间的距离,通常可以判断这种给电子基团是否可以与金属m具有相互作用。
特别是,通过基于共聚物的极性基团的作用,本发明得到的共聚物表现出优异的涂漆特性、印刷性、抗静电性能、无机填料分散性、对其它树脂的粘合性、与其它树脂的相容性等。利用这些性能,本发明的共聚物可用于各种应用。例如,所述共聚物可用于膜、片材、粘合性树脂、粘结剂、相容剂、蜡等。
2.第二实施方式
在本发明的第二实施方式中,提供可通过将由通式[i]或[ii]表示的化合物与含有属于元素周期表中第9、10或11族的过渡金属如镍、钯、钴、铜或铑的过渡金属化合物接触得到的反应产物,即由通式[iii]表示的金属配合物(以下可称为金属配合物[iii]),和在作为催化剂组分的所述金属配合物存在下制备(a)α-烯烃的聚合物或共聚物的方法,以及在作为催化剂组分的所述金属配合物存在下制备(a)α-烯烃和(b)(甲基)丙烯酸酯单体、乙烯基单体或烯丙基单体的共聚物的方法。
在本发明中,"聚合"是一种单体的均聚和多种单体的共聚合的统称,并且这两种情况简单地描述为"聚合",特别是当两种情况都不需要区分时。此外,在本发明中,"(甲基)丙烯酸酯"包括丙烯酸酯和甲基丙烯酸酯。
2-1.金属配合物
本发明的第二实施方式的金属配合物是可通过使下述通式[i]或[ii]表示的化合物与含有属于元素周期表中第9、10或11族的过渡金属的过渡金属化合物接触得到的:
在本发明中,"接触"表示由通式[i]和[ii]表示的化合物(以下,它们可统称为磷苯酚盐化合物)和过渡金属化合物彼此非常接近的存在,以使得通式[i]或[ii]中的e1可与所述过渡金属形成配位键,和/或通式中的x1可与所述过渡金属形成单键。此外,使磷苯酚盐化合物与过渡金属化合物接触表示将这些化合物混合以使得这些化合物彼此非常接近地存在并且可以形成所述两种键中的至少一种。
混合磷苯酚盐化合物和过渡金属化合物的条件没有特别限制。这些化合物可以直接混合或使用溶剂进行混合。特别是从实现均匀混合的观点,优选使用溶剂。
在如此得到的金属配合物中,所述磷苯酚盐化合物变成配体。因此,所述磷苯酚盐化合物与过渡金属化合物之间的反应通常是配体交换反应。当如此得到的金属配合物在热力学上比过渡金属化合物更稳定时,通过在室温(15℃至30℃)下混合磷苯酚盐化合物和过渡金属化合物来进行配体交换反应。另一方面,当如此得到的金属配合物在热力学上不如过渡金属化合物稳定时,优选适当地加热所述混合物以致配体交换反应充分地进行。
据估计,可通过使由通式[i]或[ii]表示的化合物与含有属于元素周期表中第9、10或11族的过渡金属的过渡金属化合物接触得到的金属配合物具有由下述通式[iii]表示的结构。
然而,当所述磷苯酚盐化合物与含有属于元素周期表中第9、10或11族的过渡金属的过渡金属化合物接触时,存在会生成具有不同于通式[iii]表示的结构的结构的金属配合物的可能性,这是因为由通式[i]或[ii]表示的化合物是二齿配体。例如,可能是下述情况:其中仅通式[i]或[ii]中的x1与过渡金属形成键,或其中仅该式中的e1可与过渡金属形成键。由通式[iii]表示的金属配合物是所述磷苯酚盐化合物与过渡金属化合物的1:1反应产物。取决于过渡金属的类型,可能有其中得到具有不同组成比例的反应产物的情形。例如,可能有其中磷苯酚盐化合物的一个或多个分子与一个过渡金属形成配合物的情形,或可能有其中磷苯酚盐化合物的一个分子与两个或多个过渡金属反应以合成多核配合物的情形。
在本发明中,没有否认具有不同于由通式[iii]表示的结构的结构的金属配合物可用于与由通式[iii]表示的金属配合物一样制备α-烯烃(共)聚合物。
以下,将描述通式[i]和[ii]中的r1至r6、e1和x1以及通式[i]中的z和m。
r2、r3和r4各自独立地表示(i)氢、(ii)卤素、(iii)任选具有选自由杂原子和含有杂原子的基团组成的组中的成员的特定基团,或(iv)含有杂原子的取代基。
作为(ii)卤素,实例包括氟原子、氯原子、溴原子和碘原子。其中,氟原子是优选的。
作为(iii)中使用的杂原子,实例包括氧、氮、磷、硫、硒、硅、卤素和硼。这些杂原子中,氟和氯是优选的。
作为(iii)中使用的"含有杂原子的基团",特别是,可提及与以下描述的(iv)含有杂原子的取代基类似的基团。作为"含有杂原子的基团",提供烷氧基(or9)、酯基(co2r9)等。r9如下所述。
对于(iii),对应于r2至r4的取代基的碳原子总数优选为1至30,更优选为2至25,还更优选为4至20。
按照上述,(iii)"任选具有选自由杂原子和含有杂原子的基团组成的组中的成员的特定基团"表示(iii-a)具有1至30个碳原子的直链状烷基、具有3至30个碳原子的支链非环状烷基、具有2至30个碳原子的烯基、具有3至30个碳原子且任选具有侧链的环烷基、具有6至30个碳原子的芳基、具有7至30个碳原子的芳烷基、和具有7至30个碳原子的烷芳基;(iii-b)其中一个或两个或更多杂原子通过取代与(iii-a)中的各基团结合的基团;(iii-c)其中一个或两个或更多上述"含有杂原子的基团"通过取代与(iii-a)中的各基团结合的基团;和(iii-d)其中一个或两个或更多的上述杂原子和一个或两个或更多的上述"含有杂原子的基团"通过取代与(iii-a)中的各基团结合的基团。对于(iii-c),实例包括通过取代结合了烷氧基的烷基,和通过取代结合了酯基的芳基,等等。
特别是,(iv)含有杂原子的取代基表示or9、co2r9、co2m’、c(o)n(r8)2、c(o)r9、sr9、so2r9、sor9、oso2r9、p(o)(or9)2-y(r8)y、cn、nhr9、n(r9)2、si(or8)3-x(r8)x、osi(or8)3-x(r8)x、no2、so3m’、po3m’2、p(o)(or2)2m’和含环氧基的基团。r8表示氢或具有1至20个碳原子的烃基。r9表示具有1至20个碳原子的烃基。m’表示碱金属、碱土金属、铵、季铵或鏻。此外,x表示0至3的整数,和y表示0至2的整数。
优选r2、r3和r4各自独立地表示(i)氢原子;(ii)氟原子、氯原子、溴原子;(iii)甲基、乙基、异丙基、丁基、苯基、三氟甲基、五氟苯基、萘基、蒽基;(iv)甲氧基、乙氧基、苯氧基、腈基、三甲基甲硅烷基、三乙基甲硅烷基、二甲基苯基甲硅烷基、三甲氧基甲硅烷基、三乙氧基甲硅烷基、三甲基甲硅烷基氧基、三甲氧基甲硅烷氧基、环己基氨基、磺酸钠、磺酸钾、磷酸钠、磷酸钾等。
它们之中,特别优选的是(i)氢原子;(iii)叔丁基、五氟苯基;(iv)甲氧基、三甲基甲硅烷基、三甲基甲硅烷基氧基、环己基氨基等。特别是,r3优选是氢或具有1至30个碳原子且具有含有杂原子的取代基的直链状烷基,r3更优选是氢。
r1表示(v)具有选自由杂原子和含有杂原子的基团组成的组中的成员的特定基团,或(vi)含有杂原子的取代基。
特别是,(v)具有选自由杂原子和含有杂原子的基团组成的组中的成员的特定基团是指选自由下述组成的组的烃基:具有1至30个碳原子的直链状烷基、具有3至30个碳原子的支链非环状烷基、具有2至30个碳原子的烯基、具有3至30个碳原子且任选具有侧链的环烷基、具有6至30个碳原子的芳基、具有7至30个碳原子的芳烷基、和具有7至30个碳原子的烷芳基,并且含有杂原子的取代基通过取代结合至所述烃基。它们之中,r1优选是具有6至30个碳原子且具有选自由杂原子和含有杂原子的基团组成的组中的成员的芳基。
对于所述直链状烷基、支链非环状烷基、烯基、任选具有侧链的环烷基、芳基、芳烷基和烷芳基中每一个,碳原子数的上限优选是25,更优选20,仍更优选15。
特别是,(vi)含有杂原子的取代基表示or9、co2r9、co2m’、c(o)n(r8)2、c(o)r9、sr9、so2r9、sor9、oso2r9、p(o)(or9)2-y(r8)y、cn、nhr9、n(r9)2、si(or8)3-x(r8)x、osi(or8)3-x(r8)x、no2、so3m’、po3m’2、p(o)(or2)2m’和含环氧基的基团。r8、r9、m’、x和y与上述r2至r4的情况相同。它们之中,r1优选是si(or8)3-x(r8)x。
作为r1,更优选的是(v)三氟甲基、五氟苯基、咔唑基和(vi)甲氧基、乙氧基、苯氧基、腈基、三甲基甲硅烷基、三乙基甲硅烷基、二甲基苯基甲硅烷基、三甲氧基甲硅烷基、三乙氧基甲硅烷基、三甲基甲硅烷基氧基、三甲氧基甲硅烷氧基、环己基氨基、磺酸钠、磺酸钾、磷酸钠、磷酸钾等。
它们之中,特别优选的是(v)五氟苯基、咔唑基和(vi)甲氧基、三甲基甲硅烷基、三甲基甲硅烷基氧基、环己基氨基等。
适当地选自r1、r2、r3和r4的多个基团任选彼此结合以形成脂环、芳环或含有选自由氧、氮和硫组成的组的杂原子的杂环。在这种情况下,环成员的数量为5至8,和所述环任选在其上具有取代基。
r1中含有的多个基团可以彼此结合以形成在r1上的环。即使r2、r3和r4中任一个含有多个基团时,这也同样适用。
r5和r6各自独立地表示具有1至6个碳原子的直链状烷基、具有3至6个碳原子的支链非环状烷基、或具有2至6个碳原子的烯基,每个所述基团任选具有选自由杂原子和含有杂原子的基团组成的组的成员;
r5和r6任选彼此结合以形成脂环、芳环或含有选自由氧、氮和硫组成的组的杂原子的杂环,并且在这种情况下,环成员的数量为5至8,和所述环任选在其上具有取代基;
r5和r6位于金属m的附近,并且通过立体的和/或电子相互作用影响m。为了具有这种效果,r5和r6优选是体积大的。
r5和r6的优选具体实例包括异丁基、叔丁基、环己基、新戊基、戊烷-3-基等。它们之中,叔丁基是更优选的。
作为用作r5和r6的杂原子,实例包括氧、氮、磷、硫、硒、硅、卤素和硼。这些杂原子中,氟和氯是优选的。此外,含有这些杂原子的基团包括:包括烷氧基、芳氧基、酰基和酯基的含氧基团;包括氨基和酰胺基的含氮基团;包括硫代烷氧基和硫代芳氧基的含硫基团;包括膦基的含磷取代基;包括甲硒烷基的含硒基团;包括三烷基甲硅烷基、二烷基芳基甲硅烷基和烷基二芳基甲硅烷基的含硅基团;包括氟烷基和氟芳基的含氟基团;和包括烷基硼基和芳基硼基的含硼基团。这些含有杂原子的基团之中,烷氧基或芳氧基是最优选的。
作为上述含有杂原子的基团中含有的杂原子,能够与过渡金属配位的杂原子是优选的。含有这种能够与过渡金属配位的杂原子的含有杂原子的基团的具体实例包括下述基团。
即,可提及含氧基团,包括烷氧基如甲氧基、乙氧基、正丙氧基、异丙氧基、正丁氧基和叔丁氧基,芳氧基如苯氧基、对甲基苯氧基和对甲氧基苯氧基,酰基如乙酰基和苯甲酰基,和酯基如乙酰氧基、羧基乙基、羧基叔丁基和羧基苯基;含氮基团,包括二烷基氨基如二甲基氨基、二乙基氨基、二正丙基氨基和环己基氨基;含硫基团,包括硫代烷氧基如硫代甲氧基、硫代乙氧基、硫代正丙氧基、硫代异丙氧基、硫代正丁氧基、硫代叔丁氧基和硫代苯氧基,和硫代芳氧基如对甲基硫代苯氧基和对甲氧基硫代苯氧基;含磷取代基,包括二烷基膦基如二甲基膦基、二乙基膦基、二正丙基膦基和环己基膦基;和含硒基团,包括甲硒烷基如甲基甲硒烷基、乙基甲硒烷基、正丙基甲硒烷基、正丁基甲硒烷基、叔丁基甲硒烷基和苯基甲硒烷基。
e1表示磷、砷或锑。它们之中,e1优选是磷。
x1表示氧或硫。它们之中,x1优选是氧。
z表示氢或离去基团。z的具体实例包括氢原子、r9so2基团(其中r9如上所述)、cf3so2基团等。
此外,m表示z的化合价。
通式[ii]以阴离子形式示出。作为其抗衡阳离子,可以使用任何阳离子,只要该阳离子不抑制与本发明的过渡金属化合物的反应即可。所述抗衡阳离子的具体实例包括铵、季铵或鏻,以及元素周期表中第1至14族的金属离子。这些阳离子之中,nh4+、r94n+(其中r9如上所述,四个r9可以彼此相同或不同(以下同样适用))、r94p+、li+、na+、k+、mg2+、ca2+和al3+是优选的,r94n+、li+、na+和k+是更优选的。
下述表2-1示出本发明的通式[i]和[ii]中取代基的具体组合。z和m仅涉及通式[i]。然而,具体实例不限于下述实例。
【表2-1】
为了理解化合物的结构,示出了上表2-1中列出的化合物1的结构式和名称。由所述结构式表示的化合物将称为2-(二叔丁基膦基)-6-五氟苯基苯酚。
由通式[i]和[ii]表示的化合物可以通过已知的合成法来合成。
由下述通式[iii]表示的本发明的第二实施方式的金属配合物包括在由通式[i]或[ii]表示的化合物与含有属于元素周期表中第9、10或11族的过渡金属的过渡金属化合物的反应产物中。然而,如上所述,通过所述制备方法得到的金属配合物的结构不限于由通式[iii]表示的结构。
在通式[iii]中,r1至r6、e1和x1如上所述。如上所述,就含有苯环和这些取代基(r1至r6、e1和x1)的主骨架而言,反应产物中的金属配合物的配合结构与由通式[iii]表示的金属配合物的配合结构之间存在相似性。
以下,将描述通式[iii]中的m、r7和l1。
在本发明的第二实施方式中,m为属于元素周期表中第9、10或11族的过渡金属。m优选是第10族中的镍、钯和铂,第9族中的钴和铑,和第11族中的铜,更优选第10族中的镍、钯和铂,最优选第10族中的镍或钯。
m的化合价优选是二价。m的化合价是指有机金属化学中使用的形式氧化数。即,当包括某些元素的键中的电子对分配给具有更大电负性的元素时,化合价是指残留在所述元素原子上的电荷数。例如,在本发明的第二实施方式的通式[iii]中,当e1是磷,x1是氧,m是镍,r7是苯基,l1是吡啶以及镍与磷、氧、苯基的碳和吡啶的氮形成键时,镍的形式氧化数即镍的化合价变成二价。理由如下:根据上述定义,在这些键中,电子对分配给具有比镍更大的电负性的磷、氧、碳和氮,磷的电荷变成0,氧的电荷变成-1,苯基的电荷变成-1,和吡啶的电荷变成0,所述配合物整体上是电中性的;因此,残留在镍上的电荷变成+2。
作为二价过渡金属,例如,镍(ii)、钯(ii)、铂(ii)和钴(ii)是优选的。作为除二价过渡金属以外的过渡金属,铜(i)或铑(iii)也是优选的。
在本发明的第二实施方式中,r7表示氢或具有1至20个碳原子且任选具有选自由杂原子和含有杂原子的基团组成的组的成员的烃基。本发明中的聚合或共聚合被认为是通过将本发明的组分(a)或组分(b)插入到m和r7的键中来引发。因此,当r7的碳原子数过大时,倾向于抑制该引发反应。为此,不包括取代基中含有的碳原子的r7的碳原子数优选是1至16,更优选1至10。
r7的具体实例包括氢化物基团、甲基、乙基、正丙基、异丙基、正丁基、异丁基、正己基、正辛基、正癸基、正十二烷基、环戊基、环己基、苄基、苯基、对甲基苯基、三甲基甲硅烷基、三乙基甲硅烷基、三苯基甲硅烷基等。
在本发明中,l1表示配位至m的配体。本发明中的配体l1是具有1至20个碳原子且具有作为能够形成配位键的原子的氧、氮或硫的烃化合物。此外,作为l1,可使用具有能够与过渡金属形成配位键的碳碳不饱和键(并且任选含有杂原子)的烃化合物。l1的碳原子数优选是1至16,更优选1至10。此外,作为与通式[iii]中的m形成配位键的l1,没有电荷的化合物是优选的。
在本发明中,优选作为l1的是环状不饱和烃、膦、吡啶、哌啶、烷基醚、芳基醚、烷基芳基醚、环状醚、烷基腈衍生物、芳基腈衍生物、醇、酰胺、脂族酯、芳族酯、胺等。更优选作为l1的是环烯烃、膦、吡啶、环状醚、脂族酯、芳族酯等。特别优选作为l1的是三烷基膦、吡啶、卢剔啶(二甲基吡啶)、皮考啉(甲基吡啶)和r9co2r8(r8和r9的定义如上所述)。
r7和l1可以彼此结合形成环。这种实例是环辛-1-烯基,该基团也是本发明中优选的实施方式。
下表2-2示出本发明的通式[iii]中的取代基的具体组合。然而,具体实例不限于下述实例。
【表2-2】
为了理解金属配合物的结构,示出了上表2-2中列出的配合物1b的结构式和名称。由所述结构式表示的化合物将称为(2-(二叔丁基膦基)-6-五氟苯基苯酚盐)苯基(三乙基膦)镍(ii)。
此外,举例说明表2-2中列出的化合物的中心金属m从镍变成钯的化合物。
对于本发明中使用的过渡金属化合物,使用能够与由通式[i]或[ii]表示的化合物反应形成具有聚合能力的配合物的那些。它们有时称为前驱体。
例如,作为含有镍的过渡金属化合物,可使用双(1,5-环辛二烯)镍(0),由通式ni(ch2cr13ch2)2表示的配合物[其中r13表示氢原子、卤素原子、具有1至30个碳原子且任选含有杂原子的烃基、or8、co2r8、co2m’、c(o)n(r9)2、c(o)r8、sr8、so2r8、sor8、oso2r8、p(o)(or8)2-y(r9)y、cn、nhr8、n(r8)2、si(or9)3-x(r9)x、osi(or9)3-x(r9)x、no2、so3m’、po3m’2、p(o)(or8)2m’或含环氧基的基团(其中r8表示具有1至20个碳原子的烃基;r9表示氢原子或具有1至20个碳原子的烃基;m’表示碱金属、碱土金属、铵、季铵或鏻;x表示0至3的整数;和y表示0至2的整数)],双(环戊二烯基)镍(ii),由通式ni(ch2sir133)2l12表示的配合物(其中r13和l1如上所述),由通式nir132l12表示的配合物(其中r13和l1如上所述)等。
此外,作为含有属于第9、10或11族的过渡金属的过渡金属化合物,可使用通式mr13pl1q(其中m表示第9、10或11族的过渡金属;r13和l1如上所述;p和q各自是满足m的化合价的0或更大的整数)。
这些过渡金属化合物之中,优选使用的是双(1,5-环辛二烯)镍(0)、niphcl(pet3)2、niphcl(pph3)2、niphcl(tmeda)(以下tmeda表示四甲基乙二胺)、由通式ni(ch2cr13ch2)2表示的配合物(其中r13如上所述)、由通式ni(ch2sir133)2l12表示的配合物(其中r13和l1如上所述)、由通式nir132l12表示的配合物(其中r13和l1如上所述)、pd(dba)2、pd2(dba)3、pd3(dba)4(其中dba表示二苄叉基丙酮)、pd(ococh3)2和(1,5-环辛二烯)pd(甲基)(氯化物)。
特别优选的是双(1,5-环辛二烯)镍(0)、niphcl(pet3)2、niphcl(pph3)2、niphcl(tmeda)、ni(ch2chch2)2、ni(ch2cmech2)2、ni(ch2sime3)2(py)2(以下,py表示吡啶)、ni(ch2sime3)2(lut)2(以下,lut表示2,6-卢剔啶))、niph2(py)2、niph2(lut)2、pd(dba)2、pd2(dba)3、pd3(dba)4(其中dba表示二苄叉基丙酮))、pd(ococh3)2、和(1,5-环辛二烯)pd(甲基)(氯化物)。
本发明的反应产物可以通过将由通式[i]或[ii]表示的上述化合物与上述过渡金属化合物[iv]例如以[i]+[ii]:[iv]=[1:99]至[99:1]的摩尔比在有机溶剂如甲苯或苯中,在0℃至100℃下,在减压至加压下接触1至86400秒来获得。当双(1,5-环辛二烯)镍(0)(ni(cod)2)在甲苯或苯中的溶液用作所述过渡金属化合物时,可以通过溶液从黄色至例如红色的变色来确认形成所述反应产物。
在本反应之后,构成过渡金属化合物但不是所述化合物的过渡金属的组分被除z以外的通式[i]的一部分或由通式[ii]表示的化合物取代,从而形成由本发明的通式[iii]表示的金属配合物。该取代反应优选定量进行;然而,在有些情况下,其可以进行不完全。在反应完成之后,除由通式[iii]表示的配合物之外,还存在衍生自通式[i]和[ii]的其他组分以及所述过渡金属化合物。当进行本发明的聚合反应或共聚合反应时,可以除去或保留这些其他组分。通常,优选除去这些其他组分,因为可以获得更高的活性。
当进行反应时,本发明的l1可以一起存在。当镍或钯用作本发明的m时,纯化的由通式[iii]表示的配合物的稳定性有时通过在体系中共存具有路易斯碱性质的l1而得到改善。在这种情况下,l1的共存是优选的,只要l1不抑制本发明的聚合反应或共聚合反应即可。
在本发明中,所述反应可以预先在不同于用于α-烯烃聚合或α-烯烃与(甲基)丙烯酸酯的共聚合的反应器的容器中进行,然后如此得到的由通式[iii]表示的配合物可用于α-烯烃的聚合或α-烯烃与(甲基)丙烯酸酯的共聚合,或所述反应可以在这些单体存在下进行。此外,所述反应可以在用于α-烯烃聚合或α-烯烃与(甲基)丙烯酸酯的共聚合的反应器中进行。在这种情况下,这些单体可以存在或不存在。作为由通式[i]和[ii]表示的每种组分,可以使用单一组分,或者可以组合使用多种组分。特别是,为了拓宽分子量分布或共聚单体含量分布,这种多种组分的组合使用是有用的。
2-2.金属配合物的制备方法
在本发明的第二实施方式的制备方法中,如上所述,由通式[iii]表示的金属配合物可以通过使通式[i]或[ii]表示的化合物与含有属于元素周期表中第9、10或11族的过渡金属的过渡金属化合物接触来制备。
2-3.用于烯烃聚合的催化剂组分
根据本发明的第二实施方式的用于烯烃聚合的催化剂组分包含上述金属配合物或可通过上述制备方法得到的金属配合物。
在本发明的第二实施方式中,由通式[iii]表示的金属配合物可用作用于聚合或共聚合的催化剂组分。如以上所述,由通式[iii]表示的金属配合物可以通过使通式[i]或[ii]与所述过渡金属配合物组分反应来形成。当由通式[iii]表示的金属配合物用作催化剂组分时,可以使用分离的金属配合物,或者可以使用负载在载体上的金属配合物。这种负载可以在用于α-烯烃聚合或α-烯烃与(甲基)丙烯酸酯共聚合的反应器中,在这些单体存在或不存在下进行,或者可以在不同于所述反应器的容器中进行。
作为可使用的载体,可使用任何载体,只要所述载体不损害本发明的范围即可。通常,可适当地使用无机氧化物和聚合物载体。特别是,可提及sio2、al2o3、mgo、zro2、tio2、b2o3、cao、zno、bao、tho2等,或它们的混合物。此外,可使用混合氧化物如sio2-al2o3、sio2-v2o5、sio2-tio2、sio2-mgo和sio2-cr2o3,并且可使用无机硅酸盐、聚乙烯载体、聚丙烯载体、聚苯乙烯载体、聚丙烯酸载体、聚甲基丙烯酸载体、聚丙烯酸酯载体、聚酯载体、聚酰胺载体、聚酰亚胺载体等。对于这些载体,粒径、粒径分布、孔容积、比表面积等没有特别限制,可使用任何载体。
作为无机硅酸盐,可使用粘土、粘土矿物、沸石、硅藻土等。对于这些物质,可以使用合成材料,或可以使用天然存在的矿物。粘土和粘土矿物的具体实例包括水铝英石类如水铝英石;高岭土类如地开石、珍珠陶土、高岭土和钙长石;埃洛石类如变埃洛石和埃洛石;蛇纹石类如纤蛇纹石、利蛇纹石和叶蛇纹石;蒙脱石类如蒙脱土、锌蒙脱石、贝得石、绿脱石、皂石和锂蒙脱石;蛭石矿物如蛭石;云母矿物如伊利石、绢云母和海绿石;绿坡缕石;海泡石;坡缕石;膨润土;木节土;gaerome粘土;硅铁石;叶蜡石;和绿泥石类。这些物质可形成混合层。人造化合物包括合成云母、合成锂蒙脱石、合成皂石和合成带云母。这些具体实例之中,优选的是高岭土类如地开石、珍珠陶土、高岭土和钙长石;埃洛石类如变埃洛石和埃洛石;蛇纹石类如纤蛇纹石、利蛇纹石和叶蛇纹石;蒙脱石类如蒙脱土、zaukonite、贝得石、绿脱石、皂石和锂蒙脱石;蛭石矿物如蛭石;云母矿物如伊利石、绢云母和海绿石;合成云母;合成锂蒙脱石;合成皂石;和合成带云母。特别优选的是蒙脱石类如蒙脱土、zaukonite、贝得石、绿脱石、皂石和锂蒙脱石;蛭石矿物如蛭石;合成云母;合成锂蒙脱石;合成皂石;和合成带云母。
这些载体可以原样使用,或者可以用盐酸、硝酸、硫酸等进行酸处理,和/或使用licl、nacl、kcl、cacl2、mgcl2、li2so4、mgso4、znso4、ti(so4)2、zr(so4)2、al2(so4)3等进行盐处理。所述处理可以通过将相应的酸和碱混合以在反应体系中形成盐来进行。此外,可以进行如粉碎和造粒等形状控制或干燥处理。
2-4.用于烯烃聚合的催化剂
根据本发明的第二实施方式的用于烯烃聚合的催化剂包含下述组分(a)和(b),和根据需要的下述组分(c):
组分(a):上述金属配合物或可通过上述制备方法得到的金属配合物
组分(b):可与组分(a)反应形成离子对的化合物,或离子交换性层状硅酸盐
组分(c):有机铝化合物。
所述组分(a)是上述金属配合物或可通过上述制备方法得到的金属配合物。可单独使用一种金属配合物,或可组合使用两种或多种金属配合物。
所述组分(b)的实例是有机铝氧化合物。所述有机铝氧化合物在分子中具有al-o-al键,和所述键的数量在通常1至100的范围内,优选1至50。这种有机铝氧化合物通常是可通过使有机铝化合物与水反应得到的产物。
有机铝与水的反应通常在惰性烃类(溶剂)中进行。作为惰性烃类,可使用脂族烃、脂环族烃和芳族烃如戊烷、己烷、庚烷、环己烷、甲基环己烷、苯、甲苯和二甲苯。优选使用脂族烃或芳族烃。
作为用于制备所述有机铝氧化合物的有机铝化合物,可使用由下述通式表示的化合物。优选使用三烷基铝。
(rx)tal(x3)(3-t)
(其中rx表示烃基如各自具有1至18个碳原子、优选1至12个碳原子的烷基、烯基、芳基和芳烷基;x3表示氢原子或卤素原子;和t表示1≤t≤3的整数。)
三烷基铝中的烷基可以是甲基、乙基、丙基、异丙基、丁基、异丁基、戊基、己基、辛基、癸基、十二烷基等中任何烷基。优选的是甲基和异丁基,特别优选的是甲基。可混合和使用两种或多种所述有机铝化合物。
水与有机铝化合物的反应比例(水/al的摩尔比)优选是0.25/1至1.2/1,特别优选0.5/1至1/1。反应温度通常在-70℃至100℃的范围内,优选-20℃至20℃。通常在5分钟至24小时、优选10分钟至5小时的范围内选择反应时间。作为反应所需的水,不仅可以使用简单的水,而且可以使用硫酸铜水合物、硫酸铝水合物等中含有的水合水,以及可以在反应体系中产生水的组分。
上述有机铝氧化合物之中,可通过烷基铝与水反应得到的有机铝氧化合物通常称为铝氧烷。甲基铝氧烷(包括基本上由甲基铝氧烷(mao)组成的那些)特别优选作为所述有机铝氧化合物。此外,固体形式的干燥甲基铝氧烷(dmao),其通过将溶剂从mao溶液中去除而得到,是优选的。
作为有机铝氧化合物,可以组合使用两种或多种上述有机铝氧化合物,或者可以使用溶解或分散在上述惰性烃溶剂中的有机铝氧化合物的溶液。
所述组分(b)的具体实例是离子交换性层状硅酸盐。离子交换性层状硅酸盐(以下可简称为"硅酸盐")是具有其中由离子键合等形成的平面彼此平行定位并由结合力堆叠的晶体结构且其中所含有的离子可交换的硅酸盐化合物。作为所述硅酸盐,各种通常已知的硅酸盐是已知的,所述硅酸盐详细描述在"nendokobutsugaku",haruoshirozu,asakurapublishingco.,ltd.(1995)中。
在本发明中,作为组分(b),优选使用属于蒙脱石类的那些。其具体实例包括蒙脱土、锌蒙脱石、贝得石、绿脱石、皂石、锂蒙脱石、镁皂石等。它们之中,从增大共聚物部分的聚合活性和分子量的观点,优选蒙脱土。
大多数硅酸盐主要作为天然粘土矿物的主要成分生产。因此,经常含有除所述离子交换性层状硅酸盐以外的夹杂物(如石英和方英石)。用于本发明的蒙脱石类的硅酸盐可以含有夹杂物。
所述硅酸盐可以进行酸处理和/或盐处理。所述处理可以通过将相应的酸和碱混合以在反应体系中形成盐来进行。
作为组分(b),可以使用上述有机铝氧化合物和离子交换性层状硅酸盐的混合物。此外,作为所述有机铝氧化合物和离子交换性层状硅酸盐,可以使用一种所述化合物和硅酸盐,或两种或多种所述化合物和硅酸盐。
用作组分(c)的有机铝化合物的实例由下述通式表示:
al(rp)ax(3-a)
其中rp表示具有1至20个碳原子的烃基;x表示氢、卤素、烷氧基或甲硅烷氧基;和a为大于0且等于或小于3的数。
由所述通式表示的有机铝化合物的具体实例包括三烷基铝如三甲基铝、三乙基铝、三丙基铝、三异丁基铝等,和含有卤素或烷氧基的烷基铝如二乙基铝一氯化物、二乙基铝单甲醚等。
它们之中,三异丁基铝是优选的。此外,可以组合使用两种或多种上述有机铝化合物。此外,上述铝化合物可以用醇、苯酚等改性来使用。作为改性剂,例举甲醇、乙醇、1-丙醇、异丙醇、丁醇、苯酚、2,6-二甲苯酚、2,6-二叔丁基苯酚等。优选的具体实例是2,6-二甲基苯酚和2,6-二叔丁基苯酚。
在根据本发明的第二实施方式的用于烯烃聚合的催化剂的制备方法中,所述组分(a)、组分(b)和根据需要的组分(c)的接触方法没有特别限制。例如,可提供下述方法。
方法(i):组分(a)和组分(b)彼此接触,然后添加组分(c)。
方法(ii):组分(a)和组分(c)彼此接触,然后添加组分(b)。
方法(iii):组分(b)和组分(c)彼此接触,然后添加组分(a)。
方法(iv):组分(a)、(b)和(c)彼此同时接触。
此外,每种组分可以通过将其与不同种类的组分混合而作为混合物使用,或者可以以不同的顺序单独接触。所述接触不仅可以在催化剂制备时进行,也可以在使用烯烃进行预聚合时或烯烃聚合时进行。
另外,可以将一种组分分开并与每种组分接触,例如,以使组分(b)和组分(c)彼此接触,然后添加组分(a)和组分(c)的混合物的方式。
所述组分(a)、(b)和(c)的接触优选在惰性气体气氛如氮气等和在惰性烃溶剂如戊烷、己烷、庚烷、甲苯、二甲苯等中进行。所述接触可以在-20℃至溶剂的沸点之间的温度下进行,特别优选在室温至溶剂的沸点之间的温度下进行。
2-5.α-烯烃聚合物的制备方法
本发明的第二实施方式的α-烯烃聚合物的制备方法的实施方式是(a)α-烯烃在用于聚合的催化剂存在下聚合或共聚合。
本发明中的组分(a)是由通式ch2=chr10表示的α-烯烃。r10是氢原子或具有1至20个碳原子的烃基,其可具有支链、环和/或不饱和键。当r10的碳原子数大于20时,倾向于较少显示聚合活性。为此,它们之中,r10是氢原子或具有1至10个碳原子的烃基的α-烯烃优选作为组分(a)。
更优选作为组分(a)的那些包括乙烯、丙烯、1-丁烯、1-戊烯、1-己烯、1-辛烯、1-癸烯、3-甲基-1-丁烯、4-甲基-1-戊烯、乙烯基环己烯和苯乙烯。作为组分(a),可以使用单一组分,或者可以组合使用多种组分。
本发明的α-烯烃聚合物的制备方法的另一实施方式是(a)α-烯烃和(b)(甲基)丙烯酸酯单体、乙烯基单体或烯丙基单体在上述用于聚合的催化剂存在下共聚合。
本发明中的(甲基)丙烯酸酯单体由通式ch2=c(r11)co2(r12)表示。r11是氢原子或具有1至10个碳原子的烃基,其可具有支链、环和/或不饱和键。r12是具有1至30个碳原子的烃基,其可具有支链、环和/或不饱和键。此外,r12可在其中任何位置含有杂原子。
当r11的碳原子数是11以上时,倾向于较少显示聚合活性。因此,r11是氢原子或具有1至10个碳原子的烃基,优选的(甲基)丙烯酸酯包括其中r11是氢原子或具有1至5个碳原子的烃基的(甲基)丙烯酸酯。更优选的(甲基)丙烯酸酯单体包括r11是甲基的甲基丙烯酸酯或r11是氢原子的丙烯酸酯。类似地,当r12的碳原子数大于30时,倾向于较少显示聚合活性。因此,r12的碳原子数是1至30,优选是1至12,更优选1至8。
此外,作为r12中任选含有的杂原子,提供氧、硫、硒、磷、氮、硅、氟、硼等。这些杂原子之中,氧、硅和氟是优选的,并且氧是更优选的。另外,不含杂原子的r12也是优选的。
还更优选的(甲基)丙烯酸酯单体包括(甲基)丙烯酸甲酯、(甲基)丙烯酸乙酯、(甲基)丙烯酸正丙酯、(甲基)丙烯酸异丙酯、(甲基)丙烯酸正丁酯、(甲基)丙烯酸异丁酯、(甲基)丙烯酸叔丁酯、(甲基)丙烯酸戊酯、(甲基)丙烯酸己酯、(甲基)丙烯酸环己酯、(甲基)丙烯酸辛酯、(甲基)丙烯酸2-乙基己酯、(甲基)丙烯酸壬酯、(甲基)丙烯酸癸酯、(甲基)丙烯酸十二烷基酯、(甲基)丙烯酸苯酯、(甲基)丙烯酸甲苯酰酯、(甲基)丙烯酸苄基酯、(甲基)丙烯酸羟乙酯、(甲基)丙烯酸二甲基氨基乙酯、(甲基)丙烯酸二乙基氨基乙酯、(甲基)丙烯酸-2-氨基乙酯、(甲基)丙烯酸2-甲氧基乙酯、(甲基)丙烯酸-3-甲氧基丙酯、(甲基)丙烯酸缩水甘油基酯、(甲基)丙烯酸环氧乙烷酯、(甲基)丙烯酸三氟甲基酯、(甲基)丙烯酸2-三氟甲基乙基酯、(甲基)丙烯酸全氟乙基酯、(甲基)丙烯酰胺、(甲基)丙烯酰基二甲基酰胺、(甲基)丙烯酸2-羟基丁酯、(甲基)丙烯酸4-羟基丁酯等。(甲基)丙烯酸酯可以单独使用,或多种(甲基)丙烯酸酯可以组合使用。
本发明中的乙烯基单体是含有极性基团的乙烯基单体,如含卤素、含氮、含氧和含硫的乙烯基单体。特别是,其是含有卤素、羟基、氨基、硝基、羧基、醛基、酯基、环氧基、腈基等的乙烯基单体。其具体实例包括5-己烯-1-醇、2-甲基-3-丁烯-1-醇、10-十一碳烯酸乙酯、10-十一碳烯-1-醇、12-十三碳烯-2-醇、10-十一烷酸、甲基-9-癸烯酸酯、叔丁基-10-十一碳烯酸酯、1,1-二甲基-2-丙烯-1-醇、9-癸烯-1-醇、3-丁烯酸、3-丁烯-1-醇、n-(3-丁烯-1-基)邻苯二甲酰亚胺、5-己烯酸、5-己烯酸甲酯、5-己烯-2-酮、丙烯腈、甲基丙烯腈、醋酸乙烯酯、三乙氧基乙烯基硅烷等。它们之中,3-丁烯-1-醇、10-十一碳烯酸乙酯、10-十一碳烯-1-醇和三乙氧基乙烯基硅烷是特别优选的。
作为本发明中的烯丙基单体,实例包括具有3个碳原子的烯丙基单体(丙烯基单体)和作为具有4个或更多碳原子和烯丙基的含烯丙基单体的烯丙基系单体。所述烯丙基单体是含有极性基团的烯丙基单体,如含卤素、含氮、含氧和含硫的烯丙基单体。特别是,其是含有卤素、羟基、氨基、硝基、羧基、醛基、酯基、环氧基、腈基等的乙烯基单体。其优选的具体实例包括乙酸烯丙酯、烯丙醇、烯丙胺、n-烯丙基苯胺、n-叔丁氧基羰基-n-烯丙胺、n-苄氧基羰基-n-烯丙胺、n-烯丙基-n-苄胺、烯丙基氯、烯丙基溴、烯丙基醚、二烯丙基醚等。它们之中,乙酸烯丙酯和烯丙醇是更优选的,乙酸烯丙酯、烯丙基醚和二烯丙基醚是再更优选的。
本发明中的聚合反应是在存在或不存在液体下进行的,所述液体可以是:烃溶剂如丙烷、正丁烷、异丁烷、正己烷、正庚烷、甲苯、二甲苯、环己烷和甲基环己烷;或液化的α-烯烃;或极性溶剂如二乙基醚、乙二醇二甲醚、四氢呋喃、二氧杂环己烷、醋酸乙酯、苯甲酸甲酯、丙酮、甲基乙基酮、甲酰胺、乙腈、甲醇、异丙醇和乙二醇。此外,在此描述的液体化合物的混合物可用作溶剂。此外,离子液体也可以用作溶剂。更优选上述烃溶剂和离子液体以获得更高的聚合活性和高分子量。
在本发明中,聚合反应可在存在或不存在已知添加剂下进行。作为添加剂,抑制自由基聚合的聚合抑制剂和具有稳定制备的共聚物的作用的添加剂是优选的。优选的添加剂的实例包括醌衍生物、受阻酚衍生物等。具体地,可使用氢醌单甲醚、2,6-二叔丁基-4-甲基苯酚(bht)、三甲基铝和bht的反应产物、钛(iv)醇盐和bht的反应产物等。此外,所述聚合可以通过使用这种填料作为添加剂在无机和/或有机填料存在下进行。此外,涉及本发明的l1或离子液体可以用作添加剂。
本发明中优选的添加剂包括路易斯碱。通过选择适合的路易斯碱,可以改善活性、分子量和丙烯酸酯的共聚合反应性。相对于聚合体系中存在的催化剂组分中的过渡金属m,路易斯碱的量为0.0001至1000当量、优选0.1至100当量、更优选0.3至30当量。将路易斯碱添加至聚合体系的方法没有特别限制,可使用任何技术。例如,路易斯碱可以通过与本发明的催化剂组分混合来添加,或可以通过与单体混合来添加,或可以独立于催化剂组分和单体添加到聚合体系中。此外,可以组合使用多种路易斯碱。此外,可以使用与本发明相关的l1相同的路易斯碱,或者可以使用不同的路易斯碱。
路易斯碱包括芳族胺、脂族胺、烷基醚、芳基醚、烷基芳基醚、环状醚、烷基腈、芳基腈、醇、酰胺、脂族酯、芳族酯、磷酸酯、亚磷酸酯、噻吩、噻蒽、噻唑、噁唑、吗啉、环状不饱和烃等。它们之中,优选的路易斯碱是芳族胺、脂族胺、环状醚、脂族酯和芳族酯,特别优选的路易斯碱是吡啶衍生物、嘧啶衍生物、哌啶衍生物、咪唑衍生物、苯胺衍生物、哌啶衍生物、三嗪衍生物、吡咯衍生物和呋喃衍生物。
具体的路易斯碱化合物包括吡啶、五氟吡啶、2,6-卢剔啶、2,4-卢剔啶、3,5-卢剔啶、嘧啶、n,n-二甲基氨基吡啶、n-甲基咪唑、2,2'-联吡啶、苯胺、哌啶、1,3,5-三嗪、2,4,6-三(三氟甲基)-1,3,5-三嗪、2,4,6-三(2-吡啶基)-s-三嗪、喹啉、8-甲基喹啉、吩嗪、1,10-菲咯啉、n-甲基吡咯、1,8-二氮杂双环-[5.4.0]-十一碳-7-烯、1,4-二氮杂双环-[2.2.2]-辛烷、三乙胺、苄腈、皮考啉、三苯胺、n-甲基-2-吡咯烷酮、4-甲基吗啉、苯并噁唑、苯并噻唑、呋喃、2,5-二甲基呋喃、二苯并呋喃、呫吨、1,4-二氧杂环己烷、1,3,5-三氧杂环己烷、二苯并噻吩、噻蒽、三苯基鏻环戊二烯、三苯基亚磷酸酯、三苯基磷酸酯、三吡咯烷基膦、三(吡咯烷基)硼烷等。
在本发明中,聚合方式没有特别限制。优选使用其中生成的聚合物的至少一部分在介质中呈淤浆形式的淤浆聚合;其中液化单体本身用作介质的本体聚合;其中聚合在汽化单体中进行的气相聚合;或其中生成的聚合物的至少一部分溶解在高温高压下液化的单体中的高压离子聚合;等。此外,可以使用任何类型的间歇聚合、半间歇聚合和连续聚合。此外,可以进行活性聚合或与链转移一起发生的聚合。此外,链穿梭或配位链转移聚合(cctp)可以通过组合使用所谓的链转移剂(csa)来进行。
未反应的单体和介质可以通过将它们与制备的共聚物分离并回收它们来使用。在回收时,这些单体和介质可以在纯化或不纯化的情况下重复使用。为了将制备的共聚物与未反应的单体和介质分离,可以使用迄今已知的方法。例如,可以使用诸如过滤、离心、溶剂萃取或用不良溶剂再沉淀等的方法。
聚合温度、聚合压力和聚合时间没有特别限制。通常,考虑到生产性和加工能力,可以从以下范围进行最佳设定。即,聚合温度可选自通常-20℃至290℃、优选0℃至250℃的范围内;共聚合压力可选自0.1mpa至300mpa、优选0.3mpa至250mpa的范围;和聚合时间可选自0.1分钟至10小时、优选0.5分钟至7小时、更优选1分钟至6小时的范围。
在本发明中,聚合通常在惰性气体气氛中进行。例如,可使用氮气气氛、氩气气氛或二氧化碳气氛,优选使用氮气气氛。允许混入少量氧气或空气。
向聚合反应器中供给催化剂和单体也没有特别限制,可以根据各自目的采用各种供给方法。例如,在间歇聚合的情况下,可以采用这样的技术:预先将预定量的单体供给到聚合反应器中,然后供给催化剂。在这种情况下,可以将额外的单体或额外的催化剂供给到聚合反应器。在连续聚合的情况下,可以采用这样的技术:将预定量的单体和催化剂连续或间歇地供给到聚合反应器中,以连续地进行聚合反应。
关于共聚物组成的控制,通常可以使用这样的方法:将多种单体供给到反应器中,并改变供给单体的比例。此外,提供了通过利用取决于催化剂结构的差异的单体竞聚率的差异来控制共聚组成的方法,以及通过利用单体竞聚率的聚合温度依赖性来控制共聚组成的方法。
对于控制聚合物的分子量,可使用迄今已知的方法。即,提供了通过控制聚合温度来控制分子量的方法,通过控制单体浓度来控制分子量的方法,通过使用链转移剂控制分子量的方法,通过控制过渡金属配合物中的配体结构来控制分子量的方法等。当使用链转移剂时,可使用迄今已知的链转移剂。例如,可使用氢气、烷基金属等。
此外,当组分(b)本身作为一种链转移剂起作用时,通过控制组分(b)与组分(a)的比例或控制组分(b)的浓度,可以进行分子量调节。当通过控制过渡金属配合物中的配体结构进行分子量调节时,可以利用这样的趋势:通常,通过控制上述r2和r3中含杂原子的基团的类型、数量和构型,通过在金属m周围设置体积大的取代基,或通过将杂原子引入上述r6中来提高分子量。优选设置给电子基团如芳基和含杂原子的取代基,以使得给电子基团可与金属m相互作用。通过使用分子模型或分子轨道计算测量给电子基团与金属m之间的距离,通常可以判断这种给电子基团是否可以与金属m相互作用。
特别是,通过基于共聚物的极性基团的作用,由本发明得到的共聚物表现出优异的涂漆特性、印刷性、抗静电性能、无机填料分散性、对其它树脂的粘合性、与其它树脂的相容性等。利用这些性能,本发明的共聚物可用于各种应用。例如,所述共聚物可用于膜、片材、粘合性树脂、粘结剂、相容剂、蜡等。
3.第三实施方式
在本发明的第三实施方式中,提供可通过将由通式[i]或[ii]表示的化合物与含有属于元素周期表中第9、10或11族的过渡金属如镍、钯、钴、铜或铑的过渡金属化合物接触得到的反应产物,即由通式[iii]表示的金属配合物(以下可称为金属配合物[iii]);和在作为催化剂组分的所述金属配合物存在下制备(a)α-烯烃的聚合物或共聚物的方法,以及在作为催化剂组分的所述金属配合物存在下制备(a)α-烯烃和(b)(甲基)丙烯酸酯单体、乙烯基单体或烯丙基单体的共聚物的方法。
在本发明中,"聚合"是一种单体的均聚和多种单体的共聚合的统称,并且这两种情况简单地描述为"聚合",特别是当两种情况都不需要区分时。此外,在本发明中,"(甲基)丙烯酸酯"包括丙烯酸酯和甲基丙烯酸酯。
3-1.金属配合物
本发明的第三实施方式的金属配合物是可通过使下述通式[i]或[ii]表示的化合物与含有属于元素周期表中第9、10或11族的过渡金属的过渡金属化合物接触得到的:
在本发明中,"接触"表示由通式[i]和[ii]表示的化合物(以下,它们可统称为磷苯酚盐化合物)和过渡金属化合物彼此非常接近的存在,以使得通式[i]或[ii]中的e1可与所述过渡金属形成配位键,和/或通式中的x1可与所述过渡金属形成单键。此外,使磷苯酚盐化合物与过渡金属化合物接触表示将这些化合物混合以使得这些化合物彼此非常接近地存在并且可以形成所述两种键中的至少一种。
混合磷苯酚盐化合物和过渡金属化合物的条件没有特别限制。这些化合物可以直接混合或使用溶剂进行混合。特别是从实现均匀混合的观点,优选使用溶剂。
在如此得到的金属配合物中,所述磷苯酚盐化合物变成配体。因此,所述磷苯酚盐化合物与过渡金属化合物之间的反应通常是配体交换反应。当如此得到的金属配合物在热力学上比过渡金属化合物更稳定时,通过在室温(15℃至30℃)下混合磷苯酚盐化合物和过渡金属化合物来进行配体交换反应。另一方面,当如此得到的金属配合物在热力学上不如过渡金属化合物稳定时,优选适当地加热所述混合物以致配体交换反应充分地进行。
据估计,可通过使由通式[i]或[ii]表示的化合物与含有属于元素周期表中第9、10或11族的过渡金属的过渡金属化合物接触得到的金属配合物具有由下述通式[iii]表示的结构。
然而,当所述磷苯酚盐化合物与含有属于元素周期表中第9、10或11族的过渡金属的过渡金属化合物接触时,存在会生成具有不同于由通式[iii]表示的结构的结构的金属配合物的可能性,这是因为由通式[i]或[ii]表示的化合物是二齿配体。例如,可能是下述情况:其中仅通式[i]或[ii]中的x1与过渡金属形式键,或其中仅该式中的e1可与过渡金属形成键。由通式[iii]表示的金属配合物是所述磷苯酚盐化合物与过渡金属化合物的1:1反应产物。取决于过渡金属的类型,可能有其中得到具有不同组成比例的反应产物的情形。例如,可能有其中磷苯酚盐化合物的一个或多个分子与一个过渡金属形成配合物的情形,或可能有其中磷苯酚盐化合物的一个分子与两个或多个过渡金属反应以合成多核配合物的情形。
在本发明中,没有否认具有不同于由通式[iii]表示的结构的结构的金属配合物可用于与由通式[iii]表示的金属配合物一样制备α-烯烃(共)聚合物。
以下,将描述通式[i]和[ii]中的r1至r6、e1和x1以及通式[i]中的z和m。
r1表示具有1至30个碳原子的直链状烷基、具有3至30个碳原子的支链非环状烷基、具有2至30个碳原子的烯基、具有3至30个碳原子且任选具有侧链的环烷基、具有6至30个碳原子的芳基、具有7至30个碳原子的芳烷基、或具有7至30个碳原子的烷芳基。它们之中,优选的是直链状烷基、支链非环状烷基、任选具有侧链的环烷基、芳基和芳烷基。
对于所述直链状烷基、支链非环状烷基、烯基、任选具有侧链的环烷基、芳基、芳烷基和烷芳基中每一个,碳原子数的上限优选是25,更优选20,仍更优选15。
r1的实例之中,作为具有1至30个碳原子的直链状烷基,更优选具有1至10个碳原子的直链状烷基,如甲基、乙基、正丙基、正丁基、正戊基、正己基、正庚基、正辛基、正壬基、正癸基等,仍更优选具有1至4个碳原子的直链状烷基。
r1的实例之中,作为具有3至30个碳原子的支链非环状烷基,更优选的具有3至10个碳原子的支链非环状烷基,如异丙基、异丁基、叔丁基(叔丁基)、仲丁基、异戊基(3-甲基丁基)、叔戊基(1,1-二甲基丙基)、仲戊基(1-甲基丁基)、2-甲基丁基、新戊基(2,2-二甲基丙基)、1,2-二甲基丙基、异己基(4-甲基戊基)等,仍更优选的具有3至8个碳原子的支链非环状烷基。
r1的实例之中,作为具有2至30个碳原子的烯基,提供乙烯基、烯丙基、丁烯基、戊烯基、己烯基、苯乙烯基和肉桂基。优选具有3至8个碳原子的烯基,如烯丙基、丁烯基、戊烯基、己烯基、苯乙烯基等。更优选具有4至8个碳原子的烯基,如丁烯基、戊烯基、己烯基、苯乙烯基等。
r1的实例之中,作为具有3至30个碳原子且任选具有侧链的环烷基,更优选具有3至10个碳原子且任选具有侧链的环烷基,如环丙基、环丁基、环戊基、2-甲基环戊基、3-甲基环戊基、环己基、4-甲基环己基、4-乙基环己基、环辛基、十氢萘基(双环[4,4,0]癸基)等,和仍更优选具有3至6个碳原子且任选具有侧链的环烷基。
r1的实例之中,作为具有6至30个碳原子的芳基,更优选具有6至18个碳原子的芳基,如苯基、萘基、甘菊环基、联苯基、蒽基、三联苯基、菲基、三亚苯基、
r1的实例之中,作为具有7至30个碳原子的芳烷基,更优选具有7至15个碳原子的芳烷基,如苄基、苯乙基(2-苯基乙基)、9-芴基、萘基甲基、1-四氢萘基(tetralinyl)等,仍更优选具有7至10个碳原子的芳烷基。
r1的实例之中,作为具有7至30个碳原子的烷芳基,优选具有7至20个碳原子的烷芳基,如甲苯基、二甲苯基、乙基苯基、丙基苯基、丁基苯基、戊基苯基、己基苯基、庚基苯基、辛基苯基、壬基苯基、癸基苯基、十一烷基苯基、十二烷基苯基等,更优选具有7至15个碳原子的烷芳基,如甲苯基、二甲苯基、乙基苯基、丙基苯基、丁基苯基、戊基苯基等。
它们之中,更优选甲基、乙基、正丙基、正丁基、异丙基、异丁基、叔丁基、环己基、苯基、苄基等,r1更优选是叔丁基。
r2、r3和r4各自独立地表示(i)氢、(ii)卤素、(iii)任选具有选自由杂原子和含有杂原子的基团组成的组中的成员的特定基团,或(iv)含有杂原子的取代基。
作为(ii)卤素,实例包括氟原子、氯原子、溴原子和碘原子。其中,氟原子是优选的。
作为(iii)中使用的杂原子,实例包括氧、氮、磷、硫、硒、硅、卤素和硼。这些杂原子中,氟和氯是优选的。
作为(iii)中使用的"含有杂原子的基团",特别是,可提及与以下描述的(iv)含有杂原子的取代基类似的基团。作为"含有杂原子的基团",提供烷氧基(or9)、酯基(co2r9)等。r9如下所述。
对于(iii),对应于r2至r4的取代基的碳原子总数优选为1至30,更优选为2至25,还更优选为4至20。
按照上述,(iii)"任选具有选自由杂原子和含有杂原子的基团组成的组中的成员的特定基团"表示(iii-a)具有1至30个碳原子的直链状烷基、具有3至30个碳原子的支链非环状烷基、具有2至30个碳原子的烯基、具有3至30个碳原子且任选具有侧链的环烷基、具有6至30个碳原子的芳基、具有7至30个碳原子的芳烷基、和具有7至30个碳原子的烷芳基;(iii-b)其中一个或两个或更多杂原子通过取代与(iii-a)中的各基团结合的基团;(iii-c)其中一个或两个或更多上述"含有杂原子的基团"通过取代与(iii-a)中的各基团结合的基团;和(iii-d)其中一个或两个或更多的上述杂原子和一个或两个或更多的上述"含有杂原子的基团"通过取代与(iii-a)中的各基团结合的基团。对于(iii-c),实例包括通过取代结合了烷氧基的烷基,和通过取代结合了酯基的芳基,等等。
特别是,(iv)含有杂原子的取代基表示or9、co2r9、co2m’、c(o)n(r8)2、c(o)r9、sr9、so2r9、sor9、oso2r9、p(o)(or9)2-y(r8)y、cn、nhr9、n(r9)2、si(or8)3-x(r8)x、osi(or8)3-x(r8)x、no2、so3m’、po3m’2、p(o)(or2)2m’和含环氧基的基团。r8表示氢或具有1至20个碳原子的烃基。r9表示具有1至20个碳原子的烃基。m’表示碱金属、碱土金属、铵、季铵或鏻。此外,x表示0至3的整数,和y表示0至2的整数。
优选r2、r3和r4各自独立地表示(i)氢原子;(ii)氟原子、氯原子、溴原子;(iii)甲基、乙基、异丙基、丁基、苯基、三氟甲基、五氟苯基、萘基、蒽基;(iv)甲氧基、乙氧基、苯氧基、腈基、三甲基甲硅烷基、三乙基甲硅烷基、二甲基苯基甲硅烷基、三甲氧基甲硅烷基、三乙氧基甲硅烷基、三甲基甲硅烷基氧基、三甲氧基甲硅烷氧基、环己基氨基、磺酸钠、磺酸钾、磷酸钠、磷酸钾等。
它们之中,特别优选的是(i)氢原子;(iii)甲基、异丁基、叔丁基(叔丁基)、仲丁基、五氟苯基;和(iv)甲氧基、三甲基甲硅烷基、三甲基甲硅烷基氧基、环己基氨基等。特别是,r3优选是氢、甲基或叔丁基,和r3更优选是氢或叔丁基。
适当地选自r2、r3和r4的多个基团任选彼此结合以形成脂环、芳环或含有选自由氧、氮和硫组成的组的杂原子的杂环。在这种情况下,环成员的数量为5至8,和所述环任选在其上具有取代基。
r2中含有的多个基团可以彼此结合以形成在r2上的环。即使r3和r4中任一个含有多个基团时,这也同样适用。
r5和r6各自独立地表示具有4至6个碳原子的直链状烷基、具有4至6个碳原子的仲烷基、具有4至6个碳原子的叔烷基、或具有4至6个碳原子的烯基,每个所述基团任选具有选自由杂原子和含有杂原子的基团组成的组的成员。在本发明中,仲烷基和叔烷基均包括具有脂族环的烷基。
r5和r6位于金属m的附近,并且通过空间和/或电子相互作用影响m。为了具有这种效果,r5和r6优选具有在上述碳数范围内的支化结构。如在此使用的支化结构包括环状结构。
r5和r6的实例之中,作为具有4至6个碳原子的直链状烷基,提供正丙基、正丁基、正戊基和正己基。它们之中,具有4至5个碳原子的直链状烷基是优选的。
r5和r6的实例之中,作为具有4至6个碳原子的仲烷基,提供异丙基、异丁基、戊烷-2-基、戊烷-3-基、3-甲基-2-戊基、2-甲基-3-戊基、2-甲基环戊基、3-甲基环戊基、环己基等。它们之中,具有4至5个碳原子的仲烷基是优选的。
r5和r6的实例之中,作为具有4至6个碳原子的叔烷基,提供叔丁基(叔丁基)、叔戊基(1,1-二甲基丙基)、2-甲基-2-戊基、3-甲基-3-戊基、叔己基(1,1-二甲基丁基)、1,2-二甲基环丁基、1-甲基环戊基等。它们之中,具有4至5个碳原子的叔烷基是优选的。
r5和r6的实例之中,作为具有4至6个碳原子的烯基,提供丁烯基、戊烯基和己烯基。它们之中,具有4至5个碳原子的烯基是优选的。
它们之中,特别优选的是叔丁基(叔丁基)、叔戊基(1,1-二甲基丙基)、2-甲基-2-戊基、3-甲基-3-戊基、1-甲基环戊基等。它们之中,优选r5和r6任一个是叔丁基,更优选r5和r6均是叔丁基。
作为用作r5和r6的杂原子,实例包括氧、氮、磷、硫、硒、硅、卤素和硼。这些杂原子中,氟和氯是优选的。此外,含有这些杂原子的基团包括:包括烷氧基、芳氧基、酰基和酯基的含氧基团;包括氨基和酰胺基的含氮基团;包括硫代烷氧基和硫代芳氧基的含硫基团;包括膦基的含磷取代基;包括甲硒烷基的含硒基团;包括三烷基甲硅烷基、二烷基芳基甲硅烷基和烷基二芳基甲硅烷基的含硅基团;包括氟烷基和氟芳基的含氟基团;和包括烷基硼基和芳基硼基的含硼基团。这些含有杂原子的基团之中,烷氧基或芳氧基是最优选的。
作为上述含有杂原子的基团中含有的杂原子,能够与过渡金属配位的杂原子是优选的。含有这种能够与过渡金属配位的杂原子的含有杂原子的基团的具体实例包括下述基团。
即,可提及含氧基团,包括烷氧基如甲氧基、乙氧基、正丙氧基、异丙氧基、正丁氧基和叔丁氧基,芳氧基如苯氧基、对甲基苯氧基和对甲氧基苯氧基,酰基如乙酰基和苯甲酰基,和酯基如乙酰氧基、羧基乙基、羧基叔丁基和羧基苯基;含氮基团,包括二烷基氨基如二甲基氨基、二乙基氨基、二正丙基氨基和环己基氨基;含硫基团,包括硫代烷氧基如硫代甲氧基、硫代乙氧基、硫代正丙氧基、硫代异丙氧基、硫代正丁氧基、硫代叔丁氧基和硫代苯氧基,和硫代芳氧基如对甲基硫代苯氧基和对甲氧基硫代苯氧基;含磷取代基,包括二烷基膦基如二甲基膦基、二乙基膦基、二正丙基膦基和环己基膦基;和含硒基团,包括甲硒烷基如甲基甲硒烷基、乙基甲硒烷基、正丙基甲硒烷基、正丁基甲硒烷基、叔丁基甲硒烷基和苯基甲硒烷基。
e1表示磷、砷或锑。它们之中,e1优选是磷。
x1表示氧或硫。它们之中,x1优选是氧。
z表示氢或离去基团。z的具体实例包括氢原子、r9so2基团(其中r9如上所述)、cf3so2基团等。
此外,m表示z的化合价。
通式[ii]以阴离子形式示出。作为其抗衡阳离子,可以使用任何阳离子,只要该阳离子不抑制与本发明的过渡金属化合物的反应即可。所述抗衡阳离子的具体实例包括铵、季铵或鏻,以及元素周期表中第1至14族的金属离子。这些阳离子之中,nh4+、r94n+(其中r9如上所述,四个r9可以彼此相同或不同(以下同样适用))、r94p+、li+、na+、k+、mg2+、ca2+和al3+是优选的,r94n+、li+、na+和k+是更优选的。
下述表3-1示出本发明的通式[i]和[ii]中取代基的具体组合。z和m仅涉及通式[i]。然而,具体实例不限于下述实例。
【表3-1】
为了理解化合物的结构,示出了上表3-1中列出的化合物7的结构式和名称。由所述结构式表示的化合物将称为2-(二叔丁基膦基)-6-叔丁基苯酚。
由通式[i]和[ii]表示的化合物可以通过已知的合成法来合成。
由下述通式[iii]表示的本发明的金属配合物包括在由通式[i]或[ii]表示的化合物与含有属于元素周期表中第9、10或11族的过渡金属的过渡金属化合物的反应产物中。然而,如上所述,通过所述制备方法得到的金属配合物的结构不限于由通式[iii]表示的结构。
在通式[iii]中,r1至r6、e1和x1如上所述。如上所述,就含有苯环和这些取代基(r1至r6、e1和x1)的主骨架而言,反应产物中的金属配合物的配合结构与由通式[iii]表示的金属配合物的配合结构之间存在相似性。
以下,将描述通式[iii]中的m、r7和l1。
在本发明中,m为属于元素周期表中第9、10或11族的过渡金属。m优选是第10族中的镍、钯和铂,第9族中的钴和铑,和第11族中的铜,更优选第10族中的镍、钯和铂,最优选第10族中的镍或钯。
m的化合价优选是二价。m的化合价是指有机金属化学中使用的形式氧化数。即,当包括某些元素的键中的电子对分配给具有更大电负性的元素时,化合价是指残留在所述元素原子上的电荷数。例如,在本发明的通式[iii]中,当e1是磷,x1是氧,m是镍,r7是苯基,l1是吡啶以及镍与磷、氧、苯基的碳和吡啶的氮形成键时,镍的形式氧化数即镍的化合价变成二价。理由如下:根据上述定义,在这些键中,电子对分配给具有比镍更大的电负性的磷、氧、碳和氮,磷的电荷变成0,氧的电荷变成-1,苯基的电荷变成-1,和吡啶的电荷变成0,所述配合物整体上是电中性的;因此,残留在镍上的电荷变成+2。
作为二价过渡金属,例如,镍(ii)、钯(ii)、铂(ii)和钴(ii)是优选的。作为除二价过渡金属以外的过渡金属,铜(i)或铑(iii)也是优选的。
在本发明中,r7表示氢原子或具有1至20个碳原子且任选具有选自由杂原子和含有杂原子的基团组成的组的成员的烃基。本发明中的聚合或共聚合被认为是通过将本发明的组分(a)或组分(b)插入到m和r7的键中来引发。因此,当r7的碳原子数过大时,倾向于抑制该引发反应。为此,不包括取代基中含有的碳原子的r7的碳原子数优选是1至16,更优选1至10。
r7的具体实例包括氢化物基团、甲基、乙基、正丙基、异丙基、正丁基、异丁基、正己基、正辛基、正癸基、正十二烷基、环戊基、环己基、苄基、苯基、对甲基苯基、三甲基甲硅烷基、三乙基甲硅烷基、三苯基甲硅烷基等。
在本发明中,l1表示配位至m的配体。本发明中的配体l1是具有1至20个碳原子且具有作为能够形成配位键的原子的氧、氮或硫的烃化合物。此外,作为l1,可使用具有能够与过渡金属形成配位键的碳碳不饱和键(任选含有杂原子)的烃化合物。l1的碳原子数优选是1至16,更优选1至10。此外,作为与通式[iii]中的m形成配位键的l1,没有电荷的化合物是优选的。
在本发明中,优选作为l1的是环状不饱和烃、膦、吡啶、哌啶、烷基醚、芳基醚、烷基芳基醚、环状醚、烷基腈衍生物、芳基腈衍生物、醇、酰胺、脂族酯、芳族酯、胺等。更优选作为l1的是环状烯烃、膦、吡啶、环状醚、脂族酯、芳族酯等。特别优选作为l1的是三烷基膦、吡啶、卢剔啶(二甲基吡啶)、皮考啉(甲基吡啶)和r9co2r8(r8和r9的定义如上所述)。
r7和l1可以彼此结合形成环。这种实例是环辛-1-烯基,该基团也是本发明中优选的实施方式。
下表3-2示出本发明的通式[iii]中的取代基的具体组合。然而,具体实例不限于下述实例。
【表3-2】
为了理解金属配合物的结构,示出了上表3-2中列出的配合物7a的结构式和名称。由所述结构式表示的化合物将称为(2-(二叔丁基膦基)-6-叔丁基苯基苯酚盐)((1,4,5-η)-4-环辛烯-1-基)镍(ii)。
此外,举例说明表3-2中列出的化合物的中心金属m从镍变成钯的化合物。
对于本发明中使用的过渡金属化合物,使用能够与由通式[i]或[ii]表示的化合物反应形成具有聚合能力的配合物的那些。它们有时称为前驱体。
例如,作为含有镍的过渡金属化合物,可使用双(1,5-环辛二烯)镍(0),由通式ni(ch2cr13ch2)2表示的配合物[其中r13表示氢原子、卤素原子、具有1至30个碳原子且任选含有杂原子的烃基、or8、co2r8、co2m’、c(o)n(r9)2、c(o)r8、sr8、so2r8、sor8、oso2r8、p(o)(or8)2-y(r9)y、cn、nhr8、n(r8)2、si(or9)3-x(r9)x、osi(or9)3-x(r9)x、no2、so3m’、po3m’2、p(o)(or8)2m’或含环氧基的基团(其中r8表示具有1至20个碳原子的烃基;r9表示氢原子或具有1至20个碳原子的烃基;m’表示碱金属、碱土金属、铵、季铵或鏻;x表示0至3的整数;和y表示0至2的整数)],双(环戊二烯基)镍(ii),由通式ni(ch2sir133)2l12表示的配合物(其中r13和l1如上所述),由通式nir132l12表示的配合物(其中r13和l1如上所述)等。
此外,作为含有属于第9、10或11族的过渡金属的过渡金属化合物,可使用通式mr13pl1q(其中m表示第9、10或11族的过渡金属;r13和l1如上所述;p和q各自是满足m的化合价的0或更大的整数)。
这些过渡金属化合物之中,优选使用的是双(1,5-环辛二烯)镍(0)、niphcl(pet3)2、niphcl(pph3)2、niphcl(tmeda)(以下tmeda表示四甲基乙二胺)、niarbr(tmeda)(其中ar为4-氟苯基)、由通式ni(ch2cr13ch2)2表示的配合物(其中r13如上所述)、由通式ni(ch2sir133)2l12表示的配合物(其中r13和l1如上所述)、由通式nir132l12表示的配合物(其中r13和l1如上所述)、pd(dba)2、pd2(dba)3、pd3(dba)4(其中dba表示二苄叉基丙酮)、pd(ococh3)2和(1,5-环辛二烯)pd(甲基)(氯化物)。
特别优选的是双(1,5-环辛二烯)镍(0)、niphcl(pet3)2、niphcl(pph3)2、niphcl(tmeda)、niarbr(tmeda)(其中ar为4-氟苯基)、ni(ch2chch2)2、ni(ch2cmech2)2、ni(ch2sime3)2(py)2(以下,py表示吡啶)、ni(ch2sime3)2(lut)2(以下,lut表示2,6-卢剔啶))、niph2(py)2、niph2(lut)2、pd(dba)2、pd2(dba)3、pd3(dba)4(其中dba表示二苄叉基丙酮))、pd(ococh3)2、和(1,5-环辛二烯)pd(甲基)(氯化物)。
本发明的反应产物可以通过将由通式[i]或[ii]表示的上述化合物与上述过渡金属化合物[iv]例如以[i]+[ii]:[iv]=[1:99]至[99:1]的摩尔比在有机溶剂如甲苯或苯中,在0℃至100℃下,在减压至增压下接触1至86400秒来获得。当双(1,5-环辛二烯)镍(0)(ni(cod)2)在甲苯或苯中的溶液用作所述过渡金属化合物时,可以通过溶液从黄色至例如红色的变色来确认形成反应产物。
在本反应之后,构成过渡金属化合物但不是所述化合物的过渡金属的组分被通式[i]的除z以外的部分或由通式[ii]表示的化合物取代,从而形成由本发明的通式[iii]表示的金属配合物。该取代反应优选定量进行;然而,在有些情况下,其可以进行不完全。在反应完成之后,除由通式[iii]表示的配合物之外,还存在衍生自通式[i]和[ii]以及所述过渡金属化合物的其他组分。当进行本发明的聚合反应或共聚合反应时,可以除去或保留这些其他组分。通常,优选除去这些其他组分,因为可以获得更高的活性。
当进行反应时,关于本发明的l1可以一起存在。当镍或钯用作关于本发明的m时,形成的由通式[iii]表示的配合物的稳定性有时通过在体系中共存具有路易斯碱性质的l1而得到改善。在这种情况下,l1的共存是优选的,只要l1不抑制本发明的聚合反应或共聚合反应。
在本发明中,所述反应可以预先在不同于用于α-烯烃的聚合或α-烯烃与(甲基)丙烯酸酯的共聚合的反应器的容器中进行,然后如此得到的由通式[iii]表示的配合物可用于α-烯烃的聚合或α-烯烃与(甲基)丙烯酸酯的共聚合,或所述反应可以在这些单体存在下进行。此外,所述反应可以在用于α-烯烃的聚合或α-烯烃与(甲基)丙烯酸酯的共聚合的反应器中进行。在这种情况下,这些单体可以存在或不存在。作为由通式[i]和[ii]表示的每种组分,可以使用单一组分,或者可以组合使用多种组分。特别是,为了拓宽分子量分布或共聚单体含量分布,这种多种组分的组合使用是有用的。
3-2.金属配合物的制备方法
在本发明的第三实施方式的制备方法中,如上所述,由通式[iii]表示的金属配合物可以通过使由通式[i]或[ii]表示的化合物与含有属于元素周期表中第9、10或11族的过渡金属的过渡金属化合物接触来制备。
3-3.用于烯烃聚合的催化剂组分
根据本发明的第三实施方式的用于烯烃聚合的催化剂组分包含上述金属配合物或可通过上述制备方法得到的金属配合物。
在本发明的第三实施方式中,由通式[iii]表示的金属配合物可用作用于聚合或共聚合的催化剂组分。如以上所述,由通式[iii]表示的金属配合物可以通过使通式[i]或[ii]与所述过渡金属配合物组分反应来形成。当由通式[iii]表示的金属配合物用作催化剂组分时,可以使用分离的金属配合物,或者可以使用负载在载体上的金属配合物。这种负载可以在用于α-烯烃的聚合或α-烯烃与(甲基)丙烯酸酯的共聚合的反应器中,在这些单体存在或不存在下进行,或者可以在不同于所述反应器的容器中进行。
作为可使用的载体,可使用任何载体,只要所述载体不损害本发明的范围即可。通常,可适当地使用无机氧化物和聚合物载体。特别是,可提及sio2、al2o3、mgo、zro2、tio2、b2o3、cao、zno、bao、tho2等,或它们的混合物。此外,可使用混合氧化物如sio2-al2o3、sio2-v2o5、sio2-tio2、sio2-mgo和sio2-cr2o3,并且可使用无机硅酸盐、聚乙烯载体、聚丙烯载体、聚苯乙烯载体、聚丙烯酸载体、聚甲基丙烯酸载体、聚丙烯酸酯载体、聚酯载体、聚酰胺载体、聚酰亚胺载体等。对于这些载体,粒径、粒径分布、孔容积、比表面积等没有特别限制,可使用任何载体。
作为无机硅酸盐,可使用粘土、粘土矿物、沸石、硅藻土等。对于这些物质,可以使用合成材料,或可以使用天然存在的矿物。粘土和粘土矿物的具体实例包括水铝英石类如水铝英石;高岭土类如地开石、珍珠陶土、高岭土和钙长石;埃洛石类如变埃洛石和埃洛石;蛇纹石类如纤蛇纹石、利蛇纹石和叶蛇纹石;蒙脱石类如蒙脱土、锌蒙脱石、贝得石、绿脱石、皂石和锂蒙脱石;蛭石矿物如蛭石;云母矿物如伊利石、绢云母和海绿石;绿坡缕石;海泡石;坡缕石;膨润土;木节土;gaerome粘土;硅铁石;叶蜡石;和绿泥石类。这些物质可形成混合层。人造化合物包括合成云母、合成锂蒙脱石、合成皂石和合成带云母。这些具体实例之中,优选的是高岭土类如地开石、珍珠陶土、高岭土和钙长石;埃洛石类如变埃洛石和埃洛石;蛇纹石类如纤蛇纹石、利蛇纹石和叶蛇纹石;蒙脱石类如蒙脱土、zaukonite、贝得石、绿脱石、皂石和锂蒙脱石;蛭石矿物如蛭石;云母矿物如伊利石、绢云母和海绿石;合成云母;合成锂蒙脱石;合成皂石;和合成带云母。特别优选的是蒙脱石类如蒙脱土、zaukonite、贝得石、绿脱石、皂石和锂蒙脱石;蛭石矿物如蛭石;合成云母;合成锂蒙脱石;合成皂石;和合成带云母。
这些载体可以原样使用,或者可以用盐酸、硝酸、硫酸等进行酸处理,和/或使用licl、nacl、kcl、cacl2、mgcl2、li2so4、mgso4、znso4、ti(so4)2、zr(so4)2、al2(so4)3等进行盐处理。所述处理可以通过将相应的酸和碱混合以在反应体系中形成盐来进行。此外,可以进行如粉碎和造粒等形状控制或干燥处理。
3-4.用于烯烃聚合的催化剂
根据本发明的第三实施方式的用于烯烃聚合的催化剂包含下述组分(a)和(b),和根据需要的下述组分(c):
组分(a):上述金属配合物或可通过上述制备方法得到的金属配合物
组分(b):可与组分(a)反应形成离子对的化合物,或离子交换性层状硅酸盐
组分(c):有机铝化合物。
所述组分(a)是上述金属配合物或可通过上述制备方法得到的金属配合物。可单独使用一种金属配合物,或可组合使用两种或多种金属配合物。
所述组分(b)的实例是有机铝氧化合物。所述有机铝氧化合物在分子中具有al-o-al键,和所述键的数量在通常1至100的范围内,优选1至50。这种有机铝氧化合物通常是可通过使有机铝化合物与水反应得到的产物。
有机铝与水的反应通常在惰性烃类(溶剂)中进行。作为惰性烃类,可使用脂族烃、脂环族烃和芳族烃如戊烷、己烷、庚烷、环己烷、甲基环己烷、苯、甲苯和二甲苯。优选使用脂族烃或芳族烃。
作为用于制备所述有机铝氧化合物的有机铝化合物,可使用由下述通式表示的化合物。优选使用三烷基铝。
(rx)tal(x3)(3-t)
(其中rx表示烃基如各自具有1至18个碳原子、优选1至12个碳原子的烷基、烯基、芳基和芳烷基;x3表示氢原子或卤素原子;和t表示1≤t≤3的整数。)所述三烷基铝中的烷基可以是甲基、乙基、丙基、异丙基、丁基、异丁基、戊基、己基、辛基、癸基、十二烷基等中任何烷基。优选的是甲基和异丁基,特别优选的是甲基。可混合和使用两种或多种所述有机铝化合物。
水与有机铝化合物的反应比例(水/al的摩尔比)优选是0.25/1至1.2/1,特别优选0.5/1至1/1。反应温度通常在-70℃至100℃的范围内,优选-20℃至20℃。通常在5分钟至24小时、优选10分钟至5小时的范围内选择反应时间。作为反应所需的水,不仅可以使用简单的水,而且可以使用硫酸铜水合物、硫酸铝水合物等中含有的水合水,以及可以在反应体系中产生水的组分。
上述有机铝氧化合物之中,可通过烷基铝与水反应得到的有机铝氧化合物通常称为铝氧烷。甲基铝氧烷(包括基本上由甲基铝氧烷(mao)组成的那些)特别优选作为所述有机铝氧化合物。此外,固体形式的干燥甲基铝氧烷(dmao),其通过将溶剂从mao溶液中去除而得到,是优选的。
作为所述有机铝氧化合物,可以组合使用两种或多种上述有机铝氧化合物,或者可以使用溶解或分散在上述惰性烃溶剂中的有机铝氧化合物的溶液。
所述组分(b)的具体实例是离子交换性层状硅酸盐。离子交换性层状硅酸盐(以下可简称为"硅酸盐")是具有其中由离子键合等形成的平面彼此平行定位并由结合力堆叠的晶体结构且其中所含有的离子可交换的硅酸盐化合物。作为所述硅酸盐,各种硅酸盐是已知的,所述硅酸盐详细描述在"nendokobutsugaku",haruoshirozu,asakurapublishingco.,ltd.(1995)中。
在本发明中,作为组分(b),优选使用属于蒙脱石类的那些。其具体实例包括蒙脱土、锌蒙脱石、贝得石、绿脱石、皂石、锂蒙脱石、镁皂石等。它们之中,从增大共聚物部分的聚合活性和分子量的观点,优选蒙脱土。
大多数硅酸盐主要作为天然粘土矿物的主要成分生产。因此,经常含有除所述离子交换性层状硅酸盐以外的夹杂物(如石英和方英石)。用于本发明的蒙脱石类的硅酸盐可以含有夹杂物。
所述硅酸盐可以进行酸处理和/或盐处理。所述处理可以通过将相应的酸和碱混合以在反应体系中形成盐来进行。
作为组分(b),可以使用上述有机铝氧化合物和离子交换性层状硅酸盐的混合物。此外,作为所述有机铝氧化合物和离子交换性层状硅酸盐,可以使用一种所述化合物和硅酸盐,或两种或多种所述化合物和硅酸盐。
用作组分(c)的有机铝化合物的实例由下述通式表示:
al(rp)ax(3-a)
其中rp表示具有1至20个碳原子的烃基;x表示氢、卤素、烷氧基或甲硅烷氧基;和a为大于0且等于或小于3的数。
由所述通式表示的有机铝化合物的具体实例包括三烷基铝如三甲基铝、三乙基铝、三丙基铝、三异丁基铝等,和含有卤素或烷氧基的烷基铝如二乙基铝一氯化物、二乙基铝单甲醚等。
它们之中,三异丁基铝是优选的。此外,可以组合使用两种或多种上述有机铝化合物。此外,上述铝化合物可以用醇、苯酚等改性来使用。作为改性剂,例举甲醇、乙醇、1-丙醇、异丙醇、丁醇、苯酚、2,6-二甲基苯酚、2,6-二叔丁基苯酚等。优选的具体实例是2,6-二甲基苯酚和2,6-二叔丁基苯酚。
在根据本发明的第三实施方式的用于烯烃聚合的催化剂的制备方法中,所述组分(a)、组分(b)和根据需要的组分(c)的接触方法没有特别限制。例如,可提供下述方法。
方法(i):组分(a)和组分(b)彼此接触,然后添加组分(c)。
方法(ii):组分(a)和组分(c)彼此接触,然后添加组分(b)。
方法(iii):组分(b)和组分(c)彼此接触,然后添加组分(a)。
方法(iv):组分(a)、(b)和(c)彼此同时接触。
此外,每种组分可以通过将其与不同种类的组分混合而作为混合物使用,或者可以以不同的顺序单独接触。所述接触不仅可以在催化剂制备时进行,也可以在使用烯烃进行预聚合时或烯烃聚合时进行。
另外,可以将一种组分分开并与每种组分接触,例如,以使组分(b)和组分(c)彼此接触,然后添加组分(a)和组分(c)的混合物的方式。
所述组分(a)、(b)和(c)的接触优选在惰性气体气氛如氮气等和在惰性烃溶剂如戊烷、己烷、庚烷、甲苯、二甲苯等中进行。所述接触可以在-20℃至溶剂的沸点之间的温度下进行,特别优选在室温至溶剂的沸点之间的温度下进行。
3-5.α-烯烃聚合物的制备方法
本发明的第三实施方式的α-烯烃聚合物的制备方法的实施方式是(a)α-烯烃在所述用于聚合的催化剂存在下聚合或共聚合。
本发明中的组分(a)是由通式ch2=chr10表示的α-烯烃。r10是氢原子或具有1至20个碳原子的烃基,其可具有支链、环和/或不饱和键。当r10的碳原子数大于20时,倾向于较少显示聚合活性。为此,它们之中,r10是氢原子或具有1至10个碳原子的烃基的α-烯烃优选作为组分(a)。
更优选作为组分(a)的那些包括乙烯、丙烯、1-丁烯、1-戊烯、1-己烯、1-辛烯、1-癸烯、3-甲基-1-丁烯、4-甲基-1-戊烯、乙烯基环己烯和苯乙烯。作为组分(a),可以使用单一组分,或者可以组合使用多种组分。
在本发明的α-烯烃聚合物的制备方法和α-烯烃共聚物的制备方法中,(a)α-烯烃特别优选是丙烯。
本发明的α-烯烃聚合物的制备方法的另一实施方式是(a)α-烯烃和(b)(甲基)丙烯酸酯单体、乙烯基单体或烯丙基单体在上述用于聚合的催化剂存在下共聚合。
本发明中的(甲基)丙烯酸酯单体由通式ch2=c(r11)co2(r12)表示。r11是氢原子或具有1至10个碳原子的烃基,其可具有支链、环和/或不饱和键。r12是具有1至30个碳原子的烃基,其可具有支链、环和/或不饱和键。此外,r12可在其中任何位置含有杂原子。
当r11的碳原子数是11以上时,倾向于较少显示聚合活性。因此,r11是氢原子或具有1至10个碳原子的烃基,优选的(甲基)丙烯酸酯包括其中r11是氢原子或具有1至5个碳原子的烃基的(甲基)丙烯酸酯。更优选的(甲基)丙烯酸酯单体包括r11是甲基的甲基丙烯酸酯或r11是氢原子的丙烯酸酯。类似地,当r12的碳原子数大于30时,倾向于较少显示聚合活性。因此,r12的碳原子数是1至30,优选是1至12,更优选1至8。
此外,作为r12中任选含有的杂原子,提供氧、硫、硒、磷、氮、硅、氟、硼等。这些杂原子之中,氧、硅和氟是优选的,并且氧是更优选的。另外,不含杂原子的r12也是优选的。
还更优选的(甲基)丙烯酸酯单体包括(甲基)丙烯酸甲酯、(甲基)丙烯酸乙酯、(甲基)丙烯酸正丙酯、(甲基)丙烯酸异丙酯、(甲基)丙烯酸正丁酯、(甲基)丙烯酸异丁酯、(甲基)丙烯酸叔丁酯、(甲基)丙烯酸戊酯、(甲基)丙烯酸己酯、(甲基)丙烯酸环己酯、(甲基)丙烯酸辛酯、(甲基)丙烯酸2-乙基己酯、(甲基)丙烯酸壬酯、(甲基)丙烯酸癸酯、(甲基)丙烯酸十二烷基酯、(甲基)丙烯酸苯酯、(甲基)丙烯酸甲苯酰酯、(甲基)丙烯酸苄基酯、(甲基)丙烯酸羟乙酯、(甲基)丙烯酸二甲基氨基乙酯、(甲基)丙烯酸二乙基氨基乙酯、(甲基)丙烯酸-2-氨基乙酯、(甲基)丙烯酸2-甲氧基乙酯、(甲基)丙烯酸-3-甲氧基丙酯、(甲基)丙烯酸缩水甘油基酯、(甲基)丙烯酸环氧乙烷酯、(甲基)丙烯酸三氟甲基酯、(甲基)丙烯酸2-三氟甲基乙基酯、(甲基)丙烯酸全氟乙基酯、(甲基)丙烯酰胺、(甲基)丙烯酰基二甲基酰胺、(甲基)丙烯酸2-羟基丁酯、(甲基)丙烯酸4-羟基丁酯等。(甲基)丙烯酸酯可以单独使用,或多种(甲基)丙烯酸酯可以组合使用。
本发明中的乙烯基单体是含有极性基团的乙烯基单体,如含卤素、含氮、含氧和含硫的乙烯基单体。特别是,其是含有卤素、羟基、氨基、硝基、羧基、醛基、酯基、环氧基、腈基等的乙烯基单体。其具体实例包括5-己烯-1-醇、2-甲基-3-丁烯-1-醇、10-十一碳烯酸乙酯、10-十一碳烯-1-醇、12-十三碳烯-2-醇、10-十一烷酸、甲基-9-癸烯酸酯、叔丁基-10-十一碳烯酸酯、1,1-二甲基-2-丙烯-1-醇、9-癸烯-1-醇、3-丁烯酸、3-丁烯-1-醇、n-(3-丁烯-1-基)邻苯二甲酰亚胺、5-己烯酸、5-己烯酸甲酯、5-己烯-2-酮、丙烯腈、甲基丙烯腈、醋酸乙烯酯等它们之中,3-丁烯-1-醇、10-十一碳烯酸乙酯和10-十一碳烯-1-醇是特别优选的。
作为本发明中的烯丙基单体,实例包括具有3个碳原子的烯丙基单体(丙烯基单体)和作为具有4个或更多碳原子的含烯丙基单体的烯丙基系单体。所述烯丙基单体是含有极性基团的烯丙基单体,如含卤素、含氮、含氧和含硫的烯丙基单体。特别是,其是含有卤素、羟基、氨基、硝基、羧基、醛基、酯基、环氧基、腈基等的乙烯基单体。其优选的具体实例包括乙酸烯丙酯、烯丙醇、烯丙胺、n-烯丙基苯胺、n-叔丁氧基羰基-n-烯丙胺、n-苄氧基羰基-n-烯丙胺、n-烯丙基-n-苄胺、烯丙基氯、烯丙基溴、烯丙基醚、二烯丙基醚等。它们之中,乙酸烯丙酯和烯丙醇是更优选的,乙酸烯丙酯、烯丙基醚和二烯丙基醚是再更优选的。
本发明中的聚合反应是在存在或不存在液体下进行的,所述液体可以是:烃溶剂如丙烷、正丁烷、异丁烷、正己烷、正庚烷、甲苯、二甲苯、环己烷和甲基环己烷;或液化的α-烯烃;或极性溶剂如二乙基醚、乙二醇二甲醚、四氢呋喃、二氧杂环己烷、醋酸乙酯、苯甲酸甲酯、丙酮、甲基乙基酮、甲酰胺、乙腈、甲醇、异丙醇和乙二醇。此外,在此描述的液体化合物的混合物可用作溶剂。此外,离子液体也可以用作溶剂。更优选上述烃溶剂和离子液体以获得更高的聚合活性和高分子量。
在本发明中,所述聚合反应可在存在或不存在已知添加剂下进行。作为添加剂,抑制自由基聚合的聚合抑制剂和具有稳定制备的共聚物的作用的添加剂是优选的。优选的添加剂的实例包括醌衍生物、受阻酚衍生物等。具体地,可使用氢醌单甲醚、2,6-二叔丁基-4-甲基苯酚(bht)、三甲基铝和bht的反应产物、钛(iv)醇盐和bht的反应产物等。此外,所述聚合可以通过使用这种填料作为添加剂在无机和/或有机填料存在下进行。此外,涉及本发明的l1或离子液体可以用作添加剂。
本发明中优选的添加剂包括路易斯碱。通过选择适合的路易斯碱,可以改善活性、分子量和丙烯酸酯的共聚合反应性。相对于聚合体系中存在的催化剂组分中的过渡金属m,路易斯碱的量为0.0001至1000当量、优选0.1至100当量、更优选0.3至30当量。将路易斯碱添加至聚合体系的方法没有特别限制,可使用任何技术。例如,路易斯碱可以通过与本发明的催化剂组分混合来添加,或可以通过与单体混合来添加,或可以独立于催化剂组分和单体添加到聚合体系中。此外,可以组合使用多种路易斯碱。此外,可以使用与本发明相关的l1相同的路易斯碱,或者可以使用不同的路易斯碱。
路易斯碱包括芳族胺、脂族胺、烷基醚、芳基醚、烷基芳基醚、环状醚、烷基腈、芳基腈、醇、酰胺、脂族酯、芳族酯、磷酸酯、亚磷酸酯、噻吩、噻蒽、噻唑、噁唑、吗啉、环状不饱和烃等。它们之中,优选的路易斯碱是芳族胺、脂族胺、环状醚、脂族酯和芳族酯,特别优选的路易斯碱是吡啶衍生物、嘧啶衍生物、哌啶衍生物、咪唑衍生物、苯胺衍生物、哌啶衍生物、三嗪衍生物、吡咯衍生物和呋喃衍生物。
具体的路易斯碱化合物包括吡啶、五氟吡啶、2,6-卢剔啶、2,4-卢剔啶、3,5-卢剔啶、嘧啶、n,n-二甲基氨基吡啶、n-甲基咪唑、2,2'-联吡啶、苯胺、哌啶、1,3,5-三嗪、2,4,6-三(三氟甲基)-1,3,5-三嗪、2,4,6-三(2-吡啶基)-s-三嗪、喹啉、8-甲基喹啉、吩嗪、1,10-菲咯啉、n-甲基吡咯、1,8-二氮杂双环-[5.4.0]-十一碳-7-烯、1,4-二氮杂双环-[2.2.2]-辛烷、三乙胺、苄腈、皮考啉、三苯胺、n-甲基-2-吡咯烷酮、4-甲基吗啉、苯并噁唑、苯并噻唑、呋喃、2,5-二甲基呋喃、二苯并呋喃、呫吨、1,4-二氧杂环己烷、1,3,5-三氧杂环己烷、二苯并噻吩、噻蒽、三苯基鏻环戊二烯、三苯基亚磷酸酯、三苯基磷酸酯、三吡咯烷基膦、三(吡咯烷基)硼烷等。
在本发明中,聚合方式没有特别限制。优选使用其中生成的聚合物的至少一部分在介质中呈淤浆形式的淤浆聚合;其中液化单体本身用作介质的本体聚合;其中聚合在汽化单体中进行的气相聚合;或其中生成的聚合物的至少一部分溶解在高温高压下液化的单体中的高压离子聚合;等。此外,可以使用任何类型的间歇聚合、半间歇聚合和连续聚合。此外,可以进行活性聚合或与链转移一起发生的聚合。此外,链穿梭或配位链转移聚合(cctp)可以通过组合使用所谓的链转移剂(csa)来进行。
未反应的单体和介质可以通过将它们与制备的共聚物分离并回收它们来使用。在回收时,这些单体和介质可以在纯化或不纯化的情况下重复使用。为了将制备的共聚物与未反应的单体和介质分离,可以使用迄今已知的方法。例如,可以使用诸如过滤、离心、溶剂萃取或用不良溶剂再沉淀等的方法。
聚合温度、聚合压力和聚合时间没有特别限制。通常,考虑到生产性和加工能力,可以从以下范围进行最佳设定。即,聚合温度可选自通常-20℃至290℃、优选0℃至250℃的范围内;共聚合压力可选自0.1mpa至300mpa、优选0.3mpa至250mpa的范围;和聚合时间可选自0.1分钟至10小时、优选0.5分钟至7小时、更优选1分钟至6小时的范围。
在本发明中,聚合通常在惰性气体气氛中进行。例如,可使用氮气气氛、氩气气氛或二氧化碳气氛,优选使用氮气气氛。允许混入少量氧气或空气。
向聚合反应器中供给催化剂和单体也没有特别限制,可以根据各自目的采用各种供给方法。例如,在间歇聚合的情况下,可以采用这样的技术:预先将预定量的单体供给到聚合反应器中,然后供给催化剂。在这种情况下,可以将额外的单体或额外的催化剂供给到聚合反应器。在连续聚合的情况下,可以采用这样的技术:将预定量的单体和催化剂连续或间歇地供给到聚合反应器中,以连续地进行聚合反应。
关于共聚物组成的控制,通常可以使用这样的方法:将多种单体供给到反应器中,并改变供给单体的比例。此外,提供了通过利用取决于催化剂结构的差异的单体竞聚率的差异来控制共聚组成的方法,以及通过利用单体竞聚率的聚合温度依赖性来控制共聚组成的方法。
对于控制聚合物的分子量,可使用迄今已知的方法。即,提供了通过控制聚合温度来控制分子量的方法,通过控制单体浓度来控制分子量的方法,通过使用链转移剂控制分子量的方法,通过控制过渡金属配合物中的配体结构来控制分子量的方法等。当使用链转移剂时,可使用迄今已知的链转移剂。例如,可使用氢气、烷基金属等。
此外,当组分(b)本身作为一种链转移剂起作用时,通过控制组分(b)与组分(a)的比例或控制组分(b)的浓度,可以进行分子量调节。当通过控制过渡金属配合物中的配体结构进行分子量调节时,可以利用这样的趋势:通常,通过控制上述r2和r3中含杂原子的基团的类型、数量和构型,通过在金属m周围设置体积大的取代基,或通过将杂原子引入上述r6中来提高分子量。优选设置给电子基团如芳基和含杂原子的取代基,以使得给电子基团可与金属m相互作用。通过使用分子模型或分子轨道计算测量给电子基团与金属m之间的距离,通常可以判断这种给电子基团是否可以与金属m相互作用。
特别是,通过基于共聚物的极性基团的作用,本公开得到的共聚物表现出优异的涂漆特性、印刷性、抗静电性能、无机填料分散性、对其它树脂的粘合性、与其它树脂的相容性等。利用这些性能,本发明的共聚物可用于各种应用。例如,所述共聚物可用于膜、片材、粘合性树脂、粘结剂、相容剂、蜡等。
实施例
在以下实施例和比较例中详细说明本公开。然而,本公开不限于此。
在以下合成例中,除非另有说明,否则操作在纯化的氮气气氛中进行,并使用脱水和脱氧的溶剂。
<本公开的第一实施方式>
1-1.评价方法
(1)重均分子量mw、数均分子量mn和分子量分布mw/mn:通过下述gpc测量来测定。
首先,将样品(约20mg)收集在用于polymerlaboratoriesltd制造的高温gpc的预处理单元pl-sp260vs用的小瓶中,并向其中添加含有bht作为稳定剂的邻二氯苯(bht的浓度=0.5g/l),以将聚合物浓度调节至0.1质量%。通过在上述用于高温gpc的预处理单元pl-sp260vs中在135℃下加热,溶解聚合物,并用玻璃过滤器过滤以制备样品溶液。在本公开的gpc测量中,玻璃过滤器没有捕获到聚合物。接着,使用由waterscorporation制造的gpcv2000进行gpc测量,所述gpcv2000配备有作为柱的由tosohcorporation制造的tskgelgmh-ht(30cm×4个)和ri检测器。采用下述测量条件:样品溶液的注入量:约520μl;柱温:135℃;溶剂:邻二氯苯;和流量:1.0ml/min。如下进行分子量的计算。即,使用可商购获得的单分散聚苯乙烯作为标准样品,由聚苯乙烯标准样品和乙烯系聚合物的粘度公式制备保留时间对分子量的校准曲线,并基于校准曲线进行分子量的计算。作为粘度公式,使用[η]=k×mα,对于聚苯乙烯,使用k=1.38e-4,α=0.70;和对于乙烯系聚合物,使用k=4.77e-4,α=0.70。对于丙烯系聚合物,使用k=1.03e-4,α=0.78。
1-2.配体的合成
(合成例1-1):配体b-350的合成
根据下述方案合成配体b-350。
在以下提及的化学式中,-omom表示甲氧基甲氧基(-och2och3)。
(1)化合物2的合成
在氩气气氛中,在80℃下搅拌化合物1(10.0g,73.4mmol)、氯化铝(10.47g,78.6mmol)和三氯化磷(50.7g,369.2mmol,32.5ml)的混合物12小时,得到橙色悬浮液。然后,在大气压下通过蒸馏从悬浮液中除去过量的三氯化磷,并将剩下的悬浮液通过c盐过滤。将滤液倒入水(150ml)中,并用二氯甲烷(150ml×2)萃取。用无水硫酸钠干燥有机相,然后浓缩,由此得到化合物2。
(2)化合物3的合成
在-14℃下,将氢化铝(3.3g,86.9mmol)经60分钟添加到150ml的化合物2(13.0g,36.8mmol)的thf溶液中。在加热至30℃后,搅拌混合物12小时,得到灰色悬浮液。将悬浮液冷却至-14℃,用注射器以逐滴方式向其中缓慢添加hcl水溶液(1m,100ml)。在如此形成的两层中,用分液漏斗分离上层,并用醋酸乙酯(100ml)萃取。用无水硫酸钠干燥有机相,然后浓缩,由此得到化合物3。
(3)化合物5a的合成
在氩气气氛中,在30℃下,向化合物3(5.8g,19.2mmol)、化合物4(5.7g,19.2mmol)、叔丁醇钠(3.7g,38.4mmol)、双[2-(二苯基膦基)苯基]醚(dpephos,2.1g,3.84mmol)和三(二苄叉基丙酮)二钯(1.8g,1.9mmol)的混合物添加甲苯(500ml)。在110℃下搅拌反应产物12小时,得到灰色悬浮液。将反应溶液冷却至30℃,并通过c盐过滤。将滤液倒入水(150ml)中,并用醋酸乙酯(150ml×2)萃取。用无水硫酸钠干燥有机相,然后浓缩,由此得到橙色残留物。通过硅胶柱(石油醚/醋酸乙酯=0:1-50:1作为洗脱液)纯化该残留物,得到化合物5a(3.0g,5.8mmol,产率30.2%)。
(4)化合物6a的合成
在氩气气氛中,在-78℃下将正丁基锂(2.5m,2.8ml,7.0mmol)添加至20ml的化合物5a(3.0g,5.8mmol)的thf溶液中。在-78℃下搅拌反应溶液2小时,得到橙色悬浮液。在-78℃下向其中添加六氟苯(1.6g,8.7mmol,1.00ml),并在30℃下搅拌12小时。将反应溶液倒入冰冷却的饱和氯化铵中,并用醋酸乙酯(100ml×2)萃取。用无水硫酸钠干燥有机相,然后浓缩,由此得到黄色残留物。通过硅胶柱(石油醚:醋酸乙酯=1:0-30:1作为洗脱液)纯化该残留物,得到化合物6a(1.3g,2.2mmol,产率37.1%)。
(5)配体b-350的合成
在氩气气氛中,在0℃下将hcl/醋酸乙酯(4m,100ml,400.0mmol)添加至化合物6a(1.7g,2.8mmol)。在加热至30℃后,搅拌反应混合物20小时,得到白色悬浮溶液。在减压下除去挥发物,得到粗产物。向其中添加二氯甲烷(100ml),用100ml饱和的碳酸氢钠水溶液洗涤有机相。然后,浓缩有机相,得到配体b-350(1.3g,2.4mmol,产率85.4%)。
1hnmr(400mhz,cdcl3,δ,ppm):8.21(s,1h),7.70(d,j=7.6hz,1h),7.25(s,1h),6.99(t,j=7.6hz,1h),2.03-1.90(m,18h),1.71(s,12h);
31pnmr(162mhz,cdcl3,δ,ppm):-5.59(s).
(合成例1-2):配体b-352的合成
根据下述方案合成配体b-352。
(1)化合物12的合成
将无水氯化锌(287.9g,2.11mol)一次都放进浓盐酸(12m,198.0ml)中。在无水氯化锌溶于盐酸之后,添加化合物11(100.0g,634.0mmol)。然后,在35℃下搅拌溶液16小时,得到黄色悬浮溶液。
在冷却悬浮溶液之后,用石油醚对其进行萃取(80ml×3)。将50ml水和浓硫酸分几部分添加至有机相,直到未观察到变色。用水(50ml×5)洗涤有机相,用无水硫酸钠干燥,过滤,然后浓缩,得到粗产物。
通过减压蒸馏纯化粗产物(沸点60℃/20mmhg),得到无色油状的化合物12。产量:90.0g(515.4mmol,产率:80.5%)
(2)化合物14的合成
在氮气气氛中,将镁(7.1g,293.1mmol)放进三颈烧瓶中,然后向其中添加无水thf(80ml)和碘(10.0mg,39.4μmol)。然后,向其中缓慢添加化合物12(40.0g,229.0mmol)。在70℃下搅拌反应溶液3小时,得到含有化合物13的黑色悬浮液。在将黑色悬浮液冷却至0℃之后,以逐滴方式向其中添加溶于甲苯(50ml)的三氯化磷(11.0g,80.1mmol)。在0℃下搅拌如此得到的悬浮溶液1小时,然后在70℃下搅拌14小时,得到白色悬浮溶液。通过过滤分离悬浮溶液,并浓缩滤液,得到黄色油状的化合物14(粗产物)。
(3)化合物16的合成
将化合物15(2.1g,15.2mmol)溶于thf(30ml),并在-78℃下向其中添加正丁基锂(2.5m,6.1ml,15.2mmol)。在0℃下搅拌它们1小时。将10ml的化合物14(3.5g,10.1mmol)的thf溶液添加到反应溶液中,并在20℃下搅拌混合溶液16小时,得到含有化合物16的黄色溶液。黄色溶液原样用于后续反应。
(4)化合物6b的合成
在氮气气氛中,在0℃下,将n-buli(2.5m,6.48ml,16.2mmol)添加至含有化合物16(4.5g,10.1mmol)的黄色溶液的thf30ml的溶液,并在0℃下搅拌它们两个小时。在0℃下将六氟苯(2.8g,15.2mmol)添加至反应溶液,并在20℃下搅拌它们16小时,得到黄色溶液。用水淬灭反应溶液,并用醋酸乙酯萃取(20ml×2)。用水(20ml)和盐水(20ml)洗涤有机相,用硫酸钠干燥,然后浓缩,得到粗产物。通过使用石油醚/醋酸乙酯=100/1作为洗脱液的硅胶柱,纯化粗产物,得到化合物6b。
(5)配体b-352的合成
在0℃下,将hcl/醋酸乙酯(4m,734.5μl,2937.9μmol)添加至10ml的化合物6b(200.0mg,293.8μmol)的醋酸乙酯溶液,并在15℃下搅拌它们30分钟。然后,浓缩混合溶液,通过向其中通过添加饱和的碳酸氢钠水溶液(30ml)淬灭,然后用二氯甲烷(20ml×2)萃取。用无水硫酸钠干燥有机相,然后浓缩,得到配体b-352。
1hnmr(400mhz,c6d6,δ,ppm):7.99(d,j=10.08hz,1h),7.51(d,j=7.60,2.52,1.76hz,1h),7.06(d,j=7.32hz,1h),6.82(t,j=7.60hz,1h),2.79(sept,j=7.08hz,1h),2.18-2.09(m,1h),1.96-1.86(m,3h),1.81-1.74(m,1h),1.69-1.65(m,1h),1.61-1.47(m,3h),1.42-1.32(m,2h),1.24-1.15(m,2h),1.07-1.02(m,1h),0.97-0.93(m,9h),0.90-0.86(m,10h),0.54-0.45(m,1h),0.34(d,j=7.84hz,3h);
31pnmr(162mhz,c6d6,δ,ppm):-37.52(s).
(合成例1-3):配体b-415的合成
根据下述方案合成配体b-415。
(1)化合物14的合成
在氮气气氛中,将镁(7.12g,293.06mmol)放进三颈烧瓶中,并在室温下,向其中添加无水thf(30ml)和碘(158.76mg,625.49μmol,126μl)。然后,以逐滴方式向其中缓慢添加10ml的化合物12(40g,228.95mmol)的thf溶液,并分两批向其中添加1,2-二溴乙烷(430.11mg,2.29mmol,172.73μl)。在68℃下搅拌反应溶液3小时,得到黑色悬浮液。将反应溶液冷却至室温,然后过滤,将滤液添加到120ml的三氯化磷(8.59g,62.55mmol)的己烷溶液中,得到白色悬浮液。将悬浮液缓慢地加热到室温,并在68℃下搅拌16小时。过滤反应溶液,并在减压下浓缩滤液,得到浅黄色油状的产物。然后,通过减压蒸馏(140℃-155℃,80pa)纯化产物,得到纯度为61%的化合物14(21.7g,38.37mmol,产率30.7%)。
(2)化合物17的合成
在氩气气氛中,在0℃下,将氢化铝锂(792.22mg,20.87mmol)添加至50ml的化合物14(6.0g,17.39mmol)的thf溶液,并在18℃下搅拌它们12小时,得到白色悬浮液。在0℃下,将脱气的水(1.2ml)和脱气的15%氢氧化钠水溶液(3.6ml)添加至反应溶液。过滤后,用二氯甲烷(50ml×3)洗涤固体残留物,得到白色固体状的化合物17(5.9g,16.72mmol,产率96.13%,纯度88%)。
(3)化合物19的合成
在0℃下,将化合物18(100.00g,665.69mmol,102.04ml)添加至氢化钠(66.30g,1.66mol)在thf(300.00ml)中的悬浮溶液,并在0℃下搅拌它们30分钟。在0℃下,将氯甲基甲基醚(107.19g,1.33mol,101.12ml)添加至所得到的反应溶液,并在15℃下搅拌它们15小时,得到白色悬浮液。用水(200ml)淬灭反应溶液,并用醋酸乙酯(200ml×3)萃取。用盐水(200ml)洗涤混合有机层。然后,用硫酸钠使有机层脱水,并过滤。浓缩滤液,由此得到粗产物。通过硅胶柱(石油醚作为洗脱液)纯化粗产物,得到化合物19(112.00g,576.52mmol,86.60%)。
(4)化合物20的合成
首先,在0℃下将n-buli(2.5m,22.65ml)添加到化合物19(10.00g,51.47mmol)的thf溶液(30.00ml)中。在0℃下搅拌反应溶液1小时。然后,向其中添加碘(15.68g,61.76mmol,12.44ml),并在25℃下搅拌它们16小时,得到黄色溶液。然后,用饱和的硫酸钠水溶液(30ml)淬灭反应溶液,并用醋酸乙酯(30ml×3)萃取。用盐水(15ml)洗涤混合有机层,用硫酸钠脱水并过滤。浓缩滤液,得到粗产物。通过硅胶柱(石油醚作为洗脱液)纯化粗产物,得到化合物20(12.00g,37.48mmol,产率72.82%)。
(5)化合物6c的合成
向化合物20(5.9g,16.72mmol)、化合物17(5.95g,16.72mmol)、pd(dba)2(961.50mg,1.67mmol)、叔丁醇钠(3.21g,33.44mmol)和双[2-(二苯基膦基)苯基]醚(1.80g,3.34mmol)的混合物添加甲苯(80ml)。在氮气气氛中,在110℃下搅拌它们18小时,得到棕色悬浮液。将反应溶液冷却至室温,然后过滤。用醋酸乙酯(100ml×4)洗涤固体残留物,与滤液混合,并浓缩,得到黑色油状的粗产物。通过硅胶柱(石油醚作为洗脱液)纯化粗产物。然后,在80℃下,减压干燥粗产物4小时,得到黄色固体状的化合物6c(5.3g,9.86mmol,产率58.95%)。
(6)配体b-415的合成
将hcl/醋酸乙酯(2m,30.00ml)添加至20ml的化合物6c(1.2g,2.39mmol)的二氯甲烷溶液中。在18℃下搅拌反应溶液24小时,得到黄色溶液。浓缩反应溶液,得到粗产物。用饱和的碳酸氢钠水溶液(30ml)将粗产物的ph调节到6.5至7.0。用二氯甲烷(35ml×3)萃取粗产物,并在减压下浓缩,得到浅黄色固体状的配体b-415(700mg,1.45mmol,产率60.74%,纯度95%)。
1hnmr(400mhz,c6d6,δ,ppm):8.19(d,j=11.81hz,1h),7.38(dt,j=7.45,1.96hz,1h),7.28(dd,j=7.64,1.20hz,1h),6.83(t,j=7.64hz,1h),2.94-2.81(m,1h),2.25-2.10(m,1h),2.00-1.78(m,4h),1.73-1.63(m,1h),1.62-1.46(m,5h),1.55(s,9h),1.44-1.30(m,2h),1.28-1.16(m,2h),1.13-0.89(m,3h),0.96(d,j=6.88hz,3h),0.93(d,j=6.76hz,3h),0.93(d,j=6.88hz,3h),0.87(d,j=6.88hz,3h),0.85(d,j=6.88hz,3h),0.61-0.40(m,1h),0.32(d,j=6.76hz,3h);
31pnmr(162mhz,c6d6,δ,ppm):-37.76(s).
(合成例1-4):配体b-414的合成
根据下述方案合成配体b-414。
(1)化合物22的合成
首先,在-78℃下,将n-buli(2.5m,2.46ml)添加到化合物21(2.00g,5.85mmol)的醚溶液(10.00ml)中,并在-78℃下搅拌它们1小时。将三甲基氯硅烷(762.65mg,7.02mmol,886.81μl)在-78℃下添加至反应溶液,并在20℃下搅拌它们16小时,得到白色悬浮液。将水(20ml)添加至反应溶液,并用醋酸乙酯(50ml×3)萃取反应溶液。用硫酸钠使混合有机相脱水,过滤,然后浓缩,得到粗产物。通过硅胶柱(石油醚作为洗脱液)纯化粗产物,得到化合物22(1.30g,3.88mmol,产率66.27%)。
(2)化合物23的合成
首先,在-78℃下,将n-buli(2.5m,1.3ml)添加到化合物22(1.00g,2.98mmol)的醚溶液(10.00ml)中,并在-78℃下搅拌它们1小时。在-78℃下将化合物17(1.94g,2.98mmol)添加至如此得到的反应溶液,并在20℃下搅拌它们12小时。在-78℃下向其中添加硼烷二甲硫醚(10m,357.60μl),并在20℃下搅拌它们12小时,得到白色悬浮液。在0℃下,将水(10ml)添加至反应溶液,并用醋酸乙酯(20ml×3)萃取反应溶液。用硫酸钠使如此得到的混合有机层脱水,并过滤。然后,浓缩滤液,得到粗产物。通过硅胶柱(石油醚作为洗脱液)纯化粗产物,得到化合物23(700.00mg,1.21mmol,产率40.59%)。
(3)化合物24的合成
首先,将1,4-二氮杂双环[2.2.2]辛烷(814.05mg,7.26mmol,798.09μl)添加至化合物23(2.10g,3.63mmol)在甲苯中的悬浮液(50.00ml),并在70℃下搅拌反应混合溶液16小时。在减压下除去所有溶剂,得到黄色油。然后,通过硅胶柱(石油醚作为洗脱液)纯化该油,得到化合物24(1.20g,2.12mmol,产率58.52%)。
(4)配体b-414的合成
在20℃下,将化合物24(1.20g,2.12mmol)的乙醇溶液(5.00ml)添加至pd/c(2.40g,2.12mmol)在乙醇(80.00ml)中的悬浮液,并在氢气存在下,在20℃下搅拌它们160小时,得到黑色悬浮液。通过c盐过滤反应溶液,并用二氯甲烷(100ml)洗涤。在减压下浓缩滤液,得到深黄色油。通过硅胶柱(石油醚作为洗脱液)纯化该油,得到黄色油状的配体b-414(350.00mg,737.20μmol,产率34.77%)。
1hnmr(400mhz,c6d6,δ,ppm):7.81(d,j=11.24hz,1h),7.50(ddd,j=7.58,2.97,1.70hz,1h),7.43(dd,j=7.14,1.52hz,1h),6.88(t,j=7.39hz,1h),2.92-2.78(m,1h),2.19-2.11(m,1h),1.99-1.76(m,4h),1.72-1.45(m,4h),1.44-1.31(m,2h),1.30-1.14(m,2h),1.13-0.99(m,4h),0.96(d,j=6.82hz,3h),0.94(d,j=6.06hz,3h),0.93(d,j=6.82hz,3h),0.87(d,j=6.00hz,3h),0.84(d,j=6.82hz,3h),0.48-0.46(m,1h),0.44(s,9h),0.32(d,j=6.82hz,3h);
31pnmr(162mhz,c6d6,δ,ppm):-39.04(s).
(合成例1-5):配体b-439的合成
根据下述方案合成配体b-439。
(1)化合物17的合成
在氩气气氛中,在0℃下,将氢化铝锂(1.13g,29.66mmol)添加至100ml的化合物14(9.3g,26.96mmol)的thf溶液,并在10℃下搅拌它们48小时,得到白色悬浮液。在0℃下,将脱气的水(1.2ml)、脱气的15%氢氧化钠水溶液(1.2ml)和脱气的水(3.6ml)以该顺序添加至悬浮液。在过滤悬浮液之后,用二氯甲烷(50ml×3)洗涤固体残留物,与滤液混合,并浓缩,得到白色固体状的化合物17(7.5g,20.77mmol,产率77.05%,纯度86%)。
(2)化合物6d的合成
向化合物25(3g,13.82mmol)、化合物17(4.99g,13.82mmol)、三(二苄叉基丙酮)二钯(794.72mg,1.38mmol)、双[2-(二苯基膦基)苯基]醚(1.49g,2.76mmol)和叔丁醇钠(2.66g,27.64mmol)的混合物添加甲苯(80ml)。将它们回流12小时,得到黑色悬浮液。在减压下除去挥发物,得到粗产物。在85℃下,减压干燥粗产物4小时,得到棕色固体状的化合物6d(3.1g,6.91mmol,产率50.02%,纯度99.6%)。
(3)配体b-439的合成
在氩气气氛中,在0℃下将盐酸/醋酸乙酯(4m,40ml)添加到化合物6d(3.1g,6.94mmol)的醋酸乙酯溶液(20ml),并在20℃下搅拌它们3.5小时,得到棕色溶液。然后,在减压下除去溶剂,得到粗产物。将粗产物溶于二氯甲烷(50ml),用饱和碳酸氢钠水溶液(50ml)洗涤有机层并浓缩,由此得到棕色固体状的配体b-439(2.36g,5.74mmol,产率82.77%,纯度98%)。
1hnmr(400mhz,c6d6,δ,ppm):7.53(dd,j=7.7hz,2.6hz,1h),7.15(t,j=3.3hz,2h),6.84-6.89(m,2h),3.0(sept,j=6.4hz,1h),2.23-2.32(m,1h),1.92-2.07(m,4h),1.76-1.81(m,1h),1.68-1.76(m,3h),1.26-1.36(m,2h),1.15-1.24(m,2h),1.09-1.13(m,1h),1.01-1.05(m,9h),0.91-0.98(m,10h),0.58-0.67(m,1h),0.43(d,j=6.6hz,3h);
31pnmr(162mhz,cdcl3,δ,ppm):-46.64(s).
(合成例1-6):配体b-412的合成
根据下述方案合成配体b-412。
(1)化合物2的合成
在氩气气氛中,在80℃下搅拌化合物1(10.00g,73.41mmol)、氯化铝(10.47g,78.55mmol,4.29ml)和三氯化磷(50.70g,369.18mmol,32.50ml)的混合物6小时,得到橙色悬浮液。通过在大气压下蒸馏除去过量的三氯化磷。然后,过滤反应溶液,将水(150ml)添加至滤液,并用二氯甲烷(150ml×2)萃取反应溶液。用硫酸钠使混合有机层脱水并过滤,浓缩滤液,由此得到橙色固体状的化合物2(12.90g,33.16mmol,产率45.0%)。
(2)化合物3的合成
在氩气气氛中,在-14℃下,将氢化铝锂(3.27g,86.27mmol)经两小时添加至化合物2(12.90g,36.56mmol)的thf溶液(150.00ml)。在加热至30℃后,搅拌反应溶液18小时,得到灰色悬浮液。将悬浮液再次冷却至-14℃,并向其中添加1m盐酸(100ml)。用醋酸乙酯萃取悬浮液,并用硫酸钠使混合有机层脱水,过滤。然后,浓缩滤液,得到化合物3(粗产物)。
(3)化合物20的合成
首先,在0℃下,将n-buli(2.5m,24.71ml)添加到化合物19(10.00g,51.47mmol)的thf溶液(25.00ml)中,并在0℃下搅拌它们1小时。然后,将碘(15.68g,61.76mmol,12.44ml)添加至反应溶液,并在25℃下搅拌它们16小时,得到棕色溶液。将水(100ml)添加至反应溶液,并用醋酸乙酯(70ml×3)萃取反应溶液。用饱和的硫代硫酸钠(50ml×2)洗涤混合有机层,用硫酸钠脱水并过滤。然后,浓缩滤液,得到黑色油状的粗产物。然后,通过硅胶柱(石油醚作为洗脱液)纯化粗产物,得到浅黄色油状的化合物20(9.38g,29.30mmol,产率56.92%)。
(4)化合物6e的合成
在氩气气氛中,向化合物20(6.88g,21.49mmol)、化合物3(6.50g,21.49mmol)、叔丁醇钠(4.13g,42.98mmol)、双[2-(二苯基膦基)苯基]醚(2.31g,4.30mmol)和三(二苄叉基丙酮)二钯(1.97g,2.15mmol)的混合物添加甲苯(100ml)。在110℃下搅拌它们15小时,得到黑色悬浮液。将反应溶液冷却至30℃,并过滤。用醋酸乙酯(100ml×4)洗涤固体残留物,与滤液混合,并浓缩,得到黑色油状的粗产物。通过硅胶柱(石油醚/醋酸乙酯=1/0-50/1作为洗脱液)纯化粗产物,并在120℃下减压干燥,得到化合物6e(2.80g,5.66mmol,产率26.34%)。
(5)配体b-412的合成
在氩气气氛中,在0℃下将盐酸/醋酸乙酯(4m,30.49ml)添加到化合物6e(1.83g,3.70mmol)的二氯甲烷溶液(10.00ml),并在15℃下搅拌它们3小时,得到深黄色溶液。然后,在减压下除去溶剂,得到粗产物。将二氯甲烷添加至粗产物,并用饱和的碳酸氢钠水溶液(50ml)洗涤粗产物,浓缩,由此得到黄色固体状的配体b-412(1.65g,3.66mmol,产率98.96%)。
1hnmr(400mhz,c6d6,δ,ppm):8.92(d,j=11.75hz,1h),7.51(d,j=7.52hz,1h),7.37(d,j=7.77hz,1h),6.88(t,j=7.70hz,1h),2.03(d(br),j=12.06hz,6h),1.94(d(br),j=12.06hz,6h),1.82-1.72(br,6h),1.60(s,9h),1.58-1.48(br,12h);
31pnmr(162mhz,c6d6,δ,ppm):3.31(s).
(比较合成例1-1):配体b-348的合成
根据下述方案合成配体b-348。
(1)化合物5f的合成
首先,在-78℃下,将正丁基锂(2.5m,4.0ml,10.0mmol)添加至30ml的化合物4(3.0g,10.0mmol)的thf溶液,并在-78℃下搅拌它们1小时。然后,在-78℃下添加二环己基氯化膦(2.3g,10.0mmol),并在10℃下搅拌它们12小时。将反应溶液倒入冰水中,并用醋酸乙酯(30ml×3)萃取。用无水硫酸钠干燥有机相并浓缩,由此得到粗产物。然后,通过硅胶柱(石油醚/醋酸乙酯=10:1作为洗脱液)纯化粗产物,得到浅黄色油状的化合物5f(2.2g,产率53.2%)。
(2)化合物6f的合成
首先,在-78℃下,将正丁基锂(2.5m,2.6ml,6.4mmol)添加至30ml的化合物5f(2.2g,5.3mmol)的thf溶液,并在-78℃下搅拌它们1小时。然后,在-78℃下添加六氟苯(1.5g,8.0mmol),并在10℃下搅拌反应溶液12小时,得到黄色溶液。将反应溶液倒入冰水(30ml)中,并用醋酸乙酯(30ml×3)萃取。用无水硫酸钠干燥有机相并浓缩,由此得到粗产物。然后,通过硅胶柱(石油醚/醋酸乙酯=10:1作为洗脱液)纯化粗产物,得到粘稠的浅黄色油状的化合物6f(0.8g,产率30.1%)。
(3)配体b-348的合成
在0℃下,将hcl/醋酸乙酯(729.3mg,20.0mmol)添加至15ml的化合物6f(1.0g,2.0mmol)的醋酸乙酯溶液,并在15℃下搅拌它们15分钟。浓缩反应溶液,并用饱和的碳酸氢钠水溶液(30ml)淬灭。然后,用二氯甲烷(50ml×2)萃取反应溶液,用无水硫酸钠干燥有机相并浓缩,由此得到粗产物。通过硅胶柱(石油醚/醋酸乙酯=5/1作为洗脱液)纯化粗产物,得到配体b-348(800.0mg,产率87.6%)。
1hnmr(400mhz,cdcl3,δ,ppm):7.42-7.36(m,1h),7.23(d,j=7.6hz,1h),7.03(t,j=7.6hz,1h),2.02-1.59(m,12h),1.32-1.11(m,10h);
31pnmr(162mhz,cdcl3,δ,ppm):-33.26(s).
1-3.配合物的合成
(实施例1-1):配合物(b-350)ni((1,4,5-η)-coe)的合成
所有下述操作均在高纯氩气气氛中进行。以下,双-1,5-环辛二烯镍(0)称为ni(cod)2,和(1,4,5-η)-4-环辛烯-1-基配体称为(1,4,5-η)-coe。
首先,将配体b-350(65mg,0.12mmol)称重并放进25ml圆底烧瓶中。接着,称量ni(cod)2(43mg,0.16mmol)并放进另一个烧瓶中,并溶于甲苯(8.0ml)中以制备20mmol/ml的ni(cod)2的甲苯溶液。如此得到的溶液是黄色透明的。将由此得到的ni(cod)2的甲苯溶液(6.2ml)添加到含有配体b-350的圆底烧瓶中以得到溶液。然后,在室温下搅拌它们1小时。此时,已确认所述溶液的颜色从暗黄色逐渐变成棕色,且没有沉淀。因此,得到20mmol/ml的b-350与ni(cod)2的反应产物((b-350)ni((1,4,5-η)-coe))的溶液。假定b-350和ni(cod)2以1:1的摩尔比反应形成镍配合物,计算反应产物的浓度。
(实施例1-2):配合物(b-352)ni((1,4,5-η)-coe)的合成
除使用配体b-352替代配体b-350以外,以与实施例1-1中相同的方式合成配合物(b-352)ni((1,4,5-η)-coe)。
(实施例1-3):配合物(b-350)niph(pet3)的合成
根据下述方案合成配合物(b-350)niph(pet3)。
将ni(cod)2(1.57g,5.71mmol)添加至80mlschlenk管,并溶于二乙基醚(10ml)。用冰水冷却该溶液,并添加三乙基膦(25mmol,1.0m的thf溶液)。将溶液升温至室温,并搅拌2小时。在除去溶剂之后,将schlenk管转移到手套箱中。添加己烷(5ml),并通过c盐过滤所得到的混合物。然后,用己烷(5ml)洗涤c盐。将氯苯(1.10g,9.77mmol)添加至滤液,并在室温下进一步搅拌滤液4小时。然后,在减压下除去溶剂,并添加戊烷(5ml)。通过c盐过滤如此得到的混合物,并用戊烷(5ml)洗涤c盐。然后,将滤液在-35℃下保存整夜,得到晶体。用冷冻的戊烷洗涤晶体,并将如此得到的晶体在室温下减压干燥2小时,得到橙色固体状的目标产物niphcl(pet3)2(2.00g,86%)。
1hnmr(500mhz,c6d6)δ7.43(d,j=7.5hz,2h),6.97(t,j=7.3hz,2h),6.80(t,j=7.0hz,1h),1.32(m,12h),1.02(m,18h);
13cnmr(126mhz,c6d6):155.31(t,j=54hz,1c),137.54(t,j=6hz,2c),126.79(t,j=4hz,2c),121.33(t,j=4hz,1c),14.25(t,j=20hz,6c),8.32(s,6c);
31pnmr(202mhz,c6d6)δ11.1;
元素分析,对于c18h35clnip2的计算值;c,53.05;h,8.66.求得c,52.81;h,8.57。
在手套箱中,将3ml的双(三甲基甲硅烷基)氨基钾(19mg,0.089mmol)的二乙基醚溶液逐渐添加到收集在15ml小瓶中的配体b-350(50mg,0.089mmol)中。在室温下搅拌反应混合物10分钟。将1.5ml的niphcl(pet3)2(36mg,0.089mmol)的二乙基醚溶液以逐滴方式添加至该反应溶液,并添加thf(3ml)。然后,在室温下整夜搅拌反应溶液。通过c盐过滤反应混合物,并用thf(2ml)洗涤c盐。在减压下除去挥发物之后,用己烷萃取产物,并通过c盐过滤。用己烷(3ml)洗涤c盐。在减压下再次除去挥发物,并添加戊烷(1.5ml)。将所得物在-35℃下静置整夜。通过过滤收集如此生产的固体,用冷冻的戊烷(1ml)洗涤,并在室温下减压干燥1小时,由此得到配合物(b-350)niph(pet3)(59mg,产率82%)。
1hnmr(400mhz,c6d6)δ7.74(d,j=8hz,2h),7.61(t,j=6.6hz,1h),6.97(d,j=6.8hz,2h),6.80(t,j=7.6hz,1h),6.65(t,j=7.0hz,1h),2.53-2.50(m,6h),2.13-2.09(m,6h),1.82(s,6h),1.65-1.54(m,12h),0.93-0.83(m,15h);
31pnmr(162mhz,c6d6)δ42.88(d,j=260hz,1p),12.83(d,j=260hz,1p).
以下述方式进行(b-350)niph(pet3)的x射线晶体结构分析。
在手套箱中,在室温下使用正戊烷再次溶解配合物(b-350)niph(pet3)。将溶液转移到小瓶中,冷却至-30℃,然后放置在-30℃的冰柜中。结果,观察到(b-350)niph(pet3)的单晶生长。
从所得到的单晶中选择尺寸为约0.25×0.20×0.18mm的单晶,并安装在环形状的支架上。将该支架放在-180℃的由rigakucorporation制造的saturn724ccd衍射仪上,该衍射仪配备有测角仪底座(goniometericstage)和ccd检测器。将单晶设置在距离衍射仪45mm的位置处。使用由石墨单色化的mo-kα束进行衍射强度测量。首先确定晶格常数,并使用程序crystalclear得到720帧的反射数据。在所得到的数据上进行洛伦兹校正。所得到的单晶的晶胞为单斜晶系,空间群为p21/n。通过使用程序shelxt2014的直接法确定结构。对于shelxl2014观察到的反射的f2,通过全矩阵最小二乘法进行精确化。在除氢以外的所有原子上,通过各向异性温度因子进行结构精确化;通过计算确定氢原子的位置;并通过各向同性温度因子进行结构精确化。使用r2(i>2σ(i))=0.1147,收敛数据。
图1是配合物(b-350)niph(pet3)的ortep图。作为x射线晶体结构分析的结果,明显的是,所得到的配合物具有化学式c44h53f5niop2和如图1所示的平面四配位结构。膦上的乙基和1,2,3,4,5-五氟苯基是无序的。ni与p2之间的距离是
(实施例1-4):配合物(b-415)ni((1,4,5-η)-coe)的合成
除使用配体b-415代替配体b-350以外,以与实施例1-1中相同的方式合成配合物(b-415)ni((1,4,5-η)-coe)。
(实施例1-5):配合物(b-414)ni((1,4,5-η)-coe)的合成
除使用配体b-414代替配体b-350以外,以与实施例1-1中相同的方式合成配合物(b-414)ni((1,4,5-η)-coe)。
(实施例1-6):配合物(b-439)ni((1,4,5-η)-coe)的合成
除使用配体b-439代替配体b-350以外,以与实施例1-1中相同的方式合成配合物(b-439)ni((1,4,5-η)-coe)。
(实施例1-7):配合物(b-412)ni((1,4,5-η)-coe)的合成
除使用配体b-412代替配体b-350以外,以与实施例1-1中相同的方式合成配合物(b-412)ni((1,4,5-η)-coe)。
(比较例1-1):配合物(b-348)ni((1,4,5-η)-coe)的合成
除使用配体b-348代替配体b-350以外,以与实施例1-1中相同的方式合成配合物(b-348)ni((1,4,5-η)-coe)。
1-4.丙烯聚合或共聚合
(实施例1-1a):使用实施例1-1的配合物的丙烯聚合
将丙烯(500ml)引入内容积为约2l的感应搅拌式高压釜中。将实施例1-1的配合物((b-350)ni((1,4,5-η)-coe))导入具有氮气的高压釜。在搅拌混合物的情况下,将高压釜升温至50℃。从高压釜温度达到50℃时的时间开始聚合,并进行一段预定时间。在除去未反应的单体之后,打开高压釜,并进行通过加热的干燥,得到聚合物。
(实施例1-2a):使用实施例1-2的配合物的丙烯聚合
除使用实施例1-2的配合物((b-352)ni((1,4,5-η)-coe))代替实施例1-1的配合物((b-350)ni((1,4,5-η)-coe))以外,以与实施例1-1a中相同的方式得到聚合物。
(实施例1-3a):使用实施例1-3的配合物的丙烯聚合
将50ml不锈钢高压釜用120℃的干燥机干燥3小时,组装,然后在125℃下减压干燥2小时。在将高压釜冷却至室温之后,在氩气气氛中,将实施例1-3的配合物((b-350)niph(pet3))(5.0μmol,10.0ml,0.50mmol/l甲苯溶液)、甲苯(5ml)和丙烯6ml添加到高压釜中。然后,将高压釜升温至50℃,并搅拌43小时。在将高压釜冷却至室温之后,进行排出剩余的丙烯,并用乙醇(20ml)淬灭反应产物,然后通过过滤收集聚合物。在100℃至120℃下,减压干燥聚合物2小时,得到目标聚合物。
(实施例1-4a):使用实施例1-4的配合物的丙烯聚合
除使用实施例1-4的配合物((b-415)ni((1,4,5-η)-coe))代替实施例1-1的配合物((b-350)ni((1,4,5-η)-coe))以外,以与实施例1-1a中相同的方式得到聚合物。
(实施例1-5a):使用实施例1-5的配合物的丙烯聚合
除使用实施例1-5的配合物((b-414)ni((1,4,5-η)-coe))代替实施例1-1的配合物((b-350)ni((1,4,5-η)-coe))以外,以与实施例1-1a中相同的方式得到聚合物。
(实施例1-6a):使用实施例1-6的配合物的丙烯聚合
除使用实施例1-6的配合物((b-439)ni((1,4,5-η)-coe))代替实施例1-1的配合物((b-350)ni((1,4,5-η)-coe))以外,以与实施例1-1a中相同的方式得到聚合物。
(实施例1-7a):使用实施例1-7的配合物的丙烯聚合
除使用实施例1-7的配合物((b-412)ni((1,4,5-η)-coe))代替实施例1-1的配合物((b-350)ni((1,4,5-η)-coe))以外,以与实施例1-1a中相同的方式得到聚合物。
(实施例1-2b):使用实施例1-2的配合物的共聚合
除使用实施例1-2的配合物((b-352)ni((1,4,5-η)-coe))代替实施例1-1的配合物((b-350)ni((1,4,5-η)-coe))且在将实施例1-2的配合物导入具有氮气的高压釜之后将10-十一碳烯酸乙酯进一步添加至高压釜以外,以与实施例1-1a中相同的方式得到共聚物。对于共聚物中共聚单体的含量比,通过1hnmr测量测定丙烯:共聚单体的摩尔比,并在表中表示为共聚单体含量mol%。
(实施例1-2c):使用实施例1-2的配合物的共聚合
除使用实施例1-2的配合物((b-352)ni((1,4,5-η)-coe))代替实施例1-1的配合物((b-350)ni((1,4,5-η)-coe))且在将实施例1-2的配合物导入具有氮气的高压釜之后将10-十一碳烯-1-醇进一步添加至高压釜以外,以与实施例1-1a中相同的方式得到共聚物。对于共聚物中共聚单体的含量比,通过1hnmr测量测定丙烯:共聚单体的摩尔比,并在表中表示为共聚单体含量mol%。
(比较例1-1a):使用比较例1-1的配合物的丙烯聚合
除使用比较例1-1的配合物((b-348)ni((1,4,5-η)-coe))代替实施例1-1的配合物((b-350)ni((1,4,5-η)-coe))以外,以与实施例1-1a中相同的方式得到聚合物。
下表4-1用来比较用于合成实施例1-1至1-7和比较例1-1的配合物的镍原料和配体。
表4-1
下表4-2示出实施例1-1a至1-7a、实施例1-2b和1-2c以及比较例1-1a的聚合条件和聚合结果。在表4-2中,聚合活性表示每1摩尔用于聚合的配合物和每1小时聚合时间的共聚物产量(g)。在表4-2中,作为关于聚合物的gpc测量结果,提及重均分子量mw和分子量分布mw/mn。表4-2中的共聚合量表示共聚单体添加量相对于提供用于聚合的单体总量的比例。
表4-2
1-5.考虑
从表4-2中的比较例1-1a清楚地是,在使用常规配合物(比较例1-1)的聚丙烯聚合的情况下,由此得到的聚合物的分子量mw为1,440,小。同时,从表4-2中的实施例1-1a至1-7a清楚地是,在使用本公开的金属配合物(实施例1-1至1-7)的聚丙烯聚合的情况下,由此得到的聚合物的分子量mw为3,300以上,大。正如刚才所描述的,揭示了与r5和r6是环己基的情况相比,体积大的取代基用作r5和r6的本公开的金属配合物提供了具有高分子量的聚丙烯。此外,在使用本公开的金属配合物的情况下,聚合活性为4.6×102(g/mol/hr)以上,优异,且将由此得到的聚丙烯的分子量分布mw/mn抑制到2.2以下。
此外,从表4-2中的实施例1-2b和1-2c清楚地是,通过本公开的金属配合物,以优异的聚合活性实现了α-烯烃与含极性基团的单体的共聚合。
基于上述理由,很清楚的是,本公开的金属配合物提供了相比于以前具有更高分子量的α-烯烃均聚物,能够以优异聚合活性实现α-烯烃与含极性基团的单体的共聚合,并且具有优越的技术意义。
<本公开的第二实施方式>
2-1.评价方法
(1)重均分子量mw、数均分子量mn和分子量分布mw/mn:通过下述gpc测量来测定。
首先,将样品(约20mg)收集在用于polymerlaboratoriesltd制造的高温gpc的预处理单元pl-sp260vs用的小瓶中,并向其中添加含有bht作为稳定剂的邻二氯苯(bht的浓度=0.5g/l),以将聚合物浓度调节至0.1质量%。通过在上述用于高温gpc的预处理单元pl-sp260vs中在135℃下加热,溶解聚合物,并用玻璃过滤器过滤以制备样品溶液。在本公开的gpc测量中,玻璃过滤器没有捕获到聚合物。接着,使用由waterscorporation制造的gpcv2000进行gpc测量,所述gpcv2000配备有作为柱的由tosohcorporation制造的tskgelgmh-ht(30cm×4个)和ri检测器。采用下述测量条件:样品溶液的注入量:约520μl;柱温:135℃;溶剂:邻二氯苯;和流量:1.0ml/min。如下进行分子量的计算。即,使用可商购获得的单分散聚苯乙烯作为标准样品,由聚苯乙烯标准样品和乙烯聚合物的粘度公式制备保留时间对分子量的校准曲线,并基于校准曲线进行分子量的计算。作为粘度公式,使用[η]=k×mα,对于聚苯乙烯,使用k=1.38e-4,α=0.70;和对于乙烯系聚合物,使用k=4.77e-4,α=0.70。对于丙烯系聚合物,使用k=1.03e-4,α=0.78。
2-2.配体的合成
(合成例2-1):配体b-349的合成
根据下述方案合成配体b-349。
在以下提及的化学式中,-omom表示甲氧基甲氧基(-och2och3)。
(1)化合物33a的合成
在氩气气氛中,在0℃下,将正丁基锂(2.5m,24.6ml,61.5mmol)添加至100ml的化合物15(8.5g,61.5mmol)的thf溶液,并在0℃下搅拌它们1小时。然后,在-78℃下,向其中添加二叔丁基氯化膦(11.1g,61.5mmol,11.7ml),并在10℃下搅拌它们2小时(化合物32的生产)。然后,在0℃下,向其中添加正丁基锂(2.5m,29.5ml,73.8mmol),并在0℃下搅拌反应溶液1小时。在-78℃下,将六氟苯(17.2g,92.3mmol)添加至该反应溶液,并在10℃下搅拌它们12小时。将反应溶液倒入冰水(50ml)中,并用醋酸乙酯(100ml×2)萃取。用无水硫酸钠干燥有机相,并浓缩,由此得到粗产物。通过硅胶柱(石油醚/醋酸乙酯=100:1-20:1作为洗脱液)纯化粗产物,并用石油醚:醋酸乙酯(20:1,50ml)再结晶,得到化合物33a(5.0g,10.7mmol,产率17.4%)。
(2)配体b-349的合成
在氩气气氛中,在0℃下,将hcl/醋酸乙酯(4m,85.1ml,340.2mmol)添加至20.0ml的化合物33a(5.0g,11.2mmol)的二氯甲烷溶液,并在10℃下搅拌它们2小时。在减压下除去挥发物,并将二氯甲烷(100ml)添加至残留物。用饱和的碳酸氢钠水溶液(100ml×2)洗涤有机相,并浓缩,由此得到b-349(3.9g,9.28mmol,产率83.2%)。
1hnmr(400mhz,cdcl3,δ,ppm):8.19(s,1h),7.71(d,j=7.6hz,1h),7.25(s,1h),7.00(t,j=7.4hz,1h),1.28(s,9h),1.25(s,9h);
31pnmr(162mhz,cdcl3,δ,ppm)-5.84(s).
(合成例2-2):配体b-395的合成
根据下述方案合成配体b-395。
(1)化合物33b的合成
首先,在0℃下,将正丁基锂(2.5m,8.7ml,21.8mmol)添加至20ml的化合物15(3.0g,21.7mmol)的thf溶液,并在0℃下搅拌它们1小时。然后,在-78℃下,向其中添加二叔丁基氯化膦(3.9g,21.7mmol,4.1ml),并在15℃下搅拌它们2小时(化合物32的生产)。然后,在0℃下,向其中添加正丁基锂(2.5m,10.9ml,27.2mmol),并在0℃下搅拌它们1小时。然后,在-78℃下添加三甲基氯硅烷(3.54g,32.6mmol,4.1ml),并在15℃下搅拌它们12小时。将反应溶液倒入冰水(50ml)中,并用醋酸乙酯(50ml×2)萃取。用无水硫酸钠干燥有机相,并浓缩,由此得到粗产物。通过硅胶柱(石油醚作为洗脱液)纯化粗产物,得到无色油状的化合物33b(2.3g,6.3mmol,产率28.7%)。
(2)配体b-395的合成
在氩气气氛中,在0℃下,将hcl/醋酸乙酯(2m,15.0ml,30.0mmol)添加至30ml的化合物33b(2.4g,6.8mmol)的二氯甲烷溶液,并在15℃下搅拌它们1.5小时。在减压下除去挥发物,得到浅黄色油。添加二氯甲烷(100ml),用饱和的碳酸氢钠水溶液(100ml)洗涤有机相并浓缩,由此得到白色固体状的b-395(1.0g,2.9mmol,产率91.0%)。
1hnmr(400mhz,cdcl3,δ,ppm):8.01(s,1h),7.56(d,j=7.6hz,1h),7.38(dd,j=7.2hz,1.6hz,1h),6.86(t,j=7.4hz,1h),1.23(s,9h),1.20(s,9h),0.29(s,9h);
31pnmr(162mhz,cdcl3,δ,ppm)-6.04(s).
(合成例2-3):配体b-396的合成
根据下述方案合成配体b-396。
(1)化合物42的合成
参考日本专利申请特开号2016-17134合成化合物41。
首先,在0℃下,将正丁基锂(2.5m,15.8ml,39.5mmol)添加至60ml的化合物41(10.0g,33.0mmol)的thf溶液,并在0℃下搅拌它们1小时。然后,在0℃下向其中添加10ml的碘(10.0g,39.6mmol,8.0ml)的thf溶液。在25℃下搅拌反应混合物16小时。通过添加水(30ml)淬灭该反应混合物,并用醋酸乙酯(30ml×3)萃取。用盐水(15ml)洗涤有机相,用无水硫酸钠干燥,浓缩,得到粗产物。通过硅胶柱(石油醚作为洗脱液)纯化粗产物,得到化合物42(7.5g,17.4mmol,产率53.7%)。
(2)化合物33c的合成
在氮气气氛中,在100℃下将化合物42(900mg,2.1mmol)、二叔丁基膦(337.8mg,2.3mmol)、三(二苄叉基丙酮)二钯(192.3mg,210.0μmol)、叔丁醇钠(403.6mg,4.2mmol)和双[2-(二苯基膦基)苯基]醚(dpephos,1.1g,2.1mmol)的甲苯溶液10.0ml搅拌16小时。浓缩反应混合物,得到粗产物。通过硅胶柱(石油醚:醋酸乙酯=10:1作为洗脱液)纯化粗产物,得到化合物33c(210.0mg,469.2μmol,产率22.34%)。
(3)配体b-396的合成
在0℃下,将hcl/醋酸乙酯(4m,40.0ml,160.0mmol)添加至3ml的化合物33c(3.1g,6.9mmol)的二氯甲烷溶液。在25℃下搅拌反应混合物2小时,得到黄色溶液。浓缩反应混合物,得到粗产物。用饱和的碳酸氢钠水溶液(30ml),将粗产物的ph调节到6.5至7.0。粗产物用二氯甲烷(25ml×3)萃取。用盐水(25ml)洗涤有机相,用无水硫酸钠干燥并浓缩,由此得到配体b-396(2.4g,6.0mmol,产率85.9%)。
1hnmr(400mhz,cdcl3,δ,ppm):8.15(d,j=7.8hz,2h),8.08(s,1h),7.76(dt,j=7.8hz,1.9hz,1h),7.49(dd,j=7.7hz,1.4hz,1h),7.40(t,j=7.6hz,2h),7.27(t,j=7.6hz,2h),7.18(d,j=8.1hz,2h),7.09(t,j=7.7hz,1h),1.32(s,9h),1.29(s,9h);
31pnmr(162mhz,cdcl3,δ,ppm):-5.75(s).
(比较合成例2-1):配体b-399的合成
根据下述方案合成配体b-399。
(1)化合物32的合成
首先,在0℃下,将正丁基锂(2.5m,12.2ml,30.0mmol)添加至30ml的化合物15(4.0g,29.0mmol)的thf溶液,并在0℃下搅拌它们1小时。然后,在-78℃下向其中添加二叔丁基氯化膦(5.2g,29.0g,5.5ml),并在15℃下搅拌它们12小时。将反应溶液倒入冰水(20ml)中,并用醋酸乙酯(20ml×2)萃取。用无水硫酸钠干燥有机相,并浓缩,由此得到粗产物。通过硅胶柱(石油醚:醋酸乙酯=1:0-50:1作为洗脱液)纯化粗产物,得到化合物32(3.5g,9.0g,产率31.2%)。
(2)化合物33d的合成
在氩气气氛中,在-78℃下,将bh3·thf(1.0m,16.7ml,16.7mmol)添加至10ml的化合物32(3.9g,13.9mmol)的thf溶液,并在10℃下搅拌它们1小时。在-78℃下,向其中添加bh3·二甲硫醚(10m,1.7ml,16.7mmol),并在10℃下搅拌它们12小时。在0℃下向该反应溶液中添加冰水(10ml),并在减压下除去挥发物。将水(20ml)添加至反应溶液,并用醋酸乙酯(20ml×3)萃取反应溶液。用无水硫酸钠干燥有机相,并浓缩,由此得到白色固体。用醋酸乙酯(10ml)使白色固体再结晶,得到化合物33d(1.5g,5.1mmol,产率36.4%)。
(3)配体b-399的合成
在氩气气氛中,在0℃下,将hcl/醋酸乙酯(4m,80.0ml,320.0mmol)添加至在二氯甲烷(20ml)中的化合物33d(5.4g,18.2mmol),并在10℃下搅拌它们3小时。在减压下除去挥发物,并添加二氯甲烷(100ml)。用饱和的碳酸氢钠水溶液(100ml)洗涤有机相,并浓缩,由此得到配体b-399(4.0g,16.8mmol,产率92.1%)。
1hnmr(400mhz,cdcl3,δ,ppm):7.85(s,1h),7.57(dt,j=7.6hz,1.4hz,1h),7.28(td,j=7.7hz,1.6hz,1h),6.94(td,j=7.2hz,1.2hz,1h),6.87(td,j=7.5hz,1.2hz,1h),1.32(s,9h),1.29(s,9h);
31pnmr(162mhz,cdcl3,δ,ppm):-6.21(s).
2-3.配合物的合成
(实施例2-1):配合物(b-349)ni((1,4,5-η)-coe))的合成
所有下述操作均在高纯氩气气氛中进行。以下,将双-1,5-环辛二烯镍(0)称为ni(cod)2,(1,4,5-η)-4-环辛烯-1-基配体称为(1,4,5-η)-coe。
首先,将配体b-349(50mg,0.12mmol)称重并放进25ml圆底烧瓶中。接着,称量ni(cod)2(40mg,0.15mmol)并放进另一个烧瓶中,并溶于甲苯(7.3ml)中以制备20mmol/ml的ni(cod)2的甲苯溶液。如此得到的溶液是黄色透明的。将由此得到的ni(cod)2的甲苯溶液(6.2ml)添加到含有配体b-349的圆底烧瓶中以得到溶液。然后,在室温下搅拌它们1小时。此时,已确认溶液的颜色从暗黄色逐渐变成棕色,且没有沉淀。因此,得到20mmol/ml的b-349与ni(cod)2的反应产物((b-349)ni((1,4,5-η)-coe))的溶液。假定b-349和ni(cod)2以1:1的摩尔比反应形成镍配合物,计算反应产物的浓度。
(实施例2-2):配合物(b-395)ni((1,4,5-η)-coe)的合成
除使用配体b-395替代配体b-349以外,以与实施例2-1中相同的方式合成配合物(b-395)ni((1,4,5-η)-coe)。
(实施例2-3):配合物(b-396)ni((1,4,5-η)-coe)的合成
除使用配体b-396替代配体b-349以外,以与实施例2-1中相同的方式合成配合物(b-396)ni((1,4,5-η)-coe)。
(合成例2-4):配合物(b-395)niphpy的合成
根据下述方案合成配合物(b-395)niphpy。
在手套箱中,将配体b-395(53mg,0.17mmol)和氢化钾(17mg,0.43mmol)投入15ml小瓶中。向其中添加二乙基醚(5ml),并搅拌它们30分钟。通过c盐过滤反应混合物,并用二乙基醚(3ml)洗涤c盐。参考非专利文献"marshall,w.j.;grushin,v.v.can.j.chem.2005,83,640"合成niphcl(tmeda)(tmeda:四甲基乙二胺)。将niphcl(tmeda)(49mg,0.17mmol)添加至二乙基醚滤液,并将它们搅拌整夜。通过c盐过滤反应溶液,并用二乙基醚(3ml)洗涤c盐。将吡啶(13mg,0.17mmol)添加至该滤液,并将它们在室温下搅拌整夜。然后,通过c盐过滤反应混合物,并用二乙基醚(1.5ml)洗涤c盐。在减压下除去挥发性组分,得到粗产物。将戊烷(1ml)添加至粗产物,并将粗产物在-35℃下静置整夜。通过过滤收集如此生产的固体,用冷冻的戊烷(1ml)洗涤,并在室温下减压干燥1小时,由此得到(b-395)niphpy(60mg,产率67%)。
1h-nmr(400mhz,c6d6)δ8.72-8.70(m,2h),7.91(d,j=8.0hz,2h),7.54-7.52(m,1h),7.48-7.44(m,1h),6.98(t,j=7.4hz,2h),6.82(t,j=7.4hz,1h),6.67-6.60(m,2h),6.38(t,j=6.8hz,2h),1.42(s,9h),1.39(s,9h),0.25(s,9h);
31p-nmr(162mhz,c6d6)δ58.416.
(实施例2-5):配合物(b-349)niph(pet3)的合成
根据下述方案合成配合物(b-349)niph(pet3)。
将ni(cod)2(1.57g,5.71mmol)添加至80mlschlenk管,并溶于二乙基醚(10ml)。用冰水冷却该溶液,并添加三乙基膦(25mmol,1.0m的thf溶液)。将溶液升温至室温,并搅拌溶液2小时。在除去溶剂之后,将schlenk管转移到手套箱中。添加己烷(5ml),并通过c盐过滤。然后,用己烷(5ml)洗涤c盐。将氯苯(1.10g,9.77mmol)添加至滤液,并在室温下进一步搅拌滤液4小时。然后,在减压下除去溶剂,并添加戊烷(5ml)。通过c盐过滤如此得到的混合物,并用戊烷(5ml)洗涤c盐。然后,将滤液在-35℃下保存整夜,得到晶体。用冷冻的戊烷洗涤晶体,并将如此得到的晶体在室温下减压干燥2小时,得到橙色固体状的目标产物niphcl(pet3)2(2.00g,86%)。
1hnmr(500mhz,c6d6)δ7.43(d,j=7.5hz,2h),6.97(t,j=7.3hz,2h),6.80(t,j=7.0hz,1h),1.32(m,12h),1.02(m,18h);
13cnmr(126mhz,c6d6):155.31(t,j=54hz,1c),137.54(t,j=6hz,2c),126.79(t,j=4hz,2c),121.33(t,j=4hz,1c),14.25(t,j=20hz,6c),8.32(s,6c);
31pnmr(202mhz,c6d6)δ11.1;
元素分析,对于c18h35clnip2的计算值;c,53.05;h,8.66.求得c,52.81;h,8.57.
在手套箱中,将3ml的双(三甲基甲硅烷基)氨基钾(26mg,0.12mmol)的二乙基醚溶液逐渐添加到收集在15ml小瓶中的配体b-349(50mg,0.12mmol)中。在室温下搅拌反应混合物10分钟。将1.5ml的niphcl(pet3)(49mg,0.12mmol)的二乙基醚溶液以逐滴方式添加至该反应溶液,并添加thf(3ml)。然后,在室温下整夜搅拌反应溶液。通过c盐过滤反应混合物,并用thf(2ml)洗涤c盐。在减压下除去挥发物之后,用己烷萃取产物,并通过c盐过滤。用己烷(3ml)洗涤c盐。在减压下再次除去挥发物,并添加戊烷(1.5ml)。将所得物在-35℃下静置整夜。通过过滤收集如此生产的固体,用冷冻的戊烷(1ml)洗涤,并在室温下减压干燥1小时,由此得到(b-349)niph(pet3)(40mg,产率52%)。
1hnmr(500mhz,c6d6)δ7.53(d,j=7.5hz,2h),7.48(t,j=6.3hz,1h),6.93(t,j=7.3hz,1h),6.78(t,j=7.3hz,1h),6.56(t,j=8.0hz,1h),1.28(s,9h),1.25(s,9h),0.89-0.79(m,15h);
31pnmr(202mhz,c6d6)δ48.710(d,j=265hz,1p),13.120(d,j=265hz,1p)
(比较例2-1):配合物(b-399)ni((1,4,5-η)-coe)的合成
除使用配体b-399替代配体b-349以外,以与实施例2-1中相同的方式合成配合物(b-399)ni((1,4,5-η)-coe)。
2-4.丙烯聚合或共聚合
(实施例2-1a):使用实施例2-1的配合物的丙烯聚合
将丙烯(500ml)导入内容积为约2l的感应搅拌式高压釜中。将实施例2-1的配合物((b-349)ni((1,4,5-η)-coe))导入具有氮气的高压釜。在搅拌混合物的情况下,将高压釜升温至50℃。从高压釜温度达到50℃时的时间开始聚合,并进行一段预定时间。在除去未反应的单体之后,打开高压釜,并进行通过加热的干燥,得到聚合物。
(实施例2-2a):使用实施例2-2的配合物的丙烯聚合
除使用实施例2-2的配合物((b-395)ni((1,4,5-η)-coe))代替实施例2-1的配合物((b-349)ni((1,4,5-η)-coe))以外,以与实施例2-1a中相同的方式得到聚合物。
(实施例2-3a):使用实施例2-3的配合物的丙烯聚合
除使用实施例2-3的配合物((b-396)ni((1,4,5-η)-coe))代替实施例2-1的配合物((b-349)ni((1,4,5-η)-coe))以外,以与实施例2-1a中相同的方式得到聚合物。
(实施例2-4a):使用实施例2-4的配合物的丙烯聚合
除使用实施例2-4的配合物((b-395)niphpy)代替实施例2-1的配合物((b-349)ni((1,4,5-η)-coe))以外,以与实施例2-1a中相同的方式得到聚合物。
(实施例2-5a):使用实施例2-5的配合物的丙烯聚合
除使用实施例2-5的配合物((b-349)niph(pet3))代替实施例2-1的配合物((b-349)ni((1,4,5-η)-coe))以外,以与实施例2-1a中相同的方式得到聚合物。
(实施例2-2b至实施例2-2d):使用实施例2-2的配合物的共聚合
除使用实施例2-2的配合物((b-395)ni((1,4,5-η)-coe))代替实施例2-1的配合物((b-349)ni((1,4,5-η)-coe)),并且在实施例2-2的配合物导入具有氮气的高压釜之后,进一步将三乙氧基乙烯基硅烷(实施例2-2b)、10-十一碳烯酸乙酯(实施例2-2c)或3-丁烯-1-醇(实施例2-2d)添加至高压釜以外,以与实施例2-1a中相同的方式得到共聚物。对于共聚物中共聚单体的含量比,通过1hnmr测量测定乙烯:共聚单体的摩尔比,并在表中表示为共聚单体含量mol%。
(实施例2-4e):使用实施例2-4的配合物的共聚合
将50ml不锈钢高压釜用120℃的干燥机干燥3小时,组装,然后在125℃下减压干燥2小时。在将高压釜冷却至室温之后,在氩气气氛中,将实施例2-4的配合物((b-395)niphpy)(5.0μmol,10.0ml,0.50mmol/l甲苯溶液)和甲苯(5ml)添加到高压釜中。然后,添加乙酸烯丙酯。然后,用乙烯(4.0mpa)填充高压釜,并在50℃下搅拌16小时。在将高压釜冷却至室温之后,进行排出剩余的乙烯,并用乙醇(20ml)淬灭反应产物,然后通过过滤收集聚合物。在100℃至120℃下,减压干燥聚合物2小时,得到目标共聚物。对于共聚物中共聚单体的含量比,通过1hnmr测量测定乙烯:共聚单体的摩尔比,并在表中表示为共聚单体含量mol%。
(比较例2-1a):使用比较例2-1的配合物的丙烯聚合
除使用比较例2-1的配合物((b-399)ni((1,4,5-η)-coe))代替实施例2-1的配合物((b-349)ni((1,4,5-η)-coe))以外,以与实施例2-1a中相同的方式得到聚合物。
下表5-1用来比较用于合成实施例2-1至2-5和比较例2-1的配合物的镍原料和配体。
表5-1
对于使用丙烯的聚合或共聚合,下表5-2示出实施例2-1a至2-5a、实施例2-2b至2-2d和比较例2-1a的聚合条件和聚合结果。对于使用乙烯的共聚合,下表5-3示出实施例2-4e的聚合条件和聚合结果。在这些表中,聚合活性表示每摩尔用于聚合的配合物和每小时聚合时间的共聚物产量(g)。在这些表中,作为关于聚合物的gpc测量结果,提及重均分子量mw和分子量分布mw/mn。这些表中的共聚合量表示共聚单体添加量相对于提供用于聚合的单体总量的比例。
表5-2
表5-3
2-5.考虑
从表5-2中的比较例2-1a清楚地是,在使用常规配合物(比较例2-1)的聚丙烯聚合的情况下,聚合活性为4.0×103(g/mol/hr),低,并且如此得到的聚合物的分子量mw为3,200,小。同时,从表5-2中的实施例2-1a至2-5a清楚地是,在使用本公开的金属配合物(实施例2-1至2-5)的聚丙烯聚合的情况下,聚合活性为6.5×103(g/mol/hr)以上,高,并且如此得到的聚合物的分子量mw为4,900以上,大。正如刚才所描述的,与r1为氢的情况(比较例2-1)相比,含有杂原子的取代基用作r1的本公开的金属配合物在聚丙烯聚合中显示出高聚合活性,并且提供具有高分子量的聚丙烯。此外,将如此得到的聚丙烯的分子量分布mw/mn抑制到2.2以下。
此外,从表5-2中的实施例2-2b至2-2d和表5-3中的实施例2-4e清楚地是,通过本公开的金属配合物,以优异的聚合活性实现了α-烯烃与含极性基团的单体的共聚合。
基于上述理由,很清楚的是,本公开的金属配合物提供了相比于以前具有更高分子量和更高聚合活性的α-烯烃均聚物,能够以优异聚合活性实现α-烯烃与含极性基团的单体的共聚合,并且具有优越的技术意义。
<本公开的第三实施方式>
3-1.评价方法
(1)重均分子量mw、数均分子量mn和分子量分布mw/mn:通过下述gpc测量来测定。
首先,将样品(约20mg)收集在用于polymerlaboratoriesltd制造的高温gpc的预处理单元pl-sp260vs用的小瓶中,并向其中添加含有bht作为稳定剂的邻二氯苯(bht的浓度=0.5g/l),以将聚合物浓度调节至0.1质量%。通过在上述用于高温gpc的预处理单元pl-sp260vs中在135℃下加热,溶解聚合物,并用玻璃过滤器过滤以制备样品溶液。在本公开的gpc测量中,玻璃过滤器没有捕获到聚合物。接着,使用由waterscorporation制造的gpcv2000进行gpc测量,所述gpcv2000配备有作为柱的由tosohcorporation制造的tskgelgmh-ht(30cm×4个)和ri检测器。采用下述测量条件:样品溶液的注入量:约520μl;柱温:135℃;溶剂:邻二氯苯;和流量:1.0ml/min。如下进行分子量的计算。即,使用可商购获得的单分散聚苯乙烯作为标准样品,由聚苯乙烯标准样品和乙烯系聚合物的粘度公式制备保留时间对分子量的校准曲线,并基于校准曲线进行分子量的计算。作为粘度公式,使用[η]=k×mα,对于聚苯乙烯,使用k=1.38e-4,α=0.70;和对于乙烯系聚合物,使用k=4.77e-4,α=0.70。对于丙烯系聚合物,使用k=1.03e-4,α=0.78。
3-2.配体的合成
(合成例3-1):配体b-394的合成
根据下述方案合成配体b-394。
在以下提及的化学式中,-omom表示甲氧基甲氧基(-och2och3)。
(1)化合物19的合成
在0℃下,将250ml的氢化钠(7.46g,186.4mmol,纯度60%)在thf中的悬浮溶液添加至2-叔丁基苯酚(化合物18,100.0g,66.6mmol,10.2ml),并在0℃下搅拌它们30分钟。在0℃下,将氯甲基醚(10.7g,133.1mmol,10.1ml)添加至反应混合物,并在15℃下搅拌它们15小时。然后,将氢氧化钾水溶液(2m,200ml)缓慢地添加至反应混合物,并在15℃下搅拌它们30分钟。然后,用醋酸乙酯(100ml×2)萃取反应混合物,用无水硫酸钠干燥并浓缩,由此得到粗产物。通过硅胶柱(石油醚作为洗脱液)纯化粗产物,得到化合物19(8.8g,45.3mmol,产率68.1%)。
(2)化合物20的合成
首先,在0℃下,将正丁基锂(2.5m,10.3ml,25.8mmol)添加至60ml的化合物19(5.0g,25.7mmol)的thf溶液,并在0℃下搅拌它们1小时。然后,在0℃下向其中添加碘(6.5g,25.7mmol,5.2ml),并在15℃下搅拌它们15小时。将冰水(20ml)添加至反应混合物,并用醋酸乙酯(20ml×2)萃取反应混合物。用硫代硫酸钠(20ml)和水(20ml)洗涤有机相,用无水硫酸钠干燥,并浓缩,由此得到化合物20。所述化合物在未纯化的情况下用于后续反应。
(3)化合物55的合成
在氮气气氛中,在0℃下,将40ml的化合物54(20.0g,110.7mmol,21.1ml)的二乙基醚溶液缓慢地添加至110ml的氢化铝锂(4.2g,110.7mmol)在thf中的悬浮溶液。在35℃下搅拌混合物5小时。在0℃下,将thf(20ml)和水(20ml)缓慢地添加至反应混合物,然后在35℃下搅拌它们3小时。通过蒸馏从反应混合物收集所有挥发性物质。然后,经硫酸镁干燥有机相并且过滤。在通过蒸发除去溶剂之后,将剩余物在70mmhg下蒸馏,收集沸点为50℃至55℃的馏分,得到无色透明油状的化合物55(8.2g,55.7mmol,产率50.4%)。
(4)化合物56a的合成
在氮气气氛中,向化合物20(200.0mg,468.5μmol)、化合物55(68.5mg,468.5μmol)、三(二苄叉基丙酮)二钯(42.9mg,46.9μmol)、双[2-(二苯基膦基)苯基]醚(50.5mg,93.7μmol)和叔丁醇钠(90.1mg,937.0μmol)的混合物添加甲苯(5ml)。在100℃下搅拌它们16小时。浓缩反应混合物,并向其中添加水(15ml)。然后,用醋酸乙酯(15ml×2)萃取反应混合物。用盐水(15ml)洗涤有机相,用无水硫酸钠干燥,并浓缩,由此得到粗产物。通过硅胶柱(石油醚作为洗脱液)纯化粗产物,得到化合物56a。
(5)配体b-394的合成
在0℃下,将hcl/醋酸乙酯(4m,40.0ml)添加至20ml的化合物56a(2.5g,7.4mmol)的二氯甲烷溶液。在25℃下搅拌它们2小时。浓缩反应混合物,得到粗产物。用饱和的碳酸氢钠水溶液(30ml),将粗产物的ph调节到6.5至7.0。然后,用二氯甲烷(25ml×3)萃取粗产物。用盐水(25ml)洗涤有机相,用无水硫酸钠干燥并浓缩,由此得到配体b-394(1.6g,5.4mmol,产率73.5%)。
1hnmr(400mhz,cdcl3,δ,ppm):8.21(d,j=12hz,1h),7.41(dt,j=7.6hz,2.8hz,1h),6.81-6.76(m,1h),6.79(t,j=7.6hz,1h),1.40(s,9h),1.23(s,9h),1.20(s,9h);
31pnmr(162mhz,cdcl3,δ,ppm)-6.75(s).
(合成例3-2):配体b-400的合成
根据下述方案合成配体b-400。
(1)化合物62的合成
将n-碘代丁二酰亚胺(6.0g,26.7mmol)添加至化合物61(5.0g,24.2mmol)和对甲苯磺酸(378.5mg,2.4mmol)的二氯甲烷溶液,并在25℃下搅拌它们16小时。用饱和的硫代硫酸钠(30ml)淬灭反应混合物,然后用醋酸乙酯(20ml×3)萃取。用盐水(25ml)洗涤有机相,用无水硫酸钠干燥,并浓缩,由此得到粗产物。通过硅胶柱(石油醚作为洗脱液)纯化粗产物,得到化合物62(8.0g,24.1mmol,产率99.4%)。
(2)化合物63的合成
在0℃下,将氢化钠(1.4g,36.1mmol,纯度60%)添加至20ml的化合物62(8.0g,24.1mmol)的thf溶液。然后,添加氯甲基甲基醚(2.5g,31.3mmol,2.4ml),并在25℃下搅拌它们16小时。通过在0℃下添加饱和的碳酸氢钠水溶液(25ml)淬灭反应混合物,并用醋酸乙酯(15ml×3)萃取。用盐水(10ml)洗涤有机相,用无水硫酸钠干燥,并浓缩,由此得到粗产物。通过硅胶柱(石油醚作为洗脱液)纯化粗产物,得到化合物63(5.2g,13.8mmol,产率57.4%)。
(3)化合物56b的合成
在氮气气氛中,向化合物63(5.2g,13.8mmol)、用于合成配体b-394的化合物55(2.0g,13.8mmol)、三(二苄叉基丙酮)二钯(1.3g,1.4mmol)、双[2-(二苯基膦基)苯基]醚(1.5g,2.8mmol)和叔丁醇钠(2.7g,27.6mmol)的混合物添加甲苯(20ml)。在100℃下搅拌它们16小时。然后,浓缩反应混合物,得到粗产物。通过硅胶柱(石油醚/醋酸乙酯=10/1作为洗脱液)纯化粗产物,然后在石油醚中再结晶,由此得到化合物56b(3.0g,7.6mmol,产率55.0%)。
(4)配体b-400的合成
在0℃下,将hcl/醋酸乙酯(4m,20.0ml)添加至在二氯甲烷(20ml)中的化合物56b(2.8g,7.1mmol)。在25℃下搅拌它们2小时。然后,浓缩反应混合物,得到粗产物。用饱和的碳酸氢钠水溶液(30ml),将粗产物的ph调节到6.5至7.0。粗产物用二氯甲烷(25ml×3)萃取。用盐水(25ml)洗涤有机相,用无水硫酸钠干燥并浓缩,由此得到配体b-400(2.2g,6.3mmol,产率88.4%)。
1hnmr(400mhz,cdcl3,δ,ppm):7.98(d,j=12.4hz,1h),7.34(t,j=2.5hz,1h),7.26-7.21(m,1h),1.32(s,9h),1.23(s,9h),1.14(s,9h),1.11(s,9h);
31pnmr(162mhz,cdcl3,δ,ppm)-5.35(s).
(比较合成例3-1):配体b-399的合成
根据下述方案合成配体b-399。
(1)化合物32的合成
首先,在0℃下,将正丁基锂(2.5m,12.2ml,30.0mmol)添加至30ml的化合物15(4.0g,29.0mmol)的thf溶液,并在0℃下搅拌它们1小时。然后,在-78℃下向其中添加二叔丁基氯化膦(5.2g,29.0g,5.5ml),并在15℃下搅拌它们12小时。将反应溶液倒入冰水(20ml)中,并用醋酸乙酯(20ml×2)萃取。用无水硫酸钠干燥有机相,并浓缩,由此得到粗产物。通过硅胶柱(石油醚:醋酸乙酯=1:0-50:1作为洗脱液)纯化粗产物,得到化合物32(3.5g,9.0g,产率31.2%)。
(2)化合物33d的合成
在氩气气氛中,在-78℃下将bh3·thf(1.0m,16.7ml,16.7mmol)添加至10ml的化合物32(3.9g,13.9mmol)的thf溶液中,并在10℃下搅拌它们1小时。在-78℃下,向其中添加bh3·二甲硫醚(10m,1.7ml,16.7mmol),并在10℃下搅拌它们12小时。在0℃下,将冰水(10ml)添加至该反应溶液,并且在减压下除去挥发物。将水(20ml)添加至反应溶液,并用醋酸乙酯(20ml×3)萃取反应溶液。用无水硫酸钠干燥有机相,并浓缩,由此得到白色固体。用醋酸乙酯(10ml)使白色固体再结晶,得到化合物33d(1.5g,5.1mmol,产率36.4%)。
(3)配体b-399的合成
在氩气气氛中,在0℃下,将hcl/醋酸乙酯(4m,80.0ml,320.0mmol)添加至在二氯甲烷(20ml)中的化合物33d(5.4g,18.2mmol),并在10℃下搅拌它们3小时。在减压下除去挥发物,并添加二氯甲烷(100ml)。用饱和的碳酸氢钠水溶液(100ml)洗涤有机相,并浓缩,由此得到配体b-399(4.0g,16.8mmol,产率92.1%)。
1hnmr(400mhz,cdcl3,δ,ppm):7.85(s,1h),7.57(dt,j=7.6hz,1.4hz,1h),7.28(td,j=7.7hz,1.6hz,1h),6.94(td,j=7.2hz,1.2hz,1h),6.87(td,j=7.5hz,1.2hz,1h),1.32(s,9h),1.29(s,9h);
31pnmr(162mhz,cdcl3,δ,ppm)-6.21(s).
3-3.配合物的合成
(实施例3-1):配合物(b-394)ni((1,4,5-η)-coe)的合成
所有下述操作均在高纯氩气气氛中进行。以下,双-1,5-环辛二烯镍(0)称为ni(cod)2,和(1,4,5-η)-4-环辛烯-1-基配体称为(1,4,5-η)-coe。
首先,将配体b-394(42mg,0.14mmol)称重并放进25ml圆底烧瓶中。接着,称量ni(cod)2(43mg,0.16mmol)并放进另一个烧瓶中,并溶于甲苯(8.0ml)中以制备20mmol/ml的ni(cod)2的甲苯溶液。如此得到的溶液是黄色透明的。将由此得到的ni(cod)2的甲苯溶液(7.1ml)添加到含有配体b-394的圆底烧瓶中以得到溶液。然后,在室温下搅拌它们1小时。此时,已确认溶液的颜色从暗黄色逐渐变成棕色,且没有沉淀。因此,得到20mmol/ml的b-394与ni(cod)2的反应产物((b-394)ni((1,4,5-η)-coe))的溶液。假定b-394和ni(cod)2以1:1的摩尔比反应形成镍配合物,计算反应产物的浓度。
(实施例3-2):配合物(b-400)ni((1,4,5-η)-coe)的合成
除使用配体b-400替代配体b-394以外,以与实施例3-1中相同的方式合成配合物(b-400)ni((1,4,5-η)-coe)。
(实施例3-3):配合物(b-394)ni(4-氟苯基)py的合成
根据下述方案合成配合物(b-394)ni(4-氟苯基)py。
在手套箱中,将配体b-394(100mg,0.34mmol)和氢化钾(27mg,0.68mmol)投入15ml小瓶中。向其中添加二乙基醚(5ml),并在室温下搅拌它们10分钟。通过c盐过滤反应混合物,并用二乙基醚(5ml)洗涤c盐。参考非专利文献"molecules(2014),19(9),13603-13613"合成ni(4-氟苯基)br(tmeda)(tmeda:四甲基乙二胺)。将ni(4-氟苯基)br(tmeda)(126mg,0.36mmol)添加至二乙基醚滤液,并在室温下搅拌它们12小时。通过c盐过滤反应混合物,并用二乙基醚(3ml)洗涤c盐。将吡啶(29mg,0.37mmol)添加至该滤液,并在室温下搅拌它们10小时。然后,除去反应混合物中的溶剂,由此得到固体。将如此得到的固体添加至己烷(20ml),通过c盐过滤混合物,并用己烷(5ml)洗涤c盐。除去如此得到的滤液中的溶剂,得到粗产物。将己烷(1.5ml)添加至粗产物,并将粗产物在-35℃下静置整夜。通过过滤收集如此沉淀的固体,并用冷冻的己烷洗涤。在室温下,将如此得到的黄色固体在减压下干燥2小时,由此得到配合物(b-394)ni(4-氟苯基)py(144mg,80%)。
1hnmr(400mhz,δ,c6d6)8.63(d,j=5.6hz,2h),7.68(t,j=7.0hz,2h),7.34-7.31(m,2h),6.78(t,j=9.0hz,2h),6.66(t,j=7.4hz,1h),6.58(td,j=7.6,2.0hz,1h),6.36(t,j=7.0hz,2h),1.41(d,j=4.0hz,18h),1.38(s,9h);
31pnmr(162mhz,δ,c6d6)60.3;
19fnmr(376mhz,δ,c6d6)-124.0;
13cnmr(101mhz,δ,c6d6)175.54(d,j=17hz,1c),161.58(dd,j=240,1.3hz,1c),150.35(s,2c),144.43(dd,j=37,3.2hz,1c),139.24(d,j=4.9hz,2c),138.47(d,j=7.4hz,1c),136.52(s,1c),131.93(d,j=1.1hz,1c),129.11(d,j=1.7hz,1c),123.37(s,2c),118.02(d,j=41hz,1c),113.14(dd,j=18,2.2hz,2c),112.71(d,j=6.6hz,1c),36.33(d,j=18hz,2c),34.97(d,j=1.4hz,1c),30.17(d,j=4.1hz,6c),29.65(s,3c).
元素分析,对于c29h39fnniop的计算值;c,66.18;h,7.47;n,2.66;求得c,66.19;h,7.73;n,2.54.
(比较例3-1):配合物(b-399)ni((1,4,5-η)-coe)的合成
除使用配体b-399替代配体b-394以外,以与实施例3-1中相同的方式合成配合物(b-399)ni((1,4,5-η)-coe)。
3-4.丙烯聚合或共聚合
(实施例3-1a):使用实施例3-1的配合物的丙烯聚合
将丙烯(500ml)导入内容积为约2l的感应搅拌式高压釜中。将实施例3-1的配合物((b-394)ni((1,4,5-η)-coe))导入具有氮气的高压釜。在搅拌混合物的情况下,将高压釜升温至50℃。从高压釜温度达到50℃时的时间开始聚合,并进行一段预定时间。在除去未反应的单体之后,打开高压釜,并进行通过加热的干燥,得到聚合物。
(实施例3-2a):使用实施例3-2的配合物的丙烯聚合
除使用实施例3-2的配合物((b-400)ni((1,4,5-η)-coe))代替实施例3-1的配合物((b-394)ni((1,4,5-η)-coe))以外,以与实施例3-1a中相同的方式得到聚合物。
(实施例3-3a):使用实施例3-3的配合物的丙烯聚合
除使用实施例3-3的配合物((b-394)ni(4-氟苯基)py)代替实施例3-1的配合物((b-394)ni((1,4,5-η)-coe))以外,以与实施例3-1a中相同的方式得到聚合物。
(实施例3-1b):使用实施例3-1的配合物的共聚合
除在将实施例3-1的配合物导入具有氮气的高压釜之后,将3-丁烯-1-醇进一步添加至高压釜以外,以与实施例3-1a中相同的方式得到共聚物。对于共聚物中共聚单体的含量比,通过1hnmr测量测定丙烯:共聚单体的摩尔比,并在表中表示为共聚单体含量mol%。
(实施例3-2c):使用实施例3-2的配合物的共聚合
除使用实施例3-2的配合物((b-400)ni((1,4,5-η)-coe))代替实施例3-1的配合物((b-394)ni((1,4,5-η)-coe))且在将实施例3-2的配合物导入具有氮气的高压釜之后进一步添加10-十一碳烯酸乙酯以外,以与实施例3-1a中相同的方式得到共聚物。对于共聚物中共聚单体的含量比,通过1hnmr测量测定丙烯:共聚单体的摩尔比,并在表中表示为共聚单体含量mol%。
(实施例3-3d):使用实施例3-3的配合物的共聚合
将50ml不锈钢高压釜用120℃的干燥机干燥3小时,组装,然后在125℃下减压干燥2小时。在将高压釜冷却至室温之后,在氩气气氛中,将实施例3-3的配合物((b-394)ni(4-氟苯基)py)(10.0μmol,10.0ml,1.00mmol/l甲苯溶液)和甲苯(10ml)添加到高压釜中。然后,添加丙烯(10g)和丙烯酸甲酯。然后,将高压釜的温度调节到50℃,并搅拌内容物64小时。在将高压釜冷却至室温之后,进行排出剩余的丙烯,并用乙醇(20ml)淬灭反应产物,然后通过过滤收集聚合物。在100℃至120℃下,减压干燥聚合物2小时,得到目标共聚物。对于共聚物中共聚单体的含量比,通过1hnmr测量测定丙烯:共聚单体的摩尔比,并在表中表示为共聚单体含量mol%。
(比较例3-1a):使用比较例3-1的配合物的丙烯聚合
除使用比较例3-1的配合物((b-399)ni((1,4,5-η)-coe))代替实施例3-1的配合物((b-394)ni((1,4,5-η)-coe))以外,以与实施例3-1a中相同的方式得到聚合物。
下表6-1用来比较用于合成实施例3-1至3-3和比较例3-1的配合物的镍原料和配体。
表6-1
对于使用丙烯的聚合或共聚合,下表6-2示出实施例3-1a至3-3a、实施例3-1b、实施例3-2c、实施例3-3d和比较例3-1a的聚合条件和聚合结果。在表6-2中,聚合活性表示每1摩尔用于聚合的配合物和每1小时聚合时间的共聚物产量(g)。在表6-2中,作为关于聚合物的gpc测量结果,提及重均分子量mw和分子量分布mw/mn。表6-2中的共聚合量表示共聚单体添加量相对于提供用于聚合的单体总量的比例。
表6-2
3-5.考虑
从表6-2中的比较例3-1a清楚地是,在使用常规配合物(比较例3-1)的聚丙烯聚合的情况下,聚合活性为4.0×103(g/mol/hr),低,并且如此得到的聚合物的分子量mw为3,200,小。同时,从表6-2中的实施例3-1a至3-3a清楚地是,在使用本公开的金属配合物(实施例3-1至3-3)的聚丙烯聚合的情况下,聚合活性为1.1×105(g/mol/hr)以上,高,并且如此得到的聚合物的分子量mw为15,900以上,大。正如刚才所描述的,与r1为氢的情况(比较例3-1)相比,烃基用作r1的本公开的金属配合物在聚丙烯聚合中显示出高聚合活性,并且提供具有高分子量的聚丙烯。此外,将如此得到的聚丙烯的分子量分布mw/mn抑制到2.3以下。
此外,从表6-2中的实施例3-1b、实施例3-2c和实施例3-3d清楚地是,通过本公开的金属配合物,以优异的聚合活性实现了α-烯烃与含极性基团的单体的共聚合。
基于上述理由,很清楚的是,本公开的金属配合物提供了相比于以前具有更高分子量和更高聚合活性的α-烯烃均聚物,能够以优异聚合活性实现α-烯烃与含极性基团的单体的共聚合,并且具有优越的技术意义。
产业上的可利用性
通过使用本公开的金属配合物,能够生产新型功能性聚烯烃。因此,本公开的金属配合物对于用途、特别是需要粘合和良好设计的用途,在工业上是非常有用的。
- 还没有人留言评论。精彩留言会获得点赞!