一种稀土有机框架晶体材料、其制备方法及应用与流程
本申请涉及一种稀土有机框架晶体材料、其制备方法及在Fe3+检测、CO2/CH4的吸附/分离方面的应用,属于晶体材料领域。
背景技术:
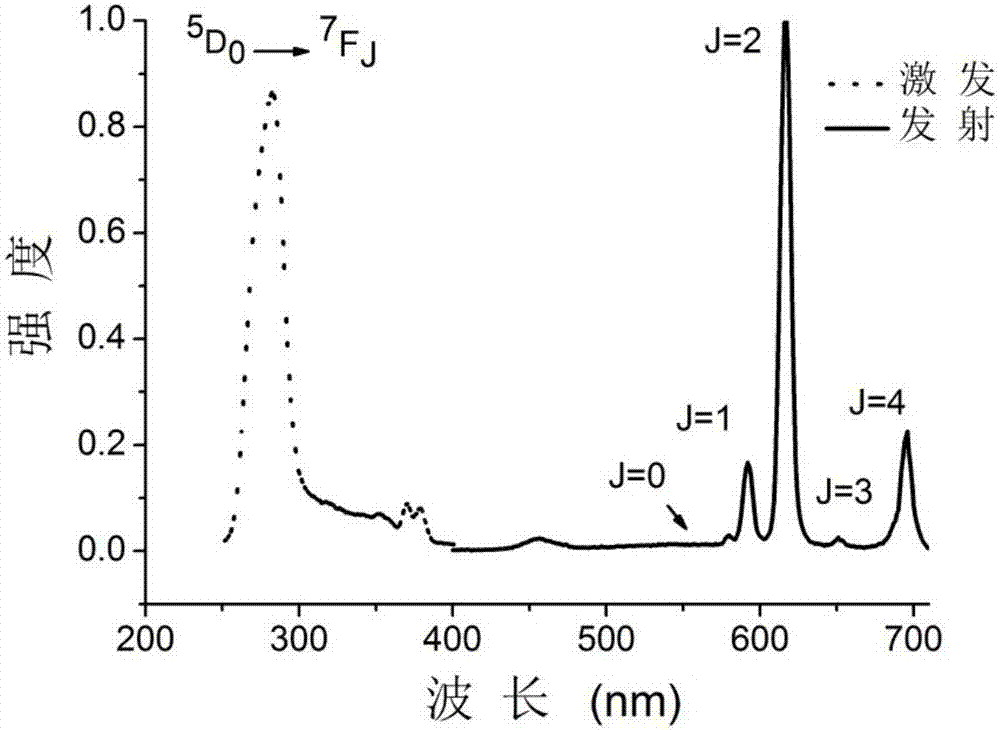
:金属-有机框架材料(metal-organicframeworks,MOFs)是一种由金属离子或金属簇与有机桥联配体通过配位作用组装形成的新型多孔晶体材料。金属-有机框架材料具有特殊的拓扑结构、内部排列的规则性以及特定尺寸和形状的孔道,但框架材料表现出更大的结构可变、可调特性以及更为丰富的物理化学性质。把具有光学活性的无机金属离子或含有共轭基元的有机配体想结合,形成的金属有机配位聚合物或金属有机框架材料,在引入有机分子的灵活性的同时,能够极大地提高荧光材料的发光性能和稳定性能,是一种新型的无机有机杂化材料。稀土-有机框架材料(lanthanidemetal-organicframeworks)结合了稀土离子优异的发光性能以及金属-有机框架材料发光形式多样以及发光可调控的优势,在荧光探测、发光与显示和生物医学成像等领域都具有极大的应用价值。稀土离子相似的配位性能可以使不同的稀土离子共掺杂到同一稀土-有机框架材料中,形成掺杂的稀土-有机框架。这类材料可以拥有不同稀土离子的发光,并能够通过调节组分的比例来调节其发光颜色。因此,新型的稀土-有机框架晶体材料的开发对于丰富金属-有机框架材料的种类和荧光晶体材料的种类有重要的意义。技术实现要素:根据本申请的一个方面,提供了一种新型稀土有机框架晶体材料,该晶体材料具有好的热稳定性、空气稳定性、酸碱稳定性以及溶剂稳定性,属于多功能晶体材料,可以在Fe2+和Fe3+混合溶液中检测Fe3+的浓度,在CH4和CO2中选择性吸附CO2。所述稀土有机框架晶体材料,其化学式如式I所示:[LnL(H2O)2]·H2O式I;式I中,Ln代表稀土元素,所述稀土元素选自Gd、Eu、Tb、Dy中的至少一种;L代表由1-(4-苯甲酸)-1氢-吡唑-3,5-二羧酸形成的有机配体;所述晶体属于单斜晶系,空间群为P-1,晶胞参数为α=106.91°~112.77°,β=93.10°~94.72°,γ=108.27°~108.88°,Z=2。所述1-(4-苯甲酸)-1氢-吡唑-3,5-二羧酸的结构式如式II:所述晶体材料的结构如附图1所示,于P-1空间群,晶胞内存在一种配位环境的稀土离子,为九配位,分别同两个螯合的羧酸氧原子,五个侨联的羧酸氧原子,以及两个水分子中的两个氧原子配位。两个稀土离子通过配体侨联而成二核的稀土羧酸簇。相邻的两个稀土簇通过两个羧酸基团连接形成一条稀土羧酸链[Ln2(μ2-COO)2]n。每个二核稀土簇与八个相邻的二核稀土簇连接形成三维框架结构;该框架结构沿b轴方向有窗口大小约为的一维孔道。作为一种实施方式,所述Ln代表Gd时,稀土有机框架晶体材料的化学式如式I-1所示:[GdL(H2O)2]·H2O式I-1;所述晶体属于单斜晶系,空间群为P-1,晶胞参数为α=108.511(7)°,β=93.793(6)°,γ=108.350(6)°,Z=2。作为一种实施方式,所述Ln代表Eu时,稀土有机框架晶体材料的化学式如式I-2所示:[EuL(H2O)2]·H2O式I-2;所述晶体属于单斜晶系,空间群为P-1,晶胞参数为α=112.766(6)°,β=94.716(5)°,γ=108.877(5)°,Z=2。作为一种实施方式,所述Ln代表Tb时,稀土有机框架晶体材料的化学式如式I-3所示:[TbL(H2O)2]·H2O式I-3;所述晶体属于单斜晶系,空间群为P-1,晶胞参数为α=106.914(7)°,β=93.967(6)°,γ=108.270(6)°,Z=2。作为一种实施方式,所述Ln代表Dy时,稀土有机框架晶体材料的化学式如式I-4所示:[DyL(H2O)2]·H2O式I-4;所述晶体属于单斜晶系,空间群为P-1,晶胞参数为α=111.502(6)°,β=93.109(5)°,γ=108.541(5)°,Z=2。作为一种实施方式,当所述Ln代表Eu时,所述稀土有机框架晶体材料在紫外光激发下,在579~581nm、591~593nm、616~618nm、652~654nm和698~700nm处存在发射峰。优选地,当所述Ln代表Eu时,所述稀土有机框架晶体材料在紫外光激发下,发射光谱在580nm、592nm、617nm、653nm和699nm处存在发射峰。作为一种实施方式,当所述Ln代表Tb时,所述稀土有机框架晶体材料在紫外光激发下,在490~492nm、542~544nm、585~587nm、652~654nm和695~697nm处存在发射峰。优选地,当所述Ln代表Tb时,所述稀土有机框架晶体材料在紫外光激发下,在491nm、543nm、586nm、653nm和696nm存在发射峰。作为一种实施方式,当所述Ln代表Dy时,所述稀土有机框架晶体材料在紫外光激发下,在479~481nm、572~574nm、659~661nm和749~751nm处存在发射峰。优选地,当所述Ln代表Dy时,所述稀土有机框架晶体材料在紫外光激发下,在480nm、573nm、660nm和750nm存在发射峰。在400~500nm左右的激发波长区域,[TbL(H2O)2]·H2O未显示出配体的发射峰,[EuL(H2O)2]·H2O显示了微小的配体发射峰,说明该配体可以很好的敏化Eu离子和Tb离子的稀土发光。可选地,所述稀土有机框架晶体材料对Fe3+具有选择性荧光淬灭响应。优选地,所述稀土有机框架晶体材料对Fe3+的荧光淬灭常数Ksv为1.9×103L/mol。可选地,所述稀土有机框架晶体材料对CO2具有选择性吸附响应。优选地,所述稀土有机框架晶体材料的分解温度≥440℃。优选地,所述稀土有机框架晶体材料在平均湿度为55%的空气中稳定寿命≥1个月。优选地,所述稀土有机框架晶体材料在水中稳定寿命≥1个月。优选地,所述稀土有机框架晶体材料在pH=2和pH=12的环境中稳定寿命≥48小时。根据本申请的另一个方面,提供了上述任一稀土有机框架晶体材料的制备方法,该方法制备方法简单,所得产物的产率和纯度高,适合大规模工业化生产。所述稀土有机框架晶体材料的制备方法,其特征在于,至少包括以下步骤:将含有1-(4-苯甲酸)-1氢-吡唑-3,5-二羧酸和稀土离子的溶液I置于110~150℃下,水热晶化不少于12小时,经分离、干燥后,即得所述稀土有机框架晶体材料。优选地,水热晶化温度为120~140℃,水热晶化时间为1~7天。优选地,所述溶液I中1-(4-苯甲酸)-1氢-吡唑-3,5-二羧酸与稀土离子的摩尔比为1~2:1。进一步优选地,所述溶液I中1-(4-苯甲酸)-1氢-吡唑-3,5-二羧酸与稀土离子的摩尔比为1:1。可选地,所述溶液I中稀土元素的摩尔浓度为0.1~0.5mol/L。可选地,所述稀土离子盐选自硝酸钆、硝酸铕、硝酸铽、硝酸镝中的至少一种。根据本申请的又一个方面,提供了所述的稀土有机框架晶体材料、根据所述制备方法制备得到的稀土有机框架晶体材料中的至少一种在定性和/或定量检测Fe3+中的应用。根据本申请的又一个方面,提供了一种定性和/或定量检测Fe3+的方法,其特征在于,包括如下步骤:a)将稀土有机框架晶体材料与待测液I混合,得到混合物A;b)对混合物A进行荧光检测;c)根据步骤b)中荧光检测结果得到荧光淬灭结果;d)根据是否存在荧光淬灭得到待测液I中是否存在Fe3+的定性检测结果;根据荧光淬灭的程度得到待测液I中Fe3+的定量或半定量检测结果;步骤a)中稀土有机框架晶体材料选自所述稀土有机框架晶体材料、根据所述制备方法制备得到的稀土有机框架晶体材料中的至少一种。所述定性和/或定量检测Fe3+的方法可用于含Fe2+和/或Fe3+的待测样品中Fe3+的定性和/或定量检测。根据本申请的又一个方面,提供了一种定量检测Fe3+的方法,其特征在于,包括如下步骤:a)将所述的稀土有机框架晶体材料与待测液II混合,得到混合物B;b)对混合物B进行荧光检测;c)根据步骤b)中荧光检测结果得到荧光淬灭结果;d)根据是否存在荧光淬灭得到待测液II中Fe3+的定量检测结果;所述待测液II中Fe3+浓度为0.1~0.8mmol/L;步骤a)中稀土有机框架晶体材料选自所述稀土有机框架晶体材料、根据所述制备方法制备得到的稀土有机框架晶体材料中的至少一种。所述定量检测Fe3+的方法可用于含Fe2+和/或Fe3+的待测样品中Fe3+的定量检测。根据本申请的再一个方面,所述的稀土有机框架晶体材料、根据所述制备方法制备得到的稀土有机框架晶体材料中的至少一种在吸附/分离CO2/CH4中的应用。所述应用基于所述稀土有机框架晶体材料对CO2和CH4不同的吸附选择性来实现。本申请能产生的有益效果包括:1)本申请所提供的晶体材料,是一种新型的稀土有机框架化合物,具有很高的热稳定性、空气稳定性、酸碱稳定性以及溶剂稳定性。2)本申请所提供的晶体材料,是一种新型的荧光晶体材料,在紫外光的激发下具有特征发射,具有较好的灵敏度和响应速度。3)本申请所提供的晶体材料,是一种多功能材料,可用于Fe3+的定性检测和定量检测,同时也可用于CO2/CH4的吸附/分离,效果显著。4)本申请所提供的晶体材料的制备方法,所述制备方法简单,所得产物的产率和纯度高,适合大规模工业化生产。附图说明图1为本申请所述稀土有机框架晶体材料从b轴方向的晶体结构示意图。图2为室温下样品EuL的荧光发射光谱。图3为室温下样品TbL的荧光发射光谱。图4为室温下样品DyL的荧发射光谱。图5为样品GdL的热重分析结果。图6为样品EuL的热重分析结果。图7为样品TbL的热重分析结果。图8为样品DyL的热重分析结果。图9为样品GdL的结构热稳定性测试结果。图10为样品GdL的结构空气稳定性测试结果。图11为样品GdL的结构水稳定性测试结果。图12为样品GdL的结构pH稳定性测试结果。图13为样品TbL对不同金属离子的悬浊液荧光对比图。图14为样品TbL对混合体系中Fe3+的荧光强度对比分析矢量图。图15为样品TbL对混合体系中Fe3+的紫外灯下荧光强度对比图。图16为样品TbL在295K下的CO2/CH4吸附脱附曲线。图17为样品TbL的CO2吸附焓曲线。图18为样品TbL在295K下的CO2/CH4选择性分析曲线。具体实施方式下面结合实施例详述本申请,但本申请并不局限于这些实施例。如无特别说明,本申请的实施例中的原料均通过商业途径购买,其中有机配体购自济南恒化试剂公司。本申请的实施例中分析方法如下:晶体结构测定采用Supernova型X-射线单晶衍射仪,使用微焦斑CuKα光源采用ω角扫描模式;荧光分析采用Horiba公司的Fluorolog-3型仪器;粉末衍射采用Rigaku公司MiniFlex600粉末衍射仪,使用CuKα辐射源热重分析采用Netzsch公司的STA449C的热分析仪;紫外可见吸收光谱采用Lambda365;荧光寿命及量子产率采用EdinburghAnalyticalInstrumentsFLS980;气体吸附采用ASAP2020吸附分析仪。实施例1样品GdL的制备将有机配体1-(4-苯甲酸)-1氢-吡唑-3,5-二羧酸、硝酸钆依照摩尔比1:1溶于CH3CN和水的混合溶剂(体积比CH3CN:水=1:1)中,得到溶液;硝酸钆在溶液中的浓度为0.1mol/L。将上述溶液放入密闭的水热釜中,在130℃温度下保持5天后,所得固体经离心分离、真空干燥后,即得所述稀土有机框架晶体材料,记为样品GdL。实施例2样品EuL的制备将有机配体1-(4-苯甲酸)-1氢-吡唑-3,5-二羧酸、硝酸铕依照摩尔比1:1溶于CH3CN和水的混合溶剂(体积比CH3CN:水=1:1)中,得到溶液;硝酸钆在溶液中的浓度为0.5mol/L。将上述溶液放入密闭的水热釜中,在150℃温度下保持1天后,所得固体经离心分离、真空干燥后,即得所述稀土有机框架晶体材料,记为样品EuL。实施例3样品TbL的制备将有机配体1-(4-苯甲酸)-1氢-吡唑-3,5-二羧酸、硝酸铽依照摩尔比1:1溶于CH3CN和水的混合溶剂(体积比CH3CN:水=1:1)中,得到溶液;硝酸钆在溶液中的浓度为0.3mol/L。将上述溶液放入密闭的水热釜中,在140℃温度下保持3天后,所得固体经离心分离、真空干燥后,即得所述稀土有机框架晶体材料,记为样品TbL。实施例4样品DyL的制备将有机配体1-(4-苯甲酸)-1氢-吡唑-3,5-二羧酸、硝酸镝依照摩尔比1:1溶于CH3CN和水的混合溶剂(体积比CH3CN:水=1:1)中,得到溶液;硝酸钆在溶液中的浓度为0.2mol/L。将上述溶液放入密闭的水热釜中,在120℃温度下保持7天后,所得固体经离心分离、真空干燥后,即得所述稀土有机框架晶体材料,记为样品DyL。实施例5样品的结构分析对样品GdL、EuL、TbL及DyL分别进行了X-射线粉末衍射测试、X-射线单晶结构测试。样品GdL、EuL、TbL及DyL的晶体结构测试结果如表1所示,样品GdL、EuL、TbL及DyL的键长键角数据如表2~7所示。表1.样品EuL,GdL,TbL,DyL晶体结构数据表2.样品GdL的键长表表3.样品GdL的键角表表4.样品TbL的键长表Tb1—O12.336(7)C6—C71.515(16)Tb1—O1i2.702(7)C5—C41.505(16)Tb1—O5ii2.427(7)C5—O31.254(12)Tb1—O4iii2.364(7)N2—N11.346(12)Tb1—O2i2.449(8)N2—C21.358(13)Tb1—O6ii2.474(8)N1—C41.367(14)Tb1—O72.476(8)C3—C21.365(15)Tb1—O82.430(8)C3—C41.373(15)Tb1—C1i2.933(10)C1—C21.492(14)Tb1—C11ii2.823(11)C11—C101.505(15)Tb1—O3iv2.252(6)C10—C121.394(16)O1—C11.267(12)C10—C91.372(17)O5—C111.254(13)C7—C131.392(17)O4—C51.241(13)C7—C81.382(17)O2—C11.257(12)C13—C121.375(18)O6—C111.283(13)C9—C81.391(17)C6—N11.475(14)表5.样品TbL的键角表表6.样品DyL的键长表表7.样品DyL的键角表晶体结构测试结果显示,样品GdL、EuL、TbL及DyL晶体结构类似,属于单斜晶系,空间群为P-1,晶胞参数为α=106.91°~112.77°,β=93.10°~94.72°,γ=108.27°~108.88°,Z=2。从b轴方向的晶体结构示意图如附图1所示,晶胞内存在一种配位环境的稀土Ln离子,为九配位,分别同两个螯合的羧酸氧原子,五个侨联的羧酸氧原子,以及两个水分子中的两个氧原子配位。两个稀土Gd离子通过配体侨联而成二核的稀土羧酸簇。相邻的两个稀土簇通过两个羧酸基团连接形成一条稀土羧酸链[Gd2(μ2-COO)2]n。每个二核稀土簇与八个相邻的二核稀土簇连接形成三维框架结构;该框架结构沿b轴方向有窗口大小约为的一维孔道。实施例6样品的荧光测试对样品GdL、EuL、TbL及DyL分别进行了荧光测试,结果如下:在283nm的紫外光激发光下,样品EuL显示了580nm、592nm、617nm、653nm和699nm的Eu特征发光,其荧光发射图如附图2所示)。在283nm的紫外激发光下,样品TbL显示了491nm、543nm、586nm、653nm和696nm的Tb特征发光,其荧光发射图如附图3所示)。在283nm的紫外激发光下,样品DyL显示了480nm、573nm、660nm和750nm的Dy特征发光,其荧光发射图如附图4所示)。在400-500nm左右的区域样品TbL未显示出配体的发射峰,样品EuL显示微小的配体发射峰,说明由1-(4-苯甲酸)-1氢-吡唑-3,5-二羧酸形成的有机配体可以很好的敏化铕离子和铽离子的稀土发光。实施例7样品结构的热稳定性测试对GdL、EuL、TbL及DyL进行了热重分析,结果显示,样品GdL、EuL、TbL及DyL的分解温度均在440℃以上,其热重检测结果分别如附图5、6、7和8所示。对样品GdL、EuL、TbL及DyL进行了变温XRD分析,结果显示,晶体材料骨架在180℃还可以可保持稳。典型代表如样品GdL,其不同温度下XRD谱图与根据单晶结构拟合得到的理论谱图的比较如附图9所示。说明本申请所提供的稀土有机框架晶体材料具有很高的热稳定性。实施例8样品结构的空气稳定性测试对样品GdL、EuL、TbL及DyL分别进行了空气稳定性测试,具体步骤为:将样品分别暴露在潮湿的空气中(平均湿度约为55%)7天、15天、30天后分别记录其X-射线粉末衍射谱图,并与最初的粉末衍射谱图及单晶拟合的粉末衍射图对比来确定其结构稳定性。结果显示,样品GdL、EuL、TbL及DyL存放30天后的XRD谱图没有太大变化(以样品GdL为典型代表,其XRD谱图随时间变化如附图10所示),所述稀土有机框架晶体材料可长期稳定存在于空气中。实施例9样品结构的水稳定性测试对样品GdL、EuL、TbL及DyL分别进行了水稳定性测试,具体步骤为:将20mg样品分别置于10mL的水中3天、7天、15天、30天后经过滤,洗涤,干燥处理后,分别记录其X-射线粉末衍射谱图,并与最初的粉末衍射谱图及单晶拟合的粉末衍射图对比来确定其结构稳定性。结果显示,样品GdL、EuL、TbL及DyL在水中存放30天后的XRD谱图没有太大变化(以样品GdL为典型代表,其XRD谱图随时间变化如附图11所示),所述稀土有机框架晶体材料骨架在水中可以稳定存在一个月以上。实施例10样品结构的酸碱稳定性测试对样品GdL、EuL、TbL及DyL分别进行了酸碱稳定性测试,具体步骤为:将20mg样品分别置于10mLpH分别为1、2、3、5、7、9、11、12、13的溶液中(溶液由氢氧化钠和盐酸溶液调配),搅拌48小时,经过滤,洗涤,干燥处理后,分别测试其X-射线粉末衍射谱图,并与最初的粉末衍射谱图及单晶拟合的粉末衍射图对比来确定其结构稳定性。结果显示,样品GdL、EuL、TbL及DyL在pH=2-12的体系中,存放48h后的XRD谱图没有太大变化(以样品GdL为典型代表,其XRD谱图随pH变化如附图12所示),所述稀土有机框架晶体材料具有很高的酸碱稳定性。实施例11样品对Fe3+的选择性荧光猝灭分别将该40mg样品GdL、EuL、TbL及DyL浸渍于4mL水中超声30分钟制成分散良好的悬浊液,当加入1mL浓度为5mmol/L的金属盐溶液[Ba(NO3)2、Sr(NO3)2、NaNO3、KNO3、Mg(NO3)2、CsNO3、Mn(NO3)2、Ni(NO3)2、Co(NO3)2、Fe(NO3)2、Cu(NO3)2、Fe(NO3)3],进行荧光测试。结果显示,GdL、EuL、TbL及DyL均对Fe3+有选择性响应。以样品TbL为典型代表,荧光测试结果如附图13所示,可以发现悬浊液的荧光对Fe3+有选择性响应,猝灭常数Ksv为1.9×103L/mol。实施例12样品用于检测H2O2氧化Fe2+反应进度的模拟实验考虑到材料的荧光对Fe3+的有明显的猝灭响应,而对Fe2+没有响应,该材料可以应用于检测Fe3+/Fe2+混合体系中Fe3+的浓度,这在生物上和工业上都有重要意义。我们模拟了一个实验来考察材料在工业上检测H2O2氧化Fe2+反应进度的应用。分别将40mg样品GdL、EuL、TbL及DyL分别溶于不同Fe3+的浓度的Fe3+/Fe2+混合体系中(该体系中Fe3+和Fe2+的总浓度为1mmol/L)。结果显示,随着Fe3+浓度不断增大,荧光发光逐步猝灭。以样品TbL为典型代表,其结果如图14和15所示。从附图15中可以看出,随着Fe3+浓度不断增大,荧光发光逐步猝灭。我们拟合了在混合体系中Fe3+浓度和荧光强度之间的关系,发现两者在Fe3+浓度为0.1-0.8mmol/L时呈现良好的线性关系(附图14),因此该材料可以在这个范围内定量的检测Fe3+/Fe2+混合体系中Fe3+的浓度。实施例13样品用于CO2/CH4的吸附/分离的测试将样品GdL、EuL、TbL及DyL分别活化后,进行了CH4和CO2的气体吸附实验。活化方法为:将样品置于真空环境下(<10μmHg),加热至150℃,保持10h。实验结果显示晶体材料对CH4和CO2吸附曲线表现出Ⅰ类吸附行为,说明了该类晶体材料是典型的微孔材料。以样品TbL为典型代表,其结果如附图16所示,在273K和295K的条件下,材料对CO2的最大吸附量分别为38.21cm3g-1和33.10cm3g-1,远远大于其CH4的吸附量(273K下10.13cm3g-1和295K下7.61cm3g-1)。以上吸附量的显著差异鼓励我们对二元体系中材料对CO2/CH4的选择性分离性能进行了研究。基于实验吸附数据,引入理想吸附溶液理论(IAST),我们得到了样品TbL对CO2/CH4选择性曲线图,如附图18。CO2/CH4(15:85)的选择性系数在低压下很大,随着负载量的增加,其数值迅速降低,压力位10Kpa后,选择性缓慢降低,最低选择性系数仍在80以上,显示了该材料具有良好的CO2和CH4选择能力。以上所述,仅是本申请的几个实施例,并非对本申请做任何形式的限制,虽然本申请以较佳实施例揭示如上,然而并非用以限制本申请,任何熟悉本专业的技术人员,在不脱离本申请技术方案的范围内,利用上述揭示的技术内容做出些许的变动或修饰均等同于等效实施案例,均属于技术方案范围内。当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1