一种杀螟丹中间体的合成工艺的制作方法
本发明涉及一种杀螟丹中间体的合成工艺,属于杂环化合物技术领域。
背景技术:
杀螟丹是沙参毒素类杀虫剂,具有杀虫谱广,杀虫效果好等优点,能够有效防治半翅目,双翅目等多种害虫和线虫。目前,杀螟丹的合成方法主要有两种:
其一是氰化钠路线,先得到关键中间体2-二甲氨基-1,3-二硫氰基丙烷,然后对其进行水解反应得到杀螟丹,具体路线如式(1)所示。
该路线由于使用了剧毒氰化钠,产生剧毒的含氰废水,其废水的处理成本高,使该合成方法的绿色性差和成本较高。
其二是硫氰酸盐路线,通过1-二甲氨基-2,3-二氯丙烷与硫氰酸盐(如NaSCN)进行亲核取代反应,该反应容易得到正构体2-二甲氨基-1,3-二硫氰基丙烷(正构体)和异构体1-二甲氨基-2,3-二硫氰基丙烷(异构体)的混合物,异构体转化所得的产物没有生物活性,具体路线如式(2)所示。
上述路线中,硫氰酸盐路线产生不需要的异构体即导致产物的产率降;虽然该无效异构体能够通过结晶分离,循环参与反应,可部分转化为正构体至正构体和异构体达到动态平衡,但是增加了操作步骤,降低了合成效率。
基于此,做出本申请。
技术实现要素:
针对现有合成工艺路线所存在的上述缺陷,本申请提供一种绿色环保、合成效率高的杀螟丹合成中间体的制备方法。
为实现上述目的,本申请采取的技术方案如下:
一种杀螟丹中间体的合成工艺,包括如下步骤:
(1)有机溶剂中,1,3-二氯丙酮与硫氰酸盐在一定温度下反应,反应结束后加入水和乙酸乙酯,分层,水相用乙酸乙酯萃取,有机相合并后减压浓缩得到结构式为的1,3-二硫氰基-2-丙酮粗产品;
(2)在高压反应釜中,依次加入有机溶剂,步骤(1)所得1,3-二硫氰基丙酮粗产品、二甲胺水溶液和催化剂,并通入一定压力的氢气进行催化氢化反应。反应结束后,将反应混合液过滤回收催化剂,滤液加入水和乙酸乙酯,分层,水相用乙酸乙酯萃取,有机相用饱和食盐水洗涤后用无水硫酸钠干燥,经减压浓缩得到结构式为的2-二甲氨基-1,3-二硫氰基丙烷粗产品,粗产品经重结晶得到高纯度的2-二甲氨基-1,3-二硫氰基丙烷。
上述过程的反应式如式(3)所示。
,式中,X=Br,Cl。
进一步的作为优选:
步骤(1)中,所述的有机溶剂为非质子性溶剂,更为优选的,所述的有机溶剂为N,N-二甲基甲酰胺(DMF)、二甲亚砜(DMSO)、乙腈(CH3CN)、四氢呋喃(THF)中的任一种。
步骤(1)中,所述的1,3-二氯丙酮为1,3-二氯丙酮或1,3-二溴丙酮。
步骤(1)中,所述的硫氰酸盐为硫氰酸钠(NaSCN)、硫氰酸钾(KSCN)或硫氰酸铵(NH4SCN);反应过程中控制-SCN过量,1,3-二氯丙酮:-SCN的摩尔比为1:2-5,更优选的,1,3-二氯丙酮:-SCN的摩尔比为1:3。反应过程中硫氰酸盐过量,既可以确保反应的正向进行,同时有保证了1,3-二氯丙酮反应充分,并将其主链完全引入到中间体的成品中,有利于提高原料利用率和成品合成率。
步骤(1)中,所述反应温度为室温至80℃。更优选的,所述的反应温度为室温到50℃。
步骤(2)中,所述的极性有机溶剂为THF、甲醇、乙醇或甲苯。
步骤(2)中,所述的催化剂为Pd/C,Ru/C。
步骤(2)中,所述的氢气的压力为0.1MPa~5Mpa。
步骤(2)中,所述的二甲胺为质量百分含量为40%的二甲胺水溶液;二甲胺水溶液会发生可逆反应,二甲胺过量,才能确保反应的正向快速进行,减少并最大程度避免副产物的生产,从而提高中间体2-二甲氨基-1,3-二硫氰基丙烷的纯度。
步骤(2)中,所述重结晶所用的溶剂为乙酸乙酯和石油醚。
上述制备方法具体过程如下:
(1)称取一定量的1,3-二氯丙酮和NaSCN于圆底烧瓶中,加入一定量的极性溶剂。反应混合液在一定温度下搅拌至1,3-二氯丙酮反应完全,向反应液加入水和乙酸乙酯,分层后取有机相,水相用乙酸乙酯萃取两次。合并有机相并饱和NaCl水溶液洗涤3次,无水Na2SO4干燥,减压浓缩,得到高纯度的1,3-二硫氰基丙酮。
(2)称取一定量的反应溶剂、1,3-二硫氰基丙酮、二甲胺、催化剂于高压反应釜中,冲入一定压力的氢气,在一定的温度下反应一定时间至1,3-二硫氰基丙酮反应完全。反应液经过滤、滤液中加入一定量的水和乙酸乙酯,分层后水相用乙酸乙酯萃取、有机相合并后用饱和食盐水洗涤、无水Na2SO4干燥、减压浓缩后得到2-二甲氨基-1,3-二硫氰基丙烷粗产品,粗产品经柱层析或重结晶提纯后得到高纯度2-二甲氨基-1,3-二硫氰基丙烷。
与常规杀螟丹中间体的制备方法相比,本申请的工作原理和有益效果如下:
(1)本申请以1,3-二氯丙酮作为起始原料,在有机溶剂存在氛围下,使1,3-二氯丙酮与硫氰酸盐直接进行反应,反应温度控制在80℃以下,先得到粗品1,3-二硫氰基-2-卤代丙烷,该1,3-二硫氰基-2-卤代丙烷不论是与1-二甲氨基-2,3-二氯丙烷相比,还是与1,3-二氯丙酮相比,其反应活性更强,反应选择性更直接,当其与二甲胺在本申请设定条件下进行亲核取代时,可直接得到纯度较高的2-二甲氨基-1,3-二硫氰基丙烷,反应起始原料简单易得,且价格低廉,反应可以充分进行,合成率高。
(2)本申请在整个反应过程中,主要使用了1,3-二氯丙酮、硫氰酸盐、二甲胺等物质,且使用醇和水的混合物为溶剂,所涉及到的物质均为无毒、易去除的物质,反应过程中没有如剧毒氰化钠的使用,反应绿色性好,且整个反应都是在有机溶剂氛围下进行,反应条件温和,合成成本低。
(3)在整个反应过程中仅涉及到两步反应:第一步是1,3-二氯丙酮与硫氰酸盐反应得到1,3-二硫氰基-2-卤代丙烷,第二步是1,3-二硫氰基-2-卤代丙烷与二甲胺反应得到2-二甲氨基-1,3-二硫氰基丙烷,反应过程中只有1,3-二硫氰基-2-卤代丙烷一个中间产物,且不会产生异构体等无效中间体,解决了原工艺产生无效异构体问题,提高了2-二甲氨基-1,3-二硫氰基丙烷的质量。
附图说明
图1为本申请中粗品1,3-二硫氰基-2-丙酮的1H-NMR谱图;
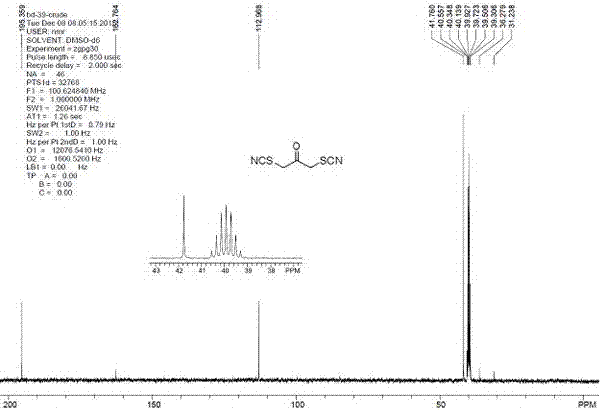
图2为本申请中粗品1,3-二硫氰基-2-丙酮的13C-NMR谱图。
具体实施方式
在整个反应过程中,反应主要分为两步,第一步是1,3-二氯丙酮与硫氰酸盐反应得到1,3-二硫氰基-2-卤代丙烷,在该工序中,对反应效果主要其影响作用的是1,3-二氯丙酮与硫氰酸盐的投料比和反应工艺条件,通过平行实验的测定我们发现:当反应温度控制在室温到80℃,1,3-二氯丙酮:-SCN的摩尔比为1:2-5,即-SCN过量时,反应速率最快,反应过程中的副产物如1-硫氰基-2,3-二溴丙烷、1,2,3-三硫氰基丙烷含量较低,尤其是当反应温度控制在室温到50℃,1,3-二氯丙酮:-SCN的摩尔比为1:3时,副产物最少,粗品得率最高,以下结合实施例1、3、5进行具体方案的阐述;第二步是1,3-二硫氰基-2-卤代丙烷与二甲胺反应得到2-二甲氨基-1,3-二硫氰基丙烷,二甲胺的投量同样保持过量,以下结合实施例2、4、6和7进行具体阐述。
实施例1
向50mL圆底烧瓶依次加入DMF(10mL)、1,3-二氯丙酮(252mg,2mmol)和NaSCN(486mg,6mmol)。反应混合物在室温搅拌过夜至1,3-二氯丙酮反应完全,向反应液加入水(50mL)和乙酸乙酯(100mL),分层后取有机相,水相用乙酸乙酯(50mL)萃取两次。将有机相合并后用饱和NaCl水溶液(50mL)洗涤4次,无水Na2SO4干燥,减压浓缩,得到1,3-二硫氰基丙酮(327mg,1.90mmol,95%产率),从粗产品的1H-NMR分析(见图1),所得粗产物具有很好的纯度。1,3-二硫氰基丙酮的结构及1H-NMR,13C-NMR数据如下:
1,3-二硫氰基-2-丙酮
结构:
1H-NMR(DMSO-d6,400MHz)ppm 4.40;
13C-NMR(acetone-d6,100MHz)ppm 195.4,113.0,41.8。
实施例2
向100mL的高压反应釜中依次加入甲醇(10mL)、实施例1所得1,3-二硫氰基丙酮(327mg)、二甲胺(40%水溶液,427mg)和Pd/C(32.7mg,10wt%)。将高压釜密封后冲入氢气至5MPa,反应混合物在100℃加热24小时后过滤。滤液加入水(50mL)和乙酸乙酯(100mL),分层后取有机相,水相用乙酸乙酯(50mL)萃取两次。将有机相合并后经饱和NaCl水溶液(50mL)洗涤1次,无水Na2SO4干燥,减压浓缩,柱层析得到2-二甲氨基-1,3-二硫氰基丙烷(350mg)。计算可知,1,3-二氯丙酮为原料,经实施例1和实施例2合成1,3-二硫氰基丙酮的两步反应总收率为87%。其结构和1H-NMR,13C-NMR,DEPT 135和DEPT 90数据如下:
2-二甲氨基-1,3-二硫氰基丙烷
结构:
1H-NMR(CDCl3,400MHz)ppm 3.37-3.29(m,2H),3.17-3.08(m,3H),2.32(s,6H);
13C-NMR(CDCl3,100MHz)ppm 112.2,62.4,39.8,34.1;
Dept 135(CDCl3,100MHz)ppm 112.2(C),62.4,39.8 34.1(CH2);
Dept 90(CDCl3,100MHz)ppm 62.4(CH),39.8(CH3);
MS(m/z)202(M+H,62),318(100)。
实施例3
向50mL圆底烧瓶依次加入DMF(10mL)、1,3-二氯丙酮(252mg,2mmol)和KSCN(582mg,6mmol)。反应混合物在室温搅拌过夜至1,3-二氯丙酮反应完全,向反应液加入水(50mL)和乙酸乙酯(100mL),分层后取有机相,水相用乙酸乙酯(50mL)萃取两次。将有机相合并后用饱和NaCl水溶液(50mL)洗涤4次,无水Na2SO4干燥,减压浓缩,得到310mg 1,3-二硫氰基丙酮,从粗产品的1H-NMR分析,所得粗产物具有很好的纯度。
实施例4
向100mL的高压反应釜中依次加入甲醇(10mL)、实施例3所得1,3-二硫氰基丙酮(310mg)、二甲胺(40%水溶液,450mg)和Pd/C(34.4mg,10wt%)。将高压釜密封后冲入氢气至5MPa,反应混合物在100℃加热24小时后过滤。滤液加入水(50mL)和乙酸乙酯(100mL),分层后取有机相,水相用乙酸乙酯(50mL)萃取两次。将有机相合并后经饱和NaCl水溶液(50mL)洗涤1次,无水Na2SO4干燥,减压浓缩,柱层析得到2-二甲氨基-1,3-二硫氰基丙烷(330mg)。计算可知,1,3-二氯丙酮为原料,经实施例3和实施例4合成1,3-二硫氰基丙酮的两步反应总收率为82%。
实施例5
向50mL圆底烧瓶依次加入CH3CN(20mL)、1,3-二氯丙酮(504mg,4mmol)和NaSCN(972mg,12mmol)。反应混合物在50℃搅拌过夜至1,3-二氯丙酮反应完全,向反应液加入水(30mL)和乙酸乙酯(200mL),分层后取有机相,水相用乙酸乙酯(100mL)萃取2次。将有机相合并后用饱和NaCl水溶液(50mL)洗涤1次,无水Na2SO4干燥,减压浓缩,得到1,3-二硫氰基丙酮粗产品(640mg,3.72mmol,93%产率)。
实施例6
向100mL的高压反应釜中依次加入甲醇(10mL)、实施例5所得1,3-二硫氰基丙酮(344mg)、二甲胺(40%水溶液,450mg)和Pd/C(34.4mg,10wt%)。将高压釜密封后冲入氢气至5MPa,反应混合物在100℃加热24小时后过滤。滤液加入水(50mL)和乙酸乙酯(100mL),分层后取有机相,水相用乙酸乙酯(50mL)萃取两次。将有机相合并后经饱和NaCl水溶液(50mL)洗涤1次,无水Na2SO4干燥,减压浓缩,用乙酸乙酯和石油醚重结晶得到2-二甲氨基-1,3-二硫氰基丙烷(300mg,1.49mmol)。计算可知,1,3-二氯丙酮为原料,经实施例5和实施例6合成1,3-二硫氰基丙酮的两步反应总收率为69%。
实施例7
向100mL的高压反应釜中依次加入甲醇(10mL)、实施例5所得1,3-二硫氰基丙酮(296mg)、二甲胺(40%水溶液,388mg)和Ru/C(29.6mg,10wt%)。将高压釜密封后冲入氢气至5MPa,反应混合物在100℃加热24小时后过滤。滤液加入水(50mL)和乙酸乙酯(100mL),分层后取有机相,水相用乙酸乙酯(50mL)萃取两次。将有机相合并后经饱和NaCl水溶液(50mL)洗涤1次,无水Na2SO4干燥,减压浓缩,用乙酸乙酯和石油醚重结晶得到2-二甲氨基-1,3-二硫氰基丙烷(320mg)。计算可知,1,3-二氯丙酮为原料,经实施例5和实施例7合成1,3-二硫氰基丙酮的两步反应总收率为86%。
以上内容是结合本发明创造的优选实施方式对所提供技术方案所作的进一步详细说明,不能认定本发明创造具体实施只局限于上述这些说明,对于本发明创造所属技术领域的普通技术人员来说,在不脱离本发明创造构思的前提,还可以做出若干简单推演或替换,都应当视为属于本发明创造的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!
- 一种丙辛吲哚盐酸盐药物中间体丙辛吲哚的合成方法与制造工艺
- 一种吲哚洛尔药物中间体(一)‑4‑(2‑羟基‑3‑异丙氨基丙氧)吲哚的合成方法与制造工艺
- 依替米贝的中间体及其合成方法与依替米贝的合成方法与制造工艺
- 一种白消安药物中间体1,4‑双甲基磺酸丁二酯的合成方法与制造工艺
- 一种塞利洛尔药物中间体3‑(4‑乙氧基苯基)‑1,1‑二乙基脲的合成方法与制造工艺
- 一种羟基保泰松药物中间体4‑羟基偶氮苯的合成方法与制造工艺
- 一种甲氧卡那霉素药物中间体γ‑氨基‑α‑羟基丁酸的合成方法与制造工艺
- 一种非那西丁药物中间体对硝基苯乙醚的合成方法与制造工艺
- 一种间尼索地平药物中间体乙酰乙酸异丁酯的合成方法与制造工艺
- 一种甲氧苄啶药物中间体3,4,5—三甲氧基苯甲酸甲酯的合成方法与制造工艺
- 依替米贝的中间体及其合成方法与依替米贝的合成方法与制造工艺
- 一种白消安药物中间体1,4‑双甲基磺酸丁二酯的合成方法与制造工艺
- 一种塞利洛尔药物中间体3‑(4‑乙氧基苯基)‑1,1‑二乙基脲的合成方法与制造工艺
- 一种羟基保泰松药物中间体4‑羟基偶氮苯的合成方法与制造工艺
- 一种甲氧卡那霉素药物中间体γ‑氨基‑α‑羟基丁酸的合成方法与制造工艺
- 一种非那西丁药物中间体对硝基苯乙醚的合成方法与制造工艺
- 一种间尼索地平药物中间体乙酰乙酸异丁酯的合成方法与制造工艺
- 一种甲氧苄啶药物中间体3,4,5—三甲氧基苯甲酸甲酯的合成方法与制造工艺
- 一种氯苯达诺药物中间体邻氯苯甲酸的合成方法与制造工艺
- 一种噢哢类抗癌化合物药物中间体2,4,6‑三羟基苯乙酮的合成方法与制造工艺