β2‑AR激动和抗炎双功能生物碱及其应用的制作方法
本发明属于药物化学技术领域,具体涉及一种β2-ar激动和抗炎双功能生物碱及其应用。
背景技术:
支气管哮喘(简称哮喘)是严重危害人类健康的常见病和多发病。据who估计,全球哮喘病的患者高达2.75亿人。流行病学调查分析,呼吸系统疾病发病率占总人口患病率的16%,占城市总死亡率的第三位,哮喘发病率在工业化国家中约为5%。随着全球范围内的空气污染和环境恶化,哮喘的发病率和死亡率呈逐年上升态势,全球范围内,每年有超过18万人死于哮喘。哮喘已成为全球性的公共卫生问题。
哮喘为慢性非特异性气道炎症性疾病,由多种炎性细胞和细胞组分参与、涉及多种炎性介质和细胞因子、以气道高反应性和气道痉挛为特征。哮喘病因复杂,包括病毒和细菌感染、过敏、某些药物或刺激性物质诱发的支气管痉挛等,其发病机制至今尚未完全明确。
扩张支气管快速缓解症状和长期抗炎控制是治疗哮喘的两大策略。支气管扩张药主要包括β2-ar激动剂和茶碱类药物;抗炎药主要包括糖皮质激素和抗白三烯类药物,其中β2-ar激动剂和糖皮质激素是哮喘防治指南推荐的一线药物。由于单用、长期使用激素易产生骨质疏松、高血压、糖尿病、下丘脑-垂体-肾上腺轴抑制、肥胖、白内障、青光眼等诸多副作用,糖皮质激素/β2-ar激动剂复合制剂具有协同抗炎平喘作用,可减少大剂量糖皮质激素用量,已成为抗哮喘创新药物研发方向之一,如布地奈德/福莫特罗、氟替卡松/沙美特罗复合制剂,但这类药物仍不适用于激素抵抗型哮喘患者,新型β2-ar激动和抗炎双功能抗哮喘药物有待发现。
肾上腺素受体(ar)包括α受体(包括α1和α2两种亚型)和β受体(包括β1、β2和β3三种亚型),其区别在于偶联的g蛋白种类不同,激活的酶系不同,产生的第二信使物质和生物效应不同。β2-ar激动剂是扩张支气管的首选药物,其作用机制是与气道平滑肌细胞表面具有高亲和力状态的β2-ar结合,导致跨膜蛋白在胞浆的末端部分发生构型重排,激活腺苷酸环化酶(ac),在激活的ac作用下三磷酸腺苷(atp)转变成3,5-环磷酸腺苷(camp),使camp在细胞内的浓度增加;camp通过使胞内的钙离子外排,造成胞内粗细丝微细结构发生改变,导致肌节延长,使气道平滑肌松弛,从而达到支气管解痉的目的。此外,β2-ar激动剂可通过抑制炎性细胞扣押、聚集、黏附、炎症介质的合成与释放等对哮喘气道炎症亦具有拮抗作用。由于β2-ar激动剂可快速缓解气道痉挛症状,且具有抗气道炎症等作用,已成为哮喘治疗的首选药物。
马齿苋(portulacaoleraceal.)广布于全世界温带和热带地区,在我国和其他许多国家作为药食两用植物使用。马齿苋具有清热解毒、抗菌消炎、散血消肿等功效。生物碱是马齿苋中的一类重要的化学成分,而且其结构类型众多。本申请发明人在前期研究中从马齿苋中分离得到多种结构新颖的生物碱,如四氢异喹啉类酰胺生物碱(马齿苋酰胺e),以及吲哚啉类酰胺生物碱(马齿苋酰胺a、b、c、d、f、g)等,并且研究发现上述生物碱具有体外自由基清除活性、体外神经元细胞保护作用和抗老年痴呆作用。但目前尚未有关于从马齿苋中分离得到具有β2-ar激动和抗炎双功能活性的儿茶酚胺类生物碱的报道。
技术实现要素:
针对现有技术,本发明的目的是提供一种β2-ar激动和抗炎双功能生物碱及其应用。
为实现上述目的,本发明采用如下技术方案:
本发明的第一方面,提供一种式i或式ii所示的生物碱,其类似物、异构体、消旋体或者衍生物;
其中,r为氢、羟基、甲氧基或烷基;所述烷基优选为甲基或乙基;
r1为氢或烷基;所述烷基优选为甲基或乙基;
r2为氢或烷基;所述烷基优选为甲基或乙基;
r3为呋喃环、被取代的呋喃环、根据电子等排定律改造的可以被取代的噻吩环、吡咯环或c1-c10的脂肪链;
r4为h、羟基、甲氧基或烷基;所述烷基优选为甲基或乙基;
r5为h、羟基、甲氧基或烷基;所述烷基优选为甲基或乙基。
优选的,r、r1、r2、r4、r5均为h。
优选的,上述式i或式ii所示的生物碱,其类似物、异构体、消旋体或者衍生物选自如下化合物:
本发明的第二方面,提供式i、式ii或式iii所示的生物碱在制备β2-肾上腺素受体激动剂中的应用。
本发明的第三方面,提供式i、式ii或式iii所示的生物碱在制备抗炎药物中的应用。
本发明的第四方面,提供式i、式ii或式iii所示的生物碱在制备β2-ar激动和抗炎双功能药物中的应用。
本发明的第五方面,提供式i、式ii或式iii所示的生物碱在制备治疗和/或预防与激动肾上腺素受体相关的疾病的药物中的应用。
所述与激动肾上腺素受体相关的疾病包括:哮喘性疾病或其它相关炎症性疾病。
所述哮喘性疾病包括:哮喘性支气管炎、肺气肿、支气管哮喘、夜间哮喘、运动性哮喘或慢性阻塞性肺病。
本发明的第六方面,提供一种β2-肾上腺素受体激动剂,其活性成分为上述式i或式ii所示的生物碱,其类似物、异构体、消旋体或者衍生物。
本发明的第七方面,提供一种治疗炎症性疾病的药物,其活性成分为上述式i或式ii所示的生物碱,其类似物、异构体、消旋体或者衍生物。
本发明的第八方面,提供一种治疗哮喘性疾病的药物,其活性成分为上述式i或式ii所示的生物碱,其类似物、异构体、消旋体或者衍生物。
本发明的第九方面,提供一种β2-ar激动和抗炎双功能药物,其活性成分为上述式i或式ii所示的生物碱,其类似物、异构体、消旋体或者衍生物。
上述技术方案具有如下有益效果:
(1)本发明首次从马齿苋中分离得到具有β2-ar激动和抗炎双功能活性的儿茶酚胺类生物碱,其结构如式i和式ii所示。
(2)本发明还发现了申请人之前从马齿苋中分离得到的生物碱oleraceine(马齿苋酰胺e)的新用途,其具有较好的β2-ar激动和抗炎双功能活性。
基于上述发现,本发明的具有β2-ar激动和抗炎双功能生物碱为治疗哮喘等呼吸系统疾病及相关的炎症性疾病提供了有用的化合物。
附图说明
构成本申请的一部分的说明书附图用来提供对本申请的进一步理解,本申请的示意性实施例及其说明用于解释本申请,并不构成对本申请的不当限定。
图1:实施例2中化合物对β2-ar受体的激动效应。
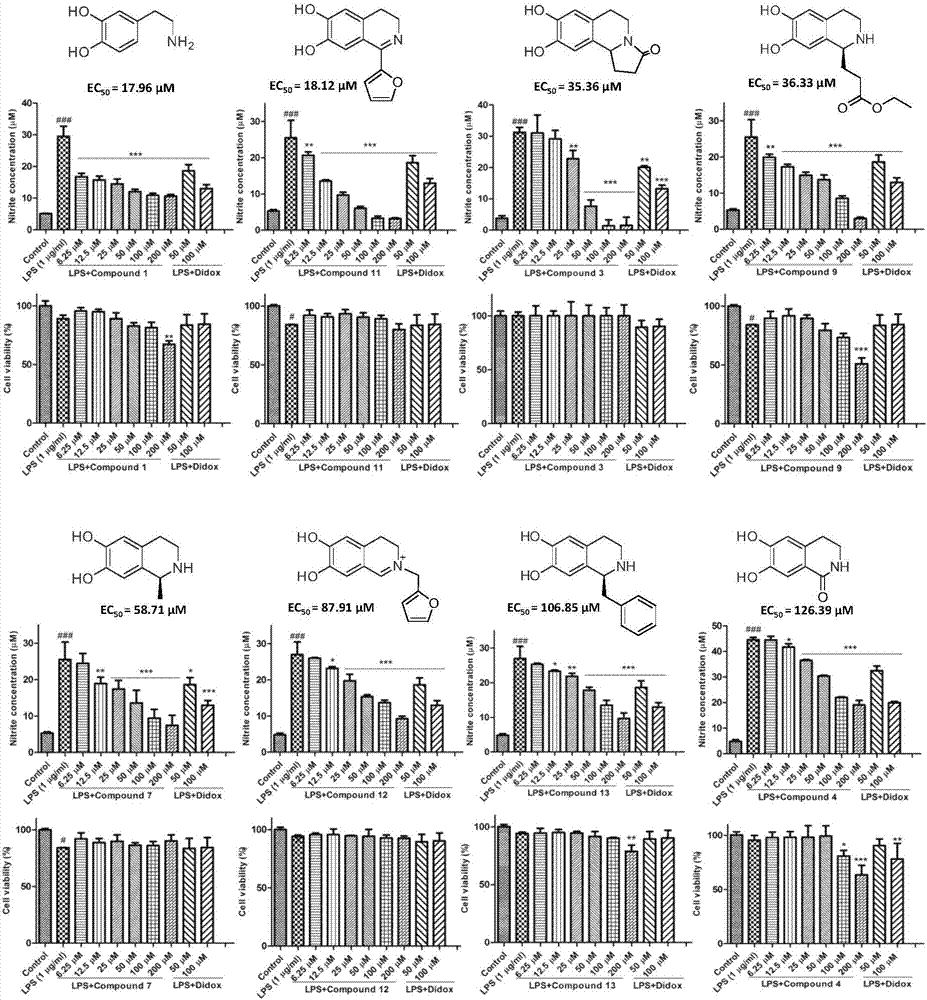
图2:实施例3中化合物的抗炎活性及对lps刺激raw264.7巨噬细胞存活率的影响。
具体实施方式
应该指出,以下详细说明都是示例性的,旨在对本发明提供进一步的说明。除非另有指明,本文使用的所有技术和科学术语具有与本发明所属技术领域的普通技术人员通常理解的相同含义。
需要注意的是,这里所使用的术语仅是为了描述具体实施方式,而非意图限制根据本发明的示例性实施方式。如在这里所使用的,除非上下文另外明确指出,否则单数形式也意图包括复数形式,此外,还应当理解的是,当在本说明书中使用术语“包含”和/或“包括”时,其指明存在特征、步骤、操作和/或它们的组合。
正如背景技术所介绍的,现有技术中尚未有关于从马齿苋中分离得到具有β2-ar激动和抗炎双功能活性的儿茶酚胺类生物碱的报道。基于此,本发明提出了一种β2-ar激动和抗炎双功能生物碱及其应用。
本发明首次从马齿苋中分离得到具有β2-ar激动和抗炎双功能活性的儿茶酚胺类生物碱(新化合物9、10、11),这类生物碱骨架类型包括四氢异喹啉、二氢异喹啉;二氢异喹啉或者四氢异喹啉的c1位与呋喃环、苄基及脂肪链等取代基连接。其结构与临床哮喘治疗药物曲托喹酚结构相似,均具有儿茶酚胺母核。
在本发明的一种实施方案中,通过钙离子荧光检测技术并结合稳定表达β2-ar受体的cho-k1/ga15/adrb2细胞模型,检测各化合物对β2-ar的激动活性。
在本发明的另一种实施方案中,采用lps刺激raw264.7小鼠巨噬细胞系,检测各化合物的抗炎活性。
结果发现,从马齿苋中分离得到的儿茶酚胺类生物碱具备不同强度的激动β2-ar作用和抗炎双功能,其中新化合物11和已知生物碱oleraceine的β2-ar激动和抗炎双功能活性最为显著,从而完成了本发明。
为了使得本领域技术人员能够更加清楚地了解本发明的技术方案,以下将结合具体的实施例详细说明本发明的技术方案。
实施例1:化合物9、10、11的分离
由于化合物9、10、11为新的化合物,本发明提供了从马齿苋中分离纯化化合物9、10、11的制备方法及其结构表征数据。
一、新化合物9、10、11的分离制备方法
马齿苋药材4kg,用6倍量60%的乙醇,加热回流提取3次,每次1h,合并三次提取液,浓缩至8l(浓度为0.5g生药/ml),静置,取上清液上样于两根聚酰胺色谱柱(60cm×10cm,800g),依次用水、20%乙醇、40%乙醇、60%乙醇、80%乙醇、95%乙醇、25%氨水:80%乙醇(1:7)梯度洗脱,洗脱流分经过薄层及hplc对比,将其合并为9个流份,编号为frs.1-9。将frs.1与frs.2合并,共634.5g,分散在1l水中,依次用等量的乙酸乙酯和正丁醇各萃取三次,得到乙酸乙酯相(11.4g)和正丁醇相(52.0g)。
正丁醇相(52.0g)过正相硅胶柱(800g,6×25cm),用乙酸乙酯-甲醇(9:1~0:10)梯度洗脱,得到流分cfr(1-3)(9.62g)和cfr(4-12)(24.8g)。
cfr(4-12)(24.8g)过聚酰胺柱(100-200目,10×30cm),依次用含1%甲酸的石油醚-乙酸乙酯(9:1~0:10)梯度洗脱和乙酸乙酯-甲醇(9:1~0:10)梯度洗脱,得到10个流分。
①其中cfr(4-12)-(40-60)(9.6g)过聚酰胺柱(100-200目,6×50cm),依次用含石油醚-乙酸乙酯(9:1~0:10)梯度洗脱和乙酸乙酯-甲醇(9:1~0:10)梯度洗脱,得到10个流分。其中cfr(4-12)-(40-60)-(23-38)(2.00g)过mci柱(4×30cm),用水-甲醇(95:5~0:10)梯度洗脱,得到12个流分,其中cfr(4-12)-(40-60)-(23-38)-(19-21)(25mg)过凝胶柱(2×120cm),甲醇洗脱得到化合物11(4mg)。
②其中cfr(4-12)-(61-70)(1.72g)过聚酰胺柱(100-200目,4.5×35cm),依次用含石油醚-乙酸乙酯(9:1~0:10)梯度洗脱和乙酸乙酯-甲醇(20:1~0:10)梯度洗脱,得到10个流分,cfr(4-12)-(61-70)-(13-19)(506mg)过聚酰胺柱(100-200目,6×50cm),依次用含石油醚-乙酸乙酯(9:1~0:10)梯度洗脱和乙酸乙酯-甲醇(9:1~0:10)梯度洗脱,得到5个流分,cfr(4-12)-(61-70)-(13-19)-(8-10)(112mg)过反相柱(3.0×33cm),用水-甲醇(95:5~0:10)梯度洗脱,得到10个流分,cfr(4-12)-(61-70)-(13-19)-(8-10)-(6-10)(14mg)过凝胶柱(2.5×150cm),甲醇洗脱,得到化合物10(3mg)。
③其中cfr(4-12)-(71-77)(2.88g)过聚酰胺柱(100-200目,4.5×35cm),依次用含石油醚-乙酸乙酯(9:1~0:10)梯度洗脱和乙酸乙酯-甲醇(20:1~0:10)梯度洗脱,得到15个流分,cfr(4-12)-(71-77)-(5-10)(450mg)过聚酰胺柱(100-200目,4.5×35cm),用水-甲醇(10:0~7:3)梯度洗脱得到2个流分,cfr(4-12)-(71-77)-(5-10)-(1-4)(180mg)过反相硅胶柱(4.0×20cm),用水-甲醇(95:5~0:10)梯度洗脱,得到化合物9(5mg)。
二、新化合物9、10、11的数据表征
1.化合物9:(s)-(-)-3-(6,7-二羟基-1,2,3,4-四氢异喹啉-1-基)丙酸乙酯的数据表征
化合物9的结构式
化合物9:白色粉末;溶于甲醇、水,不溶于石油醚。聚酰胺薄层板以乙酸乙酯-甲醇4:1为展开剂,rf=0.31;碘熏显红棕色,0.5%三氯化铁乙醇溶液呈棕色。[α]20d–18.6°(c0.04,meoh);hr-p-esi-msm/z266.1393[m+h]+(calcd.forc14h20no4,266.1348),hr-n-esi-msm/z264.1233[m-h]-(calcd.forc14h18no4,264.1236);1hnmr(600mhz,d2o)δ:4.30(1h,s,h-1),3.38(1h,s,h-3a),3.19(1h,s,h-3b),2.80(2h,s,h-4),6.54(1h,s,h-5),6.55(1h,s,h-8),2.15(1h,s,h-1′a),2.06(1h,s,h-1′b),2.40(2h,s,h-2′),3.91(2h,q,j6.0hz,h-5′),1.04(3h,s,h-6′);13cnmr(150mhz,d2o)δ:54.0(c-1),38.8(c-3),23.7(c-4),115.7(c-5),144.0(c-6),142.9(c-7),113.7(c-8),122.7(c-9a),123.8(c-10b),27.7(c-1′),29.7(c-2′),174.9(c-3′),61.9(c-5′),13.1(c-6′).
2.化合物10:1-(5-羟甲基呋喃-2-基)-6,7-二羟基-3,4-二氢异喹啉的数据表征
化合物10的结构式
化合物10:红色粉末,易溶于甲醇、水,难溶于乙酸乙酯、二氯甲烷、石油醚。在聚酰胺薄膜上以乙酸乙酯-甲醇(4:1)展开,rf值为0.55,自然光下显红色斑点,0.5%三氯化铁乙醇溶液呈棕色,碘化铋钾溶液显红色。hr-esi-msm/z260.0917[m+h]+(calcd.forc14h14no4,260.0923).ir:3202,1504,1612,1077cm-1;1hnmr(600mhz,d2o)δ:3.56(2h,t,j7.2hz,h-3),2.77(2h,t,j7.2hz,h-4),6.51(1h,s,h-5),7.16(1h,s,h-8),7.22(1h,d,j3.6hz,h-3′),6.61(1h,d,j3.6hz,h-4′),4.61(2h,s,h-6′);13cnmr(150mhz,d2o)δ:154.5(c-1),39.6(c-3),25.7(c-4),117.3(c-5),165.4(c-6),146.0(c-7),115.6(c-8),136.9(c-9a),109.3(c-10b),143.9(c-2′),124.1(c-3′),111.5(c-4′),160.3(c-5′),55.9(c-6′).
3.化合物11:1-(呋喃-2-基)-6,7-二羟基-3,4-二氢异喹啉的数据表征
化合物11的结构式
化合物11:红色粉末,易溶于甲醇、水,难溶于乙酸乙酯、二氯甲烷、石油醚。在聚酰胺薄膜上以乙酸乙酯-甲醇4:1展开,rf值为0.65,自然光下显红色斑点,0.5%三氯化铁乙醇溶液呈棕色,碘化铋钾溶液显红色。hr-esi-msm/z230.0818[m+h]+(calcd.forc13h12no3,230.0817),hr-esi-msm/z228.0669[m-h]-(calcd.forc13h10no3,228.0661),457.1336[2m-h]-(calcd.forc26h21n2o6,457.1400);1hnmr(600mhz,d2o)δ:3.69(2h,t,j6.0hz,h-3),2.77(2h,t,j6.0hz,h-4),6.81(1h,s,h-5),7.35(1h,s,h-8),7.43(1h,br.s,h-3′),6.78(1h,br.s,h-4′),7.94(1h,br.s,h-5′);13cnmr(150mhz,d2o)δ:156.7(c-1),39.8(c-3),24.7(c-4),115.9(c-5),155.0(c-6),143.9(c-7),118.2(c-8),135.0(c-9a),114.2(c-10b),143.7(c-2′),125.4(c-3′),114.2(c-4′),150.5(c-5′).
实施例2:马齿苋中儿茶酚胺类生物碱激动β2-ar受体的活性筛选
一、实验材料、试剂与实验系统
1.待测化合物
14个化合物(化合物9、10、11为从马齿苋中分离得到的新化合物,其他的化合物为已知的化合物)在-20℃下保存以备用。实验时,所有待测化合物均用dmso溶解制成储液,检测时用hbss-20mmhepes缓冲液进行稀释,配制成相应浓度的工作浓度。
2.试剂
稳定表达β2-ar受体的cho-k1/ga15细胞株(genscript,m00308);
3.实验系统
稳定表达β2-ar受体的cho-k1/ga15细胞培养于10cm培养皿中,在37℃/5%co2培养箱中培养,当细胞汇合度达到85%时,进行消化处理,将收集到的细胞悬液接种到384微孔板,即可用于实验。
(1)细胞培养条件:
cho-k1/ga15/adrb2细胞系常规培养,传代在含有10%胎牛血清和100μg/mlhygromycinb,200μg/mlzeocin的ham’sf12中。
(2)化合物的配制:
在检测前,用hbss-20mmhepes稀释待测化合物,配制成五倍于检测浓度的溶液。所有检测浓度中dmso对照为0.1%,化合物最高检测浓度为100μm,三复孔。
二、检测方法
1.钙流检测的准备工作
激动剂检测的准备工作方案为:将细胞接种到384微孔板,每孔接种20μl细胞悬液含1.5万个细胞,放置到37℃/5%co2培养箱中继续培养,18个小时后将细胞取出,加入染料,每孔20μl,然后将细胞板放到37℃/5%co2培养箱孵育1个小时,最后于室温平衡15分钟。检测时加入10μl5×检测浓度的激动剂检测rfu值。
2.钙流信号检测
将装有化合物溶液(5×检测浓度)的384微孔板,细胞板和枪头盒放到fliprtetra(moleculedevices)内,运行检测程序,仪器总体检测时间为120秒,在第21秒时自动将激动剂10μl加入到细胞板内。
3.数据分析
通过screenworks(version3.1)获得原始数据以*fmd文件保存。数据采集和分析使用excel和graphpadprism6软件程序。对于每个检测孔而言,以1到20秒的平均荧光强度值作为基线,21到120秒的最大荧光强度值减去基线值即为相对荧光强度值(△rfu),根据该数值并依据以下方程可计算出激活百分比。
激活率(%)=(△rfucompound-△rfubackground)/(△rfuagonistcontrol-△rfubackground)×100%
使用graphpadprism6用四参数方程对数据进行分析,从而计算出ec50值。四参数方程如下:y=bottom+(top-bottom)/(1+10^(logec50/ic50-x)*hillslope))
x是浓度的log值,y是激动率。
三、实验结果
检测14个化合物对adrb2受体的激动活性,化合物最高检测浓度为100μm,三复孔。
化合物对β2-ar受体的激动效应见图1a-d,结果表明,新化合物11(91.77±2.78%)>化合物13(90.83±5.98%)>化合物1(多巴胺,86.42±8.42%)>化合物8(70.89±9.13%)>新化合物10(70.60±5.18%)>化合物3(oleraceine,70.20±1.93%)>新化合物9(42.03±2.70%)>化合物6(41.06±3.80%)>化合物2(39.25±3.55%)>化合物5(37.70±3.62%)>化合物7(猪毛菜碱,35.47±1.14%)>新化合物12(11.44±5.77%)>化合物4(0.49±2.52%)>化合物30(-11.50±1.18%),其中11、13、1、3、10、8活性强。
剂量效应曲线(图1c-d)首次发现13和11为高效β2-ar激动剂,其ec50值分别为87.86nm和5.125μm。
实施例3:马齿苋中儿茶酚胺类生物碱对lps刺激raw264.7小鼠巨噬细胞系的抗炎活性筛选。
一、细胞培养:
raw264.7小鼠巨噬细胞株购自中科院上海细胞库(atcc);用含10%胎牛血清、100μg/ml的链霉素、100u/ml青霉素的dmem培养液,于37℃二氧化碳培养箱中常规培养,隔天传代,细胞于对数生长期呈半贴壁状态生长。
二、一氧化氮(no)的测定:
raw264.7细胞接种于96孔板(8.0×104细胞/孔),培养1h后分别加入不同浓度的化合物及lps(终浓度为1μg/ml),同时设空白对照组。50和100μm3,4-二羟基-苯基异羟肟酸(3,4-dihydroxy-benzohydroxamicacid,didox)作为阳性对照。培养24h后,吸取100μl细胞上清液置于一个新的96孔板中,加入100μlgriess试剂[0.1%萘乙二胺溶液与1%磺胺(5%)磷酸溶液于用前12h等体积混合],室温放置15min,用酶标仪测定570nm的吸光度。根据亚硝酸钠标准曲线计算no2-的含量。由于no自由基不稳定,在体内和水溶液中极易氧化生成较稳定的不易挥发的no2-,在酸性条件下,其与磺胺发生重氮反应,生成重氮化合物,后者进一步与萘乙二胺发生耦合反应,该反应生成的产物浓度与no2-浓度具有线性关系,间接反应了no的含量。
三、细胞存活率的测定:
为避免no测定出现假阳性结果,利用mtt法检测化合物对raw264.7细胞的存活率是否存在影响。即在吸取培养液上清100μl测定no浓度后,于上述96孔板内每孔加入100μl含0.4%mtt[即3-(4,5-二甲基噻唑-2)-2,5-二苯基四氮唑溴盐]的dmem培养基,37℃孵育3h后,弃去培养基,每孔加入100μldmso,振摇至生成的蓝色甲瓒结晶完全溶解后,用酶标仪测定570nm的吸光度值(a570)。
细胞存活率(%)=100×试验组平均a570值/空白对照组平均a570值。
四、实验结果
化合物的抗炎活性及对lps刺激raw264.7巨噬细胞存活率的影响见图2。实验首次发现,马齿苋中16个水溶性儿茶酚胺类生物碱对lps诱导raw264.7巨噬细胞no过量释放均有不同程度的抑制活性(ec50值在17.96-497.67μm)。其中多巴胺(1)和生物碱11(新化合物)、3、9(新化合物)活性很强,其ec50值分别为17.96、18.12、35.36和36.33μm,强于已报道具有显著抗炎活性的结构类似物3,4-二羟基-苯甲羟肟酸(ec50=82.39μm)
上述实施例为本发明较佳的实施方式,但本发明的实施方式并不受上述实施例的限制,其他的任何未背离本发明的精神实质与原理下所作的改变、修饰、替代、组合、简化,均应为等效的置换方式,都包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!