预防、改善或治疗退行性神经系统疾病的含茯苓皮提取物的组合物的制作方法
本发明涉及一种用于预防、改善或治疗退行性神经系统疾病的、含茯苓皮提取物的组合物。
背景技术:
退行性神经系统疾病是其中心智功能由于神经细胞(神经元)逐渐发生结构和功能性的丢失而恶化的疾病。由于神经系统特定区域中的神经细胞发生退行性变性,退行性神经系统疾病可能伴随诸如痴呆、锥体外系异常、小脑异常、感觉障碍和运动障碍等症状。此外,由于同时发生多种异常而可能出现复杂的症状。按照患者的临床表现对疾病进行诊断。但是症状差异很大,不同的疾病常常具有相同的临床症状,这使得诊断很困难(soc.sci.med.vol.40.no.6,pp.847-858,1995)。
在退行性神经系统疾病中,疾病的症状是慢慢发展的,而且该疾病常常是由衰老引起的。一旦疾病已经显现出来,就会持续进行数年或数十年,直至死亡,因此增加了社会负担。已知遗传影响,诸如家族史,很可能是疾病的病因,但获得性因素也起到重要作用。按照其临床症状,可对退行性神经系统疾病进行分类,例如进行性痴呆(阿尔茨海默氏病等)、神经系统障碍(例如皮克病)、姿势和运动障碍(例如帕金森氏病)、进行性共济失调、肌肉萎缩和无力,以及感知和运动障碍等(internationaljournalofengineeringandtechnology,vol.2,no.4,august2010classificationofneurodegenerativedisordersbasedonmajorriskfactorsemployingmachinelearningtechniques)。
aβ斑块和过磷酸化tau蛋白缠结的细胞毒性作为阿尔茨海默氏痴呆(一种典型的退行性脑病)的直接病因正在得到关注。
aβ是从前体app,通过诸如β-分泌酶和γ-分泌酶等酶的作用而生成,分布在神经细胞外部。当aβ浓度高于一定水平时,aβ蛋白之间结合而形成不溶的老年斑(senileplaque)。该物质可导致炎症和神经毒性,并且破坏周围的神经细胞。例如,已知在阿尔茨海默氏病患者中观察到的神经元死亡和小神经胶质细胞增生与老年斑相关。体外测试示出aβ肽能诱导小神经胶质细胞活化(脑巨噬细胞),这支持了aβ肽引起阿尔茨海默氏病患者脑部中所发现的小神经胶质细胞增生和脑部炎症的假说。迄今为止,还没有被广泛接受的预期一旦形成老年斑就可显著溶解aβ,或预防沉积物形成的疗法或治疗药物。
tau蛋白由四部分组成:n末端突出部,脯氨酸聚集结构域、微管结合结构域和c-末端(mandelkowetal.,acta.neuropathol.,103,26-35,1996)。起到连接微管的作用,其中微管形成神经细胞的物理结构。已知在中枢神经系统神经元细胞中的tau蛋白经异常过磷酸化或修饰,会导致退行性脑病,例如tau蛋白病变(tauopathy)。阿尔茨海默氏病(alzheimer'sdisease)、皮克病(picksdisease)、17号染色体相关的额颞痴呆合并帕金森症(ftdp-17)是典型的tau蛋白病变(leeetal.,annu.rev.neurosci.,24,1121-1159,2001;bergeronetal.,j.neuropathol.exp.neurol.,56,726-734,1997;bugianietal.,j.neuropathol.exp.neurol.,58,667-677,1999;delacourteetal.,ann.neurol.,43,193-204,1998;ittnerandgotz,nat.rev.neurosci.,12,65-72,2011)。
在二十世纪八十年代对阿尔茨海默氏病的研究中,暗示神经营养因子具有对退行性神经系统疾病的治疗潜力(nature.1987sep3-9;329(6134):65-8.ameliorationofcholinergicneuronatrophyandspatialmemoryimpairmentinagedratsbynervegrowthfactor)。研究示出了通过向侧脑室给予神经生长因子(ngf)恢复了基底前脑中的胆碱能神经元,从而使实验动物的记忆力得到改善,其中胆碱能神经元由于衰老而丢失,并已知是阿尔茨海默氏病的病因之一。因此,对使用神经营养因子来治疗退行性神经系统疾病进行了持续研究。在后来的研究中,通过将脑源性神经营养因子(bdnf)、神经营养蛋白-3(nt-3)、神经营养蛋白-4(nt-4)和睫状神经营养因子(cntf)(这些是神经营养因子家族的一部分)注射到由于面神经和坐骨神经结节而运动神经功能受损的实验动物中,进行了恢复运动神经功能的研究,并且获得了阳性结果(nature.1992dec24-31;360(6406):757-9.brain-derivedneurotrophicfactorpreventsthedeathofmotoneuronsinnewbornratsafternervesection)。进一步地,在使用患运动神经元的数量和功能随着年龄增长而逐渐丧失的疾病的重组小鼠(wobbler)的实验中,通过给予小鼠bdnf和cntf,使运动神经元的数量增加,并且改善了功能(science.1994aug19;265(5175):1107-10.arrestofmotorneurondiseaseinwobblermiceco-treatedwithcntfandbdnf)。除了上述研究之外,还报道了神经营养因子通过增加多种感知和运动神经病变模型中的神经元的数量和功能,改善了实验动物的记忆、认知和行为障碍。
茯苓(茯)的学名是poriacocos。茯苓在分类上属于真担子菌纲、层菌亚纲,非褶菌目,多孔菌科的真菌。茯苓是一类属于杆菌的真菌,是褐腐菌,是在松树中的一类腐生生物,但也寄生于活的松树的根部。菌丝体生长,同时长出白色分枝,并且菌丝开始长在一起。当适当的环境条件,诸如温度和湿度持续存在时,形成菌核硬块,这被称为茯苓。根据内部的颜色,白色是白茯苓,淡红色是赤茯苓。茯苓的外皮被称为茯苓皮。
茯苓的主要成分是茯苓酸(c33h52o5)、松苓酸(c30h18o3)、松苓新酸(3β羟基-7,9(11),24-羊毛甾三烯-21-酸(3β-hyderoxy-lanosta-7.9(11),24-trien-21-oicacid)、土莫酸(c31h50o)和齿孔酸(c31h50o3)等,已经报道了在茯苓和茯苓皮中分离出了三萜茯苓新酸及其衍生物。还含有麦角甾醇、卵磷脂、腺嘌呤、胆碱、葡萄糖、果糖、蛋白质,大量的无机物质,以及破坏敏酸
茯苓皮味甘性暖,味道和性质均轻,故为良性的药物物质。在过去的文献中,记载了茯苓皮可缓解口渴、便于排尿、去湿气、适当地调整身体状态,通过协调消化系统的功能而增加能量,并且通过舒缓腰部来改善腹部淤血的血液循环。茯苓皮主要用于与记忆力相关的药方。在最近的文献中,还报道了茯苓皮具有抗糖尿病和抗癌效果(linghui,evaluationofthechemotherapeuticandchemopreventivepotentialoftriterpenoidsfromporiacocos,linghui,doctoralthesisofdepartmentofpharmacy,nationaluniversityofsingapore,2010)。
茯苓皮是属于多孔菌科的茯苓菌核的外皮。已知作为药用物质,具有利水消肿的效果。它尤其含有丰富的羊毛甾烷类三萜茯苓新酸,并且《东医宝鉴》中记载了茯苓皮用于水肿药方的五皮散(橘皮、大腹皮、茯苓皮、生姜皮、桑白皮)的成分。在最近的研究中,报道了茯苓皮具有如利尿、促进排尿、消除水肿等治疗效果(triterpenesfromthesurfacelayerofporiacocos,takaakitai,phytochem,39,5,1995;urinarymetabonomicstudyofthesurfacelayerofporiacocosasaneffectivetreatmentforchronicrenalinjuryinrats,yingyongzhaoetal,journalofethnopharmacology,148,2,2013)。
在这一背景下,本发明人进行了研究,以开发用于有效预防、改善和治疗退行性神经系统疾病的药物组合物和食品组合物的材料。结果,在研究茯苓皮的神经心理活性过程中,本发明的发明人证明了这些茯苓皮提取物在由多种脑损伤或记忆抑制药物所诱导的脑神经病变模型中,显示出显著的记忆恢复活性。此外,本发明人通过证明这些茯苓皮提取物示出抑制导致脑中神经细胞死亡的物质的生成,并且促进促神经细胞再生和分化的蛋白的表达来保护神经细胞,从而完成了本发明。
技术实现要素:
【技术问题】
本发明的目的是提供用于预防和治疗退行性神经系统疾病的药物组合物,和用于预防和改善退行性神经系统疾病的食品组合物,所述药物组合物和所述食品组合物包含作为活性成分的茯苓(学名:poriacocos)皮提取物。
【技术方案】
为了实现上述目的,本发明提供了用于预防和治疗退行性神经系统疾病的药物组合物,和用于预防和改善退行性神经系统疾病的食品组合物,所述药物组合物和所述食品组合物包含茯苓皮提取物。
【有益效果】
根据本发明,茯苓皮提取物抑制β-淀粉样肽(aβ)的生成和tau蛋白的磷酸化,这显示出保护神经细胞的效果。此外,它还显示出以下效果:抑制乙酰胆碱酯酶(ache),从而提高神经传导且介导记忆增强作用。因此,茯苓皮提取物可有效用于开发预防和治疗退行性神经系统疾病(包括痴呆)的药物组合物,或预防和改善退行性神经系统疾病的健康食品组合物。
附图说明
图1是示出了实验动物模型中的被动回避测试结果的图,其中经茯苓皮提取物处理之后,通过东莨菪碱抑制记忆形成。
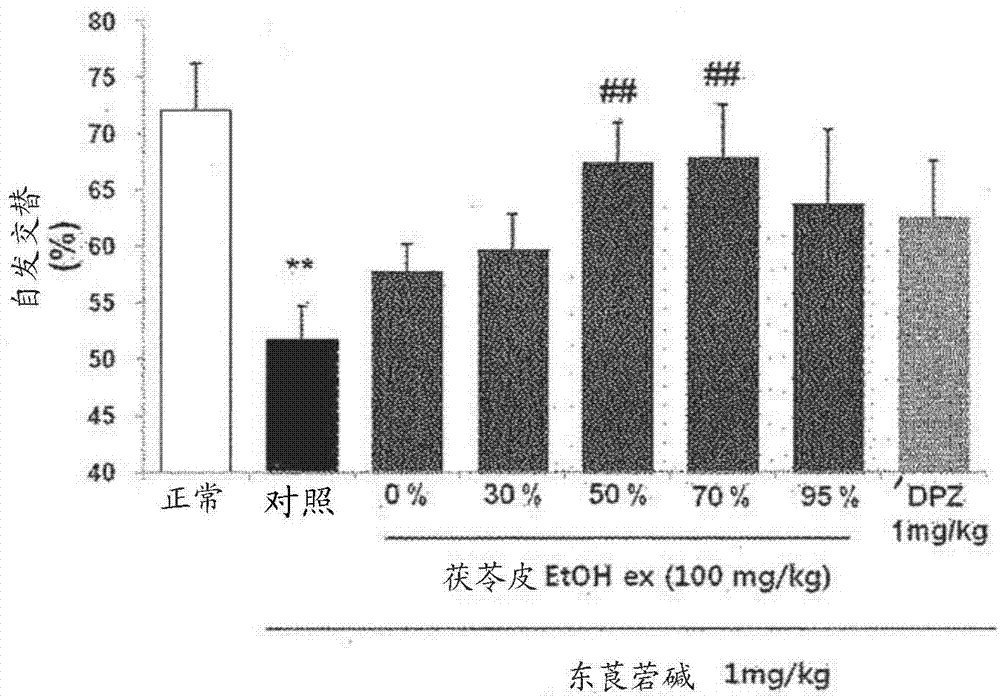
图2是示出了实验动物模型中的y-迷宫测试结果的图,其中经茯苓皮提取物处理之后,通过东莨菪碱抑制记忆形成。
图3是示出了实验动物模型中的新物体识别(nor)测试结果的图,其中经茯苓皮提取物处理之后,通过东莨菪碱抑制记忆形成。
图4是示出了当经茯苓皮提取物处理时,动物模型中的y-迷宫测试结果的图,其中将β-淀粉样肽灌注到脑中以诱导阿尔茨海默氏痴呆的症状。
图5是示出了当经茯苓皮提取物处理时,动物模型中的新物体识别测试(nort)结果的图,其中将β-淀粉样肽灌注到脑中以诱导阿尔茨海默氏痴呆的症状。
图6是示出了当经茯苓皮提取物处理时,动物模型中的神经细胞染色结果的图,其中将β-淀粉样肽灌注到脑中以诱导阿尔茨海默氏痴呆的症状。
图7是示出了在使用茯苓皮提取物处理正常动物之后,β-淀粉样肽测量结果的图。
图8是示出了在使用茯苓皮提取物处理正常动物之后,ngf生成量的测量结果的图。
图9示出了在使用茯苓皮提取物处理神经细胞系sh-sy5y之后,测量ache活性的结果。
图10示出了在使用茯苓皮提取物处理神经细胞系sh-sy5y之后,通过mtt测量凋亡程度的结果。
图11示出了在使用茯苓皮提取物处理神经细胞系sh-sy5y之后,测量tau蛋白磷酸化程度的结果。
图12示出了在使用茯苓皮提取物处理神经细胞系sh-sy5y之后,测量ngf生成程度的结果。
具体实施方式
下面,将详细描述本发明。
本发明涉及用于预防或治疗退行性神经系统疾病的药物组合物,所述药物组合物包含作为活性成分的茯苓(学名:poriacocos)皮提取物。
本发明的茯苓皮提取物可按照制备草药提取物的常规方法来提供,但具体指作为粗提物使用水、醇,或水和醇的混合物获得的提取物。为提取溶剂之一的醇可以是,但并不限于具有1至4个碳原子的低级醇,优选是甲醇、乙醇、丁醇或酒精,更优选是乙醇。在此,“酒精”指通过发酵淀粉原料或糖原料,并且进行蒸馏所产生的乙醇。进一步地,水和醇的混合溶剂不受特别限制,可以以任意期望的比例进行混合。
在本发明的一个实施方式中,茯苓皮提取物可以使用60(v/v)~80%(v/v)的乙醇,65(v/v)~75(v/v)%的乙醇或70(v/v)%的乙醇来提取,但并不限于此。
在具体实施方式中,可以通过如下过程来获得本发明的茯苓皮提取物。首先,洗涤和干燥本发明的茯苓,然后切制干燥的草药以获得切制的草药。将1~20(v/w)倍、优选5~10(v/w)倍的水、具有1至4个碳原子的低级醇或水和具有1至4个碳原子的低级醇(优选70(v/v)%的乙醇)的混合物,添加到干燥的切制茯苓中。在10℃至100℃的温度下,优选在室温下进行1至72小时的提取,优选通过以下方法进行48小时的提取:冷提取、热水提取、超声提取、回流冷却提取、加热提取、超临界提取、使用热水提取法的提取,优选进行一次冷提取,并且在减压下进行浓缩以产生茯苓皮提取物。
本发明的含茯苓皮提取物作为活性成分的组合物可用于治疗退行性神经系统疾病。相应地,本发明提供了含茯苓皮提取物作为活性成分的、用于预防和治疗退行性神经系统疾病的药物组合物,茯苓皮提取物在制备退行性神经系统疾病的治疗剂中的应用,并且提供了通过向个体给予治疗有效量的茯苓皮提取物来治疗退行性神经系统疾病的方法。
如上所述,本发明的退行性神经系统疾病指,由神经细胞(神经元)逐渐发生结构和功能性丢失所引起的心智功能退行性疾病。具体地,它包括选自由阿尔茨海默氏病、克雅二氏病、亨廷顿氏舞蹈病、多发性硬化症、格林-巴利综合征、帕金森氏病、卢伽雷氏病、进行性共济失调和由神经元逐渐死亡所引起的进行性痴呆所组成的组中的疾病。
在本发明的一个实施方式中,用于预防和治疗退行性神经系统疾病的药物组合物基于100重量份的全部药物组合物,可包含作为活性成分的0.01至90重量份、0.1至90重量份、1至90重量份、或10至90重量份的茯苓皮提取物,但并不限于此,可依据疾病的状态、类型和进展的不同而不同。
在本发明的另一实施方式中,含茯苓皮提取物作为活性成分的、用于预防和治疗退行性神经系统疾病的药物组合物可被配制成用于预防和治疗退行性神经系统疾病的药物制剂,该药物制剂包括药学上可接受的载剂、稀释剂或赋形剂。
载剂、赋形剂和稀释剂的实例包括乳糖、右旋糖、蔗糖、山梨醇、甘露醇、木糖醇、赤藓糖醇、麦芽糖醇、淀粉、阿拉伯胶、藻酸盐、明胶、磷酸钙、硅酸钙、纤维素、甲基纤维素、微晶纤维素、聚乙烯吡咯烷酮、水、羟苯甲酯、羟苯丙酯、滑石、硬脂酸镁和矿物油。
另外,本发明的组合物可被配制成如下形式的药物组合物:口服制剂,例如粉剂,颗粒剂,片剂,胶囊,混悬剂,乳剂,糖浆剂和气雾剂;外用制剂,栓剂或无菌注射液。通常来讲,在配制的情况中,可通过使用常用的如填充剂的稀释剂、增量剂、粘结剂、润湿剂、崩解剂、表面活性剂或赋形剂进行制备。口服给药的固体形式的制剂包括片剂、丸剂、粉剂、颗粒剂、胶囊等,可包含至少一种赋形剂,例如淀粉、碳酸钙、蔗糖、乳糖、明胶等。除了简单的赋形剂之外,还可使用润滑剂,例如硬脂酸镁和滑石。除了常用的简单稀释剂如水和液体石蜡之外,口服用液体制剂的实例包括混悬剂、溶液、乳剂和糖浆剂,以及各种赋形剂,例如润湿剂、甜味剂、芳香剂、防腐剂等。肠胃外给药的制剂包括无菌水溶液、非水溶液、混悬剂、乳剂、冻干制剂和栓剂。悬浮剂的实例包括丙二醇,聚乙二醇,植物油如橄榄油,可注射性酯如油酸乙酯,等等。栓剂基质的实例包括外特坡松(witepsol)、聚乙二醇、吐温(tween)61、可可油脂、月桂酯和甘油明胶。
本发明的含茯苓皮提取物作为活性成分的、用于预防和治疗退行性神经系统疾病的药物组合物的剂量可依据患者的年龄、性别和体重的不同而不同。通常,0.1至100mg/kg,优选1至30mg/kg的量可一天给药一次至几次。剂量也可依据给药途径、疾病程度、性别、体重、年龄、健康状态、饮食、给药时间、给药方法、排泄率等增加或减小。相应地,上述用量不是要以任何方式限制本发明的范围。
本发明的含茯苓皮提取物的用于预防和治疗退行性神经系统疾病的药物组合物可以各种途径给予哺乳动物,例如大鼠、小鼠、牲畜和人。可预期所有的给药方式,例如口服给药、直肠或静脉内给药、肌内给药、皮下给药、子宫内硬膜给药或大脑内注射给药。
本发明的茯苓皮提取物的毒副作用小,因此可用于预防目的而安全地长期使用。
本发明还提供了含茯苓皮提取物的食品组合物。茯苓皮提取物抑制导致脑中神经细胞死亡的物质的生成,促进促神经细胞再生和分化的蛋白的表达来保护神经细胞,从而可有效用于生产健康功能性食品和普通食品,该健康功能性食品和普通食品尤其可显示出预防和改善神经退行性疾病的效果。
具体地,本发明所限定的健康功能性食品被定义为:最近通过“2002年对于健康功能性食品的规定”所定义的“在已充分确立了在人体内的功能性和安全性基础上,韩国食品药品管理局的通知2004-12中规定的关于健康功能性食品成分或识别成分的规定的列表上的健康食品”。
本发明的含茯苓皮提取物的食品组合物可用于各种食品中以缓解退行性神经系统疾病症状。可向其中添加本发明的草药提取物的食品是各种食品,例如饮料、口香糖、茶、维生素复合物、健康功能性食品和健康功能性饮料,并且可以丸剂、粉剂、颗粒剂、浸剂、片剂、胶囊或饮料的形式来使用。
茯苓皮提取物在健康食品组合物中的量通常为0.1wt%至15wt%,优选0.2wt%至10wt%,而在健康饮料组合物的情况中,基于100ml可包含0.1g至30g,优选0.2g至5g的茯苓皮提取物。
当本发明的食品组合物制备为饮料形式时,除了以所示比例含所述草药提取物作为必要成分的那些之外,对于液体成分没有特别限制。此外,如普通饮料那样,可添加各种调味剂或天然碳水化合物作为额外的成分。
上述天然碳水化合物的实例包括单糖,例如葡萄糖和果糖;双糖,例如麦芽糖、蔗糖等;多糖;糊精,环糊精等,或糖醇,例如木糖醇、山梨糖醇和赤藓糖醇。除了上面提到的天然香料之外,可有利地使用天然调味剂(甘味料、甜菊提取物(如莱苞迪甙a、甘草甜素等))和合成的香料(糖精、阿斯巴甜等)。天然碳水化合物的比例通常为每100ml完全健康饮料组合物约1g至20g,优选约5g至12g。
除了上面的描述之外,本发明的食品组合物可进一步包括各种添加剂,例如各种营养物、维生素、矿物质(电解质),调味剂例如合成的香料和天然的香料,色素和增稠剂(奶酪、巧克力等),果胶酸及其盐,褐藻酸及其盐,保护胶体增稠剂,ph调节剂,稳定剂,防腐剂,甘油,醇,碳酸饮料中使用的碳酸化剂等。此外,本发明的组合物可包括天然果汁和果肉,用于生产果汁饮品和植物饮品。这些成分可独立使用或组合使用。这些添加剂的比例不受特别的限制,但通常选自每100重量份的本发明的总食品组合物的0至约20重量份的范围内。
在另一实施方式中,本发明是用于预防、改善或治疗退行性神经系统疾病的方法,所述方法包括给予含茯苓皮提取物的活性成分的组合物。或者,本发明提供了茯苓皮提取物在预防、改善或治疗退行性神经系统疾病中的应用。用于所述方法或应用的所述含茯苓皮提取物的组合物的用量、剂型、给药方法等如上所述。
【本发明的实施方式】
将参考下面的实施例和实验,对本发明进行详细的解释。但是,下面的实施例和实验仅是用于示例本发明,本发明的范围并不限于此。
<实施例1>本发明的茯苓皮提取物的制备
在京东(kyungdong)市场的草药店购买干燥的茯苓(poriacocos)皮,去除污染物,将完全干燥的草药用于实验。100g切制的茯苓皮与1l的蒸馏水(dw),或30(v/v)%、50(v/v)%、70(v/v)%或95(v/v)%乙醇水溶液混合,将混合物在室温保持48小时。过滤后,在减压下浓缩混合物,然后进行冻干以获得实施例1的茯苓皮提取物(粗提物)(参见表1)。
【表1】
本发明的茯苓皮提取物的制备
<实验例1>对茯苓皮的记忆改善和神经细胞保护效果的测试
<1-1>实验动物的准备
东莨菪碱诱导的记忆受损(scopolamineinducedmemoryimpairment)模型
六周龄icr小鼠用于本实验,并且每一实验组均由8只动物组成。
在给予茯苓皮提取物和对比药物30分钟之后,腹腔内(i.p)给予1mg/kg东莨菪碱。向正常动物注射相同量的生理盐水。
在给予东莨菪碱30分钟之后,进行行为研究。
aβ灌注模型
六周龄的icr小鼠用于本实验。麻醉动物,固定在立体定位器(stoelting)中,使用hamilton微量注射器(配备有26号针头)注射3ul溶媒(vehicle)(人造csf)或aβ426分钟。
将经aβ42处理的动物随机分成实验组。从给予aβ422天后开始,每天给予一次实验药物和阳性对照药物多奈哌齐(donepezil)连续给药11天。
将冻干的药物,茯苓皮乙醇提取物和对照药物悬浮在3%hpmc水溶液中,所有药物均在实验当天制备。
测量脑中的蛋白
为了检验茯苓皮提取物对神经细胞死亡诱导物或参与细胞保护的物质生成的效力,持续5天给予六周龄icr小鼠茯苓皮提取物和对照药物。在第五天,给药后4小时,处死实验动物并且分离出脑。分离出海马区用于蛋白分析。进行蛋白测定,以量化样品中的总蛋白含量。测量值表示为每单位蛋白的测量值。
<1-2>被动回避测试(passiveavoidancetask)
在两个独立分开的明亮方盒和黑暗方盒中进行被动回避实验。使用50w白炽灯对明亮区域(20×20×20cm)进行照明。明亮区域和黑暗区域(20×20×20cm)相隔1cm,并且安装了2mm不锈钢杆。
在习惯期期间,两个部分通过闸门(5×5cm)分隔开,将实验动物放置在明亮部分中30秒之后,打开闸门。允许动物自由通过。当它们抵达黑暗区域时,关闭闸门,3秒之后拿出动物。
24小时后进行获得实验(acquisitiontrial)。在药物和对照药物给药30分钟后,腹腔内给予1mg/kg东莨菪碱,并且在30分钟之后进行行为实验。实验小鼠最初放置在明亮区域中,30秒之后打开区域之间的门。当实验小鼠进入黑暗区域中时,关闭闸门,通过不锈钢杆立即施加持续2秒,强度为0.5ma的电击(electricalfootshock),测量实验动物进入黑暗区域的时间。
在进行获得试验并且给予了24小时休息时间之后,将实验动物放置在明亮区域中以进行保留试验(retentiontrial),测量直至进入黑暗区域的时间。获得试验和保留试验都测定小鼠的四只爪子全部从明亮房间进入黑暗房间所花费的时间。
结果如图1所示,证实了当口服给予0、30(v/v)%、50(v/v)%、70(v/v)%和95(v/v)%的乙醇茯苓皮提取物时,获得了显著改善空间记忆的效果。最有效的70%乙醇茯苓皮提取物示出了与1mg/kg多奈哌齐(dpz)类似的效力,其中已知多奈哌齐是乙酰胆碱酯酶抑制剂(图1)。
<1-3>y-迷宫测试
进行y-迷宫实验,来研究短期记忆效果。将动物放置在y-迷宫的一个臂上,允许动物自由移动8分钟。测量自发交替和总进入次数。当动物相继进入三个臂时,它们被定义为交替(alternation)进入,通过下面的等式1计算比率。
[等式1]
自发交替率(%)=[(变换次数)/(总进臂数-2)]×100
结果如图2所示,以100mg/kg的药量口服给予0、30(v/v)%、50(v/v)%、70(v/v)%和95(v/v)%的乙醇茯苓皮提取物,改善了东莨菪碱诱导的实验动物模型的空间记忆力,在东莨菪碱诱导的实验动物模型中,记忆形成被抑制。如图4所示,在给予aβ42的阿尔茨海默氏痴呆模型中也恢复了空间记忆力(图2和图4)。
<1-4>新物体识别(nor)测试
在45cm宽、45cm长和50cm高的黑暗盒子内,放置相同尺寸但不同形状的两个塑料物体。允许实验动物自用移动8分钟,测量在每一物体上花费的时间(训练过程)。24小时后,将实验动物放置在具有一个来自训练过程的熟悉物体和一个新物体的盒子中,测量在每一物体上花费的时间(测试过程)。使用下面的等式(2)计算记录的值,表示为新物体的识别结果。
[等式2]
新物体的识别率(%)=在新物体上花费的时间/(在新物体上花费的时间+在有经验的物体上花费的时间)×100
如图3所示,当以100mg/kg的药量口服给予0、30(v/v)%、50(v/v)%、70(v/v)%和95(v/v)%的乙醇茯苓皮提取物时,东莨菪碱诱导的记忆形成被抑制的实验动物模型示出认知记忆得到改善。如图5所示,由于给予aβ42的阿尔茨海默氏痴呆模型也恢复了认知记忆(图3、图5)。
<1-5>免疫组化染色
对于免疫组化染色,向如实验例1-1中所述的aβ灌注动物注入1×pbs(磷酸盐缓冲盐水),经4%多聚甲醛固定,并且摘取脑。将脑在相同的溶液中固定一天,并且保存在30%蔗糖溶液中,4℃中,每两天换一次溶液,直至进行冷冻切片。然后,在冷冻切片机(cryostat)中通过滴加oct(优化的切片温度)化合物,在-20℃使脑组织充分冷冻,然后进行30μm厚的切片,并且在防腐液中储存在4℃。使用海马区进行免疫组化染色。经pbs冲洗过的组织用1%h2o2处理15分钟。之后,组织用0.05mpbs、1.5%常规山羊血清、0.5mg/ml牛血清白蛋白、0.3%tritonx-100和山羊neun一级抗体(1:500)处理,并且为了防止非特异性反应,在4℃反应24小时。在去除一级抗体之后,使组织与缀合过氧化物酶的二级抗体(1:200)反应90分钟,将abc稀释在缓冲液中并在室温反应约1小时。使用pbs冲洗三次之后,使用0.02%dab和0.01%h2o2对组织进行显影,并且进行乙醇和二甲苯脱水来制备玻片样本。
结果如图6所示,当以100mg/kg的药量口服给予茯苓皮的0、30(v/v)%、50(v/v)%、70(v/v)%和95(v/v)%乙醇提取物时,显著增加了因β淀粉样肽毒性而减少的神经元(neun阳性)(图6)。证实了茯苓皮提取物对神经元细胞具有保护效果,能提高记忆力。
<1-6>测量脑中的aβ生成
进行elisa实验来研究茯苓皮提取物对β淀粉样肽生成的抑制效果,其中β淀粉样肽生成已知是导致阿尔茨海默氏病的主要原因。
摘取实验例<1-1>中的正常动物的脑,添加ripa缓冲液并且进行机械均质化。离心后,获取上清液,并且使用β淀粉样肽分析试剂盒(ibl)测量脑中β淀粉样肽的浓度。
结果如图7所示,当口服给予100mg/kg茯苓皮的0、30(v/v)%、50(v/v)%、70(v/v)%和95(v/v)%乙醇提取物时,显著降低了脑中β淀粉样肽的浓度(图7)。上述结果证明了茯苓皮提取物去除了导致阿尔茨海默氏痴呆的β淀粉样肽。
<1-7>ngf(神经生长因子)水平的测量
进行elisa实验来证明茯苓皮提取物对ngf生成的效力,其中ngf已知具有使神经元再生和分化的活性。摘取实验例<1-1>中的正常动物的脑后,分离出海马区,向其中添加ripa缓冲液并且进行机械均质化。对于ngf测量,添加对应于每一脑的重量的高盐高去垢剂缓冲液,并且进行机械均质化。在添加了10ul4nhcl并且静置15分钟之后,使与受体结合的ngf分离,添加4nnaoh,使混合物再静置15分钟。通过离心,取出上清液,并且使用ngf测量试剂盒(millipore)测量脑中的ngf浓度。
结果如图8所示,当口服给予100mg/kg茯苓皮的0、30(v/v)%、50(v/v)%、70(v/v)%和95(v/v)%乙醇提取物时,显著降低了脑中的ngf浓度。这些结果表明茯苓皮提取物通过促进ngf的生成而促进对神经细胞的保护。
<实验例2>证明茯苓皮提取物的体外(invitro)神经细胞的保护效果
<2-1>测量神经细胞系中的乙酰胆碱酯酶(ache)的活性
已经开发并且使用了多种乙酰胆碱酯酶抑制剂,因为这些抑制剂通过增加神经节神经递质中的乙酰胆碱浓度来活化胆碱能神经元,从而增强记忆力并且改善痴呆。测量乙酰胆碱酯酶的活性,来证明茯苓皮提取物的乙酰胆碱酯酶抑制效果。从kclb(韩国细胞系库)购买了sh-sy5y细胞,一种神经细胞系。将sh-sy5y细胞(1×106细胞/孔)接种在六孔培养板上,并且在含10%胎牛血清的dmem/f12(杜尔贝科改良伊格尔培养基,dulbecco'smodifiedeagle'smedium)培养基中培养48小时。使用含10μm视黄酸和3%fbs的dmem/f12培养基分化5天之后,使用10、100μg/ml茯苓皮提取物处理细胞。使用ripa缓冲液(150mmnacl、0.5%tritonx-100、50mmtris-hcl、ph7.4、25mmnaf、20mmegta、1mmdtt、1mmna3vo4、蛋白酶抑制剂鸡尾酒)裂解细胞,并且使用购自pierce的bca试剂对蛋白含量进行定量。按照ellman法,使用乙酰胆碱作为底物来确定乙酰胆碱酯酶的活性。乙酰胆碱酯酶所产生的硫代胆碱与dtnb反应,通过测量405nm的吸光度变化来确定所产生的5-硫代-2-硝基苯甲酸盐。
结果如图9所示,当以10μg/ml的浓度给予神经细胞系茯苓皮的0、30(v/v)%、50(v/v)%、70(v/v)%、95(v/v)%乙醇提取物时,aβ42诱导的乙酰胆碱酯酶活性恢复至正常水平(图9)。
<2-2>神经细胞系中的细胞保护效果
在由人造聚集物aβ42引起对神经细胞系毒性的模型中,使用mtt(3-(4,5-二甲基噻唑-2-基)-2,5-二苯基四氮唑溴盐)测定,来测量茯苓皮提取物的细胞保护效果。将sh-sy5y(1×104细胞/孔)接种在96孔培养板中,并且在含10%胎牛血清的dmem/f12(杜尔贝科改良伊格尔培养基:营养物混合物f-12)培养基中培养48小时。在使用含10μm视黄酸和3%fbs的dmem/f12培养基分化5天之后,使用浓度为0.01、0.1、1、10、100或200ug/ml的茯苓皮提取物处理细胞并且保持6小时。之后,使用aβ42处理并且培养总共48小时。使用2mg/mlmtt处理4小时之后,将formazon溶解在dmso中,并且测量590nm处的吸光度。
如图10所示,在给予10μg/ml茯苓皮的0、30(v/v)%、50(v/v)%、70(v/v)%、95(v/v)%乙醇提取物之后,aβ42诱导的细胞毒性以浓度依赖的方式降低,而且细胞数量增加(图10)。
<2-3>对神经元细胞系中的磷酸化tau蛋白的测量
测量磷酸化tau蛋白的水平,以证明茯苓皮提取物对tau蛋白过磷酸化的抑制效果。将sh-sy5y细胞(1×106细胞/孔)接种在六孔培养板上,并且在含10%fbs(胎牛血清)的dmem/f12(杜尔贝科改良伊格尔培养基)培养基中培养48小时。在使用含10μm视黄酸和3%fbs的dmem/f12培养基分化5天后,使用10或100ug/ml茯苓皮提取物处理6小时,然后经aβ42处理并且培养总共48小时。使用ripa缓冲液裂解细胞之后,使用购自pierce的bca试剂对蛋白含量进行定量。使用购自invitrogen的人tau[ps199]酶联免疫吸附测试(elisa)试剂盒,测量磷酸化的tau蛋白。
如图11所示,当神经元细胞系经10ug/ml茯苓皮的0、30(v/v)%、50(v/v)%、70(v/v)%、95(v/v)%的乙醇提取物处理时,由aβ42诱导的tau蛋白磷酸化被抑制,并且恢复至正常水平。广泛用于痴呆(一种代表性退行性脑病)的多奈哌齐是没有示出对tau蛋白磷酸化的抑制效果(图11)。
<2-4>神经细胞系中的神经生长因子(ngf)水平的测量
测量ngf水平,以确定茯苓皮提取物的认知改善的机制。将sh-sy5y细胞(1×106细胞/孔)接种在六孔培养板上,并且在含10%胎牛血清的dmem/f12(杜尔贝科改良伊格尔培养基)培养基中培养48小时。使用含10μm视黄酸和3%fbs的dmem/f12培养基分化5天之后,使用10或100μg/ml茯苓皮提取物处理细胞。使用ripa缓冲液裂解细胞,并且使用购自pierce的bca试剂对蛋白含量进行定量。使用购自abcam的β神经生长因子人酶联免疫吸附测定(elisa)试剂盒,测量ngf水平。
如图12所示,在使用10ug/ml茯苓皮的0、30(v/v)%、50(v/v)%、70(v/v)%和95(v/v)%的乙醇提取物处理的神经元细胞系中,ngf生成显著增加。广泛用于痴呆(一种典型的退行性脑病)的多奈哌齐是没有示出与ngf相关的效果(图12)。
如上所述,本发明的茯苓皮提取物通过抑制β淀粉样肽的生成和tau蛋白磷酸化(其通过引起神经元细胞死亡而导致退行性脑病)抑制了疾病的发生或进行,并且通过抑制乙酰胆碱酯酶而提高了记忆力。本发明的茯苓皮提取物还促进了ngf的生成,这促进了对神经元的保护和神经分化。因此,本发明可用于预防、改善和治疗由于神经元逐渐死亡而导致的进行性痴呆,不仅可用于如阿尔茨海默氏痴呆的疾病,还可用于克雅二氏病、亨廷顿氏舞蹈病、多发性硬化症、格林-巴利综合征、帕金森氏病和卢伽雷氏病。本发明还可用于预防、改善和治疗退行性神经障碍,包括姿势和运动障碍、进行性共济失调、肌肉萎缩和无力以及感觉和运动障碍。
下文中,将描述本发明实施例1中的含茯苓皮提取物的组合物的制备例,但这仅是是对本发明的详细描述,本发明并不限于此。
制备例1:注射剂的制备
实施例1的提取物..............................100mg
焦亚硫酸钠...................................3.0mg
对羟基苯甲酸甲酯.............................0.8mg
对羟基苯甲酸丙酯.............................0.1mg
注射用无菌蒸馏水.............................适量
通过常规的注射剂制备方法,混合上述成分制成2ml。之后,将混合物填充到2ml安瓿中并且灭菌,以制备成注射剂。
制备例2:片剂的制备
实施例1的提取物.............................200mg
乳糖........................................100mg
淀粉........................................100mg
硬脂酸镁....................................适量
按照常规的片剂制备方法,混合上述组分并且进行压片来制备片剂。
制备例3:胶囊的制备
实施例1的提取物............................100mg
乳糖.......................................50mg
淀粉.......................................100mg
滑石.......................................2mg
硬脂酸镁...................................适量
按照常规的胶囊制备方法,混合上述组分并且填充到明胶胶囊中来制备胶囊。
制备例4:液体剂的制备
实施例1的乙醇提取物........................1000mg
糖...............................................20g
异构糖
柠檬香........................................适量
添加了纯化水之后,总液体体积................100ml
按照生产液体制剂的常规方法混合上述组分,填充在100ml棕色瓶中,灭菌来制备液体制剂。
- 还没有人留言评论。精彩留言会获得点赞!
- SeZn7MT3的组成、制备方法及其在防治阿尔茨海默症中的应用与流程
- 纤维支架材料、其制备方法、及亚甲蓝负载量的调节方法与流程
- 大驳骨在制备预防和/或治疗神经退行性疾病的药物中的应用及药物的制造方法与工艺
- 花叶假杜鹃在制备预防和/或治疗神经退行性疾病的药物中的应用及药物的制造方法与工艺
- 大脑内稳态调节蛋白的组成、制备方法及其在防治阿尔茨海默症中的应用与流程
- 一种药物组合物及其制备方法和在制备防治神经退行性疾病的药物中的应用与流程
- 片层碳‑四氧化三铁复合体在抑制Aβ聚集中的应用的制造方法与工艺
- 一种干细胞球切割收集装置及干细胞球的切割分离传代方法与流程
- 一种具有改善记忆功效的多肽及其分离制备方法和应用与制造工艺
- 治疗或预防神经退行性病症的组合物和方法与制造工艺