UQCRC1激动剂的制作方法
本发明涉及泛醇-细胞色素c还原酶核心蛋白1(ubiquinol-cytochromecreductasecoreprotein1,uqcrc1)激动剂在制备治疗缺血缺氧性心脏病药物中的应用。
背景技术:
心脏是重要的生命器官,心脏规律的收缩和舒张运动能够将氧通过血液循环传输至机体组织,保障机体能量代谢进行,而心脏运动需要消耗大量的atp,因此心肌的能量供应影响到机体生命活动的进行。缺血缺氧导致机体组织细胞获得的氧减少,而氧是机体atp生成的必要因素,缺血缺氧导致心肌细胞atp水平下降,心脏供能不足而导致功能下降,另外缺氧会导致脂质过氧化物如丙二醛(mda)等浓度上升,导致细胞膜和亚细胞膜通透性增加,堆积的脂酰coa,脂肪酸可致心肌细胞死亡,破坏心脏的结构而导致功能下降,最终导致缺血缺氧性心脏病,如心绞痛、心肌梗塞、心肌梗死、高原心脏病等。因此,保护缺血缺氧的心肌细胞是防治缺血缺氧性心脏病的重要治疗策略,对维持机体生命活动具有重要的意义。有研究表明,泛醇-细胞色素c还原酶核心蛋白1(ubiquinol-cytochromecreductasecoreprotein1,uqcrc1)表达上调参与了心肌保护效应。
缺血预处理(ischemiapreconditioning,ipc)是通过触发机体内源性抗损伤机制而增强心肌细胞对缺血缺氧的耐受能力。ipc的保护作用呈双相过程,第一相称为预处理的快速相,出现在预处理的数分钟,持续1-3h。第二相称为预处理的延迟相(secondwindowofprotection,swop),出现在初次缺血后的12-72h。研究结果表明,ipc时心肌保护效果最强的时间位点是在延迟相。uqcrc1是线粒体呼吸链复合体iii上的一个亚单位,具有重要的生理功能。近年来的研究结果表明,uqcrc1的表达改变与大鼠心肌的swop呈正相关。线粒体katp通道是ipc和药物预处理如吗啡、舒芬太尼、七氟醚、异氟醚等延迟预处理的共同“终末效应器”,开放线粒体katp通道是它们产生心肌保护作用的共同信号通路。二氮嗪(diazoxide,dz)是线粒体katp通道的特异性开放剂,通过开放氧糖剥夺(oxygenglucosedeprivation,ogd)模型缺血/再灌注损伤后心肌细胞的线粒体katp通道来实现uqcrc1蛋白表达的上调,使细胞保护性蛋白bcl-2和cox-2等表达增加、bcl-2/bax比率增高,继而抑制caspase-3凋亡信号通路激活,激活akt/gsk-3β细胞保护信号通路,显著增加ogd损伤后的心肌细胞的存活率,从而产生心肌保护作用。采用线粒体katp通道特异性阻滞剂5-羟葵酸(5-hydroxydecanote,5-hd)进行干扰实验,会使二氮嗪预处理时线粒体katp通道关闭,则完全消除二氮嗪延迟预处理后uqcrc1的表达上调,消除swop对心肌细胞bcl-2和cox-2蛋白表达的影响,其心肌保护作用也随之消失。
因此uqcrc1是swop中的保护性蛋白,它可能成为心肌保护的新靶点。提示能够与uqcrc1结合且有激动作用,是能够增强uqcrc1活性的化合物,具有治疗缺血缺氧性心脏病的药理效应,如心绞痛、心肌梗塞、心肌梗死、高原心脏病等。
技术实现要素:
本发明的目的在于提供一种uqcrc1激动剂,并将其应用于制备治疗缺血缺氧性心脏病药物。
本发明的技术方案是:先确定一个uqcrc1的药物口袋。通过计算机辅助,将小分子化合物作用于该药物口袋,进行生物学活性检测。最后用药理学试验予以验证。具体如下:
1)、采用同源建模法确定靶蛋白uqcrc1的结构,确定一个uqcrc1的药物口袋。
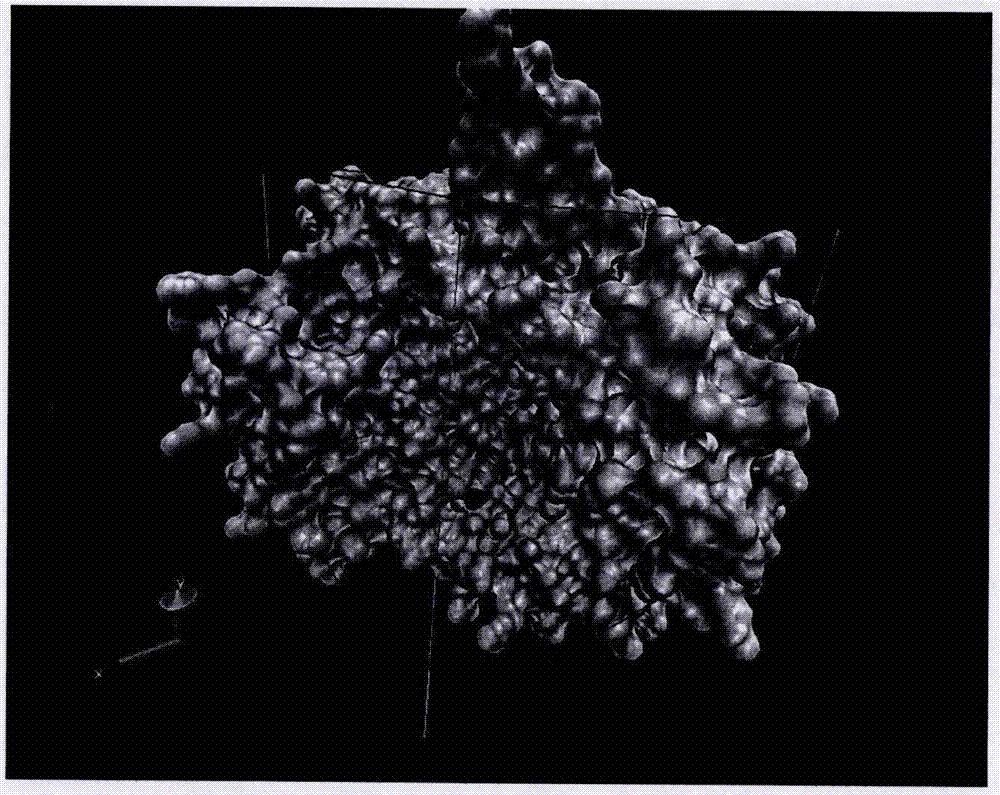
对人、牛的uqcrc1蛋白质进行多序列比对显示,uqcrc1为高度保守的蛋白质,在四个物种间,序列差异很小。由于牛的该蛋白质结构已经解析,因此使用同源建模工具swiss-model,以牛2.26a分辨率的蛋白质晶体结构1fyu为模板,建立人uqcrc1的蛋白质结构模型,如图1所示。
从结构可以看出,uqcrc1蛋白质表面有一个很大的疏水“口袋”,该口袋为该蛋白质与complexsubunit2形成复合物的主要结合部位。因此理论上,作用于该“口袋”的小分子化合物,将对该蛋白质的功能带来影响。
2)使用ledock分子对接程序进行初步活性筛选。
使用vmd1.9.3来处理人uqcrc1蛋白质。先使用lepro_linux_x64程序,去除杂原子,并加极性氢,残基的名字也改为charmm的命名方式。然后在vmd中打开受体蛋白质结构,使用pythom程序boxer计算对接盒子,将口袋中心设为盒子中心,设定边长40a的立方体盒子的空间作为对接盒子,该盒子包含了整个疏水口袋和周边区域。设置好的受体盒子如图2所示。
在高性能计算平台上,使用ledock分子对接程序包来处理受体和配体。使用shell编程,调用lefrag_linux_x64程序,将chemdiv的约170万个化合物分割到15个目录,每个目录下约110000个化合物小分子。准备ligands文件、dock文件,编写sge作业脚本,使用ledock_linux_x64程序,将每个分割包中的小分子分别与受体蛋白质进行分子对接。调用200个cpu进行并行计算。每次对接均计算10个可能的结合位点,对接区域以蛋白质表面疏水口袋为中心,边长40a的立方体盒子。
使用python编程,提取每个小分子对接结果中最优的得分,保存到文本文件中。然后通过matlab程序,从文本文件中筛选出228个对接自由能小于-8kj/mol,对接效率高于0.3的小分子化合物。
3)使用autodock_vina软件进行二次筛选。
首先使用autodocktools1.5.6对人uqcrc1蛋白质进行处理,去掉水分子和杂原子,添加极性氢键,保存为pdtqt格式。对接盒子包含整个蛋白质表面,如图3所示,box设置为边长66a的立方体盒子。
然后从zinc数据库批量下载228个化合物的结构,使用lefrag分割为单个mol2结构的小分子,使用python脚本程序和autodocktools,将mol2格式的小分子转换为pdbqt格式。最后,编写sge作业脚本,提交计算任务到计算节点,使用autodock_vina程序,将228个小分子分别于受体蛋白质进行分子对接。使用shell编程提取对接自由能最低的结果,保存到文本文件。对autodock_vina分子对接结果进行统计和筛选,结果显示在228个化合物中,有24个低于-8.6kj/mol,14个低于-9kj/mol。
4)对接自由能低于-8.6kj/mol的化合物与人uqcrc1具有高亲和力,选择这24个合物作为uqcrc1激动剂,用于制备治疗缺血缺氧性心脏病药物。这24个化合物的化学结构式及其与人uqcrc1的对接自由能如表1所示。
表1:24个化合物与人uqcrc1的对接自由能及其化学结构式
附图说明
图1是人uqcrc1蛋白质cartoon形式的三维结构。
图2是使用vmd1.9.3设置好的人uqcrc1蛋白质受体盒子。
图3是使用autodocktools1.5.6设置好的人uqcrc1蛋白质受体盒子。
具体实施方式
下面结合具体实施例对本发明作进一步说明:
从与人uqcrc1结合亲和力最高的24个化合物选择4个作为实施例,进行药理活性评价。本发明的分子结构有的存在药学上可接受的盐或立体异构体,这些药学上可接受的盐或立体异构体在实施例中未全部说明但不限制本发明。
实施例1
化合物a:compoundid为zinc35429578,纯度为99.5%,化学结构式为
化合物b:compoundid为zinc35429587,纯度为99.7%,化学结构式为
化合物c:compoundid为zinc46031528,纯度为99.6%,化学结构式为
化合物d:compoundid为zinc06193999,纯度为99.8%,化学结构式为
化合物a、b、c、d对缺氧原代心肌细胞的影响实验:
分组与给药:雄性sd大鼠乳鼠70只,单笼喂养3天后,按体重随机分为空白组、模型组、阳性组、给药a组、给药b组、给药c组、给药d组,提取心肌细胞,溶剂对照组和模型对照组给予生理盐水20ul/ml,阳性对照组给予氟桂利嗪20ug/ml,给药a组给予化合物a20ug/ml,给药b组给予化合物b20ug/ml,给药c组给予化合物c20ug/ml,给药d组给予化合物d20ug/ml,正常环境培养5d。
实验方法:将培养好的sd大鼠乳鼠放入75%酒精中浸泡消毒1min,取出后开胸取心脏放入预冷的d-hanks液中。剔除心脏周边的血凝块及纤维组织,置于另一含d-hanks液的小烧杯中,将心脏剪成1mm3左右的碎块。取0.08%胰酶,0.05%ii型胶原酶混合消化液6ml37℃消化6min,加600ul胎牛血清终止消化。200目网筛滤过,1500rpm离心取沉淀后用含1%青链霉素、10%fbs、0.1mmbrdu的dmem完全培养基接种于培养瓶中。37℃、5%的co2饱和湿度下培养贴壁1.5h,收集未贴壁细胞,即为纯度较高的心肌细胞。离心,显微镜下计数后随机接种在24孔板中,每孔放在co2恒温培养箱中培养,培养5d后,更换不含胎牛血清的dmem培养基。空白组在正常氧气浓度为21%的培养箱中培养,模型组、阳性组、给药a组、给药b组、给药c组和给药d组细胞放入温度为37℃,co2浓度为5%,o2浓度为1%的三气培养箱中进行缺氧处理,缺氧时间为8h。缺氧后收集细胞培养上清液,按照试剂盒的要求分别测试乳酸脱氢酶(ldh)、丙二醛(mda)、肌酸激酶(ck)、超氧化物歧化酶(sod)的水平。取余下细胞按凯基细胞凋亡检测试剂盒的要求,用流式细胞仪测试细胞凋亡的情况及用mtt法,在酶联免疫检测仪od490nm处测量各孔的吸光值,计算心肌细胞的活力水平。
检测指标:细胞凋亡指数、细胞活力、细胞上清液酶学指标:ldh、mda、ck、sod。
统计处理:实验数据以均数±标准差
实验结果:见表2和表3。
表2化合物a、b、c、d对缺氧培养大鼠原代心肌细胞活力的影响
注:△p<0.05,△△p<0.01,△△△p<0.001vs模型对照组
表3化合物a、b、c、d对原代缺氧培养大鼠心肌细胞酶学的影响
注:△p<0.05,△△p<0.01,△△△p<0.001vs模型对照组
结果分析与结论:
与空白组相比,模型组细胞活力显著下降,细胞凋亡指数显著上升,模型组细胞培养上清液中ldh、ck、mda含量显著增加,细胞培养上清液中sod含量显著下降,说明缺氧对大鼠原代心肌细胞活力以及心肌细胞酶学产生了影响显著,缺氧导致心肌细胞损伤、凋亡。
与模型组相比较,给药a组、给药b组、给药c组、给药d组大鼠原代培养心肌细胞的细胞活力显著增强,细胞凋亡指数显著下降,lhd、ck、mda浓度显著降低,sod浓度显著增高,说明化合物a、b、c、d对保护缺氧心肌细胞,减轻因细胞坏死造成心肌酶的外溢以及对缺氧引起的氧化应激有较好的保护作用。提示化合物a、b、c、d具有治疗缺血缺氧性心脏病的作用,如心绞痛、心肌梗塞、心肌梗死、高原心脏病等。
- 还没有人留言评论。精彩留言会获得点赞!