二硫化钼‑吲哚菁绿纳米复合颗粒及其制备方法和应用与流程
本发明涉及光声成像造影剂领域,具体涉及一种二硫化钼-吲哚菁绿纳米复合颗粒及其制备方法和应用。
背景技术:
近来,二硫化钼(molybdenumdisulfide,mos2)作为过渡金属硫化物家族中的一员,由于其极佳的电学、光学和半导体特性,引起了物理、化学、材料和生物医药等领域研究人员的极大关注。二硫化钼具有许多优异的特性,例如光学吸收性优于金纳米棒和石墨烯衍生物、良好的生理稳定性和生物相容性、以及对实体肿瘤的epr效应,迅速的被用于生物医学领域。
二硫化钼纳米颗粒自2014年由英国南安普顿大学的研究人员制备成功以来,短短两年多的时间内,已经有研究人员尝试将二硫化钼用作生物医学成像造影剂。尹文艳等人在单层二硫化钼-铯的复合纳米颗粒上装载阿霉素,对小鼠胰腺癌皮下模型进行了光热治疗,治疗后的小鼠肿瘤有明显缩小。刘腾等人将基于二硫化钼-氧化铁的纳米颗粒制备成用于正电子发射型计算机断层成像(pet)、光声成像和磁共振成像的多模态成像探针,对小鼠乳腺癌皮下模型进行光热治疗,取得了较好的效果。本专利发明人所在研究团队采用绿色环保、简单易行的方法,从二硫化钼粉末中制备出单层二硫化钼纳米颗粒,在小鼠原位脑胶质瘤的光声成像中得到了较强的光声信号。
但上述文献的研究主要是将基于二硫化钼的纳米复合材料用于皮下肿瘤的光声成像或光热治疗,并未对位于颅骨下方的原位脑胶质瘤进行研究。虽然有的文献在增强原位脑胶质瘤的光声信号研究方面进行了有益的探索,其制备的单层二硫化钼纳米颗粒的吸收峰值在可见光波长670nm处,然而肿瘤的成像深度仅在颅骨下方约1.8mm处,这是因为可见光穿透颅骨时会产生强烈的光散射,限制了肿瘤区域的成像深度。
技术实现要素:
为解决上述问题,本发明提供了一种二硫化钼-吲哚菁绿纳米复合颗粒。所述二硫化钼-吲哚菁绿纳米复合颗粒的光学吸收峰值红移至近红外波段范围,进一步提高了其成像深度。
本发明第一方面提供了二硫化钼-吲哚菁绿纳米复合颗粒,包括单层的二硫化钼纳米片和吸附在所述单层的二硫化钼纳米片表面的吲哚菁绿。
其中,所述二硫化钼-吲哚菁绿纳米复合颗粒中,所述吲哚菁绿与所述单层的二硫化钼纳米片的质量比为1-5:1。
其中,所述二硫化钼-吲哚菁绿纳米复合颗粒的粒径为100nm-300nm。
其中,所述单层的二硫化钼纳米片的边缘厚度为0.65nm,中间厚度为10.65nm。
本发明第一方面提供的二硫化钼-吲哚菁绿纳米复合颗粒在单层二硫化钼纳米片上装载吲哚菁绿,既能提高吲哚菁绿在体内的稳定性并延长其循环时间,又能实现单层二硫化钼的光学吸收峰的红移,充分利用生物组织对近红外波段光的高穿透性,提高生物组织的光声成像深度。此外,本发明制备的二硫化钼-吲哚菁绿纳米颗粒,硫、钼都是人体必需的微量元素,纳米复合颗粒具有低生物毒性和良好的生物相容性。
本发明第二方面提供了一种二硫化钼-吲哚菁绿纳米复合颗粒的制备方法,包括:
将单层的二硫化钼纳米片溶液和吲哚菁绿溶液混合,得到混合溶液,将所述混合溶液在室温下搅拌5-7小时,得到二硫化钼-吲哚菁绿纳米复合颗粒。
其中,所述混合溶液中,所述吲哚菁绿与所述单层的二硫化钼纳米片的质量比为1-5:1。
其中,所述单层的二硫化钼纳米片溶液的制备方法包括:将二硫化钼粉末和牛血清白蛋白加入到纯水中得到混合液,随后将所述混合液冰浴超声破碎10-15小时,然后以5000-7000转/分的速度离心分离10-15分钟,收集上清液,得到单层的二硫化钼纳米片溶液。
其中,所述吲哚菁绿溶液的制备方法包括:将吲哚菁绿粉末置于有机溶剂中进行溶解,得到吲哚菁绿溶液,所述有机溶剂包括二甲基亚砜。
其中,将搅拌后的混合溶液透析8-12小时,得到二硫化钼-吲哚菁绿纳米复合颗粒。
本发明实施方式第二方面采用物理方法制备二硫化钼-吲哚菁绿纳米复合颗粒,方法绿色环保,操作简单易行。
本发明第三方面提供了一种二硫化钼-吲哚菁绿纳米复合颗粒在制备治疗肿瘤的光声成像造影剂中的应用。
本发明第三方面提供的所述纳米复合颗粒的光学吸收波长范围在近红外波段,从而能够充分利用生物组织对近红外波长光的高穿透性,提高肿瘤的光声成像深度。
综上,本发明有益效果包括以下几个方面:
1、本发明提供的二硫化钼-吲哚菁绿纳米复合颗粒,包括单层的二硫化钼纳米片和吸附在所述单层的二硫化钼纳米片表面的吲哚菁绿。所述纳米复合颗粒的光学吸收波长范围在近红外波段,从而能够充分利用生物组织对近红外波长光的高穿透性,提高原位脑胶质瘤的光声成像深度;
2、本发明提供的二硫化钼-吲哚菁绿纳米复合颗粒的制备方法为物理方法,方法绿色环保,操作简单易行;
3、本发明提供的所述纳米复合颗粒的光学吸收波长范围在近红外波段,从而能够充分利用生物组织对近红外波长光的高穿透性,提高原位脑胶质瘤的光声成像深度,能够很好地用于治疗肿瘤。
附图说明
图1为单层二硫化钼和二硫化钼-吲哚菁绿纳米复合颗粒的紫外可见光吸收光谱图;
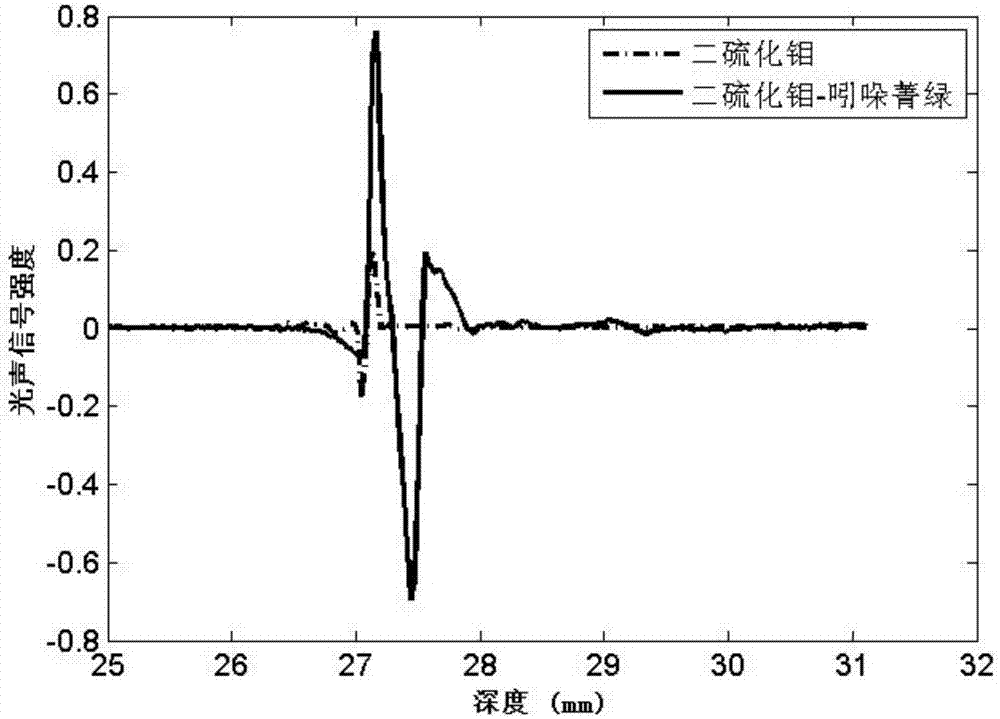
图2为单层二硫化钼和二硫化钼-吲哚菁绿纳米复合颗粒的光声信号强度图;
图3为二硫化钼-吲哚菁绿纳米复合颗粒的粒度直径分布图;
图4为二硫化钼-吲哚菁绿纳米复合颗粒的表征图;其中,图4a为二硫化钼-吲哚菁绿纳米复合颗粒的原子力显微镜外貌表征;图4b为该颗粒的厚度;
图5为二硫化钼-吲哚菁绿纳米复合颗粒用于活体小鼠的原位脑胶质瘤光声成像结果。
具体实施方式
以下所述是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也视为本发明的保护范围。
本发明实施方式第一方面提供了一种二硫化钼-吲哚菁绿纳米复合颗粒,包括单层二硫化钼纳米片和吸附在所述单层二硫化钼纳米片表面的吲哚菁绿。
本发明实施方式中,吲哚菁绿通过静电吸附的作用吸附在单层二硫化钼纳米片的表面。可选地,单层的二硫化钼纳米片的边缘厚度为0.65nm,中间厚度为10.65nm。具体地,单层的二硫化钼纳米片的晶体结构为六角点模式。可选地,所述二硫化钼-吲哚菁绿纳米复合颗粒中,所述吲哚菁绿与所述单层的二硫化钼纳米片的质量比为1-5:1。可选地,所述二硫化钼-吲哚菁绿纳米复合颗粒的粒径为100nm-300nm。可选地,所述二硫化钼-吲哚菁绿纳米复合颗粒的粒径小于或等于200nm。进一步可选地,所述二硫化钼-吲哚菁绿纳米复合颗粒的粒径为100nm-200nm。所述二硫化钼-吲哚菁绿纳米复合颗粒的纳米粒径较小,便于细胞吞噬。可选地,二硫化钼-吲哚菁绿纳米复合颗粒的光学吸收峰值在近红外波段范围。进一步可选地,二硫化钼-吲哚菁绿纳米复合颗粒的光学吸收峰值在780-800nm范围。
本发明在单层二硫化钼纳米片上装载吲哚菁绿,既能提高吲哚菁绿在体内的稳定性并延长其循环时间,又能实现单层二硫化钼的光学吸收峰的红移,充分利用生物组织对近红外波段光的高穿透性,提高生物组织的光声成像深度。此外,本发明制备的二硫化钼-吲哚菁绿纳米颗粒,硫、钼都是人体必需的微量元素,吲哚菁绿是被批准用于临床的成像造影剂,无生物毒副作用。
本发明实施方式中提供的二硫化钼-吲哚菁绿纳米复合颗粒,包括单层的二硫化钼纳米片和吸附在所述单层的二硫化钼纳米片表面的吲哚菁绿。所述纳米复合颗粒的光学吸收波长范围在近红外波段,从而能够充分利用生物组织对近红外波长光的高穿透性,提高原位脑胶质瘤的光声成像深度。并降低组织内源性吸收物质的背景信号干扰;纳米复合颗粒具备足够的稳定性,确保在光声成像时间内不发生特性改变;该纳米复合颗粒具备较高的光学吸收系数,从而获得较高信噪比;同时,纳米复合颗粒具有低生物毒性和良好的生物相容性。
本发明实施方式第二方面提供了一种二硫化钼-吲哚菁绿纳米复合颗粒的制备方法,包括:
将单层的二硫化钼纳米片的溶液和吲哚菁绿溶液混合,得到混合溶液,将所述混合溶液在室温下搅拌5-7小时,形成含有二硫化钼-吲哚菁绿纳米复合颗粒的溶液,即得所述二硫化钼-吲哚菁绿纳米复合颗粒。
本发明实施方式中,混合溶液中,所述吲哚菁绿与所述单层的二硫化钼纳米片的质量比为1-5:1。
本发明实施方式中,所述单层的二硫化钼纳米片溶液的制备方法包括:将二硫化钼粉末和牛血清白蛋白加入到纯水中得到混合液,随后将所述混合液冰浴超声破碎10-15小时,然后以5000-7000转/分的速度离心分离10-15分钟,收集上清液,得到含有单层的二硫化钼纳米片的溶液。具体地,得到上清液后,用移液管小心将上清液进行收集,然后用原子力显微镜和高分辨率透射电镜对上清液进行形态和结构分析,如果上清液中颗粒的边缘厚度约在0.65nm、中间厚度约在10.65nm、晶体结构为六角点模式,即为单层的二硫化钼纳米片,证明上清液即为单层的二硫化钼片溶液。具体地,二硫化钼粉末为购买得到。可选地,所述单层的二硫化钼纳米片溶液浓度为1-2mg/ml。具体单层的二硫化钼纳米片溶液浓度可通过电感耦合等离子体发射光谱仪(icp-oes)测试得到。
本发明实施方式中,所述吲哚菁绿溶液的制备方法包括:将吲哚菁绿粉末置于有机溶剂中进行溶解,得到吲哚菁绿溶液,所述有机溶剂包括二甲基亚砜。具体地,吲哚菁绿粉末为购买得到。可选地,所述吲哚菁绿溶液的浓度为2-4mg/ml。
本发明实施方式中,搅拌方式包括磁力搅拌。
本发明实施方式中,将搅拌后的混合溶液透析8-12小时,得到二硫化钼-吲哚菁绿纳米复合颗粒。吲哚菁绿与单层的二硫化钼经过搅拌吸附后,采用透析袋进行透析,目的在于将溶液中未被二硫化钼吸附的、具有游离状态的吲哚菁绿颗粒过滤掉。
本发明实施方式第二方面采用物理方法制备二硫化钼-吲哚菁绿纳米复合颗粒,方法绿色环保,操作简单易行。
本发明实施方式第三方面提供了一种二硫化钼-吲哚菁绿纳米复合颗粒在制备治疗肿瘤的光声成像造影剂中的应用。可选地,二硫化钼-吲哚菁绿纳米复合颗粒在制备治疗脑胶质瘤的光声成像造影剂中的应用。
本发明第三方面提供的所述纳米复合颗粒的光学吸收波长范围在近红外波段,从而能够充分利用生物组织对近红外波长光的高穿透性,提高原位脑胶质瘤的光声成像深度。并降低组织内源性吸收物质的背景信号干扰;纳米复合颗粒具备足够的稳定性,确保在光声成像时间内不发生特性改变;该纳米复合颗粒具备较高的光学吸收系数,从而获得较高信噪比。
实施例1:
一种二硫化钼-吲哚菁绿纳米复合颗粒的制备方法,包括:
(1)将50mg的二硫化钼粉末和10ml的牛血清蛋白加入到10mg的纯水中,随后将混合液冰浴超声破碎10小时,然后以5000转/分的速度离心分离10分钟,此时二硫化钼混合液分为上清液和沉淀液,用移液管小心将上清液进行收集。
(2)用原子力显微镜和高分辨率透射电镜对上清液进行形态和结构分析,如果上清液颗粒的边缘厚度约在0.65nm、中间厚度约在10.65nm、晶体结构为六角点模式,即为单层二硫化钼纳米片,证明上清液即为单层二硫化钼片溶液。
(3)1mg的吲哚菁绿粉末用500μl的二甲基亚砜溶液进行溶解得到吲哚菁绿溶液,然后将吲哚菁绿溶液加入浓度为1mg/ml的单层二硫化钼片溶液中得到混合溶液,吲哚菁绿与单层的二硫化钼纳米片的质量比为2:1,室温下磁力搅拌5小时、用透析袋透析8小时,得到二硫化钼-吲哚菁绿纳米复合颗粒。
采用纳米粒度分析仪测量二硫化钼-吲哚菁绿溶液的粒径和zeta电位,其纳米颗粒直径小于200nm、zeta电位绝对值在30mv以上为理想值,因为此时纳米颗粒容易进入细胞并且纳米颗粒在水溶液中的稳定性好。
对实施例1制得的二硫化钼-吲哚菁绿纳米复合颗粒的可行性进行了研究,包括:(1)对实施例1制备的二硫化钼-吲哚菁绿纳米颗粒溶液使用光谱仪进行光谱吸收分析。(2)对实施例1制备的二硫化钼-吲哚菁绿纳米颗粒进行光声信号测试。(3)对实施例1制备的二硫化钼-吲哚菁绿纳米颗粒进行纳米粒径尺寸、zeta电位测试和原子力显微镜外貌表征。(4)将实施例1制备的二硫化钼-吲哚菁绿纳米颗粒用于活体小鼠的原位脑胶质瘤光声成像测试。
预实验结果表明:(1)图1为单层二硫化钼和二硫化钼-吲哚菁绿纳米复合颗粒的紫外可见光吸收光谱图。如图1所示,二硫化钼-吲哚菁绿纳米复合颗粒(图中显示为二硫化钼-吲哚菁绿)在近红外波段800nm左右有较窄的强吸收峰;(2)图2为单层二硫化钼和二硫化钼-吲哚菁绿纳米复合颗粒(图中显示为二硫化钼-吲哚菁绿)的光声信号强度图。如图2所示,二硫化钼-吲哚菁绿纳米复合颗粒的光声信号强度要强于单层二硫化钼产生的信号强度;(3)图3为二硫化钼-吲哚菁绿纳米复合颗粒(图中显示为二硫化钼-吲哚菁绿)的粒度直径分布图,如图3所示,二硫化钼-吲哚菁绿纳米复合颗粒的粒径尺寸比较理想,平均粒径小于200nm,此外,zeta电位测量结果也比较理想,zeta电位绝对值大于30mv,此时纳米颗粒容易进入细胞并且纳米颗粒在水溶液中的稳定性好;图4为二硫化钼-吲哚菁绿纳米复合颗粒的表征图;图4a为二硫化钼-吲哚菁绿纳米复合颗粒的原子力显微镜外貌表征。如图4a所示,该颗粒外貌为片状;图4b为该片状颗粒(图中显示为二硫化钼-吲哚菁绿)的厚度。如图4b所示,该颗粒中间厚度约为31nm,这是由于二硫化钼吸附吲哚菁绿导致厚度增加的缘故;(4)图5为二硫化钼-吲哚菁绿用于活体小鼠的原位脑胶质瘤光声成像结果。左图为注射二硫化钼-吲哚菁绿纳米复合颗粒前的光声成像结果,右图为注射二硫化钼-吲哚菁绿纳米复合颗粒后5小时后的光声成像结果,如图5所示,光声信号深度可达颅骨下方2.5mm处。
实施例2:
一种二硫化钼-吲哚菁绿纳米复合颗粒的制备方法,包括:
(1)将50mg的二硫化钼粉末和10ml的牛血清蛋白加入到10mg的纯水中,随后将混合液冰浴超声破碎15小时,然后以7000转/分的速度离心分离15分钟,此时二硫化钼混合液分为上清液和沉淀液,用移液管小心将上清液进行收集。
(2)用原子力显微镜和高分辨率透射电镜对上清液进行形态和结构分析,如果上清液颗粒的边缘厚度约在0.65nm、中间厚度约在10.65nm、晶体结构为六角点模式,即为单层二硫化钼纳米片,证明上清液即为单层二硫化钼片溶液。
(3)1mg的吲哚菁绿粉末用500μl的二甲基亚砜溶液进行溶解得到吲哚菁绿溶液,然后将吲哚菁绿溶液加入浓度为1mg/ml的单层二硫化钼片溶液中得到混合溶液,吲哚菁绿与单层的二硫化钼纳米片的质量比为1:1,室温下磁力搅拌7小时、用透析袋透析12小时,得到二硫化钼-吲哚菁绿纳米复合颗粒。
实施例3:
一种二硫化钼-吲哚菁绿纳米复合颗粒的制备方法,包括:
(1)将50mg的二硫化钼粉末和10ml的牛血清蛋白加入到10mg的纯水中,随后将混合液冰浴超声破碎10小时,然后以6000转/分的速度离心分离12分钟,此时二硫化钼混合液分为上清液和沉淀液,用移液管小心将上清液进行收集。
(2)用原子力显微镜和高分辨率透射电镜对上清液进行形态和结构分析,如果上清液颗粒的边缘厚度约在0.65nm、中间厚度约在10.65nm、晶体结构为六角点模式,即为单层二硫化钼纳米片,证明上清液即为单层二硫化钼片溶液。
(3)1mg的吲哚菁绿粉末用500μl的二甲基亚砜溶液进行溶解得到吲哚菁绿溶液,然后将吲哚菁绿溶液加入浓度为1mg/ml的单层二硫化钼片溶液中得到混合溶液,吲哚菁绿与单层的二硫化钼纳米片的质量比为5:1,室温下磁力搅拌6小时、用透析袋透析10小时,得到二硫化钼-吲哚菁绿纳米复合颗粒。
本发明实施例制备了一种二硫化钼-吲哚菁绿纳米复合颗粒,通过在单层二硫化钼纳米颗粒中装载吲哚菁绿制备成纳米复合颗粒,既能实现单层二硫化钼的光学吸收峰红移至近红外波段,又能提高吲哚菁绿的在体稳定性并延长其体内循环时间,作为光声成像造影剂时最终提高肿瘤区域的光声成像深度。
以上所述实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对本发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。
- 还没有人留言评论。精彩留言会获得点赞!