一种水相“一锅法”合成含异噁唑环结构的物质的方法与流程
本发明涉及有机合成技术领域,具体为一种水相“一锅法”合成含异噁唑环结构的物质的方法。
背景技术:
杂环化合物是提供药物核心骨架的重要物质,异噁唑是一种含氮杂环结构的化合物,广泛用于在有机合成中,是一种重要的有机合成中间体。另外,异噁唑环也是许多抗糖尿病活性分子的重要骨架结构,其衍生物具有葡萄糖苷酶抑制活性,例如:化合物(A),(B),(C)已显示出了一定的抗糖尿病活性。此外,一些含异噁唑环结构的物质具有抑制杂草和土壤细菌生长的效能,因此它在农药和杀虫剂领域具有广泛的应用。
绿色化学是近现代才发展起来的一门重要化学分支,其已在整个化学领域备受关注,是当代解决环境污染问题和实现可持续发展的有效途径,是对环境友好型的化学研究方向。绿色化学的根本目是减少资源消耗和避免有危害的化合物的产生,达到高效,零污染,可持续,经济的目标。据所查文献,之前关于合成含异噁唑环结构物质的相关报道,其合成大都在有机溶剂中进行,且利用无机酸作为催化剂,这些会对环境造成污染,无法达到可持续发展的目的。绿色化学合成要求反应过程中采用无毒无害的试剂、溶剂或催化剂,以达到经济、可持续的应用的要求。而其中水又被认为是最理想的溶剂,因此,以绿色化学的概念来看,开发具有价格低廉、无毒无害和环境友好的方法合成含异噁唑环结构的物质具有重要的意义。
技术实现要素:
本发明的目的在于提供一种水相“一锅法”合成含异噁唑环结构的物质的方法,它能有效的解决背景技术中存在的问题。
为实现上述目的,本发明提供如下技术方案:一种水相“一锅法”合成含异噁唑环结构的物质的方法,包括结构式III所示的芳香醛、结构式IV所示的2-萘酚、结构式V所示的3-氨基-5-甲基异噁唑和结构式VI所示的苯乙酮;将结构式III所示的芳香醛与结构式V所示的3-氨基-5-甲基异噁唑,以及结构式IV所示的2-萘酚(或结构式VI所示的苯乙酮)为原料,在无机盐存在下,利用水为溶剂,于70-95℃反应1-4h,冷却至室温后过滤,粗产品经重结晶即得到产物,其反应通式如下:
其中R1为苯基或取代苯基;分离纯化方式可采用过滤后重结晶等。
进一步,所述R1为苯基,对甲基苯基、对甲氧基苯基、对氯苯基、间硝基苯基。
进一步,所述结构式III所示的芳香醛与结构式IV所示的2-萘酚(或结构式VI所示的苯乙酮)的摩尔比为1:1—1:2,优选为1:1;所述结构式III所示的芳香醛与所述结构式V所示的3-氨基-5-甲基异噁唑的摩尔比为1:1。
进一步,所述无机盐为氯化钠、硝酸钠、氯化锂、硝酸钾或硫酸钠中的一种,优选为氯化锂。
进一步,每1mmol结构式III所示的芳香醛,所需的溶剂水为3mL。
进一步,结构式III所示的芳香醛与无机盐的摩尔比为1:5—1:8,优选为1:6。
进一步,所述反应温度在70-95℃间,优选反应温度为90℃。
进一步,所述反应时间为3h。
与现有技术相比,本发明的有益效果是:本发明方法避免了用无机酸做催化剂时腐蚀设备、污染环境的不足之处,反应溶剂环境友好,易于得到,且终产物容易分离纯化、反应收率较高,达到80%以上。
附图说明
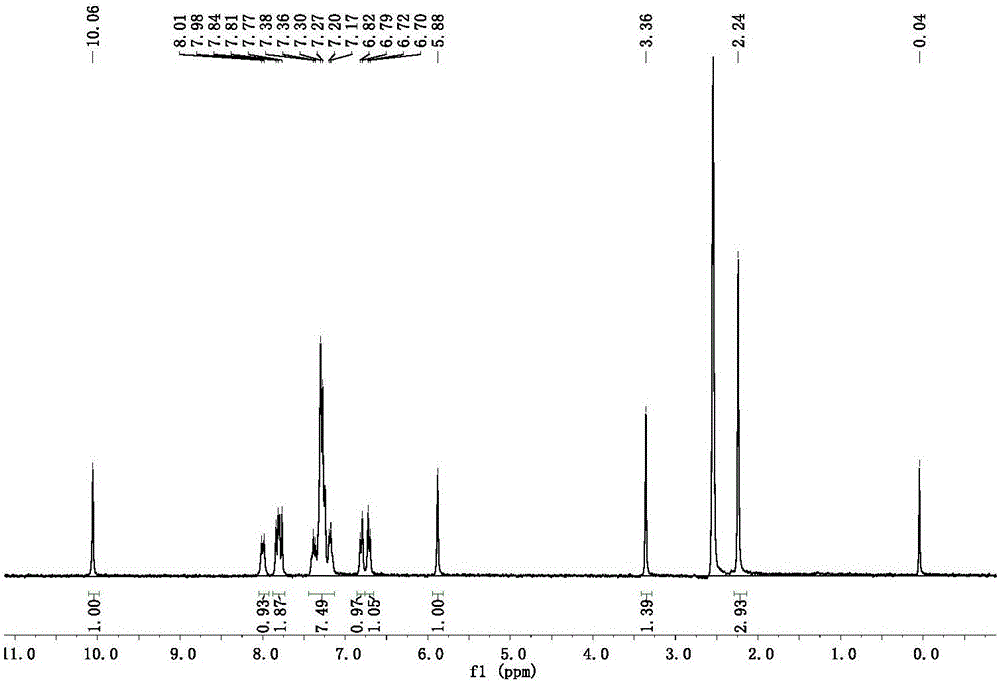
图1为实施例1中化合物I-a的1H NMR图;
图2为实施例1中化合物I-a的13C NMR图。
具体实施方式
下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其它实施例,都属于本发明保护的范围。
一种水相“一锅法”合成含异噁唑环结构的物质的方法,包括结构式III所示的芳香醛、结构式IV所示的2-萘酚、结构式V所示的3-氨基-5-甲基异噁唑和结构式VI所示的苯乙酮;将结构式III所示的芳香醛与结构式V所示的3-氨基-5-甲基异噁唑,以及结构式IV所示的2-萘酚(或结构式VI所示的苯乙酮)为原料,在无机盐存在下,利用水为溶剂,于70-95℃反应1-4h,冷却至室温后过滤,粗产品经重结晶即得到产物,其反应通式如下:
其中R1为苯基或取代苯基;分离纯化方式可采用过滤后重结晶等;所述R1为苯基,对甲基苯基、对甲氧基苯基、对氯苯基、间硝基苯基;所述结构式III所示的芳香醛与结构式IV所示的2-萘酚(或结构式VI所示的苯乙酮)的摩尔比为1:1—1:2,优选为1:1;所述结构式III所示的芳香醛与所述结构式V所示的3-氨基-5-甲基异噁唑的摩尔比为1:1;所述无机盐为氯化钠、硝酸钠、氯化锂、硝酸钾或硫酸钠中的一种,优选为氯化锂;每1mmol结构式III所示的芳香醛,所需的溶剂水为3mL;结构式III所示的芳香醛与无机盐的摩尔比为1:5—1:8,优选为1:6;所述反应温度在70-95℃间,优选反应温度为90℃;所述反应时间为3h。
实施例一:
取0.14g(1mmol)2-萘酚,0.1mL(1mmol)苯甲醛和0.10g(1mmol)3-氨基-5-甲基异噁唑,并将它们加入到装有搅拌子的10mL反应瓶中,再向其中加入0.50g(6mmol)LiCl,3mL蒸馏水。将混合物升温至90℃,并在此温度反应3h,瓶中有淡红色固体析出。待此混合物静置冷却至室温,过滤,用水洗涤,得粗产品,用丙酮重结晶,干燥,得白色颗粒晶体,产率90%。
1H NMR(400MHz,DMSO-d6,TMS)δ:10.06(s,1H),8.0(d,J=9.0Hz,1H),7.84-7.77(m,2H),7.38-7.17(m,7H),6.82-6.70(m,2H),5.88(s,1H,-CHNH),3.3(s,1H,-NH),2.24(s,3H,-CH3);13C NMR(100MHz,DMSO-d6,TMS)δ:168.00,165.19.153.41,143.86,132.85,129.79,129.26,129.20,128.59,126.86,126.69,124.38,123.05,122.84,120.64,119.08,94.68,53.26,12.74。
得到的白色颗粒晶体的结构式为:(I-a)
实施例二:
取2.09g(5mmol)对甲基苯甲醛,0.73g(5mmol)2-萘酚和0.50g(5mmol)3-氨基-5-甲基异噁唑,并将它们加入到装有搅拌子的50mL反应瓶中,再加入2.5g(30mmol)LiCl和15mL蒸馏水。将混合物升温至90℃,并在此温度反应3h。待此混合物静置冷却至室温,过滤,用丙酮重结晶,得粉红色颗粒晶体,产率82%。
1H NMR(400MHz,DMSO-d6)δ10.05(s,1H),8.02(d,J=7.7Hz,1H),7.81-7.75(m,2H),7.37(s,1H),7.30–7.16(m,4H),7.07(d,J=8.0Hz,2H),6.79(d,J=7.8Hz,1H),6.70(d,J=7.7Hz,1H),5.88(s,1H),2.24(s,3H),2.21(s,3H);13C NMR(100MHz,DMSO)δ167.89,165.21,153.02,140.64,135.49,132.80,129.52,129.09,128.96,127.85,126.63,126.59,124.06,122.77,120.59,118.93,94.39,52.92,21.66,13.27。
得到的粉红色颗粒晶体的结构式为:(I-b)
实施列三:
取2.18g(5mmol)4-甲氧基苯甲醛,0.72g(5mmol)2-萘酚和0.50g(5mmol)3-氨基-5-甲基异噁唑,并将它们加入到50mL反应瓶中,再加入2.5g(30mmol)LiCl和15mL蒸馏水。将混合物升温至90℃,并在此温度反应3h。待此混合物静置冷却至室温,过滤,用丙酮重结晶,得淡黄色颗粒晶体,产率75%。
1H NMR(400MHz,DMSO)δ10.05(s,1H),8.02(d,J=7.7Hz,1H),7.81-7.75(m,2H),7.37(s,1H),7.30–7.16(m,4H),7.07(d,J=8.0Hz,2H),6.79(d,J=7.8Hz,1H),6.70(d,J=7.7Hz,1H),5.88(s,1H),2.19(s,3H),2.08(s,3H);13C NMR(100MHz,DMSO)δ167.73,166.01,157.77,153.50,135.93,132.56,129.49,129.09,128.96,127.79,126.55,122.81,120.46,118.93,113.80,94.49,55.63,52.93,31.04,12.57。
得到的淡黄色颗粒晶体的结构式为:(I-c)
尽管已经示出和描述了本发明的实施例,对于本领域的普通技术人员而言,可以理解在不脱离本发明的原理和精神的情况下可以对这些实施例进行多种变化、修改、替换和变型,本发明的范围由所附权利要求及其等同物限定。
- 还没有人留言评论。精彩留言会获得点赞!