复合负载生长因子微球的3D打印支架及其制备方法与流程
本发明属于生物医学领域,尤其涉及一种复合负载生长因子微球的3d打印支架及其制备方法。
背景技术:
运动损伤、炎症、肿瘤和自然退化造成软骨缺损。软骨缺损后自身修复能力有限,特别是关节软骨,损伤后不能自行愈合。据估计,仅在美国,到2020年,就将有4千万相关的软骨缺损病例。中国是人口大国,在膝关节镜检查的人群中,软骨损伤的发病率在61-68%之间,并且呈现逐年增加的趋势。目前临床上常用的治疗方法主要有微骨折术、自体软骨细胞移植和人工关节置换等,这些修复方法各有缺点。组织工程的兴起为软骨缺损修复研究提供了一个新的方向。在体外构建人工软骨的过程中,面临诸多问题,如活性生长因子的长期稳定缓释、细胞行为的调控和支架孔隙结构及尺寸的精确控制。其中,生长因子的长期稳定缓释是体外构建人工软骨的一个关键问题。特别是诱导干细胞向软骨细胞分化构建人工软骨过程中,需要生长因子发挥长期稳定的作用。
快速成型技术又称3d打印技术(3dp)。低温快速成型制造技术(ldm)是基于快速成型技术原理,结合相分离法的一种新型快速成型技术。3dp的发展为复合缓释微球支架的制备提供了新的选择。它制备支架的过程,与其他快速成型技术不同之处在于其成型腔内温度被控制在-30℃左右,喷头挤出的溶液在低温下快速凝结,并且喷头在计算机控制下按程序运动,打印层通过层层叠加最终使支架成型为三维结构,最后,冻结的支架经过冷冻干燥去除溶剂后成型为三维多孔支架。与其他常用的快速成型技术相比,ldm在处理材料过程中对材料的性质和结构没有损坏,属于绿色制造的范围。
目前,有研究者尝试利用3d打印技术,通过程序设计,打印过程中把药物包裹在药片内,可以实现多种药物同时给药,但是这种方法适于大剂量给药。有研究者活性生长因子吸附在ldm打印三维支架上,结果表明活性生长因子会很快缓释,使支架失去长期诱导组织再生能力。利用ldm成型支架过程不需要加热的特点,研究者尝试把活性分子直接和溶液混合后打印,而这会造成活性分子的突释,并且依然难以解决长期稳定释放的问题。
技术实现要素:
本发明的目的在于提供一种复合负载生长因子微球的3d打印支架及其制备方法,旨在解决现有ldm成型支架难以解决生长因子长期稳定释放的问题。
本发明是这样实现的,一种复合负载生长因子微球的3d打印支架的制备方法,包括以下步骤:
提供负载生长因子的复合微球和合成生物材料溶液,将所述负载生长因子的复合微球加入所述合成生物材料溶液,搅拌均匀形成合成生物材料/微球溶液;
使用ldm系统的cark软件设计三维复合材料支架的打印参数,依次连接料罐、送料管、喷头,将所述合成生物材料/微球溶液倒入料罐内;待成型室温度降至-25~-35℃时,启动温控、数控,使用所述cark软件设置造型参数开始打印造型,层层叠加形成一个三维冻结支架;将所述三维冻结支架取出后进行冷冻干燥处理,得到复合负载生长因子微球的3d打印支架。
以及,一种由上述方法制备获得的复合负载生长因子微球的3d打印支架,所述复合负载生长因子微球的3d打印支架为合成生物材料和负载生长因子的复合微球制成的三维多孔支架。
本发明提供的复合负载生长因子微球的3d打印支架的制备方法,所述负载生长因子的复合微球为生物因子的缓释提供了一层基本保障;进一步的,将负载生长因子的复合微球与合成生物材料溶液混合后,采用ldm技术制备三维多孔复合支架,使支架具有可控的一级孔径尺寸和结构,不仅赋予所述支架具有优异的力学性能支撑,而且所述负载生长因子的复合微球在所述合成生物材料中整体均匀分散,同时所述合成生物材料对所述负载生长因子的复合微球进行局部包裹,为生长因子的突释设置了通行障碍,从而为生长因子的稳定长期缓释提供了双层保障。此外,本发明通过ldm技术精确控制支架一级孔隙的尺寸,赋予所制备支架中尺寸在10-50μm左右的相互连通的次级孔隙,从而为生长因子的稳定缓慢持久释放提供了有效的通道。
本发明提供的复合负载生长因子微球的3d打印支架,不仅具有良好的力学性能,而且所述合成生物材料对所述负载生长因子的复合微球进行局部包裹,为生长因子的突释设置了双层通行障碍,从而赋予所述复合负载生长因子微球的3d打印支架优异的稳定缓释性能。
附图说明
图1是本发明实施例提供的制备负载tgf-β1的coli/cs复合微球的流程示意图;
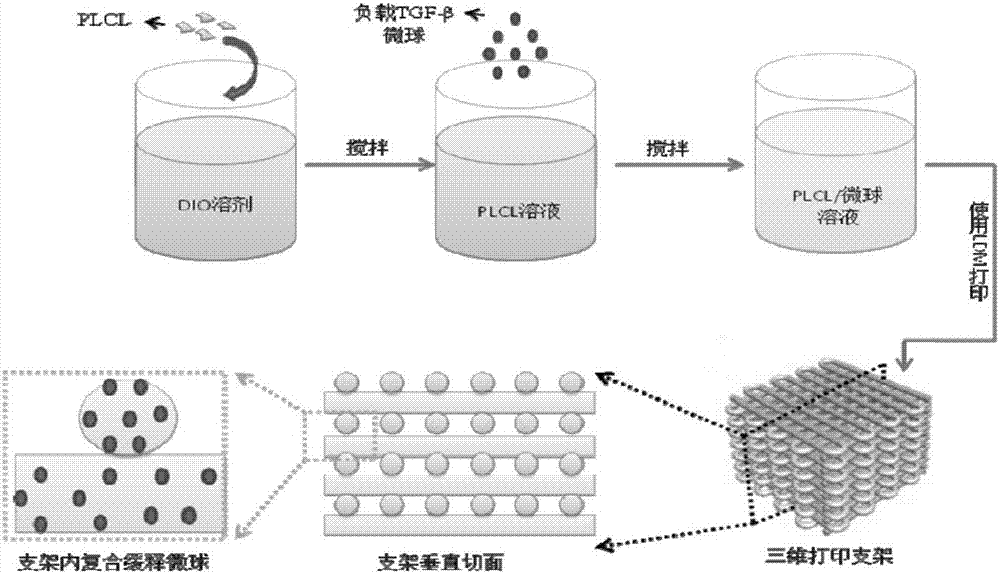
图2是本发明实施例提供的复合负载生长因子微球的3d打印支架的制备方法的流程示意图。
具体实施方式
为了使本发明要解决的技术问题、技术方案及有益效果更加清楚明白,以下结合实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。
本发明实施例提供了一种复合负载生长因子微球的3d打印支架的制备方法,包括以下步骤:
s01.提供负载生长因子的复合微球和合成生物材料溶液,将所述负载生长因子的复合微球加入所述合成生物材料溶液,搅拌均匀形成合成生物材料/微球溶液;
s02.使用ldm系统的cark软件设计三维复合材料支架的打印参数,依次连接料罐、送料管、喷头,将所述plcl/微球溶液倒入料罐内;待成型室温度降至-25~-35℃时,启动温控、数控,使用所述cark软件设置造型参数开始打印造型,层层叠加形成一个三维冻结支架;将所述三维冻结支架取出后进行冷冻干燥处理,得到复合负载生长因子微球的3d打印支架。
上述步骤s01中,本发明实施例中,所述负载生长因子的复合微球中的微球为天然材料制成的微球层,从而能够保证所述3d支架的生物相容性。优选的,所述天然材料包括天然高分子蛋白和多糖。具体优选的,所述天然材料包括胶原蛋白(coli)、硫酸软骨素(cs)、壳聚糖(ch)、丝素(sf)、透明质酸(ha)、海藻酸钠(sa)中的一种或两种。进一步的,生长因子与微球结合形成负载生长因子的复合微球,赋予良好的缓释性能。其中,所述生长因子包括但不限于转化生长因子(tgf)、骨形态发生蛋白(bmp)、胰岛素样生长因子(igf)。更进一步地,当采用两种所述天然材料时,一种天然材料与所述生长因子混合形成微球,另一种天然材料可交联在微球表面形成网络结构,进一步提高了缓释效果。
本发明实施例所述负载生长因子的复合微球中的微球可采用多种方法制备获得,包括电喷法、水包油法。作为一个具体实施例,结合图1,所述负载生长因子的复合微球可以通过下述方法制备获得:以0.5mol/l的稀醋酸为溶剂,配置浓度为13mg/ml的coli溶液,然后按10μg/l的量加入tgf-β1并搅拌混匀,得到coli/tgf-β1溶液;把coli/tgf-β1溶液加入针管后,在27g的针头上连接高压发生器的正极,设置推进速率为26ml/h,电压为18kv,coli/tgf-β1溶液被推进泵挤出后,在高压静电作用下向下方喷射;液滴用质量体积比为0.1%的cs溶液接收,形成负载tgf-β1的coli/cs微球;将负载tgf-β1的coli/cs微球移出后,用浓度为0.25%的戊二醛交联30min,微球取出洗去残留ga后冷冻干燥,得到负载tgf-β1的coli/cs复合微球。由此得到的负载生长因子的复合微球,将tgf-β1与coli溶液混合后喷入cs溶液中形成负载tgf-β1的coli/cs微球,将活性生长因子(tgf-β1)的微球外壳包裹一层cs网络结构,为tgf-β1的稳定缓释提供第一层保障,具有良好的球状形态和结构,且缓释性能较好,降解时间可长达8周。当然,应当理解,这只是制备一种具体的负载生长因子的复合微球的其中一种方法,并不用于限定本发明。
本发明实施例所述负载生长因子的复合微球具有良好的球状形态和结构,且缓释性能较好。但是,若以所述述负载生长因子的复合微球作为支架材料主体制备生物支架,则所得到的生物支架由于缺乏足够的力学性能,难以和周围缺损组织良好整合,因此可利用性差。有鉴于此,本发明实施例将所述负载生长因子的复合微球和合成生物材料溶液混合制备支架,提高上述复合微球制备的生物支架的力学性能。
优选的,所述合成生物材料/微球溶液中,所述负载生长因子的复合微球的质量浓度为0.001-1000mg/ml,具体根据不同生长因子的性质和使用对象进行调节。
优选的,所述合成生物材料溶液的质量浓度百分比优选为8-20wt%,从而可以保证合适的粘度、使得ldm打印能够顺利成型。进一步优选的,所述合成生物材料为左旋乳酸-己内酯共聚物(plcl)、乳酸-羟基乙酸共聚物(plga)、聚乳酸(pla)、聚左旋乳酸(plla)、聚羟基脂肪酸(pha)、聚羟基乙酸或聚乙交酯(pga)、聚乙烯醇(pva)的至少一种。作为一个具体实施例,以1,4-二氧六烷(dio)为溶剂,配制浓度为13wt%的plcl溶液。
作为优选实施例,在将所述负载生长因子的复合微球加入所述合成生物材料溶液前,将所述负载生长因子的复合微球进行过筛处理,筛目为10-60目,以便ldm打印能够顺利进行。
上述步骤s02中,采用计算机辅助建模、分层及堆积。具体的,利用ldm系统的cark软件,设计支架的打印参数。然后,依次连接料罐、送料管、喷头,将所述plcl/微球溶液倒入料罐内,冰箱制冷,准备成型。待成型室温度降至-25~-35℃左右,启动温控、数控,开始造型。在软件控制下,喷嘴软件设置的运动轨迹及造型参数在x、y轴上进行扫描并挤压喷出溶液,溶液在成型室内的低温下,迅速凝固。当第一层打印结束,成型平台在z轴上下降一定高度,喷嘴继续进行打印新的一层,层层叠加形成一个三维冻结支架。成型后处于冻结状态的支架迅速取出后放置进冷冻干燥机中,固化的有机溶剂如1,4-二氧六环(dio)升华,与支架发生气固相分离,从而去除有机溶剂,复合负载tgf-β的3d打印支架最终成型。其中,冷冻干燥的时间为70-80h,优选为72h。以plcl的dio、图1制备的负载tgf-β1的coli/cs复合微球为例,制备复合负载生长因子微球的3d打印支架的流程示意图如图2所示。
作为一个优选实施例,所述造型参数设置为:支架规格为23.6×23.6×23.6cm3,成型温度在-30℃左右,喷嘴直径0.6mm,喷丝间距0.8mm,扫描速度22mm/s,喷头速度1.0~2.0mm/s。
本发明实施例为保证生长因子长期稳定缓释,除了将生长因子包裹于微球内外,还进步一包裹支架材料,从而形成多重保护,具有长期稳定的缓释行为。具体的,在复合负载生长因子微球的3d打印支架成型后生长因子的复合微球均匀分布在合成生物材料内,为生长因子的突释设置了通行障碍,从而为生长因子的稳定长期缓释提供第二层的保障。此外,所述复合负载生长因子微球的3d打印支架的材料均为可降解材料,具有较高的安全性和良好的生物相容,且支架结构具有可控的孔径和孔隙结构。
本发明实施例提供的复合负载生长因子微球的3d打印支架的制备方法,所述负载生长因子的复合微球为生物因子的缓释提供了一层基本保障;进一步的,将负载生长因子的复合微球与合成生物材料溶液混合后,采用ldm技术制备三维多孔复合支架,使支架具有可控的一级孔径尺寸和结构,不仅赋予所述支架具有优异的力学性能支撑,而且所述负载生长因子的复合微球在所述合成生物材料中整体均匀分散,同时所述合成生物材料对所述负载生长因子的复合微球进行局部包裹,为生长因子的突释设置了通行障碍,从而为生长因子的稳定长期缓释提供了双层保障。此外,本发明通过ldm技术精确控制支架一级孔隙的尺寸,赋予所制备支架中尺寸在10-50μm左右的相互连通的次级孔隙,从而为生长因子的稳定缓慢持久释放提供了有效的通道。
以及,本发明实施例还提供了一种由上述方法制备获得的复合负载生长因子微球的3d打印支架,所述复合负载生长因子微球的3d打印支架为合成生物材料和负载生长因子的复合微球制成的三维多孔支架。
作为一个具体实施例,一种由上述方法制备获得的复合负载生长因子微球的3d打印支架,所述复合负载生长因子微球的3d打印支架为plcl和负载tgf-β1的coli/cs复合微球制成的单位多孔支架,其中,所述负载tgf-β1的coli/cs复合微球包括tgf-β1与coli形成的混合微球,以及所述混合微球表面包裹的cs,且所述cs与所述coli交联结合形成表面网络结构。优选的所述复合负载生长因子微球的3d打印支架的cs网络结构、以及plcl的整体均匀分散和局部包裹,为生长因子tgf-β1的突释设置了双层通行障碍,从而赋予所述复合负载生长因子微球的3d打印支架优异的稳定缓释性能。
本发明实施例提供的复合负载生长因子微球的3d打印支架,不仅具有良好的力学性能,而且所述合成生物材料对所述负载生长因子的复合微球进行局部包裹,为生长因子的突释设置了双层通行障碍,从而赋予所述复合负载生长因子微球的3d打印支架优异的稳定缓释性能。
以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!
- 一种阿法替尼有关物质的分离检测方法与流程
- 用于检测人血清中HER2含量的ELISA试剂盒、使用方法及用途与流程
- 用于预防或治疗皮疹的药物组合物的制造方法与工艺
- 用于汽车内饰表皮的30ST/R双面布的制造方法与工艺
- 检测EGFR耐药性突变的方法和组合物与制造工艺
- 一种肝素结合表皮生长因子的单域抗体及其应用的制造方法与工艺
- 3‑[(3‑{[4‑(4‑吗啉基甲基)‑1H‑吡咯‑2‑基]亚甲基}‑2‑氧代‑2,3‑二氢‑1H‑吲哚‑5‑基)甲基]‑1,3‑噻唑烷‑2,4‑二酮和EGFR TYR激酶抑制剂的组合的制造方法与工艺
- 一种二甲苯磺酸拉帕替尼片剂及其制备方法与制造工艺
- 苯并咪唑衍生物作为ERBB酪氨酸激酶抑制剂用于治疗癌症的制造方法与工艺
- 包含STP和生长因子的活性组合物及其化妆品或护肤品的制造方法与工艺
- UCP1在人重组FGF21蛋白活性检测中的应用的制造方法与工艺
- UCP3在人重组FGF21蛋白活性检测中的应用的制造方法与工艺
- 原核表达载体及rbFGF‑2表达方法与工程菌和应用与流程
- 一种利用鱼卵母细胞提取物诱导成纤维细胞重编程为成骨细胞样细胞的试剂盒及方法与流程
- 控制影响角化细胞和/或成纤维细胞和真皮的皮肤失调和皮肤老化的组合产品和美容组合物的制造方法与工艺
- 在CHO细胞中rhIL‑12表达系统的构建方法与制造工艺
- 人皮肤成纤维细胞诱导为神经细胞的方法与应用与制造工艺
- 一种制备人皮肤成纤维细胞膜片的细胞培养基和使用方法与制造工艺
- 检测人FGFR3基因突变的引物组及其试剂盒的制造方法与工艺
- 一种氧调控性碱性成纤维细胞生长因子修饰细胞的方法与制造工艺