一种引物组合物及其应用的制作方法
本发明涉及生物技术领域,涉及医学分子诊断及生物技术,具体涉及一种引物组及其应用,尤其涉及一种用于肥厚型心肌病相关致病基因热点突变的检测的引物组合物及其应用。
背景技术:
肥厚型心肌病(HCM)为一种最常见的遗传性心脏疾病,主要表现为左心室或双心室不对称性肥厚,较少患者表现出左室流出道梗阻。主要病理特征为心肌细胞弥漫性肥大、畸形、核大、深染和心肌纤维紊乱等。HCM临床表现从无征兆到呼吸困难、晕厥、胸痛甚至发生心源性猝死和致命性的心律失常。
HCM是第一个从遗传角度阐明病因的遗传性心脏疾病。1990年在一个加拿大家族性肥厚型心肌病患者中发现第一个致病基因MYH7,其遵循的是常染色体显性遗传模式。HCM的全球发病率和年死亡率分别约为1/500和1%。相关证据表明,Zou等人随机抽查中国9个省的成年人8080人,其中男性4064人,女性4016人,并对其进行超声心动图检测,结果表明中国人群患HCM的概率大约为0.8/500。实际上,超声心动图对肥厚型心肌病的检测为一种患病后的诊断方式,还存在更多潜在的HCM患者,依此推断,中国人群中至少存在200万HCM患者。该病也是是青少年和年轻运动员猝死的最主要原因之一,Morn等人对1986-2006年猝死的1886名美国年轻运动员进行统计分析发现,死亡的主要原因为心血管疾病1056名,占约56%,其中HCM的患者就占据了36%。
众多研究表明,HCM主要由肌节基因突变所致,故HCM又称为肌小节疾病。HCM主要遵循常染色体显性遗传模式,大约有50%的HCM患者为家族性遗传,称为家族性肥厚型心肌病(FHCM)。对HCM患者进行基因检测和家族筛 查能够为临床诊断提供重要的指导作用,主要体现为:1)产前诊断,指导优生优育;2)辅助明确诊断,进行临床干预;3)家族筛查,进行家族疾病发生风险评估及管理。
目前,遗传疾病基因突变的检测方法较多,如:限制性片段长度多太性、单链构象多态性、高分辨率溶解曲线分析、荧光定量PCR的检测方法、PCR扩增直接测序和高通量测序。上方法各有优缺点,毛细管电泳技术是基因突变检测的金标准,但因其对设备的要求高、价格昂贵等缺点,很难从实验室普及到临床,荧光定量PCR具有快速、简便、经济和准确等特点。
CN 102965428A公开了一种检测遗传性心肌肥厚相关基因突变样品制备试剂盒。该试剂盒采用探针捕获测序,与其他传统的DNA芯片杂交和毛细管电泳测序技术一样,不仅费时费力,而且价格昂贵,根本不能满足对HCM的基因检测。
值得一提的是TaqMan-MGB荧光定量PCR的检测方法,该方法与传统的TaqMan不同的是在探针的3’端连接了非荧光的猝灭基团MGB(minor groove binder,MGB),当探针序列与模板结合时,MGB能高度结合于DNA双链的小沟,增加了寡核苷酸探针和单链模板结合的稳定性,由此通过缩短探针序列长度,增加探针序列的特异性,实现了能区分一个碱基的差别。当具有5’-3’外切酶活性的DNA聚合酶对碱基进行延伸时,可把发光基团解离下来,解除了非荧光的猝灭基团对发光基团的抑制,实现了荧光信号的积累与PCR产物的同步进行,从而能较好的区分野生型、纯合突变和杂合突变样本。TaqMan-MGB对单核苷酸多态性检测方面有较多的应用,如:慢性骨髓增殖性疾病、病原微生物的耐药突变检测和肿瘤细胞P53基因突变等。
CN 104388595 A公开了一种猪圆环病毒2型实时荧光定量 PCRMGB-TaqMan探针检测方法,该方法利用荧光定量PCR技术,采用MGB探针,建立了猪圆环病毒2型(PCV2)检测方法。但目前MGB探针还未用于HCM的检测。
因此,为肥厚型心肌病建立一种简便、快速、经济和准确的突变筛查方法,为肥厚型心肌病的预防、辅助临床诊断和预后评估提供技术平台显得尤为重要。
技术实现要素:
针对现有技术的不足及实际的需求,本发明提供了一种引物组及其应用,本发明通过所述引物组可以构建阳性野生型和纯合突变型五个热点突变位点(MYH7-c.1987C>T、TNNI3-c.370G>C、MYH7-c2155C>T、TNNI3-c.433C>G和PRKAG2-c.298G>A)的载体,应用ABI7500实时荧光PCR仪,对每个阳性样品同时进行联合检测,建立一种简便、快速、准确和经济的肥厚型心肌病基因突变检测方法,为肥厚型心肌病的临床早期诊断和预防提供了新的技术平台。
为达到上述目的,本发明采用以下技术方案:
第一方面,本发明提供一种引物组合物,所述引物组合物包括检测MYH7-c.1987C>T、TNNI3-c.370G>C、MYH7-c2155C>T、TNNI3-c.433C>G或PRKAG2-c.298G>A这五个热点突变位点的五组实时荧光PCR引物和Taqman-MGB探针序列中的至少一组。
优选地,所述检测MYH7-c.1987C>T热点突变位点的实时荧光PCR引物的核酸序列如SEQ ID NO.1-2所示,所述Taqman-MGB探针的核酸序列如SEQ ID NO.3-4所示;
优选地,所述检测TNNI3-c.370G>C热点突变位点的实时荧光PCR引物的核酸序列如SEQ ID NO.5-6所示,所述Taqman-MGB探针的核酸序列如SEQ ID NO.7-8所示;
优选地,所述检测MYH7-c2155C>T热点突变位点的实时荧光PCR引物的核酸序列如SEQ ID NO.9-10所示,所述Taqman-MGB探针的核酸序列如SEQ ID NO.11-12所示;
优选地,所述检测TNNI3-c.433C>G热点突变位点的实时荧光PCR引物的核酸序列如SEQ ID NO.13-14所示,所述Taqman-MGB探针的核酸序列如SEQ ID NO.15-16所示;
优选地,所述检测PRKAG2-c.298G>A热点突变位点的实时荧光PCR引物的核酸序列如SEQ ID NO.17-18所示,所述Taqman-MGB探针的核酸序列如SEQ ID NO.19-20所示。
具体的序列如下所示:
优选地,所述Taqman-MGB探针的核酸序列5’端标记有发光的报告荧光基团,3’端标记有不发光的淬灭基团MGB。
优选地,所述发光的报告荧光基团为FAM、HEX或Cy5中的任意一种。
优选地,所述不发光的淬灭基团为MGB小分子化合物。
第二方面,本发明提供一种试剂盒,所述试剂盒包括权利要求1-3中任一项所述的引物组合物中的五组实时荧光PCR引物和Taqman-MGB探针序列中的至少一组。
第三方面,本发明提供一种如第一方面所述的引物组合物或如第二方面所述的试剂盒用于肥厚型心肌病相关致病基因热点突变的检测。
第四方面,本发明提供一种肥厚型心肌病相关致病基因热点突变的检测方法,包括如下步骤:
(1)提取基因组;
(2)以步骤(1)的基因组为模板,进行PCR扩增,构建野生型、纯合突变型及杂合突变型阳性质控品;
(3)将步骤(2)得到的阳性质控品采用如第一方面所述的引物组合物进行实时荧光PCR检测。
优选地,步骤(1)所述的基因组来自于人的外周血、心肌组织、淋巴器官、脾脏、骨髓或肝脏中的任意一种或至少两种的组合。
优选地,步骤(2)所述的PCR扩增的引物的核酸序列如SEQ ID NO.21-30所示,所述PCR扩增的引物的核酸序列如下:
优选地,步骤(2)所述的PCR扩增的反应条件为:95℃预变性3分钟;95℃变性30秒,57℃退火30秒,72℃延伸1分钟,共40个循环;72℃延伸5分钟;
优选地,构建阳性质控品的具体步骤如下:将PCR扩增产物进行纯化,将纯化后的片段克隆到PMD-18T载体上,转化到大肠杆菌JM109,挑选单克隆,测序验证野生型及纯合突变型阳性质粒,将野生型和纯合突变型阳性质粒按摩尔比1:1混合后即得到杂合突变型阳性质控品。
优选地,步骤(3)所述的实时荧光PCR的条件中检测MYH7-c.1987C>T热点突变位点的反应体系为:Premix Ex Taq酶5μL,50×的Rox DyII缓冲液0.1μL,上下游引物各0.2μL,Taqman-MGB探针SEQ ID NO.3 0.2μL,Taqman-MGB探针SEQ ID NO.4 1μL,基因组0.5μL和ddH2O为2.8μL;
优选地,步骤(3)所述的实时荧光PCR的条件中检测MYH7-c.1987C>T热点突变位点的PCR反应条件为循环外95℃预变性30s,循环内95℃变性5s、56℃退火及延伸34s、45个循环,循环外60℃延伸1min;
优选地,步骤(3)所述的实时荧光PCR的条件中检测TNNI3-c.370G>C热点突变位点的反应体系为:Premix Ex Taq酶5μL,50×的Rox DyII缓冲液0.1μL, 上下游引物各0.2μL,Taqman-MGB探针SEQ ID NO.7 0.1μL,Taqman-MGB探针SEQ ID NO.8 1.2μL,基因组0.5μL和ddH2O为2.7μL;
优选地,步骤(3)所述的实时荧光PCR的条件中检测TNNI3-c.370G>C热点突变位点的PCR反应条件为循环外95℃预变性30s,循环内95℃变性5s、56℃退火及延伸34s、45个循环,循环外60℃延伸1min;
优选地,步骤(3)所述的实时荧光PCR的条件中检测MYH7-c2155C>T热点突变位点的反应体系为:Premix Ex Taq酶5μL,50×的Rox DyII缓冲液0.1μL,上下游引物各0.2μL,Taqman-MGB探针SEQ ID NO.11 0.2μL,Taqman-MGB探针SEQ ID NO.12 1.2μL,基因组0.5μL和ddH2O为2.6μL;
优选地,步骤(3)所述的实时荧光PCR的条件中检测MYH7-c2155C>T热点突变位点的PCR反应条件为循环外95℃预变性30s,循环内95℃变性5s、56℃退火及延伸34s、45个循环,循环外60℃延伸1min;
优选地,步骤(3)所述的实时荧光PCR的条件中检测TNNI3-c.433C>G热点突变位点的反应体系为:Premix Ex Taq酶5μL,50×的Rox DyII缓冲液0.1μL,上下游引物各0.2μL,Taqman-MGB探针SEQ ID NO.15 0.2μL,Taqman-MGB探针SEQ ID NO.16 0.8μL,基因组0.5μL和ddH2O为3μL;
优选地,步骤(3)所述的实时荧光PCR的条件中检测TNNI3-c.433C>G热点突变位点的PCR反应条件为循环外95℃预变性30s,循环内95℃变性5s、56℃退火及延伸34s、45个循环,循环外60℃延伸1min;
优选地,步骤(3)所述的实时荧光PCR的条件中检测PRKAG2-c.298G>A热点突变位点的反应体系为:Premix Ex Taq酶5μL,50×的Rox DyII缓冲液0.1μL,上下游引物各0.2μL,Taqman-MGB探针SEQ ID NO.19 0.1μL,Taqman-MGB探针SEQ ID NO.20 0.5μL,基因组0.5μL和ddH2O为3.8μL;
优选地,步骤(3)所述的实时荧光PCR的条件中检测PRKAG2-c.298G>A热点突变位点的PCR反应条件为循环外95℃预变性30s,循环内95℃变性5s、56℃退火及延伸34s、45个循环,循环外60℃延伸1min。
与现有技术相比,本发明具有如下有益效果:
(1)本发明一次可检测多个病例样本,且可对每个样本同时进行5个突变位点的联合检测,具有简便、快速、准确和经济等特点,为肥厚型心肌病的临床早期分子诊断和预防建立了新的方法;
(2)本发明方法可用于产前诊断,指导优生优育,辅助明确诊断,进行临床干预,家族筛查,进行家族疾病发生风险评估及管理。
(3)本发明的方法方便快捷,成本低,利用96孔PCR反应管一次性检测多个样本,每个样本可联合检测5个突变位点。
附图说明
图1是本发明阳性质控品TNNI3,c.370G>C菌液PCR琼脂糖凝胶电泳图;
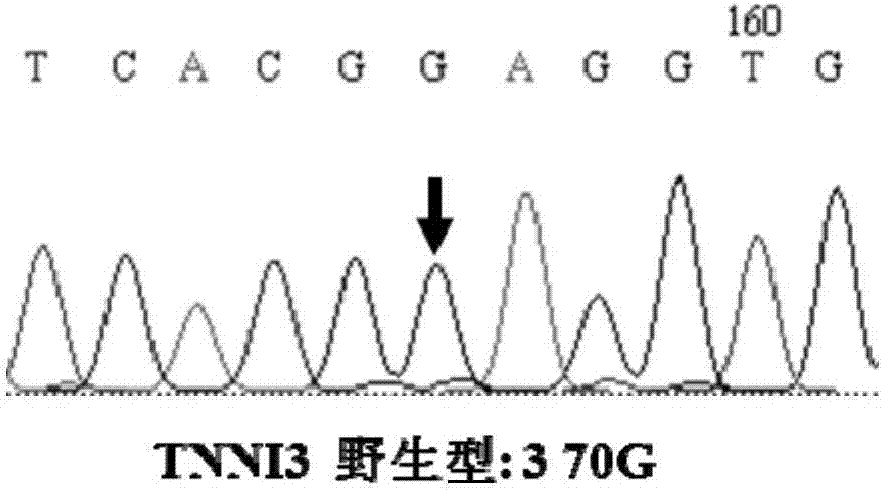
图2是本发明阳性质控品TNNI3,c.370G毛细管电泳检测;
图3是本发明阳性质控品TNNI3,c.370C毛细管电泳检测;
图4是本发明阳性质控品TNNI3,c.433C>G菌液PCR琼脂糖凝胶电泳图;
图5是本发明阳性质控品TNNI3,c.433C毛细管电泳检测;
图6是本发明阳性质控品TNNI3,c.433G毛细管电泳检测;
图7是本发明阳性质控品MYH7,c.2155C>T菌液PCR琼脂糖凝胶电泳图;
图8是本发明阳性质控品MYH7,c.2155C毛细管电泳检测;
图9是本发明阳性质控品MYH7,c.2155T毛细管电泳检测;
图10是本发明阳性质控品MYH7,c.1987C>T菌液PCR琼脂糖凝胶电泳图;
图11是本发明阳性质控品MYH7,c.1987C毛细管电泳检测;
图12是本发明阳性质控品MYH7,c.1987T毛细管电泳检测;
图13是本发明阳性质控品PRKAG2,c.298G>A菌液PCR琼脂糖凝胶电泳图;
图14是本发明阳性质控品PRKAG2,c.298G毛细管电泳检测;
图15是本发明阳性质控品PRKAG2,c.298A毛细管电泳检测;
图16 TaqMan-MGB的灵敏性检验,其中,图16(A)-图16(B)分别为MYH7,1987CC基因型的扩增曲线和标准曲线,图16(C)-图16(D)分别为MYH7,1987TT的扩增曲线和标准曲线;
图17变异位点MYH7,1987C>T的TaqMan-MGB特异性检测,其中,FAM代表野生型探针,HEX代表突变型探针,图17(A)为野生型模板,图17(B)为纯合突变型模板,图17(C)为杂合突变模板,图17(D)为不同基因型的散点图分布;
图18 TaqMan-MGB的灵敏性检验,其中,图18(A)-图18(B)分别为TNNI3,370GG基因型的扩增曲线和标准曲线,图18(C)-图18(D)分别为TNNI3,370CC的扩增曲线和标准曲线;
图19变异位点TNNI3,370G>C的TaqMan-MGB特异性检测,其中,FAM代表野生型探针,HEX代表突变型探针,图19(A)为野生型模板,图19(B)为纯合突变型模板,图19(C)为杂合突变模板,图19(D)为不同基因型的散点图分布;
图20 TaqMan-MGB的灵敏性检验,其中,图20(A)-图20(B)分别为MYH7,2155CC基因型的扩增曲线和标准曲线,图20(C)-图20(D)分别为MYH7,2155TT的扩增曲线和标准曲线;
图21变异位点MYH7,2155C>T的TaqMan-MGB特异性检测,其中,FAM 代表野生型探针,Cy5代表突变型探针,图21(A)为野生型模板,图21(B)为纯合突变型模板,图21(C)为杂合突变模板,图21(D)为不同基因型的散点图分布;
图22 TaqMan-MGB的灵敏性检验,其中,图22(A)-图22(B)分别为TNNI3,433CC基因型的扩增曲线和标准曲线,图22(C)-图22(D)分别为TNNI3,433GG的扩增曲线和标准曲线;
图23变异位点TNNI3,433C>G的TaqMan-MGB特异性检测,其中,FAM代表野生型探针,HEX代表突变型探针,图23(A)为野生型模板,图23(B)为纯合突变型模板,图23(C)为杂合突变模板,图23(D)为不同基因型的散点图分布;
图24 TaqMan-MGB的灵敏性检验,其中,图24(A)-图24(B)分别为PRKAG2,298GG基因型的扩增曲线和标准曲线,图24(C)-图24(D)分别为PRKAG2,298AA的扩增曲线和标准曲线;
图25变异位点PRKAG2,298G>A的TaqMan-MGB特异性检测,其中,FAM代表野生型探针,HEX代表突变型探针,图25(A)为野生型模板,图25(B)为纯合突变型模板,图25(C)为杂合突变模板,图25(D)为不同基因型的散点图分布。
图26 10例已知基因型的肥厚型心肌病患者进行实时荧光检测。图26(A)-图26(E)分别代表MYH7,c.1987C>T、TNNI3,c.370G>C、MYH7,c.2155C>T、TNNI3,c.433C>G及PRKAG2,c.298G>A 5个变异位点的基因分型散点图。
具体实施方式
为更进一步阐述本发明所采取的技术手段及其效果,以下结合附图并通过具体实施方式来进一步说明本发明的技术方案,但本发明并非局限在实施例范 围内。
实施例1
应用本发明方法对在云南省第一人民医院心血管内科临床确诊的5例肥厚型心肌病先证者(除收集HCM患者的人口统计学资料外,还收集了其心电图及超声心动图)外周血基因组进行实时荧光PCR的突变筛查,寻找可能的与HCM发病相关的致病性变异位点。
一种肥厚型心肌病相关致病基因热点突变的检测方法,包括如下步骤:
(1)提取基因组:对入选临床确诊的肥厚型心肌病5例先证者,抽取其外周静脉血1ml,EDTA抗凝后,采用商业化的Miniprep Kit(Axygen,美国)提取其全基因组后,进行琼脂糖凝胶电泳后、对浓度和OD值进行测定,OD260/280为1.8-2.0之间为可用。;
(2)以步骤(1)的基因组为模板,进行PCR扩增,构建野生型、纯合突变及杂合突变阳性质控品;
其中,步骤(2)所述的PCR扩增的引物的核酸序列如SEQ ID NO.21-30所示,具体如下:
,PCR扩增的反应条件如下:
,PCR扩增反应完成后,进行琼脂糖凝胶电泳,电泳结果显示目的片段大小与预期大小一致,结果如图1、4、7、10和13分别代表携带有TNNI3,c.370G>C;TNNI3,c.433C>G;MYH7,c.2155C>T;MYH7,c.1987C>T和PRKAG2,c.298G>A突变位点的PCR扩增产物琼脂糖凝胶电泳图;
构建野生型、纯合突变及杂合突变阳性质控品的具体步骤如下:将纯化后的片段克隆到PMD-18T载体上,转化到大肠杆菌JM109,挑选单克隆,测序验证野生型和纯合突变型阳性质粒,将野生型和纯合突变型阳性质粒按摩尔比1:1混合后即得到杂合突变型阳性质控品;
(3)将步骤(2)得到的阳性质控品采用所述的引物组合物进行实时荧光PCR检测,所述引物组合物如下:
具体各个热点突变位点的反应体系如下:
5个热点突变位点(MYH7-c.1987C>T、TNNI3-c.370G>C、MYH7-c2155C>T、TNNI3-c.433C>G或PRKAG2-c.298G>A)的实时荧光PCR反应条件均为:利用ABI7500实时荧光PCR仪,循环外95℃预变性30s,循环内95℃变性5s、56℃退火及延伸34s、45个循环,循环外60℃延伸1min。
实施例2
应用本发明方法对在云南省第一人民医院心血管内科临床确诊的5例肥厚型心肌病先证者(除收集HCM患者的人口统计学资料外,还收集了其心电图及超声心动图)外周血基因组进行实时荧光PCR的突变筛查,寻找可能的与HCM 发病相关的致病性变异位点。
一种肥厚型心肌病相关致病基因热点突变的检测方法,包括如下步骤:
(1)提取基因组:对入选临床确诊的肥厚型心肌病5例先证者,抽取其外周静脉血1ml,EDTA抗凝后,采用商业化的Miniprep Kit(Axygen,美国)提取其全基因组后,进行琼脂糖凝胶电泳后、对浓度和OD值进行测定,OD260/280为1.8-2.0之间为可用;
(2)以步骤(1)的基因组为模板,进行PCR扩增:其中,步骤(2)所述的PCR扩增的引物的核酸序列如SEQ ID NO.21-30所示,具体如下:
,PCR扩增的反应条件如下:
,PCR扩增反应完成后,进行琼脂糖凝胶电泳并进行纯化;
(3)PCR产物经琼脂糖凝胶DNA纯化试剂盒纯化后,用PMD-18T载体 进行T-A克隆后,筛选出阳性克隆菌株,提取其质粒载体。
(4)利用ABI3130毛细管电泳仪对含有克隆目的片段后的质粒载体进行毛细管电泳,其检测反应体系为:模板DNA 1μL,引物(3.2pmol/uL)1μL,BigDye(2.5x)8μL,ddH2O 10μL;
(5)克隆载体毛细管电泳PCR反应条件如下
(6)以靶基因MYH7(GenBank:NG_007884.1)、TNNI3(GenBank:NG_007866.2)和PRKAG2(GenBank:NG_007486.1)的基因序列为模板,利用bioedit序列分析软件对变位点进行分析。
结果如图2、3、5、6、8、9、11、12、14和15,可以看出,全部成功构建野生型和突变型的阳性质控品,
实施例3
经条件优化,步骤(4)所述的引物-探针的序列的重复性验证,分别进行3次重复试验(批间和批内重复)。观察模板的Ct值,并计算其变异系数,变异系数(p)=标准偏差(SD)/平均数(X),测试检测方法的灵敏性和重复性。
结果如表1-2所示:
表1
表2
从表1-2可见,批间和批内重复变异系数均小于2%,具有较好的批间和批内重复性。
实施例4
经条件优化,步骤(4)所述的引物-探针的序列的特异性验证。
特异性验证以5个变异位点的野生型、纯合突变型和杂合突变型的阳性质粒为模板,同时加入双标记探针,按照优化好的条件对其进行TaqMan-MGB的特异性实验验证,结果如图16-25所示。
结果显示:图16-25(A)野生型样本反应的曲线表现为野生型探针产生的荧光信号增高,而纯合突变无荧光信号或仅有很低的荧光信号;图16-25(B) 杂合突变样本能使野生型和突变型探针都表现出相对较高的荧光信号;图16-25(C)纯合突变表现为只有突变型探针产生荧光信号,图16-25(D)野生型探针不产生荧光信号或产生较少的荧光信号。更重要的是,通过反应结果的散点图可以明显看出不同基因型的样本单独成簇。
实施例5
本发明中,对来自于已知(Sanger测序)基因型的10例肥厚型心肌病患者进行该5个热点突变位点进行突变检测。图26(A-E)分别代表MYH7,c.1987C>T、TNNI3,c.370G>C、MYH7,c.2155C>T、TNNI3,c.433C>G及PRKAG2,c.298G>A 5个变异位点的基因分型散点图。检测结果与Sanger测序结果一致,准确率为100%,具体基因型检测结果比例见表3所示。
表3
综上所述,由实施例5的结果分析可得出,本发明建立了肥厚型心肌病主要致病基因的简便、快速、准确和经济的遗传筛查方法。
申请人声明,本发明通过上述实施例来说明本发明的详细方法,但本发明并不局限于上述详细方法,即不意味着本发明必须依赖上述详细方法才能实施。所属技术领域的技术人员应该明了,对本发明的任何改进,对本发明产品各原料的等效替换及辅助成分的添加、具体方式的选择等,均落在本发明的保护范围和公开范围之内。
SEQUENCE LISTING
<110> 昆明理工大学
<120> 一种引物组合物及其应用
<130> 2017
<160> 30
<170> PatentIn version 3.3
<210> 1
<211> 18
<212> DNA
<213> 人工合成序列
<400> 1
cctccagccc catgtctg 18
<210> 2
<211> 20
<212> DNA
<213> 人工合成序列
<400> 2
taggagaacg ggaacacggt 20
<210> 3
<211> 15
<212> DNA
<213> 人工合成序列
<400> 3
aagaccagcc ccggc 15
<210> 4
<211> 15
<212> DNA
<213> 人工合成序列
<400> 4
aagaccagcc ccagc 15
<210> 5
<211> 22
<212> DNA
<213> 人工合成序列
<400> 5
gaccttcgag gcaagtttaa gc 22
<210> 6
<211> 17
<212> DNA
<213> 人工合成序列
<400> 6
cagcgcctgc atcatgg 17
<210> 7
<211> 14
<212> DNA
<213> 人工合成序列
<400> 7
accctgcgga gagt 14
<210> 8
<211> 14
<212> DNA
<213> 人工合成序列
<400> 8
accctgggga gagt 14
<210> 9
<211> 21
<212> DNA
<213> 人工合成序列
<400> 9
tggccacagg aaaatctgaa c 21
<210> 10
<211> 20
<212> DNA
<213> 人工合成序列
<400> 10
tgtggcctca cctggagact 20
<210> 11
<211> 14
<212> DNA
<213> 人工合成序列
<400> 11
caacttgcgc tcca 14
<210> 12
<211> 15
<212> DNA
<213> 人工合成序列
<400> 12
ccaacttgtg ctcca 15
<210> 13
<211> 22
<212> DNA
<213> 人工合成序列
<400> 13
gtgtggacaa ggtggatgaa ga 22
<210> 14
<211> 20
<212> DNA
<213> 人工合成序列
<400> 14
ccaagtccca gccatctcac 20
<210> 15
<211> 17
<212> DNA
<213> 人工合成序列
<400> 15
aagaacatca cggaggt 17
<210> 16
<211> 17
<212> DNA
<213> 人工合成序列
<400> 16
aagaacatca cgcaggt 17
<210> 17
<211> 19
<212> DNA
<213> 人工合成序列
<400> 17
cccaaccgca tcctctacg 19
<210> 18
<211> 20
<212> DNA
<213> 人工合成序列
<400> 18
gagctctggt gcaccctcat 20
<210> 19
<211> 14
<212> DNA
<213> 人工合成序列
<400> 19
cttccggcag aggt 14
<210> 20
<211> 15
<212> DNA
<213> 人工合成序列
<400> 20
acttctggca gaggt 15
<210> 21
<211> 21
<212> DNA
<213> 人工合成序列
<400> 21
gcagaatcca tgtccacctg t 21
<210> 22
<211> 21
<212> DNA
<213> 人工合成序列
<400> 22
tgtcctagga ggtcctgttc c 21
<210> 23
<211> 22
<212> DNA
<213> 人工合成序列
<400> 23
aggtctccct gtttttggtt cc 22
<210> 24
<211> 25
<212> DNA
<213> 人工合成序列
<400> 24
ggaccttcat gtacctcttt gctct 25
<210> 25
<211> 25
<212> DNA
<213> 人工合成序列
<400> 25
gctaatcagt gacaaagcca ggatc 25
<210> 26
<211> 23
<212> DNA
<213> 人工合成序列
<400> 26
agggtggaag agccaacagt agc 23
<210> 27
<211> 24
<212> DNA
<213> 人工合成序列
<400> 27
gcctaagccg ggaagagact ggta 24
<210> 28
<211> 24
<212> DNA
<213> 人工合成序列
<400> 28
gaggacccct tactagctgc ttct 24
<210> 29
<211> 24
<212> DNA
<213> 人工合成序列
<400> 29
cagtcctgtg tggtcagaac ttgg 24
<210> 30
<211> 24
<212> DNA
<213> 人工合成序列
<400> 30
ggaccagaag gattacgctt tgat 24
- 还没有人留言评论。精彩留言会获得点赞!
- 一种荧光定量PCR技术检测意大利蜜蜂王浆主蛋白MRJP 2基因表达的方法与流程
- 一种用于对不同银杏进行基因分型的SNP引物及检测方法与流程
- 用于基因甲基化检测的引物和探针、采样方法、试剂盒与流程
- 一种基于荧光PCR检测ESR1基因突变的引物及探针的制造方法与工艺
- 转基因甜菜GTSB77品系特异性实时荧光PCR检测引物、探针、方法和试剂盒与流程
- 一种基于单核苷酸多态性的葡萄球菌种水平鉴定和菌株分型一体化方法与流程
- 一套毛花猕猴桃和中华猕猴桃物种间杂交子代的鉴定引物的制造方法与工艺
- 检测黄杉大小蠹的引物、试剂盒及检测方法与流程
- 环介导等温扩增技术检测铜绿假单胞菌的引物和试剂盒的制造方法与工艺
- 一种用于鉴定浙贝母的引物对及其应用的制造方法与工艺