一种治疗丙型肝炎病毒药物的制备方法和用途与流程
本发明属于细胞免疫学、分子生物学领域,涉及一种全人源的单克隆抗体药物,尤其涉及一种全人源抗丙型肝炎病毒的单克隆中和抗体药物。另外,本发明还涉及该中和抗体药物的制备方法和用途。
背景技术:
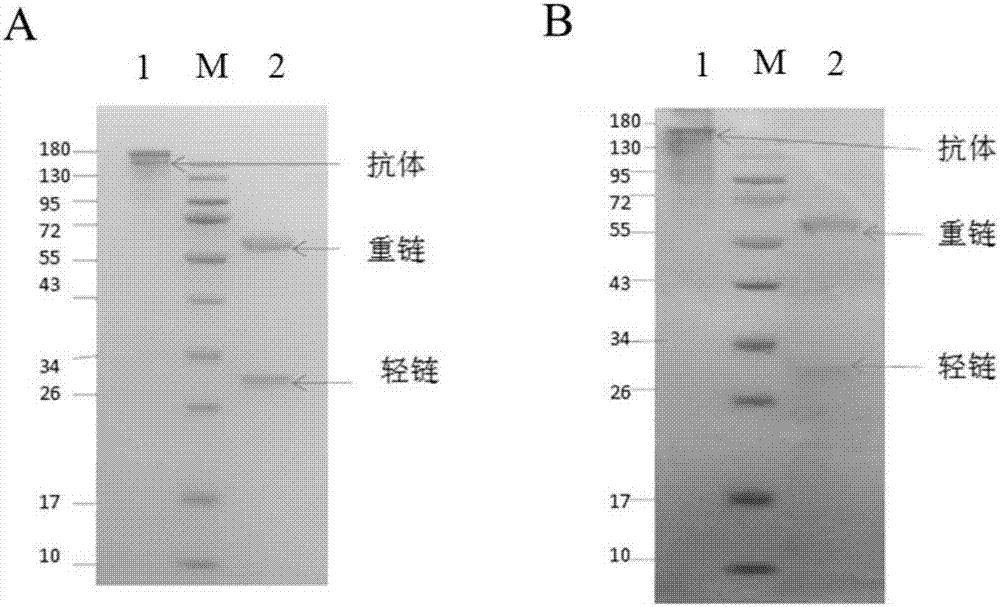
:丙型肝炎由丙型肝炎病毒(hcv)感染所致,主要由血液/体液传播。据世界卫生组织估计,全球有1.7亿人感染hcv。在我国健康人群抗hcv阳性率为0.7%~3.1%,约3800万人。由于病毒生物学特点和宿主免疫功能等多方面因素,机体免疫往往难以有效清除病毒,致使约50%~80%hcv感染者发展为慢性肝炎,其中20%~30%将发展成肝硬化。肝硬化患者中每年有1%~4%发展成为肝细胞癌症。目前,针对丙型肝炎的治疗药物有干扰素、核苷类似物、多肽类药物及中草药、以及小分子药物等,每种药物虽具有不同程度的疗效,但均未能彻底根除hcv。随着研究的发展,治疗性抗体成为了丙型肝炎治疗的新方向。治疗性抗体是近年来增长势头较强劲的生药产品,至目前为止,已有约30种单克隆抗体获批上市用于多种疾病的诊断和治疗。在各种急慢性病毒性肝炎的治疗及研究中,单克隆抗体的应用尤为广泛且具有不可替代的作用。就发展进程而言,单克隆抗体可分为鼠源性单抗、鼠源抗体人源化以及全人源性单抗三种阶段类型的抗体。鼠源性单克隆抗虽然具有获取方法较为成熟,且抗体具有高亲和力等优势,但是伴随着该内抗体在体内半衰期短、人抗鼠排斥反应(humananti-murine-antibodyresponse,hama)强烈、抗体依赖的细胞毒(antibody-dependentcellcytotoxicity,adcc)和补体依赖的细胞毒(complement-dependentcytotoxicity,cdc)作用激发强度不合适弊端的出现,从而限制此类抗体的有效应用。鼠源抗体人源化即嵌合抗体是将鼠抗体的部分序列置换成人的序列,该方法在一定程度上降低了hama,但亲和力也随之降低。为了获得更安全、高效的单克隆抗体,研究人员尝试了多种获得全人源性的单克隆抗体方法,较为常见的有,利用基因工程小鼠制备单克隆抗体,噬菌体抗体库技术以及单个b淋巴细胞抗体制备技术等。本发明所涉及的单个b淋巴细胞抗体制备技术,是将单细胞分离鉴定技术结合多种pcr技术形成的一种单克隆抗体的体外表达系统,即从人b淋巴细胞中直接获取全人源的单克隆抗体的方法。产生的抗体具有全人源性、高度抗原特异性、亲和性等优势,在治疗肿瘤、感染性疾病、自身免疫性疾病和器官移植等方面显出了独特的优势和良好的应用前景。因此,非常有必要选择先进高效的单克隆抗体制备技术制备抗体治疗和预防hcv感染。技术实现要素:本发明的目的在于提供一种与丙型肝炎病毒(hcv)的结合分子,该结合分子对丙型肝炎病毒具有有效的中和作用。为了实现上述目的,本发明采用了如下技术方案:本发明提供了一种分离的结合分子,所述结合分子包括:(1)seqidno:2所示的重链cdr1、seqidno:3所示的重链cdr2、seqidno:4所示的重链cdr3;和/或(2)seqidno:6所示的轻链cdr1、seqidno:7所示的轻链cdr2、seqidno:8所示的轻链cdr3。作为本发明的一个方面,本发明的结合分子包括:(1)重链可变区,所述重链可变区具有seqidno:1所示的氨基酸序列;和/或(2)轻链可变区,所述轻链可变区具有seqidno:5所示的氨基酸序列。本发明的“结合分子”是指抗体分子及具有免疫学活性的片段,即含有免疫特异性结合抗原的抗原结合位点的分子。本发明的抗体分子可以是任何类型(例如igg、ige、igm、igd、iga)、任何类别(例如igg1、igg2、igg3、igg4、iga1、higa2)或亚类的抗体分子。抗体分子的免疫学活性部分包括但不限于fab、fab’和f(ab’)2、fd、单链fv(scfv)、单链抗体、二硫键连接的fv(sdfv)和包括vl或vh结构域的单域抗体。包括单链抗体在内的结合抗原的抗体片段可以包括单独的可变区或与以下的全部或一部分组合的可变区:绞链区、ch1、ch2和ch3结构域。本发明也包括抗原结合片段,其包括可变区与绞链区、ch1、ch2和ch3结构域的任一组合。本发明的结合分子还包括与多肽重组融合的或化学缀合的(包括共价和非共价缀合的)结合分子。多肽重组融合的例子包括将本发明的结合分子与标记物序列融合,标记物序列包括但不限于ha标签、6xhis标签、c-myc标签、flag标签。化学缀合的例子包括将本发明的结合分子与可检测物质缀合。通过将抗体偶联到可检测物质可以促进检测。可检测物质的实例包括各种酶、辅基、荧光材料、发光材料、生物发光材料、放射性材料、利用各种正电子发射断层扫描的正电子发射金属、以及非放射性的顺磁性金属离子。利用本领域已知的技术,可检测物质可以直接地与抗体(或其片段)偶联或缀合,或经中间物(例如本领域已知的接头)间接地偶联或缀合。参见例如关于金属离子的美国专利no.4,741,900,其中所述金属离子可以与抗体缀合,用作本发明的诊断剂。合适的酶的实例包括辣根过氧化物酶、碱性磷酸酶、β-半乳糖苷酶、或乙酰胆碱酯酶;合适的辅基复合物的实例包括链霉抗生物素蛋白/生物素和抗生物素蛋白/生物素;合适的荧光材料的实例包括伞形酮、荧光素、异硫氰酸荧光素、罗丹明、dichlorotriazinylamine荧光素、丹磺酰氯或藻红蛋白;发光材料的实例包括鲁米诺;生物发光材料的实例包括萤光素酶、萤光素、和水母发光蛋白;合适的放射性材料的实例包括125i、131i、111in或99tc。本发明的结合分子还包括前面所述的结合分子的功能变体。如果变体能与亲代结合分子竞争特异性结合丙型肝炎病毒或其蛋白片段,则认为该变体分子是本发明结合分子的功能变体。换句话说,所述功能变体仍能结合丙型肝炎病毒或其蛋白片段。所述功能变体可以具有保守序列修饰,包括氨基酸取代、添加和缺失。这些修饰可以通过本领域己知的标准技术导入,例如定向诱变和随机pcr介导的诱变,并且可包含天然以及非天然氨基酸。此外,功能变体可包含氨基酸序列在氨基末端或者羧基末端或者这两端的截短体。本发明的功能变体与亲代结合分子相比可具有相同或不同的、更高或更低的结合亲和性,但是仍能结合丙型肝炎病毒或其片段。本发明的功能变体对于丙型肝炎病毒具有中和活性。所述中和活性与亲代结合分子相比可以相同或者更高或更低。此后,当使用术语“结合分子”时,其也涵盖所述结合分子的功能变体。作为本发明的另一方面,本发明还提供了前面所述的结合分子的多核苷酸。本发明还包括在严格或较低严格的条件下能与编码本发明的结合分子的多核苷酸杂交的多核苷酸。本领域技术人员将意识到这些多核苷酸的功能变体也是本发明的一部分。功能变体是这样的核甘酸序列,通过使用标准遗传密码可以将其直接翻译以提供与从亲代核酸分子中翻译的序列相同的氨基酸序列。可以利用本领域任一已知的方法得到多核苷酸序列,并确定出多核苷酸的核苷酸序列。例如,如果已知抗体的核苷酸序列,就可以从化学合成的寡核苷酸装配出编码所述抗体的多核苷酸。或者,可以从来自合适来源的核酸中产生编码抗体的多核苷酸。如果无法得到含有编码特定抗体的核酸的克隆,但已知所述抗体分子的序列,那么可以通过化学合成得到编码所述免疫球蛋白的核酸,或利用与所述序列的3’和5’末端可杂交的合成引物从合适的来源(例如抗体cdna文库、或从表达所述抗体的任一组织或细胞例如所选择的用于表达本发明的抗体的杂交瘤细胞中所产生的cdna文库,或从中所分离到的核酸,优选聚a+rna)通过pcr扩增得到编码所述免疫球蛋白的核酸,或通过利用特异于所述特定基因序列的寡核苷酸探针通过克隆得到编码所述免疫球蛋白的核酸,以例如从cdna文库中鉴定出编码所述抗体的cdna克隆。然后可以利用本领域任一熟知的方法将pcr所产生的扩增核酸克隆到可复制的克隆载体内。一旦确定了抗体的核苷酸序列以及相应的氨基酸序列,就可以利用本领域熟知的处理核苷酸序列的方法例如重组dna技术、定位诱变、pcr等处理抗体的核苷酸序列以产生具有不同氨基酸序列的抗体,例如产生氨基酸取代、缺失、和/或插入。可以用熟知的方法检查重链和/或轻链可变结构域的氨基酸序列以鉴定出cdr的序列,所述方法例如通过与其它重链和轻链可变区的已知氨基酸序列比较以确定出序列的高变异性区域。利用常规重组dna技术,可以将一个或多个cdr插入到构架区内,例如插入到人构架区内以人源化非人抗体,如上面所述。构架区可以是天然发生的或共有的构架区,以及优选地是人构架区(见例如,293tthiaetal.,j.mol.biol.278:457-479(1998)中的人构架区的列表)。优选地,通过构架区和cdr的组合所产生的多核苷酸编码与本发明的多肽特异结合的抗体。优选地,如上面所讨论的,在构架区内可以进行一个或多个氨基酸取代,以及优选地所述氨基酸取代提高了抗体与其抗原的结合。另外,可以用这些方法对参与链内二硫键的一个或多个可变区半胱氨酸残基进行取代或删除,以产生缺少一个或多个链内二硫键的抗体分子。本发明包括对多核苷酸的其它改变,这也在本领域人员的技术范围之内。本发明还提供了一种含有前面所述的多核苷酸的重组表达载体。利用熟知的技术可以制备含有编码本发明结合分子的核苷酸序列的重组表达载体。所述表达载体包括与合适的转录或翻译调节核苷酸序列可操纵地连接的核苷酸序列,所述转录或翻译调节核苷酸序列例如那些起源于哺乳动物、微生物、病毒、或昆虫基因的序列。调节序列的实例包括转录启动子、操纵子、增强子、mrna核糖体结合位点、和/或其它控制转录和翻译起始和终止的合适序列。当所述调节序列与合适的多肽的核苷酸序列功能性相关时,核苷酸序列是“可操纵地连接的”。因此,如果一个启动子核苷酸序列控制合适的核苷酸序列的转录,那么所述启动子核苷酸序列就是可操纵地连接于例如抗体重链序列的。本发明还提供了一种含有前面所述的多核苷酸或前面所述的重组表达载体的宿主细胞。可用于本发明的宿主细胞包括但不限于微生物,例如经含有抗体编码序列的重组噬菌体dna、质粒dna或粘粒dna表达载体转化的细菌(例如大肠杆菌(e.coli)、枯草芽孢杆菌(b.subtilis));经含有抗体编码序列的重组酵母表达载体转化的酵母菌例如酵母属(saccharomyces)、毕赤酵母属(pichia));经含有抗体编码序列的重组病毒表达载体(例如杆状病毒)感染的昆虫细胞系统;经重组病毒表达载体(例如花椰菜花叶病毒(camv);烟草花叶病毒(tmv)感染的或经含有抗体编码序列的重组质粒表达载体(例如ti质粒)转化的植物细胞系统;或携带含有来源于哺乳动物细胞基因组的启动子(例如金属硫蛋白启动子)或来源于哺乳动物病毒的启动子(例如,腺病毒晚期启动子、痘苗病毒7.5k启动子)的重组表达构建体的哺乳动物细胞系统(例如cos、cho、bhk、293、3t3细胞)。在本发明的具体实施方案中,所述宿主细胞是哺乳动物细胞,更优选cho细胞。用重组dna转化、转染宿主细胞可用本领域技术人员熟知的常规技术进行。一些采用的转化、转染方法包括但并不限于:常规化学方法如磷酸钙共沉淀法、pei转染法,常规机械方法如显微注射、电穿孔、脂质体包装等。获得的转化子可以用常规方法培养,以表达本发明的结合分子。根据所用的宿主细胞,培养中所用的培养基可选自各种常规培养基。在适于宿主细胞生长的条件下进行培养。当宿主细胞生长到适当的细胞密度后,用合适的方法(如温度转换或化学诱导)诱导选择的启动子,将细胞再培养一段时间。本发明的结合分子优选的是采用哺乳动物细胞来生产,哺乳动物细胞通常需要在含血清的培养基中进行培养。需要对细胞进行无血清的适应过程后,方可让细胞在无血清培养基中正常的生长。本发明提供了一种抑制丙型肝炎病毒,或者,治疗或预防丙型肝炎病毒感染疾病的药物组合物,所述药物组合物包括有效量的本发明的结合分子。本发明也提供了包括一个或多个装有本发明的药物组合物的一种或多种组分的容器的药物包装或试剂盒。与这些容器任选地伴随的可以是以管理药物或生物产品的生产、使用或销售的政府机构所规定的形式的说明,这些说明反映了管理人体施用的药物的生产、使用或销售的机构的认证。本发明还提供了一种包括前面所述结合分子的hcv检测产品。所述检测产品包括但不限于检测试剂、试剂盒、芯片或试纸。凡是包括前面所述结合分子的能够检测出hcv的检测产品均包括在本发明的范围之内。本发明还提供了一种非诊断目的的检测hcv水平的方法,其特征在于,所述方法包括如下步骤:(1)获取含有hcv的样品;(2)将步骤(1)获取的样品与前面所述的结合分子接触;(3)检测样品与结合分子的结合反应。本发明还提供了制备所述的结合分子的方法,其包括在适合于引起从编码本发明的抗体分子的dna表达蛋白质的条件下培养包含本发明的载体的宿主细胞,以及分离结合分子。具体地,本发明提供了一种前面所述的结合分子的制备方法,所述制备方法采用的是单个b细胞抗体制备技术。所述单个b细胞抗体制备技术是将单细胞分离鉴定技术结合多种pcr技术形成的一种单克隆抗体的体外表达系统,即从人b细胞中直接获取全人源的单克隆抗体的方法。进一步,所述制备方法包括如下步骤:(1)采集hcv感染者血液样本;(2)分离外周血单个核细胞(pbmc);(3)利用流式细胞仪进行pbmc细胞分选,首先去除细胞碎片、黏连细胞和死细胞,通过荧光抗体染色得到cd3-/cd14-/cd16-/igm-的细胞,选择表达cd235a-/igd-/cd20+的b细胞,圈出cd27all记忆b细胞,用特异性标记荧光素的抗原得到e2双荧光标记的靶细胞。(4)利用单细胞rt-pcr扩增步骤(2)获得的单个b细胞中的抗体轻链和重链可变区的核苷酸片段;(5)将步骤(3)获得的抗体轻链和重链可变区的核苷酸片段融合到含有人类抗体恒定区的表达载体中形成重组表达载体,之后导入宿主细胞表达;(6)筛选获得具有结合活性和中和活性的本发明的结合分子。本发明还提供了前面所述的结合分子在制备hcv检测产品中的应用。所述检测产品包括前面所述的结合分子;所述检测产品包括但不限于检测试剂、试剂盒、芯片或试纸。凡是包括前面所述的结合分子能够检测出hcv的检测产品均包括在本发明的范围之内。本发明还提供了前面所述的结合分子在制备前面所述的药物组合物中的应用。本发明还提供了前面所述的结合分子在制备抑制丙型肝炎病毒,或,预防或治疗丙型肝炎病毒感染疾病的药物制剂中的应用。进一步,所述疾病包括肝病,如肝炎、肝硬化或肝癌;肝外疾病,如皮肤的异常,如冷球蛋白血症、迟发性皮肤卟啉症、白细胞破碎性血管炎、网状青斑等。进一步,所述肝炎是急性或慢性丙型肝炎。本发明的结合分子还可以与其他具有相同或者互补功能的药物联合应用,联合应用的效果可以是结合分子与其他药物功能之和,还可以远远大于结合分子与其他药物功能之和,这种情况表明该结合分子与其他药物之间产生了协同作用。本文所用的术语“单克隆抗体”指从一类基本均一的群体获得的抗体,除少数可能存在的天然发生的突变外,该群体中包含的单个抗体是相同的。修饰语“单克隆”仅表示抗体的特性,是从基本均一的抗体群中获得的,这不能解释成需要用任何特殊方法来生产抗体。本文所用的术语“可变”表示抗体中可变区的某些部分在序列上有所不同,它形成了各种特定抗体对其特定抗原的结合和特异性。可变性集中于轻链和重链可变区中称为互补决定区(cdr)或超变区中的三个片段中。天然重链和轻链的可变区中各自包含四个fr区(可变区中较保守的部分),它们大致上呈β-折叠构型,由形成连接环的三个cdr相连,可形成部分β折叠结构。每条链中的cdr通过fr区紧密地靠在一起并与另一链的cdr一起形成了抗体的抗原结合部位。恒定区不直接参与抗体与抗原的结合,但是它们表现出不同的效应功能,例如参与抗体的依赖于抗体的细胞毒性。如本文所用,“有效量”是足够减轻一或多种通常与hcv感染相关的症状或任何由hbv感染引起或与之相关的疾病或病症的剂量。当考虑预防性的用途时,本术语意指足够预防或延缓hcv感染确立的剂量。本文所述的“样品”涵盖了多种样品类型,包括生物学来源的血液及其它体液样品,实体组织样品如活检组织样品或者组织培养物,或者衍生自其中的细胞或者其后代。该术语还包括在获得后已经通过任何方式处理的样品,例如用试剂处理、溶解、或者富集某些成分如蛋白质或者多核苷酸。该术语涵盖了得自任何物种的各种临床样品,也包括培养的细胞、细胞上清和细胞溶解产物。如本文所用,术语“分离的”是指从其天然环境中分离出的蛋白质(即,从至少一种其天然伴随的其它组分中分离)。本文提及的所有专利和出版物均在法律允许的程度内引入本文作为参考,以用于描述和披露这些专利和出版物中报道的可能用于本发明的蛋白质、酶、载体、宿主细胞和方法学。但是本文内容不应被理解为承认本发明由于在先发明而使本发明无法占先于这种披露。附图说明图1为本发明实施例的trn1008抗体的sds-page与western-blot检测图,其中a:sds-page;b:western-blot;图2为本发明实施例的trn1008抗体与8种不同基因型hcv抗原的结合活性检测图;图3为本发明实施例的trn1008抗体与7种不同亚型hcv真病毒中和活性效果图;图4为本发明实施例的trn1008抗体与4种不同基因型的hcv抗原e2-core蛋白的亲和活性测定图,其中,a:e2-core-2a;b:e2-core-4a;c:e2-core-6a;d:e2-core-7a。具体的实施方式本发明不限于本文所述的特定方法学、方案、细胞系、载体或试剂,因为这些是可以变化的。另外,本文所用术语只是为了描述特定的实施方案而无限制本发明的范围之意。除非另外限定,则本文所用的所有技术和学术术语和任何缩写均具有与本领域技术人员普遍理解的含义相同的含义。尽管在实施本发明时可以使用与本文所述相似或相同的任何方法和材料,但本文还是描述了使用设备和材料。实施例1全人源抗hcv的单克隆中和抗体trn1008的制备1、样本获取:hcv感染者抗凝外周血采自云南省昆明市,该患者确认感染时间为2010年。2、记忆性b细胞分选采集hcv感染者血液样本,分离外周血单个核细胞(peripheralbloodmononuclearcell,pbmc),bdfacsria流式细胞仪(bdbiosciences,sanjose,ca)进行细胞分选,首先去除细胞碎片、黏连细胞和死细胞,通过荧光抗体染色得到cd3-/cd14-/cd16-/igm-的细胞,选择表达cd235a-/igd-/cd20+的b细胞,圈出cd27all记忆b细胞,用特异性标记荧光素的抗原得到e2双荧光标记的靶细胞。3、单细胞rt-pcr将含有单个b淋巴细胞的96孔板的pcr预测混液中加入0.5μm的各亚型重链与轻链的恒定区引物与superscriptiv逆转录酶(invitrogen,carlsbad,ca),同时设置阳性及阴性对照;逆转录pcr条件:55℃60min,降至4℃。产物cdna-20℃长期保存。4、抗体可变区目的基因的扩增以逆转录产物(cdna)为模板,加入amplitaqgold360mastermix(invitrogen,carlsbad,ca),及0.5μm的各亚型重链与轻链抗体的特异性引物。反应条件:预变性95℃5min,然后进行35个pcr循环,每个循环为:94℃×30s,58/60/64(h/k/l)℃×30s,72℃×1.5min,用72℃延伸7min后降至10℃。5、dna凝胶电泳鉴定使用2%琼脂糖凝胶进行电泳实验进行鉴定。取2μlpcr反应产物与18μl0.1%的loadingbuffer混匀后上样,在e-base电泳系统的eg模式下进行电泳12min。凝胶成像系统检测pcr产物大小。6、重组抗体的表达载体的构建用特异性引物获取elisa检测为阳性的抗体重链与轻链基因片段(包括可变区和恒定区),利用ta克隆的方法分别将重链和轻链基因链接到pcdna3.3载体上,将连接产物转化dh5α感受态细菌中,在含有氨苄青霉素的平板上37℃培养过夜,随即挑取12个单菌落用特异性引物进行pcr鉴定(pcr反应条件:94℃预变性3min,94℃变性30s,55℃退火30s,72℃延伸1min40s,28个循环,最后72℃再延伸5min),取2μlpcr产物在1%琼脂糖凝胶上进行电泳检测,选取pcr鉴定为阳性的菌落进行基因测序,比对结果正确的即为抗体重链和轻链的重组表达质粒。7、elisa检测目的基因的表达在大肠杆菌dh5α中大量扩增表达阳性抗体重链和轻链基因的质粒,无内毒素抽提试剂盒抽提。用转染试剂polyetherimide共转染cho细胞,转染后4-6小时添加新鲜无血清培养基,置于37℃,8%co2恒温培养箱中培养96小时,收集细胞上清进行检测。培养72h后细胞上清采用直接竞争elisa检测目的基因表达的抗体。elisa筛选:以不同的hcv包膜糖蛋白为抗原,并用包被液将抗原稀释浓度为100ng/ml,包被于elisa96孔板,每孔100μl,4℃过夜。封闭液37℃封闭2个小时。封闭后加一抗,抗体起始浓度为25μg/ml,3倍梯度稀释,每孔体积为100μl,37℃孵育1个小时,同时用hcv阳性病人血清作为阳性对照,狂犬抗体为阴性对照。用hrp标记的羊抗人igg(1:2000稀释)作为二抗37℃孵育1个小时。加入底物显色液(tmb),37℃避光放置5min后,用2m硫酸中止反应,用450nm波长进行比色。8、抗体中和实验将elisa筛选到的有结合活性的抗体进行中和实验。将不同的hcv包膜糖蛋白的编码序列包装成质粒,加入荧光素luciferase基因转染293t细胞用于包装hcv病毒(hcvpp),收取上清用于感染。铺huh7细胞于96孔板中,每孔细胞约1*104个,每孔体积为100μl,过夜培养,感染时细胞约30%铺满。hcvpp与抗体混合,室温放置30min。加入hcvpp与抗体混合液于96孔板,感染huh7细胞。对照组仅加入hcvpp,感染24h后换液,继续培养1-2天。感染后2-3天后测定luciferase活性,测量方法为去掉细胞上清,每孔用30μl裂解液,充分裂解后取20μl细胞裂解液加30μl底物,读取荧光值。比较抗体与对照组,计算中和效率。9、抗体大量表达与纯化将中和实验鉴定出的有中和活性的编号为trn1008的抗体重链与轻链的表达载体(其中,重链可变区的氨基酸序列如seqidno:1所示;抗体轻链可变区的氨基酸序列如seqidno:5所示)共转染cho细胞(细胞密度达到1.6×106个/ml),转染后6-8小时补培养基,37℃,8%co2,125rpm摇床中培养120小时。然后收集转染上清,4000rp,4℃,离心1小时,弃沉淀,利用蛋白(protein)a亲和层析法进行纯化。通过sds-page和western-blot检验抗体trn1008的表达及纯化结果,结果如图1所示,得到较纯蛋白,并可清晰观察到解链后的抗体轻、重链。实施例2trn1008抗体的结合活性检测1、trn1008抗体与hcv包膜糖蛋白的特异性结合检测用实施例1提到的elisa方法对表达纯化的抗体的结合特异性进行检测:将不同的hcv包膜糖蛋白编码序列包装成质粒,加入荧光素luciferase基因转染293t细胞用于包装hcv病毒(hcvpp),收取上清用于感染。铺huh7细胞于96孔板中,每孔细胞约1*104个,每孔体积为100μl,过夜培养,感染时细胞约30%铺满。hcvpp与不同浓度的抗体hcv混合,起始浓度75μg/ml,3倍稀释,室温放置30min。加入hcvpp与抗体hcv混合液于96孔板,感染huh7细胞。对照组仅加入hcvpp,感染24h后换液,继续培养1-2天。感染后2-3天后测定luciferase活性,测量方法为去掉细胞上清,每孔用30μl裂解液,充分裂解后取20μl细胞裂解液加30μl底物,读取荧光值。结果:trn1008抗体能100%与hcv包膜糖蛋白特异性结合,荧光值降低。2、trn1008抗体与不同基因型hcv抗原的结合活性检测以8种不同基因型hcv包膜糖蛋白为抗原,并用包被液将抗原稀释浓度为100ng/ml,包被于elisa96孔板,每孔100μl,4℃过夜。封闭液37℃封闭2个小时。封闭后加一抗,每孔体积为100μl,37℃孵育1个小时。用hrp标记的羊抗人igg(1:2000稀释)作为二抗37℃孵育1个小时。加入底物显色液(tmb)100μl/孔,37℃避光放置5min后,用2m硫酸中止反应,用450nm波长进行比色。结果如图2所示,trn1008抗体可以与不同基因型的hcv抗原结合,且trn1008的结合活性极强,其中图2中的1b、1a、2、3、4、5、6、7分别代表hcv1b、hcv1a、hcv2、hcv3、hcv4、hcv5、hcv6、hcv7。实施例3trn1008抗体与不同的hcv真病毒株的中和活性检测铺huh7细胞于96孔板中,过夜培养,感染时细胞约30%铺满。hcv真病毒株(h77、con1、jfh1、s52、ed43、sa13、hk6a)与不同浓度的抗体混合,起始浓度25μg/ml,3倍稀释,室温放置30min。加入hcv病毒株(h77、con1、jfh1、s52、ed43、sa13、hk6a)与抗体混合液于96孔板,感染huh7细胞。对照组仅加入hcv病毒株2g9,感染24h后换液,继续培养1-2天。感染后2-3天后测定活性,读取荧光值。比较抗体与对照组,计算中和效率。结果如图3所示,trn1008抗体与不同的hcv病毒株的中和效率见下表,trn1008抗体对hcv真病毒株h77(1a)、con1(1b)、jfh1(2a)、s52(3a)、ed43(4a)、sa13(5a)和hk6a的中和效率都非常好,能够显示其在免疫治疗和预防的良好应用前景。表1trn1008抗体与不同的hcv病毒株的中和效率实施例4trn1008抗体与hcv的包膜糖蛋白的亲和活性检测用biacorex-100进行trn1008与hcv的包膜糖蛋白(hcv-e2-core,抗原)结合的亲和力和动力学分析:hcv-e2-core蛋白用hbs-ep缓冲液稀释作为分析物,分析物以逐渐增高的浓度依次流过芯片,分别得到信号曲线。biacorex-100system软件进行分析,进而得到trn1008的亲和力和动力学参数结果。结果如图4和表2所示。trn1008抗体与抗原e2-core-2a、e2-core-4a、e2-core-6a和e2-core-7a的kd值分别为1.32e-11m、1.12e-9m、2e-11m、2.98e-12m,显示trn1008具有较高的亲和力活性。表2trn1008抗体与hcv病毒抗原的亲和力动力学结果参数表抗原ka(1/ms)kd(1/s)kd(m)e2-core-2a130101.72e-071.32e-11e2-core-4a3.48e+043.89e-051.12e-09e2-core-6a244104.87e-072e-11e2-core-7a4.06e+041.21e-072.98e-12虽然以上仅描述了本发明的具体实施方式范例,但是本领域的技术人员应当理解,这些仅是举例说明,本发明的保护范围是由所附权利要求书限定的。本领域的技术人员在不背离本发明的原理和实质的前提下,可以对这些实施方式做出多种变更或修改,但这些变更或修改均落入本发明的保护范围。sequencelisting<110>广州泰诺迪生物科技有限公司珠海泰诺麦博生物技术有限公司暨南大学<120>一种治疗丙型肝炎病毒药物的制备方法和用途<160>8<170>patentinversion3.5<210>1<211>123<212>prt<213>人源<400>1glnvalglnleuvalglnserglyalagluvallyslysproglyala151015servallysvalsercyslysproserglyglyserphethrglyhis202530tyrilehistrpvalargglnalaproglyglnglyproglutrpmet354045glycysileasnproasnserglygluthrasntyrgluglnlysphe505560argglyargvalthrleuthrargaspthrserileasnthralatyr65707580metgluvalserserleuthrseraspaspthralavaltyrtyrcys859095alathrproglygluglythrthrprophetyrpheglymetaspval100105110trpglyglnglythrthrvalthrvalserser115120<210>2<211>8<212>prt<213>人源<400>2glyglyserphethrglyhistyr15<210>3<211>8<212>prt<213>人源<400>3ileasnproasnserglygluthr15<210>4<211>16<212>prt<213>人源<400>4alathrproglygluglythrthrprophetyrpheglymetaspval151015<210>5<211>107<212>prt<213>人源<400>5aspilevalmetthrglnserproproservalseralaservalgly151015aspargvalthrilethrcysargalathrglnglyalaserthrtrp202530valalatrptyrglnglnlysproglylysalaprogluleuleuile354045tyralathrasnileleuglnserglyvalproserargphesergly505560serglyserglythraspphethrleuthrilethrasnleuglnpro65707580gluaspphealathrtyrtyrcysglnhisilelysargpheproleu859095thrpheglyglyglythrlysvalaspilelys100105<210>6<211>6<212>prt<213>人源<400>6glnglyalaserthrtrp15<210>7<211>3<212>prt<213>人源<400>7alathrasn1<210>8<211>9<212>prt<213>人源<400>8glnhisilelysargpheproleuthr15当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1