获得绒毛膜间充质干细胞的方法及试剂盒与流程
本发明涉及生物工程领域。具体地,本发明涉及获得绒毛膜间充质干细胞的方法及试剂盒。
背景技术:
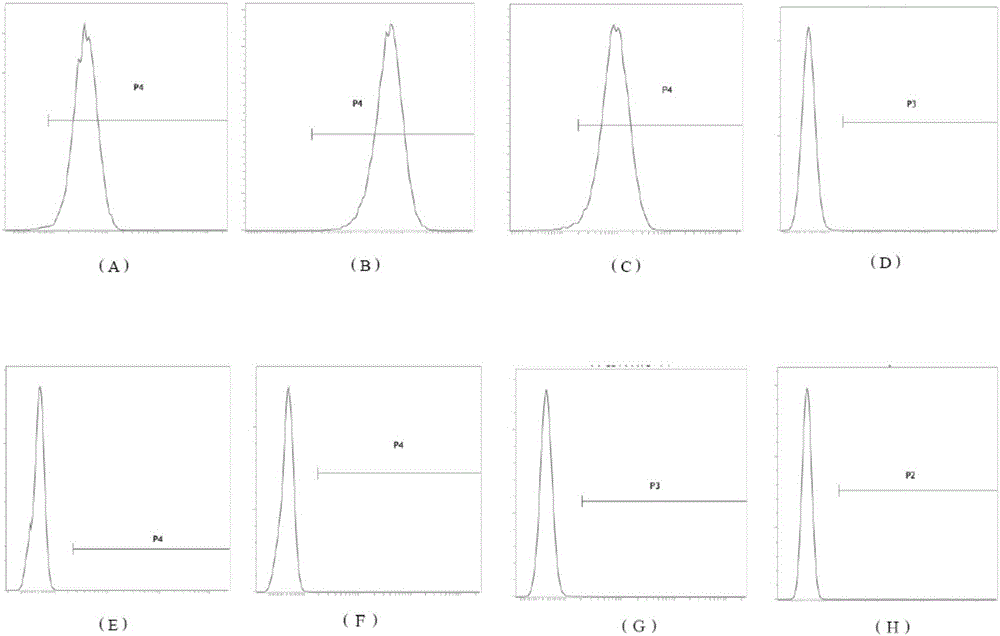
:绒毛膜间充质干细胞与绒毛的分布密切相关,多分布于绒毛内皮下以及绒毛附近间质内。绒毛膜间充质干细胞因取材方便、操作无侵入性、多向分化潜能大、增殖能力强、免疫原性低、病原污染风险低等优点而成为再生医学的重要细胞来源和最具临床应用前景的功能干细胞。然而,目前获得绒毛膜间充质干细胞的方法仍有待改进。技术实现要素:本发明旨在至少在一定程度上解决现有技术中存在的技术问题至少之一。需要说明的是,本发明是基于发明人的下列发现而完成的:目前常用的绒毛膜间充质干细胞分离方法是将绒毛膜剪碎后直接用组织块法培养,或者采用酶消化法,但是酶消化方法复杂,需多次酶消化,很容易造成细胞的损伤,难以获得大量且纯度较高的绒毛膜间充质干细胞。发明人发现,酶消化处理过程中,酶的种类、用量、消化时间等因素显著影响酶消化处理效果,尤其是酶的种类,进而影响绒毛膜间充质干细胞的得率及活性。发明人经深入研究发现,单一酶的消化效果不佳,难以获得大量且纯度较高的绒毛膜间充质干细胞,而混合酶能够有效地对绒毛膜进行消化,从而获得大量、纯度较高且活性较高的绒毛膜间充质干细胞。进一步地,发明人惊奇地发现,胰酶、胶原酶Ⅳ以及胶原酶Ⅱ的混合酶的消化效果最佳。为此,在本发明的一个方面,本发明提出了一种获得绒毛膜间充质干细胞的方法。根据本发明的实施例,所述方法包括:利用混合酶制剂将绒毛膜进行消化处理,得到消化产物;以及从所述消化产物中分离所述绒毛膜间充质干细胞,其中,所述混合酶制剂包括:胰酶;胶原酶Ⅳ;以及胶原酶Ⅱ。利用消化处理方法,能够将绒毛膜组织中细胞之间的蛋白质降解,从而分离出单个细胞。发明人发现,单一酶很难将绒毛膜消化完全,所得到的绒毛膜间充质干细胞量较少,由此需要进行多次消化。但是,多次消化容易造成细胞的损伤,难以获得大量且活性较高的绒毛膜间充质干细胞。进而,发明人发现,采用混合酶制剂进行消化的效果较好,且无需多次消化,以减少对细胞的损伤。发明人意外地发现,采用包括胰酶、胶原酶Ⅳ以及胶原酶Ⅱ的混合酶制剂进行消化,能够获得大量、纯度较高且活性较高的绒毛膜间充质干细胞。然而,利用其他种类酶的效果不佳。根据本发明的实施例,所述获得绒毛膜间充质干细胞的方法还可以具有下列附加技术特征:根据本发明的实施例,所述混合酶制剂包括:0.05质量%~0.25质量%的胰酶;1~2μg/mL的胶原酶Ⅳ;以及0.1质量%的胶原酶Ⅱ。发明人意外地发现,胰酶、胶原酶Ⅳ以及胶原酶Ⅱ的浓度显著影响消化效率,进而影响绒毛膜间充质干细胞的得率、纯度及活性。在上述最优混合浓度下,绒毛膜间充质干细胞的得率、纯度及活性较高。根据本发明的具体实施例,混合酶制剂中胰酶浓度可以为0.08质量%、0.10质量%、0.13质量%、0.18质量%或0.21质量%。当胰酶、胶原酶Ⅳ以及胶原酶Ⅱ的浓度过高,将对绒毛膜间充质干细胞造成损伤,使其活性下降,若胰酶、胶原酶Ⅳ以及胶原酶Ⅱ浓度过低,无法充分消化,从而使得到的绒毛膜间充质干细胞的得率及纯度较低。由此,根据本发明实施例的获得绒毛膜间充质干细胞的方法能够获得大量、纯度较高且活性较好的绒毛膜间充质干细胞。根据本发明的实施例,所述混合酶制剂与绒毛膜的用量比为0.5~2:1,优选1:1。发明人发现,混合酶制剂的添加量显著影响消化处理效果,进而影响绒毛膜间充质干细胞的产率及活性。发明人意外地发现,当混合酶制剂与绒毛膜的用量比为0.5~2:1,优选1:1时,能够获得大量、纯度较高且活性较高的绒毛膜间充质干细胞。若添加量过多,容易造成细胞损伤,活性下降。在实际情况下,本领域技术人员可以根据需要选择消化处理条件,例如反应温度、时间,对此本申请不作严格限定,只要能够得到绒毛膜间充质干细胞即可。根据本发明的一些实施例,所述消化处理是在35~37℃的温度、100~200rpm的转速下震荡30~60min。根据本发明的优选实施例,所述消化处理是在37℃的温度、150rpm的转速下震荡30min。发明人意外地发现,在此条件下能够获得大量、纯度较高且活性较高的绒毛膜间充质干细胞。消化处理温度显著影响酶活性,温度过高或过低都将造成酶活力过低,导致消化效率降低,所得到的细胞量较少。消化处理时间过长,会造成细胞损伤,使其活性降低,时间过短,酶消化不充分,所得到的细胞量较少。若震荡时间过长,将破坏细胞的结构,造成损伤。根据本发明的具体实施例,消化处理后,通过向消化反应体系中加入胎牛血清(FBS),以终止消化反应。需要说明的是,对于从消化产物中分离绒毛膜间充质干细胞的方法不作严格限定,只要能够获得绒毛膜间充质干细胞即可。根据本发明的实施例,为了得到纯度较高的绒毛膜间充质干细胞,所述分离包括:将所述消化产物进行过滤,收集滤液;将所述滤液进行离心,收集细胞;以及将所述细胞进行清洗,以便获得所述绒毛膜间充质干细胞。由此,能够有效地除去附着于细胞上的消化液,且避免对细胞造成损伤,从而获得纯度较高且活性较强的绒毛膜间充质干细胞。根据本发明的实施例,所述方法包括:利用混合酶制剂将裁剪成尺寸为4cm×4cm的所述绒毛膜进行消化处理,得到消化产物;将所述消化产物进行稀释,并利用100目筛网将所得到的稀释液进行过滤,收集滤液;以及将所述滤液在1200rpm的转速下离心6min,弃上清,得到所述绒毛膜间充质干细胞。发明人发现,将绒毛膜裁剪至尺寸为4cm×4cm,使得进行消化反应的细胞面积较大,促使消化反应充分发生。接着,将消化产物稀释,以便于后续过滤。然后将稀释液过筛,以除去大块组织。此外,将滤液在1200rpm下离心6min,既能够沉淀细胞,便于收集,同时较小地破坏细胞的结构及活性。从而,能够获得大量、纯度较高且活性较高的绒毛膜间充质干细胞。根据本发明的实施例,所述方法进一步包括扩增处理,所述扩增处理包括:将所述绒毛膜间充质干细胞重悬于培养基中,得到混合液;将所述混合液接种于所述培养基中,37℃,5%CO2下培养至出现克隆,长至传代。发明人发现,分离获得的绒毛膜间充质干细胞为单个细胞,将其进行扩增以得到大量的绒毛膜间充质干细胞。在上述最优扩增处理条件下,扩增的同时还可以使其活性进一步提高。在本发明的另一方面,本发明提出了一种试剂盒。根据本发明的实施例,所述试剂盒包括:胰酶;胶原酶Ⅳ;以及胶原酶Ⅱ。根据本发明的具体实施例,所述试剂盒用于获得绒毛膜间充质干细胞。利用消化处理方法,能够将绒毛膜组织中细胞之间的蛋白质降解,从而分离出单个细胞。发明人发现,单一酶很难将绒毛膜消化完全,所得到的绒毛膜间充质干细胞量较少,由此需要进行多次消化。但是,多次消化容易造成细胞的损伤,难以获得大量且活性较高的绒毛膜间充质干细胞。进而,发明人发现,采用混合酶制剂进行消化的效果较好,且无需多次消化,以减少对细胞的损伤。发明人意外地发现,采用包括胰酶、胶原酶Ⅳ以及胶原酶Ⅱ的混合酶制剂进行消化,能够获得大量、纯度较高且活性较高的绒毛膜间充质干细胞。根据本发明的实施例,所述试剂盒包括:0.05质量%~0.25质量%的胰酶;1~2μg/mL的胶原酶Ⅳ;以及0.1质量%的胶原酶Ⅱ。发明人意外地发现,胰酶、胶原酶Ⅳ以及胶原酶Ⅱ的浓度显著影响消化效率,进而影响绒毛膜间充质干细胞的得率、纯度及活性。在上述最优浓度下,绒毛膜间充质干细胞的得率、纯度及活性较高。根据本发明的具体实施例,胰酶浓度可以为0.08质量%、0.10质量%、0.13质量%、0.18质量%或0.21质量%。当胰酶、胶原酶Ⅳ以及胶原酶Ⅱ的浓度过高,将对绒毛膜间充质干细胞造成损伤,使其活性下降,若胰酶、胶原酶Ⅳ以及胶原酶Ⅱ浓度过低,无法充分消化,从而使得到的绒毛膜间充质干细胞的得率及纯度较低。由此,根据本发明实施例的试剂盒能够获得大量、纯度较高且活性较好的绒毛膜间充质干细胞。本发明的附加方面和优点将在下面的描述中部分给出,部分将从下面的描述中变得明显,或通过本发明的实践了解到。附图说明本发明的上述和/或附加的方面和优点从结合下面附图对实施例的描述中将变得明显和容易理解,其中:图1显示了根据本发明一个实施例的显微镜照片,其中,(A)为放大40倍,(B)为放大100倍;图2显示了根据本发明一个实施例的细胞表型鉴定分析图,其中,(A)为间质干细胞标志CDl05;(B)为间质干细胞标志CD90;(C)为间质干细胞标志CD73;(D)为造血细胞标志CD19;(E)为造血细胞标志CD34;(F)为造血细胞标志CD45;(G)为造血细胞标志CD14;(H)为人白细胞抗原HLA-DR;图3显示了根据本发明一个实施例的放大倍数为400倍的显微镜照片,其中(A)为成脂细胞,染色剂为油红O;(B)为早期成骨细胞,染色剂为茜素红;(C)为晚期成骨细胞,染色剂为VonKossa;(D)为成软骨细胞的HE染色;(E)为成软骨细胞,染色剂为阿尔辛兰;(F)为成软骨细胞,染色剂为甲苯胺蓝;以及图4显示了根据本发明一个实施例的细胞活力分析图。具体实施方式下面将结合实施例对本发明的方案进行解释。本领域技术人员将会理解,下面的实施例仅用于说明本发明,而不应视为限定本发明的范围。实施例中未注明具体技术或条件的,按照本领域内的文献所描述的技术或条件或者按照产品说明书进行。所用试剂或仪器未注明生产厂商者,均为可以通过市购获得的常规产品。下面将结合实施例对本发明的方案进行解释。本领域技术人员将会理解,下面的实施例仅用于说明本发明,而不应视为限定本发明的范围。实施例中未注明具体技术或条件的,按照本领域内的文献所描述的技术或条件或者按照产品说明书进行。所用试剂或仪器未注明生产厂商者,均为可以通过市购获得的常规产品。实施例在该实施例中,按照下列方法获得绒毛膜间充质干细胞:(1)将平滑绒毛膜剪至4cm×4cm大小,生理盐水洗三次,尽量将血洗净;(2)再将洗净的5g组织块转移到10cm平皿中,每平皿加入5ml的混合酶制剂,其中含0.25%胰酶,2μg/mL胶原酶Ⅳ和0.1质量%的胶原酶Ⅱ,37℃的温度、150rpm的转速下震荡30min。加入胎牛血清终止胰酶消化,并向所得到的消化产物中加入生理盐水,稀释5倍,得到稀释液;(3)将稀释液通过100目筛网过滤,收集滤液,1200rpm离心6min,生理盐水洗两次,弃上清,得到绒毛膜间充质干细胞;(4)用2ml原代培养基重悬绒毛膜间充质干细胞并接种,37℃,5%CO2下培养直至克隆出现,长至传代,期间每隔48h换液一次,以得到扩增的绒毛膜间充质干细胞。对比例按照实施例的方法获得绒毛膜间充质干细胞,区别在于,步骤(2)中,仅用0.1质量%的胶原酶Ⅱ进行消化。对实施例扩增后的绒毛膜间充质干细胞进行检测1.细胞形态:将绒毛膜间充质干细胞在显微镜下观察,结果如图1所示。可以看出,细胞贴壁,呈梭形,片状生长。2.细胞表型鉴定:取传至3代的绒毛膜间充质干细胞,消化后成单细胞悬液,按4×105个每管进行分装。1×PBS洗一次,300g离心5min,弃上清。100μl1×PBS重悬细胞,每管分别加入携带荧光标记的一抗CD90-FITC、CD73-PE、CD105-PE、CD34-PE、CD19-PE、CD45-PE、CD14-FITC及HLA-DR-PE(购自美国BDPharmingen公司,按说明书给量),设一管为直标抗体PE-isotype空白对照,一管为直标抗体FITC-isotype空白对照,4℃摇床,避光反应40min。1×PBS清洗3次,每次300g离心5min,1%多聚甲醛固定,4℃放置,流式细胞仪检测,结果如图2和表1所示,可以看出,细胞表型均一,细胞表达间质细胞标记CD73、CD90、CD105,不表达造血细胞标记CD34、CD14、CD45、CD19,且不表达人白细胞抗原HLA-DR,完全符合“国际细胞治疗协会”关于间充质干细胞表面标志物规定的标准。表1流式细胞仪检测细胞表型检测值正常参考值CD90100%>95%CD7398.33%>95%CD10599.21%>95%CD340.10%<2%CD450%<2%CD140.33%<2%CD190.09%<2%HLA-DR0.%<2%3.三系分化:3.1脂肪诱导分化:3.1.1取传至3代的绒毛膜间充质干细胞以1.0×105/孔接种于24孔培养板中,待细胞密度达到100%时,弃上清(用移液枪轻轻吸走)加入提前配置好的成脂分化诱导A液(成脂诱导启动培养基),3天后再换成诱导B液(成脂诱导维持培养基)。24h后再换成A液,如此循环3-5个周期,完成后用B液换掉旧的B液,每三天跟换一次,再放置七天,得到诱导细胞。3.1.2油红O染色鉴定脂滴形成诱导细胞去掉培养基,PBS洗一次,加入4%多聚甲醛固定30min,蒸馏水洗3次,原液(0.5%油红O)6ml,加蒸馏水4ml,静置5~10min,滤纸过滤;染色20min,蒸馏水洗3次,镜下观察照相,如图3所示。可以看出,诱导后出现明显的脂滴,油红O染色呈阳性,说明细胞具有较强的向脂肪细胞分化的能力。3.2成骨诱导分化3.2.1取传至3代的绒毛膜间充质干细胞以5×104/孔接种于24孔培养板中,正常培养24h后弃上清(用移液枪轻轻吸走)加入提前配置好的成骨诱导培养基,每3天换液。3.2.2成骨诱导检测方法茜素红染色:诱导14d绒毛膜间充质干细胞,得到早期成骨细胞,吸弃诱导培养液,PBS冲洗,4%多聚甲醛室温固定30min,双蒸水冲洗,使用茜素红工作液37℃孵育30min,双蒸水冲洗。Vonkossa染色:诱导21d绒毛膜间充质干细胞,得到晚期成骨细胞,参照细胞VonKossas钙染色试剂盒进行染色。分别将染色后的早期成骨和晚期成骨在显微镜下观察,如图3所示。可以看出,早期成骨细胞的茜素红染色呈阳性,说明细胞具有较强的向成骨细胞分化的能力。晚期成骨细胞Vonkossa染色为阳性,说明诱导分化的细胞已形成骨细胞的钙化结节,证明细胞具有较强的向成骨细胞分化的能力。3.3软骨诱导分化3.3.1取传至3代的绒毛膜间充质干细胞以5×105/管接种于15ml离心管中,正常培养24h后弃上清(用移液枪轻轻吸走)加入提前配置好的成软骨诱导培养基,临用前加TGF-β3,每3天换一次液。3.3.2软骨诱导检测方法形成的微团在上述体系内培养4周,每隔3天换液,诱导完毕后,进行石蜡包埋和切片。切片分别经1%甲苯胺蓝、阿尔辛兰染色、HE染色鉴定软骨特异性蛋白聚糖。如图3所示。可以看出,HE染色、甲苯胺蓝染色、阿尔辛兰染色呈阳性,说明细胞具有很强的向软骨细胞分化的能力。活力测定比较实施例和对比例的步骤(3)所得到的绒毛膜间充质干细胞的活力,具体步骤如下:分别将实施例和对比例的步骤(3)所得到的绒毛膜间充质干细胞用生理盐水洗2遍,加入不含动物成分的TrypLEExpress消化约30s,镜下可见短梭形贴壁细胞变圆并悬浮起来后,加入生理盐水吹打细胞并将细胞转移至离心管,1200rpm离心5min,弃掉上清液,用2ml的生理盐水重悬,通过细胞活力分析仪检测细胞的活力。实施例步骤(3)所得到的绒毛膜间充质干细胞为91.6%。说明利用本发明的方法获得绒毛膜间充质干细胞过程中,消化处理条件温和,对绒毛膜间充质干细胞损伤较小,使得到的绒毛膜间充质干细胞活性较强。对比例所得到的绒毛膜间充质干细胞的活力仅为74.4%(如图4所示),且实施例步骤(3)的绒毛膜间充质干细胞的得率为对比例的3倍。说明本发明的方法所得到的绒毛膜间充质干细胞的得率及活性均较高。在本说明书的描述中,参考术语“一个实施例”、“一些实施例”、“示例”、“具体示例”、或“一些示例”等的描述意指结合该实施例或示例描述的具体特征、结构、材料或者特点包含于本发明的至少一个实施例或示例中。在本说明书中,对上述术语的示意性表述不必须针对的是相同的实施例或示例。而且,描述的具体特征、结构、材料或者特点可以在任一个或多个实施例或示例中以合适的方式结合。此外,在不相互矛盾的情况下,本领域的技术人员可以将本说明书中描述的不同实施例或示例以及不同实施例或示例的特征进行结合和组合。尽管上面已经示出和描述了本发明的实施例,可以理解的是,上述实施例是示例性的,不能理解为对本发明的限制,本领域的普通技术人员在本发明的范围内可以对上述实施例进行变化、修改、替换和变型。当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1