带覆膜的锂‑镍复合氧化物粒子和带覆膜的锂‑镍复合氧化物粒子的制造方法与流程
本发明涉及镍含量高的带覆膜的锂-镍复合氧化物粒子,涉及提高大气环境下的稳定性且容易处理的带覆膜的锂-镍复合氧化物粒子及其制造方法。
背景技术:
近年来,随着手机、笔记本等小型电子设备的迅速扩大,作为可充放电的电源,锂离子二次电池的需求急剧增加。作为有助于在锂离子二次电池的正极充放电的正极活性物质,锂-钴氧化物(以下也称为钴系)被广泛应用。,然而,通过优化电池设计,将钴系正极的容量提高至与理论容量同等的程度、更进一步的高容量化逐渐变得困难。
因此,采用了理论容量高于现有钴系的锂-镍氧化物的锂-镍复合氧化物粒子的开发正在进行。然而,由于纯的锂-镍氧化物对水、二氧化碳等的反应性高,存在安全性、循环特性等问题,很难用作实用电池。因此,作为上述问题的改进方法,正在开发加入了钴、锰、铁等过渡金属元素或铝的锂-镍复合氧化物粒子。
在锂-镍复合氧化物中,存在分别加入等摩尔量的镍、锰、钴而形成的被称为所谓的三元系且以过渡金属组成Ni0.33Co0.33Mn0.33表示的复合氧化物粒子(以下也称为三元系),以及被称为所谓的镍系且镍含量大于0.65摩尔的锂-镍复合氧化物粒子(以下也称为镍系)。从容量的观点来看,镍含量多的镍系具有比三元系更大的优势。
然而,由于镍系对水、二氧化碳等的反应性高,因此,具有比钴系、三元系对环境更敏感,且更易吸收空气中水、二氧化碳(CO2)的特点。已报道水分、二氧化碳分别作为氢氧化锂(LiOH)、碳酸锂(Li2CO3)等杂质在粒子表面堆积,给正极制造工序、电池性能带来不良影响。
但是,在正极的制造工序中,会经过将锂-镍复合氧化物粒子、导电助剂、粘合剂与有机溶剂等混合而成的正极合剂浆料涂布在铝等集电体上并干燥的工序。通常,在正极合剂浆料的制造工序中,氢氧化锂与粘合剂反应使浆料粘度急剧增加,这也是使浆料凝胶化的原因。这些现象会引起品质不良或缺陷、制造正极的成品率下降,造成产品的品质差异。另外,在充放电时,这些杂质会与电解液反应产生气体,很有可能产生电池的稳定性问题。
因此,当使用镍系作为正极活性物质时,为了防止上述氢氧化锂(LiOH)等杂质的产生,需要在脱二氧化碳的干燥(低湿度)环境下进行上述正极制造工序。因此,虽然镍系有希望作为理论容量高的锂离子二次电池材料,但由于维持其制造环境需要巨额的引入设备成本和运行成本,成为妨碍其普及应用的问题。
为了解决这个问题,提出了使用涂布剂包覆锂-镍复合氧化物粒子表面上的方法。这种涂布剂大致分为无机类涂布剂和有机类涂布剂,作为无机类涂布剂,提出了氧化钛、氧化铝、磷酸铝、磷酸钴、氟化锂等材料,作为有机类涂布剂,提出了气相二氧化硅、羧甲基纤维素、含氟聚合物等材料。
例如,在专利文献1中,提出了在锂-镍复合氧化物粒子表面形成氟化锂(LiF)或含氟聚合物层的方法,在专利文献2中,提出了在锂-镍复合氧化物粒子上形成含氟聚合物层,进而还添加用于中和杂质的路易斯酸化合物的方法。任一处理均可通过含有氟系材料的涂层将锂-镍复合氧化物粒子表面改质为疏水性,抑制水分的吸附,并抑制氢氧化锂(LiOH)等杂质的堆积。
然而,含有在这些涂布方法中所用的上述氟系材料的涂层,只不过是仅仅通过静电引力附着在锂-镍复合氧化物粒子上。因此,在浆料制造工序中再溶解于作为溶剂使用的N-甲基-2-吡咯烷酮(NMP)中,由此,涂层容易从锂-镍复合氧化物粒子脱离。其结果,必须在脱二氧化碳的干燥(低湿度)环境下储存正极,不仅不能充分抑制镍系中早已成为问题的品质不良或缺陷、成品率降低的问题,还无法在实质上充分解决由于杂质产生而引起的电池稳定性的问题。
现有技术文献
专利文献
专利文献1:日本特开2013-179063号公报
专利文献2:日本特表2011-511402号公报
技术实现要素:
发明要解决的问题
本发明是鉴于上述现有技术中存在的问题而完成的,其目的是,提供一种能够在大气环境下处理,且能够得到对电池特性无不良影响的锂-镍复合氧化物粒子覆膜的带覆膜的锂-镍复合氧化物粒子及其制造方法。
解决问题的方法
本发明人为了解决上述现有技术中存在的问题而进行了悉心研究,结果是发现了:使环状硅氧烷接触镍系锂-镍复合氧化物粒子的表面而形成表面覆膜的带覆膜的锂-镍复合氧化物粒子,与涂层具有强的粘附性,并且该化合物能够抑制水分和二氧化碳气体的透过并且具有锂离子传导性。另外,对该带覆膜的锂-镍复合氧化物粒子而言,在对正极合剂浆料进行混炼的情况下,涂层也不会从粒子表面脱落。因此,还发现了一种即使在并不是脱二氧化碳的干燥(低湿度)环境的一般环境下,涂层也不会脱离,能够稳定地抑制水分和二氧化碳气体吸附的优异的带覆膜的锂-镍复合氧化物粒子及其制造方法,从而完成了本发明。
具体而言,本发明提供以下技术方案。
即,本发明的第一发明是带覆膜的锂-镍复合氧化物粒子的制造方法,其特征在于,使环状硅氧烷接触镍系锂-镍复合氧化物粒子的表面而形成表面覆膜。
本发明的第二发明是在第一发明所述的带覆膜的锂-镍复合氧化物粒子的制造方法中,所述环状硅氧烷是下述通式(1)的2,4,6,8-四甲基环四硅氧烷,通过气相接触形成表面覆膜。
[化1]
本发明的第三发明是在第二发明所述的带覆膜的锂-镍复合氧化物粒子的制造方法中,所述气相接触时的环境温度为40℃~100℃。
本发明的第四发明是在第二或第三发明所述的带覆膜的锂-镍复合氧化物粒子的制造方法中,在所述气相接触后的剩余氢原子上,加成一端具有不饱和键的有机醚化合物或有机酯化合物。
本发明的第五发明是在第一至第四发明中任一项所述的带覆膜的锂-镍复合氧化物粒子的制造方法中,所述锂-镍复合氧化物以下述通式(2)表示。
LixNi(1-y-z)MyNzO2···(2)
(式中,x为0.80~1.10,y为0.01~0.20,z为0.01~0.15,1-y-z为大于0.65的值,M表示选自于Co和Mn中的至少一种元素,N表示选自于Al、In和Sn中的至少一种元素。)
本发明的第六发明是一种带覆膜的锂-镍复合氧化物粒子,其是通过第一至第五发明中任一项所述的制造方法得到,且所述表面覆膜以下述通式(3)表示。
(R1R2SiO)a[(R1)(R2)2SiO1/2]b(R1SiO3/2)c···(3)
(式中,R1表示甲基,R2表示至少包含选自于由醚基和氢基所组成的组中的一种以上的官能团。a、b和c表示包括0的正整数。)
本发明的第七发明是在第六发明所述的带覆膜的锂-镍复合氧化物粒子中,所述通式(3)中的R2是下述通式(4)的醚基。
-CnH2n-O-CmH2m+1···(4)
(式中,n、m分别为从2到10的整数)
本发明的第八发明是在第六或第七发明所述的带覆膜的锂-镍复合氧化物粒子中,相对于锂-镍复合氧化物粒子,所述表面覆膜的质量为0.1~1.0质量%。
本发明的第九发明是在第六至第八发明中任一项所述的带覆膜的锂-镍复合氧化物粒子中,所述带覆膜的锂-镍复合氧化物粒子被用作锂离子电池的正极活性物质。
本发明的第十发明是在第六至第九发明中任一项所述的锂离子电池用的复合氧化物正极活性物质中,所述带覆膜的锂-镍复合氧化物粒子是平均粒径为5~20μm的球状粒子。
发明效果
根据本发明优异的带覆膜的锂-镍复合氧化物粒子及其制造方法,通过使环状硅氧烷接触镍系锂-镍复合氧化物粒子的表面而制成的带覆膜的锂-镍复合氧化物粒子,由于其环境稳定性高,因此,能够抑制因吸收水分、二氧化碳而引起的杂质的产生,且粘附性高,涂层不容易脱离,而且,具有锂离子传导性。
上述带覆膜的锂-镍复合氧化物粒子可作为高容量锂离子电池用的复合氧化物正极活性物质,其中,可采用钴系(LCO)、三元系(NCM)中一直使用的制造设备来代替至今严格控制二氧化碳气体浓度和水分浓度的正极制造设备。
附图说明
图1是表示表面被实施例1的通式(3)所表示的化合物包覆的锂-镍复合氧化物粒子的透射电子显微镜(Transmission electron microscope,TEM)照片。
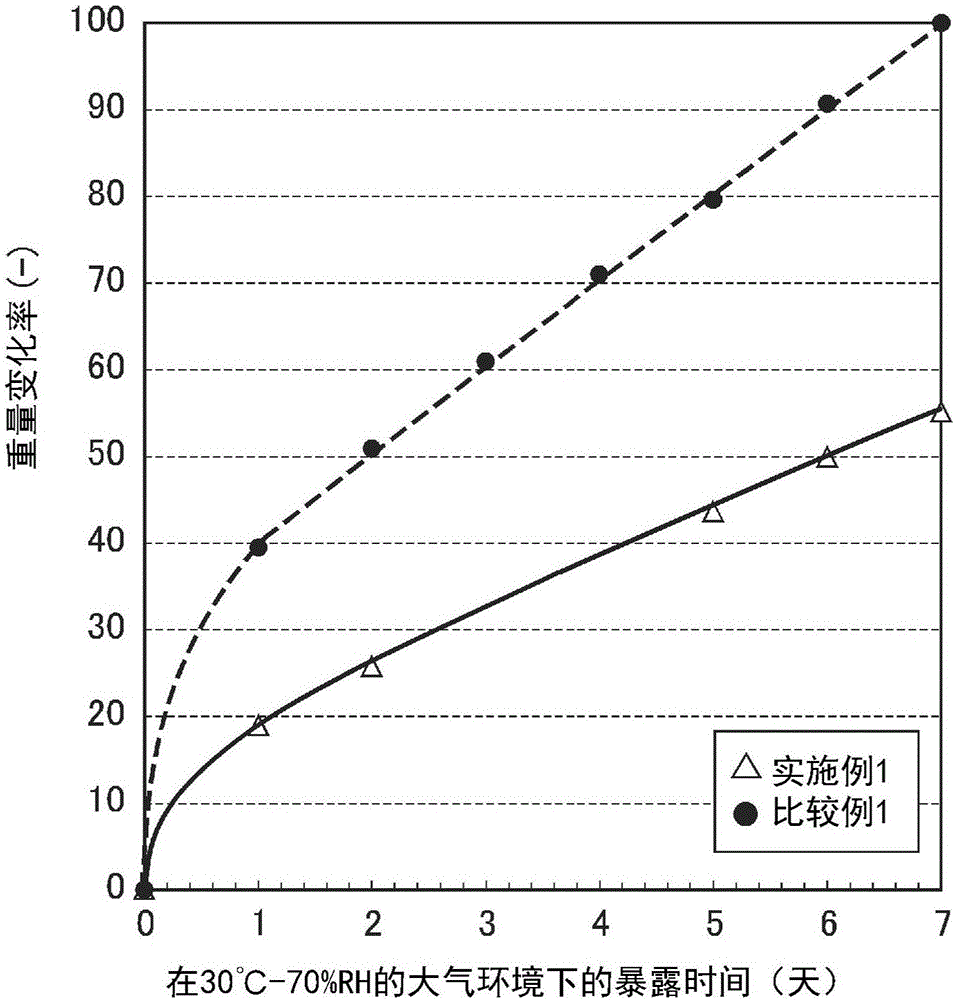
图2是实施例1和比较例1的静置一周时单位粒子质量的变化率。
图3是根据实施例1和比较例1的循环试验而得到的容量変化率。
图4是根据循环试验前的阻抗试验而得到的Cole-Cole图。
图5是根据500次循环试验后的阻抗试验而得到的Cole-Cole图。
具体实施方式
下面,详细说明本发明的带覆膜的锂-镍复合氧化物粒子及其制造方法。需要说明的是,对本发明的解释并不限定于以下的详细说明。在本发明中,也有时将由一次粒子凝集而成的二次粒子称为锂-镍复合氧化物粒子。
[在镍系锂-镍复合氧化物粒子表面包覆的化合物]
包覆镍系锂-镍复合氧化物粒子表面的化合物具有下述通式(3)的结构,具有三维构成的网状结构。
(R1R2SiO)a[(R1)(R2)2SiO1/2]b(R1SiO3/2)c···(3)
通式(3)中R1表示甲基,R2表示含醚键的烃(以下,也称为醚基)或氢原子。a、b和c表示包括0的正整数。其中,R2优选为以下述通式(4)表示的醚基。通过在R2中引入含醚结构的烃,进一步提高锂离子的传导性。
-CnH2n-O-CmH2m+1···(4)
(式中,n、m分别为从2到10的整数)
作为包覆的化合物,可以是环状硅氧烷,从后述的制造容易的方面来看,特别优选以下述式(1)表示的2,4,6,8-四甲基环四硅氧烷。
[化2]
该化合物在被称为镍系锂-镍复合氧化物粒子的表面活性位点的、反应性高的位点,进行开环反应和聚合反应,形成具有三维结构的覆膜。与此同时,也与锂-镍复合氧化物粒子表面的羟基反应。因此,与仅通过静电引力附着的情况相比,具有更强的粘附性,在浆料制造工序等中,该化合物难以脱离,从而能够形成环境稳定性更高的带覆膜的锂-镍复合氧化物粒子。因此,不会因溶剂等原因而脱落,由此能够形成环境稳定性极高的带覆膜的锂-镍复合氧化物粒子。
另外,相对于镍系锂-镍复合氧化物粒子100质量%,式(3)化合物的包覆量优选为0.1~1.0质量%,更优选为0.2~0.5质量%。低于0.1质量%时有处理不充分的倾向,高于1.0质量%时有粒子之间容易凝集的倾向。
[镍系锂-镍复合氧化物粒子]
镍系锂-镍复合氧化物粒子是球状粒子,其平均粒径优选为5~20μm。通过选定该范围,锂-镍复合氧化物粒子可同时具有良好的电池性能和良好的电池循环寿命(循环特性),因此优选该范围。
另外,镍系锂-镍复合氧化物粒子优选以下述通式(2)表示。
LixNi(1-y-z)MyNzO2···(2)
式中,x为0.80~1.10,y为0.01~0.20,z为0.01~0.15,1-y-z为大于0.65的值,M表示选自于Co和Mn中的至少一种元素,N表示选自于Al、In和Sn中的至少一种元素。
另外,从容量的观点来看,1-y-z的值(镍含量)优选为大于0.70的值,更优选为大于0.80的值。
钴系(LCO)、三元系(NCM)、镍系(NCA)的电极能量密度(Wh/L)分别为2160Wh/L(LiCoO2)、2018.6Wh/L(LiNi0.33Co0.33Mn0.33Co0.33O2)、2376Wh/L(LiNi0.8Co0.15Al0.05O2)。因此,通过将该镍系锂-镍复合氧化物粒子用作锂离子电池的正极活性物质,能够制作高容量的电池。
[带覆膜的锂-镍复合氧化物粒子的制造方法]
作为带覆膜的锂-镍复合氧化物粒子的制造方法,即作为采用式(3)化合物包覆镍系锂-镍复合氧化物粒子的方法,只要是通过接触而形成表面覆膜的方法,即可采用各种方法而无特别限定。例如,使镍系锂-镍复合氧化物粒子分散在有机二氯硅烷溶液中,并通过交联反应在镍系锂-镍复合氧化物粒子表面生成涂膜,由此可制造本发明的带覆膜的锂-镍复合氧化物粒子。此时,通过添加碳酸钙也能够控制反应速度。
具体而言,既可以通过使镍系锂-镍复合氧化物粒子分散在硅氧烷化合物溶液中后进行干燥来制造,也可以通过将溶剂中溶解的硅氧烷化合物喷雾在该锂-镍复合氧化物粒子上并加热干燥来制造。
另外,例如,也可以通过将锂镍复合氧化物和式(1)所示的2,4,6,8-四甲基环四硅氧烷等环状硅氧烷化合物在球磨机中进行混合来制造本发明的带覆膜的锂-镍复合氧化物粒子。
如此地,可以采用各种处理方法制造本发明所用的带覆膜的锂-镍复合氧化物粒子,特别是,利用在上述锂-镍复合氧化物粒子表面存在的催化活性的方法,能够简单且有效地进行包覆,因此特别优选。
即,通过将式(1)所示的环状硅氧烷和锂-镍复合氧化物分别放入容器内,在密闭体系内的气相条件下放置,或者,设置挥发槽,由装有环状硅氧烷的装置外部导入等方式,在无需施加物理上的力的情况下,即可得到自然包覆的带覆膜的锂-镍复合氧化物粒子。总之,挥发的环状硅氧烷到达该锂-镍复合氧化物粒子,并以分子形式吸附在上述锂-镍复合氧化物粒子表面。由于吸附引起密闭体系中环状硅氧烷的蒸气压下降,因此,连续不断地挥发新的环状硅氧烷。
优选在密闭体系内,在减压或常压条件下将整个容器加热至40~100℃,持续1~24小时进行加热处理。即,在包覆膜的形成中,通过使放入另一容器的环状硅氧烷化合物挥发,并使挥发的环状硅氧烷化合物与上述锂-镍复合氧化物粒子进行气相接触,从而在上述全部锂-镍复合氧化物粒子的整个表面适当地形成包覆膜(通过气相法形成包覆膜)。
作为包覆膜形成时的温度条件,由于本制造方法是利用上述锂-镍复合氧化物粒子表面存在的催化活性的方法,因此不需要在特殊的高温环境下进行,但是,当整个真空容器的温度低于40℃时,环状硅氧烷化合物挥发不充分,会出现难以包覆整个上述锂-镍复合氧化物粒子的情况。另一方面,当温度为高于100℃的高温时,有可能会引起环状硅氧烷化合物或上述锂-镍复合氧化物粒子的变质。因此,作为温度条件,如上所述优选将整个真空容器在40~100℃环境下进行。
另外,关于处理时间,当处理时间过少时,包覆膜的形成不充分,另一方面,即使处理时间长,包覆量达到一定量以后也不会再增加。因此,作为处理时间,如上所述为1小时~24小时,更优选为6小时~12小时。
作为基于气相法的包覆膜的形成条件,控制在上述温度条件、处理时间条件,由此,能够进行在容器内设置上述锂-镍复合氧化物粒子和具有挥发性的环状硅氧烷化合物的操作。通过上述简单的操作,使挥发的环状硅氧烷化合物接触上述锂-镍复合氧化物粒子表面,能够在上述整个锂-镍复合氧化物粒子表面以及全部细微部分有效地形成包覆膜。另外,为了更有效且更可靠地在上述全部锂-镍复合氧化物粒子上包覆环状硅氧烷化合物,优选在真空容器内部内置如搅拌器这类的混合装置。
如此地,上述在锂-镍复合氧化物粒子表面吸附的环状硅氧烷化合物,通过开环聚合形成网状结构的硅化合物,并在上述锂-镍复合氧化物粒子表面交联并包覆。因此,与仅通过静电引力包覆的情况不同,粘附更加牢固,从而能够制造出环境稳定性高的优异的带覆膜的锂-镍复合氧化物粒子。
[氢化硅烷化反应(Hydrosilylation)]
在式(1)所示的2,4,6,8-四甲基环四硅氧烷等环状硅氧烷中,存在很多Si-H基。因此,采用仅进行了上述包覆处理的带覆膜的锂-镍复合氧化物粒子来制成的正极合剂浆料,可能会产生氢气,并溶胀。因此,优选在该剩余的Si-H基上加成烯烃、炔烃等脂肪族不饱和烃以置换Si-H键,即优选进行氢化硅烷化。通过氢化硅烷化,能够减少涂层中硅氧烷化合物的Si-H基,防止生成的正极合剂浆料中的Si-H基导致氢气产生。
上述加成至硅氧烷化合物的脂肪族不饱和烃是,在任意位置,优选在末端有至少一个不饱和键(双键、三键)的脂肪族不饱和烃。由于在末端位置具有不饱和键(双键、三键),氢化硅烷化反应快速地进行,因此优选。另外,通过使用引入了醚结构的脂肪族不饱和烃,能够进一步提高锂离子传导性,因此优选。需要说明的是,上述醚基的醚键除了以通式(4)表示的键外,还包括以-C-O-C-表示的键,例如酯键等。
作为脂肪族不饱和烃,例如,可以是1-(乙烯氧基)甲烷、1-(乙烯氧基)乙烷、1-(乙烯氧基)丙烷、1-(乙烯氧基)丁烷、1-(乙烯氧基)戊烷、1-(乙烯氧基)己烷、1-(乙烯氧基)庚烷、1-(乙烯氧基)辛烷、1-(乙烯氧基)壬烷、1-(乙烯氧基)癸烷等乙烯烷基醚,1-(2-丙烯氧基)甲烷、1-(2-丙烯氧基)乙烷、1-(2-丙烯氧基)丙烷、1-(2-丙烯氧基)丁烷、1-(2-丙烯氧基)戊烷、1-(2-丙烯氧基)己烷、1-(2-丙烯氧基)庚烷、1-(2-丙烯氧基)辛烷、1-(2-丙烯氧基)壬烷、1-(2-丙烯氧基)癸烷等烯丙基烷基醚类及上述烷基内含有一个以上双键的衍生物等。
如果醚键的一端具有不饱和键,则可以在醚键的一端位置加成Si-H基。通过在醚键的一端位置的Si-H基上加成,氢化硅烷化反应快速进行,因此优选。
在催化剂存在的条件下能够优选进行氢化硅烷化反应,例如,能够通过在10℃~300℃的气相或液相中接触1小时左右的方法等进行上述反应。
作为催化剂,例如,可使用铂族催化剂。作为铂族催化剂,例如,钌系催化剂、铑系催化剂、钯系催化剂、锇系催化剂、铱系催化剂、铂系催化剂等较好,特别是,钯系催化剂和铂系催化剂较好。作为钯系催化剂,例如,可以是氯化钯(II)、四氨钯(II)酸氯化铵(塩化テトラアンミンパラジウム(Ⅱ)酸アンモニウム)、氧化钯(Ⅱ)等。作为铂系催化剂,例如,可以是氯化铂(Ⅱ)、四氯铂酸(Ⅱ)、氯化铂(IV)、六氯铂(Ⅳ)、六氯铂酸(Ⅳ)铵、氧化铂(Ⅱ)、氢氧化铂(II)、二氧化铂(IV)、氧化铂(IV)、二硫化铂(IV)、硫化铂(IV)、六氯铂酸(IV)钾等。另外,也可以使用在这些钯系催化剂、铂系催化剂中加入三-n-烷基(n=1~8)甲基氯化铵和三-n-烷基胺,采用水/有机溶剂体系进行离子对提取后的有机溶剂相。
另外,根据需要,也可以与上述方法结合使用胺类催化剂,还可以使用紫外线、γ射线或X射线等电磁波或等离子体等。需要说明的是,脂肪族不饱和烃对于Si-H基的加成率可以通过红外吸收光谱中的Si-H基吸收率而求得。
实施例
下面,列举比较例具体地说明本发明的实施例。但是,本发明不仅由以下实施例而限定。
(实施例1)
作为镍系锂-镍复合氧化物粒子,将过渡金属组成以Li1.03Ni0.82Co0.15Al0.03表示的复合氧化物粒子10g放入密闭型恒温槽内,与放入到另一容器的2,4,6,8-四甲基环四硅氧烷1.0g一同在减压条件下、在40℃条件下放置8小时。然后,从体系中除去2,4,6,8-四甲基环四硅氧烷,在90℃条件下真空干燥4小时。测定干燥后的质量,由于每1g该锂-镍复合氧化物粒子质量增加3mg,确认包覆了0.3质量%的硅氧烷化合物。
然后,将50g得到的处理粉状体用300g异丙醇稀释,加入50g烯丙基丁基醚[(1-(2-丙烯氧基)丁烷)]和0.07g六氯铂(IV)酸六水合物,一边搅拌一边在75℃条件下反应6小时。然后,过滤,用异丙醇洗涤两次,在100℃的真空干燥器中干燥2小时,得到处理粉状体。采用图1所示的透射电子显微镜确认覆膜,确认在整个粒子表面形成了约5nm的均匀覆膜。
将包覆有上述硅氧烷化合物的粒子作为实施例1的带覆膜的锂-镍复合氧化物粒子,进行下面所示的大气稳定性试验、凝胶化试验和电池特性试验(充放电试验、循环试验)。
(比较例1)
将未包覆硅氧烷化合物的粒子作为比较例1的锂-镍复合氧化物粒子,进行下面所示的大气稳定性试验、凝胶化试验和电池特性试验(充放电试验、循环试验)。
<大气稳定性试验>
将实施例和比较例的锂-镍复合氧化物粒子分别装入2.0g玻璃瓶内,在温度为30℃、湿度为70%的恒湿恒温槽内静置1周,测定由初始质量增加的质量,计算单位粒子质量的变化率。将比较例1的锂-镍复合氧化物粒子1周后的单位粒子质量的变化率作为100,在图2中示出实施例1和比较例1的每日变化率。
由图2可知,与比较例1中未包覆硅氧烷化合物的锂-镍复合氧化物粒子相比,实施例1中包覆硅氧烷化合物的带覆膜的锂-镍复合氧化物粒子单位质量的变化率更小。根据本结果,证实了通过包覆硅氧烷化合物,能够抑制大气中水分和二氧化碳气体的透过。
<凝胶化试验>
根据以下顺序制作正极合剂浆料,测定正极合剂浆料粘度的经时变化,观察粘度增加和凝胶化。
以各质量比为45:2.5:2.5:50的配比,称量实施例1和比较例1的锂-镍复合氧化物粒子、导电助剂、粘合剂和N-甲基-2-吡咯烷酮(NMP),再加入1.5质量%的水后,采用自转公转混合器搅拌,得到正极合剂浆料。将得到的浆料储存在25℃培养箱内,针对实施例1和比较例1,分别用刮铲搅拌并确认粘度增加和凝胶度的经时变化,并储存至完全凝胶化。
实施例1的浆料达到完全凝胶化需要4天,相对于此,比较例1的浆料达到完全凝胶化需要1天。由此,证实了实施例1的浆料通过用硅氧烷化合物包覆镍系锂-镍复合氧化物粒子,能够抑制氢氧化锂(LiOH)、碳酸锂(Li2CO3)等杂质的生成,能够防止这些杂质与粘合剂反应引起的浆料凝胶化和浆料粘度的增加。
另外,当采用氟化物包覆锂-镍复合氧化物粒子时,认为由于氟化物通常溶解在N-甲基-2-吡咯烷酮(NMP)中,所以即使氟化物进行包覆,覆膜也会溶解。因此,认为其与实施例1的带覆膜的锂-镍复合氧化物粒子不同,在储存制成的正极时,难以抑制杂质生成。因此,在电池驱动时难以抑制储存正极时生成的杂质引起的与电解液反应并伴有气体产生,需要高额的储存设备。
<电池特性评价>
按照以下步骤,制作评价用非水电解质二次电池(锂离子二次电池),进行电池特性评价。
[二次电池的制造]
本发明得到的锂-镍复合氧化物粒子的电池特性评价是,制作硬币型电池和叠层型电池,采用硬币型电池进行充放电容量测定,采用叠层型电池进行充放电循环试验和电阻测定。
(a)正极
将得到的实施例1和比较例1的锂-镍复合氧化物粒子与作为导电助剂的乙炔黑、作为粘合剂的聚偏氟乙烯(PVdF)以85:10:5的质量比混合,溶解在N-甲基-2-吡咯烷酮(NMP)溶液中,制成正极合剂浆料。采用逗点涂布机将该正极合剂浆料涂布在铝箔上,在100℃条件下加热并干燥,进而得到正极。将得到的正极通过辊压机施加负荷,制成正极密度增加的正极片。将该正极片冲切成直径φ9mm用于评价硬币型电池,再切出50mm×30mm用于叠层型电池,分别用作评价用正极。
(b)负极
将作为负极活性物质的石墨与作为粘合剂的聚偏氟乙烯(PVdF)以92.5:7.5的质量比混合,溶解在N-甲基-2-吡咯烷酮(NMP)溶液中,得到负极合剂糊料。
与正极同样地,采用逗点涂布机将该负极合剂浆料涂布在銅箔上,在120℃条件下加热、干燥,进而得到负极。将得到的负极通过辊压机施加负荷,制成电极密度增加的负极片。将得到的负极片冲切成直径φ14mm用于硬币型电池,再切出54mm×34mm用于叠层型电池,分别用作评价用负极。
(c)硬币型电池和叠层型电池
将制成的评价用电极在真空干燥机中以120℃干燥12小时。然后,使用该正极在露点控制为-80℃的氩气环境的手套箱内制作2032型硬币型电池和叠层型电池。在电解液中,以1M的LiPF6为支持电解质的碳酸乙烯酯(EC)与碳酸二乙酯(DEC)比例为3:7(富山药品工业株式会社制),使用玻璃隔板作为隔板,制作各评价电池。
<<充放电试验>>
对于制成的硬币型电池,组装后静置24小时,开路电压OCV(Open Circuit Voltage)稳定后,在25℃恒温槽内,以0.2C倍率的电流密度充电直至截止电压达4.3V,停止1小时后,测定放电至截止电压达3.0V时的放电容量,进行充放电试验。
实施例1的硬币型电池的初始放电容量为191.82mAh/g,相对于此,比较例1的硬币型电池的初始放电容量为191.93mAh/g。
<<循环试验>>
对于制成的叠层型电池,与硬币型电池同样地,组装后静置24小时,开路电压稳定后,在25℃恒温槽内,以0.2C倍率的电流密度充电直至截止电压达4.1V,停止1小时后,放电至截止电压达3.0V。然后,将该电池在60℃恒温槽内进行以2.0C倍率的电流密度重复4.1V-CC充电、3.0V-CC放电的循环试验,进行确认500次循环后的容量保持率的循环试验。根据循环试验得到的容量变化率如图3所示,循环试验前的阻抗试验结果如图4所示,500次循环试验后的阻抗试验结果如图5所示。
根据图3和图4,关于循环试验前的容量保持量和阻抗Cole-Cole图,实施例1和比较例1的叠层电池几乎相同,根据图3和图5,关于500次循环试验后阻抗试验后的容量保持量,与比较例1的叠层型电池相比,实施例1的叠层型电池保持更高的电池容量保持量。这是因为,实施例1的叠层电池所用的锂-镍复合氧化物粒子包覆了硅氧烷化合物,因此在长循环的使用中容量保持量的降低量也少。因此,可证实实施例1的带覆膜的锂-镍复合氧化物粒子是容量保持率更高的优越的带覆膜的锂-镍复合氧化物粒子。
- 还没有人留言评论。精彩留言会获得点赞!