抗PCSK9单克隆抗体的制作方法
本发明涉及抗体工程
技术领域:
,具体涉及本发明涉及全人源的抗PCSK9的单克隆抗体、及其获得方法与应用。
背景技术:
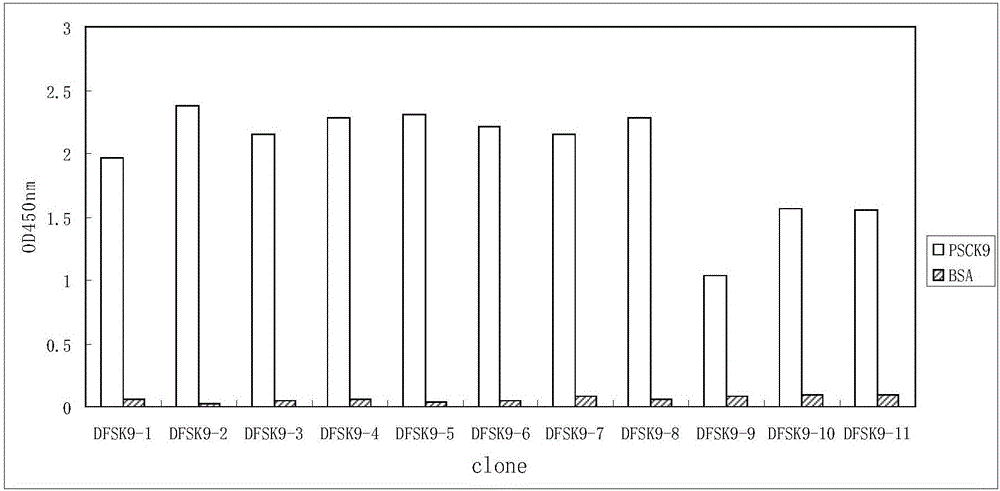
:PCSK9(前蛋白转化酶枯草溶菌素9,Proproteinconvertasesubtilisin/kexintype9)属于前蛋白转化酶家族蛋白酶K亚家族。人PCSK9基因定位于染色体1p32.3,长约22kb,共有12个外显子,编码含692个氨基酸残基的蛋白质。PCSK9蛋白由信号肽、前结构域、催化结构域和羧基末端结构域(V结构域)组成,它作为可溶性的74kDa的前体合成,在内质网中经过自身催化裂解产生14kDa的前肽和60kDa的成熟的蛋白酶。PCSK9主要在肝脏、肠道和肾脏表达,皮肤和神经系统也有少量表达,但是只有肝脏中的PCSK9可以分泌到血液循环系统中。研究表明,PCSK9能介导低密度脂蛋白受体(LDLR)降解从而调节血浆中LDL胆固醇(LDL-C)水平,而LDLR介导肝内的LDL胞吞过程是从循环系统中清除LDL的主要途径。LDLR是1个多结构域的蛋白,胞外域与表皮生长因子前体同源结构域EGF-A、EGF-B、EGF-C紧连。PCSK9介导LDLR降解首先需要与LDLR结合,LDLR上结合位点主要是EGF-A,形成PCSK9与EGF-A复合物。有研究表明,PCSK9也可通过极低密度脂蛋白受体、载脂蛋白B受体、载脂蛋白E受体2调节胆固醇代谢,但其中的分子机制并不明确。基础研究和临床试验表明,通过外源性的干预措施抑制PCSK9活性,可以加速血浆中LDL的清除,从而达到降血脂的作用。目前PCSK9的抑制剂主要包括单克隆抗体、反义核苷酸、小分子干扰RNA、模拟肽和小分子抑制剂等。单克隆抗体药物是今年生物医药领域的研发热点,具有靶向性强、特异性高和毒副作用低等特点,代表了药品治疗领域的最新发展方向。以PCSK9为靶标的单克隆抗体可以与PCSK9发生特异性结合,阻断PCSK9与LDLR的相互作用,减慢LDLR的降解过程从而发挥降低LDL-C水平的作用。临床实验数据显示了抗PCSK9单抗药物的安全性、有效性及独特的临床应用价值。全人源抗体是治疗性抗体发展的主要方向。抗体库技术的出现为人源抗体的制备筛选提供了良好的技术平台。抗体库技术绕过了以往单抗研制过程中必须的杂交瘤过程,甚至不需要经过免疫过程即可获得各种抗体基因及抗体分子片段。噬菌体抗体库是最早出现也是目前应用最广泛的抗体库。噬菌体抗体库根据抗体基因的来源分为免疫库和非免疫库,非免疫库又包括天然库、半合成库和全合成库。噬菌体抗体库的筛选模拟了抗体亲和力成熟的过程,通常将抗原包被在固相介质上,加入待筛选的噬菌体抗体库,通过数轮“吸附-洗涤-洗脱-扩增”的过程(即淘选)直至筛选到高亲和力特异的抗体。目前多家制药公司都在积极开发针对PCSK9的单抗药物。安进的Repatha(evolocumab)和赛诺菲/再生元的Praluent(alirocumab)均为全人源抗体,已于2015年先后被批准上市,用于原发性高胆固醇血症和家族性高胆固醇血症(杂合子和纯合子)的治疗。在他汀基础上加用Evolocumab可使原发性高胆固醇血症患者的LDL-C降低77%,杂合子家族性高胆固醇血症患者的LDL-C降低68%,纯合子家族性高胆固醇血症患者的LDL-C降低31%。evolocumab耐受性良好,目前无任何明显的安全性问题。辉瑞的人源化单抗bococizumab正在进行三期临床,诺华的人源化单抗lodelcizumab正在进行二期临床。罗氏及默沙东也在开展临床试验。目前国内该领域依然缺乏自主研发的具有高亲和力的抗PCSK9的全人源抗体。技术实现要素:本发明提供了抗PCSK9的单克隆抗体;本发明从全合成抗体库中筛选出抗PCSK9的单克隆抗体,然后通过计算机辅助设计分析,构建小容量合成噬菌体抗体轻链库的方法,对筛选获得的抗PCSK9单克隆抗体的轻链的CDR1、2、3区突变建库;筛选后,选取亲和力较高的单克隆抗体,再对其重链CDR1、2、3区突变建库进行筛选,最终筛选到了高亲和力的抗PCSK9的单克隆抗体。本发明抗PCSK9抗体具有全新的序列,该抗体在体外特别是细胞水平上功能良好,极具医学应用前景。为实现上述目的,本发明一种抗PCSK9的单克隆抗体,包括:轻链和重链;所述轻链的互补决定区CDR1、CDR2和CDR3分别用LCDR1、LCDR2和LCDR3表示;并且所述重链的互补决定区CDR1、CDR2和CDR3分别用HCDR1、HCDR2和HCDR3表示;LCDR1包含RASQSIDNRLT(SEQNO.22)、RASQSVRNWLD(SEQNO.23)、RASQGINSWLN(SEQNO.24)、RASQNVNNWLN(SEQNO.25)、RASQNINSWLN(SEQNO.26)、RASQNINNWLN(SEQNO.27)、RASQGIHNWLN(SEQNO.28)、RASQDVDSWLT(SEQNO.29)、RASQSVRNWLN(SEQNO.30)、RASQDVRNWLT(SEQNO.31)或RASQSIRSYLN(SEQNO.32)中的任一种;LCDR2包含DASSRQS(SEQNO.33)、GASTLES(SEQNO.34)、AASTRET(SEQNO.35)、GASSRQS(SEQNO.36)、GASTRPT(SEQNO.37)、DASNRQS(SEQNO.38)、GASNLAS(SEQNO.39)、DASNLQS(SEQNO.40)或DASSRPT(SEQNO.41)中的任一种;LCDR3包含QQPENDPTT(SEQNO.42)、QQDNDIPLT(SEQNO.43)、QQWNNTPNT(SEQNO.44)、QQDNDMPLT(SEQNO.45)、QQWFDVPTT(SEQNO.46)、QQWDDTPNT(SEQNO.47)、QQNSNIPLT(SEQNO.48)、QQDSKIPLT(SEQNO.49)、QQWTDTPLT(SEQNO.50)、QQDDSTPPT(SEQNO.51)或QQGDSMPMT(SEQNO.52)中的任一种;HCDR1包含GGTFTNNA(SEQNO.53)、GYTVTSYG(SEQNO.54)或GYSLTSYG(SEQNO.55)中的任一种;HCDR2包含RIIPMFGMA(SEQNO.56)、WLSFYNGNT(SEQNO.57)、WVTFYNGNT(SEQNO.58)、WVSFYQGNT(SEQNO.59)、WVSFYNGQT(SEQNO.60)或WVSFYNGNS(SEQNO.61)中的任一种;HCDR3包含AREGIPMI(SEQNO.62)、ARGYSLDV(SEQNO.63)、ARGYGMSI(SEQNO.64)、ARGFGMDR(SEQNO.65)、ARGYGMTV(SEQNO.66)或ARGFGLSV(SEQNO.67)。其中,所述轻链可变区氨基酸序列优选SEQNO.11、SEQNO.12、SEQNO.13、SEQNO.14、SEQNO.15、SEQNO.16、SEQNO.17、SEQNO.18、SEQNO.19、SEQNO.20或SEQNO.21中的任一种。其中,所述重链可变区氨基酸序列优选SEQNO.1、SEQNO.2、SEQNO.3、SEQNO.4、SEQNO.5、SEQNO.6、SEQNO.7、SEQNO.8、SEQNO.9或SEQNO.10中的任一种。其中,所述重链可变区HCDR1序列为选自GYTVTSYG(SEQNO.54)或GYSLTSYG(SEQNO.55)的氨基酸序列;所述轻链可变区LCDR1序列选自RASQSVRNWLD(SEQNO.23)、RASQNVNNWLN(SEQNO.25)、RASQNINSWLN(SEQNO.26)、RASQNINNWLN(SEQNO.27)或RASQDVDSWLT(SEQNO.29)中的任一种氨基酸序列;所述重链可变区HCDR2序列选自WVSFYQGNT(SEQNO.59)、WVSFYNGQT(SEQNO.60)或WVSFYNGNS(SEQNO.61)中的任一种氨基酸序列;所述轻链可变区LCDR2序列选自GASTLES(SEQNO.34)、AASTRET(SEQNO.35)、GASSRQS(SEQNO.36)、GASTRPT(SEQNO.37)或GASNLAS(SEQNO.39)中的任一种氨基酸序列;所述重链可变区HCDR3序列选自ARGYSLDV(SEQNO.63)、ARGYGMSI(SEQNO.64)、ARGFGMDR(SEQNO.65)或ARGYGMTV(SEQNO.66)中的任一种氨基酸序列;所述轻链可变区LCDR3序列选自QQDNDIPLT(SEQNO.43)、QQDNDMPLT(SEQNO.45)、QQWFDVPTT(SEQNO.46)、QQWDDTPNT(SEQNO.47)或QQDSKIPLT(SEQNO.49)中的任一种氨基酸序列。其中,本发明还提供了多种包含上述轻链或上述重链的抗体、多肽或蛋白。其中,本发明还提供了多种包含上述轻链或上述重链的抗体,所述抗体能够特异性与PCSK9结合,阻断PCSK9与LDLR的结合,提高细胞表面LDLR的数量或血液循环系统中LDLR的水平,降低血液循环系统中LDL或LDL-C的水平。其中,本发明还提供了多种包含上述轻链或上述重链的多核苷酸序列或组合。其中,所述抗PCSK9的单克隆抗体的重链恒定区包含IgG1、IgG2、IgG3和IgG4;所述轻链恒定区包含Cκ或Cλ。其中,所述重链恒定区优选IgG4或IgG2;所述重链的真核表达载体或原核生物表达载体。其中,所述轻链恒定区优选Cκ;所述轻链的真核表达载体或原核生物表达载体。其中,本发明还提供了一种包含上述多核苷酸序列或组合的重组DNA表达载体;所述重组DNA表达载体的DNA序列中包含编码抗PCSK9抗体的上述重链可变区、重链恒定区、轻链可变区和轻链恒定区的氨基酸序列。其中,本发明还提供了一种转染上述重组DNA表达载体的宿主细胞,所述宿主细胞包含原核细胞、酵母、昆虫或哺乳动物细胞。其中,所述原核细胞优选大肠杆菌。其中,所述哺乳动物细胞优选HEK293E细胞、CHO细胞或NS0细胞。其中,本发明还提供了多种含有上述轻链或上述重链的全长抗体、单链抗体、单域抗体、双特异抗体、抗体药物偶联物。其中,本发明还提供了多种含有上述轻链或上述重链的单克隆抗体、人工载体、药物或药物组合物。其中,所述单克隆抗体包含全长抗体和抗PCSK9单克隆抗体的片段,所述片段包含但不限于Fab、Fab’、F(ab’)2、Fv或ScFv。其中,本发明还提供了一种含有上述轻链或上述重链的检测试剂或试剂盒。本发明所述抗体可用于通过消除、抑制或降低PCSK9活性而被改善、缓解、抑制或预防的疾病;所述疾病包含血脂异常、心脑血管疾病和血栓闭塞性疾病。其中,所述血脂异常包含胆固醇升高、甘油三脂升高、低密度脂蛋白升高和高密度脂蛋白降低。所述心血管疾病包含冠状动脉硬化性心脏病、急性心肌梗塞、动脉粥状硬化、中风和外周动脉闭塞性疾病。本发明一种抗PCSK9的单克隆抗体的获得方法,包括如下步骤:(1)、抗PCSK9单链抗体的生物淘选,通过三轮抗体库的富集筛选,从全合成的ScFv噬菌体库中获得了一种亲和力较高的抗体序列DFSK9-1,其重链DFSK9-H1具有SEQNO.1的氨基酸序列,其轻链DFSK9-L1具有SEQNO.11的氨基酸序列;(2)、以DFSK9-1为基础,通过计算机三级结构模拟,设计并构建轻链互补决定区CDR1、CDR2、CDR3突变抗体库,并对这个突变抗体库进行生物淘选和阳性克隆的筛选及鉴定,获得了10种含有不同轻链的单链抗体序列,分别命名为DFSK9-2、DFSK9-3、DFSK9-4、DFSK9-5、DFSK9-6、DFSK9-7、DFSK9-8、DFSK9-9、DFSK9-10、DFSK9-11,对应的轻链可变区分别命名为DFSK9-L2、DFSK9-L3、DFSK9-L4、DFSK9-L5、DFSK9-L6、DFSK9-L7、DFSK9-L8、DFSK9-L9、DFSK9-L10和DFSK9-L11,其对应的氨基酸序列分别见SEQNO.12、SEQNO.13、SEQNO.14、SEQNO.15、SEQNO.16、SEQNO.17、SEQNO.18、SEQNO.19、SEQNO.20和SEQNO.21;将上述单链抗体在噬菌体水平上进行亲和力比较;(3)、选出5株亲和力较高的克隆DFSK9-2、DFSK9-4、DFSK9-5、DFSK9-6和DFSK9-8,设计并构建重链互补决定区CDR1、CDR2、CDR3突变抗体库,再对这个重链突变的抗体库进行生物淘选和阳性克隆的筛选及鉴定,获得了10种不同的单链抗体序列,分别命名为DFSK9-12、DFSK9-13、DFSK9-14、DFSK9-15、DFSK9-16、DFSK9-17、DFSK9-18、DFSK9-19、DFSK9-20和DFSK9-21;其中,DFSK9-12、DFSK9-13、DFSK9-14、DFSK9-15、DFSK9-16、DFSK9-17、DFSK9-18、DFSK9-19、DFSK9-20和DFSK9-21的轻链可变区序列分别是DFSK9-L2、DFSK9-L8、DFSK9-L5、DFSK9-L6、DFSK9-L5、DFSK9-L6、DFSK9-L5、DFSK9-L4、DFSK9-L6、DFSK9-L6;其对应的氨基酸序列分别见SEQNO.12、SEQNO.18、SEQNO.15、SEQNO.16、SEQNO.15、SEQNO.16、SEQNO.15、SEQNO.14、SEQNO.16、SEQNO.16;DFSK9-12、DFSK9-13、DFSK9-14、DFSK9-15、DFSK9-16、DFSK9-17、DFSK9-18、DFSK9-19、DFSK9-20和DFSK9-21的重链可变区序列分别是DFSK9-H2、DFSK9-H8、DFSK9-H7、DFSK9-H3、DFSK9-H6、DFSK9-H4、DFSK9-H4、DFSK9-H9、DFSK9-H5、DFSK9-H10;其对应的氨基酸序列分别见SEQNO.2、SEQNO.8、SEQNO.7、SEQNO.3、SEQNO.6、SEQNO.4、SEQNO.4、SEQNO.9、SEQNO.5、SEQNO.10;将上述单链抗体在噬菌体水平上进行亲和力比较;(4)、将(3)中所述单克隆重链可变区基因和轻链可变基因克隆到真核表达载体,转染宿主细胞,获得抗PCSK9单克隆抗体的全抗。其中,所述CDR为互补决定区(complementarity-determiningregion);所述ScFv为单链抗体(single-chainfragmentvariable);所述ADCs为抗体药物偶联物(antibody-drugconjugates);所述LDLR为低密度脂蛋白受体(LowDensityLipoproteinReceptor);所述LDL-C为低密度脂蛋白胆固醇(LowDensityLipoprotein-Cholesterol);所述HEK293E细胞为人胚肾293E细胞(humanembryonickidney293Ecell);CHO细胞为中国仓鼠卵巢细胞(chinesehamsterovarycell);NS0细胞为小鼠NS0胸腺瘤细胞。本发明相对于现有技术而言,具备的有益效果是:本发明提供的是多种全新的抗PCSK9抗体,与底物结合的亲和力高,能够很好的阻断PCSK9与LDLR的结合,并且影响细胞表面的LDLR的分布和表达,从而提高细胞表面的LDL-R与LDL结合能力,增加细胞对LDL摄取和降解,达到降低保外的LDL和LDL-C的含量,达到降低LDL、LDL-C和总胆固醇目的。本发明提供的单克隆抗体可以用于通过消除、抑制或降低PCSK9活性而改善、缓解、抑制或预防的疾病;所述疾病包含血脂异常、心脑血管疾病和血栓闭塞性疾病;血脂异常包含胆固醇升高、甘油三脂升高、低密度脂蛋白升高和高密度脂蛋白降低等;心血管疾病包含冠状动脉硬化性心脏病、急性心肌梗塞、动脉粥状硬化、中风和外周动脉闭塞性疾病等。说明书附图图1、pScFvDisb-S1质粒图谱;图2、轻链突变抗体库阳性克隆噬菌体单克隆ELISA鉴定单链抗体的相对亲和力;图3、轻链突变抗体库阳性克隆噬菌体梯度ELISA比较单链抗体的相对亲和力;图4、重链突变抗体库阳性克隆噬菌体单克隆ELISA鉴定单链抗体的相对亲和力;图5、重链突变抗体库阳性克隆噬菌体梯度ELISA比较单链抗体的相对亲和力;图6、pTSEG4质粒图谱;图7、pTSEK质粒图谱图8、抗PCSK9全抗体与PCSK9在分子水平上结合试验;图9、抗PCSK9全抗体竞争抑制LDLR与PCSK9结合实验;图10、抗PCSK9全抗体生物学活性实验。具体实施方式本发明详细的实施方法参见实施例,实施例中所述的实验方法和试剂,若无特殊说明均为常规实验方法和试剂。以下实施例仅用于说明和解释本发明,而不是以任何方式限制本发明。本发明提供了一种特异性结合PCSK9的单克隆抗体,所述重链可变区序列包含SEQNO.1、2、3、4、5、6、7、8、9和10中的任一种,所述轻链可变区序列包含SEQNO.11、12、13、14、15、16、17、18、19、20和21中的任一种。优选地,所述特异性结合PCSK9的单克隆抗体的重链可变区序列选自SEQNO.2、3、4、5、6、7、8、9和10中的任一种,所述轻链可变区序列选自SEQNO.12、14、15、16和18中的任一种。通过轻链噬菌体库筛选,所述抗体轻链或其功能性片段的轻链互补决定区LCDR1、LCDR2和LCDR3的氨基酸序列选自以下氨基酸序列中的任一组合(如表1所示):表1、轻链各个CDR区的氨基酸序列通过重链噬菌体库筛选,所述抗体重链或其功能性片段重链的互补决定区CDR1、CDR2和CDR3分别用HCDR1、HCDR2和HCDR3表示:HCDR1为GGTFTNNA(SEQNO.53)、GYTVTSYG(SEQNO.54)或GYSLTSYG(SEQNO.55)中的任一种;HCDR2为RIIPMFGMA(SEQNO.56)、WLSFYNGNT(SEQNO.57)、WVTFYNGNT(SEQNO.58)、WVSFYQGNT(SEQNO.59)、WVSFYNGQT(SEQNO.60)或WVSFYNGNS(SEQNO.61)中的任一种;HCDR3为AREGIPMI(SEQNO.62)、ARGYSLDV(SEQNO.63)、ARGYGMSI(SEQNO.64)、ARGFGMDR(SEQNO.65)、ARGYGMTV(SEQNO.66)或ARGFGLSV(SEQNO.67)中的任一种。优选地,通过重链噬菌体库筛选,所述特异性结合PCSK9的单克隆抗体包含HCDR1、HCDR2和HCDR3序列的重链可变区及含LCDR1、LCDR2和LCDR3序列的轻链可变区;其中,所述重链可变区HCDR1序列为选自GYTVTSYG(SEQNO.54)或GYSLTSYG(SEQNO.55)的氨基酸序列;所述轻链可变区LCDR1序列选自RASQSVRNWLD(SEQNO.23)、RASQNVNNWLN(SEQNO.25)、RASQNINSWLN(SEQNO.26)、RASQNINNWLN(SEQNO.27)或RASQDVDSWLT(SEQNO.29)中的任一种氨基酸序列;所述重链可变区HCDR2序列选自WVSFYQGNT(SEQNO.59)、WVSFYNGQT(SEQNO.60)或WVSFYNGNS(SEQNO.61)中的任一种氨基酸序列;所述轻链可变区LCDR2序列选自GASTLES(SEQNO.34)、AASTRET(SEQNO.35)、GASSRQS(SEQNO.36)、GASTRPT(SEQNO.37)或GASNLAS(SEQNO.39)中的一种氨基酸序列;所述重链可变区HCDR3序列选自ARGYSLDV(SEQNO.63)、ARGYGMSI(SEQNO.64)、ARGFGMDR(SEQNO.65)或ARGYGMTV(SEQNO.66)中的任一种氨基酸序列;所述轻链可变区LCDR3序列选自QQDNDIPLT(SEQNO.43)、QQDNDMPLT(SEQNO.45)、QQWFDVPTT(SEQNO.46)、QQWDDTPNT(SEQNO.47)或QQDSKIPLT(SEQNO.49)中的任一种氨基酸序列。本发明用全合成ScFv单链噬菌抗体库获得特异性抗体的方法,所述全人源的特异性结合PCSK9的单克隆抗体是用噬菌体抗体库技术筛选而得,其步骤在于:(1)、抗PCSK9单链抗体的生物淘选,通过三轮抗体库的富集筛选,获得了一种亲和力较高的抗体序列DFSK9-1;(2)、以DFSK9-1为基础,通过计算机辅助设计,构建轻链CDR123突变库并对该抗体库进行生物淘选和阳性克隆的筛选及鉴定,获得了10种不同轻链的抗体序列的克隆DFSK9-2、DFSK9-3、DFSK9-4、DFSK9-5、DFSK9-6、DFSK9-7、DFSK9-8、DFSK9-9、DFSK9-10、DFSK9-11。将上述10种单链抗体在噬菌体水平进行亲和力比较;(3)、选出两株亲和力较高的克隆,构建重链CDR123库并对该库进行生物淘选和阳性克隆的筛选,获得了种10不同序列的单链抗体DFSK9-12、DFSK9-13、DFSK9-14、DFSK9-15、DFSK9-16、DFSK9-17、DFSK9-18、DFSK9-19、DFSK9-20、DFSK9-21;将上述单链抗体在噬菌体水平上进行亲和力比较;(4)、将(3)中所述单克隆重链可变区基因和轻链可变基因克隆到真核表达载体,转染宿主细胞,获得抗PCSK9单克隆抗体的全抗。优选地,对(4)的抗PCSK9单克隆抗体的全抗再进行亲和力和生物活性试验。具体实施例以下结合附图和实施例详述本发明。实施例1、抗PCSK9单链抗体的生物淘选采用基因克隆的方法改造pCom3载体,改造后的载体命名为pScFvDisb-S1(图1)。以该载体为基础构建全合成噬菌体抗体库。免疫管中包被抗原PCSK9-His10μg/1ml/管,4℃包被过夜。用PBST-4%milk分别封闭免疫管和噬菌体抗体库(噬菌体投入量约为109-1012),37℃封闭1h。封闭后的噬菌体抗体库加入免疫管中进行抗原抗体结合,37℃反应1h。PBST-PBS洗去未结合的噬菌体,0.1MpH2.2的Glycine-HCl洗脱,用1.5MpH8.8的Tris-HCl中和洗脱液至pH7.0左右。洗脱液感染10ml生长至OD值约0.5-0.8的XL1-Blue菌液,37℃先静置30min后150rpm摇床振荡培养1h。取出1%菌液进行梯度稀释,涂布于2YTATG小平皿上,用于计算噬菌体产出量。剩余的菌液离心后涂布于2YTATG大平皿,37℃过夜培养。将过夜培养菌转接至2YTATG液体培养基,摇至对数期后加入M13K07辅助噬菌体感染,28℃培养过夜扩增噬菌体,PEG6000-NaCl沉降纯化噬菌体用于下一轮筛选。共进行3轮噬菌体库富集筛选。实施例2、抗PCSK9单链抗体阳性克隆的筛选经过三轮筛选后,挑取分隔良好的单克隆菌落,接种于加有2YTATG液体培养基的96孔深孔板,37℃,220rpm培养约5h至其对数生长期,每孔加入约1010的辅助噬菌体M13KO7,37℃静置30min后150rpm振荡培养1h。4000rpm,离心15min,沉淀重悬于2YTATKA液体培养基中,28℃,220rpm培养过夜。4000rpm,4℃离心15min,吸取含噬菌体上清进行单克隆ELISA鉴定。筛选得到亲和力较高的单链抗体DFSK9-1,其重链可变区命名为DFSK9-H1,其氨基酸序列见SEQNO.1;其轻链可变区命名为DFSK9-L1,氨基酸序列见SEQNO.11;SEQNO.1(DFSK9-H1重链可变区序列):QVQLVQSGAEVKRPGASVKVSCKASGGTFTNNAISWVRQAPGQGLEWMGRIIPMFGMANYAQKLQGRGTMTTDPSTSTAYMELRSLRSDDTAVYYCAREGIPMIWGQGTTVTVSSSEQNO.11(DFSK9-L1轻链可变区序列):DIQMTQSPSSLSASVGDRVTITCRASQSIDNRLTWYQQKPGKAPKLLIYDASSRQSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQPENDPTTFGQGTKVEIK实施例3、对单链抗体DFSK9-1进行体外亲和力成熟3.1.构建DFSK9-1轻链CDR123突变库用NheI和NotI对pScFvDisb-DFSK9-1质粒进行双酶切,酶切产物琼脂糖凝胶电泳后,切胶回收大小5.5kb的条带;用NheI和NotI对合成的轻链突变库基因VLCDR123M进行双酶切,通用产物回收试剂盒回收产物。突变库基因与载体按摩尔比3:1比例经T4DNA连接酶16℃连接4h。将连接产物电击法转化至XL1-Blue电转感受态中。37℃,150rpm振动培养1h复苏。取1%菌液,稀释后涂小平皿,计算库容量。其余菌液4000rpm离心15min后,沉淀涂布于2YTATG大平皿上,37℃倒置培养过夜。建成的抗体库库容大约为108,随机挑取20个克隆进行序列分析,序列正确率和多样性都大于90%。3.2.噬菌体抗体库的生物淘选和阳性克隆的筛选在按照实施例1和实施例2的方法进行生物淘选和阳性克隆筛选,对亲和力较高的克隆进行测序,共得到10种不同的单链抗体序列,分别命名为DFSK9-2、DFSK9-3、DFSK9-4、DFSK9-5、DFSK9-6、DFSK9-7、DFSK9-8、DFSK9-9、DFSK9-10、DFSK9-11,对应的轻链可变区命名为DFSK9-L2、DFSK9-L3、DFSK9-L4、DFSK9-L5、DFSK9-L6、DFSK9-L7、DFSK9-L8、DFSK9-L9、DFSK9-L10、DFSK9-L11,它们对应的氨基酸序列分别见SEQNO.12、SEQNO.13、SEQNO.14、SEQNO.15、SEQNO.16、SEQNO.17、SEQNO.18、SEQNO.19、SEQNO.20和SEQNO.21;轻链可变区序列SEQNO.12-SEQNO.21如下:SEQNO.12(DFSK9-L2轻链可变区序列):DIQMTQSPSSLSASVGDRVTITCRASQSVRNWLDWYQQKPGKAPKLLIYGASTLESGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQDNDIPLTFGQGTKVEIKSEQNO.13(DFSK9-L3轻链可变区序列):DIQMTQSPSSLSASVGDRVTITCRASQGINSWLNWYQQKPGKAPKLLIYAASTRETGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQWNNTPNTFGQGTKVEIKSEQNO.14(DFSK9-L4轻链可变区序列):DIQMTQSPSSLSASVGDRVTITCRASQNVNNWLNWYQQKPGKAPKLLIYAASTRETGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQDNDMPLTFGQGTKVEIKSEQNO.15(DFSK9-L5轻链可变区序列):DIQMTQSPSSLSASVGDRVTITCRASQNINSWLNWYQQKPGKAPKLLIYGASSRQSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQWFDVPTTFGQGTKVEIKSEQNO.16(DFSK9-L6轻链可变区序列):DIQMTQSPSSLSASVGDRVTITCRASQNINNWLNWYQQKPGKAPKLLIYGASTRPTGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQWDDTPNTFGQGTKVEIKSEQNO.17(DFSK9-L7轻链可变区序列):DIQMTQSPSSLSASVGDRVTITCRASQGIHNWLNWYQQKPGKAPKLLIYDASNRQSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQNSNIPLTFGQGTKVEIKSEQNO.18(DFSK9-L8轻链可变区序列):DIQMTQSPSSLSASVGDRVTITCRASQDVDSWLTWYQQKPGKAPKLLIYGASNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQDSKIPLTFGQGTKVEIKSEQNO.19(DFSK9-L9轻链可变区序列):DIQMTQSPSSLSASVGDRVTITCRASQSVRNWLNWYQQKPGKAPKLLIYDASNLQSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQWTDTPLTFGQGTKVEIKSEQNO.20(DFSK9-L10轻链可变区序列):DIQMTQSPSSLSASVGDRVTITCRASQDVRNWLTWYQQKPGKAPKLLIYGASNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQDDSTPPTFGQGTKVEIKSEQNO.21(DFSK9-L11轻链可变区序列):DIQMTQSPSSLSASVGDRVTITCRASQSIRSYLNWYQQKPGKAPKLLIYDASSRPTGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQGDSMPMTFGQGTKVEIK单克隆噬菌体ELISA鉴定结果如图2所示;3.3.噬菌体水平梯度稀释ELISA鉴定抗PCSK9单链抗体的相对亲和力将本实施例3.2中获得的克隆进行单克隆噬菌体的展示和纯化,进行噬菌体水平的梯度稀释ELISA鉴定单链抗体的相对亲和力。用pH7.2的0.01MPBS缓冲液包被PCSK9-His(300ng/孔/100μl),4℃包被过夜。PBST洗涤3次,PBST-4%milk37℃封闭1h。加入PBST-4%milk五倍梯度稀释的纯化噬菌体样品(100μl/孔),37℃静置1h。用PBST洗涤5次,加入PBST-4%milk1:5000稀释的anti-M13-HRP单克隆抗体(100μl/孔),37℃放置1h。TMB显色试剂盒显色(100μl/孔),室温显色10min,用2MH2SO4(50μl/孔)终止显色,。酶标仪波长450nm和630nm读数。使用软件GraphPadPrism5Demo分析数据并作图,结果如图3所示:结果显示筛选出的噬菌体单链抗体均能与PCSK9进行结合,而且DFSK9-2、DFSK9-4、DFSK9-5、DFSK9-6和DFSK9-8的亲和力明显高于其它克隆,选取上述5个单链抗体进行下一步试验。实施例4、对筛选出的抗PCSK9的单链抗体再次进行体外亲和力成熟4.1链置换法构建重链CDR123突变库用NcoI-HF和KpnI对实施例3.3中DFSK9-2、DFSK9-4、DFSK9-5、DFSK9-6和DFSK9-8等5种单链抗体的混合质粒进行双酶切,切胶回收大小5.5kb的条带;用NcoI-HF和KpnI对合成的重链突变库基因VHCDR123M进行双酶切,通用回收试剂盒回收酶切产物。突变库基因与载体按摩尔比3:1比例经T4DNA连接酶16℃连接4h。将连接产物电击法转化至XL1电转感受态中。37℃,150rpm培养1h复苏。取1%菌液,稀释后涂小平皿,计算库容量。其余菌液4000rpm,离心15min后,沉淀涂布于2YTATG大平皿上,37℃倒置培养过夜。构建成的抗体库库容大约为5*108,随机挑取20个克隆进行序列分析,正确率和多样性均大于90%。4.2噬菌体抗体库的生物淘选和阳性克隆的筛选将实施例4.1中的抗体库进行噬菌体展示和纯化回收。从该库中淘选抗PCSK9的单链抗体。噬菌体抗体库的生物淘选方法和阳性克隆的筛选同实施案例1和实施例2。测序后发现共筛选到10种不同的抗PCSK9抗体序列,分别命名为DFSK9-12、DFSK9-13、DFSK9-14、DFSK9-15、DFSK9-16、DFSK9-17、DFSK9-18、DFSK9-19、DFSK9-20、DFSK9-21。其中DFSK9-12的轻链可变区序列是DFSK9-L2,对应的氨基酸序列见SEQNO.12;DFSK9-13的轻链可变区序列是DFSK9-L8,对应的氨基酸序列见SEQNO.18;DFSK9-14、DFSK9-16和DFSK9-18的轻链可变区序列是DFSK9-L5,对应的氨基酸序列见SEQNO.15;DFSK9-15、DFSK9-17、DFSK9-20和DFSK9-21的轻链可变区序列是DFSK9-L6,对应的氨基酸序列见SEQNO.16;DFSK9-19的轻链可变区序列是DFSK9-L4,对应的氨基酸序列见SEQNO.14。DFSK9-12的重链可变区序列是DFSK9-H2,对应的氨基酸序列见SEQNO.2;DFSK9-13的重链可变区序列是DFSK9-H8,对应的氨基酸序列见SEQNO.8;DFSK9-14的重链可变区序列是DFSK9-H7,对应的氨基酸序列见SEQNO.7;DFSK9-15的重链可变区序列是DFSK9-H3,对应的氨基酸序列见SEQNO.3;DFSK9-16的重链可变区序列是DFSK9-H6,对应的氨基酸序列见SEQNO.6;DFSK9-17和DFSK9-18的重链可变区序列是DFSK9-H4,,对应的氨基酸序列见SEQNO.4;DFSK9-19的重链可变区是DFSK9-H9,对应的氨基酸序列见SEQNO.9;DFSK9-20的重链可变区是DFSK9-H5,对应的氨基酸序列见SEQNO.5;DFSK9-21的重链可变区序列是DFSK9-H10,对应的氨基酸序列见SEQNO.10。轻链可变区序列参照实施例3.2中氨基酸序列SEQNO.12、SEQNO.14、SEQNO.15、SEQNO.16和SEQNO.18,重链可变区氨基酸序列SEQNO.2-SEQNO.10如下:SEQNO.2(DFSK9-H2重链可变区序列):QVQLVQSGAEVKKPGASVKVSCKASGYTVTSYGISWVRQAPGQGLEWMGWLSFYNGNTNYAQKLQGRGTMTTDPSTSTAYMELRSLRSDDTAVYYCARGYSLDVWGQGTTVTVSSSEQNO.3(DFSK9-H3重链可变区序列):QVQLVQSGAEVKKPGASVKVSCKASGYTVTSYGISWVRQAPGQGLEWMGWVSFYNGQTNYAQKLQGRGTMTTDPSTSTAYMELRSLRSDDTAVYYCARGYSLDVWGQGTTVTVSSSEQNO.4(DFSK9-H4重链可变区序列):QVQLVQSGAEVKKPGASVKVSCKASGYTVTSYGISWVRQAPGQGLEWMGWVSFYNGNSNYAQKLQGRGTMTTDPSTSTAYMELRSLRSDDTAVYYCARGYSLDVWGQGTTVTVSSSEQNO.5(DFSK9-H5重链可变区序列):QVQLVQSGAEVKKPGASVKVSCKASGYSLTSYGISWVRQAPGQGLEWMGWVSFYNGNSNYAQKLQGRGTMTTDPSTSTAYMELRSLRSDDTAVYYCARGFGMDRWGQGTTVTVSSSEQNO.6(DFSK9-H6重链可变区序列):QVQLVQSGAEVKKPGASVKVSCKASGYTVTSYGISWVRQAPGQGLEWMGWVSFYQGNTNYAQKLQGRGTMTTDPSTSTAYMELRSLRSDDTAVYYCARGFGMDRWGQGTTVTVSSSEQNO.7(DFSK9-H7重链可变区序列):QVQLVQSGAEVKKPGASVKVSCKASGYSLTSYGISWVRQAPGQGLEWMGWVSFYNGQTNYAQKLQGRGTMTTDPSTSTAYMELRSLRSDDTAVYYCARGYGMSIWGQGTTVTVSSSEQNO.8(DFSK9-H8重链可变区序列):QVQLVQSGAEVKKPGASVKVSCKASGYSLTSYGISWVRQAPGQGLEWMGWVSFYQGNTNYAQKLQGRGTMTTDPSTSTAYMELRSLRSDDTAVYYCARGYGMTVWGQGTTVTVSSSEQNO.9(DFSK9-H9重链可变区序列):QVQLVQSGAEVKKPGASVKVSCKASGYSLTSYGISWVRQAPGQGLEWMGWVTFYNGNTNYAQKLQGRGTMTTDPSTSTAYMELRSLRSDDTAVYYCARGFGLSVWGQGTTVTVSSSEQNO.10(DFSK9-H10重链可变区序列):QVQLVQSGAEVKKPGASVKVSCKASGYSLTSYGISWVRQAPGQGLEWMGWVSFYNGQTNYAQKLQGRGTMTTDPSTSTAYMELRSLRSDDTAVYYCARGYGMDRWGQGTTVTVSS单克隆phageELISA鉴定phage-Abs的相对亲和力如图4所示。4.3.梯度稀释噬菌体ELISA鉴定抗PCSK9单链抗体的亲和力将本实施例4.2中获得的克隆进行单克隆噬菌体的展示和纯化,进行噬菌体梯度稀释ELISA实验鉴定单链抗体的亲和力,方法同实施例3中3.3。结果如图5所示:筛选出的10种不同的单链抗体均能与PCSK9进行很好的结合,且亲和力均高于最初的单链DFSK9-1。实施例5、抗PCSK9全抗体的亲和力鉴定5.1抗PCSK9全抗体的制备将实施例4中筛到抗体的重链VH克隆至含有重链恒定区基因(γ4)的载体pTSEG4(图6)上,轻链VK基因克隆到含有轻链恒定区基因(κ链)的载体pTSEK(图7)上,载体pTSEG4和pTSEK均以PTT载体为基础改造获得。PTT载体的制备过程在参考文献(Yves.Durocher,Sylvie.PerretandAmine.KamenNucleicAcidsResearch,2002Vol.30,No.2e9)中有详细描述。瞬时转染HEK293E细胞,进行全抗体表达。使用AKTA仪器proteinA亲和柱纯化获得全抗体蛋白。5.2全抗体与PCSK9的结合实验用pH7.2的0.01MPBS缓冲液包被PCSK9-His(300ng/孔/100μl),4℃包被过夜。用300μl/孔PBST(1‰Tween20)洗3次,再加入PBST-4%milk37℃封闭1h。加入不同稀释度的全抗体DFSK9-1,DFSK9-12、DFSK9-13、DFSK9-14、DFSK9-15、DFSK9-16、DFSK9-17、DFSK9-18、DFSK9-19、DFSK9-20和DFSK9-21。11种全抗体最高浓度是50ug/ml,5倍梯度稀释,每个全抗体做8个梯度,37℃孵育1h。用300μl/孔PBST洗5次,再加入用PBST-4%milk1:5000稀释的山羊抗人IgG-HRP二抗37℃孵育1h。用300μl/孔PBST洗5次,TMB显色试剂盒显色(100μl/孔),室温显色10min,然后用2MH2SO4(50μl/孔)终止显色。酶标仪波长450nm和630nm读数。使用软件GraphPadPrism5Demo分析数据作图,实验结果如图8和表2所示,所有抗体均能很好的与PCSK9分子结合,其中DFSK9-14、DFSK9-15、DFSK9-16、DFSK9-17、DFSK9-18、DFSK9-20和DFSK9-21具有相对较高的亲和力。表2、全抗体亲和力EC50值5.3全抗体竞争抑制LDLR与PCSK9结合实验用pH7.2的0.01MPBS包被LDLR-Fc(100ng/孔/100μl),4℃包被过夜。PBST洗涤3次,再加入PBST-4%milk37℃封闭1h。加入PBST-4%milk稀释的浓度为2μg/ml的PCSK9-His(100μl/孔),37℃孵育1h。加入PBST-4%milk稀释不同稀释度的全抗体DFSK9-1,DFSK9-12、DFSK9-13、DFSK9-14、DFSK9-15、DFSK9-16、DFSK9-17、DFSK9-18、DFSK9-19、DFSK9-20和DFSK9-21。11种全抗体最高浓度是100ug/ml,五倍梯度稀释,每个全抗体做8个梯度,37℃孵育2h。PBST洗5次,加入用PBST-4%milk稀释的小鼠抗HisIgG-HRP二抗,37℃孵育1h。TMB显色试剂盒显色(100μl/孔),室温显色10min,用2MH2SO4(50μl/孔)终止显色。酶标仪波长450nm和630nm读数。使用软件GraphPadPrism5Demo作图,实验结果如图9和表3所示,所有抗体均能有效的抑制PCSK9与LDLR的结合,其中DFSK9-14、DFSK9-15、DFSK9-16、DFSK9-17、DFSK9-18、DFSK9-20和DFSK9-21抑制能力稍强一些。表3、全抗体竞争实验IC50值5.4BIAcoreX100测定全抗体的亲和力采用捕获法测定全抗体的亲和力。将山羊抗人IgG偶联到CM5芯片表面,分别稀释DFSK9-1、DFSK9-12、DFSK9-13、DFSK9-14、DFSK9-15、DFSK9-16、DFSK9-17、DFSK9-18、DFSK9-19、DFSK9-20和DFSK9-21保证大约200RU左右的抗体被山羊抗人IgG捕获。将PCSK9设置一系列的浓度梯度(200nM、100nM、50nM、25nM、12.5nM、6.25nM、3.125nM、1.5625nM、0.78125nM)流经固定相表面,测定抗体的亲和力。结果发现筛出的抗体都具有较高的亲和力(见表4),选取亲和力最高的8种全抗体进行生物学活性实验。表4、抗PCSK9全抗体亲和力常数测定数值实例6、抗PCSK9全抗体生物学活性实验将HepG2细胞以2.5X105cells/ml接种到96孔中。次日,将10%FBS的EMEM生长培养基换成80μl含5%除脂蛋白FBS的分析培养基,37℃培养24h。次日,将分析培养基稀释的不同稀释度的全抗体(10μl/孔)加入到已接种HepG2细胞的培养板中。8种全抗体样品初始浓度为900nmol/L,3倍梯度稀释,每个全抗体做8个梯度。然后再加入30nmol/L的PCSK9溶液(10μl/孔),混匀后37℃,5%CO2条件下培养4h。每孔加入10ul0.1mg/mLBODIPY标记的LDL溶液,混匀后37℃,5%CO2条件下继续培养15-20h。洗涤每孔加入200μlPBS洗涤2次。每孔加入100μlPBS,酶标仪波长490nm和520nm读取相对荧光单位RFU数值。GraphPadPrism5Demo软件分析数据作图,结果如图10所示,以同型IgG为阴性对照,由图上可以看出8个抗体均能以剂量依赖性方式阻断PCSK9与低密度脂蛋白受体LDLR结合,增加低密度脂蛋白LDL在HepG2细胞内摄取率,各抗体之间的生物学活性相差不多。表5、生物学活性实验EC50值No.SampleEC50(nmol/L)No.SampleEC50(nmol/L)1DFSK9-1329.617DFSK9-1718.512DFSK9-1416.598DFSK9-1823.913DFSK9-1515.319DFSK9-2017.954DFSK9-1623.8010DFSK9-2120.33对于本领域的普通技术人员而言,具体实施例只是对本发明进行了示例性描述,显然本发明具体实现并不受上述方式的限制,只要采用了本发明的方法构思和技术方案进行的各种非实质性的改进,或未经改进将本发明的构思和技术方案直接应用于其它场合的,均在本发明的保护范围之内。<110>北京东方百泰生物科技有限公司.<120>一种全人源的抗PCSK9的单克隆抗体及其获得方法.<210>1:DFSK9-H1重链可变区氨基酸序列QVQLVQSGAEVKRPGASVKVSCKASGGTFTNNAISWVRQAPGQGLEWMGRIIPMFGMANYAQKLQGRGTMTTDPSTSTAYMELRSLRSDDTAVYYCAREGIPMIWGQGTTVTVSS2:DFSK9-H2重链可变区氨基酸序列QVQLVQSGAEVKKPGASVKVSCKASGYTVTSYGISWVRQAPGQGLEWMGWLSFYNGNTNYAQKLQGRGTMTTDPSTSTAYMELRSLRSDDTAVYYCARGYSLDVWGQGTTVTVSS3:DFSK9-H3重链可变区氨基酸序列QVQLVQSGAEVKKPGASVKVSCKASGYTVTSYGISWVRQAPGQGLEWMGWVSFYNGQTNYAQKLQGRGTMTTDPSTSTAYMELRSLRSDDTAVYYCARGYSLDVWGQGTTVTVSS4:DFSK9-H4重链可变区氨基酸序列:QVQLVQSGAEVKKPGASVKVSCKASGYTVTSYGISWVRQAPGQGLEWMGWVSFYNGNSNYAQKLQGRGTMTTDPSTSTAYMELRSLRSDDTAVYYCARGYSLDVWGQGTTVTVSS5:DFSK9-H5重链可变区氨基酸序列QVQLVQSGAEVKKPGASVKVSCKASGYSLTSYGISWVRQAPGQGLEWMGWVSFYNGNSNYAQKLQGRGTMTTDPSTSTAYMELRSLRSDDTAVYYCARGFGMDRWGQGTTVTVSS6:DFSK9-H6重链可变区氨基酸序列QVQLVQSGAEVKKPGASVKVSCKASGYTVTSYGISWVRQAPGQGLEWMGWVSFYQGNTNYAQKLQGRGTMTTDPSTSTAYMELRSLRSDDTAVYYCARGFGMDRWGQGTTVTVSS7:DFSK9-H7重链可变区氨基酸序列QVQLVQSGAEVKKPGASVKVSCKASGYSLTSYGISWVRQAPGQGLEWMGWVSFYNGQTNYAQKLQGRGTMTTDPSTSTAYMELRSLRSDDTAVYYCARGYGMSIWGQGTTVTVSS8:DFSK9-H8重链可变区氨基酸序列QVQLVQSGAEVKKPGASVKVSCKASGYSLTSYGISWVRQAPGQGLEWMGWVSFYQGNTNYAQKLQGRGTMTTDPSTSTAYMELRSLRSDDTAVYYCARGYGMTVWGQGTTVTVSS9:DFSK9-H9重链可变区氨基酸序列QVQLVQSGAEVKKPGASVKVSCKASGYSLTSYGISWVRQAPGQGLEWMGWVTFYNGNTNYAQKLQGRGTMTTDPSTSTAYMELRSLRSDDTAVYYCARGFGLSVWGQGTTVTVSS10:DFSK9-H10重链可变区氨基酸序列QVQLVQSGAEVKKPGASVKVSCKASGYSLTSYGISWVRQAPGQGLEWMGWVSFYNGQTNYAQKLQGRGTMTTDPSTSTAYMELRSLRSDDTAVYYCARGYGMDRWGQGTTVTVSS11:DFSK9-L1轻链可变区氨基酸序列DIQMTQSPSSLSASVGDRVTITCRASQSIDNRLTWYQQKPGKAPKLLIYDASSRQSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQPENDPTTFGQGTKVEIK12:DFSK9-L2轻链可变区氨基酸序列DIQMTQSPSSLSASVGDRVTITCRASQSVRNWLDWYQQKPGKAPKLLIYGASTLESGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQDNDIPLTFGQGTKVEIK13:DFSK9-L3轻链可变区氨基酸序列DIQMTQSPSSLSASVGDRVTITCRASQGINSWLNWYQQKPGKAPKLLIYAASTRETGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQWNNTPNTFGQGTKVEIK14:DFSK9-L4轻链可变区氨基酸序列DIQMTQSPSSLSASVGDRVTITCRASQNVNNWLNWYQQKPGKAPKLLIYAASTRETGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQDNDMPLTFGQGTKVEIK15:DFSK9-L5轻链可变区氨基酸序列DIQMTQSPSSLSASVGDRVTITCRASQNINSWLNWYQQKPGKAPKLLIYGASSRQSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQWFDVPTTFGQGTKVEIK16:DFSK9-L6轻链可变区氨基酸序列DIQMTQSPSSLSASVGDRVTITCRASQNINNWLNWYQQKPGKAPKLLIYGASTRPTGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQWDDTPNTFGQGTKVEIK17:DFSK9-L7轻链可变区氨基酸序列DIQMTQSPSSLSASVGDRVTITCRASQGIHNWLNWYQQKPGKAPKLLIYDASNRQSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQNSNIPLTFGQGTKVEIK18:DFSK9-L8轻链可变区氨基酸序列DIQMTQSPSSLSASVGDRVTITCRASQDVDSWLTWYQQKPGKAPKLLIYGASNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQDSKIPLTFGQGTKVEIK19:DFSK9-L9轻链可变区氨基酸序列DIQMTQSPSSLSASVGDRVTITCRASQSVRNWLNWYQQKPGKAPKLLIYDASNLQSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQWTDTPLTFGQGTKVEIK20:DFSK9-L10轻链可变区氨基酸序列DIQMTQSPSSLSASVGDRVTITCRASQDVRNWLTWYQQKPGKAPKLLIYGASNLASGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQDDSTPPTFGQGTKVEIK21:DFSK9-L11轻链可变区氨基酸序列DIQMTQSPSSLSASVGDRVTITCRASQSIRSYLNWYQQKPGKAPKLLIYDASSRPTGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQGDSMPMTFGQGTKVEIK22:DFSK9-L1轻链CDR1区氨基酸序列RASQSIDNRLT23:DFSK9-L2轻链CDR1区氨基酸序列RASQSVRNWLD24:DFSK9-L3轻链CDR1区氨基酸序列RASQGINSWLN25:DFSK9-L4轻链CDR1区氨基酸序列RASQNVNNWLN26:DFSK9-L5轻链CDR1区氨基酸序列RASQNINSWLN27:DFSK9-L6轻链CDR1区氨基酸序列RASQNINNWLN28:DFSK9-L7轻链CDR1区氨基酸序列RASQGIHNWLN29:DFSK9-L8轻链CDR1区氨基酸序列RASQDVDSWLT30:DFSK9-L9轻链CDR1区氨基酸序列RASQSVRNWLN31:DFSK9-L10轻链CDR1区氨基酸序列RASQDVRNWLT32:DFSK9-L11轻链CDR1区氨基酸序列RASQSIRSYLN33:DFSK9-L1轻链CDR2区氨基酸序列DASSRQS34:DFSK9-L2轻链CDR2区氨基酸序列GASTLES35:DFSK9-L3和DFSK9-L4轻链CDR2区氨基酸序列AASTRET36:DFSK9-L5轻链CDR2区氨基酸序列GASSRQS37:DFSK9-L6轻链CDR2区氨基酸序列GASTRPT38:DFSK9-L7轻链CDR2区氨基酸序列DASNRQS39:DFSK9-L8和DFSK9-L10轻链CDR2区氨基酸序列GASNLAS40:DFSK9-L9轻链CDR2区氨基酸序列DASNLQS41:DFSK9-L11轻链CDR2区氨基酸序列DASSRPT42:DFSK9-L1轻链CDR3区氨基酸序列QQPENDPTT43:DFSK9-L2轻链CDR3区氨基酸序列QQDNDIPLT44:DFSK9-L3轻链CDR3区氨基酸序列QQWNNTPNT45:DFSK9-L4轻链CDR3区氨基酸序列QQDNDMPLT46:DFSK9-L5轻链CDR3区氨基酸序列QQWFDVPTT47:DFSK9-L6轻链CDR3区氨基酸序列QQWDDTPNT48:DFSK9-L7轻链CDR3区氨基酸序列QQNSNIPLT49:DFSK9-L8轻链CDR3区氨基酸序列QQDSKIPLT50:DFSK9-L9轻链CDR3区氨基酸序列QQWTDTPLT51:DFSK9-L10轻链CDR3区氨基酸序列QQDDSTPPT52:DFSK9-L11轻链CDR3区氨基酸序列QQGDSMPMT53:DFSK9-H1重链CDR1区氨基酸序列GGTFTNNA54:DFSK9-H2、DFSK9-H3、DFSK9-H4和DFSK9-H6重链CDR1区氨基酸序列GYTVTSYG55:DFSK9-H5、DFSK9-H7、DFSK9-H8、DFSK9-H9和DFSK9-H10重链CDR1区氨基酸序列GYSLTSYG56:DFSK9-H1重链CDR2区氨基酸序列RIIPMFGMA57:DFSK9-H2重链CDR2区氨基酸序列WLSFYNGNT58:DFSK9-H9重链CDR2区氨基酸序列WVTFYNGNT59:DFSK9-H6和DFSK9-H8重链CDR2区氨基酸序列WVSFYQGNT60:DFSK9-H3、DFSK9-H7和DFSK9-H10重链CDR2区氨基酸序列WVSFYNGQT61:DFSK9-H4和DFSK9-H5重链CDR2区氨基酸序列WVSFYNGNS62:DFSK9-H1重链CDR3区氨基酸序列AREGIPMI63:DFSK9-H2、DFSK9-H3和DFSK9-H4重链CDR3区氨基酸序列ARGYSLDV64:DFSK9-H7重链CDR3区氨基酸序列ARGYGMSI65:DFSK9-H5、DFSK9-H6和DFSK9-H10重链CDR3区氨基酸序列ARGFGMDR66:DFSK9-H8重链CDR3区氨基酸序列ARGYGMTV67:DFSK9-H9重链CDR3区氨基酸序列ARGFGLSV当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1