PPAP亚胺类化合物及其制备方法、药物组合物和用途与流程
本发明涉及一种ppap亚胺类化合物及其制备方法、药物组合物和用途,属于医药领域。
背景技术:
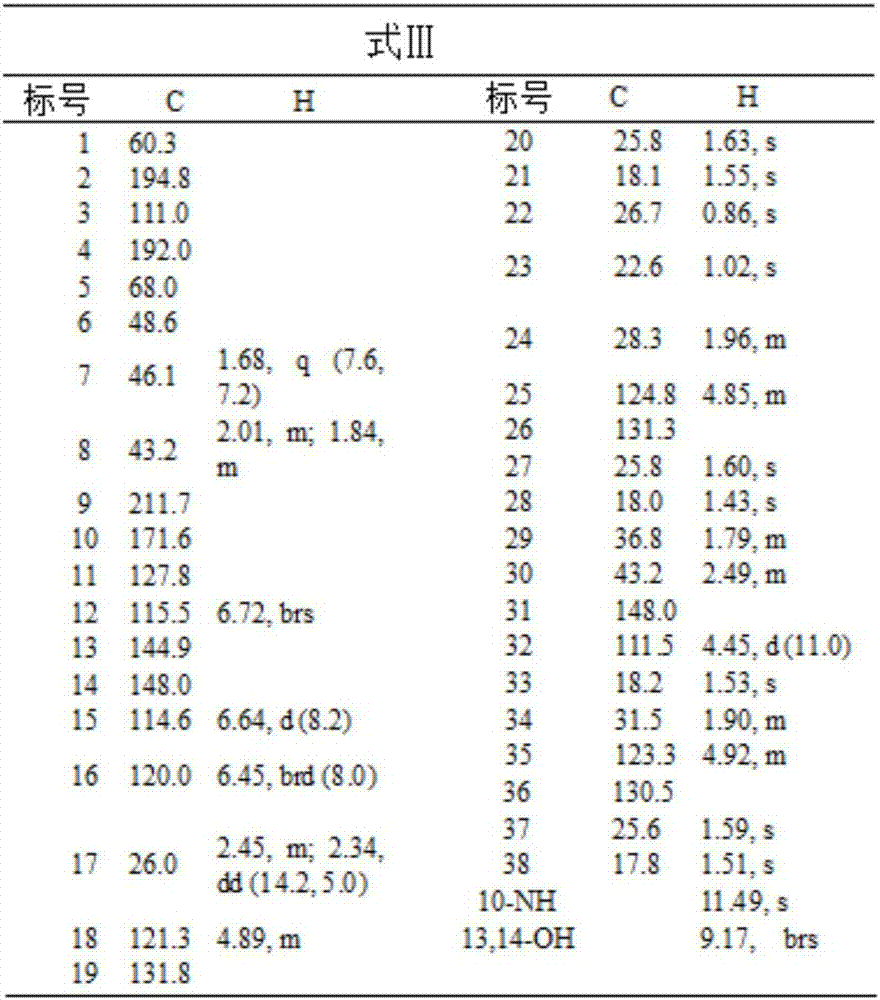
:恶性肿瘤是世界上主要的致死性疾病之一,严重威胁着人类健康和生命。中国医学科学院肿瘤医院、国家癌症中心赫捷院士,全国肿瘤登记中心主任陈万青教授等在ca:acancerjournalforclinicians杂志上发表的2015年中国癌症统计数据表明,2015年中国约有429.2万例新肿瘤病例和281.4万例死亡病例。随着人口的老龄化问题的加剧,我国癌症的发病率呈上升趋势,对我国卫生资源及国民经济造成巨大负担,癌症控制已成为现今我国卫生战略的重点。国家科技重大专项“重大新药创制”项目将其列为临床亟需药物研发的10类(种)重大疾病之一。藤黄科(guttiferae)藤黄属(garcinialinn)植物云南藤黄(garciniayunnanensishu)是我国的特有种,分布于云南省西南部,果实酸甜可食,木材可制作家具,其富含多环多异戊烯基间苯三酚类(polycyclicpolyprenylatedacylphloroglucinols,简称ppaps)和口山酮类(xanthones)化合物,这两类化合物具有新颖多变的结构和广泛的生物活性,研究表明ppaps和xanthones都具有抗肿瘤的作用,例如中国专利cn201210507960.8、cn201410366679.6、cn201510056911.0、cn201610914347.6等报道了ppaps类化合物在抗肿瘤方面的作用,中国专利cn201410280756.6、cn201510907922.5等报道了xanthones类化合物在抗肿瘤方面的作用。虽然ppaps已经成为天然化合物的研究热点,目前相关报道也较多,但是目前还没有关于ppap亚胺类化合物的相关报道,更没有ppap亚胺类化合物在抗肿瘤方面的相关报道。技术实现要素:针对现有技术存在的上述问题,本发明的目的是提供一种ppap亚胺类化合物及其制备方法、药物组合物和用途,以促进该类化合物在医药领域的广泛应用。本发明所述的ppap亚胺类化合物是具有式ⅰ结构的化合物或所述化合物的药学上可接受的盐、互变异构体、立体异构体、前体化合物或水合物:其中:r1、r2、r3、r4、r5各自独立地选自氢、ora、取代或未取代的c1~c12烷基、取代或未取代的c2~c12烯基、取代或未取代的c2~c12炔基、取代或未取代的c6~c30芳基、取代或未取代的c1~c30杂芳基中的任意一种,ra为选自氢、取代或未取代的c1~c12烷基、取代或未取代的c2~c12烯基、取代或未取代的c2~c12炔基、取代或未取代的c6~c30芳基、取代或未取代的c1~c30杂芳基中的任一种。作为优选方案,r1、r2、r3、r4各自独立地选自h、ch3、och3、oh、x中的任意一种,r5选自h、ch3、och3、oh、x、y中的任意一种;x具有式x-1、x-2、x-3、x-4、x-5、x-6或x-7所示结构:其中:rx1、rx2、rx3、rx4、rx5、rx6、rx7、rx8、rx9、rx10、rx12、rx13各自独立地选自氢、甲基、甲氧基、羟基、异戊烯基中的任意一种,rx11为异戊烯基,rx14选自氢、甲基、甲氧基、异戊烯基中的任意一种,rx15、rx16各自独立地选自氢、甲基、甲氧基、羟基、异戊烯基中的任意一种,且当rx15、rx16中任意一个为羟基时,剩余一个不能为氢、甲氧基或羟基;y具有式y-1或y-2所示结构:其中:ry1、ry2、ry3、ry4、ry5和ry6各自独立地选自氢、甲基、甲氧基、羟基或异戊烯基。作为进一步优选方案,所述ppap亚胺类化合物选自如下化合物或所述化合物的药学上可接受的盐、互变异构体、立体异构体、前体化合物或水合物:我们将其命名为garciyunnaniminea;我们将其命名为garciyunnanimineb;我们将其命名为garciyunnaniminec;我们将其命名为garciyunnanimined;我们将其命名为garciyunnaniminee。本领域人员应理解,在得知了本发明ppap亚胺类化合物的结构以后,可通过多种本领域熟知的方法、利用公知的原料,来获得本发明的ppap亚胺类化合物,比如从植物(例如云南藤黄)中提取或化学合成(例如ppaps亚胺化反应)等。本发明所述的ppap亚胺类化合物中式ⅱ、式ⅲ、式ⅳ化合物的分离纯化方法,包括如下步骤:a)将云南藤黄粉碎后用95wt%乙醇热回流提取3~5次,减压蒸发提取液,得提取物;b)将步骤a)所得的提取物混悬在水中,依次用石油醚、乙酸乙酯萃取,分别得到云南藤黄提取物的石油醚萃取部位、乙酸乙酯萃取部位;c)将步骤b)所得云南藤黄提取物的石油醚萃取部位通过硅胶柱分离,用石油醚和丙酮按照100:0~50:50的体积比形成的混合溶液依次梯度洗脱,每份洗脱液减压蒸发后经tlc薄层分析,将tlc薄层板上显示的主要的点相同的洗脱物合并,按洗脱顺序得到十六个组分;d)将步骤c)中得到的第五个组分用ods柱分离,用甲醇和水依照30:70~100:0的体积比形成的混合溶液依次梯度洗脱,每份洗脱液减压蒸发后经tlc薄层分析,将tlc薄层板上显示的主要的点相同的洗脱物合并,按洗脱顺序得到二十六个组分;e)将步骤d)中的第十七个组分用sphadexlh20凝胶柱分离,用甲醇洗脱,得到十个组分,其中第三个组分用制备液相色谱纯化,得到式ⅲ化合物(garciyunnanimineb);f)将步骤d)中的第十八个组分用制备液相色谱纯化,得到式ⅱ化合物(garciyunnaniminea);g)将步骤d)中的第二十三个组分用制备液相色谱纯化,得到式ⅳ化合物(garciyunnaniminec)。本发明所述的ppap亚胺类化合物的制备方法,是使式ⅶ化合物在有机溶剂存在下与氨气反应获得式ⅰ化合物,或者在乙酸催化剂和有机溶剂存在下与氨气反应获得式ⅰ化合物,具体反应式如下所示:其中r1、r2、r3、r4、r5如式ⅰ中的定义。作为优选方案,所述有机溶剂为非醇溶剂,例如:二氧六环;反应温度为70~90℃。一种防治肿瘤的药物组合物,所述组合物包含治疗有效量的具有式ⅰ结构的化合物或其药学上可接受的盐、互变异构体、立体异构体、前体化合物、水合物中的至少一种。作为优选方案,所述肿瘤选自肝癌、肺癌、血癌中的至少一种。本发明所述的ppap亚胺类化合物可作为活性成分用于制备预防和/或治疗肿瘤的药物或保健品。作为优选方案,所述肿瘤选自肝癌、肺癌、血癌中的至少一种。本发明所述组合物、抗肿瘤药物的剂型可以是多种多样的,只要是能够使活性成分有效地到达体内的剂型都是可以的。比如可选自:片剂、胶囊剂、粉末、颗粒剂、糖浆、溶液、悬浮液、注射剂、酊剂、口服液、气雾剂、口含剂、冲剂、丸剂、散剂等常见剂型或纳米制剂等缓释剂型。本发明所述活性成分的有效施用剂量可随所用的组合物、给药的模式和待治疗的疾病的严重程度而变化。本发明中所述术语的定义如下:术语“c1-c12烷基”是指具有1-12个碳原子的直链或支链烷基或环烷基,例如:甲基、亚甲基、乙基、丙基、异丙基、丁基、异丁基、仲丁基、叔丁基、环丙基、环丁基、环戊基、环己基、环庚基,或类似基团。术语“c2-c12烯基”是指具有2-6个碳原子的、具有一个或多个双键的直链或支链的烯基或环烯基,例如:乙烯基、烯丙基、1-丙烯基、异丙烯基、1-丁烯基、2-丁烯基、异戊烯基、环己烯基、环庚烯基、1,3-环己二烯基、1,4-环己二烯基、或类似基团。术语“c2-c12炔基”是指具有2-12个碳原子的、具有一个或多个三键的直链或支链的炔基,例如:乙炔基、丙炔基、或类似基团。术语“c6~c30芳基”是指具有6~30个碳原子的芳基,包括单环或二环芳基,例如:苯基、萘基、或类似基团。术语“c1~c30杂芳基”是指具有1~30个碳原子的杂芳基,例如:吡咯基、吡啶基、呋喃基、或类似基团。术语“取代”是指基团上的一个或多个氢原子被选自下组的取代基取代:c1~c10烷基、c3~c10环烷基、c1~c10烷氧基、卤素、羟基、氨基、苯基、异戊烯基;所述的苯基包括未取代的苯基或具有1-3个取代基的取代苯基,所述的取代基选自卤素、c1-c10烷基、氰基、羟基、硝基、c3~c10环烷基、c1~c10烷氧基、氨基或异戊烯基。术语“药学上可接受的盐”是指所述化合物与药学上可接受的无机酸或有机酸所形成的盐,所述的无机酸包括:盐酸、氢溴酸、磷酸、硝酸、硫酸;所述的有机酸包括:甲酸、乙酸、丙酸、丁二酸、萘二磺酸(1,5)、亚细亚酸、草酸、酒石酸、乳酸、水杨酸、苯甲酸、戊酸、二乙基乙酸、丙二酸、琥珀酸、富马酸、庚二酸、己二酸、马来酸、苹果酸、氨基磺酸、苯丙酸、葡糖酸、抗坏血酸、烟酸、异烟酸、甲磺酸、对甲苯磺酸、柠檬酸,以及氨基酸。术语“互变异构体”是指因分子中某一原子在两个位置迅速移动而产生的官能团异构体,例如:烯醇与相应的酮。术语“立体异构体”是指由分子中原子在空间上排列方式不同所产生的异构体,例如:顺反异构体、对映异构体、构象异构体、非对映异构体等。术语“前体化合物”是指在体外无活性,但能够在生物体内进行代谢或化学反应转化为本发明的活性成分,从而发挥其药理作用的化合物。术语“组合物”是指在组合物中,除了含有主要活性成分之外,还可含有少量的且不影响有效成分的次要成分和/或药学上可接受的载体。例如,可以含有甜味剂以改善口味、抗氧化剂以防止氧化,以及各种制剂所必要的辅料。术语“药学上可接受的”是指适用于人而无过度不良副反应(如毒性、刺激和变态反应),即有合理的效益/风险比的物质。与现有技术相比,本发明具有如下显著性有益效果:本发明的研究结果显示:本发明所述的具有通式ⅰ结构的ppap亚胺类化合物能明显抑制人肝癌细胞hepg2、人非小细胞肺癌细胞a549和人多发性骨髓瘤细胞株rpmi-822672增殖的活性,这说明本发明所述的具有通式ⅰ结构的ppap亚胺类化合物具有抑制肿瘤细胞增殖的作用,可以用于制备预防和/或治疗肿瘤的药物或保健品,具有广泛应用前景。附图说明图1是式ⅱ化合物的1hnmr和13cnmr的数据;图2是式ⅲ化合物的1hnmr和13cnmr的数据;图3是式ⅳ化合物的1hnmr和13cnmr的数据;图4是式ⅴ化合物的1hnmr和13cnmr的数据;图5是式ⅵ化合物的1hnmr和13cnmr的数据。具体实施方式下面结合具体实施例,进一步阐述本发明。应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。下列实施例中未注明具体条件的实验方法,通常按照常规条件或按照制造厂商所建议的条件。除非另外说明,否则百分比和份数按重量计算。下列实施中,云南藤黄选用云南省德宏傣族景颇族自治州云南藤黄的果、枝和叶;mci柱选用chp20pmcigel(75-150μm,mitsubishichemical;coparation,japan);硅胶柱层析选用青岛海洋化工有限公司柱层析硅胶(200-300目);tlc薄层分析选用烟台江友硅胶开发有限公司hsgf254薄层层析硅胶板;ods中压制备色谱柱选用reversed-phasec18silicagel(50μm,ymc,kyoto,japan);凝胶柱选用sephadexlh-20(gehealthcarebio-sciencesab,sweden)为填料;质谱为watersacquityuplc/synaptg2-sims超高效液相色谱/电喷雾四级杆-飞行时间质谱联用,所用色谱柱为watersacquitybehc18(2.1mm*100mm,1.7μm);制备hplc为waters2535,制备色谱柱为xbridgeprepc18obdcolumn(19×250mm,5μm),分析用hplc色谱柱为xbridgec18column(4.6×250mm,5μm);旋光测试仪器为autopolvipolarimeter;紫外分光光度计为uv-2401pcspectrophotometer;红外光谱使用perkin-elmer577spectrometer测试;核磁使用brukerav-400spectrometer测试;液相用乙腈为色谱级,水为蒸馏水,甲酸为分析级;质谱用乙腈为质谱级,水为经mill-q处理的蒸馏水,甲酸为质谱级;ods中压和凝胶用甲醇为分析级,水为蒸馏水;其他试剂均为合成级。实施例1从云南藤黄中分离纯化式ⅱ(garciyunnaniminea)、式ⅲ(garciyunnanimineb)、式ⅳ(garciyunnaniminec)化合物:a)52kg干燥的云南藤黄(包括果实12kg,枝34kg和叶6kg)粉碎后经过提取罐提取,每次用10倍量的95wt%乙醇(520l)热回流提取1小时,重复提取3次,减压蒸发提取液,得提取物;b)将步骤a)所得的提取物混悬在水中,依次用石油醚、乙酸乙酯萃取,分别得到云南藤黄提取物的石油醚萃取部位(2.5kg)、乙酸乙酯萃取部位(3.3kg);c)将步骤b)所得云南藤黄提取物的石油醚萃取部位通过硅胶柱分离(300-400目硅胶用作分离,6kg;100-200目硅胶拌样,1.8kg),用石油醚和丙酮按照100:0~50:50的体积比形成的混合溶液依次梯度洗脱,每份洗脱液减压蒸发后经tlc薄层分析,将tlc薄层板上显示的主要的点相同的洗脱物合并,按洗脱顺序得到十六个组分;d)将步骤c)中得到的第五个组分用ods柱分离,用甲醇和水依照30:70~100:0的体积比形成的混合溶液依次梯度洗脱,洗脱液每次收集2000ml,每份洗脱液减压蒸发后经tlc薄层分析,将tlc薄层板上显示的主要的点相同的洗脱物合并,按洗脱顺序得到二十六个组分;e)将步骤d)中的第十七个组分用sphadexlh20凝胶柱分离,用甲醇洗脱,得到十个组分,其中第三个组分用制备hplc纯化(乙腈:0.1%甲酸水=65:35,v/v),得到式ⅲ化合物garciyunnanimineb(浅黄色胶状固体,6mg);f)将步骤d)中的第十八个组分用制备hplc纯化(乙腈:0.1%甲酸水=72:28,v/v),得到式ⅱ化合物garciyunnaniminea(浅黄色胶状固体,10mg);g)将步骤d)中的第二十三个组分用制备hplc纯化(乙腈:0.1%甲酸水=77:23,v/v),得到式ⅳ化合物garciyunnaniminec(浅黄色胶状固体,9mg)。式ⅱ化合物garciyunnaniminea的结构鉴定数据:[α]20d11.7(c0.03,meoh);uv(meoh)λmax(logε)255(4.03),317(3.85),350(3.78)nm;ecd(c4.99×10-4m,meoh)λmaxnm(δε)208(+13.22),257(–3.39),282(2.70),305(–3.36);ir(kbr)νmax3258,2969,2922,2857,1715,1639,1577,1442,1376,1281,1202,1115,1048,1024,1003,822,762,735,688cm-1;hresimsm/z602.3850[m+h]+(calcdforc38h52no5,602.3845);1hnmr(dmso-d6,400mhz)和13cnmr(dmso-d6,100mhz)的数据见图1所示。式ⅲ化合物garciyunnanimineb的结构鉴定数据:[α]20d–69.0(c0.035,meoh);uv(meoh)λmax(logε)257(4.45),322(3.94),352(3.90)nm;ecd(c3.99×10-4m,meoh)λmaxnm(δε)230(+5.17),265(–0.94),287(+16.73),320(–5.90);ir(kbr)νmax3237,3068,2968,2919,1715,1637,1577,1524,1442,1391,1373,1282,1114,1048,1024,1003,887,862,762cm-1;hresimsm/z602.3845[m+h]+(calcdforc38h52no5,602.3845);1hnmr(dmso-d6,400mhz)和13cnmr(dmso-d6,100mhz)的数据见图2所示。式ⅳ化合物garciyunnaniminec的结构鉴定数据:[α]20d11.4(c0.041,meoh);uv(meoh)λmax(logε)255(4.16),317(3.97),352(3.92)nm;ecd(c4.37×10-4m,meoh)λmaxnm(δε)206(+10.48),259(–1.97),282(+1.83),302(–2.73);ir(kbr)νmax3214,2967,2915,2857,1716,1639,1577,1441,1376,1280,1114,1048,1024,1003,823,763cm-1;hresimsm/z670.4471[m+h]+(calcdforc43h60no5,670.4471);1hnmr(dmso-d6,400mhz)和13cnmr(dmso-d6,100mhz)的数据见图3所示。实施例2化学合成法制备式ⅱ化合物garciyunnaniminea:向反应器中加入guttiferonek(20mg,0.033mmol),0.5m氨气的二氧六环溶液(13.3ml,6.6mmol,200equiv.),乙酸(1.89ml,0.033mmol,1equiv.),于80℃保温反应四小时,结束反应,反应液冷却至室温后将其减压浓缩除去反应溶剂,浓缩物用甲醇溶解后,采用制备hplc液相,使用流速为20ml/min的乙腈-0.1%甲酸水(80:20,v/v)洗脱,得到式ⅱ化合物(浅黄色胶状固体,13.2mg),产率66%。所得式ⅱ化合物的结构鉴定数据与实施例1中的对应数据相一致。实施例3化学合成法制备式ⅲ化合物garciyunnanimineb:向反应器中依次加入garcinol(20mg,0.033mmol),0.5m氨气的二氧六环溶液(13.3ml,6.6mmol,200equiv.),乙酸(1.89ml,0.033mmol,1equiv.),在80℃下搅拌反应四小时,反应液冷却至室温后将其减压浓缩除去反应溶剂,浓缩物用甲醇溶解后,采用制备hplc液相,使用流速为20ml/min的乙腈-0.1%甲酸水(80:20,v/v)洗脱,得到式ⅲ化合物(浅黄色胶状固体,13.8mg),产率69%。所得式ⅲ化合物的结构鉴定数据与实施例1中的对应数据相一致。实施例4化学合成法制备式ⅳ化合物garciyunnaniminec:向反应器中依次加入oblongifolinc(20mg,0.030mmol),0.5m氨气的二氧六环溶液(14.8ml,7.3mmol,200equiv.),乙酸(2.10ml,0.030mmol,1equiv.),在80℃下搅拌反应四小时,反应液冷却至室温后将其减压浓缩除去反应溶剂,浓缩物用甲醇溶解后,采用制备hplc液相,使用流速为20ml/min的乙腈-0.1%甲酸水(80:20,v/v)洗脱,得到式ⅳ化合物(浅黄色胶状固体,14.2mg),产率71%。所得式ⅳ化合物的结构鉴定数据与实施例1中的对应数据相一致。实施例5化学合成法制备式ⅴ化合物garciyunnanimined:向反应器中依次加入oblongifolina(20mg,0.033mmol),0.5m氨气的二氧六环溶液(13.3ml,6.6mmol,200equiv.),乙酸(1.89ml,0.033mmol,1equiv.),于80℃下搅拌反应四小时,反应液冷却至室温后将其减压浓缩除去反应溶剂,浓缩物用甲醇溶解后,采用制备hplc液相,使用流速为20ml/min的乙腈-0.1%甲酸水(68:32,v/v)洗脱,得到式ⅴ化合物(浅黄色胶状固体,12.4mg),产率62%。式ⅴ化合物garciyunnanimined的结构鉴定数据:[α]20d25.4(c0.04,meoh);uv(meoh)λmax(logε)255(4.48),317(3.94),352(3.90)nm;ecd(c6.66×10-4m,meoh)λmaxnm(δε)202(+14.90),251(–3.13),282(+3.10),314(–2.71);ir(kbr)νmax3207,2970,2913,1718,1640,1577,1525,1441,1375,1283,1114,1048,1025,1004,877,823,762,682cm-1;hresimsm/z602.3844[m+h]+(calcdforc38h52no5,602.3845);1hnmr(dmso-d6,400mhz)和13cnmr(dmso-d6,100mhz)的数据见图4所示。实施例6化学合成法制备式ⅵ化合物garciyunnaniminee:向反应器中依次加入oblongifolinb(20mg,0.033mmol),0.5m氨气的二氧六环溶液(13.3ml,6.6mmol,200equiv.),乙酸(1.89ml,0.033mmol,1equiv.),在80℃下搅拌反应四小时,反应液冷却至室温后将其减压浓缩除去反应溶剂,浓缩物用甲醇溶解后,采用制备hplc液相,使用流速为20ml/min的乙腈-0.1%甲酸水(80:20,v/v)洗脱,得到式ⅵ化合物(浅黄色胶状固体,11.8mg),产率59%。式ⅵ化合物garciyunnaniminee的结构鉴定数据:[α]20d15.6(c0.047,meoh);uv(meoh)λmax(logε)255(4.11),317(3.92),352(3.85)nm;ecd(c7.82×10-4m,meoh)λmaxnm(δε)207(+5.83),263(+3.11),307(–92);ir(kbr)νmax3255,2970,2916,2856,1716,1639,1578,1525,1441,1393,1282,1115,1024,1003,822,762cm-1;hresimsm/z602.3852[m+h]+(calcdforc38h52no5,602.3845).;1hnmr(dmso-d6,400mhz)和13cnmr(dmso-d6,100mhz)的数据见图5所示。实施例7式ⅱ、式ⅲ、式ⅳ、式ⅴ、式ⅵ化合物抑制人肿瘤细胞增殖试验:7.1实验材料a549(人肺腺癌细胞),rpmi-8226(多发性骨髓瘤细胞)购于atcc和中国科学院上海生物化学与细胞生物学研究所细胞库;细胞置放于37℃、5%co2培养箱中进行培养,当细胞传至8到15代时用于体外活性测试;cck-8试剂盒购自日本同仁化学研究所(dojindo)。7.2细胞增殖实验将细胞悬液以每孔180μl加入96孔板中,37℃、5%co2培养过夜,使细胞贴壁;次日将已配制好的粗提物或者化合物溶液加入相应孔中;培养72h后,吸弃培养基,加入含10%cck-8的培养基,置于培养箱中培养2h;于酶联免疫检测仪(mds,sunnyvale,ca450nm)波长下测定每孔光吸收值。细胞抑制率计算公式如下:抑制率(%)=(oddmso-od试验组)/oddmso×100%;实验数据均用平均值±标准误差表示。7.3实验结果garciyunnaniminea(式ⅱ化合物)、garciyunnanimineb(式ⅲ化合物)、garciyunnaniminec(式ⅳ化合物)、garciyunnanimined(式ⅴ化合物)、garciyunnaniminee(式ⅵ化合物)作用于多种人肿瘤72h的ic50如表1所示。表1化合物的ic50值(μm)化合物a549hepg2rpmi-8226garciyunnaniminea3.9±0.54.7±1.03.5±0.4garciyunnanimineb4.4±0.210.1±2.31.7±0.1garciyunnaniminec7.7±0.823.7±3.43.5±1.9garciyunnanimined6.8±1.815.0±3.51.9±0.3garciyunnaniminee8.2±1.512.8±2.75.8±0.9etoposide9.2±1.411.7±1.5<0.25由表1可见,新化合物garciyunnaniminea(式ⅱ化合物)、garciyunnanimineb(式ⅲ化合物)、garciyunnaniminec(式ⅳ化合物)、garciyunnanimined(式ⅴ化合物)、garciyunnaniminee(式ⅵ化合物)对于人肝癌细胞hepg2、人非小细胞肺癌细胞a549和人多发性骨髓瘤细胞株rpmi-8226均具有显著的抑制肿瘤细胞增殖的作用,强于阳性对照药etoposide(依托泊甙),具有潜在的抗肿瘤作用,可以作为预防和/或治疗肿瘤的药物或保健品。最后需要在此指出的是:以上仅是本发明的部分优选实施例,不能理解为对本发明保护范围的限制,本领域的技术人员根据本发明的上述内容做出的一些非本质的改进和调整均属于本发明的保护范围。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1