瓜蒌皮注射液中离子含量的测定方法与流程
本发明涉及瓜蒌皮注射液中离子含量的测定方法。
背景技术:
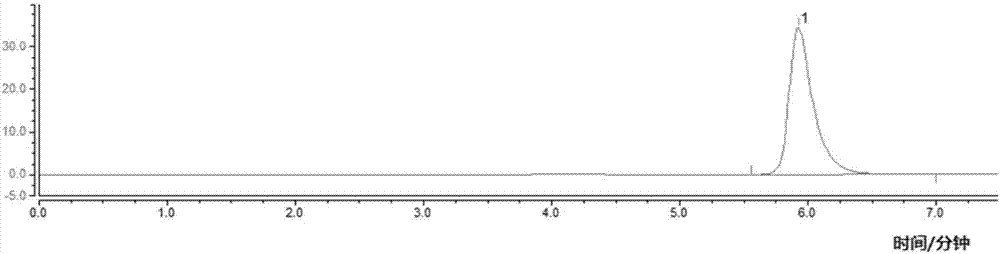
:瓜蒌皮(trichosanthispericarpium)为葫芦科植物栝楼(trichosantheskirilowiimaxim.)或双边栝楼trichosanthesrosthoriniiharms)的干燥成熟果皮。瓜蒌皮注射液是瓜蒌皮经提取纯化制成的中药注射剂,临床上主要用于冠心病稳定型心绞痛的治疗,具有活血化瘀、抗血小板聚集、稳定血管内皮和抗自由基等作用。瓜蒌皮注射液临床应用广泛,但物质基础研究较少,其中阴阳离子的测定也未见报道。传统无机阴离子的测定多采用氧化还原法、电位滴定法等,但此类方法操作繁琐,灵敏度低,一次只能测定一种离子;注射液中阳离子则多采用原子吸收分光光度法,但该方法需要对应的元素灯、每次同样只能测定一种离子;而离子色谱法具有专属、灵敏、准确、环保无污染、自动化程度高等特点,适用于分析阴阳离子、有机酸、胺、醇类和氨基酸等离子型物质。目前,对于瓜蒌皮注射液中的离子含量尚未有报道,但因阴阳离子含量在一定程度反映制剂辅料、工艺的稳定性,其可作为企业控制瓜蒌皮注射液工艺质量的一个重要参数。因此,建立一种可测定瓜蒌皮注射液的物质基础组成的方法,对瓜蒌皮注射液的安全性、有效性和质量可控性有很大的指导意义。技术实现要素:本发明所要解决的技术问题是为了克服现有技术中对瓜蒌皮注射液物质基础组成研究较少的现状,尤其是为了填补瓜蒌皮注射液中氯离子、钠离子及铵离子含量研究的空白,从而提供了一种瓜蒌皮注射液中离子含量的测定方法。该方法通过离子色谱法对瓜蒌皮注射液中的氯离子、钠离子和铵离子进行了含量测定。该方法可在同台离子色谱仪上将氯离子、钠离子和铵离子实现基线分离;操作简便快捷,结果准确可靠,有助于进一步阐明瓜蒌皮注射液的物质基础组成,更能够为其安全性、有效性和质量可控性研究提供一定的参考。本发明是通过以下技术方案解决上述技术问题的。本发明提供了一种瓜蒌皮注射液中离子含量的测定方法,其包含以下步骤:采用离子色谱法对瓜蒌皮注射液待测品中的离子进行含量测定;所述瓜蒌皮注射液待测品中包含钠离子、铵离子和氯离子中的一种或多种离子;所述离子色谱法中,所述离子为钠离子和/或铵离子时,色谱柱为阳离子交换柱;淋洗液为20mmol/l的甲烷磺酸溶液;淋洗方式为等度;所述离子为氯离子时,色谱柱为阴离子交换柱;淋洗液为20mmol/l的氢氧化钾溶液;淋洗方式为等度。本发明中,所述阳离子交换柱可为ionpaccs12a。本发明中,所述阴离子交换柱可为ionpacas11-hc。本发明中,所述色谱柱前还可有保护柱;当所述色谱柱为阳离子交换柱时,所述保护柱可为ionpaccg12a;当所述色谱柱为阴离子交换柱时,所述保护柱可为ionpacag11-hc。本发明中,所述离子色谱法中的流速可为1.0ml/min。本发明中,所述离子色谱法中的抑制器可为asrs-300型,优选自循环抑制模式,抑制电流为59ma。本发明中,所述离子色谱法中的检测器可为电导检测器,所述检测器的检测池温度较佳地为30℃。本发明中,所述色谱柱的温度可为30℃。本发明中,所述色谱柱的进样量可为25μl。本发明中,所述离子色谱仪可为美国thermo公司的ics-5000型离子色谱仪。本发明中,所述瓜蒌皮注射液待测品一般是通过将瓜蒌皮注射液进行稀释处理得到;例如,将瓜蒌皮注射液用水稀释得到瓜蒌皮注射液待测品。本发明中,所述含量测定的方法可参考本领域的常规含量测定方法,例如:步骤(1)、分别配置一定浓度的标准品溶液和瓜蒌皮注射液待测品,采用上述离子色谱法对所述标准品溶液和所述瓜蒌皮注射液待测品进行检测;测得所述标准品溶液和所述瓜蒌皮注射液待测品中各离子的峰面积;步骤(2)、根据所述标准品溶液中所述钠离子、铵离子或氯离子的峰面积和相应的组分浓度,得到回归方程;步骤(3)、所述瓜蒌皮注射液待测品中钠离子、铵离子或氯离子的含量由步骤(1)中测得的各离子的峰面积的代入步骤(2)中得到的回归方程,即可算得。在不违背本领域常识的基础上,上述各优选条件,可任意组合,即得本发明各较佳实例。本发明所用试剂和原料均市售可得。本发明的积极进步效果在于:该方法可在同台离子色谱仪上将氯离子、钠离子和铵离子实现基线分离;操作简便快捷;结果准确可靠;有助于进一步阐明瓜蒌皮注射液的物质基础组成,更能够为其安全性、有效性和质量可控性研究提供一定的参考。附图说明图1为实施例1中标准品的离子色谱图。图2为实施例1中供试品的离子色谱图。图3为实施例2中标准品的离子色谱图。图4为实施例2中供试品的离子色谱图。具体实施方式下面通过实施例的方式进一步说明本发明,但并不因此将本发明限制在所述的实施例范围之中。下列实施例中未注明具体条件的实验方法,按照常规方法和条件,或按照商品说明书选择。仪器与试药ics-5000型离子色谱仪(美国thermo公司);瓜蒌皮注射液超纯水(milli-q,默克密理博公司);氯化铵(sigma,a9434-500g,优级纯)水中氯标准溶液(1.0mg/ml,国家有色金属及电子材料分析测试中心gsb04-1770-2004,149033-2);水中钠(1.0mg/ml,上海市计量测试技术研究院gbw(e)080276,130201)。实施例1:阴离子(氯离子)测定1、色谱条件色谱柱:ionpacas11-hc(4mm×250mm)阴离子交换柱;保护柱:ionpacag11-hc(4mm×50mm);淋洗液:20mmol/l氢氧化钾溶液等度洗脱;流速:1.0ml·min-1;抑制器:asrs-300型,自循环抑制模式,抑制电流50ma;检测器:电导检测器;检测池温度:30℃;柱温:30℃;进样量:25μl。2、供试品溶液的制备精密量取瓜蒌皮注射液0.1ml,置10ml量瓶中,加水稀释至刻度,摇匀,将溶液通过dionexonguardtmiirp小柱,弃去先流出的3ml流出液,收集其余的流出液即得。3、标准品溶液的制备精密吸取水中氯适量,用水稀释成氯离子浓度分别为1,5,10,20,50,100mg/l的系列标准品溶液。实验结果:1、方法检出限、定量限和线性范围分别吸取氯离子系列标准品溶液各25ul,注入离子色谱仪,测定峰面积,以标准品溶液浓度为横坐标,峰面积为纵坐标,绘制标准曲线,结果显示各成分线性关系良好。色谱图见图1。其中,峰1代表氯离子,保留时间为5.917min。回归方程、最低检测限(llod)和最低定量限(lloq)结果见表1。表1名称lod(μg/ml)loq(μg/ml)线性范围(mg/l)回归方程r氯离子0.0110.0381~1000.279x-0.3340.99992、精密度、重复性和稳定性试验2.1精密度取瓜蒌皮注射液,按上述实施例1中第2节中的方法制备供试品溶液,依上述实施例1中第1节中色谱条件连续进样6次。第一次进样的色谱图见图2,峰1为氯离子,保留时间为5.924min。结果显示:氯离子的峰面积的rsd为0.53%,表明仪器精密度良好。2.2重复性取同批号瓜蒌皮注射液6份,按上述实施例1中第2节中的方法制备待测品溶液,依上述实施例1中第1节中色谱条件进样测定含量。结果氯离子的峰面积的rsd为1.27%,表明方法重复性良好。2.3稳定性取重复性项下同一待测品溶液,在制备后0,4,8,12,16,20,24h进样测定,结果氯离子的峰面积的rsd为1.98%,表明待测品溶液在24h内成分稳定性良好。3、加样回收率试验取瓜蒌皮注射液50μl,一式9份,置10ml量瓶中,分别精密加入1.0mg/ml氯离子标准溶液110μl、140μl和170μl,各3份,按上述实施例1中第2节中的方法制备供试品溶液,进样分析,进行低、中、高3个浓度水平的加样回收试验,结果氯离子平均加样回收率为98.2%,rsd为2.06%,表明方法加样回收率良好。实施例2:阳离子(钠离子、铵离子)测定1、色谱条件色谱柱:ionpaccs12a(4mm×250mm)阳离子交换柱;保护柱:ionpaccg12a(4mm×50mm);淋洗液:20mmol/l甲烷磺酸溶液等度洗脱;流速:1.0mlml/min;抑制器:asrs-300型,自循环抑制模式,抑制电流59ma;检测器:电导检测器;检测池温度:30℃;柱温:30℃;进样量:25μl。2、供试品溶液的制备精密量取瓜蒌皮注射液0.1ml,置10ml量瓶中,加水稀释至刻度,摇匀,将溶液通过dionexonguardtmiirp小柱,弃去先流出的3ml流出液,收集其余的流出液即得。3、标准品溶液的制备精密称取优级纯氯化铵固体0.7430g,置250ml量瓶中,加水溶解并稀释至刻度,即得铵离子标准品储备液(浓度为1000mg/l)。分别精密吸取水中钠和铵离子标准品储备液适量,用水稀释成钠离子和铵离子浓度分别为1,5,10,20,50,100mg/l的系列混合标准品溶液。实验结果:1、方法检出限、定量限和线性范围分别吸取钠离子和铵离子系列混合标准品溶液各25ul,注入离子色谱仪,测定峰面积,以标准品溶液浓度为横坐标,峰面积为纵坐标,绘制标准曲线,结果显示各成分线性关系良好。回归方程、最低检测限(llod)和最低定量限(lloq)结果见表2。色谱图见图3,其中,峰1代表钠离子,保留时间为4.293min;峰2代表铵离子,保留时间为4.893min。表2名称lod(μg/ml)loq(μg/ml)线性范围(mg/l)回归方程r钠离子0.0040.0131~1000.281x-0.0090.9999铵离子0.0050.0151~20-0.004x2+0.211x+0.0560.99822、精密度、重复性和稳定性试验2.1精密度取瓜蒌皮注射液,按上述实施例2中第2节中的方法制备供试品溶液,依上述色谱条件连续进样6次。第一次进样的色谱图见图4,峰1为钠离子,保留时间为4.297min;峰2为铵离子,保留时间为4.890min。结果钠离子和铵离子的峰面积的rsd分别为0.03%和0.07%,表明仪器精密度良好。2.2重复性取同批号瓜蒌皮注射液6份,按上述实施例2中第2节中的方法制备待测品溶液,依上述色谱条件进样测定含量。结果钠离子和铵离子的峰面积的rsd分别为0.10%和0.13%,表明方法重复性良好。2.3稳定性取重复性项下同一待测品溶液,在制备后0,4,8,12,16,20,24h进样测定,结果钠离子和铵离子的峰面积的rsd分别为0.28%和1.43%,表明待测品溶液在24h内成分稳定性良好。3、加样回收率试验取瓜蒌皮注射液50μl,一式9份,置10ml量瓶中,分别精密加入1.0mg/ml钠离子标准溶液48μl、60μl、72μl和铵离子对照品储备液36μl、45μl、54μl,各3份,按上述实施例2中第2节中的方法制备供试品溶液,进样分析,进行低、中、高3个浓度水平的加样回收试验,结果钠离子和铵离子平均加样回收率分别为99.9%和99.4%,rsd分别为1.71%和2.77%,表明该方法加样回收率良好。实施例3:待测品测定取21批瓜蒌皮注射液,,上海上药第一生化药业有限公司,4ml/支编号批号114104022141040331410404416074015160740361607404716074058160740691607407101609402111609403121609404131609405141501401151501403161503401171503402181503403191503405201503406211503407分别按实施例1中第2节和实施例2中第2节的方法制备待测品溶液,并按上述实施例1和实施例2中的色谱条件进样测定,结果不同批次瓜蒌皮注射液中氯离子、钠离子和铵离子的含量分别在2.441~3.322mg/ml、0.943~1.404mg/ml和0.720~1.185mg/ml之间。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1