一种可见光促进药物释放的药物载体及其制备方法与流程
本发明涉及药物载体,具体属于一种可见光促进药物释放的药物载体及其制备方法。
背景技术:
近年来,癌症已逐渐成为人类致死的主要原因,如何治疗癌症已成为当今医学界亟待解决的重大难题之一。传统的化学疗法是癌症综合治疗中不可缺少的重要手段,但是传统的化疗方法具有毒副作用大、缺乏特异识别性、药物利用率低等缺点,大大的限制了其在癌症治疗中的应用与发展。环境响应性载药系统可以根据不同的外界刺激实现药物的智能释放,比如Ph、温度、光照、氧化还原等刺激都可以实现药物的智能释放。利用正常细胞与肿瘤细胞的差异或外界刺激,将抗肿瘤药物特异性的送进肿瘤细胞并智能释放药物,这样不仅可以减少对人体正常细胞的损伤,还有利于难溶性药物的吸收和提高生物利用度。
目前,环境响应性药物载体系统分别有Ph型响应、温敏型响应、光响应、氧化还原型响应等多种类型响应。但是,与众多环境响应性药物载体相比,光响应药物载体具有不受空间限制、且能源干净的优点。而众多光响应药物载体的研究中,实现刺激所用的光大多数为波长为365nm的紫外光,这样就大大限制了其在医学上的使用。本发明利用常见的光致变色分子螺吡喃与β-环糊精反应合成了β-环糊精-SPCOOH,构造了一种可以利用可见光照射促进药物释放的光响应药物载体。
技术实现要素:
本发明的目的在于构造一种由可见光促进药物释放的药物载体及其制备方法。
为实现上述目的,本发明提供如下技术方案:
一种可见光促进药物释放的药物载体,它是β-环糊精-SPCOOH,结构式为:
一种可见光促进药物释放的药物载体的备方法,包括如下步骤:
(1)1-(2-羟乙基)-2,3,3-三甲基吲哚啉的合成
取2,3,3-三甲基吲哚7.4mmol和3-溴丙酸7.4mmol加入到50ml单口烧瓶中。15ml甲苯做溶剂。115℃加热回流13-15h。回流结束后,自来水冷却降温,有紫黑色固体析出,强力粘在底部。甲苯洗涤一次,然后用二氯甲烷溶解,溶解后缓慢倒入乙酸乙酯中,有固体析出(橘红色)。抽滤,获得产物。
(2)带有羧基的光致变色螺吡喃分子SPCOOH的合成
取1-(2-羟乙基)-2,3,3-三甲基吲哚啉0.64mmol和0.77mmol 5-硝基水杨醛加入到50ml单口烧瓶中,10ml乙醇做溶剂,并加入0.15ml三乙胺,90℃加热回流8h。回流结束后,自来水冷却30min,有固体析出,过滤,晾干,获得产物。
(3)β-环糊精-SPCOOH的合成
SPCOOH 4mmol和β-环糊精1.5mmol加入到干燥的DMF(30ml)中,其中加入DCC(0.021mol)和DMAP(0.0021mol)25℃搅拌24h。混合物过滤,滤液加到冷的甲醇里析出沉淀。重新溶于DMF,再重新沉淀于甲醇中,重复几次。最后产物用大量去离子水洗涤。通过硅胶柱进一步纯化。
本发明与现有的光响应药物释放药物载体相比的优点:大多数利用螺吡喃分子的光响应药物释放体系是利用紫外光促进药物释放,紫外光不仅穿透性差,而且容易灼烧皮肤,长时间照射也会对正常细胞造成损害。本发明首次用光致变色分子螺吡喃与β-环糊精结合,将光响应药物载体促使药物释放的波长由365nm的紫外光延伸到400-800nm的可见光范围。可改善现有光响应药物释放药物载体存在的一些缺陷。
附图说明
图1 1-(2-羟乙基)-2,3,3-三甲基吲哚啉的1H核磁谱图
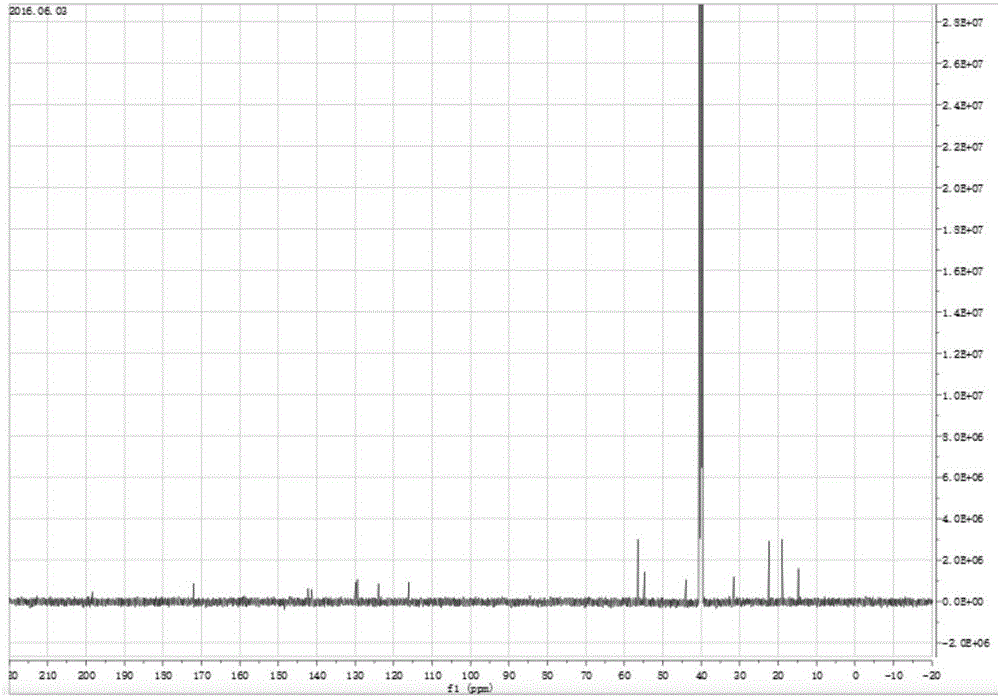
图2 1-(2-羟乙基)-2,3,3-三甲基吲哚啉的13C核磁谱图
图3 1-(2-羟乙基)-2,3,3-三甲基吲哚啉的傅里叶红外谱图
图4带有羧基的螺吡喃分子SPCOOH的1H核磁谱图
图5带有羧基的螺吡喃分子SPCOOH的13C核磁谱图
图6β-环糊精-SPCOOH的1H核磁谱图
图7β-环糊精、SPCOOH与β-环糊精-SPCOOH的傅里叶红外对比图
图8可见光不同时间照射条件下阿霉素的荧光吸收强度变化图
图9 365nm紫外光不同时间照射条件下阿霉素的荧光吸收强度变化图
具体实施方式
实施例1:β-环糊精-SPCOOH的合成
(1)1-(2-羟乙基)-2,3,3-三甲基吲哚啉的合成
首先用移液枪量取2,3,3-三甲基吲哚1.2ml,然后称取3-溴丙酸(1.14g),两者分别加入到50ml单口烧瓶中。用50ml量筒量取15ml甲苯做溶剂。加入到单口烧瓶中,115℃加热回流15h。回流结束后,自来水冷却降温,有紫黑色固体析出,强力粘在底部。甲苯洗涤一次,然后用二氯甲烷溶解,溶解后缓慢倒入乙酸乙酯中,有固体析出(橘红色)。抽滤,获得产物。产物表征见图1-3。
(2)带有羧基的螺吡喃分子SPCOOH的合成
秤取1-(2-羟乙基)-2,3,3-三甲基吲哚啉0.2g和0.13g 5-硝基水杨醛加入到25ml单口烧瓶中,10ml乙醇做溶剂,并加入0.15ml三乙胺,90℃加热回流8h。回流结束后,自来水冷却30min,有固体析出,过滤,晾干,获得产物。产物表征见图4、图5。
(3)β-环糊精-SPCOOH的合成
分别称取SPCOOH 1.5g和β-环糊精1.70g分别加入到干燥的DMF 30ml中,其中再加入DCC 2.163g和DMAP0.13g 25℃搅拌24h。混合物过滤,滤液加到冷的甲醇里析出沉淀。然后将沉淀重新溶于DMF,再重新沉淀于甲醇中,重复3次。最后产物用大量去离子水洗涤。通过硅胶柱进一步纯化,获得产物。(洗脱剂所用系统为乙酸乙酯:石油醚=2:8,乙腈:水=10:1)。产物表征见图6、图7。
实施例2:β-环糊精-SPCOOH对药物阿霉素光控释放的性能
取β-环糊精-SPCOOH 5mg,1mg/ml的阿霉素水溶液100微升,分别加入到体积比1:1的乙醇和水的混合溶液中,黑暗条件下磁力搅拌5h。5h后,将溶液分成两部分,分别在可见光和365nm的紫外光下按照不同的时间间隔进行照射,然后用荧光测定溶液中阿霉素的浓度来确定阿霉素的释放与不同波长光照射之间的关系。图8为在激发波长480nm,发射波长为592nm条件下的荧光图(阿霉素的激发波长在480nm)。由图可以看出,随着可见光光照时间的增加,阿霉素的浓度逐渐增大,说明可见光促进了药物阿霉素的释放。图9则为在365nm的紫外光条件下阿霉素的荧光强度变化图。证明了本药物载体随着不同波长光变换的环境响应性能。
- 还没有人留言评论。精彩留言会获得点赞!
- 一种基质金属蛋白酶响应性聚合物药物载体及其制备方法和应用与流程
- 环糊精-金属有机骨架材料的快速合成方法与流程
- 一种谷胱甘肽/超声双重刺激响应纳米聚合物囊泡、其制备方法及应用与流程
- 一种多重刺激响应交联型聚合物纳米水凝胶、其制备方法及应用与流程
- 一种新型铃铛结构的介孔二氧化硅纳米颗粒的制备方法及其应用与流程
- 羧酸改性聚苹果酸的方法及其产品和应用与流程
- 一种多孔沸石类催化剂载体及其制备方法以及催化剂与流程
- 一种纳米载药系统(DOX‑RGD‑BSA@AuNCs)药物传递和生物成像的制造方法与工艺
- 一种携载抗肿瘤药物连接CD22单抗靶向淋巴瘤的血小板靶向载药体系的制备方法与流程
- 肿瘤靶向光热响应可控释放药物纳米传输载体的制备方法与流程