特异性抗人上皮细胞粘附分子(EpCAM)的单克隆抗体的制备、鉴定及应用的制造方法与工艺
本发明涉及到两株抗人EpCAM的单克隆抗体。具体地说,涉及到对EpCAM第24至265位氨基酸序列中的位点有特异性的单克隆抗体,本发明还涉及产生这两种单克隆抗体的杂交瘤细胞株,以及所述单克隆抗体的制备方法和应用。
背景技术:
循环肿瘤细胞的发现最早在1869年,被定义为起源于原位肿瘤病灶或肿瘤转移病灶,并能够在病人的外周血中循环而在正常人的外周血中极少存在的一类肿瘤细胞。肿瘤诱发的血管生成通常伴随着肿瘤的侵袭,其结果是增加原位肿瘤释放高侵袭性肿瘤细胞进入外周循环的可能性。而高侵袭能力的循环肿瘤细胞不仅可以在远端器官内建立新的肿瘤病灶,也能够以肿瘤自播的形式回到原位肿瘤所在的器官内建立新的肿瘤病灶。临床癌症患者死亡率高的一个重要因素就是转移后肿瘤细胞的存在,另外循环肿瘤细胞的存在也是肿瘤手术切除后复发的主要原因。目前可行的几种循环肿瘤细胞检测平台已经通过多项临床研究证实,对于循环肿瘤细胞的检测有助于对恶性肿瘤的诊断和预后评估以及对肿瘤复发和抗癌治疗效果的监测。上皮细胞粘附分子(EpCAM:epithelialcelladhesionmolecule),又称:ESA;KSA;M4S1;MK-1;DIAR5;EGP-2;EGP40;KS1/4;MIC18;TROP1;EGP314;HNPCC8;TACSTD1等,表达于所有正常的上皮细胞,在肿瘤细胞和增殖活跃的细胞上则呈现不同程度的表达上升,是最早被鉴定出与肿瘤相关的抗原之一。研究表明EpCAM也在肿瘤干细胞表面表达,它是wnt通路的信号受体和激活蛋白,而wnt通路调节着癌基因(比如c-myc)的表达。因此,EpCAM分子的表达从基础上关系到肿瘤的发生和发展。由于EpCAM分子表达于多种肿瘤细胞的表面,将抗EpCAM的抗体用于循环肿瘤细胞的诊断和治疗会获得更广泛的应用。同时通过鉴定该抗体的功能,探讨以EpCAM分子作为靶标的生物治疗也具有重要的临床意义。
技术实现要素:
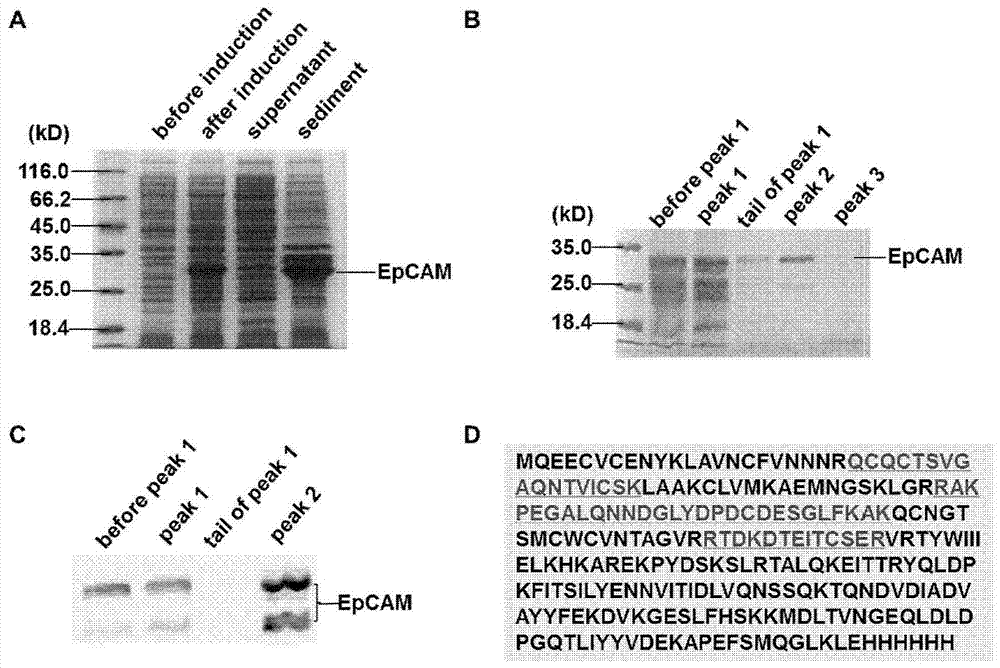
本发明的一个目的是提供一种对人上皮细胞粘附分子(EpCAM)分子有特异性的单克隆抗体,所述单克隆抗体特异性针对人EpCAM第24至265位的氨基酸序列。本发明的又一个目的是提供产生单克隆抗体的杂交瘤细胞株EpCAM-mAb-AE4和EpCAM-mAb-AE7。由这两株杂交瘤细胞株所分泌的单克隆抗体在本文中分别简称为AE4单克隆抗体和AE7单克隆抗体。本发明的又一个目的是提供本发明的单克隆抗体的制备方法。本发明的又一个目的是提供AE4和AE7的单克隆抗体在流式细胞术检测白血病患者外周血内EpCAM表达实验中的应用。本发明的又一个目的是提供AE4和AE7的单克隆抗体在细胞免疫荧光检测肿瘤细胞的EpCAM表达实验中的应用。本发明的又一个目的是提供AE4和AE7的单克隆抗体在体外能够通过抗体依赖性细胞介导的细胞毒作用杀伤肿瘤细胞并且能够抑制体内肿瘤的生长。有益效果:本发明提供了两株抗人EpCAM的单克隆抗体、其制备方法、鉴定及应用,其特异性好,灵敏度高。能够应用于检测人外周血和肿瘤组织中EpCAM的表达,作为癌症转移诊断和预后评估指标之一。另外,本发明的单克隆抗体可以通过抗体依赖性细胞介导的细胞毒作用杀伤肿瘤细胞以及抑制体内肿瘤的生长,因此,此发明对癌症的诊断及治疗具有重大的临床意义。具体说来,本发明的一个方面涉及两种EpCAM特异性的单克隆抗体及其制备方法,这两种单克隆抗体在本发明中分别称为AE4和AE7,它们的类型分别为IgG2b,κ和IgG2a,κ,它们均针对EpCAM第24-265位氨基酸序列。本发明的另外一个方面涉及稳定分泌EpCAM单克隆抗体的杂交瘤细胞株EpCAM-mAb-AE4和EpCAM-mAb-AE7。这两株杂交瘤细胞株已经于2013年5月15日保藏于中国典型培养物保藏中心(CCTCC,中国武汉,武汉大学,邮编:430072),保藏编号分别为CCTCCNO:C201371和CCTCCNO:C201373。本发明的另外一个方面涉及制备所述单克隆抗体的方法。制备方法包括重组蛋白EpCAM的表达与纯化,用纯化后蛋白免疫小鼠,取免疫后小鼠的脾细胞与骨髓瘤Sp2/0细胞融合,筛选出能够稳定分泌对重组EpCAM有反应性的单克隆抗体的杂交瘤细胞,从杂交瘤细胞培养上清中或者从小鼠腹水中获取单克隆抗体。本发明的另一方面涉及AE4和AE7单克隆抗体在流式检测肿瘤细胞系和癌症患者血液标本中的EpCAM表达的应用。用本发明的AE4或AE7单克隆抗体通过流式技术检测肿瘤细胞系和癌症患者外周血中的EpCAM蛋白的表达,结果显示:AE4和AE7单克隆抗体能在流式水平用于检测肿瘤细胞和癌症患者外周血中的EpCAM表达。本发明的另一方面涉及AE4和AE7单克隆抗体在免疫荧光检测肿瘤细胞及肿瘤组织内EpCAM表达中的应用。用本发明的AE4或AE7单克隆抗体通过免疫荧光实验鉴定肿瘤细胞系和肿瘤组织上EpCAM蛋白的表达,结果显示:AE4和AE7单克隆抗体能在免疫荧光水平用于检测肿瘤细胞系和肿瘤组织中的EpCAM表达。本发明的另一方面涉及AE4和AE7单克隆抗体在体外通过抗体依赖性细胞介导的细胞毒作用杀伤肿瘤细胞,将本发明的AE4或AE7单克隆抗体与小鼠脾细胞(或NK细胞)和51Cr标记的NCI-H292(或K562)细胞共孵育,通过检测上清中的51Cr的释放量计算杀伤效率,结果显示这两株抗体都具有抗体依赖性细胞介导的细胞毒作用。本发明的另一方面涉及AE4和AE7单克隆抗体能够体内抑制移植性肿瘤(移植性肿瘤:人肺癌细胞系NCI-H292细胞接种于裸鼠皮下)的生长,肿瘤大小测量结果显示:AE4和AE7单克隆抗体能够减缓肿瘤的生长。可以使用本发明的AE4或AE7单克隆抗体检测或抑制的癌症选自白血病、肺癌等。因此,本发明提供下列各项:1.一种特异性抗人上皮细胞粘附分子(EpCAM)的单克隆抗体,所述单克隆抗体特异性针对人上皮细胞粘附分子第24至265位的氨基酸序列。2.根据第1项所述的单克隆抗体,其亚型为IgG2a,κ或IgG2b,κ。3.分泌第1项所述的单克隆抗体的杂交瘤细胞株,其保藏编号为CCTCCNO:C201371或CCTCCNO:C201373。4.第1项所述的特异性抗人上皮细胞粘附分子的单克隆抗体在制备用于检测癌症的存在和/或转移的检测剂或试剂盒中的应用。5.根据第4项所述的应用,其中通过第1项所述的单克隆抗体检测人外周血和肿瘤组织中上皮细胞粘附分子的表达来判断癌症的存在和/或转移。6.根据第4项所述的应用,其中所述癌症选自白血病或肺癌。7.第1项所述的特异性抗人上皮细胞粘附分子的单克隆抗体在制备用于抑制体内肿瘤生长和/或转移的药物中的应用。8.根据第7项所述的应用,其中所述癌症选自白血病或肺癌。9.一种用于检测癌症存在和/或转移的检测剂或试剂盒,所述检测剂或试剂盒包含有效量的第1项所述的特异性抗人上皮细胞粘附分子的单克隆抗体。10.根据第9项所述的检测剂或试剂盒,其中所述癌症选自白血病或肺癌。11.一种用于抑制肿瘤细胞增殖和/或抑制肿瘤生长和/或转移的药物,所述药物包含治疗有效量的第1项所述的特异性抗人上皮细胞粘附分子的单克隆抗体。12.根据第11项所述的药物,其中所述癌症选自白血病或肺癌。本发明中,术语“单克隆抗体的特异性”是指单克隆抗体识别抗原上的特定表位或者抗原决定簇并与之结合的性质。术语“单克隆抗体的反应性”是指在合适的反应条件下,单克隆抗体与抗原结合的能力。术语“细胞株”是指通过筛选或者有限稀释方法,从原代培养物或者细胞系获得的单细胞培养物。根据本发明的公开,选择EpCAM蛋白的C端(第24个氨基酸-第265个氨基酸),按照本文描述的方法制备有特异性的单克隆抗体对本领域的技术人员而言是显而易见的,应该视为包含在本发明的范围内。附图说明从下面结合附图的详细描述中,本发明的上述特征和优点将更明显,其中:图1,原核重组表达载体pET22b(+)-EpCAM的构建流程图。图2,EpCAM重组蛋白的表达、纯化和鉴定。A.重组蛋白诱导表达并以包涵体形式存在的鉴定结果;B.重组蛋白免疫印迹鉴定结果;C.蛋白纯化结果;D.纯化后EpCAM蛋白的质谱鉴定结果。图3,单克隆抗体纯度鉴定结果。图4,AE4和AE7单克隆抗体应用于流式检测。A.EpCAM抗体AE4和AE7流式检测肿瘤细胞表面EpCAM分子的表达结果;B.EpCAM抗体AE4和AE7流式检测白血病患者外周血内EpCAM分子的表达结果。图5,AE4和AE7单克隆抗体应用于免疫荧光检测。A.EpCAM抗体AE4和AE7免疫荧光检测肿瘤细胞表面EpCAM分子的表达结果;B.EpCAM抗体AE4和AE7免疫荧光检测肺癌患者肿瘤内EpCAM分子的表达结果。图6,AE4和AE7单克隆抗体应用于体外杀伤肿瘤细胞。A.EpCAM抗体AE4和AE7体外杀伤肺癌细胞NCI-H292细胞结果;B.EpCAM抗体AE4和AE7体外杀伤白血病细胞K562细胞结果。图7,AE4和AE7单克隆抗体应用于抑制移植性皮下肿瘤(肺癌)的生长。序列表说明SEQIDNo.1人EpCAM的cDNA序列(NCBIReferenceSequence:NP_002345)SEQIDNo.2人EpCAM的蛋白序列(UniProtKB/Swiss-Prot:P16422.2)SEQIDNo.3原核重组表达的EpCAM氨基酸序列具体实施方式下面参照具体的实施例进一步描述本发明,有助于本领域的普通技术人员进一步理解本发明,但是本领域技术人员应该理解,本发明并不限于这些具体的实施例。实施例中的实验方法,如无特别说明,均采用本领域常规技术,实验试剂均为市售分析级产品。实施例1:原核重组表达载体pET22b(+)-EpCAM的构建通过RT-PCR技术从A549细胞(购自美国ATCC)中获取EpCAM胞外段cDNA(人EpCAM的cDNA序列见NCBIReferenceSequence:NP_002345,SEQIDNo.1,其胞外段cDNA序列是指SEQIDNo.1的第70-795位核苷酸序列),并克隆到pMD18T载体(购自TAKARA公司)中构建pMD18T-EpCAM重组载体。设计上游引物5’-GGAATTCCATATGCAGGAAGAATGTGTCTGTGA-3’和下游引物5’-CCGCTCGAGTTTTAGACCCTGCATTGAG-3’。以pMD18T-EpCAM为目的片段来源,经过NdeI和XhoI酶切之后克隆到pET-22b(+)载体(购自Novagen公司),转入DH5α菌(购自全式金公司)中,筛选阳性克隆进行DNA测序鉴定,测序结果表明重组表达载体pET22b(+)-EpCAM构建成功。原核重组表达载体pET22b-EpCAM的构建流程如图1所示。实施例2:重组EpCAM蛋白的表达,复性,纯化及鉴定。1,重组EpCAM蛋白的诱导表达将pET22b(+)-EpCAM转入到大肠杆菌BL21感受态细胞(购自Novagen公司)中,挑选单克隆菌落接种于含有50μg/ml氨苄青霉素的LB培养基中,置于37℃摇床,200转/分钟培养至OD600nm=0.6-0.8时,加入1mM异丙基-β-D-硫代半乳糖苷(IPTG),继续培养4小时诱导蛋白表达。4℃、6000g离心10分钟收菌,沉淀用裂菌缓冲液(50mM三羟甲基氨基甲烷、100mM氯化钠,pH8.5)洗涤之后,用高压破碎方法裂菌。裂菌后的混合体进行十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(SDS-PAGE)鉴定,如图2A结果显示,和对照相比,IPTG诱导后菌裂解液在28kDa处有一条明显的条带。裂菌后的上清和沉淀分别进行SDS-PAGE鉴定,结果显示重组蛋白主要以包涵体形式存在,如图2A所示。2,重组EpCAM蛋白的复性及纯化。采用稀释复性的方法对重组EpCAM蛋白进行复性。具体方法:大量诱导BL21/pET22b(+)-EpCAM菌,通过高压破碎,4℃、6000g离心10分钟,弃上清,沉淀用包涵体洗涤缓冲液(50mM三羟甲基氨基甲烷、100mM氯化钠、2M尿素、1mM二硫苏糖醇,pH8.5)洗涤3次,每次4℃、6000g离心10分钟,弃上清。包涵体沉淀用包涵体裂解液(50mM三羟甲基氨基甲烷、100mM氯化钠、8M尿素、1mM二硫苏糖醇,pH8.5)溶解,室温搅拌1小时。4℃、12000g离心10分钟,取上清,以1∶500比例缓慢加入到复性缓冲液(50mM三羟甲基氨基甲烷、100mM氯化钠、0.5ML-精氨酸、3mM还原型谷胱甘肽、0.3mM氧化性谷胱甘肽,pH9.5)中,4℃静置24小时,复性蛋白用Millipore公司的LabScaleTEFsystem(5kDa浓缩膜)进行浓缩,蛋白浓缩液在透析缓冲液(50mM三羟甲基氨基甲烷、100mM氯化钠,pH9.0)中透析过夜。浓缩后的复性蛋白用镍柱亲和层析纯化,不同浓度的咪唑洗脱目的蛋白,在100mM咪唑洗脱液(50mM三羟甲基氨基甲烷、100mM氯化钠、200mM咪唑,pH9.0)中得到纯度一般的重组EpCAM蛋白。进一步用分子筛层析(S-200)纯化,洗脱缓冲液(50mM三羟甲基氨基甲烷、100mM氯化钠,PH9.2)洗脱到90ml时,得到纯度较高复性效果较好的重组EpCAM蛋白洗脱液,将含有目的蛋白的洗脱液用Millipore浓缩管进行浓缩和Bio-Rad蛋白定量试剂盒进行定量,最后可以得到纯度大于90%、浓度为1mg/ml的EpCAM重组蛋白。由于EpCAM蛋白在表达和纯化过程中存在降解,所以其以两条带的形式存在,结果如图2B所示。3,重组EpCAM蛋白的鉴定。对上述纯化后的目的条带进行免疫印迹检测,即小鼠抗His-tag抗体(购自Abmart公司,货号M20001)1∶1000稀释作为一抗,辣根过氧化物酶标记的...
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1