一种具有螺吡喃特性的手性荧光探针及其制备方法和应用与流程
本发明属于荧光探针技术领域,具体涉及一种具有螺吡喃特性的手性荧光探针及其制备方法和应用。
背景技术:
手性是自然界的基本属性,参与生命活动的重要生物大分子,如蛋白质,多糖,酶等都具有手性;生命活动中发生的各种生物、化学反应过程均与手性识别和变化密切相关。因此设计和合成具有对映选择性识别和传感性能的主体分子,并将其用于手性化合物手性组成的快速分析具有重要的研究意义。相比其他识别方法,荧光识别由于具有高灵敏性、多重信号模式、背景零干扰、实时性、仪器方便易得等优点,利用荧光法来识别手性分子得到极大的关注。
螺吡喃作为一种有机光致变色化合物,能够发生无色闭环体螺吡喃与有色开环体部花菁之间可逆的结构异构化,由于具有特殊的分子识别能力和信号传导功能,已经成为分子探针领域极具吸引力的主体分子之一。由于其特殊的光致变色性质,螺吡喃在化学和生物传感方面得到了广泛的应用,但是目前还没有报道将其应用于对手性分子的荧光识别。
技术实现要素:
针对现有技术中存在的上述问题,本发明提供一种具有螺吡喃特性的手性荧光探针及其制备方法和应用,该荧光探针能够实现对水溶液中的手性氨基酸的对映选择性,并能进一步用于细胞中对氨基酸的手性识别。
为实现上述目的,本发明解决其技术问题所采用的技术方案是:
一种具有螺吡喃特性的手性荧光探针,其结构式如下:
上述具有螺吡喃特性的手性荧光探针的制备方法,包括以下步骤:
将1-丙酸-2,3,3-三甲基吲哚季铵盐与(s)-2,2’-二羟基-1,1’-联萘-3,3’-二醛基在哌啶存在下于乙醇中加热反应,反应结束后分离提纯,制得,合成路线如下:
进一步地,1-丙酸-2,3,3-三甲基吲哚季铵盐、(s)-2,2’-二羟基-1,1’-联萘-3,3’-二醛基和哌啶的摩尔比为0.8-1.5:1-2:1-2。
进一步地,1-丙酸-2,3,3-三甲基吲哚季铵盐、(s)-2,2’-二羟基-1,1’-联萘-3,3’-二醛基和哌啶的摩尔比为0.8:1.32:1.58。
进一步地,反应温度为70-80℃,反应时间为6-8h。
进一步地,分离提纯过程具体为:对反应产物进行中蒸馏,除去溶剂,然后以二氯甲烷和甲醇按体积比为40:1进行混合作为淋洗液,进行柱层析提纯。
上述具有螺吡喃特性的手性荧光探针可用于对映性选择识别溶液或细胞中氨基酸。
进一步地,氨基酸为苯丙氨酸、亮氨酸、缬氨酸、色氨酸或甲硫氨酸。
采用上述具有螺吡喃特性的手性荧光探针检测手性分子的方法,包括以下步骤:
将荧光探针、有机溶液、缓冲溶液、金属离子和手性分子混合,测定其荧光响应值,根据荧光响应值判断待测物质的构型或对映异构体组成比例。
进一步地,手性分子为氨基酸,有机溶液为四氢呋喃溶液,缓冲溶液为hepes缓冲液,金属离子为锌离子。
本发明提供的具有螺吡喃特性的手性荧光探针及其制备方法和应用,具有以下有益效果:
本发明螺吡喃手性荧光探针原料易得,合成简单,不仅能在水溶液中对映选择性识别苯丙氨酸,还可对细胞中的苯丙氨酸进行荧光成像,在手性识别领域具有广阔的应用前景。
附图说明
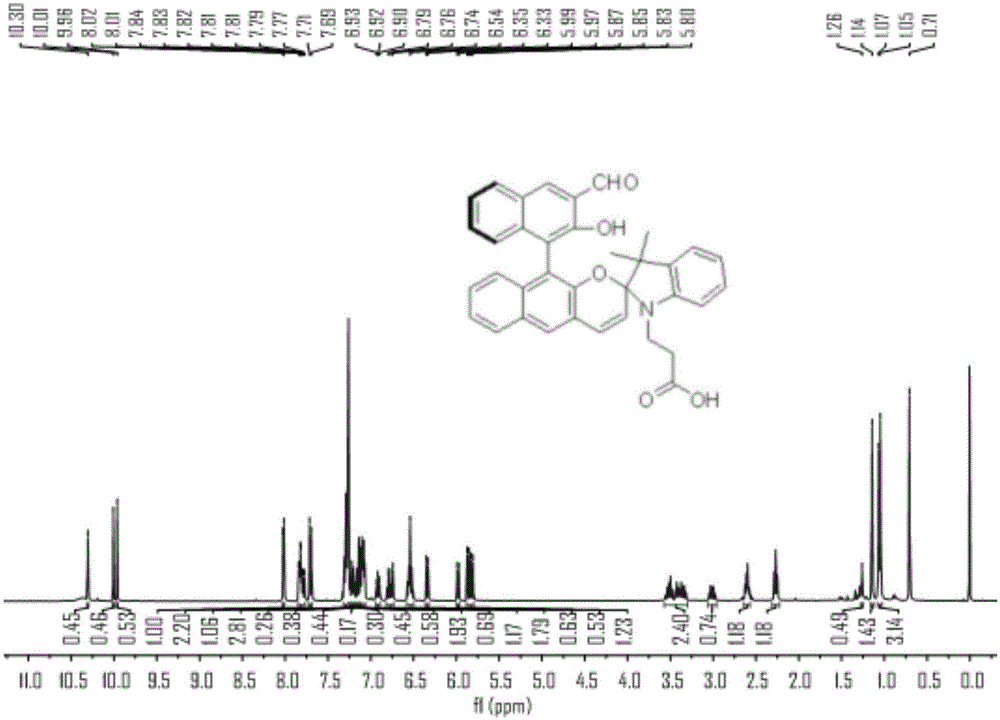
图1为探针(s)-3的1hnmr谱图。
图2为探针(s)-3的13cnmr谱图。
图3为探针(s)-3的质谱图。
图4为探针(s)-3在1%thf/hepes体系中对l-苯丙氨酸的荧光响应情况。
图5为荧光强度随d-苯丙氨酸浓度增加的变化情况,横坐标是波长,纵坐标是荧光强度;曲线从下到上表示当量为5-200eq。
图6为荧光强度随苯丙氨酸(d-苯丙氨酸、l-苯丙氨酸)浓度增加的变化情况,横坐标是当量,纵坐标是荧光强度。
图7为探针(s)-3和(r)-3在1%thf/hepes体系中,荧光强度随苯丙氨酸对映体组成比例改变的变化情况,横坐标是l-苯丙氨酸的质量百分比,纵坐标是荧光强度。
图8为探针(s)-3在1%thf/hepes体系中对l-亮氨酸的荧光响应情况。
图9为荧光强度随d-亮氨酸浓度增加的变化情况,横坐标是波长,纵坐标是荧光强度;曲线从下到上表示当量为5-200eq。
图10为荧光强度随亮氨酸(d-亮氨酸、l-亮氨酸)浓度增加的变化情况,横坐标是当量,纵坐标是荧光强度。
图11为探针(s)-3在1%thf/hepes体系中对l-缬氨酸的荧光响应情况。
图12为荧光强度随d-缬氨酸浓度增加的变化情况,横坐标是波长,纵坐标是荧光强度;曲线从下到上表示当量为5-200eq。
图13为荧光强度随缬氨酸(d-缬氨酸、l-缬氨酸)浓度增加的变化情况,横坐标是当量,纵坐标是荧光强度。
图14为探针(s)-3在1%thf/hepes体系中对l-色氨酸的荧光响应情况。
图15为荧光强度随d-色氨酸浓度增加的变化情况,横坐标是波长,纵坐标是荧光强度;曲线从下到上表示当量为5-200eq。
图16为荧光强度随色氨酸(d-色氨酸、l-色氨酸)浓度增加的变化情况,横坐标是当量,纵坐标是荧光强度。
图17为探针(s)-3在1%thf/hepes体系中对l-甲硫氨酸的荧光响应情况。
图18为荧光强度随d-甲硫氨酸浓度增加的变化情况,横坐标是波长,纵坐标是荧光强度;曲线从下到上表示当量为5-200eq。
图19为荧光强度随甲硫氨酸(d-甲硫氨酸、l-甲硫氨酸)浓度增加的变化情况,横坐标是当量,纵坐标是荧光强度。
图20为探针(s)-3对细胞内苯丙氨酸的荧光成像。
具体实施方式
实施例1手性荧光探针的制备
具有螺吡喃特性的手性荧光探针的制备方法,包括以下步骤:
将1-丙酸-2,3,3-三甲基吲哚季铵盐(377mg,0.8mmol)、(s)-2,2’-二羟基-1,1’-联萘-3,3’-二醛基(450mg,1.32mmol)与哌啶(134mg,1.58mmol)加入到15ml乙醇溶液中,加热回流反应6h,反应结束后对产物进行蒸馏除去溶剂,然后以二氯甲烷和甲醇按体积比为40:1进行混合作为淋洗液,进行柱层析提纯,制得目标产物,目标产物记为探针(s)-3,其1hnmr谱图如图1所示,13cnmr谱图如图2所示,质谱图如图3所示。
探针(r)-3的制备过程与探针(s)-3的制备过程一样,区别仅在于起始原料不同,制备探针(r)-3所用的起始原料为(r)-2,2’-二羟基-1,1’-联萘-3,3’-二醛基。
实施例2手性分子的识别
1、对苯丙氨酸的识别
将实施例1制得的荧光探针(s)-3和(r)-3分别溶于四氢呋喃溶液中,使其浓度为2mm,然后吸取20μl加到玻璃试管中,加入50mm的hepes缓冲液稀释至2ml(稀释后的探针浓度为2×10-5mol/l;h2o/thf=99/1,thf为1%,体系为1%thf/hepes体系),再加入2当量的醋酸锌和不同当量的苯丙氨酸,2h后测荧光强度变化情况,结果见图4-7。由图4-7可知,手性荧光探针探针(s)-3对于不同构型的苯丙氨酸的荧光强度差别较大,有很好的对映选择性,ef值约为9.6。
2、对亮氨酸、缬氨酸、色氨酸、甲硫氨酸的识别
根据上述对苯丙氨酸的识别方法测定分别加入亮氨酸、缬氨酸、色氨酸、甲硫氨酸后荧光强度变化情况,其结果见图8-19。
由图8-19可知,手性荧光探针探针(s)-3对于不同构型的亮氨酸、缬氨酸、色氨酸、甲硫氨酸的荧光强度差别较大,有很好的对映选择性。
实施例3对苯丙氨酸手性分子的细胞成像
将实施例1荧光探针(s)-3应用于hela细胞中进行荧光成像,具体操作步骤如下:
(1)将3份密度为3×105个/ml的hela细胞在温度为37℃,co2浓度为5%的培养箱中培养至细胞贴壁;
(2)取一份细胞,加20μm(s)-3孵育30min,用pbs缓冲液冲洗细胞3次,制样后在荧光显微镜下成像,激发波长为445nm;
(3)取一份细胞,加20μm(s)-3孵育30min,加入d-苯丙氨酸孵育2h,用pbs缓冲液冲洗细胞3次,制样后在荧光显微镜下成像,激发波长为445nm;
(3)取一份细胞,加20μm(s)-3孵育30min,加入l-苯丙氨酸孵育2h,用pbs缓冲液冲洗细胞3次,制样后在荧光显微镜下成像,激发波长为445nm。
探针(s)-3对细胞内苯丙氨酸的荧光成像结果图见图20,由图20可知,荧光探针(s)-3不仅在水溶液中对苯丙氨酸有很好的对映选择性,在细胞这样复杂微环境中也表现出很好选择性,加入不同构型的外源性苯丙氨酸,表现出不同的荧光增强,其中l-苯丙氨酸增强倍数明显大于d-苯丙氨酸。
- 还没有人留言评论。精彩留言会获得点赞!