人类ALK基因表达的检测引物、探针及检测试剂盒的制作方法
本发明涉及生物技术及医学领域,具体地说,涉及人类alk基因表达的检测。
背景技术:
间变性淋巴瘤激酶(anaplasticlymphomakinase,alk)最早发现于间变性大细胞淋巴瘤(anaplasticlargecelllymphoma,alcl)的一个亚型。alk基因位于染色体2p23位点,含有29个外显子,可编码含1620个氨基酸,分子量为200kda的i型跨膜蛋白alk。alk蛋白为一种受体酪氨酸激酶(receptortyrosinekinase,rtk),是rtk胰岛素超家族的成员。完整的alk具有三部分结构,即胞外区、亲脂性跨膜区和胞内酪氨酸激酶,其氨基酸激酶结构域由254个(1123至1376位)氨基酸残基组成。
alk的蛋白表达与神经外胚层的分化有关,正常的alk专一表达于神经系统中,如脑和神经索,尤其是新生儿的脑中,在正常人的其它组织中,alk几乎不表达。alk是重要的肿瘤相关基因,在许多恶性肿瘤中发现alk基因的异常表达,包括alcl、弥漫性大b细胞淋巴瘤、炎性肌纤维母细胞瘤及神经母细胞瘤、非小细胞肺癌(nsclc)等。alk基因异常引起的细胞过度增殖和凋亡下调是其主要致瘤原因。在3%-7%的nsclc中,alk基因可与其它基因发生融合,其中alk基因的主要融合断裂点绝大多数位于20号外显子。alk基因的融合会导致断裂点两侧的mrna发生差异表达,其3’端(外显子20-29)的mrna序列表达量明显高于5’端(外显子1-18)。故通过alk基因5’与3’端的差异表达,可以定性检测alk基因是否发生融合。
alk激酶抑制剂的效果与患者是否存在alk基因融合密切相关。克唑替尼是一种atp竞争性酪氨酸激酶抑制剂,既可特异性靶向抑制alk,也可抑制c-met和ros1等信号通路。克唑替尼分别于2011年和2013年被美国食品与药品管理局(fda)和中国国家食品药品监督管理总局(cfda)批准上市,用于治疗alk阳性的局部晚期或转移性nsclc患者。2015年的《中国间变性淋巴瘤激酶(alk)阳性非小细胞肺癌诊疗指南》中建议晚期非小细胞肺癌患者使用alktki治疗前必须检测alk融合变异状态。推荐所有含腺癌成分的非小细胞肺癌患者在诊断时常规进行alk融合基因或融合蛋白检测(1类证据)。
目前alk基因检测方法主要有荧光原位杂交(fish)、免疫组织化学法(ihc)、eml4-alk融合基因rt-qpcr方法以及alk基因表达荧光pcr法。虽然fish检测仍是经典alk诊断手段,但仍有以下缺点。1)fish检测对于操作和判读技术要求较高;2)晚期nsclc患者通常只能提供2mm左右的小活检组织,很难保证每个视野均存在50个以上的肺癌细胞进行判读。3)fish检测结果的判断界值(cut-off值)也存在商榷之处,已有多项研究发现少数alkfish阴性、ihc阳性的患者也能从克唑替尼治疗中明显获益。4)目前fish检测的成本昂贵。ihc法包括ventanaihc和普通ihc法。虽然ventanaihc具有操作简便、检测的准确度较高、相对于其他诊断方法价格便宜等优势,但ventanaihc需要专门的自动化染色仪器,这在一定程度限制了它在临床上的广泛使用。常规ihc存在灵敏度偏低,关键实验操作需要统一规范的问题。rt-qpcr法操作简单、灵敏度高,可以检测已知的alk融合变体类型,但无法检测未知的融合型是其最大的不足之处。
cn103290120a公开了用于检测人类alk基因表达的引物、探针及检测试剂盒,使用荧光pcr法进行alk基因表达检测,可检出浓度为5拷贝/μl,总量为25拷贝的阳性质粒。但该方法有以下不足:1)检测过程耗时较长,需要160分钟。2)未对体系的特异性进行验证,如体系对基因组dna耐受性,对野生型样本的耐受性。3)未引入质控体系,对样本的质量进行监控,可能会因样本质量较差,产生假阴性结果。4)体系的结果判读方式比较复杂,临床适用性稍差。
技术实现要素:
为了解决现有技术中存在的问题,本发明的目的是提供人类alk基因表达的检测引物、探针及检测试剂盒。
为了实现本发明目的,本发明的技术方案如下:
第一方面,本发明提供了用于检测人类alk基因表达的引物组合,包括seqidno:1-seqidno:8所示的序列。
不仅如此,本发明还提供了与所述引物组合配合使用的特异性探针,如seqidno:9-seqidno:12所示,所述探针的5’端修饰有fam或vic,3’端修饰有nfq-mgb。
第二方面,本发明提供了用于检测人类alk基因表达的试剂盒,其含有前述的引物组合与特异性探针。
为了提高所述试剂盒的检测准确度,所述试剂盒还含有质控系统,阳性对照液和空白对照液。
所述质控系统包含质控引物和质控探针,质控引物的序列如seqidno:13和seqidno:14所示,所述质控探针的序列如seqidno:15所示,所述质控探针的5’端修饰有fam或vic,3’端修饰有nfq-mgb。
所述阳性对照液含有3种质粒dna混合液,所述3种质粒dna分别含有alk基因外显子13-外显子15序列、alk基因外显子25-外显子27序列,以及b2m基因的一段序列,所述空白对照为tris-hcl缓冲液。上述3种质粒可为本领域技术人员熟知的质粒。
进一步地,所述试剂盒还包括本领域其他荧光pcr试剂盒的必要成分,如pcr缓冲液,hotstarttaq酶和ung酶。
所述试剂盒的使用方法包括以下步骤:
(1)提取检测样本中的rna,检测样本包括新鲜病理组织、石蜡包埋组织或胸腔液;
(2)将提取的rna逆转录为cdna,以cdna为模板进行实时荧光pcr扩增反应;
(3)根据荧光pcr扩增仪显示的ct值判断检测结果:检测反应体系的fam和vic/hex荧光强度,以fam达到设定的阈值时所需要的循环次数ct值作为阴阳性判定标准。
若样本的质控体系ct值≤30,则样本质量较好,可以进行下面的结果判读:
如果3’端ct值≥38:阴性;
如果3’端ct值<38:
若5’端有ct值,根据δct1值(ct值5’-ct值3’)计算,δct1值≥3,阳性,δct1值<3,阴性;
若5’端无ct值,根据δct2值(ct值3’-ct值质控)计算,δct2<10,阳性,δct2≥10,阴性。
表1alk基因表达差异的结果判读方法
其中,pcr扩增反应的反应体系如下:
rna逆转录为cdna的方法涉及反转录体系以及如下操作步骤:
反转录体系包括如下成分:
逆转录混合液(含逆转录酶)2μl
rna3μl
加dnase/rnase-freeddh2o10μl。
操作步骤为:
a)将逆转录反应混合液混匀,置于冰上,取2μl逆转录反应混合液加入无菌无酶的离心管中,混匀。
b)加入待测样品rna3μl,rna总量在0.1~5μg范围内,补水至10μl。
c)37℃保温15分钟。
d)85℃保温5秒后冰上冷却,得到cdna模板。
本发明涉及到的原料或试剂均为普通市售产品,涉及到的操作如无特殊说明均为本领域常规操作。
本发明的有益效果在于:
本发明开发一种快速、廉价、操作简便、结果判读简单的alk基因差异表达检测试剂盒及检测方法。本发明基于taqman探针法收集荧光信号,特异性得到保障。本发明的试剂盒具有以下优点:1)检测灵敏度高,可检出浓度为5拷贝/μl,总量为10拷贝的阳性质粒;2)检测时间短,只需80分钟即可完成检测;3)体系特异性好,可以耐受600ng的基因组dna、5μg的野生型rna的逆转录产物;4)引入质控体系,可以有效防止样本质量较差导致的假阴性结果;5)体系结果判读方式简单,只需3步即可准确判断样本是否有alk基因融合;6)样本检测范围广,样本可以为新鲜病理组织,石蜡包埋组织或胸腔液;7)检测过程均为闭管反应,显著降低污染,并且加入ung酶防污染系统,能更好的防止假阳性结果的产生,确保结果真实可信。
附图说明
图1为alk基因无表达(野生型)。
图2为alk基因无差异表达(野生型)。
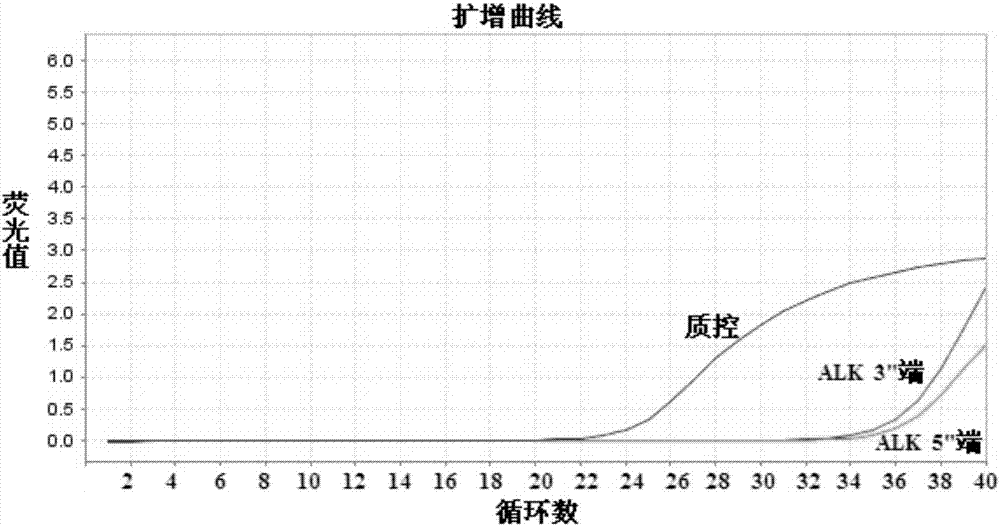
图3为alk基因差异表达(突变型)。
图4为alk基因差异表达(突变型)。
具体实施方式
下面将结合实施例对本发明的优选实施方式进行详细说明。需要理解的是以下实施例的给出仅是为了起到说明的目的,并不是用于对本发明的范围进行限制。本领域的技术人员在不背离本发明的宗旨和精神的情况下,可以对本发明进行各种修改和替换。
下述实施例中所使用的实验方法如无特殊说明,均为常规方法。
下述实施例中所用的材料、试剂等,如无特殊说明,均可从商业途径得到。
本发明实施例是这样实现的,一种用于alk基因表达检测的试剂盒,该试剂盒包括pcr缓冲液,4组特异性引物,4条特异性探针和质控系统,hotstarttaq酶,ung酶。
所述pcr缓冲液中含有1.0~5.0mm的mgcl2,1.0~5.0mm的dntps,即datp、dutp、dgtp和dctp各1.0~5.0mm。
所述4组特异性引物序列分别为seqidno:1与seqidno:2;seqidno:3与seqidno:4;seqidno:5与seqidno:6;seqidno:7与seqidno:8。
各引物序列列举如下:
alk-f1:gacgcctgccccagtaca(seqidno:1);
alk-r1:tcttctatcacattgttctctccaatg(seqidno:2);
alk-f2:tggagccacctacgtatttaagatg(seqidno:3);
alk-r2:gtaggccctgccaccacc(seqidno:4);
alk-f3:gattggagacttcgggatgg(seqidno:5);
alk-r3:gcagcatggcacagcctc(seqidno:6);
alk-f4:ccttcatggaaggaatattcacttc(seqidno:7);
alk-r4:gaaaagatttcccatagcagcac(seqidno:8)。
所述特异性探针5’端修饰有fam或vic,3’端修饰有非荧光淬灭基团nfq(non-fluorescentquencher),该基团本身不产生荧光,因此可以大大降低本底信号的强度,同时该特异性探针上还连接有mgb修饰基团,可以将该探针的tm值提高10℃左右,因此同样的tm值,mgb探针可以比普通taqman探针设计的更短,特异性更强。
优选地,所述4条特异性探针序列为seqidno:9-12,可特异性识别alk基因13-15号外显子和25-27号外显子上的序列。
探针序列列举如下:
alk-p1:ccagttaatccagaaagt(seqidno:9);
alk-p2:ccctgatcattgcagc(seqidno:10);
alk-p3:catctacagggcgagcta(seqidno:11);
alk-p4:cagacacatggtccttt(seqidno:12)。
本发明实施例中,使用质控系统监测样本质量。rna容易降解,对样本制备与保存、rna提取及逆转录过程要求较高。采用表达量稳定的基因构建质控系统,可以有效监测样本质量,避免产生假阴性结果。因此本发明实施例中采用质控系统来消除上述隐患,保证了检测结果的准确性。该质控系统包含质控引物和质控探针,本发明实施例中可采用本领域技术人员熟知的其它质控系统。优选地,所述质控系统包含质控引物和质控探针。质控引物序列为seqidno:13和seqidno:14,所述质控探针序列为seqidno:15,所述质控探针5’端修饰有fam或vic,3’端修饰有nfq-mgb。
优选地,本发明实施例中的质控系统针对人b2m基因设计。其中包含的质控引物序列如下所示:
b2m-f:atgagtatgcctgccgtgtg(seqidno:13);
b2m-r:gcttacatgtctcgatcccact(seqidno:14)。
本发明实施例中的质控探针5′端标记有报告基团,如fam、vic等,3′端标记有不发光荧光淬灭基团,如nfq-mgb等。当探针完整的时候,报告基团所发射的荧光能量被淬灭基团吸收,仪器检测不到信号。随着pcr的进行,taq酶在dna链延伸过程中遇到与模板结合的探针,其5′→3′外切核酸酶活性就会将探针切断,报告基团远离荧光淬灭基团,产生荧光信号。因此检测到的信号强度就代表了模板dna的拷贝数。
优选地,所述质控探针为:
b2m-p:ccatgtgactttgtcacagc(seqidno:15)。
优选地,本发明实施例中的酶溶液中含有taq酶,其为pcr反应所必需的且该酶溶液还含有ung酶,其中ung(uracil-n-glycosylase)酶为尿嘧啶-n-糖基化酶,其特点是最佳活性温度为50℃,95℃灭活,其作用原理是选择性水解断裂含有du的双链或单链dna中的尿嘧啶糖苷键,形成的有缺失碱基的dna链。在pcr反应中,使用ung酶可预防非特异性pcr扩增和污染。
优选地,本发明实施例中的检测试剂盒还包括阳性对照液和空白对照液,设置阳性对照和空白对照可监测实时定量pcr反应的正常进行,所述阳性对照液含有3种质粒dna混合液,所述3种质粒dna分别含有alk基因外显子13-15序列、alk基因外显子25-27序列,以及b2m基因的一段序列,该质粒可为本领域技术人员熟知的质粒,3种质粒浓度相同,均为2000copies/μl;所述空白对照液为tris-hcl(10mm)缓冲液。
本发明实施例的另一目的在于提供一种alk基因表达的检测方法,该检测方法包括以下步骤:
(1)设计并筛选特异性扩增与检测alk基因外显子13-14、14-15、25-26、26-27的引物组合和探针组合;制备本发明的alk基因表达检测试剂盒。
(2)获得待测样品总rna;
(3)将rna逆转录为cdna;
(3)以cdna为模板进行荧光定量pcr扩增:每个样本分三个反应管检测alk基因差异表达,将上述获得的cdna先后取相同的量加入所述三个反应管中并同时进行pcr反应。
优选地,以25μl反应体系为例,向反应管中加入待检测样品后得到的混合物中各组分终浓度及含量如下:
上述体系仅为例证性,在实际应用中可以按照比例扩大或缩小该混合物体积及其中各组分含量。
具体地,在上述25μl反应体系中,所述各对引物包括上述步骤(1)中的4对特异性引物,1对质控引物及质控引物,所述各条探针包括上述步骤(1)中的特异性探针,所述样品为cdna。
具体地,在步骤(3)中的荧光定量pcr反应条件为:
37℃处理10分钟,95℃预变性5分钟,
40个循环:95℃15秒,60℃35秒并收集荧光信号。
在上述pcr反应后,所得结果按以下步骤进行结果判定:
1.根据弱阳性对照和空白对照,对试剂盒有效性判定:
2.根据质控体系结果,进行样本有效性的判定,质控pcr反应液:fam通道ct值≤30,样本rna质量较好,加量适中。
3.对样本检测结果进行判定,确定样本是否存在融合。
a)如果3’端ct值≥38:阴性;
b)如果3’端ct值<38:
若5’端有ct值,根据δct1值(ct值5’-ct值3’)计算,δct1值≥3,阳性,δct1值<3,阴性;
若5’端无ct值,根据δct2值(ct值3’-ct值质控)计算,δct2<10,阳性,δct2≥10,阴性。
本发明的检测方法具有灵敏度高、特异性强、结果真实可信的优点,同时该检测方法操作简单快速,能在80分钟内完成检测,并且结果判读简单客观,便于分析。
实施例1
本实施例用于说明本发明所述人类alk基因表达检测试剂盒的制备。
具体包括以下步骤:
1、引物及探针合成:
设计并合成4组特异性引物:seqidno:1与seqidno:2;seqidno:3与seqidno:4;seqidno:5与seqidno:6;seqidno:7与seqidno:8;4条特异性探针seqidno:9-12,并在探针的5’端标记fam荧光基团,3’端标记nfq-mgb不发光淬灭基团。将引物、探针分别制备成100μm的母液储存。
2、制备质控系统:设计并合成针对人b2m基因的1对质控引物,该引物对序列为seqidno:13和seqidno:14;设计并合成质控探针,该探针为seqidno:15。将该质控引物和探针分别配制成100μm的母液储存。
3、制备其他试剂:制备pcr缓冲液,其中含有1.0mm的mgcl2,datp、dutp、dgtp和dctp各1.0mm;制备酶混合液,其中含有taq酶0.5×103u/ml,ung酶0.1×103u/ml。
4、制备阳性对照液和空白对照液,该阳性对照液中含有3种质粒dna混合液,所述3种质粒dna分别含有alk基因外显子13-15序列、alk基因外显子25-27序列,以及b2m基因的一段序列,该质粒的选择及设计为本领域技术人员熟知,均为2000copies/μl;该空白对照液为tris-hcl(10mm)缓冲液。
5、pcr反应液配制:按照下表进行四个不同体系pcr反应液配制
表2:pcr反应液配制
6、组装试剂盒:试剂盒中包含3管pcr反应液,根据pcr反应体系各成分使用量,计算20人份规格各成分使用量,配制试剂盒各管中成分并组装。
实施例2
用实施例1制备的alk基因检测试剂盒对对野生型肺癌患者的ffpe样本进行检测,评估体系的特异性;对阳性质粒进行检测,评估体系的灵敏度。
本实施例中收集20例alk融合野生型肺癌患者的ffpe样本,分别从其中提取dna和rna,其中dna直接用实施例1中得到的alk基因表达检测试剂盒进行检测,rna逆转录成cdna后,用实施例1中得到的alk基因表达检测试剂盒进行检测,评估试剂盒的特异性。同时提取阳性质粒,稀释后用实施例1中得到的alk基因表达检测试剂盒进行检测,评估体系的灵敏度。
一、样本制备
1.ffpe样本dna制备
使用qiagen56404试剂盒进行ffpe样本dna提取,具体操作步骤如下:
1)将≤25mg的石蜡包埋组织放置在1.5ml的离心管中,加入1000μl的二甲苯,剧烈涡旋10s,12000rmp室温离心5分钟。
2)小心吸去上清,切勿吸去颗粒(沉淀),弃上清液。
3)加入1000μl无水乙醇,以除去残留的二甲苯,轻轻涡旋混匀。12000rmp室温离心5分钟。弃上清,注意不要倒掉沉淀。
4)重复3步。
5)打开离心管,在37℃孵育10-15分钟,直至乙醇完全蒸发。
6)加入180μlatl,再添加20μl的蛋白酶k,彻底涡旋,56℃孵育过夜,直到该组织完全解(在孵育过程中可以偶尔涡旋)。
7)90℃孵育1小时(在bufferatl中90℃孵化可逆转部分甲醛修饰的核酸)。
8)涡旋15s,加入200μlal,涡旋后加入200μl无水乙醇(96%-100%),可能会产生白色絮状沉淀,混合后再次彻底涡旋震荡。
9)将第8步最后的混合物加入到离心柱上,8000rpm离心1分钟,弃废液。
10)加入500μlaw1buffer,8000rpm离心1分钟,弃废液。
11)加入500μlaw2buffer,12000pm离心3分钟,弃废液。
12)12000rpm空转1分钟。
13)将离心柱放置在新的1.5ml离心管中,加入50μltris-hcl,室温放置1分钟,12000rmp离心1分钟,收集纯化的基因组dna。
用紫外吸收分光光度计测定样本dna浓度,od260/od280为1.6-1.8,统一稀释至300ng/μl。
2、野生型ffpe样本cdna制备
1)ffpe样本rna提取
使用qiagen73504试剂盒进行ffpe样本rna提取,具体步骤如下:
(a)取上述各肺癌样本,分别加入1ml二甲苯,混匀,室温下13000rpm离心2分钟,弃上清液,加入1ml无水乙醇到沉淀中,震荡混匀(去除二甲苯),室温下13000rpm离心2分钟弃上清液,打开离心管盖,37℃放置10分钟,使残留的乙醇蒸发干净;
(b)在离心管中加240μlbufferpkd及10μl蛋白酶k,震荡混匀,56℃孵育15分钟,80℃孵育15分钟,冰上孵育3分钟,然后13000rpm离心15分钟,将上清转移到一个新的离心管。往上清中加入25μldnaseboosterbuffer和10μldnasei原液,室温孵育15分钟,后加入500μlbufferrbc,混匀;
(c)往上清液加入1200μl无水乙醇,混匀,取700μl样品包括前面生成的沉淀转移到带有2ml收集管的rnaminelute离心柱里,大于10000rpm离心15s,弃废液,重复上一步直到样品转移到rnaminelute离心柱里。
(d)打开盖子加入500μlbufferrpe,盖紧盖子,大于10000rpm离心2分钟,重复本步骤一次后,将柱子转移到收集管中,向吸附膜中间部位滴加14-30μlrnase-freewater,离心1分钟后收集rna。
2)rna逆转录成cdna
用紫外分光光度计检测rna提取质量及浓度,确定其浓度od260/od280为1.8-2.0。取5μg的rna作为其cdna合成的模板,采用武汉友芝友医疗科技股份有限公司的试剂盒合成cdna,cdna合成体系如下:
逆转录混合液(含逆转录酶)2μl
rna3μl
加dnase/rnase-freeddh2o10μl。
(a)将逆转录反应混合液混匀,置于冰上,取2μl逆转录反应混合液加入无菌无酶的离心管中,混匀。
(b)加入待测样品rna3μl,rna总量为5μg,补水至10μl。
(c)37℃保温15分钟。
(d)85℃保温5秒后冰上冷却,得到cdna模板。
3、阳性质粒制备
使用天根dp103试剂盒进行质粒提取,具体操作步骤如下:
1)柱平衡步骤:向吸附柱cp3中(吸附柱放入收集管中)加入500柱放的平衡液bl,12,000rpm离心1分钟,倒掉收集管中的废液,将吸附柱重新放回收集管中。(请使用当天处理过的柱子)。
2)取1-5ml过夜培养的菌液,加入离心管中,使用常规台式离心机,12,000rpm离心1分钟,尽量吸除上清(菌液较多时可以通过多次离心将菌体沉淀收集到一个离心管中)。
3)向留有菌体沉淀的离心管中加入250μl溶液p1(请先检查是否已加入rnasea),使用移液器或涡旋振荡器彻底悬浮细菌沉淀。注意:如果有未彻底混匀的菌块,会影响裂解,导致提取量和纯度偏低。
4)向离心管中加入250μl溶液p2,温和地上下翻转6-8次使菌体充分裂解。注意:温和地混合,不要剧烈震荡,以免打断基因组dna,造成提取的质粒中混有基因组dna片断。此时菌液应变得清亮粘稠,所用时间不应超过5分钟,以免质粒受到破坏。如果未变得清亮,可能由于菌体过多,裂解不彻底,应减少菌体量。
5)向离心管中加入350μl溶液p3,立即温和地上下翻转6-8次,充分混匀,此时将出现白色絮状沉淀。12,000rpm离心10分钟。注意:p3加入后应立即混合,避免产生局部沉淀。如果上清中还有微小白色沉淀,可再次离心后取上清。
6)将上一步收集的上清液用移液器转移到吸附柱cp3中(吸附柱放入收集管中),注意尽量不要吸出沉淀。12,000rpm离心30-60秒,倒掉收集管中的废液,将吸附柱cp3放入收集管中。
7)可选步骤:向吸附柱cp3中加入500μl去蛋白液pd,12,000rpm离心30-60秒,倒掉收集管中的废液,将吸附柱cp3重新放回收集管中。如果宿主菌是enda+宿主菌(tg1,bl21,hb101,jm系列,et12567等),这些宿主菌含有大量的核酸酶,易降解质粒dna,推荐采用此步。如果宿主菌是enda-宿主菌(dh5α,top10等),这步可省略。
8)向吸附柱cp3中加入600μl漂洗液pw(请先检查是否已加入无水乙醇),12,000rpm离心30-60秒,倒掉收集管中的废液,将吸附柱cp3放入收集管中。
9)重复操作步骤8。
10)将吸附柱cp3放入收集管中,12,000rpm离心2分钟,目的是将吸附柱中残余的漂洗液去除。注意:漂洗液中乙醇的残留会影响后续的酶反应(酶切、pcr等)实验。为确保下游实验不受残留乙醇的影响,建议将吸附柱cp3开盖,置于室温放置数分钟,以彻底晾干吸附材料中残余的漂洗液。
11)将吸附柱cp3置于一个干净的离心管中,向吸附膜的中间部位滴加50-100μl洗脱缓冲液eb,室温放置2分钟,12,000rpm离心2分钟将质粒溶液收集到离心管中。注意:洗脱缓冲液体积不应少于50μl,体积过小影响回收效率。
用紫外分光光度计测定质粒浓度,将质粒分别稀释至10拷贝/μl和5拷贝/μl。
二、样本的荧光定量pcr检测
分别取2μl上述步骤中得到的gdna,cdna和阳性质粒,加入三个反应体系中,使反应体系总体积均为25μl,并放入荧光定量pcr仪,按如下所示设置pcr反应程序后进行扩增反应:
95℃5分钟;
95℃15s,60℃35s,40个循环;每个循环后收集fam、vic的荧光信号。
三、样本的检测结果分析
1)根据阳性对照和空白对照,对试剂盒有效性判定:
2)根据质控体系结果,进行样本有效性的判定,质控pcr反应液:fam通道ct值≤30,样本rna质量较好,加量适中。
3)对样本检测结果进行判定,确定样本是否存在融合。
a)如果3’端ct值≥38:阴性;
b)如果3’端ct值<38:
若5’端有ct值,根据δct1值(ct值5’-ct值3’)计算,δct1值≥3,阳性,δct1值<3,阴性;
若5’端无ct值,根据δct2值(ct值3’-ct值质控)计算,δct2<10,阳性,δct2≥10,阴性。
检测结果表明,试剂盒检测300ng/μl的ffpe样本基因组dna,5’非激酶域pcr反应液、3’激酶域pcr反应液及质控pcr反应液均无扩增ct值,说明体系对基因组dna的特异性很好;试剂盒检测5μgrna逆转录成的cdna,只有质控pcr反应液能正常扩增,5’非激酶域pcr反应液和3’激酶域pcr反应液均无扩增ct值,说明体系对野生型cdna的特异性很好;试剂盒分别检测5拷贝/μl的阳性质粒,5’非激酶域pcr反应液、3’激酶域pcr反应液及质控pcr反应液均能正常扩增,说明体系能检测5拷贝/μl的阳性质粒。
实施例3
用实施例1制备的alk基因检测试剂盒对待测样品进行检测。
本实施例中收集200例肺癌患者的ffpe样本,从其中提取rna,逆转录成cdna后,用实施例1中得到的alk基因表达检测试剂盒检测待检样品的alk表达情况。
1、ffpe样本rna提取
(a)取上述各肺癌样本,分别加入1ml二甲苯,混匀,室温下13000rpm离心2分钟,弃上清液,加入1ml无水乙醇到沉淀中,震荡混匀(去除二甲苯),室温下13000rpm离心2分钟弃上清液,打开离心管盖,37℃放置10分钟,使残留的乙醇蒸发干净;
(b)在离心管中加240μlbufferpkd及10μl蛋白酶k,震荡混匀,56℃孵育15分钟,80℃孵育15分钟,冰上孵育3分钟,然后13000rpm离心15分钟,将上清转移到一个新的离心管。往上清中加入25μldnaseboosterbuffer和10μldnasei原液,室温孵育15分钟,后加入500μlbufferrbc,混匀;
(c)往上清液加入1200μl无水乙醇,混匀,取700μl样品包括前面生成的沉淀转移到带有2ml收集管的rnaminelute离心柱里,大于10000rpm离心15s,弃废液,重复上一步直到样品转移到rnaminelute离心柱里。
(d)打开盖子加入500μlbufferrpe,盖紧盖子,大于10000rpm离心2分钟,重复本步骤一次后,将柱子转移到收集管中,向吸附膜中间部位滴加14-30μlrnase-freewater,离心1分钟后收集rna。
2、rna逆转录成cdna
用紫外分光光度计检测rna提取质量及浓度,确定其浓度od260/od280为1.8-2.0。取0.1~5μg的rna作为其cdna合成的模板,采用武汉友芝友医疗科技股份有限公司的试剂盒合成cdna,cdna合成体系如下:
逆转录混合液(含逆转录酶)2μl
rna3μl
加dnase/rnase-freeddh2o10μl。
(a)将逆转录反应混合液混匀,置于冰上,取2μl逆转录反应混合液加入无菌无酶的离心管中,混匀。
(b)加入待测样品rna3μl,rna总量在0.1~5μg范围内,补水至10μl。
(c)37℃保温15分钟。
(d)85℃保温5秒后冰上冷却,得到cdna模板。
3、样本的荧光定量pcr检测
取2μl步骤2中得到的cdna,加入三个反应体系中,使反应体系总体积均为25μl,并放入荧光定量pcr仪,按如下所示设置pcr反应程序后进行扩增反应:
95℃5分钟;
95℃15s,60℃35s,40个循环;每个循环后收集fam、vic的荧光信号。
4、样本的检测结果分析
1)根据阳性对照和空白对照,对试剂盒有效性判定:
2)根据质控体系结果,进行样本有效性的判定,质控pcr反应液:fam通道ct值≤30,样本rna质量较好,加量适中。
3)对样本检测结果进行判定,确定样本是否存在融合。
a)如果3’端ct值≥38:阴性;
b)如果3’端ct值<38:
若5’端有ct值,根据δct1值(ct值5’-ct值3’)计算,δct1值≥3,阳性,δct1值<3,阴性;
若5’端无ct值,根据δct2值(ct值3’-ct值质控)计算,δct2<10,阳性,δct2≥10,阴性。
检测结果表明所检测200例肺癌样本中有17例发生alk基因差异表达,突变率为8.5%,同时对上述所有样本进行ihc对比检测,ihc结果表明alk阳性有17例,两种检测方法的符合率为100%,进一步证明了本发明体系检测的准确性,结果见表4。图1-图4为选取的具有代表性的样本扩增曲线,图1为alk基因无表达(野生型);图2为alk基因无差异表达(野生型);图3为alk基因差异表达(突变型);图4为alk基因差异表达(突变型)。
以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明的保护范围之内。
表3试剂盒的组成
表4临床样本检测结果对比
虽然,上文中已经用一般性说明及具体实施方案对本发明作了详尽的描述,但在本发明基础上,可以对之作一些修改或改进,这对本领域技术人员而言是显而易见的。因此,在不偏离本发明精神的基础上所做的这些修改或改进,均属于本发明要求保护的范围。
序列表
<110>武汉友芝友医疗科技股份有限公司
<120>人类alk基因表达的检测引物、探针及检测试剂盒
<130>khp171112144.2tq
<160>15
<170>patentinversion3.5
<210>1
<211>18
<212>dna
<213>人工序列
<400>1
gacgcctgccccagtaca18
<210>2
<211>27
<212>dna
<213>人工序列
<400>2
tcttctatcacattgttctctccaatg27
<210>3
<211>25
<212>dna
<213>人工序列
<400>3
tggagccacctacgtatttaagatg25
<210>4
<211>18
<212>dna
<213>人工序列
<400>4
gtaggccctgccaccacc18
<210>5
<211>20
<212>dna
<213>人工序列
<400>5
gattggagacttcgggatgg20
<210>6
<211>18
<212>dna
<213>人工序列
<400>6
gcagcatggcacagcctc18
<210>7
<211>25
<212>dna
<213>人工序列
<400>7
ccttcatggaaggaatattcacttc25
<210>8
<211>23
<212>dna
<213>人工序列
<400>8
gaaaagatttcccatagcagcac23
<210>9
<211>18
<212>dna
<213>人工序列
<400>9
ccagttaatccagaaagt18
<210>10
<211>16
<212>dna
<213>人工序列
<400>10
ccctgatcattgcagc16
<210>11
<211>18
<212>dna
<213>人工序列
<400>11
catctacagggcgagcta18
<210>12
<211>17
<212>dna
<213>人工序列
<400>12
cagacacatggtccttt17
<210>13
<211>20
<212>dna
<213>人工序列
<400>13
atgagtatgcctgccgtgtg20
<210>14
<211>22
<212>dna
<213>人工序列
<400>14
gcttacatgtctcgatcccact22
<210>15
<211>20
<212>dna
<213>人工序列
<400>15
ccatgtgactttgtcacagc20
- 还没有人留言评论。精彩留言会获得点赞!
- 一种快速区分prv中国型、欧美型及疫苗株的双色荧光检测方法、引物及探针的制作方法
- 实时荧光pcr技术定量检测myd88基因l265p突变的方法、引物和探针的制作方法
- 用于定性检测白血病融合基因的引物、探针、试剂盒及方法
- 在体外检测或/及定量乙型肝炎病毒的方法及其所使用的引物、探针的制作方法
- 用于检测多种呼吸道病毒的pcr引物组、探针组及试剂盒的制作方法
- 一种检测人类met基因14外显子剪接突变的引物、探针及试剂盒的制作方法
- 使用重叠引物和熔解探针检测单核苷酸多态性的制作方法
- 用于检测多种呼吸道病毒的pcr引物组、探针组及试剂盒的制作方法
- 一种检测人类met基因14外显子剪接突变的引物、探针及试剂盒的制作方法
- 使用重叠引物和熔解探针检测单核苷酸多态性的制作方法
- 一种木瑚菌属食用菌鉴别用分子标记及引物和探针的制造方法与工艺
- 一组用于驴源性的实时荧光PCR检测的特异性引物和探针的制造方法与工艺
- 一组用于鸡源性实时荧光PCR检测的特异性引物和探针的制造方法与工艺
- 一种快速检测异鳞蛇鲭和棘鳞蛇鲭源性成分的方法与制造工艺
- 一种检测食管癌相关标志物的探针组合及其试剂盒的制造方法与工艺
- 一种检测皮肤癌相关标志物的探针组合及其试剂盒的制造方法与工艺
- 一种检测骨髓瘤相关标志物的探针组合及其试剂盒的制造方法与工艺
- 一种用于检测样品中牛凸隆病毒的荧光RT-PCR引物、探针和试剂盒及检测方法与制造工艺
- CYP2C19基因多态性检测引物、探针及试剂盒的制造方法与工艺
- 检测CYP2C9和VKORC1基因多态性的引物、探针和试剂盒的制造方法与工艺