一种肝细胞癌患者外周血GPC3检测方法与流程
本发明涉及一种检测外周血GPC3的方法,尤其对未获得病理诊断的肝细胞癌患者,通过检测外周血中GPC3,进一步明确肝细胞癌诊断。
背景技术:
GPC3(Glypican-3,磷脂酰肌醇蛋白聚糖-3)是一种膜性硫酸乙酰肝素多糖蛋白(heparan sulfate proteoglycan,HSPG),相对分子质量约66kDa,其基本结构包含核心蛋白、硫酸乙酰肝素(heparin sulfate,HS)链和糖基磷脂酰肌醇(GPI),通过GPI锚定于细胞表面,可以结合多种生长因子并调节其活性,进而在生长发育和癌变过程中起关键作用。GPC3主要通过Wnts信号途径产生作用,GPC3在正常组织中表达及分布有明显的组织特异性和组织分化的时相特异性。研究表明在人体的胚胎期,胎盘和胎儿组织中富含GPC3mRNA,胃肠道和肝、肾和肺中都有GPC3的高度表达,其中以肝脏表达水平最高。而在成人,GPC3高表达在胎盘组织,在卵巢、肾脏、肺脏、心脏等少数组织呈低水平表达,不表达于正常的肝脏组织。研究证实GPC3蛋白在肝癌组织中高表达,而在非癌组织中没有表达或表达量极低,说明GPC3和肝癌有特定的关系,GPC3具有抑制肿瘤的生长,更加说明GPC3在肝癌表达的特异性和在肝癌作用机制的特异性;同时还有研究表明GPC3在肺癌、乳腺癌、间皮瘤、肾癌和卵巢癌组织中表达缺失。有研究表明研究显示:GPC3在80%-90%肝癌组织中表达显著上调,在正常成人组织及肝炎、肝硬化患者组织和其它肿瘤中低水平表达或不表达,在AFP阴性的HCC中也有较高表达。对肝癌、肝细胞癌、肝硬化再生性瘤、结节增生的肝组织进行免疫组化检测,发现肝癌组织中GPC3阳性率达75.7%,而在良性肿瘤中GPC3阴性。GPC3在90%的HCC中呈阳性,且特异性高达100%,但在转移性肝癌和良性肝病中阴性。因此,GPC3不仅可以用于鉴别肿瘤的良、恶性,还可以鉴别HCC与转移性肝癌。
目前肝细胞癌的诊断包括病理学诊断和临床诊断,病理学诊断是肝癌诊断的金标准,临床诊断标准主要包括慢性肝病背景、影像学检查结果和血清肿瘤标记物水平三方面内容。但对于无法获得病理诊断或临床诊断依据不充分的部分肝癌患者,检测GPC3的表达状况变得十分困难。
技术实现要素:
循环肿瘤细胞(Circulating tumor cell,CTC)是从实体肿瘤脱落而进入外周血液循环的肿瘤细胞,聚集成团形成循环肿瘤微栓(Circulating tumor thrombus,CTM),它们存在于多种恶性肿瘤中,其检测对于评估肿瘤患者尤其是晚期肿瘤患者的预后以及选择合适的个体化治疗具有重要的临床意义。因CTC检测具有微创、实时等特点,被称为“液态活检”。
为了克服临床诊断依据不足的肝癌患者不适宜组织标本取材或避免穿刺活检造成肿瘤播散等问题,无法明确肝癌诊断的不足,本发明提供了一种肝细胞癌患者外周血GPC3检测方法:利用膜过滤装置分离获取无法获得组织标本的肝癌患者外周血中的CTC,运用细胞蜡块技术制作薄层切片,进而检测GPC3表达情况。
本发明所采用的技术方案如下:
一、利用膜过滤装置分离获取无法获得组织标本的肝癌患者外周血中的CTC:
1、采集晚期肝癌患者外周血:肘正中静脉5ml;
2、外周血样预处理:将采集的外周血样10倍稀释,稀释液成分:1mmol/l EDTA+0.1%BSA,稀释后加多聚甲醛固定外周血样10分钟,固定终浓度为0.25%;
3、利用膜过滤分离肿瘤细胞装置过滤外周血样,分离获得外周血循环肿瘤细胞:将预处理的外周血样加入到膜过滤分离肿瘤细胞装置的血样容器中,使其依靠重力自然过滤;
4、过滤结束后,从膜过滤分离肿瘤细胞装置中取下滤器,将循环肿瘤细胞染色液加入到滤器中,染色2min,PBS缓冲液冲洗干净,取下滤膜,放置在载玻片上,干燥后在显微镜下观察,确定是否存在CTC。
二、运用细胞蜡块技术制作薄层切片:
1、脱色:从载玻片上取下带有CTC的滤膜,置于脱色液中浸泡4-6小时,脱去CTC染色液,所述脱色液为:95%酒精与100%二甲苯按容积比1:1混匀。
2、包裹:浸泡结束后取出滤膜,用吸水纸包裹;
3、固定:将包裹物置于10%中性福尔马林中,固定4-6h;
4、浸蜡包埋:固定结束后取出包裹物,脱水后置于石蜡包埋盒中,浸蜡包埋制作细胞石蜡块;
5、薄层切片:用切片机将细胞石蜡块连续切片,制成厚度为4μm的薄层切片。
三、检测GPC3表达情况:
1.烤片:CTC蜡块薄层切片在60℃恒温箱中烤片2小时;
2.脱蜡:切片于两瓶二甲苯中分别放置5分钟;
3.水化:将切片依次在无水乙醇、95%乙醇、85%乙醇中分别放置5分钟(视室内温度情况稍作调整),自来水、蒸馏水冲洗2次,每次3分钟;
4.抗原修复:将高压锅内的修复液EDTA煮沸,放入切片至完全没入修复液盖上高压锅盖及压力阀,加热至高压锅喷气后1.5分钟,离火,将高压锅稍冷却打开锅盖,切片在修复液中自然冷却;
5.蒸馏水冲洗;
6.去除内源性过氧化物酶:用3%H2O2作用切片10分钟;
7.蒸馏水冲洗;
8.PBS浸洗5次各1.5分钟;
9.滴加GPC3一抗;
10. 4℃冰箱中过夜;
11.PBS浸洗5次各1.5分钟;
12.滴加通用型IgG抗体-HRP多聚体;
13. 37℃水浴锅中孵育20分钟;
14.PBS浸洗5次各1.5分钟;
15.显微镜下控制,DAB显色:每张切片加2滴或100μl新鲜配制的DAB溶液,显微镜下观察3-10分钟;
16.蒸馏水冲洗2次,每次3分钟;苏木素复染1分钟;
17. 0.1%盐酸酒精分化;
18. 0.1%氨水溶液返蓝;
19. 50%、70%、85%、95%梯度无水乙醇脱水干燥;
20.二甲苯透明,中性树脂胶封片;
21.细胞病理学专家阅片,根据细胞膜和细胞浆着色程度判定GPC3表达情况。
本发明技术步骤中所述的膜过滤分离肿瘤细胞装置,包括滤器、血样容器、废液缸和铁架台,所述铁架台设有底座、立架和支架,所述血样容器通过支架设置于铁架台上部,血样容器的下方为滤器,滤器通过输液器联通至废液缸,废液缸设置于底座上。
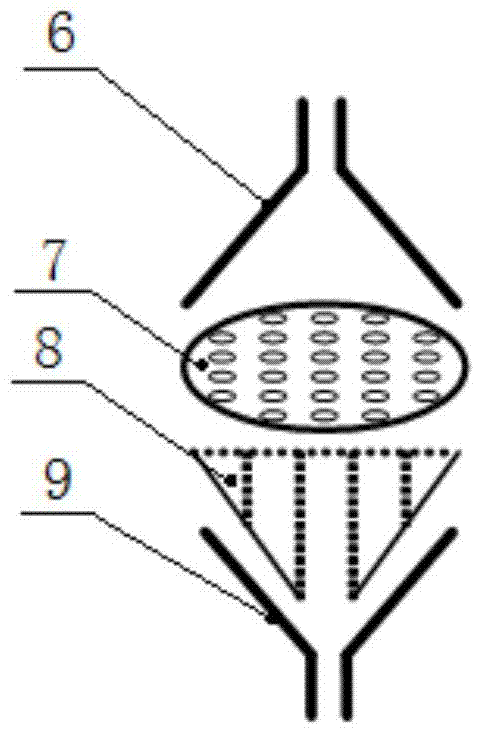
所述滤器包括滤器上口、滤膜、载滤膜平台和滤器下口,滤膜置于载滤膜平台上;滤器上口接血样容器,滤器下口通过输液器接废液缸。
所述滤膜为疏水材料制成,其上均匀布满口径为10微米的滤孔。
本发明的有益效果是:通过该技术方法,不用取材肝癌组织即可检测到肝癌患者外周血中GPC3表达情况,为肝细胞癌诊断提供依据。该技术属于微创甚至无创,并能够实时检测。
附图说明
图1为本发明的膜过滤装置结构示意图;
图2为本发明膜过滤装置的滤器的结构示意剖视图;
图3为本发明膜过滤装置的滤器滤膜的结构示意图;
图4为肝癌外周血循环肿瘤细胞镜像图;
图5为肝癌外周血循环肿瘤细胞GPC3表达镜像图。
图中:1铁架台、2血样容器、3滤器、4输液器、5废液缸、6滤器上口、7滤膜、8载滤膜平台、9滤器下口、10滤孔、11底座、12立架、13支架。
具体实施方式
下面结合附图和实施例对本发明进行阐述。
实施例
运用此技术方法分离获取并鉴定8例肝癌患者(同时检测8例正常人样本做阴性对照)外周血循环肿瘤细胞,检测GPC3表达情况。
一、利用膜过滤装置分离获取无法获得组织标本的肝癌患者外周血中的CTC:
采集各样本外周血5ml,用45ml稀释液(成分:1mmol/l EDTA+0.1%BSA)稀释外周血,然后加入3ml的4%多聚甲醛固定稀释后的血样10分钟。
在固定的间期,组装膜过滤装置:如附图1、图2、图3所示,该过滤装置由滤器3、滤膜7、血样容器2、废液缸5、铁架台1构成。
用10mlPBS润湿滤器3,然后将固定好的外周血样加入到膜过滤装置的血样容器2中,使其依靠重力自然过滤,CTC被截留在滤膜7上。
肿瘤细胞直径一般大于15微米,而血细胞(包括红细胞、白细胞)直径一般小于10微米,因此当含有CTC的外周血经过滤后,血细胞因直径小于滤孔10能够被滤过,而CTC因直径大于滤孔10被截留在滤膜7上。
过滤结束后,从过滤装置中取下滤器3,打开并移走滤器上口6,将循环肿瘤细胞Diff染色液加入到滤器3中,染色2min。
PBS缓冲液将滤器3冲洗干净,用精细镊子取下滤膜7,细胞面朝上,放置在载玻片上。
将滤膜7适当干燥后在显微镜下观察,确认是否存在CTC。
检测结果:8例健康志愿者均未查到循环肿瘤细胞;8例确诊肝癌患者外周血中,2例未检测到CTC或CTM,6例检测到CTC或CTM,检出率为75%。
二、运用细胞蜡块技术制作薄层切片:
将上述载玻片上带有CTC的滤膜取下,置于脱色液中浸泡4-6小时,脱去CTC染色液(脱色液为:95%酒精与100%二甲苯按体积比1:1混匀);浸泡结束后取出滤膜7,用吸水纸包裹;将包裹物置于10%中性福尔马林中,固定4-6h;固定结束后取出包裹物,脱水后置于石蜡包埋盒中,浸蜡包埋制作细胞石蜡块;用切片机将细胞石蜡块连续切片,制成厚度为2-4μm的薄层切片。
三、检测GPC3表达情况:
将CTC蜡块薄层切片在60℃恒温箱中烤片2小时;将切片置于两瓶二甲苯中分别脱蜡5分钟;水化:将切片依次在无水乙醇、95%乙醇、85%乙醇中分别放置5分钟(视室内温度情况稍作调整),蒸馏水冲洗2次,每次3分钟;
抗原修复:将高压锅内的修复液EDTA煮沸,放入切片至完全没入修复液盖上高压锅盖及压力阀,加热至高压锅喷气后1.5分钟,离火,将高压锅稍冷却打开锅盖,切片在修复液中自然冷却;
蒸馏水冲洗干净后,用3%H2O2作用切片10分钟,去除内源性过氧化物酶;蒸馏水冲洗干净,PBS浸洗5次,每次1.5分钟;
滴加GPC3一抗,4℃过夜,PBS冲洗5次,每次1.5分钟;滴加通用型IgG抗体-HRP多聚体,37℃水浴锅中孵育20分钟;PBS浸洗5次各1.5分钟;
显微镜下控制,DAB显色:甩去PBS液,每张切片加100μl新鲜配制的DAB溶液,显微镜下观察5分钟;
蒸馏水冲洗、复染、脱水、透明封片:蒸馏水冲洗2次,每次3分钟;苏木素复染1分钟;0.1%盐酸酒精分化;0.1%氨水溶液返蓝;50%、70%、85%、95%梯度无水乙醇脱水干燥;二甲苯透明,中性树脂胶封片;
细胞病理学专家阅片,根据细胞膜和细胞浆着色程度判定GPC3表达情况。
检测结果:在8例确诊肝癌患者外周血中,6例检测到CTC,其中5例免疫组化检测到CTC有GPC3表达,阳性率为62.5%(表1)。
图4所示为肝癌患者外周血分离获取的循环肿瘤细胞影像图,其细胞核较大,细胞核形状不规则;高核质比。
图5所示为肝癌患者外周血循环肿瘤细胞GPC3免疫组化染色图像,细胞膜和细胞浆黄染。根据其染色分布和强度判定阳性程度,细胞着色占细胞小于10%为(-),着色10%-25%为(+),着色25%-50%为(++),着色大于50%为(+++)。
表1实施例检测结果
- 还没有人留言评论。精彩留言会获得点赞!