染色体基因引物对和探针组合以及染色体核酸检测试剂盒的制作方法
本发明涉及一种基因引物与探针的组合以及包含该组合的试剂盒。更确切的说,是一种染色体基因引物对和探针组合以及染色体核酸检测试剂盒。属于医用检测领域。
背景技术:
目前检测染色体一般采用原位杂交技术(fish),其缺点:自身杂交物的干扰,不稳定、时间长、操作较繁琐等,特别是在应用较短的cdna探针时效率明显下降。使测试结果造成错误,正确率难以保证。针对有效游离dna保存、提取鉴定方法,日益引起广大医学家的关注。现有技术中,缺少有效鉴定游离dna、dna保存效果,及游离dna、dna提取效果的技术和检测试剂盒。
为此,需要设计一种染色体基因引物对和探针组合以及染色体核酸检测试剂盒,具有适用于无创基因管游离dna保存效果鉴定、游离dna提取效果鉴定、单细胞dna提取效果鉴定、法医鉴定。
技术实现要素:
本发明的目的是为了解决现有技术中缺少有效鉴定游离dna、dna保存效果及游离dna、dna提取效果的技术和相关检测试剂盒的问题;提供一种染色体基因引物对和探针组合以及染色体核酸检测试剂盒通过探针与染色体基因引物对的组合适用于无创基因管游离dna保存效果鉴定、游离dna提取效果鉴定、单细胞dna提取效果鉴定、法医鉴定。
本发明通过如下技术方案达到:
一种染色体基因引物对和探针组合,包括一个探针、一对染色体基因引物,其结构特点是:所述探针为taqman探针,所述一对染色体基因引物为一对基因序列反向的引物;
所述探针的序列为:acgcggctggtggatcagtgct;
所述第一引物对中的正向引物的序列为ttatgagcgcgaagcaaacg;
所述第一引物对中的反向引物的序列为:ccgtgggtggtctttaccg。
一种染色体核酸检测试剂盒,包括chromosome反应混合液、dna提取液i;
所述chrmosome反应混合液包括taq酶系、dntp缓冲液混合物终浓度1×加量25μl、如权利要求1所述的正向引物25pmol/μl终浓度30~900nm加量1μl、如权利要求1所述的反向引物25pmol/μl终浓度30~900nm加量1μl、如权利要求1所述的探针25pmol/μl终浓度200nm加量0.5μl、无菌去离子水加量20.5μl。
所述dna提取液i包括na0h100mmol/l、edta1.5mmol/l、tristonx-10050mmol/l、1%np-40、ph=8.0的tris-hc150mmol/l。
本发明有益效果
本发明适用于无创基因管游离dna保存效果鉴定、游离dna提取效果鉴定、单细胞dna提取效果鉴定、法医鉴定,检测精确,避免了漏检。
【附图说明】
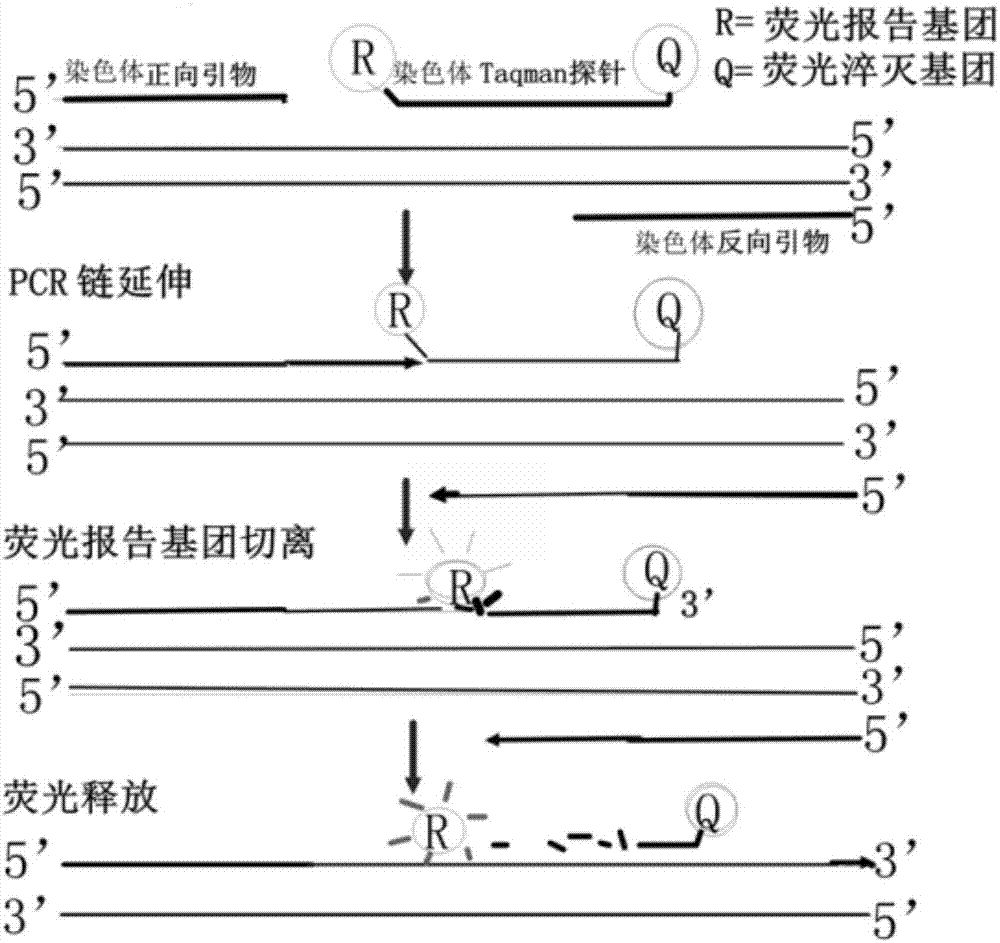
图1为第一引物对和探针pcr荧光扩增原理图;
图2为核酸扩增荧光检测结果分析阴性图;
图3为核酸扩增荧光检测结果分析阳性图。
具体实施例
以下本实施例结合附图具体阐述本发明:
一种染色体基因引物对和探针组合,包括一个探针、一对染色体基因引物,其结构特点是:所述探针为taqman探针,所述一对染色体基因引物为一对基因序列反向的引物;
所述探针的序列为:acgcggctggtggatcagtgct;
所述第一引物对中的正向引物的序列为ttatgagcgcgaagcaaacg;
所述第一引物对中的反向引物的序列为:ccgtgggtggtctttaccg。
一种染色体核酸检测试剂盒,包括chromosome反应混合液、dna提取液i;
所述chrmosome反应混合液包括taq酶系、dntp缓冲液混合物终浓度1×加量25μl、如权利要求1所述的正向引物25pmol/μl终浓度30~900nm加量1μl、如权利要求1所述的反向引物25pmol/μl终浓度30~900nm加量1μl、如权利要求1所述的探针25pmol/μl终浓度200nm加量0.5μl、无菌去离子水加量20.5μl。
所述dna提取液i包括na0h100mmol/l、edta1.5mmol/l、tristonx-10050mmol/l、1%np-40、ph=8.0的tris-hc150mmol/l。
使用该染色体核酸检测试剂盒,实验证明:100例样本,用单细胞基因序列提取液提取单细胞dna产物30例,样本编号d160501-d160530使用该染色体核酸扩增荧光检测试剂盒来鉴定提取效果,染色体基因阳性,其平均浓度为(560000.00±50.00)拷贝/毫升。
如使用现有技术的上海医脉赛科技有限公司提供的核酸提取试剂盒的磁珠法,血浆游离dna提取试剂盒提取无创基因管保存3天的40名孕妇游离dna,样本编号c160531-c160570,染色体基因阳性,其平均浓度为(570.00±80.00)拷贝/毫升;其它试管保存3天的30名孕妇游离dna,样本编号e160971-e1609100均为阴性。
结论用染色体核酸检测试剂盒鉴定提取、保存效果有效,即呈阳性时游离dna、dna提取成功或保存有效;呈阴性时游离dna、dna提取或保存失败。
样本数据显示如下:
参照附图1至3,以上表格表示呈阳性时游离dna、dna提取成功或保存有效;呈阴性时游离dna、dna提取或保存失败。广泛应用于无创基因管游离dna保存效果鉴定、游离dna提取效果鉴定、单细胞dna提取效果鉴定、法医鉴定等。
实时荧光定量pcr技术,是指在pcr反应体系中加入荧光基团,利用荧光信号积累实时监测整个pcr进程,最后通过标准曲线对未知模板进行定量分析的方法。
以下为检测原理:
ct值的定义:
在荧光定量pcr技术中,c代表cycle,t代表threshold,ct值的含义是:每个反应管内的荧光信号到达设定的域值时所经历的循环数荧光域值(threshold)的设定pcr反应的前10个循环的荧光信号作为荧光本底信号,荧光域值的缺省设置是3-10个循环的荧光信号的标准偏差的10倍,即:threshold=10′sdcycle6-10
ct值与起始模板的关系
研究表明,每个模板的ct值与该模板的起始拷贝数的对数存在线性关系即起始拷贝数越多,ct值越小。只要获得未知样品的ct值,即可从标准曲线上计算出该样品的起始拷贝数。
荧光定量pcr所使用的荧光化学现将其原理简述如下:
taqman荧光探针:pcr扩增时在加入一对引物的同时加入一个特异性的荧光探针,该探针为一寡核苷酸,两端分别标记一个报告荧光基团和一个淬灭荧光基团。探针完整时,报告基团发射的荧光信号被淬灭基团吸收;pcr扩增时,taq酶的5'-3'外切酶活性将探针酶切降解,使报告荧光基团和淬灭荧光基团分离,从而荧光监测系统可接收到荧光信号,即每扩增一条dna链,就有一个荧光分子形成,实现了荧光信号的累积与pcr产物形成完全同步。
现有技术中上海医脉赛科技有限公司提供的核酸提取试剂盒---磁珠法,该试剂盒适合于从血浆等无细胞组织液中提取游离dna(circulatingfreedna,cfdna)片段。该试剂盒中的提取过程,具体操作步骤请按照该试剂盒说明书指引进行。
染色体核酸检测试剂盒:
【检验原理】
本试剂盒利用荧光pcr技术,以chromosome基因组中相对保守区为靶区域,设计特异性引物及荧光探针,在样本核酸纯化之后,通过pcr对chromosomedna进行快速检测。使用本试剂盒提供的核酸提取试剂对临床样本进行处理和核酸提取,以试剂盒中提供的pcr检测试剂配制成pcr反应管,将提取的核酸加入pcr反应管,使用荧光定量pcr仪进行pcr扩增,并检测荧光信号,仪器软件自动绘制出实时扩增曲线,根据阈循环值(ct值)实现对未知样本的定性检测。
【储存条件及有效期】
经包装后的试剂盒(包含核酸提取试剂、质控品组分、pcr检测试剂组分)保存于—20±5℃环境下,有效期6个月。
避免反复冻融。冻融次数不超过4次。试剂开瓶后,在室温条件下放置时间不应超过8小时。运输采用干冰(或者冰袋)保持低温,运输时间不应超过4天。
【适用仪器】abiprism7300abiprism7500,lightcycler480,da7600
【样本要求】
1适用标本类型:血清、血浆、体液或组织。
2标本采集:
2.1血清一用一次性无菌注射器抽取受检者静脉血2毫升,注入无菌的干燥试管,室温
2.2血浆用一次性无菌注射器抽取受检者静脉血2毫升,注入含乙二胺四乙酸二钾
(edta-2k)或无创基因管,立即轻轻颠倒试管混合10次,充分混匀,
3标本保存和运送:所采集的标本可立即用于测试,也可以保存于-20℃,可存期为6个月。标本运送采用0℃冰壶,无创基因管的标本常温运送。
【检验方法】
1dna提取(样本制备区)
将待测样本、阳性定量参考品、阴性质控品、chromosome强阳性临界阳性质控品进行同步处理。
1.12次离心的方法分离血浆:4℃,1,600转离心10min分离血浆勿触动白膜层;4℃,16,000转离心10min仔细吸取上清50μ1样品,加入100μ1dna提取液i,用振荡器剧烈振荡混匀10秒,8000转离心数秒。100℃恒温处理10±1min;
1.212,000转离心5min,备用。
2pcr试剂准备(试剂准备区)
直接使用chromosome反应混合液管。
3加样(样本制备区)
往上述chromosome反应管中用带滤芯吸嘴分别加入提取后的待测样本核酸、chromosome阴性质控品、chromosome强阳性质控品、chromosome临界阳性质控品和阳性定量参考品的上清各5μl。盖紧管盖,8,000转离心数秒后转移至扩增检测区。
4pcr扩增(扩增和产物分析区)
4.1abiprism7500仪器设置(7300参照此操作)
4.1.1打开“setup”窗口,按样本对应顺序设置阴性质控(ntc)、阳性质控以及未知样本(unknow)、阳性定量参考品(standard),并在“samplename”一栏中设置样本名称;探针检测模式设置为:reporterdyel:fam,quencherdyel:none;reporterdye2:vic,quencherdye2:none;passivereference:rox。
4.1.2打开instrument窗口,设置循环条件如下:94℃2min,93℃45秒→55℃60秒→10个循环,93℃40秒→55℃55秒→30个循环,保存档,运行。
4.2lightcycler480仪器设置
4.2.1打开软件后,选择“newexperiment”,设置检测模式为“multicolorhydrolysisprobe”,检测通首为fam,vic。
4.2.2设置循环条件:
4.2.3选择“sampleeditor”,设定样品的名称、类型,在“standardconcentration”框中输入阳性定量参考品浓度,设置完成后,保存文件,运行程序。
4.3da7600仪器设置
4.3.1打开软件后,在设置程序参数接口中,设置扩增程序和温度设置,条件如下:
4.3.2点击样本参数接口,按样本对应顺序设置阴性质控(ntc)、阳性质控以及未知样本(unk),并在“样本名称”一栏中设置样本名称:阳性定量参考品在“样品类型”中选择“标准”,“标准浓度”中输入浓度。探针染料类型选择:fam和hex。
4.3.3设置完成后,保存文件,运行程序。
5结果分析
反应结束后自动保存结果,根据分析后图像调节baseline的start值、end值以及threshold值(使用者可根据实际情况自行调整,start值可以在
6质量控制
阴性质控品:全部阴性
阳性质控品:全部阳性,弱阳性质控品检测值允许范围1×102~5.0×102copy/ml;
阳性定量参考品:均为阳性,且0.97≤|r|≤1(correlation数值即为r)
以上要求需在同一实验中同时满足,否则,本次实验无效,全部实验应重新进行。
7结果判断
7.1如果在fam检测信道扩增曲线无明显对数增长期或ct值等于30,在vic检测信道扩增曲线有对数增长期,则判样品的chromosomedna浓度小于检测灵敏度。
7.2如果在fam检测信道扩增曲线有对数增长期且ct值<30,则按以下方法判断:
若样品的c<100,则该样品的chromosomedna浓度<100copy/ml;
若样品的100≤c≤1.00×108,则该样品的chromosomedna浓度=ccopy/ml;
若样品的c>1.00×108,则该样品的chromosomedna浓度>5×106copy/ml。如果需要精确定量结果,可将样品阴性质控品稀释到线性范围后再检测。则该样品的chromosomedna浓度=(c×稀释倍数)copy/ml。
8检验结果的解释
1每次实验均需检测阴性质控品,chromosome强阳性质控品,chromosome临界阳性质控品,质控品结果满足质量控制要求时方可进行检测结果的判定。
2阳性结果判定标准:在fam检测信道扩增曲线有对数增长期且ct值<30。
3阴性结果判定标准:在fam检测通首扩增曲线无明显对数增长期或ct值等于30,在vic检测信道扩增曲线有对数增长期。
9检验方法的局限性
1样本检测结果和样本收集、处理、运送及保存质量有关,其中任务失误都将会导致假阴性结果。如果样本处理时没有控制好交叉污染,可能出现假阳性结果。
3临床实验室应严格按照《临床基因扩增实验室工作规范》配备设备及操作人员,应严格按照说明书要求进行操作。
4本试剂盒检测仅限于规定的样本类型及适用机型。
10产品性能
根据临床试验结果显示,本试剂盒的灵敏度为1×102copy/ml,线性范围为
11注意事项
1试剂盒的内质控品等组分,虽已经通过了hiv1/2-ab、hbs-ag和hcv-ab等项止的检测,但截止目前,没有任务一项检测可以确保绝对安全,故仍应将这些组份作为潜在传染源对待。为了避免样本中任何潜在的生物危险,检测样本应视为具有传染性物质,避免接触到皮肤和粘膜;样本的处理建议在可防止气雾外流的生物安全柜中操作,样本制备区所用过的试管、吸头需打入盛有消毒剂的容器,并与废弃物一起灭菌后方可丢弃;样本操作和处理均需符合相关法规要求:卫生部《微生物生物医学实验室生物安全通用准则》和《医疗废物管理条例》。
1试剂盒中组分需在效期内使用,不使用本试剂盒提供的组分进行实验将可能导致错误结果。
2实验室管理应严格按照pcr基因扩增实验室的管理规范,实验人员必进行专业培训,实验过程严格分区进行(试剂准备区、样本制备区、扩增和产物分析区,所用的消耗品应灭菌后一次性使用,实验操作的每个阶段使用专用的仪器和设备,各区各阶段用品不能交叉使用。
3使用经高压灭菌的一次性离心管和吸头或购买无dna酶、rna酶的离心管和吸头。
4pcr检测试剂使用前要完全解冻,8,000转离心数秒后使用,但应避免反复冻融。
5完成样本核酸提取后,建议马上进行下一步实验,否则请保存于—20℃待用(24h内)。
6如果在标本处理中没有控制好交叉污染,可能出现假阳性。
7对每次实验进行质量控制。
8实验完毕用10%次氯酸或75%酒精处理工作台和移液器,然后用紫外线灯照射30min。
11本试剂盒内的阳性质控品和检测样本均应视为具有传染性物质,因此标本操作和处理均需符合相关法规要求:卫生部《微生物生物医学实验室生物安全通用准则》和《医疗废物管理条例》。
以上内容仅为优选下的实施例方案,不因此而限制本发明的保护范围,凡是利用本发明说明书内容所作的等效结构变换,或直接或间接运用附属在其他相关产品的技术领域,均同理包括在本发明的专利保护范围内。
sequencelisting
<110>胡松
<120>一种染色体基因引物对和探针组合以及染色体核酸检测试剂盒
<130>
<160>3
<170>patentinversion3.3
<210>1
<211>22
<212>dna
<213>人工序列
<400>1
acgcggctggtggatcagtgct22
<210>2
<211>20
<212>dna
<213>人工序列
<400>2
ttatgagcgcgaagcaaacg20
<210>3
<211>19
<212>dna
<213>人工序列
<400>3
ccgtgggtggtctttaccg19
- 还没有人留言评论。精彩留言会获得点赞!
- 一种快速区分prv中国型、欧美型及疫苗株的双色荧光检测方法、引物及探针的制作方法
- 实时荧光pcr技术定量检测myd88基因l265p突变的方法、引物和探针的制作方法
- 用于定性检测白血病融合基因的引物、探针、试剂盒及方法
- 在体外检测或/及定量乙型肝炎病毒的方法及其所使用的引物、探针的制作方法
- 用于检测多种呼吸道病毒的pcr引物组、探针组及试剂盒的制作方法
- 一种检测人类met基因14外显子剪接突变的引物、探针及试剂盒的制作方法
- 使用重叠引物和熔解探针检测单核苷酸多态性的制作方法
- 用于检测多种呼吸道病毒的pcr引物组、探针组及试剂盒的制作方法
- 一种检测人类met基因14外显子剪接突变的引物、探针及试剂盒的制作方法
- 使用重叠引物和熔解探针检测单核苷酸多态性的制作方法
- 一种木瑚菌属食用菌鉴别用分子标记及引物和探针的制造方法与工艺
- 一组用于驴源性的实时荧光PCR检测的特异性引物和探针的制造方法与工艺
- 一组用于鸡源性实时荧光PCR检测的特异性引物和探针的制造方法与工艺
- 一种快速检测异鳞蛇鲭和棘鳞蛇鲭源性成分的方法与制造工艺
- 一种检测食管癌相关标志物的探针组合及其试剂盒的制造方法与工艺
- 一种检测皮肤癌相关标志物的探针组合及其试剂盒的制造方法与工艺
- 一种检测骨髓瘤相关标志物的探针组合及其试剂盒的制造方法与工艺
- 一种用于检测样品中牛凸隆病毒的荧光RT-PCR引物、探针和试剂盒及检测方法与制造工艺
- CYP2C19基因多态性检测引物、探针及试剂盒的制造方法与工艺
- 检测CYP2C9和VKORC1基因多态性的引物、探针和试剂盒的制造方法与工艺